近年来我国畜牧业得到快速发展,广大农牧科技人员在开发利用中草药资源、促进农牧业发展方面,取得了一定成果[1]。2013年,农业部修订的《饲料原料目录》将115种中草药列入饲用植物原料目录。2020年我国规定,退出除中药外的所有促生长类药物饲料添加剂品种。因此,开发中草药饲料添加剂替代抗生素成为行业研究的热点。
我国是中药生产大国,但随着中药材在人体及动物体上的广泛应用,中药也出现供不应求现象[2]。发酵是中药传统炮制工艺之一,工艺简单,发酵中药性质稳定,不易产生抗药性,避免了原料的浪费,提高了中药的利用率,可作为药食同源的饲料添加剂,是防治动物疾病、替代抗生素的理想选择[3-4]。王福刚[5]研究发现,日粮中添加5%复合益生菌培养物可以显著提高肉羊生长性能、血液中免疫球蛋白含量以及抗氧化活性。史洪涛等[6]研究发现,口服0.2%液体发酵中药蛋鸡的过氧化氢酶(catalase,CAT)、超氧化物歧化酶(superoxide dismutase,SOD)、总抗氧化能力(total antioxidant capacity,T-AOC)活性均显著高于对照组(P<0.05)。益生菌发酵中药可以使益生菌和中药协同增效,如李继开等[7]研究发现,利用植物乳杆菌(Lactobacillus plantarum)与枯草芽孢杆菌(Bacillus subtilis)对黄芪、绞股蓝、马齿苋3种中药构成的组方进行液体发酵,可显著提高中药粗多糖的含量。耿江苏[8]研究发现,使用益生菌发酵鱼腥草等中药,可提高中药益生菌数量至5.68×108 CFU/mL。但中药成分错综复杂,目前研究比较多的主要是液体发酵,关于固体发酵中药作为饲料添加剂的报道比较少。
本研究使用3种植物乳杆菌对黄芪、甘草和益母草等复方中药进行固体发酵,研究其对复方中药微生物和有效成分的影响,以期为中药原料作为饲料添加剂提供数据支撑。
1 材料与方法
1.1 材料与试剂
1.1.1 材料与菌株
植物乳杆菌(Lactobacillus plantarum)BLCC2-0015、BLCC2-0126和BLCC2-0410:山东宝来利来生物工程股份有限公司菌种保藏中心;黄芪、茯苓、益母草、甘草和当归:泰安永春堂药店。
1.1.2 试剂
乳酸、阿魏酸、芦丁等标准品(纯度均>98%):上海源叶生物科技有限公司。其他试剂均为国产分析纯。
1.1.3 培养基MRS肉汤培养基、LBS培养基、伊红美蓝培养基、孟加拉红培养基:青岛海博生物技术有限公司。
1.2 仪器与设备
LC-20A高效液相色谱(high performance liquid chromatography,HPLC)仪、InertSustain AQ-C18色谱柱(5 μm,4.6 mm×250 mm):日本岛津公司;AL204电子分析天平:瑞士梅特勒托利多有限公司;GL21M高速冷冻离心机:湖南凯达科学仪器有限公司;CLDC271509超纯水净化系统(超纯水仪):重庆潺林热能设备有限公司;PHS-3C雷磁精密酸碱度计:上海精密科学仪器有限公司;SB120D超声波清洗机:宁波新芝生物科技股份有限公司。
1.3 方法
1.3.1 植物乳杆菌发酵液的制备
将4 ℃保存的植物乳杆菌(Lactobacillus plantarum)BLCC2-0015、BLCC2-0126和BLCC2-0410斜面活化,转接至装有100 mL MRS液体培养基的盐水瓶中,37 ℃静置培养24 h,活菌数均≥109 CFU/mL,备用。
1.3.2 植物乳杆菌固体发酵复方中药
选择甘草、黄芪、茯苓、益母草和当归五味中药,按质量比4∶2∶2∶2∶1进行充分混合。按复方中药、麸皮和豆粕质量比为7∶2∶1配制基料。称取一定质量的基料,按照基料与水比为1.0∶0.5(g∶mL)配制好发酵底物,按100 g/袋进行装袋,每个处理设3个平行。分别按2.0%的接种量接入培养好的植物乳杆菌发酵液,以不接种任何菌株的空白料为对照组,压实后于37 ℃培养箱进行生料厌氧发酵,分别于发酵24 h、48 h和72 h取样,测定pH值、微生物含量、总酸含量、有机酸含量、甘草酸、粗多糖、总黄酮、阿魏酸和甘草次酸含量。
1.3.3 检测方法
pH值:准确称取10.00 g样品加入90 mL灭菌后的生理盐水中,搅拌均匀后静置10 min用玻璃电极pHS-3C型pH计测定。
微生物含量:准确称取10.00 g样品加入90 mL带有玻璃珠的无菌生理盐水中,振荡均匀,采用10倍梯度稀释法稀释,取适当稀释度的样品分别涂布于LBS培养基、孟加拉红培养基和伊红美兰培养基中,分别于37 ℃、30 ℃和37 ℃培养48 h、48 h和24 h。乳杆菌参照GB 4789.35—2016《食品安全国家标准食品微生物学检验乳酸菌检验》进行菌落计数;霉菌参照GB 4789.15—2016《食品安全国家标准食品微生物学检验霉菌和酵母计数》进行菌落计数;大肠杆菌(Escherichia coli)参照GB 4789.38—2012《食品安全国家标准食品微生物学检验大肠埃希氏菌计数》进行菌落计数。根据菌落数计算发酵中药中乳杆菌、霉菌和大肠杆菌的活菌数,结果用CFU/g表示。
总酸含量:参照国标GB/T 12456—2021《食品中总酸的测定》,采用酸碱滴定法测定。
有机酸含量:参照国标GB 5009.157—2016《食品安全国家标准食品中有机酸的测定》,采用高效液相色谱法测定。
粗多糖含量:参照牛晓方等[9]的方法,以葡萄糖质量浓度(x)为横坐标,吸光度值(y)为纵坐标,绘制葡萄糖标准工作曲线,得到葡萄糖标准曲线回归方程为y=0.010 3x-0.002 3(相关系数R2=0.999),根据标准曲线回归方程计算粗多糖含量。
总黄酮含量:参照GB/T 20574—2006《蜂胶中总黄酮含量的测定方法分光光度比色法》检测,以芦丁对照品的质量浓度(x)为横坐标,吸光度值(y)为纵坐标,绘制芦丁标准曲线,得到芦丁标准曲线回归方程为y=13x-0.000 6(相关系数R2=0.996 7),根据标准曲线回归方程计算总黄酮含量。
甘草酸、甘草次酸含量:参照SN/T3854—2014《出口食品中天然甜味剂甜菊糖苷、甜菊双糖苷、甘草酸、甘草次酸的测定高效液相色谱法》测定。阿魏酸含量:参照团体标准T/SHRH025—2019《化妆品中阿魏酸含量的测定》测定。
1.3.4 数据处理
试验数据用Excel 2016软件进行初步处理后,采用SPSS 22.0软件进行统计分析,采用One-way ANOVA进行方差分析,最小显著差别(least significant difference,LSD)法进行组间多重比较,结果以“平均值±标准差”表示,P<0.05表示差异显著。
2 结果与分析
2.1 植物乳杆菌发酵对复方中药pH值和微生物数量的影响
植物乳杆菌发酵对复方中药pH值和微生物数量的影响见表1。由表1可知,与对照组相比,实验组均可显著降低发酵复方中药pH值(P<0.05),发酵72 h时均降至4.50以下,实验组间差异不显著(P>0.05)。实验组均可显著提高发酵复方中药的乳杆菌数量(P<0.05),发酵24h、48h和72h时,实验组的乳杆菌数量均可达到109 CFU/g。发酵过程中,对照组大肠杆菌活菌数呈增加趋势,发酵72 h时达到(1.13±0.20)×103 CFU/g,而实验组均未检出大肠杆菌;对照组霉菌活菌数呈增加趋势,发酵72 h时达到(5.61±0.23)×103CFU/g,而植物乳杆菌BLCC2-0015发酵复方中药的霉菌活菌数呈下降趋势,发酵72 h时低于100 CFU/g,植物乳杆菌BLCC2-0126和BLCC2-0410发酵复方中药均未检出霉菌。结果表明,植物乳杆菌发酵可提高复方中药的乳杆菌活菌数,降低大肠杆菌及霉菌活菌数,且植物乳杆菌BLCC2-0126效果最好,其次为植物乳杆菌BLCC2-0410。耿江苏[8]研究证实,使用益生菌发酵鱼腥草等中药,可提高中药益生菌数量至5.68×108 CFU/mL,4 ℃保存一个月后活菌数为4.80×108 CFU/mL,显微镜检查无杂菌污染,与本试验结果一致。
表1 植物乳杆菌发酵对复方中药pH值和微生物数量的影响
Table 1 Effects of Lactobacillus plantarum fermentation on pH and microbial number of compound Chinese medicine
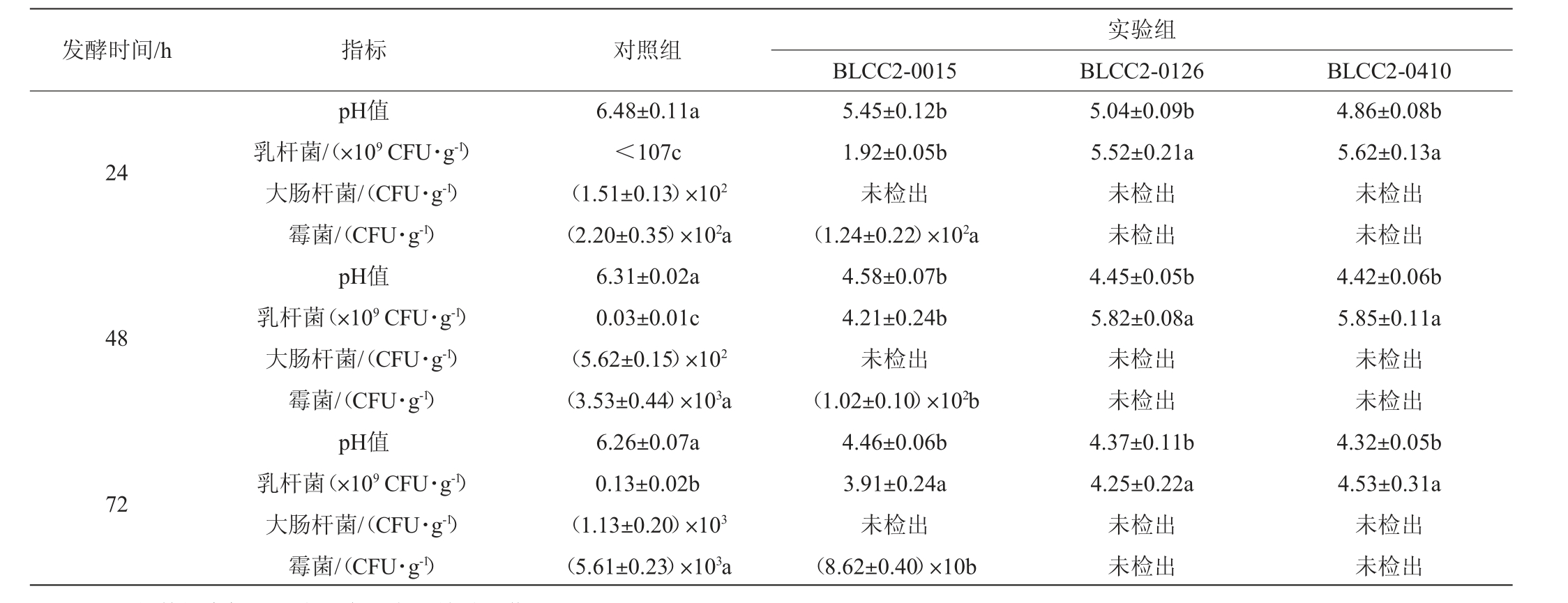
注:同行数据肩标不同小写字母表示差异显著(P<0.05)。下同。
发酵时间/h 指标 对照组24 48 72 pH值乳杆菌/(×109 CFU·g-1)大肠杆菌/(CFU·g-1)霉菌/(CFU·g-1)pH值乳杆菌(×109 CFU·g-1)大肠杆菌/(CFU·g-1)霉菌/(CFU·g-1)pH值乳杆菌(×109 CFU·g-1)大肠杆菌/(CFU·g-1)霉菌/(CFU·g-1)6.48±0.11a<107c(1.51±0.13)×102(2.20±0.35)×102a 6.31±0.02a 0.03±0.01c(5.62±0.15)×102(3.53±0.44)×103a 6.26±0.07a 0.13±0.02b(1.13±0.20)×103(5.61±0.23)×103a BLCC2-0015 5.45±0.12b 1.92±0.05b未检出(1.24±0.22)×102a 4.58±0.07b 4.21±0.24b未检出(1.02±0.10)×102b 4.46±0.06b 3.91±0.24a未检出(8.62±0.40)×10b实验组BLCC2-0126 BLCC2-0410 5.04±0.09b 5.52±0.21a未检出未检出4.45±0.05b 5.82±0.08a未检出未检出4.37±0.11b 4.25±0.22a未检出未检出4.86±0.08b 5.62±0.13a未检出未检出4.42±0.06b 5.85±0.11a未检出未检出4.32±0.05b 4.53±0.31a未检出未检出
2.2 植物乳杆菌发酵对复方中药总酸和机酸含量的影响
植物乳杆菌发酵对复方中药总酸及有机酸含量的影响分别见表2和表3。
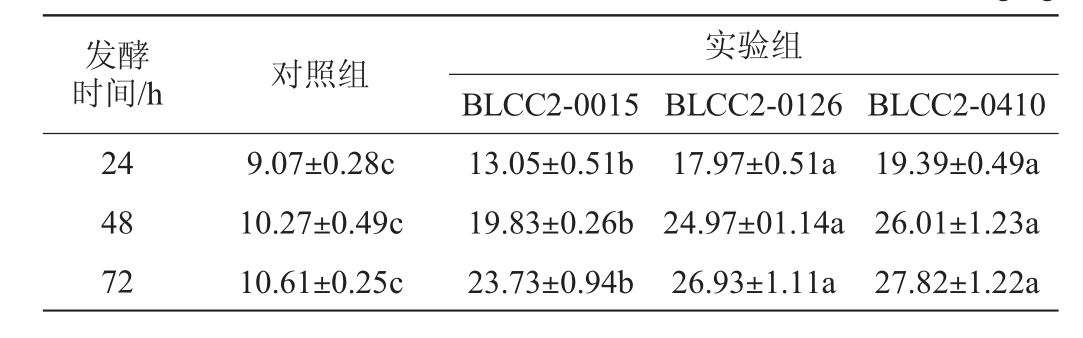
表2 植物乳杆菌发酵对复方中药总酸含量的影响
Table 2 Effects of Lactobacillus plantarum fermentation on total acid contents of compound Chinese medicine g/kg
发酵时间/h 对照组BLCC2-0015实验组BLCC2-0126 BLCC2-0410 24 48 72 9.07±0.28c 10.27±0.49c 10.61±0.25c 13.05±0.51b 19.83±0.26b 23.73±0.94b 17.97±0.51a 24.97±01.14a 26.93±1.11a 19.39±0.49a 26.01±1.23a 27.82±1.22a
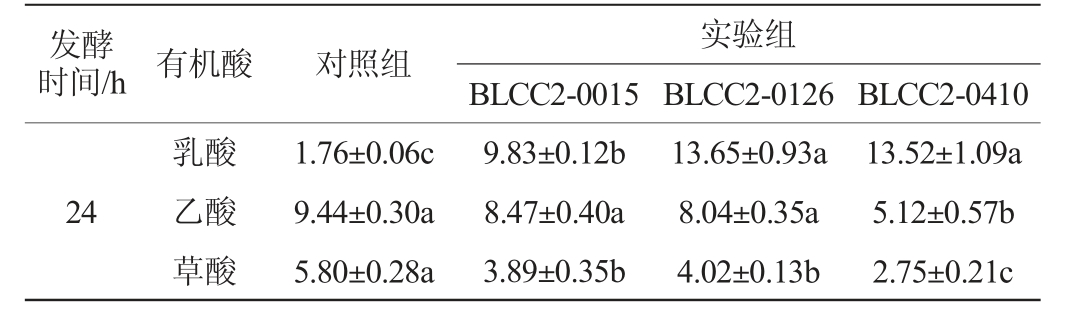
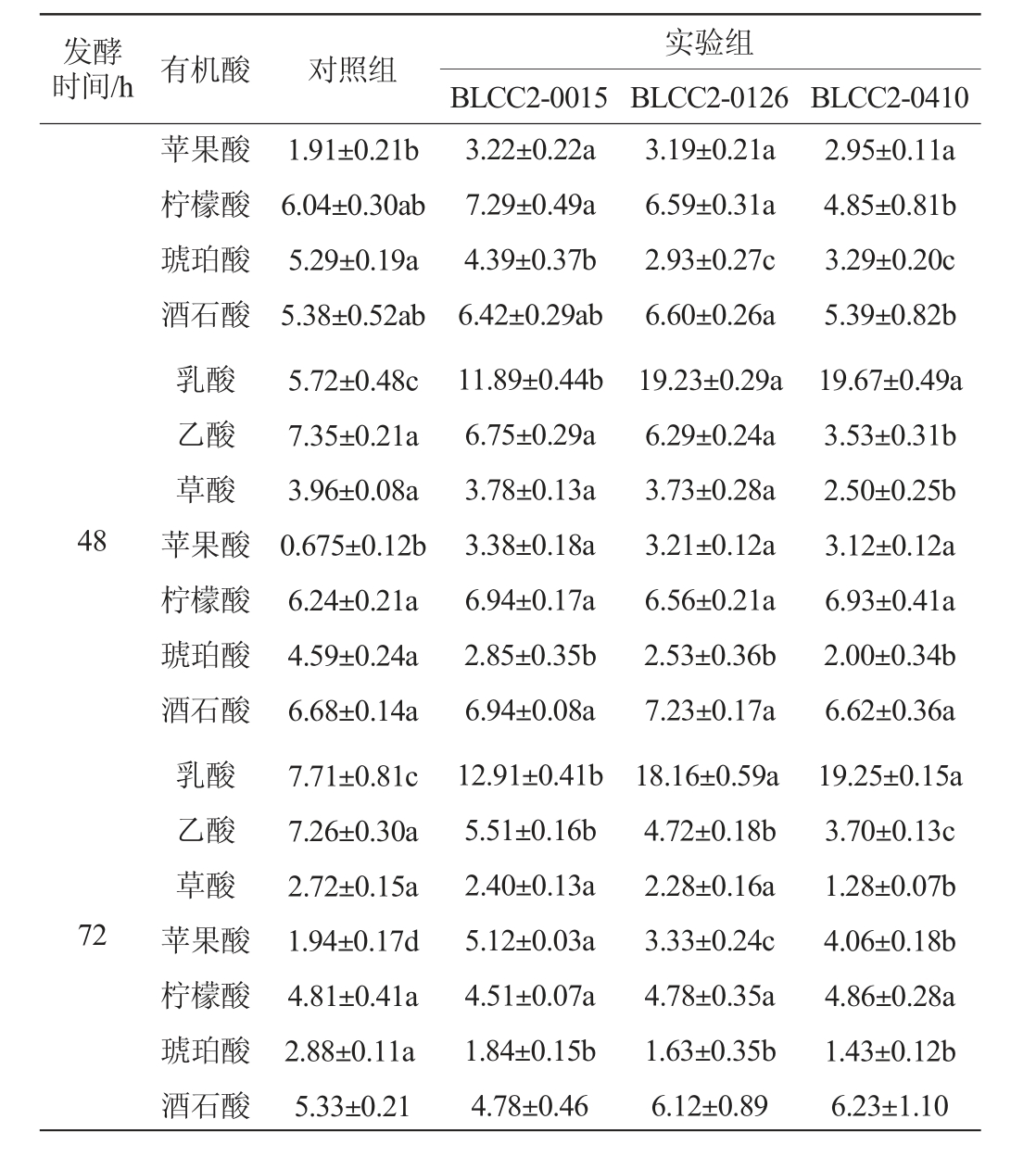
表3 植物乳杆菌发酵对复方中药有机酸含量的影响
Table 3 Effect of Lactobacillus plantarum fermentation on organic acid contents of compound Chinese medicine g/kg
发酵时间/h BLCC2-0015实验组BLCC2-0126 BLCC2-0410 24有机酸 对照组乳酸乙酸草酸1.76±0.06c 9.44±0.30a 5.80±0.28a 9.83±0.12b 8.47±0.40a 3.89±0.35b 13.65±0.93a 8.04±0.35a 4.02±0.13b 13.52±1.09a 5.12±0.57b 2.75±0.21c
续表
发酵时间/h 48 72有机酸 对照组苹果酸柠檬酸琥珀酸酒石酸乳酸乙酸草酸苹果酸柠檬酸琥珀酸酒石酸乳酸乙酸草酸苹果酸柠檬酸琥珀酸酒石酸1.91±0.21b 6.04±0.30ab 5.29±0.19a 5.38±0.52ab 5.72±0.48c 7.35±0.21a 3.96±0.08a 0.675±0.12b 6.24±0.21a 4.59±0.24a 6.68±0.14a 7.71±0.81c 7.26±0.30a 2.72±0.15a 1.94±0.17d 4.81±0.41a 2.88±0.11a 5.33±0.21 BLCC2-0015 3.22±0.22a 7.29±0.49a 4.39±0.37b 6.42±0.29ab 11.89±0.44b 6.75±0.29a 3.78±0.13a 3.38±0.18a 6.94±0.17a 2.85±0.35b 6.94±0.08a 12.91±0.41b 5.51±0.16b 2.40±0.13a 5.12±0.03a 4.51±0.07a 1.84±0.15b 4.78±0.46实验组BLCC2-0126 BLCC2-0410 3.19±0.21a 6.59±0.31a 2.93±0.27c 6.60±0.26a 19.23±0.29a 6.29±0.24a 3.73±0.28a 3.21±0.12a 6.56±0.21a 2.53±0.36b 7.23±0.17a 18.16±0.59a 4.72±0.18b 2.28±0.16a 3.33±0.24c 4.78±0.35a 1.63±0.35b 6.12±0.89 2.95±0.11a 4.85±0.81b 3.29±0.20c 5.39±0.82b 19.67±0.49a 3.53±0.31b 2.50±0.25b 3.12±0.12a 6.93±0.41a 2.00±0.34b 6.62±0.36a 19.25±0.15a 3.70±0.13c 1.28±0.07b 4.06±0.18b 4.86±0.28a 1.43±0.12b 6.23±1.10
由表2可知,与对照组相比,实验组均可显著提高总酸含量(P<0.05),其中,植物乳杆菌BLCC2-0410发酵复方中药中总酸含量最高,其次为植物乳杆菌BLCC2-0126发酵复方中药,且均显著高于植物乳杆菌BLCC2-0015发酵复方中药(P<0.05)。植物乳杆菌BLCC2-0410发酵复方中药72 h时总酸含量达到(27.82±1.22)g/kg。结果表明,植物乳杆菌发酵可以显著提高复方中药中的总酸含量,且植物乳杆菌BLCC2-0410提高效果最好,其次为BLCC2-0126。亓秀晔等[10]研究发现,植物乳杆菌发酵猪全价料,总酸含量可达到20.68 g/kg,与本试验结果一致。
有机酸是乳酸菌发酵饲料提高饲料风味的重要指标,能够改善中药气味和口感辛辣刺鼻等动物适口性的问题,其含量的多少与发酵程度密切相关[11]。吴锦兰等[12]研究发现,在乳酸菌LB-1-23接种量2.6%、pH值5.5、发酵温度32 ℃条件下发酵30 h,乳酸产量达到12.74 g/L。由表3可知,与对照组相比,实验组可显著提高乳酸和苹果酸含量(P<0.05),降低乙酸、草酸和琥珀酸含量,对酒石酸和柠檬酸影响不显著(P>0.05)。这与王芮东等[13]的研究结果一致,发酵过程中乳杆菌繁殖利用乙酸、草酸等产生更多的乳酸、苹果酸,导致乳酸、苹果酸含量升高。乳酸、苹果酸的增加可以提高中药的酸香味,乙酸、草酸的降低可以减少中药的刺鼻味[11]。其中,植物乳杆菌BLCC2-0410发酵效果最好,发酵复方中药72 h时,乳酸、苹果酸含量分别达到(19.25±0.15)g/kg、(4.06±0.18)g/kg,乙酸、草酸分别降低至(3.70±0.13)g/kg、(1.28±0.07)g/kg。
2.3 植物乳杆菌发酵对复方中药粗多糖和总黄酮含量的影响
植物乳杆菌发酵对复方中药粗多糖及总黄酮含量的影响分别见表4和表5。
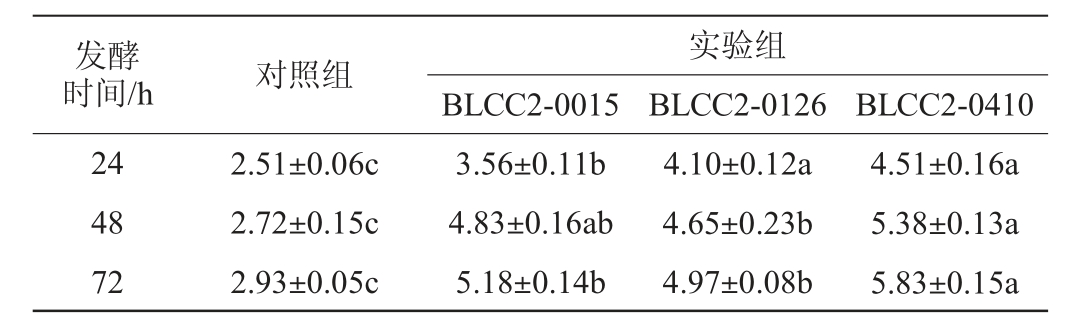
表4 植物乳杆菌发酵对复方中药粗多糖含量的影响
Table 4 Effect of Lactobacillus plantarum fermentation on crude polysaccharide contents of compound Chinese medicine%
发酵时间/h 对照组BLCC2-0015实验组BLCC2-0126 BLCC2-0410 24 48 72 2.51±0.06c 2.72±0.15c 2.93±0.05c 3.56±0.11b 4.83±0.16ab 5.18±0.14b 4.10±0.12a 4.65±0.23b 4.97±0.08b 4.51±0.16a 5.38±0.13a 5.83±0.15a
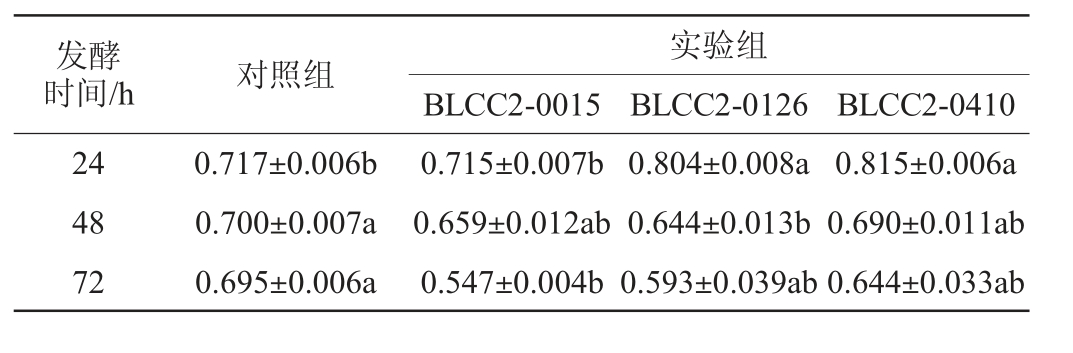
表5 植物乳杆菌发酵对复方中药总黄酮含量的影响
Table 5 Effect of Lactobacillus plantarum fermentation on total flavonoid contents of compound Chinese medicine%
发酵时间/h 对照组BLCC2-0015实验组BLCC2-0126 BLCC2-0410 24 48 72 0.717±0.006b 0.700±0.007a 0.695±0.006a 0.715±0.007b 0.659±0.012ab 0.547±0.004b 0.804±0.008a 0.644±0.013b 0.593±0.039ab 0.815±0.006a 0.690±0.011ab 0.644±0.033ab
粗多糖对氧自由基和羟自由基都有很好的清除作用,是一种天然抗氧化剂[14]。由表4可知,与对照组相比,实验组均可显著提高粗多糖含量(P<0.05),且以植物乳杆菌BLCC2-0410发酵复方中药的粗多糖含量最高,发酵72 h时达到(5.83±0.15)%。分析原因主要是微生物代谢过程中会分泌大量纤维素酶、蛋白酶、果胶酶、淀粉酶等胞外酶,可以使细胞间隙增大,细胞破裂,中药成分溶出,提高中药有效成分得率,随着处理时间的延长,溶出的多糖不断积累[15]。唐鑫等[16]研究发现,植物乳杆菌CCFM8661发酵天山雪莲粗多糖可达1.29 g/L。
有研究表明,总黄酮具有非常强的抗氧化以及消除自由基的作用[17]。由表5可知,与对照组相比,发酵24 h时,植物乳杆菌BLCC2-0126和BLCC2-0410发酵复方中药总黄酮含量显著升高(P<0.05),分别提高12.13%和13.67%。总黄酮含量的增加,从结构上增加了活性OH基团,减少空间位阻,可以提高中药的抗氧化活性[17]。随发酵时间延长,植物乳杆菌发酵复方中药总黄酮含量均呈下降趋势,发酵48 h时,植物乳杆菌BLCC2-0126发酵复方中药中总黄酮含量显著低于对照组(P<0.05),这可能是因为营养物质消耗殆尽,植物乳杆菌分泌多种糖苷酶分解黄酮糖苷类物质作为能源物质消耗[2]。
2.4 植物乳杆菌发酵对复方中药阿魏酸、甘草酸及甘草次酸含量的影响
2.4.1 植物乳杆菌发酵对复方中药阿魏酸含量的影响
阿魏酸是一种安全环保的天然抗菌剂,能够有效抑制大肠杆菌、金黄色葡萄球菌和志贺氏菌[18]。植物乳杆菌发酵复方中药对阿魏酸含量的影响见表6。
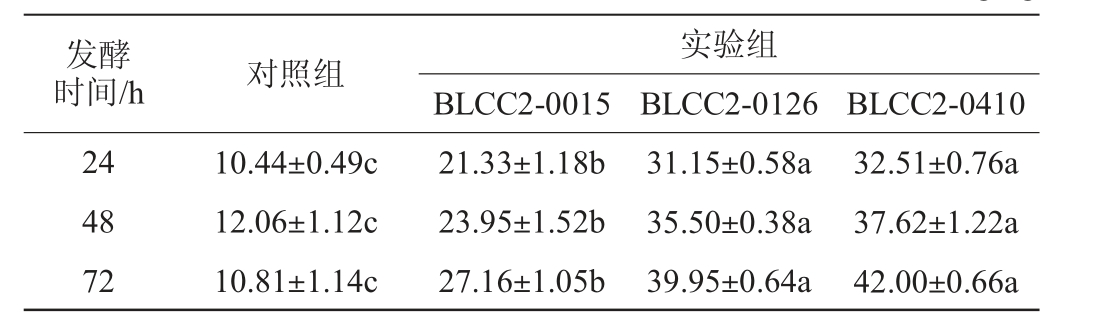
表6 植物乳杆菌发酵对复方中药阿魏酸含量的影响
Table 6 Effect of Lactobacillus plantarum fermentation on ferulic acid contents of compound Chinese medicine mg/kg
发酵时间/h 对照组BLCC2-0015实验组BLCC2-0126 BLCC2-0410 24 48 72 10.44±0.49c 12.06±1.12c 10.81±1.14c 21.33±1.18b 23.95±1.52b 27.16±1.05b 31.15±0.58a 35.50±0.38a 39.95±0.64a 32.51±0.76a 37.62±1.22a 42.00±0.66a
由表6可知,与对照组相比,实验组均可显著提高阿魏酸含量(P<0.05),且植物乳杆菌BLCC2-0126和BLCC2-0410发酵复方中药的阿魏酸含量显著高于植物乳杆菌BLCC2-0015(P<0.05)。发酵24 h、48 h和72 h时均以植物乳杆菌BLCC2-0410发酵复方中药时阿魏酸含量最高,分别比对照组高211%、212%和289%,且随发酵时间的延长呈增加趋势。分析原因可能是,在植物细胞中阿魏酸通过苷键或酯键与纤维素等相连接,益生菌发酵可以产阿魏酸酯酶,水解阿魏酸与纤维素、半纤维素、木质素等相互作用的酯键,破坏细胞壁的致密网状结构释放出阿魏酸,使得阿魏酸含量升高[19-20]。结果表明,植物乳杆菌发酵可以提高复方中药中阿魏酸的含量,这与尹志娜等[21-22]的研究结果一致。
2.4.2 植物乳杆菌发酵对复方中药甘草酸及甘草次酸含量的影响
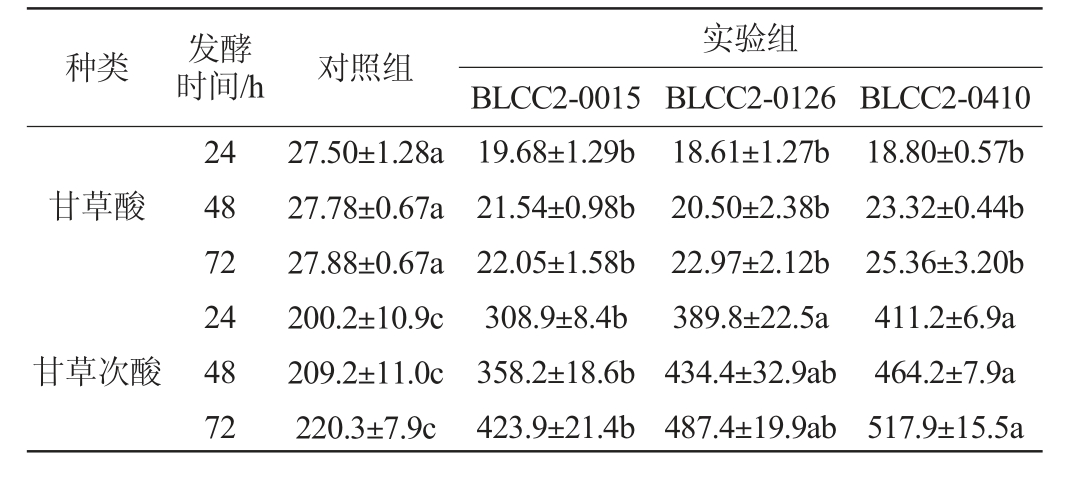
植物乳杆菌发酵对复方中药甘草酸和甘草次酸含量的影响见表7。甘草次酸具有抗炎、抗病毒和提高机体免疫力等作用[23]。由表7可知,与对照组相比,实验组甘草酸含量显著降低(P<0.05),甘草次酸含量显著升高(P<0.05),其中,植物乳杆菌BLCC2-0410发酵复方中药72 h时甘草次酸含量最高为517.9 mg/kg,比对照组高135.09%。分析原因可能是植物乳杆菌发酵复方中药产生甘草酸水解酶,水解甘草酸产生甘草次酸[24]。吕丽静等[25]研究发现,酿酒酵母(Saccharomyces cerevisiae)与植物乳杆菌发酵甘草药渣,甘草苷和甘草酸含量有所下降;樊梅娜等[26]研究发现,植物乳杆菌NBL-B3003发酵甘草24 h,甘草酸含量较未发酵降低90.44%。本研究中植物乳杆菌发酵甘草后甘草酸含量下降,推测亦可能是由于植物乳杆菌促进了甘草酸的生物转化引起的。同时已有研究表明,在体内甘草酸转化成甘草次酸后才发挥药理作用,包括解毒、抑制肝纤维化、抗炎和抗肿瘤等[27]。
表7 植物乳杆菌发酵对复方中药甘草酸和甘草次酸含量的影响
Table 7 Effect of Lactobacillus plantarum fermentation on glycyrrhizic acid and glycyrrhetinic acid contents of compound Chinese medicine mg/kg
种类发酵时间/h 对照组BLCC2-0015实验组BLCC2-0126 BLCC2-0410甘草酸甘草次酸24 48 72 24 48 72 27.50±1.28a 27.78±0.67a 27.88±0.67a 200.2±10.9c 209.2±11.0c 220.3±7.9c 19.68±1.29b 21.54±0.98b 22.05±1.58b 308.9±8.4b 358.2±18.6b 423.9±21.4b 18.61±1.27b 20.50±2.38b 22.97±2.12b 389.8±22.5a 434.4±32.9ab 487.4±19.9ab 18.80±0.57b 23.32±0.44b 25.36±3.20b 411.2±6.9a 464.2±7.9a 517.9±15.5a
3 结论
采用植物乳杆菌(Lactobacillus plantarum)BLCC2-0015、BLCC2-0126和BLCC2-0410固体发酵复方中药(黄芪、甘草和益母草等)后,可降低复方中药的pH值;提高乳杆菌活菌数,抑制大肠杆菌(Escherichia coli)及霉菌的生长;提高总酸、乳酸、苹果酸、粗多糖、阿魏酸及甘草次酸的含量。其中,植物乳杆菌BLCC2-0410发酵效果最好,发酵72 h时,复方中药的pH为4.32,乳杆菌活菌数为4.53×109 CFU/g,大肠杆菌及霉菌未检出;总酸、乳酸、苹果酸、粗多糖、阿魏酸和甘草次酸含量均显著升高(P<0.05),分别为27.82 g/kg、19.25 g/kg、4.06 g/kg、5.83%、42.00 mg/kg和517.9 mg/kg。
[1]闫冰,刘来亭,牛菁懿.可饲用天然植物及其提取物在养殖业中的应用现状[J].饲料研究,2022,45(13):127-130.
[2]谢炎福,押辉远,张新雨,等.植物乳杆菌对淫羊藿黄酮苷类成分的转化作用[J].中国酿造,2022,41(12):103-109.
[3]屈青松,周晴,石艳双,等.乳酸菌发酵中药功能及其增效机制的研究进展[J].环球中医药,2022,15(9):1707-1715.
[4]侯金江,孙兴滨,高浩泽,等.促生长抗生素禁用后养猪场多重耐药菌群及耐药特征变化[J].农业环境科学学报,2023,42(3):682-691.
[5]王福刚.复合益生菌培养物对肉羊生长性能、血清生化指标、抗氧化指标、免疫指标的影响[J].饲料研究,2022,45(20):14-17.
[6]史洪涛,乔宏兴,刘松,等.发酵扶正解毒口服液对蛋鸡生产性能、抗氧化功能及肠道组织结构的影响[J].中国畜牧杂志,2020,56(5):152-156.
[7]李继开,贾琳,石建存,等.益生菌发酵中药饲料添加剂工艺的优化[J].饲料研究,2021,44(16):59-62.
[8]耿江苏.中药-益生菌复合微生态饲料添加剂的制备[D].合肥:安徽农业大学,2022.
[9]牛晓方,高一军,怀宝刚,等.硫酸-苯酚法测定六种牡丹叶中总多糖的含量[J].山东农业工程学院学报,2021,38(4):33-35.
[10]亓秀晔,谢全喜,陈振,等.乳杆菌酵母菌及混菌对发酵饲料品质的影响[J].中国酿造,2017,36(1):75-78.
[11]谢全喜,侯楠楠,陈静,等.复合益生菌和纤维素酶联合发酵对小麦秸秆营养品质的影响[J].中国酿造,2021,40(9):196-199.
[12]吴锦兰,付玉麟,周小玲,等.酸笋中高产乳酸乳酸菌的筛选、鉴定及发酵条件优化[J].中国酿造,2021,40(1):65-69.
[13]王芮东,李楠,卫博慧,等.不同发酵方式萝卜泡菜中有机酸的变化分析[J].中国调味品,2021,46(5):139-143.
[14]李玲玉,邱志常,朱姗姗,等.响应面法优化牛蒡多糖超声辅助提取工艺与抗氧化活性评价[J].食品科技,2020,45(11):197-204,211.
[15]汪鹏,黄鹏,饶力群,等.发酵型中药饲料添加剂的研究进展[J].饲料研究,2019,42(11):115-118.
[16]唐鑫,蔡美君,崔树茂,等.发酵天山雪莲粗多糖的菌株筛选及护肤功效研究[J].微生物学报,2023,63(4):1551-1565.
[17]杨丹,杨放晴,燕娜娜,等.黑曲霉发酵对陈皮黄酮类成分及抗氧化活性的影响[J].食品科技,2019,44(12):23-27.
[18]王宁.黑曲霉和好食脉孢菌发酵麸皮产总阿魏酸的工艺优化及抑菌效果检测[D].晋中:山西农业大学,2020.
[19]王清龙,陈园园,刘延波,等.高产阿魏酸酯酶菌株的筛选鉴定及产酶条件优化[J].中国酿造,2022,41(10):83-88.
[20]刘蓓一,韦青,田吉鹏,等.羊瘤胃液中产阿魏酸酯酶乳酸菌的筛选及对水稻秸秆青贮品质的影响[J].江苏农业学报,2022,38(5):1306-1314.
[21]尹志娜,吴晖,赖富饶,等.两种丝状真菌发酵小麦麸皮中酚酸的释放及与阿魏酸酯酶和木聚糖酶的关系[J].现代食品科技,2017,33(3):81-87.
[22]赵苏苏,高佳,吕冰,等.黑曲霉发酵麸皮产总阿魏酸工艺优化及其抑菌活性初探[J].中国粮油学报,2023,38(12):167-175.
[23]赵文俊,吴嘉南,何国庆,等.甘草次酸生物合成菌株的筛选与发酵条件优化[J].中国食品学报,2020,20(5):113-119.
[24]李艳宾,张琴.产黄酮甘草内生真菌YF-A的发酵工艺优化[J].食品科技,2016,41(11):25-30.
[25]吕丽静,屈青松,周晴,等.甘草药渣发酵工艺优化及成分分析、抗氧化活性的研究[J].中南药学,2022,20(10):2312-2317.
[26]樊梅娜,王丽荣,张国珍,等.益生菌发酵甘草对甘草酸含量及其抑菌活性的影响[J].中国畜牧杂志,2022,58(10):282-286.
[27]周菲.甘草次酸衍生物的设计、合成与抗肿瘤活性初步研究[D].北京:北京中医药大学,2020.