山西食醋年产量已超过80万吨,在全国食醋市场占有率达20%左右,产品遍布我国大江南北,依靠自身独特风味,深受广大消费者喜爱。在山西食醋生产过程中熏醅技术至关重要,对醋风味的改善十分显著[1]。传统熏醅过程是将发酵完成的醋醅置于陶缸之中,用煤火烘烤陶缸将醋醅加热,每天倒缸一次,经过连续3~5 d烘烤后,醋醅色泽由淡黄色变为深褐色后结束熏醅,醋由此获得了焦香、酯香、醋香有机融合的风味特色和特殊的光泽[2]。
山西老陈醋的风味主要由非挥发性化合物和挥发性化合物组成。其中有关于山西老陈醋熏醅过程中的挥发性化合物目前共检测出醇类、酸类、酯类、醛类、酮类、酚类、杂环类、烃类、硫醚类9个大类[3]。有研究通过熏醅前后的对比揭示了熏醅过程中部分化合物的一些变化规律,如熏醅过程中可挥发性酸类和酯类物质含量降幅较大,醛类和杂环类化合物含量明显升高等[4-6]。在这些物质中吡嗪类属于熏醅过程中新产生的化合物种类之一,且在新化合物中占比较大,是熏醅贡献的重要风味物质[7],后期的陈酿过程中含量仍会小幅升高[8],其中四甲基吡嗪已被列为山西老陈醋标志成分[10],为山西老陈醋提供了烘焙、烧烤、坚果等多种香味[9]。吡嗪及其衍生物除用于香料及食品添加外,其表现出的多种生物活性在医药领域也具有很高的应用价值,研究发现,其在抗癌、抗菌、抗结核、抗氧化剂、抗抑郁和抗惊厥等方面均有一定的应用价值[11]。
吡嗪类化合物作为山西老陈醋中重要的保健和风味组分,目前对其在熏醅过程中的积累规律并未深入研究。有关于山西老陈醋熏醅过程中吡嗪类化合物的变化,大多仅将其作为气味组成的一部分对比熏醅前后含量变化[4-6],然而仅通过熏醅前后含量的对比不能完全揭示熏醅过程中吡嗪类化合物的产生过程、变化规律等问题,因此熏醅工艺改进和环保熏醅设备研发中面临的吡嗪类变化问题也没有得到有效解决[12-13]。为了进一步对煤火熏醅中吡嗪类产生过程进行研究,本研究将对传统煤火陶缸熏醅进行分区定点采样,通过顶空固相微萃取(headspace solidphase-microextraction,HS-SPME)结合气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)联用技术对其进行定量分析,揭示熏醅过程中不同时间不同陶缸位点的吡嗪类的生成过程,为进一步提升山西老陈醋熏醅工艺的精准控制及产品质量提供科学依据。
1 材料与方法
1.1 材料与试剂
NaCl(分析纯):天津市风船化学试剂科技有限公司;正辛醇标品(优级纯):美国Sigma公司。其他试剂均为国产分析纯。
1.2 仪器与设备
手动SPME进样器、SPME萃取头(50/30 μm DVB-CARPDMS):美国Supelco公司;7890A/5975C型气相色谱-质谱联用仪、HP-5 MS毛细管气相色谱柱(30 m×0.25 mm×0.25 μm):美国Agilent公司。
1.3 方法
1.3.1 熏醅方法及取样方法
本研究所用山西老陈醋熏醅过程为传统煤火5 d熏醅法,将发酵完成的醋醅置于陶缸之中,用煤火烘烤陶缸将醋醅加热,每天倒缸一次,经过连续5 d烘烤后,完成熏醅。
样品取自山西某醋企的山西老陈醋传统熏醅生产车间,每日在翻醅过程中依次在缸的顶部、中部、下部按照缸中心位点,缸半径1/2位点,缸边缘三个截面取样,并测定熏醅温度,图1中所标注的每个三角位点为取样分布点,每缸取9个样品,样品迅速冷却后存入-80 ℃冰箱中待测,连续取3批次样品进行测定。
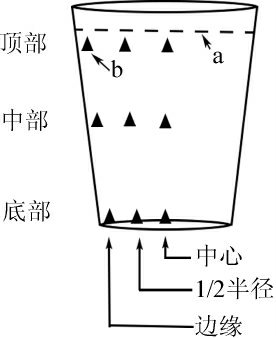
图1 陶缸熏醅取样位点示意图
Fig.1 Schematic diagram of sampling sites for fumigation process in pottery jar
a 陶缸中醋醅高度;b 取样点。
1.3.2 顶空固相微萃取条件
SPME萃取头每次萃取前,先在GC进样口老化至无杂峰,老化条件:230 ℃保持30 min。萃取方法:在15 mL萃取瓶中加入1 g样品、1 g NaCl、2 mL蒸馏水,将瓶盖拧紧。先将萃取瓶放置在45 ℃水浴中搅拌保温平衡30 min,将萃取针头插入萃取瓶,推出萃取针中的纤维头,使其与样品保持约1.5 cm的距离,萃取40 min。萃取完成后直接进样,进样口温度设置为250 ℃,无分裂模式下解吸5 min[2]。
1.3.3 GC-MS参数条件
色谱条件:HP-5 MS柱(30 m×0.25 mm×0.25 μm),进样口温度250 ℃,起始温度40 ℃,保持3.5 min,之后以5 ℃/min的速率上升至90 ℃,再以6 ℃/min的速率上升至230 ℃,保持2 min。分离载气为氦气(He),流速为1 mL/min[2]。质谱条件:离子源温度230 ℃,电离方式采用电子离子化模式,电子能量70 eV,扫描范围33~450 m/z。
1.3.4 挥发性化合物的定性及定量
通过对比美国国家标准与技术研究院(national institute of standards and technology,NIST)的参考谱库对化合物进行定性,要求匹配度>91%,采用内标法(正辛醇)定量。
1.3.5 数据分析
数据分析及作图均使用R软件(V 4.2.2),显著性分析使用Tukey法(P<0.05)。
2 结果与分析
2.1 熏醅温度变化分析
温度可以促进吡嗪类化合物的生成和积累[14],但山西老陈醋醋酸发酵是在一个湿润疏松多孔隙的固态发酵环境下进行[15],发酵完成后的醋醅直接用于熏醅,这种疏松的醋醅不利于热传导,熏醅过程中不同陶缸位点的醋醅温度变化见表1。
表1 熏醅过程中不同陶缸位点的醋醅温度变化
Table 1 Changes of temperature of vinegar grains at different locations in jars during the fumigation process
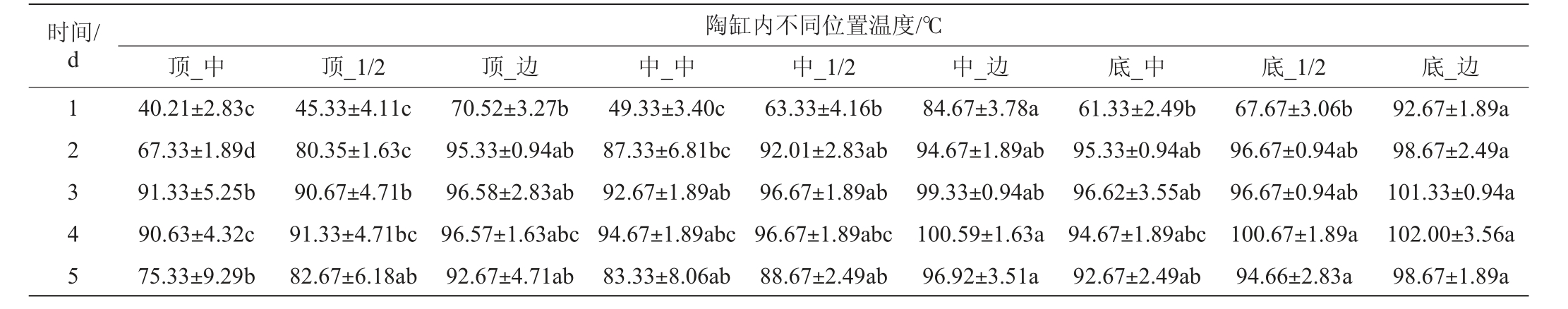
注:同行不同字母表示样品之间差异显著(P<0.05)。陶缸位置名称为图1中横截面与纵截面取样位点标注的第一个字,组合方式为(横截面_纵截面)。
时间/d 1 2 3 4 5陶缸内不同位置温度/℃顶_中 顶_1/2 顶_边 中_中 中_1/2 中_边 底_中 底_1/2 底_边40.21±2.83c 67.33±1.89d 91.33±5.25b 90.63±4.32c 75.33±9.29b 45.33±4.11c 80.35±1.63c 90.67±4.71b 91.33±4.71bc 82.67±6.18ab 70.52±3.27b 95.33±0.94ab 96.58±2.83ab 96.57±1.63abc 92.67±4.71ab 49.33±3.40c 87.33±6.81bc 92.67±1.89ab 94.67±1.89abc 83.33±8.06ab 63.33±4.16b 92.01±2.83ab 96.67±1.89ab 96.67±1.89abc 88.67±2.49ab 84.67±3.78a 94.67±1.89ab 99.33±0.94ab 100.59±1.63a 96.92±3.51a 61.33±2.49b 95.33±0.94ab 96.62±3.55ab 94.67±1.89abc 92.67±2.49ab 67.67±3.06b 96.67±0.94ab 96.67±0.94ab 100.67±1.89a 94.66±2.83a 92.67±1.89a 98.67±2.49a 101.33±0.94a 102.00±3.56a 98.67±1.89a
由表1可知,经过第1天(24 h)熏醅后,边缘与中心的醋醅温度差异显著(P<0.05),底部边缘的醋醅温度已经达到92 ℃左右,但顶部中心位点的醋醅仍只有40 ℃左右,可见固态醋醅的传热过程十分缓慢。醋醅翻缸后继续加热,第2天(48 h)加热完成后,仍有中心位置几个位点的醋醅温度未达到90 ℃,但差异范围缩小,主要的温度差异为上部中心与其他位点之间。熏醅第3天和第4天醋醅温度最高,陶缸中所有位点的醋醅温度均超过90 ℃,底部靠近缸壁位置的醋醅温度甚至超过100 ℃,温度差异主要存在于由下至上不同取样层面之间,同一层面温度没有显著差异(P<0.05)。熏醅第5天时,陶缸中醋醅温度出现回落,靠近中上部位的醋醅温度重新降低至90 ℃以下,温度差异仍主要存在于陶缸由下至上不同层面之间。熏醅过程中醋醅内部始终存在较大温度差,除特定温度会影响吡嗪类化合物的形成外[16],较大温差所形成的温度梯度也会影响吡嗪类化合物的形成[17]。
2.2 熏醅过程中吡嗪类生成变化分析
在5 d熏醅过程中,吡嗪类化合物生成种类及相对比例测定结果见图2。
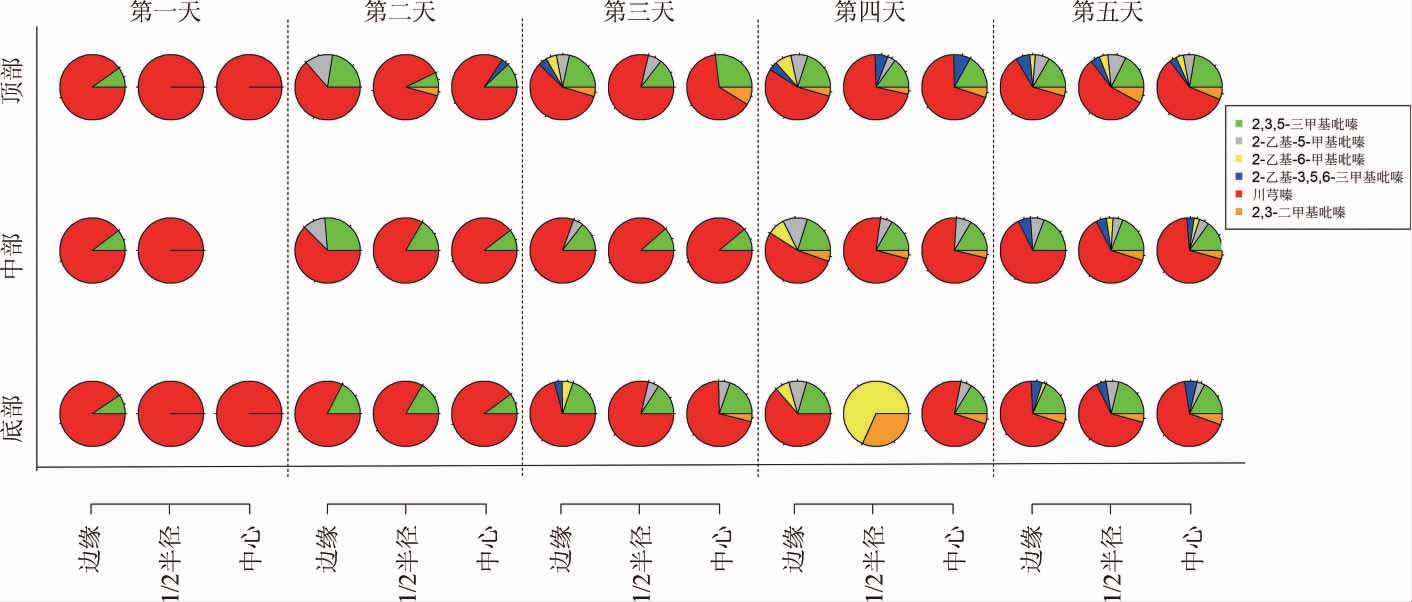
图2 熏醅过程中吡嗪类化合物生成种类及相对比例变化
Fig.2 Changes of types and relative proportions of pyrazines produced during the fumigation process
图中位点与图1取样位点相对应。下同。
由图2可知,所有熏醅样品共检测出6种吡嗪类化合物,分别为2,3,5-三甲基吡嗪、2-乙基-5-甲基吡嗪、2-乙基-6-甲基吡嗪、2-乙基-3,5,6-三甲基吡嗪、4-甲基吡嗪、2,3-二甲基吡嗪。其中4-甲基吡嗪含量最高,其次为2,3,5-三甲基吡嗪。
有两个位点与其他位点有显著不同,一个位点为第1天中部中心位置,未检测出任何吡嗪类化合物,而温度低于此位点的顶部中心和顶部1/2半径两个位置均检测出有4-甲基吡嗪生成;另一个位点为第4天底部1/2半径位点,仅含有2-乙基-6-甲基吡嗪和2,3-二甲基吡嗪,未检测出其他位点中含量较高的4-甲基吡嗪或2,3,5-三甲基吡嗪。吡嗪类化合物不是美拉德反应的终产物,其生成并积累需相应的pH值、氧气含量、温度及水分活度等多种条件[11]。有研究发现加热条件下产生的多种吡嗪类化合物,在相同加热条件加入微波辅助后不会产生,而是产生新的吡嗪类化合物[18]。推断这两个位点未积累在其他位点含量较高的4-甲基吡嗪或2,3,5-三甲基吡嗪,可能是这两个位点条件更利于分解而造成未检出的现象。
由图2亦可知,不同的吡嗪化合物生成时间和位点也有一定的区别,熏醅第1天检测出4-甲基吡嗪和2,3,5-三甲基吡嗪两种吡嗪类化合物,其中4-甲基吡嗪在第1天除中部中心位置外其他位点均有生成,而2,3,5-三甲基吡嗪仅在靠近缸壁边缘的顶中底三个位点生成。熏醅第2天在陶缸的顶中部开始生成三种吡嗪类物质,其中2-乙基-5-甲基吡嗪在边缘顶部、中部两个位点开始生成,2,3-二甲基吡嗪在顶部1/2半径位点开始生成,2-乙基-3,5,6-三乙基吡嗪在顶部中心位点开始生成。熏醅第3天在边缘顶部、底部两个位点检测出第6种吡嗪类化合物2-乙基-6-甲基吡嗪。熏醅第4、5天未发现其他新生成的吡嗪类化合物,仅为前3 d生成的6种吡嗪类化合物含量在动态变化。除4-甲基吡嗪和2,3,5-三甲基吡嗪外,其他含量较低的吡嗪种类在不同的研究中并不固定,如李攀恒等[19]检测多批次山西老陈醋发现有些可检出2-甲基吡嗪。山西老陈醋陈酿完成后也可能出现一些含量较低的吡嗪类化合物,如2-乙酰基-3,5-二甲基吡嗪[20]。但经过气味阈值分析发现对山西老陈醋风味影响较大的吡嗪类物质主要为4-甲基吡嗪,其次是2,3,5-三甲基吡嗪[21]。
2.3 主要吡嗪类化合物分析
2.3.1 4-甲基吡嗪含量变化分析
4-甲基吡嗪可以由微生物代谢产生[22],但山西老陈醋发酵过程中产生的4-甲基吡嗪相对于熏醅产生的4-甲基吡嗪几乎可以忽略不计[23],熏醅过程中4-甲基吡嗪含量变化见图3。
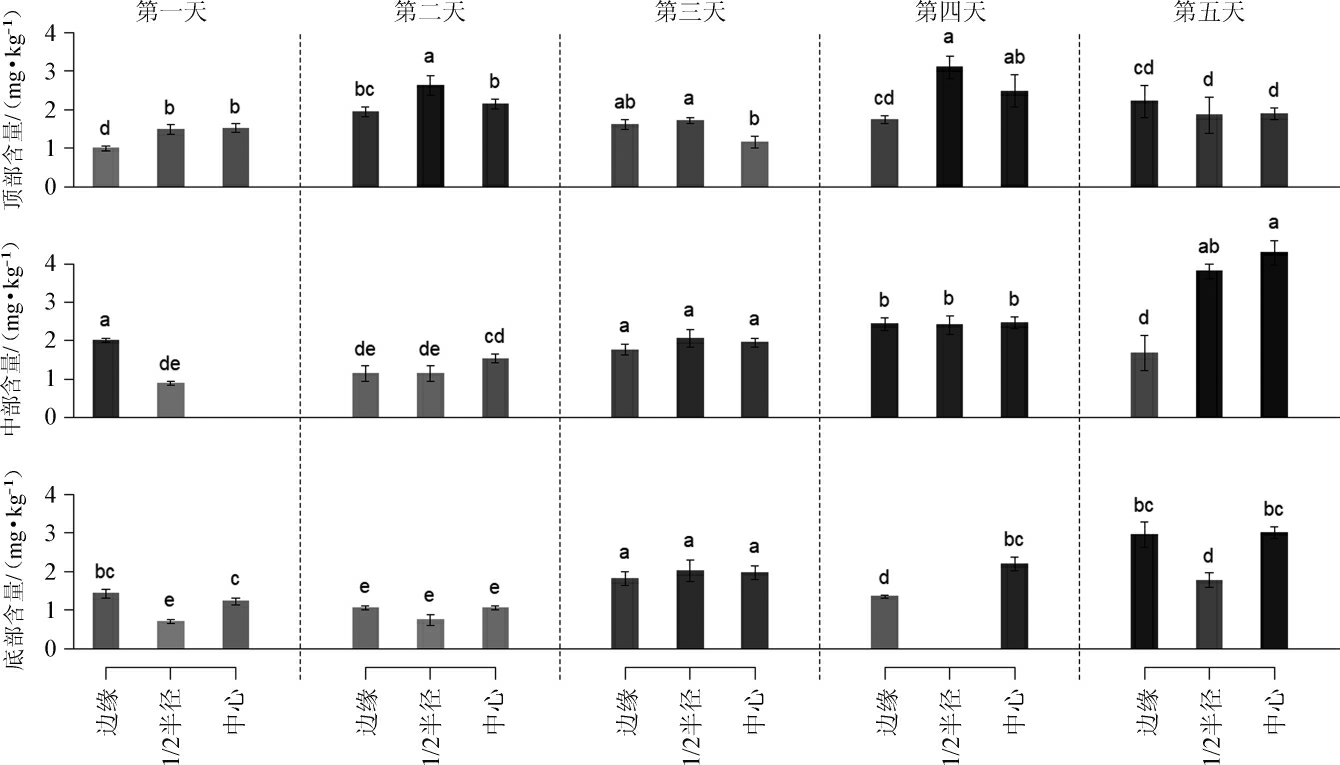
图3 熏醅过程中4-甲基吡嗪含量变化规律
Fig.3 Changes of 4-methylpyrazine contents during the fumigation process
同一天中不同字母表示样品之间差异显著(P<0.05)。下同。
由图3可知,在5 d的熏醅过程中,每天4-甲基吡嗪含量最高的点会出现在不同的部位。熏醅第1天结束后陶缸内除中部中心位点外,其他位点均产生了一定量的4-甲基吡嗪,此位点温度(49 ℃)虽然高于顶部1/2半径(45 ℃)和顶部中心(40 ℃),但其他两个位点均有4-甲基吡嗪生成,第1天所有位点中边缘中部位点产生的4-甲基吡嗪含量最高,位点温度为86 ℃。第2天熏醅结束后,4-甲基吡嗪含量在醋醅横截面之间出现显著差异(P<0.05),陶缸顶部的醋醅中4-甲基吡嗪含量显著上升(P<0.05),其中顶部1/2半径位点的含量最高,位点温度为80 ℃。熏醅第3天结束后,陶缸各位点4-甲基吡嗪含量差异较小,除顶部中心位点外,其他位点均无显著差异(P>0.05),此时陶缸内温度均超过90 ℃,各位点温度差相对于第1、2天进一步缩小。熏醅第4天后4-甲基吡嗪含量最高的位点为顶部1/2半径处,但同时底部1/2半径位点未检测到4-甲基吡嗪,熏醅过程中产生的4-甲基吡嗪是美拉德反应的中间产物,始终处于生成和消耗的过程中,因此含量变化是一个动态过程[24],此位点出现了消耗大于生成的现象,还需要进一步研究。熏醅第5天4-甲基吡嗪含量最高的位点为中部中心,其次为中部1/2半径处,两个位点无显著差异(P>0.05)。
熏醅第4、5天醋醅已充分升温,结合表1可知,4-甲基吡嗪含量较高的位点温度基本集中在82~92 ℃之间,第2天含量最高的位点也在此温度区间,此温度区间与模型研究结果较为相似[24]。温度是促进熏醅过程中吡嗪类化合物生成的重要条件,但同样也会促进美拉德反应其他步骤的速度,加快吡嗪类化合物参与美拉德下游产物生成[11]。
2.3.2 2,3,5-三甲基吡嗪含量变化分析
2,3,5-三甲基吡嗪可以为食品提供烤坚果、焙土豆香气[25],其含量虽然整体低于4-甲基吡嗪,但其气味阈值较低[26],因此也是山西老陈醋香气的重要组分,熏醅过程中2,3,5-三甲基吡嗪含量的变化见图4。
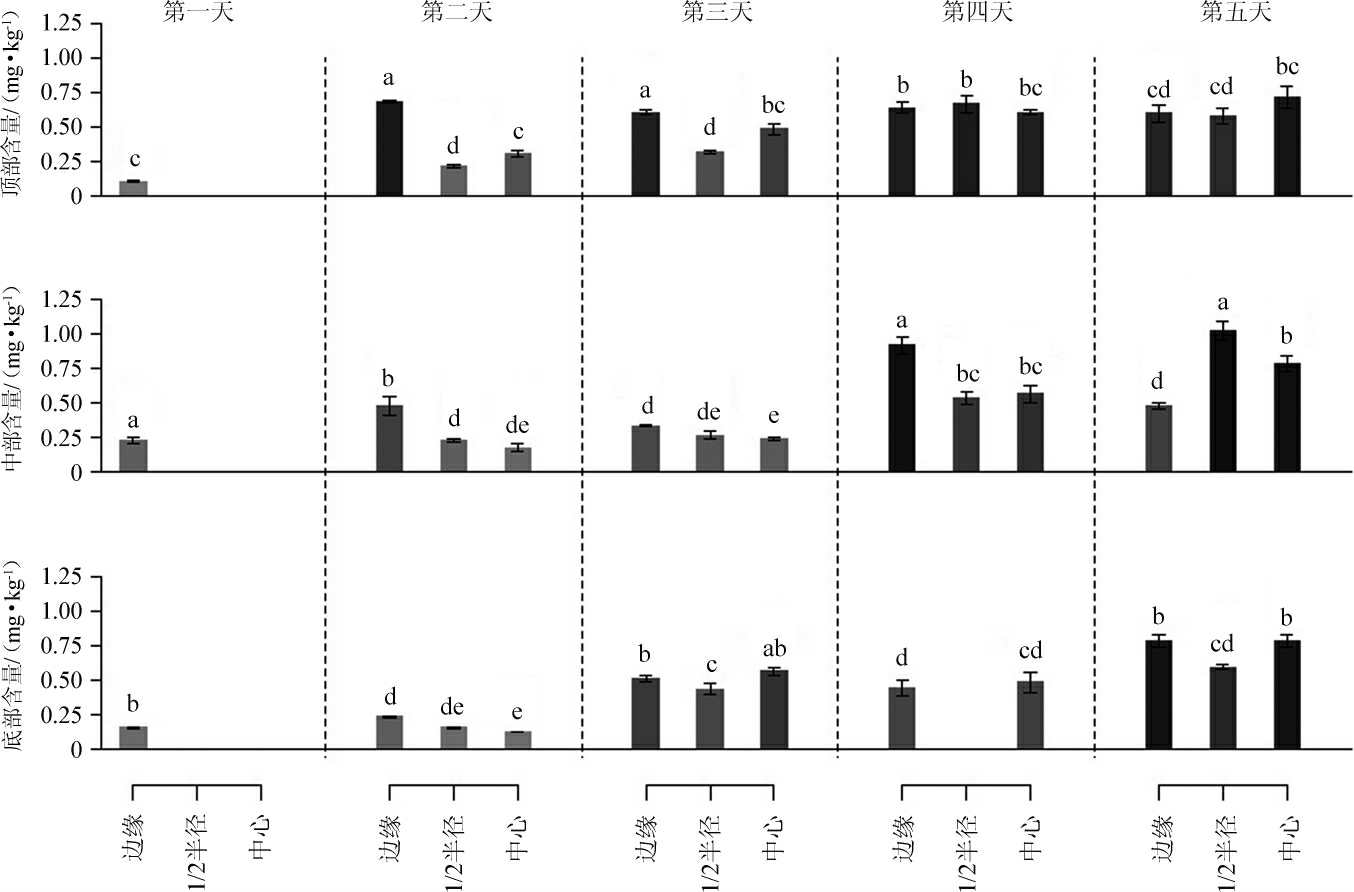
图4 熏醅过程中2,3,5-三甲基吡嗪含量变化规律
Fig.4 Changes of 2,3,5-trimethylpyrazine contents during the fumigation process
由图4可知,在5 d的熏醅过程中,每天2,3,5-三甲基吡嗪含量最高的位点均处于陶缸的中部或顶部区域,且位点为边缘或1/2半径处。熏醅第1天2,3,5-三甲基吡嗪仅在靠近陶缸壁的边缘受热位置开始生成;熏醅第2天,陶缸内其他位点的温度进一步上升,2,3,5-三甲基吡嗪也开始生成积累,但边缘各位点的2,3,5-三甲基吡嗪含量相对高于其他位点,特别是边缘顶部和边缘中部显著高于其他位点(P<0.05)。第3天和第4天2,3,5-三甲基吡嗪含量最高的位点虽然仍在靠近陶缸边缘的位置,但由于缸内各位点温度普遍升高,其他位点的含量也大幅升高。第5天2,3,5-三甲基吡嗪含量最高的位点为中部1/2半径位点,顶部位点和底部位点呈现相对均匀分布的状态。升温完成后(3~5 d),2,3,5-三甲基吡嗪生成规律与4-甲基吡嗪差有相似之处,第3天各位点含量差异缩小,第4、5天含量升高,最终含量较高的区域均在中部,这些变化除温度影响外,可能还与其他因素有关,如表层有蒸发作用[24],靠近缸壁或缸底直接加热温度较高其稳定性低于其他区域等[27]。
2.4 升温后吡嗪类生成分析
大量研究表明吡嗪类生成量会随温度的升高而逐步增大,但在不同的条件下吡嗪类最终累积量也有较大区别。为了进一步了解山西老陈醋煤火熏醅过程中不同位点与吡嗪类积累的关系,对熏醅升温完成后(3~5 d)的醋醅进行主成分分析,结果见图5。
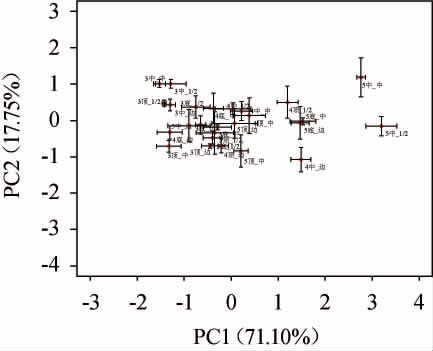
图5 熏醅过程中陶缸不同位点吡嗪类物质含量主成分分析
Fig.5 Principal component analysis of pyrazine contents at different locations during the fumigation process
由图5可知,第1主成分(PC1)方差贡献率为71.10%,第2主成分(PC2)方差贡献率为17.75%,累计方差贡献率为88.85%,因此具有代表性。PC1将完成升温后的位点分为3个区域,最右边区域包含第5天中部中心和中部1/2两个位点,中间区域包含第4天顶部1/2、中部边缘以及第5天底部中心、底部边缘四个位点,最左边区域包含剩余的其他位点。结合吡嗪类含量分析可知,最右边区域(第5天中部中心和中部1/2)的吡嗪类积累条件最好,其次为中间区域的四个位点。结合位点温度分析发现,温度和位置相近的位点并未聚集在一个区域,如第5天顶部1/2(82.67 ℃)和第5天中部中心(83.33 ℃),第4天顶部1/2(91.33 ℃)和第4天顶部中心(90.63 ℃)等。可能是因为山西老陈醋熏醅时醋醅是较为疏松的固态形式,而其他模拟吡嗪类生成条件的模型实验大多是在溶液条件下完成,溶液相对醋醅的固态形式条件较好,反应产物均匀分布[11]。因此,传统固态熏醅中吡嗪类含量变化与液态模拟美拉德反应中吡嗪类含量与温度成线性关系的结果不同,传统固态熏醅过程中除温度以外不同位点对吡嗪类的积累也具有较大的影响。
3 结论
经过分析发现,熏醅前两天醋醅一直处于升温过程中,不同区域醋醅温差较大,成品中含量较高的4-甲基吡嗪和2,3,5-三甲基吡嗪在此期间开始生成并积累,同时两种吡嗪含量与不同位点温度呈现出一定相关性;第3、4天熏醅温度最高,4-甲基吡嗪和2,3,5-三甲基吡嗪含量升高较快,同时生成了其他几种含量较少的吡嗪类化合物;第5天虽然温度相对于第3、4天有小幅降低但吡嗪类化合物含量均有升高。通过分析山西老陈醋熏醅过程中陶缸不同位点的温度变化和吡嗪类化合物的生成和积累变化,进一步明确了熏醅过程中不同吡嗪类化合物的生成顺序及其在陶缸中生成、积累的位置和温度信息。为山西老陈醋熏醅过程中吡嗪类化合物指标的控制提供参考。
[1]李江涌,王如福,焦玉双.山西老陈醋熏醅前后香气成分的变化分析[J].中国酿造,2016,35(9):47-50.
[2]HAN K,JI W,WANG R F.Effect of the different baking processes on the aroma profiles of Shanxi aged vinegar mashes[J].Int Food Res J,2020,27(5):814-824.
[3]LIANG J,XIE J,HOU L,et al.Aroma constituents in Shanxi aged vinegar before and after aging[J].J Agr Food Chem,2016,64(40):7597-7605.
[4]刘丹彤,刘峰,康帅帅,等.传统山西老陈醋熏醅工艺过程风味物质及功能活性成分的变化[J].中国酿造,2021,40(2):163-169.
[5]李弘文,王旭苹,杨小兰.不同熏醅工艺对山西老陈醋香气成分的影响[J].食品科学,2015,36(20):90-94.
[6]张详龙.山西老陈醋含糖大分子及其免疫活性研究[D].天津:天津科技大学,2022.
[7]郑宇,赵翠梅,吴亚楠,等.山西老陈醋风味物质组成特征及风味轮分析[J].食品科学技术学报,2019,37(4):24-34.
[8]范梦蝶,王天泽,杜文斌,等.山西老陈醋晾晒前、后挥发性香味物质比较分析[J].中国食品学报,2019,19(12):229-242.
[9] AL-DALALI S, ZHENG F, SUN B, et al.Effects of different brewing processes on the volatile flavor profiles of Chinese vinegar determined by HS-SPME-AEDA with GC-MS and GC-O[J].LWT-Food Sci Technol,2020,133:109969.
[10]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 19777—2013 地理标志产品山西老陈醋[S].北京:中国标准出版社,2013.
[11]ZHANG Y H,YANG R Y,XIE F W,et al.Control strategies of pyrazines generation from Maillard reaction[J].Trend Food Sci Technol,2021,112:795-807.
[12]王宏霞,闫裕峰,郎繁繁,等.山西老陈醋不同熏醅工艺对风味物质的影响[J].中国酿造,2021,40(7):38-42.
[13]张春杰,张茜.山西老陈醋熏醅工业化进展[J].中国酿造,2019,38(1):204-206.
[14]杨彩霞,王瑶,汪艳蛟,等.不同烘焙条件下成品滇红茶香气及化学成分的变化[J].现代食品科技,2021,37(9):242-251.
[15]苏槟楠,萧晋川,潘佩平,等.山西老陈醋醋酸发酵阶段醋醅疏松度的研究[J].中国酿造,2015,34(11):52-55.
[16] WANG B, QU F, WANG P, et al.Characterization analysis of flavor compounds in green teas at different drying temperature[J].LWT-Food Sci Technol,2022,161:113394.
[17]RAMLI N,HASSAN O,SAID M,et al.Influence of roasting conditions on volatile flavor of roasted malaysian cocoa beans[J].J Food Process Preserv,2006,30:280-298.
[18]HANG Y,YIXIN S,PETER K,et al.Kinetic study of high-intensity ultrasound-assisted Maillard reaction in a model system of D-glucose and glycine[J].Food Chem,2018,269:628-637.
[19]李攀恒,郑吴伟,汪超,等.HS-SPME-GC-MS测定中国四大名醋的香气成分[J].中国酿造,2018,37(4):164-168.
[20]LIANG J,XIE J,HOU L,et al.Aroma constituents in Shanxi aged vinegar before and after aging[J].J Agr Food Chem,2016,64(40):7597-7605.
[21]郑宇,赵翠梅,吴亚楠,等.山西老陈醋风味物质组成特征及风味轮分析[J].食品科学技术学报,2019,37(4):24-34.
[22]许伟.镇江香醋醋酸发酵过程微生物群落及其功能分析[D].无锡:江南大学,2011.
[23]丁伟,魏莎莎,闫裕峰,等.山西老陈醋大曲制备过程中理化因子,微生物群落变化及风味形成规律[J].中国酿造,2022,41(5):52-59.
[24]王家东,刘丹彤,王馨宇,等.山西老陈醋酿造过程四甲基吡嗪形成规律及稳定性研究[J].食品与发酵工业,2022,48(15):62-68.
[25]中华人民共和国国家卫生和计划生育委员会.GB 1886.292—2016食品安全国家标准食品添加剂2,3,5-三甲基吡嗪[S].北京:中国标准出版社,2016.
[26]AL-DALALI S,ZHENG F,SUN B,et al.Tracking volatile flavor changes during two years of aging of Chinese vinegar by HS-SPME-GC-MS and GC-O[J].J Food Compos Anal,2022,106:104295.
[27]TOKER O S,PALABIYIK I,PIROUZIAN H R,et al.Chocolate aroma:Factors,importance and analysis[J].Trends Food Sci Technol, 2020,99:580-592.