保健酒是我国传统的酒类饮品之一,通常是以蒸馏酒、发酵酒或食用酒精为基酒,加入符合国家有关规定的原料、辅料或食品添加剂,经注册或备案,并声称具有保健功能的饮料酒,其适用于特定的人群,具有调节免疫,抗疲劳等功能,但是一般没有治疗作用[1]。酒与药的结合在我国具有至少3 600年的历史,《汉书·食货志》中描述:“酒,百药之长,嘉会之好”,汉末《名医别录》中描述:“酒行药势”,宋代《杨氏家藏方》中描述:“酒:引药入经络”,因此,也有了“酒为百药之长”、“药借酒而行药势”的说法[2]。充分说明了酒能更好的帮助药物发挥作用,达到更好的治疗效果。早在殷商时期就有以黑黍为酿酒原料,再加入郁金香草的记载,这便是最早的药酒;东汉时期张仲景的《伤寒杂病论》中记载:“以清酒七升,水八升,先煮八味,取三升”;之后宋代名著《太平圣惠方》中描述:“酒能和养神气,性剽悍,功甚变通,能宣利肠胃,善导引药势”;而在隋唐时期《千金方》则是我国现存最早的对药酒的专题论著;明代时期《普济方》通卷收载的药酒达到300余方。
人参作为一种补益药具有大补元气,复脉固脱,补脾益肺,生津养血,安神益智等功效[3]。其主要化学成分包括皂苷类化合物[4]、挥发油[5]、多糖[6]、氨基酸[7-8]等。其茎叶中含有丰富的皂苷类成分,药理活性强,具有免疫调节、促进细胞增殖、抗肿瘤等作用[9-10]。市面上多数保健食品均含有人参,并配伍多种中药,共同发挥药效作用。人参作为参鹿酒中的主要原料,其主要成分人参皂苷作为参鹿酒的功能性成分,检测其含量具有重要意义。而目前我国人参类保健品的质量控制方法主要有比色法[11]和高效液相色谱法(high performance liquid chromatography,HPLC)[12]。比色法易受基体其他成分的干扰,造成检测方法的不稳定,且参鹿酒所含原料较多,基体复杂,对其检测结果有影响;高效液相色谱法基本采用外标法,且人参皂苷Rg1、Re和Rb1不能代表人参的优劣[13]。因中药复杂的成分决定了单一成分或单一指标不能有效地判断中药的质量,并由此提出了多成分质量控制模式[14]。人参皂苷Rg1、Rb1、Re、Rc、Rb2、Rf、Rd占人参总皂苷的90%以上,是人参皂苷类最重要的组成成分[15-17]。但是外标法需要足够量的对照品,然而由于某些对照品难以制备分离,导致难以获得且价格较高。一测多评(quantitative analysis of multi-components by single marker,QAMS)法是近年来中药领域用于多成分质量控制的研究思路,其运用同系列成分间存在的内涵比例关系,采用单个易获得的对照品对多个成分进行定量,实现多个成分的同步监控,目前已用于解决中药[18-21]、中成药[22-23]、食品[24]、化妆品[25]质量控制中缺乏对照品这一问题。冯飞等[26-27]研究证明,超高效液相色谱法(ultra performance liquid chromatography,UPLC)结合多指标人参皂苷成分一测多评定量分析为人参药材、饮片、提取物及相关产品的质量评价提供了科学的技术依据。
基于此,本研究首先采用UPLC测定参鹿酒样品中7种人参皂苷的含量,并进行方法学考察;然后以人参皂苷Rg1为参照物,计算其余6种人参皂苷的相对校正因子及含量,并考察QAMS法的耐用性;最后与外标法相比,验证QAMS的可行性,以期建立UPLC-QAMS法同时测定参鹿酒中7种人参皂苷含量方法,对参鹿酒的质量控制提供。
1 材料与方法
1.1 材料与试剂
13批参鹿酒样品(S1~S13):自制;人参皂苷Rg1、人参皂苷Re、人参皂苷Rf、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rd:中国食品药品检定研究院;人参皂苷Rc:上海源叶生物有限公司;超纯水:自制;氨水(分析纯):天津市致远化学试剂有限公司;甲醇、乙腈(均为色谱纯):德国默克股份有限公司。其他试剂均为国产分析纯。
1.2 仪器与设备
ACQUITY超高效液相色谱仪、BEH C18色谱柱(1.7 μm,2.1 mm×100 mm)、BEH Shield RP18色谱柱(1.7 μm,2.1 mm×100 mm)、BEH RP18色谱柱(1.7 μm,2.1 mm×50 mm):美国Waters公司;xs204分析天平:美国MettlerTolrdo公司;KQ-800DE超声波清洗器:昆山市超声仪器有限公司;Milli-Q纯水仪:美国Millipore公司。
1.3 方法
1.3.1 对照品溶液及供试品溶液的制备
对照品溶液的制备:分别精密称取对照品人参皂苷Rg1、人参皂苷Re、人参皂苷Rf、人参皂苷Rb1、人参皂苷Rc、人参皂苷Rb2及人参皂苷Rd,采用甲醇制成质量浓度分别为1.931 μg/mL、1.627 μg/mL、0.64 μg/mL、2.02 μg/mL的母液;分别取人参皂苷Rg1对照品溶液1.5 mL、人参皂苷Re对照品溶液0.8 mL、人参皂苷Rf对照品溶液1.0 mL、人参皂苷Rb1对照品溶液1.2 mL、人参皂苷Rc对照品溶液1.5 mL、人参皂苷Rb2对照品溶液1.5 mL、人参皂苷Rd对照品溶液0.3 mL于10 mL的容量瓶中,并用甲醇定容至刻度,摇匀,作为混合对照品溶液。
供试品溶液的制备:精确量取参鹿酒50 mL,于60 ℃旋转蒸发至浸膏状,然后用水复溶并定容至10 mL容量瓶中,待用。采用预处理好的YWGC-C18小柱(80~100目,1.0 g,甲醇20 mL、水20 mL活化),先用20%甲醇-4%氨-水溶液15 mL冲洗,再用水淋洗至中性,最后用甲醇洗脱至5 mL容量瓶中,并定容至刻度,用0.22 μm滤膜过滤,备用。
1.3.2 UPLC色谱条件[28-33]
BEH Shield RP18色谱柱(1.7 μm,2.1 mm×100 mm);检测波长为203 nm;流速为0.4 mL/min;柱温为30 ℃;进样量为4 μL;流动相为乙腈(A)-水(B);梯度洗脱(0~3.0 min,81.5%~81.0%A;3.0~8.5 min,81.0%~71.0%A;8.5~8.8 min,71.0%A;8.8~12.5 min,71.0%~60.0%A;12.5~13.0 min,60.0%~10.0%A;13.0~14.3 min,10.0%A;14.3~14.8 min,10.0%~81.5%A;14.8~16 min,81.5%A)。
1.3.3 一测多评法方法学考察
线性关系考察:设置混合对照品液的进样量分别为1.0 μL、1.5 μL、2.0 μL、2.5 μL、3.0 μL、3.5 μL、4.0 μL,采用UPLC测定,记录峰面积,以质量浓度(X)为横坐标,峰面积(Y)为纵坐标,绘制标准曲线,得到各对照品标准曲线的回归方程、相关系数(R2)及线性范围。
精密度试验:制备供试品S1溶液一份,连续进样6针,采用UPLC测定,记录人参皂苷Rg1、Re、Rf、Rb1、Rc、Rb2、Rd的峰面积,并计算其相对标准偏差(relative standard deviation,RSD)。
重复性试验:取6份参鹿酒制备供试品S1溶液,采用UPLC测定,记录人参皂苷Rg1、Re、Rf、Rb1、Rc、Rb2、Rd的峰面积,并计算其RSD。
稳定性试验:取对照品和供试品S1溶液各一份,分别在制备样品后的0、4 h、8 h、12 h、16 h、20 h、24 h进样,采用UPLC测定,记录人参皂苷Rg1、Re、Rf、Rb1、Rc、Rb2、Rd的峰面积,并分别计算7种皂苷成分的RSD。
加标回收率试验:精密量取参鹿酒样品S1 50 mL共6份,按照上述色谱条件所测人参皂苷Rg1、Re、Rf、Rb1、Rc、Rb2及Rd的含量作为对照品加入的依据,分别加入约为供试品中待测成分含量100%的对照品,制备供试品溶液,精密吸取4 μL进样,采用UPLC测定,计算样品中人参皂苷Rg1、Re、Rf、Rb1、Rc、Rb2及Rd的加标回收率。
1.3.4 相对校正因子的计算
以人参皂苷Rg1为参照物,设置混合对照品溶液的进样量分别为1.0 μL、1.5 μL、2.0 μL、2.5 μL、3.0 μL、3.5 μL、4.0 μL,采用UPLC进行测定,并记录峰面积,参照文献[34-37]计算其他6种人参皂苷成分的相对校正因子,其计算公式如下:
式中:fk/s为相对校正因子;Ck为待测成分的质量浓度,mg/mL;Ak为待测成分的峰面积;Cs为参照物的质量浓度,mg/mL;As为参照物的峰面积。
1.3.5 一测多评法耐用性考察
不同色谱柱对相对校正因子的影响[28-30]:精密吸取混合对照品溶液适量,采用UPLC进行测定,计算各个成分的fk/s,考察不同色谱柱(BEH Shield RP18色谱柱(1.7 μm,2.1×100 mm)、BEH C18色谱柱(1.7 μm,2.1×100 mm)、BEH RP18色谱柱(1.7 μm,2.1×50 mm))对fk/s的影响。
不同流速对相对校正因子的影响[38-40]:精密吸取混合对照品溶液适量,采用UPLC进行测定,计算各个成分的fk/s,考察不同流速(0.3 mL/min、0.4 mL/min、0.5 mL/min)对fk/s的影响。
不同柱温对相对校正因子的影响:精密吸取混合对照品溶液适量,采用UPLC进行测定,计算各个成分的fk/s,考察不同柱温(25 ℃、30 ℃、35 ℃)对fk/s的影响。
1.3.6 待测组分色谱峰的定位
以内参物人参皂苷Rg1为基准峰,考察在不同色谱柱(BEH Shield RP18色谱柱(1.7 μm,2.1×100 mm)、BEH C18色谱柱(1.7 μm,2.1×100 mm)、BEH RP18色谱柱(1.7 μm,2.1×50 mm))条件下的相对保留时间,并采用相对保留时间值法对色谱峰进行定位。
1.3.7 一测多评法与外标法测定结果比较
为了验证QAMS法的可靠性,分别采用传统的外标法(external standard method,ESM)和QAMS法测定13批参鹿酒样品中人参皂苷Rg1、Re、Rf、Rb1、Rc、Rb2及Rd的含量,采用相对误差(relative error,RE)对两种方法所得的结果进行评价[41]。
1.3.8 数据处理
计算方法采用平均值法计算不同批次样品间的相似性,采用Excel2013软件对数据进行处理。
2 结果与分析
2.1 方法学考察结果
2.1.1 线性关系考察
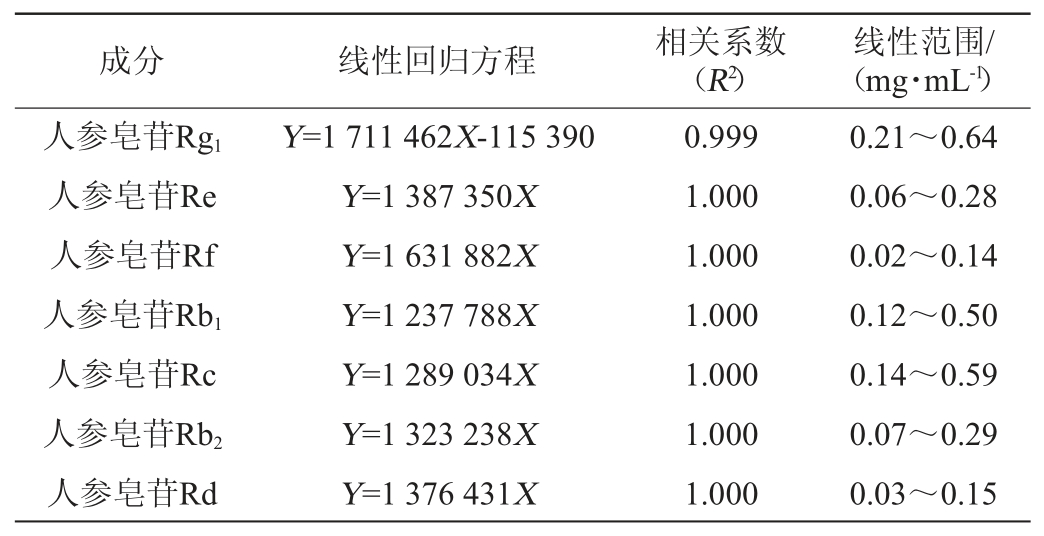
UPLC测定7种人参皂苷的标准曲线回归方程、相关系数及线性范围见表1。由表1可知,人参皂苷Rg1、人参皂苷Re、人参皂苷Rf、人参皂苷Rb1、人参皂苷Rc、人参皂苷Rb2及人参皂苷Rd在各自质量浓度范围内线性关系良好,相关系数R2>0.999。
表1 7种人参皂苷的线性关系
Table1 Linear relationships of 7 ginsenosides
2.1.2 精密度试验
精密度试验结果表明,人参皂苷Rg1、Re、Rf、Rb1、Rc、Rb2及Rd峰面积的RSD分别为0.33%、2.44%、1.65%、0.90%、0.86%、0.76%、2.83%,说明该方法精密度良好。
2.1.3 重复性试验
重复性试验结果表明,人参皂苷Rg1、Re、Rf、Rb1、Rc、Rb2及Rd峰面积的RSD分别为2.37%、1.17%、1.97%、2.44%、1.44%、2.38%、2.27%,说明该方法重复性良好。
2.1.4 稳定性试验
稳定性试验结果表明,供试品中人参皂苷Rg1、Re、Rf、Rb1、Rc、Rb2及Rd峰面积的RSD分别为1.36%、1.61%、2.44%、2.20%、2.01%、2.37%、0.84%,对照品人参皂苷Rg1、Re、Rf、Rb1、Rc、Rb2及Rd 峰 面 积 的RSD 分 别 为1.26%、2.51%、2.88%、1.01%、0.86%、1.51%、2.83%,说明该方法稳定性良好。
2.1.5 加标回收率试验
加标回收率试验结果表明,人参皂苷Rg1、Re、Rf、Rb1、Rc、Rb2及Rd 的加标回收率分别为100.69%、100.13%、100.51%、100.93%、101.12%、101.73%、99.72%,其RSD分别为1.80%、3.59%、2.50%、2.33%、3.08%、1.79%、2.66%。说明该测定方法准确度良好。
2.2 相对校正因子的计算结果
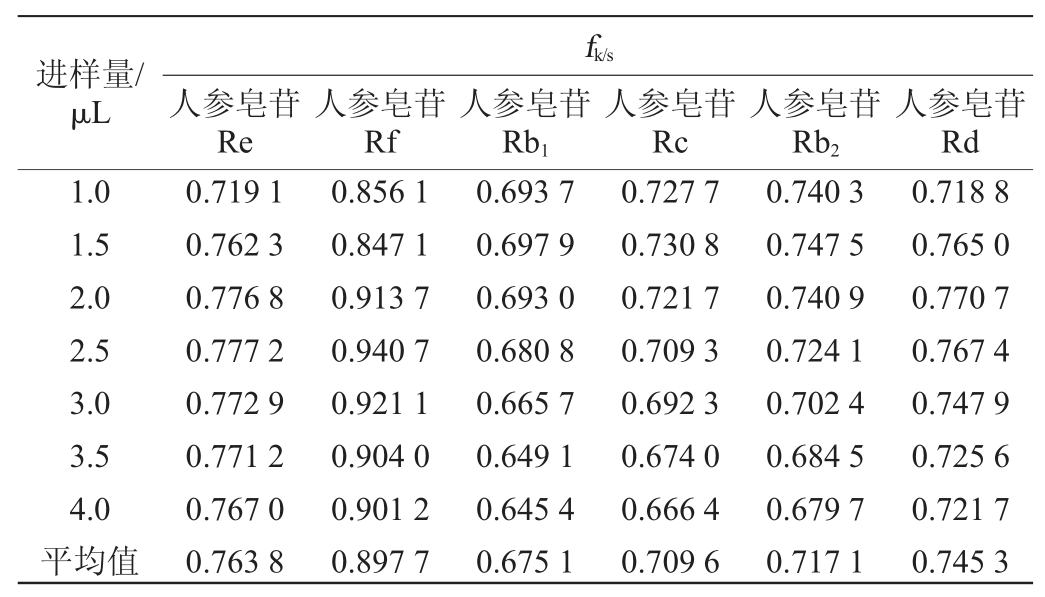
以人参皂苷Rg1为参照物,对不同体积的混合对照品溶液进样检测,计算人参皂苷Re、Rf、Rb1、Rc、Rb2及Rd的相对校正因子,结果见表2。由表2可知,人参皂苷Re、Rf、Rb1、Rc、Rb2及Rd的相对校正因子分别为0.763 8、0.897 7、0.675 1、0.709 6、0.717 1、0.745 3,6种人参皂苷成分的相对校正因子RSD均<5%,说明相对校正因子的重现性良好。
表2 6种人参皂苷的相对校正因子
Table 2 Relative correction factors of 6 ginsenoside
续表

2.3 耐用性
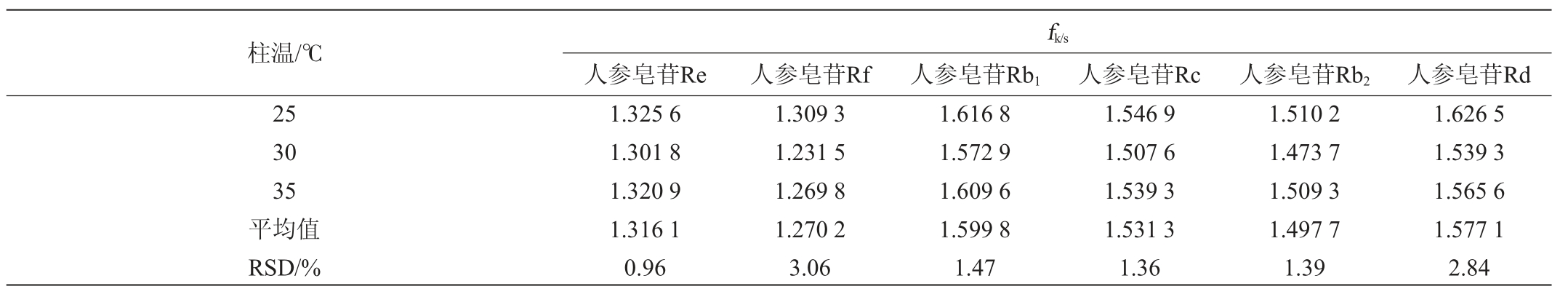
不同色谱柱、柱流速及柱温对6种人参皂苷相对校正因子的影响见表3~表5。由表3~表5可知,6种人参皂苷在不同色谱柱、柱流速及柱温条件下的相对校正因子(fk/s)的RSD均<5%,表明不同色谱柱、柱流速及柱温对各个成分的相对校正因子无明显影响,对相对校正因子具有较好的重现性。
表3 不同色谱柱对6种人参皂苷相对校正因子的影响(n=3)
Table 3 Effect of different chromatographic columns on the relative correction factors of 6 ginsenosides (n=3)
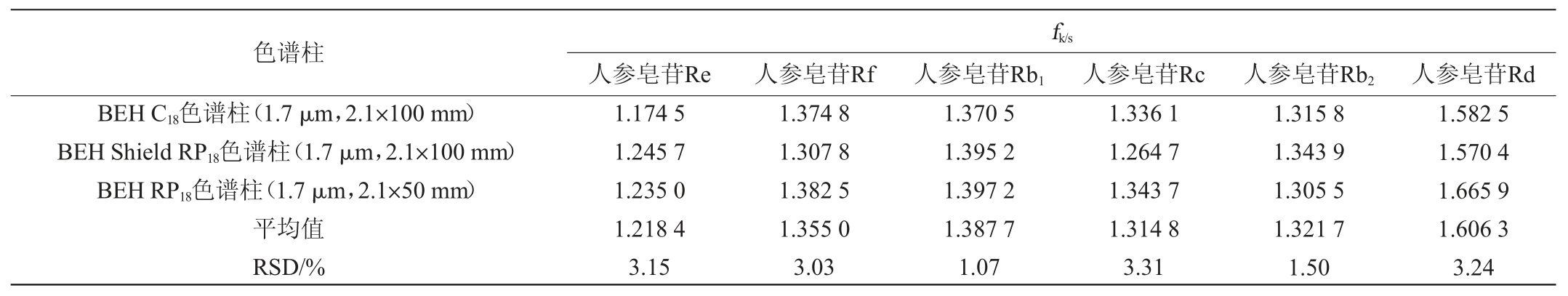
表4 不同流速对6种人参皂苷相对校正因子的影响(n=3)
Table 4 Effect of different flow velocity on relative correction factors of 6 ginsenosides (n=3)
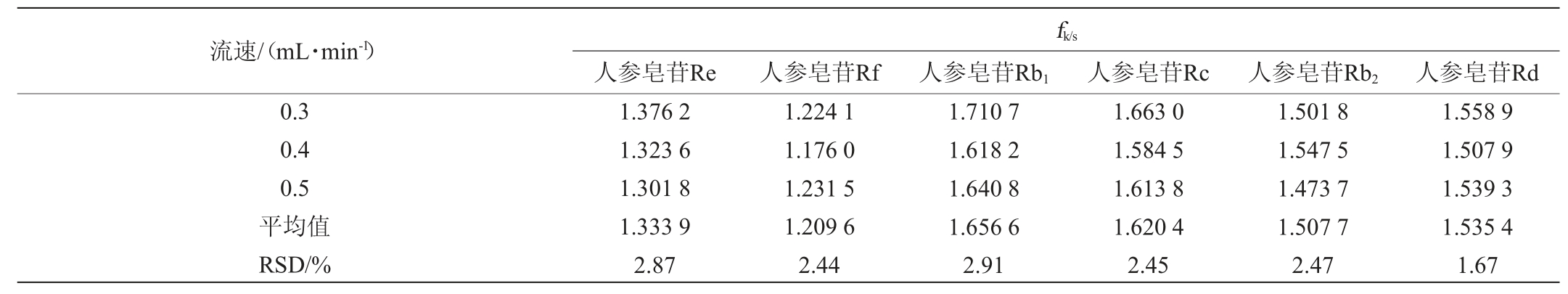
表5 不同柱温对6种人参皂苷相对校正因子的影响(n=3)
Table 6 Effect of different column temperature on relative correction factors of 6 ginsenosides (n=3)
2.4 人参皂苷色谱峰的定位
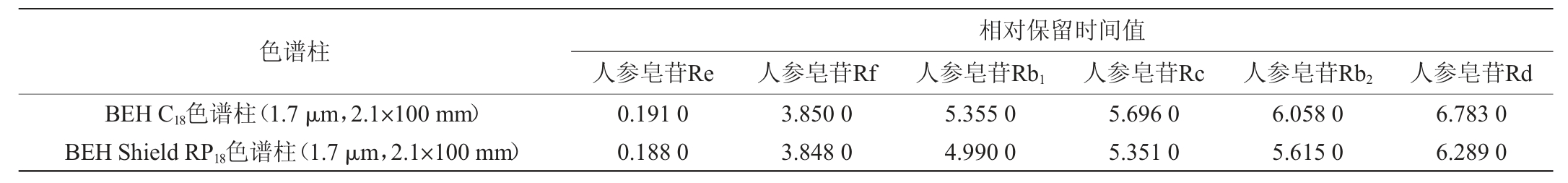
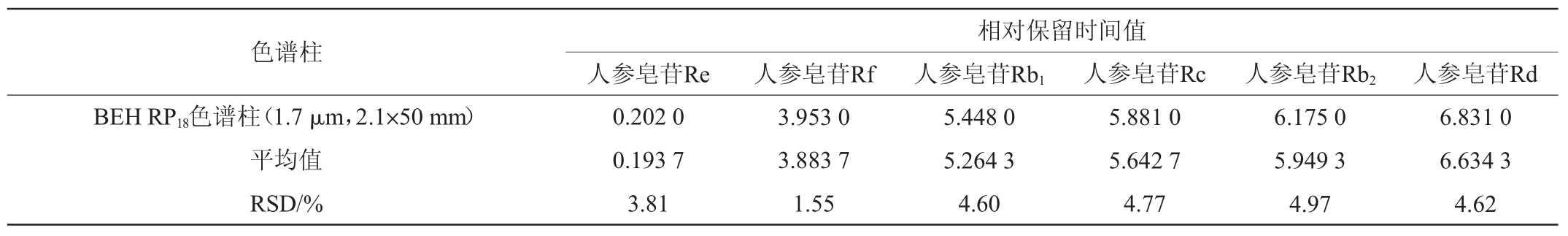
采用相对保留时间值法,以人参皂苷Rg1为参照物,考察6种人参皂苷在不同色谱柱下的相对保留时间,结果见表6。由表6可知,各成分相对保留时间值的RSD均<5%,表明不同色谱柱对各成分的相对保留时间无明显影响,说明采用相对保留值的方法可以准确定位各待测物的色谱峰。
表6 不同色谱柱对6种人参皂苷保留时间的影响(n=3)
Table 6 Effect of different chromatographic columns on retention time of 6 ginsenosides (n=3)
续表
2.5 QAMS法与外标法测定结果比较
采用RE对两种方法所得的结果进行评价,以此验证QAMS法用于参鹿酒质量评价的准确性,结果见表7。由表7可知,RE均<5%,证明两种方法测得的化合物含量无显著性差异,且QAMS法对参鹿酒中7种人参皂苷活性成分的同时定量分析是可行的。
表7 参鹿酒样品中7种人参皂苷不同方法测定结果比较(n=3)
Table 7 Comparison of the determination results of 7 ginsenosides in Shenlu wine samples by different methods(n=3)

3 结论
本研究建立了UPLC-QAMS法同时测定参鹿酒中人参皂苷Rg1、Re、Rf、Rb1、Rc、Rb2及Rd的含量。方法学考察结果发现,7种人参皂苷在各自范围内线性关系良好(R2>0.999),精密度、重复性及稳定性试验结果的相对标准偏差(RSD)均<3%,加样回收率为100.13%~101.73%。以人参皂苷Rg1为参照物,其余6种人参皂苷的相对校正因子的RSD值均<5%,重现性良好,采用相对校正因子计算得到的13批参鹿酒样品中7种人参皂苷的含量与外标法实测值的相对误差(RE)均<5%,说明所建立的UPLC-QAMS法可有效、快速的评价参鹿酒的质量,为全面评价参鹿酒的质量提供依据。
[1]李雅新,梁慧珍,张文生,等.保健酒制作工艺的研究进展[J].中国酿造,2022,41(5):23-27.
[2]唐颂.谈保健酒产品的中医养生文化属性[J].酿酒,2022,49(2):130-132.
[3]中华人民共和国卫生部药典委员会.中华人民共和国药典一部[M].北京:中国医药科技出版社,2020:8-9.
[4]QI L W,WANG C Z,YUAN C S.Isolation and analysis of ginseng: advances and challenges[J].Nat Prod Rep,2011,28(3):467-495.
[5]WANG J,ZHANG L X,ZHAO Y,et al.Volatile oil contents and their variation law of Radix et Rhizoma Ginseng in Changbai mountain areas[J].Med PIant,2011,2(3):40.
[6]ZHAO B,LV C N,LU J C.Natural occurring polysaccharides from Panax ginseng C.A.Meyer:a review of isolation structures and bioactivities[J].Int J Biol Macromol,2019,133:324-336.
[7]张浩.人参活性成分蛋白质、氨基酸、有机酸及核苷类成分研究[D].长春:吉林大学,2016.
[8]SUN H,LIU F,SUN L,et al.Proteomic analysis of amino acid metabolism differences between wild and cultivated Panax ginseng[J].J Ginseng Res,2016,40(2):113-120.
[9]RIAZ M,RAHMANN N U,ZIA-UL-H AQ M,et al.Ginseng: a dietary supplement as immune-modulator in various diseases[J].Trends Food Sci Tech,2018,83:12-30.
[10]CHEN L X,QI Y L,QI Z,et al.A comparative study on the effects of different parts of panax ginseng on the immune activity of cyclophosphamide-induced immunosuppressed mice[J].Molecules,2019,24(6):1096.
[11]国家市场监督管理总局.保健食品理化及卫生指标检验与评价技术指导原则:保健食品中总皂苷的测定[EB/OL].(2020-10-31).https://www.samr.gov.cn/tssps/zcwj/art/2023/art_fc451604b4e141a59009d 184 a49305cd.html.
[12]国家市场监督管理总局.保健食品理化及卫生指标检验与评价技术指导原则:保健食品中人参皂苷的高效液相色谱测定[EB/OL].(2020-10-31).https://www.samr.gov.cn/tssps/zcwj/art/2023/art_fc451604b4e 141a59009d184a49305cd.html.
[13]李金花,冯有龙,张再平,等.一测多评法测定西洋参类保健食品中9个皂苷类成分的含量[J].药物分析杂志,2018,38(12):2160-2166.
[14]鲁辉,吴杨,闵春艳.基于UPLC一测多评法测定西洋参及其保健食品中人参皂苷的含量[J].食品与药品,2018,20(3):173-179.
[15]杨鑫宝,杨秀伟,刘建勋.人参中皂苷类化学成分的研究[J].中国现代中药,2013,15(5):349-358.
[16]SHI Z Y,ZENG J Z,WONG A S T.Chemical structures and phaemacological profiles of ginseng saponins[J].Molecules,2019,24(13):2443.
[17]PIAO X M,ZHANG H,KANG J P,et al.Advances in saponin diversity of Panax ginseng[J].Molecules,2020,25(15):3452.
[18]王智民,高慧敏,付雪涛,等.“一测多评”法中药质量评价模式方法学研究[J].中国中药杂志,2006(23):1925-1928.
[19]罗祖良,仇峰,韦日伟,等.相对校正因子在中药多指标测定中的应用研究进展[J].中草药,2012,43(7):1448-1452.
[20]李丽敏,程益清,杨盈盈,等.一测多评法测定保健食品中6种大豆异黄酮类成分[J].食品研究与开发,2016,37(9):170-174.
[21]LI D W,ZHU M,SHAO Y D,et al.Determination and quality evaluation of green tea extracts through qualitative and quantitative analysis of multicomponents by single marker(QAMS)[J].Food Chem,2016,197:1112-1120.
[22]翟宏宇,单柏宇,王海洋,等.一测多评法测定保心宁片中6个丹参类指标性成分的含量[J].药物分析杂志,2018,38(6):973-978.
[23]靳瑞婷,杨素德,付娟,等.一测多评法测定芪白平肺颗粒中8种皂苷类成分[J].中草药,2015,46(24):3682-3686.
[24]魏丽娟,易倩,张曲,等.一测多评法测定藜麦中6种酚类成分[J].食品工业科技,2018,39(19):232-236,242.
[25]左雪,韩萧茜,刘成浩,等.一测多评法测定化妆品中10种α-羟基酸的含量[J].卫生研究,2020,49(2):285-289,319.
[26]冯飞,许金国,严国俊,等.基于UPLC特征图谱与一测多评法的人参药材质量评价研究[J].中国中药杂志,2022,47(13):3530-3538.
[27]李佳寅,张小平,方梦婷,等.一测多评法同时测定生脉注射液中12个成分[J].中草药,2021,52(24):7484-7492.
[28]常阿倩,程睿旸,肖水明,等.经典名方保元汤UPLC特征图谱和多指标成分含量测定研究[J].世界科学技术-中医药现代化,2021,23(8):2643-2651.
[29]李天佑,何羽.超高效液相色谱法同时测定颈舒颗粒中4种皂苷类成分含量[J].中国药业,2021,30(17):82-85.
[30]段宇,杨静,谢金伯,等.基于UPLC-Q-Trap-MS技术的热处理前后绞股蓝中9种皂苷成分同时定量分析[J].中国中药杂志,2021,46(20):5314-5319.
[31]杨秀伟,王洪平,徐嵬,等.不同产地人参根和根茎中人参皂苷的含量分析[J].药物分析杂志,2017,37(1):30-36.
[32]王敏,赵振霞,刘永利,等.红参中5种人参皂苷含量的超高效液相色谱法同时测定[J].时珍国医国药,2019,30(1):56-58.
[33]逄世峰,李亚丽,许世泉,等.人参不同部位人参皂苷类成分研究[J].人参研究,2015,27(1):5-8.
[34]吴笛,叶秋雄,李楚源.一测多评法测定复方丹参片中5种酚酸类成分的含量[J].中国新药杂志,2013,22(18):2130-2135,2173.
[35]李娟,狄留庆,李俊松,等.HPLC-MS法同时测定六神丸中9种蟾蜍二烯内酯类化合物[J].中草药,2017,48(4):700-705.
[36]骆航,李华生.基于一测多评法的长城感冒片质量控制[J].药物分析杂志,2020,40(3):536-543.
[37]丁梦磊,张雯,张越,等.一测多评法测定六神丸中的6个蟾蜍二烯内酯类化合物[J].药物分析杂志,2019,39(11):2003-2009.
[38]曹玉.UPLC同时测定参芪降糖颗粒中人参皂苷Rg1、Re、Rb1、Rb2和Rd的含量[J].当代化工研究,2022(16):41-43.
[39]张思敏,张也,伍红年,等.不同产地竹节参中7种皂苷含量测定及化学计量学评价[J].食品与机械,2022,38(3):65-70,79.
[40]李彦超,曲正义,王英平,等.UPLC法同时测定人参香皂中8种人参皂苷[J].特产研究,2020,42(5):50-53.
[41]徐小力.基于一测多评和指纹图谱评价七制香附丸的质量研究[D].重庆:重庆医科大学,2022.