酱油是一种以大豆、小麦或麸皮为原料酿造的一种具有独特风味的调味品,深受大众喜爱[1]。酱油发酵包含了制曲和酱醪发酵两个步骤,制曲阶段以米曲霉(Aspergillus oryzae)的生长和作用为主,发酵阶段以耐盐酵母和乳酸菌的生长代谢为主,发酵过程中形成的糖醇类、有机酸类及酯类等挥发性化合物,对酱油风味品质起到重要的作用[2-4],所以风味研究是评价酱油质量的一种有效方法[5]。其中,生香酵母是一类能够合成具有芳香性气味有机物的酵母,在调味品、功能饮料、酿造等领域应用广泛[6]。
生香酵母在国内最早应用于白酒,是为了弥补酒香不浓郁的不足,之后才不断扩展应用于酱油、果醋、面包等发酵食品中[7]。目前,主要应用于酱油的生香酵母有鲁氏接合酵母(Zygosaccharomyces rouxii)、埃契氏球拟酵母(Toru-lopsis etchellsii)、易变球拟酵母(Torulopsis utilis)等[8],这些酵母可以产生几百种香气和滋味化合物,如氨基酸、糖、有机酸、挥发性成分和其他化合物,这些化合物直接构成酱油产品的独特风味[9]。JIANG X W等[10]在高盐稀态发酵酱油中添加3株生香酵母,可以极大地提高酯类和醇类风味化合物的浓度,提高酱油风味;李学伟等[11]在低盐稀态酱油中添加2株耐盐酵母进行生香发酵,并对比发酵前后的风味,结果表明,酱油生香发酵后总酸、总酯、酒精含量明显提高;WANG J W等[12]分离出3株天然风味增强酵母菌,其中Wickerhamiella versatilis可以提高醇类、酯类化合物的浓度,山梨假丝酵母(Candida sorbosivorans)可以使2,6-二甲基吡嗪、甲基吡嗪和苯乙醛的含量显著增加,Starmerella etchellsii可以使酱油中糠醛、甲硫醛和麦芽酚的浓度提高,呈现出甜味和焦糖香气;冯杰[13]研究发现埃切假丝酵母(Candida etchellsii)的添加可以提升酱油的品质和风味,并确定两阶段添加酵母的策略来改进酱油风味。因此,筛选一株生香良好的酵母,研究其特性并应用于酱油酿造,成为酱油酿造微生物的一个重要方向[7]。
本研究从酱醪中筛选耐盐生香优良的酵母,结合形态观察、生理生化试验及分子生物学技术对其进行菌种鉴定,采用单因素试验及响应面试验对其培养条件进行优化,以期为其应用于酱油酿造奠定基础,并在此基础上研究和建立该菌的生长规律和底物消耗的动力学方程及模型,为发酵过程的预测和控制提供理论基础。
1 材料与方法
1.1 材料与试剂
酱醪:由李锦记(新会)食品有限公司提供。
葡萄糖、蔗糖、麦芽糖、乳糖、果糖、氯化钠、蛋白胨:广东广试试剂科技有限公司;硫酸铵、硝酸钠、尿素:广州化学试剂厂;3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS):广检(广州)检测科技有限公司;麦芽汁固体(液体)培养基、酵母浸膏、琼脂:广东环凯生物科技有限公司;2xT8聚合酶链式反应(polymerase chain reaction,PCR)试剂、酵母基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:广州擎科生物技术有限公司。本研究所用试剂均为分析纯或生化试剂。
1.2 仪器与设备
JJ223BC型电子天平:常熟市双杰测试仪器厂;TS-200B恒温摇床:广州市绿向生物科技有限公司;759紫外可见分光光度计:上海仪电分析仪器有限公司;TGL—16gR型台式高速冷冻离心机:上海安亭科学仪器厂;BA310-T生物显微镜:麦克奥迪(成都)仪器有限公司;FPG3三温区培养箱:宁波莱福科技有限公司;A300朗基全触屏PCR仪:广州市飞迪生物科技有限公司。
1.3 方法
1.3.1 酵母的分离纯化
将酱醪样品按10倍梯度稀释至10-4、10-5和10-6后,取0.1 mL样品稀释液涂布于含100 g/L NaCl的麦芽汁琼脂培养基中,每个梯度进行3个重复试验,30 ℃培养3~4 d,挑取形态近似酵母(菌落较大较厚,表明湿润、易挑起)的单菌落进行镜检,将初步镜检为酵母的菌株进一步分离纯化,获得纯培养菌株。纯化后的菌株接种于斜面试管进行保藏(-4 ℃)。
1.3.2 生香酵母的筛选
将纯化好的菌株接种于麦芽汁固体培养基中30 ℃培养4 d,接种于麦芽汁液体培养基中30 ℃、180 r/min振荡培养4 d,培养结束后,参考黄鑫等[14]的嗅闻方法进行分析。通过感官评定的方式,根据培养液整体所呈现出来的风味是否具有特殊性、是否愉悦、是否舒适、是否刺鼻等,筛选出整体风味较好的一株菌株,进行后续试验。
1.3.3 生香酵母的鉴定
(1)形态学观察
观察菌株的形状、颜色、光滑度、质地等形态特征;用接种环取菌落制片,用美蓝染色后,采用显微镜观察菌体形态大小并采集图像。
(2)生理生化实验
参考《酵母菌的特征与鉴定手册》[15]并进行碳氮源同化实验[16]、糖发酵实验[4]、脲酶实验[17]及产类淀粉实验[6]。
(3)分子生物学鉴定
采用酵母基因组DNA提取试剂盒提取生香酵母的DNA,以其为模板,使用引物为DNA的通用引物ITS1(5'-TCCGTAGGTGAACCTGCGG-3)和ITS4(5'-TCCTCCGCTTATTGATATGC-3')对酵母菌株的内部转录间隔(internal transcribed spacer,ITS)区域序列进行PCR扩增。PCR扩增体系(20 μL):基因组DNA模板1 μL,引物各0.8 μL,脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTP)1.6 μL,Ex Taq DNA聚合酶0.1 μL,Taq buffer 2.0 μL,双蒸水(ddH2O)13.7 μL。PCR扩增条件:95 ℃预变性10 min;95 ℃变性30 s,58 ℃退火30 s,72 ℃延伸35 s,共30个循环;72 ℃再延伸10 min。PCR产物送至广州擎科生物技术有限公司进行测序,测序结果提交至美国国家生物技术信息中心(national center for biotechnology information,NCBI)的GeneBank数据库,基于局部比对搜索工具(basic local alignment search tool,BLAST)进行同源性比对,并通过MEGA 7.0软件中的邻接(neighbor-joining,NJ)法构建系统发育树。
1.3.4 生香酵母耐盐性分析
用接种环取一环斜面试管保藏的菌株,接种于25 mL麦芽汁液体培养基,培养温度30 ℃,转速180 r/min振荡培养40 h获得活化液。将活化后的菌株按5%(V/V)的接种量接种于含0、5%、10%、15%、18%、20%NaCl的麦芽汁培养基,30 ℃、180 r/min振荡培养72 h,每隔3 h取样检测波长600 nm处的吸光度(OD600nm)值,比较菌株在不同盐浓度中的生长情况。
1.3.5 生香酵母培养条件优化
单因素试验:固定菌株接种量为1%,培养温度为30 ℃,转速为180 r/min,培养基装液量为25 mL/250 mL,培养时间为48 h,自然pH值。以酵母的细胞数为评价指标,分别考察培养温度(26 ℃、28 ℃、30 ℃、32 ℃)、初始pH值(4.0、5.0、6.0、7.0)、转速(160 r/min、180 r/min、200 r/min、220 r/min)对菌株生长情况的影响。
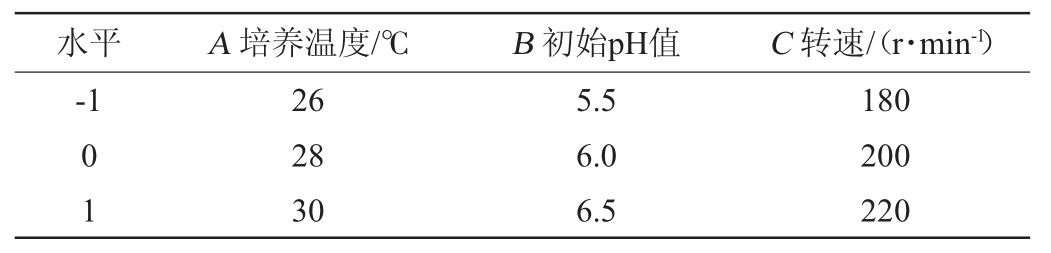
响应面试验:根据单因素试验结果,固定接种量为1%,选取培养温度(A)、初始pH值(B)和转速(C)3个因素为自变量,以酵母细胞数(Y)为响应值,设计3因素3水平的响应面试验进行优化,响应面试验设计因素与水平见表1。
表1 生香酵母培养条件优化响应面试验设计因素与水平
Table 1 Factors and levels of response surface test for culture conditions optimization of aroma-producing yeast
1.3.6 分析检测
根据上述优化的条件进行培养得到发酵液,每隔6 h取5 mL发酵液于10 mL离心管中,8 000 r/min离心10 min,弃上清,用无菌水清洗2次,105 ℃鼓风干燥至恒质量,采用干质量法测定生物量[18];通过3,5-二硝基水杨酸法[19]测定离心后培养基中还原糖的含量。细胞数的测定:参考《微生物学实验》[26]中的血球计数法。
1.3.7 发酵动力学模型的建立
细胞生长动力学模型:Logistic模型是描述细胞生长的最佳动力学模型之一,并且是一个典型的S型曲线,在符合菌体生长趋势的同时,也能较好的反映菌体自身生长对自己的抑制作用[20-21]。根据试验结果显示,此酵母的生长呈现S型,因此选用Logistic模型[22]来描述菌体细胞的生长。
细胞生长模型的微分表达式如数学式(1)所示:
数学式(1)积分得数学式(2),即为细胞生长动力学的代数方程:

式中:X0为菌体初始生物量,g/L;Xm为菌体最大生物量,g/L;Xt为t时刻的菌体生物量,g/L;μm为最大比生长速率,h-1;t为发酵时间,h。
底物消耗动力学模型:根据物料平衡,发酵过程中底物的消耗通常用作新生菌体的合成、细胞基本生命活动的维持以及产物的合成[23-24]。因此底物消耗动力学模型可用与Luedeking-piret[25]相似的方程来描述,Luedeking-piret方程的表达式如数学式(3)所示:
式中:S为底物质量浓度,g/100 mL;YX/S为菌体对底物的得率系数;YP/S为产物对底物的得率系数;m为细胞维持系数;t为发酵时间,h。
在菌体生长期阶段,底物的消耗主要用于菌体的生长和细胞维持上[24],因此数学式(3)可转化为数学式(4):

由于菌体处于稳定期时,![]() ,X=Xm,将其代入数学式(5)可得数学式(6):
,X=Xm,将其代入数学式(5)可得数学式(6):
将数学式(1)、(2)代入数学式(5)并积分可得:S=S0-k1A(t)-k2B(t),即数学式(7):
1.3.8 数据分析
利用SPSS 22软件进行方差分析和显著性分析,使用Origin 2019软件进行制图,培养条件的优化利用Design-Expert 11软件进行设计。
2 结果与分析
2.1 生香酵母的筛选
将初步镜检为酵母的菌株,接种于麦芽汁固体培养基和液体培养基中,30 ℃培养4 d后进行嗅闻,其风味特征见表2。
表2 生香酵母在固体和液体麦芽汁培养基培养条件下的风味特征
Table 2 Flavor characteristics of aroma-producing yeast cultured in solid and liquid wort medium
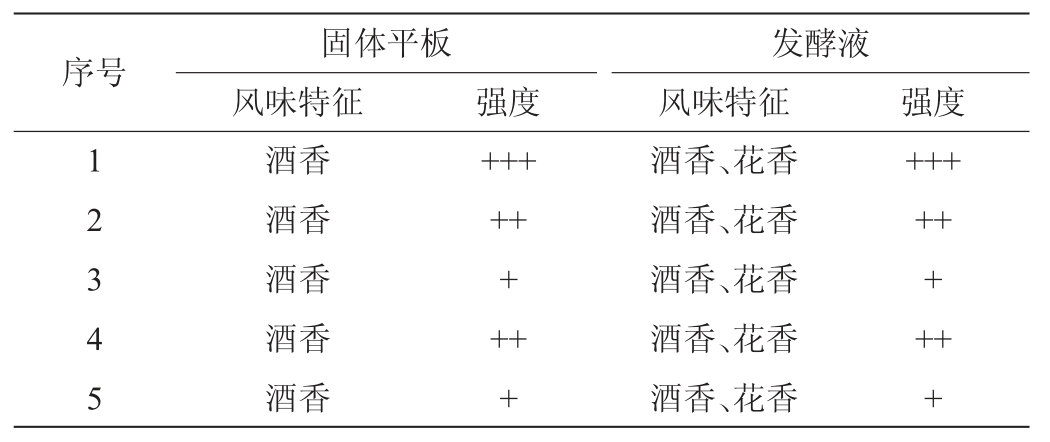
注:“+++”表示风味强;“++”表示风味中等;“+”表示风味较弱。
由表2可知,筛选得到5株生香良好的菌株,固体平板上培养时其风味特征表现为酒香,但其风味强度略有差异;在液体培养基中培养时其风味特征表现为酒香和花香,同样在风味强度方面存在差异,最终选取具有浓郁酒香和花香的1号菌株进行后续试验,命名为菌株Flae04。
2.2 生香酵母的鉴定
2.2.1 形态观察
将筛选所得酵母Flae04采用平板划线分离法划线于含100 g/L NaCl的麦芽汁琼脂培养基中,30 ℃培养4 d后观察菌落形态并进行镜检,其菌落及细胞形态见图1。由图1a可知,该菌株的菌落光滑,呈圆形,隆起,边缘整齐,不透明,易挑,颜色呈乳白色,具有怡人的酒香味;由图1b可知,该菌株细胞呈椭圆形、卵圆形,单边芽殖,细胞大小为长轴3.6~6.0 μm,短轴2.3~4.8 μm。
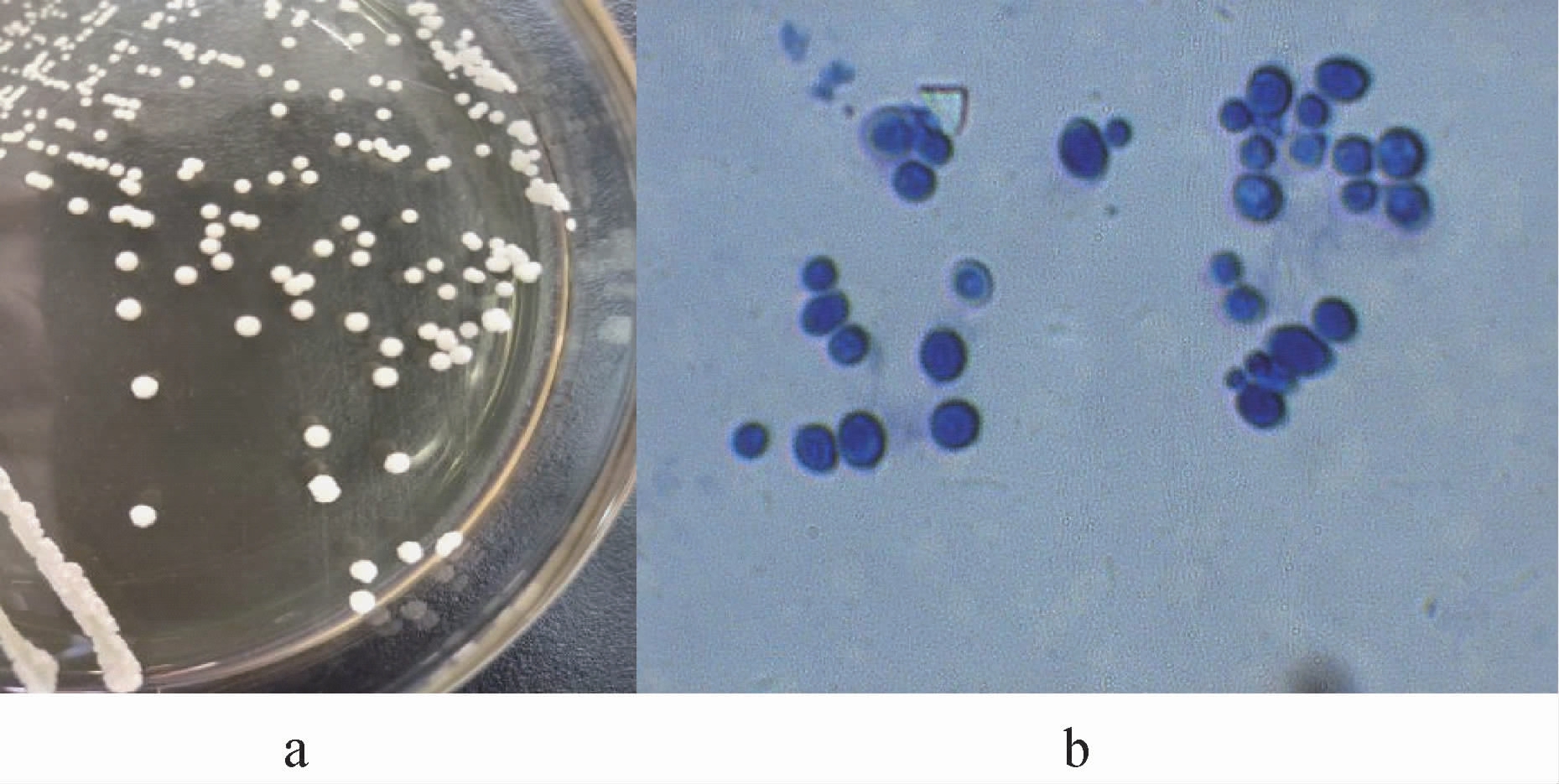
图1 酵母Flae04菌落(a)和细胞(b)形态
Fig.1 Colony (a) and cell (b) morphologies of yeast Flae04
2.2.2 生理生化特性
将筛选所得酵母Flae04进行生理生化特性的研究,结果见表3。由表3可知,该菌株能利用葡萄糖、麦芽糖、果糖等碳源;不能利用硝酸钠、硫酸铵等无机氮;不能产生类淀粉化合物,不能分解尿素;37 ℃时可生长。试验结果与徐成龙等[27]的研究结果类似,初步确定为鲁氏接合酵母(Zygosaccharomyces rouxii)。
表3 酵母Flae04的生理生化特性
Table 3 Physiological and biochemical characteristics of yeast Flae04

注:“+”表示结果呈阳性;“-”表示结果呈阴性。
2.2.3 分子生物学鉴定
采用MEGA 7.0软件中的NJ法构建系统发育树,结果见图2。

图2 酵母Flae04基于ITS基因序列的系统发育树
Fig.2 Phylogenetic tree of yeast Flae04 based on ITS gene sequence
由图2可知,酵母Flae04与鲁氏接合酵母(Zygosaccharomyces rouxii)聚于一支,经序列比对分析,发现其相似度高达99.84%。按照分子生物学鉴定结果,再参考《酵母菌特征及鉴定手册》[15]对酵母的分类,结合酵母Flae04的生理生化特性,可以确定该酵母为鲁氏接合酵母(Zygosaccharomyces rouxii)。
2.3 生香酵母菌株的耐盐性分析
耐盐性是酵母可在酱油酿造中发挥作用的一个重要性能,高盐稀态发酵过程中盐浓度约在17%~18%左右[4],酵母Flae04在不同盐浓度条件下的生长曲线见图3。由图3可知,NaCl浓度为0~10%时,菌株Flae04的生长几乎不受盐浓度的影响,0~3 h为菌株Flae04的迟滞期,3~21 h为对数生长期,21~42 h为稳定期,42~72 h为衰亡期;NaCl浓度增加到15%时,0~9 h为菌株Flae04的迟滞期,9~30 h为对数生长期,30~48 h为稳定期,48~72 h为衰亡期;当NaCl浓度增加到18%时,0~15 h为迟滞期,15~48 h为对数生长期,48~72 h为稳定期;当NaCl浓度增加到20%时,0~27 h为菌株Flae04的迟滞期,27~72 h时处于对数生长期。说明菌株Flae04耐受20%的盐度环境,具有较高的耐盐性,可在酱油生产中发挥作用,也可应用在其他高含盐发酵食品中,与谭戈等[28]的研究结果一致。
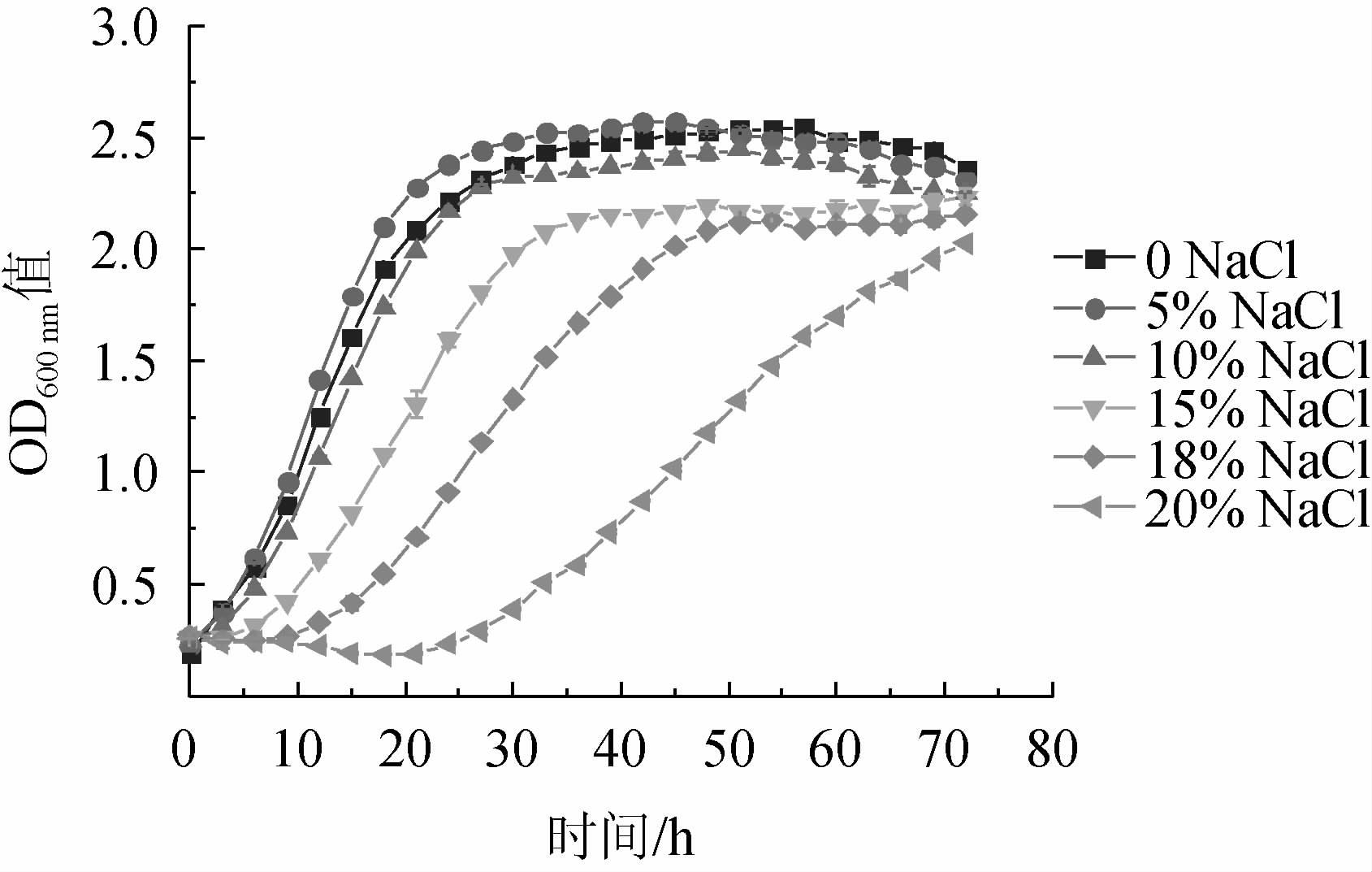
图3 生香酵母在不同浓度NaCl中的生长曲线
Fig.3 Growth curves of aroma-producing yeast in different concentrations of NaCl
2.4 生香酵母Flae04的培养条件优化单因素试验结果
2.4.1 培养温度对酵母Flae04生长的影响
培养温度对酵母Flae04细胞数的影响见图4。由图4可知,当培养温度在26~28 ℃时,酵母Flae04的细胞数逐渐增加;培养温度为28 ℃时,细胞数达到最大值,为3.10×108个/mL;当培养温度>28 ℃时,细胞数逐渐减少,说明过高的培养温度不利于酵母的生长。因此,确定最适的培养温度为28 ℃。
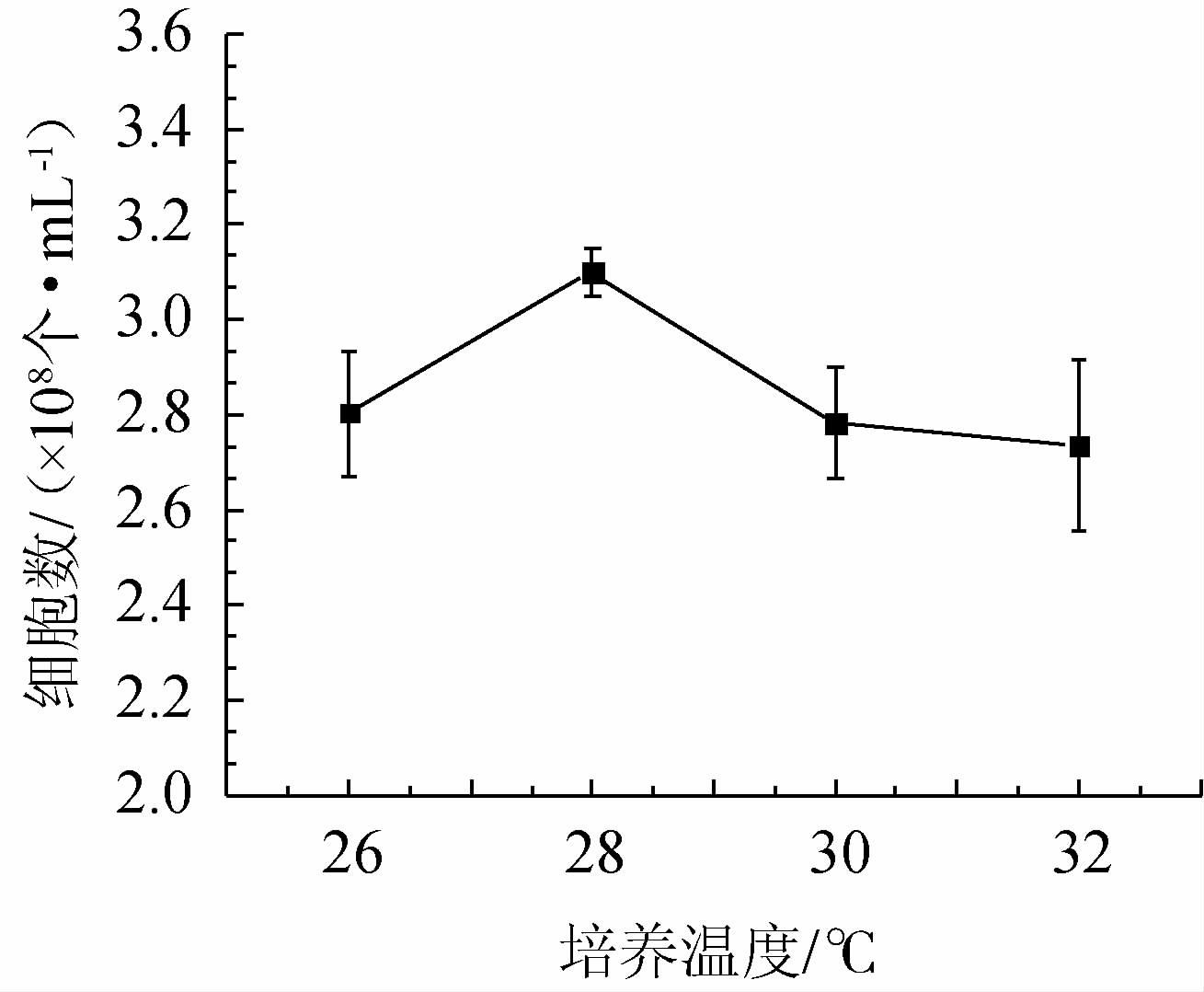
图4 培养温度对酵母Flae04细胞数的影响
Fig.4 Effect of culture temperature on cell counts of yeast Flae04
2.4.2 初始pH值对酵母Flae04生长的影响
初始pH值对酵母Flae04细胞数的影响见图5。由图5可知,当初始pH值为4.0~6.0时,酵母菌Flae04细胞数逐渐增加;当初始pH值为6.0时,酵母菌Flae04细胞数达到最大值,为3.06×108个/mL;当初始pH值>6.0时,酵母菌Flae04细胞数逐渐减少,说明该酵母菌适宜生长在偏酸的环境。因此,确定最适的初始pH值为6.0。
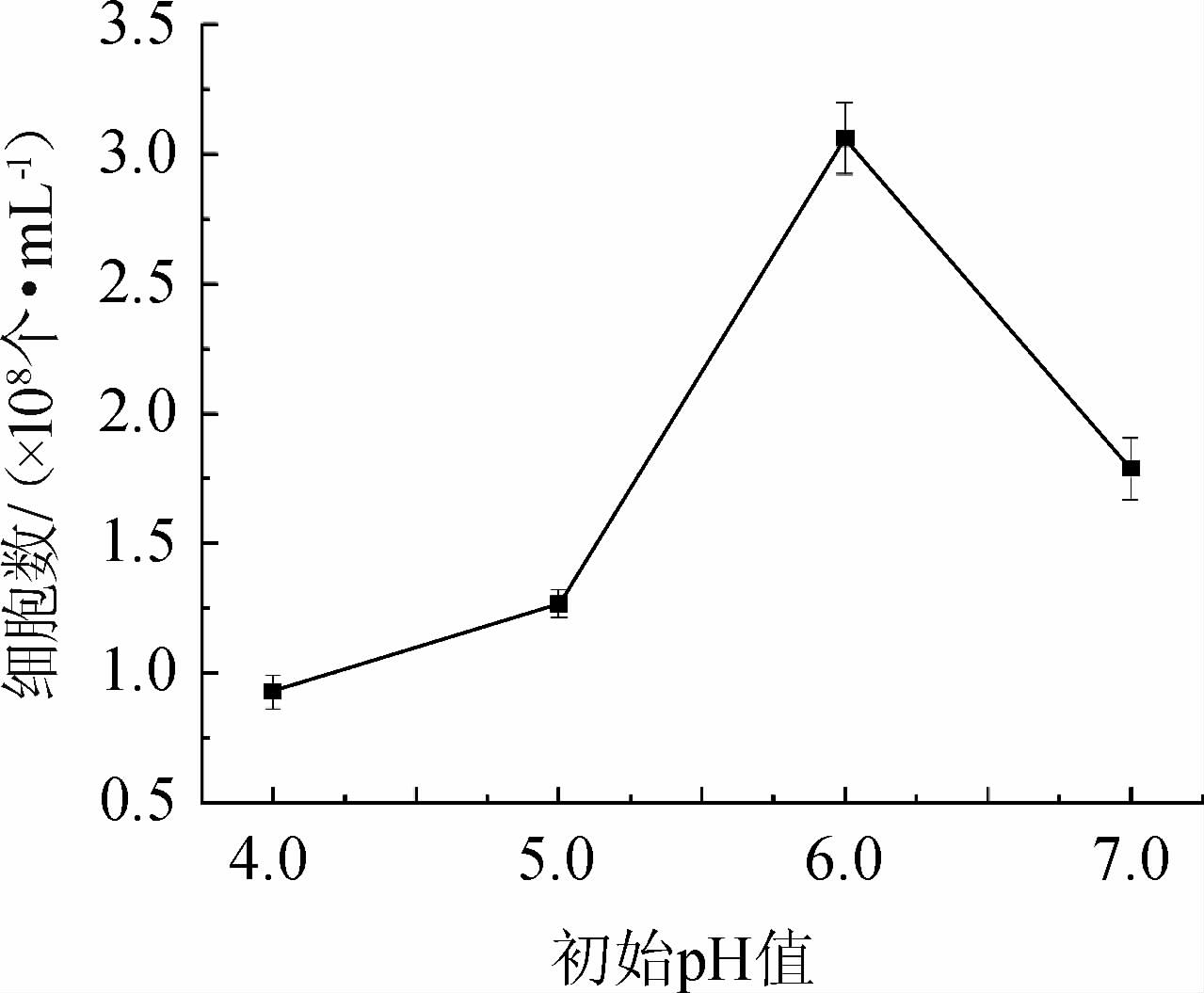
图5 初始pH值对酵母Flae04细胞数的影响
Fig.5 Effect of initial pH on cell counts of yeast Flae04
2.4.3 转速对酵母Flae04生长的影响
转速对酵母Flae04细胞数的影响见图6。由图6可知,当转速为160~200 r/min时,酵母菌Flae04细胞数逐渐增加;当转速为200 r/min时,酵母菌Flae04细胞数达到最大值,为2.69×108个/mL;当转速>200 r/min时,酵母菌Flae04细胞数逐渐减少,说明转速的改变影响液体中溶解氧值,进而影响菌体的生长代谢[29]。因此,确定最适的转速为200 r/min。
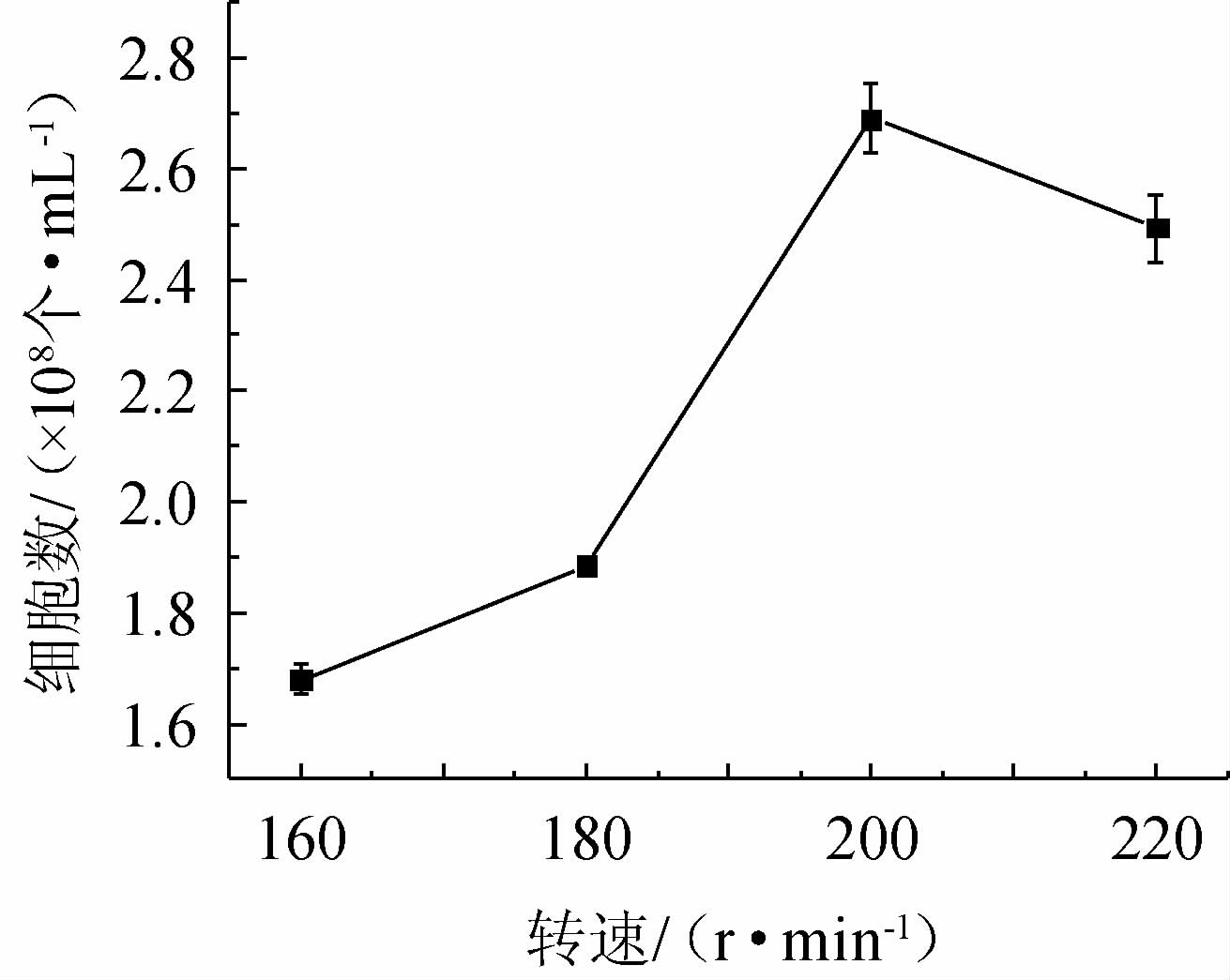
图6 转速对酵母Flae04细胞数的影响
Fig.6 Effect of rotation speed on cell counts of yeast Flae04
2.5 生香酵母Flae04培养条件优化响应面试验
在单因素试验结果的基础上,固定接种量为1%,以培养温度(A)、初始pH值(B)和转速(C)为自变量,以酵母细胞数(Y)为响应值,利用Design-Expert11.0软件进行Box-Behnken试验设计,试验设计与结果见表4,方差分析见表5。
表4 生香酵母培养条件优化Box-Behnken试验设计及结果
Table 4 Design and results of Box-Behnken test for culture conditions optimization of aroma-producing yeast
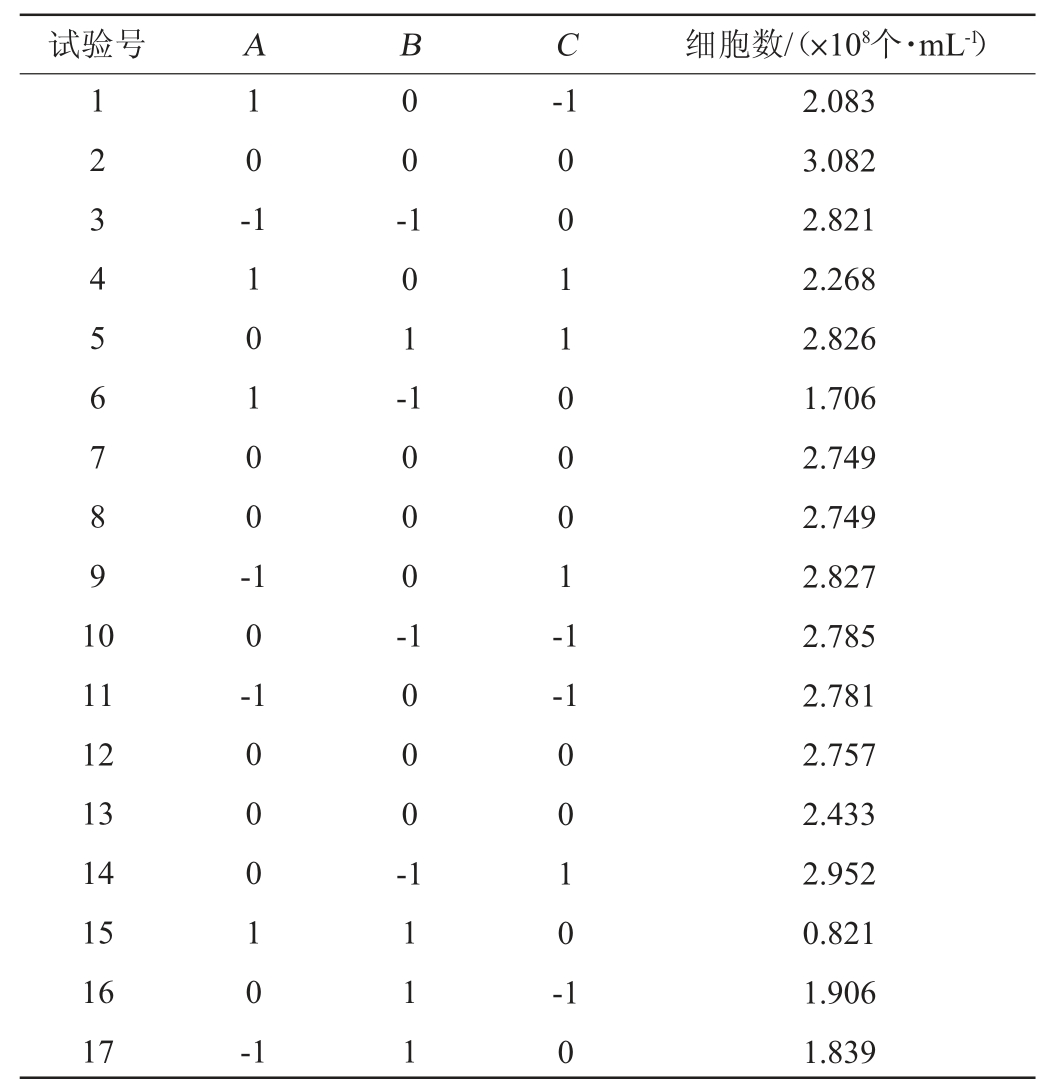
对表4中的数据进行多元二次回归拟合,其回归方程为:
由表5可知,回归模型的P值为0.005 8<0.01,表明该模型极显著,且失拟项P=0.290 9>0.05,表明失拟项差异不显著,试验误差较小,拟合度较好,回归模型可充分反应实际情况。模型的决定系数R2=0.912 4,调整决定系数R2Adj=0.799 8,表明试验结果有79.98%受试验因素的影响。因此可利用此模型对菌株培养条件进行分析和预测。由表5亦可知,一次项A、B、二次项A2对酵母Flae04细胞数的影响极显著(P<0.01),二次项B2对酵母Flae04细胞数的影响显著(P<0.05),其他项不显著(P>0.05)。由F值可知,影响酵母细胞数的因素主次顺序为A>B>C,即培养温度>初始pH值>转速。
表5 回归模型方差分析
Table 5 Variance analysis of regression model
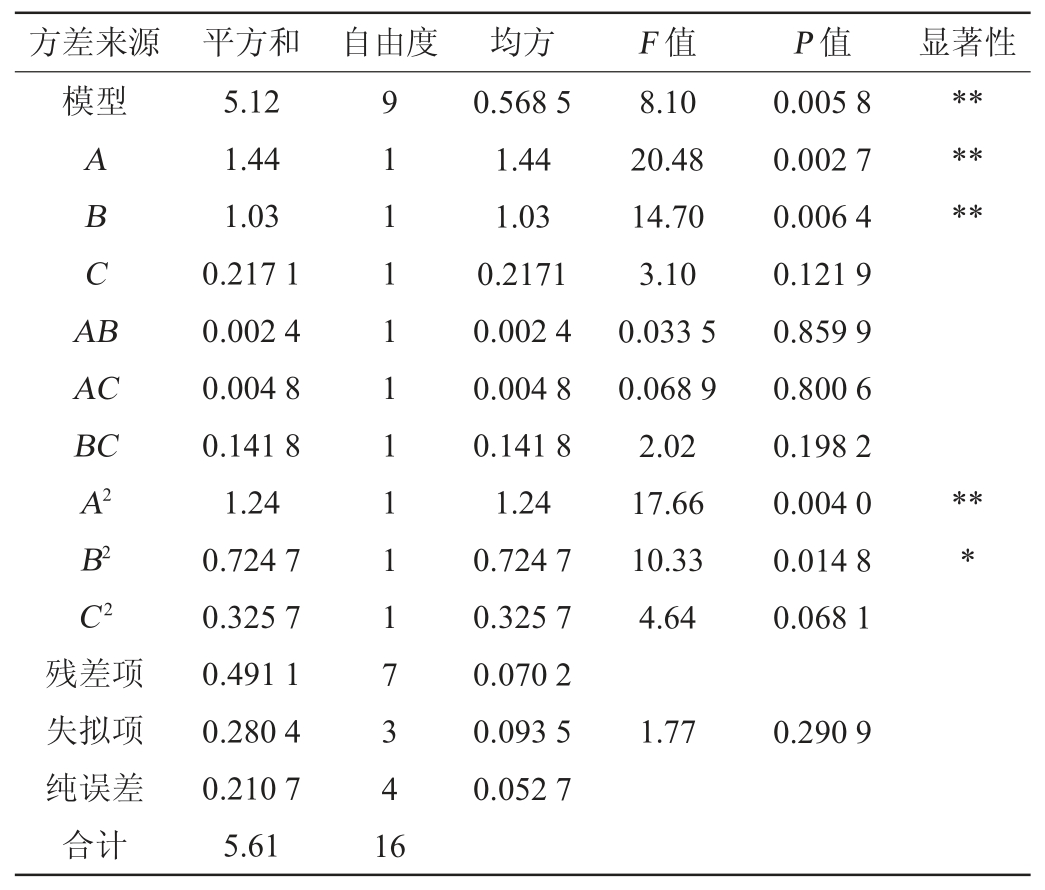
注:“**”表示对结果影响极显著(P<0.01);“*”表示对结果影响显著(P<0.05)。
利用Design-Expert11.0软件对响应面试验所得结果进行分析,得出菌株培养条件为培养温度27.71 ℃、初始pH值5.65、转速181.44 r/min,在此条件下,细胞数预测值为3.18×108个/mL;考虑到实际操作可行性,将最佳培养条件修正为培养温度28 ℃、初始pH值5.7、转速181 r/min,在该优化条件下进行验证试验,酵母细胞数实际值为3.33×108个/mL,实际值与预测值接近,表明此模型可以较好地预测酵母的生长情况。
2.6 发酵动力学模型的建立
2.6.1 细胞生长动力学模型
利用Origin 2019对试验数据进行拟合,得到动力学参数为X0=0.2,Xm=13.4,μm=0.055,将其代入数学式(2)得到细胞生长动力学方程:
用Logistic方程对试验数据进行非线性拟合,细胞生长动力学模型拟合曲线见图7。由图7可知,相关系数R2=0.997,说明该方程的试验值与预测值拟合良好,能够很好地描述酵母在分批发酵过程中菌体的生长情况。
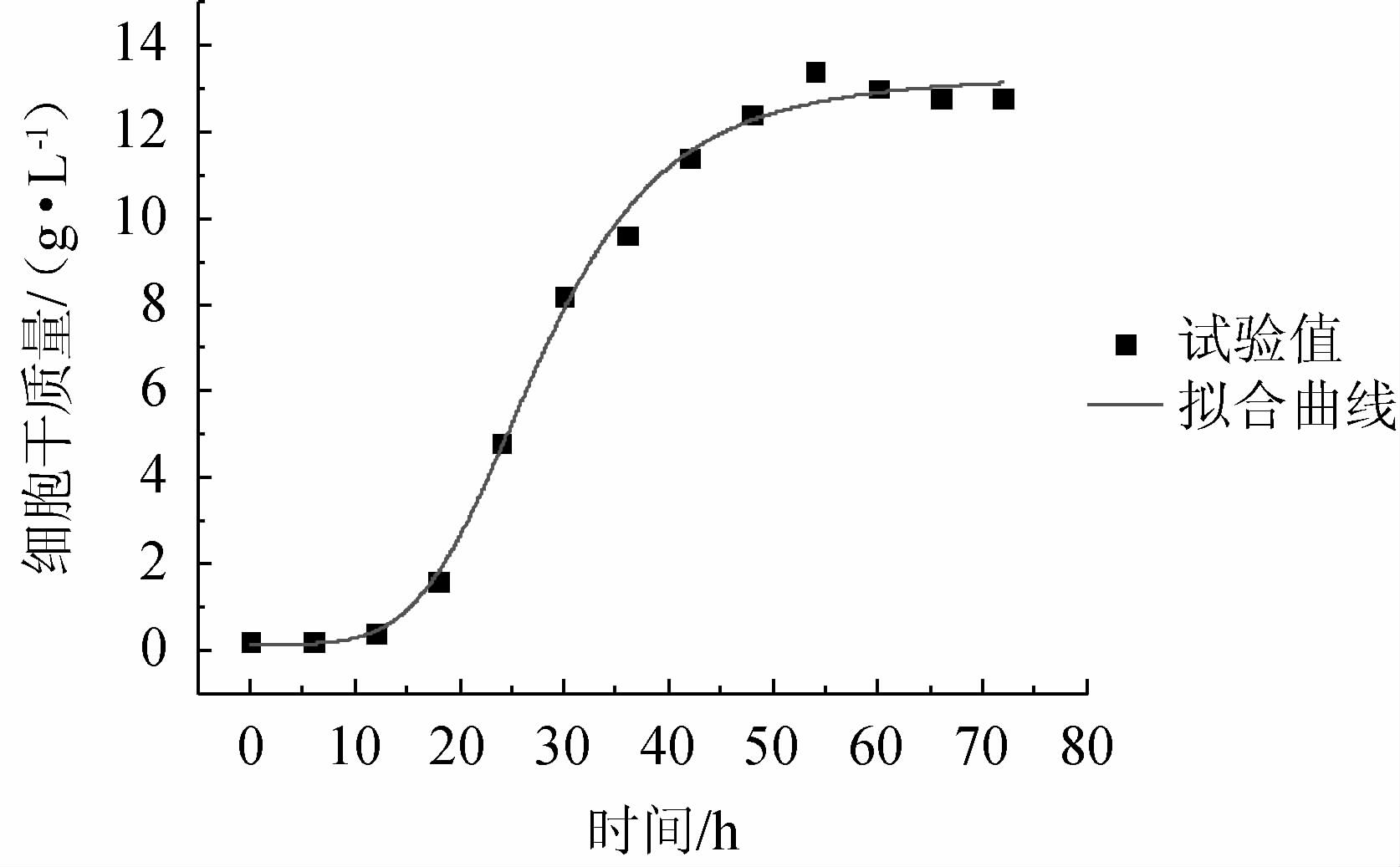
图7 细胞生长动力学模型拟合曲线
Fig.7 Fitting curve of kinetic model of cell growth
2.6.2 底物消耗动力学模型
利用Origin 2019软件对发酵过程中底物S和发酵时间t作图,进行拟合得到:S=-0.193 1t+11.605,由此可知![]() =-0.1931,由数学式(6)可知k2=0.01441。随后以S=S0-k2B(t)~A(t)作图,进行拟合后得到:S=S0-k2B(t)=-0.130 2A(t)-2.717 2,可得k1=0.130 2,将X0=0.2,Xm=13.4,μm=0.055,k1=0.130 2,k2=0.014 41,S0=11.113 9,代入数学式(7)得到底物消耗动力学方程:
=-0.1931,由数学式(6)可知k2=0.01441。随后以S=S0-k2B(t)~A(t)作图,进行拟合后得到:S=S0-k2B(t)=-0.130 2A(t)-2.717 2,可得k1=0.130 2,将X0=0.2,Xm=13.4,μm=0.055,k1=0.130 2,k2=0.014 41,S0=11.113 9,代入数学式(7)得到底物消耗动力学方程:
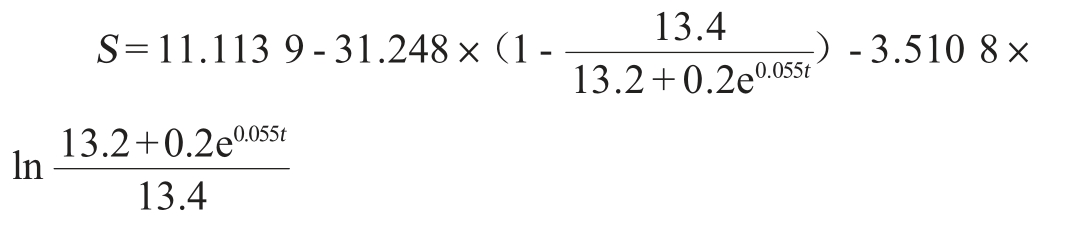
底物消耗动力学模型的拟合曲线如图8所示,相关系数R2=0.995,说明该方程与试验值拟合良好,能很好地描述酵母发酵过程中底物浓度的变化。
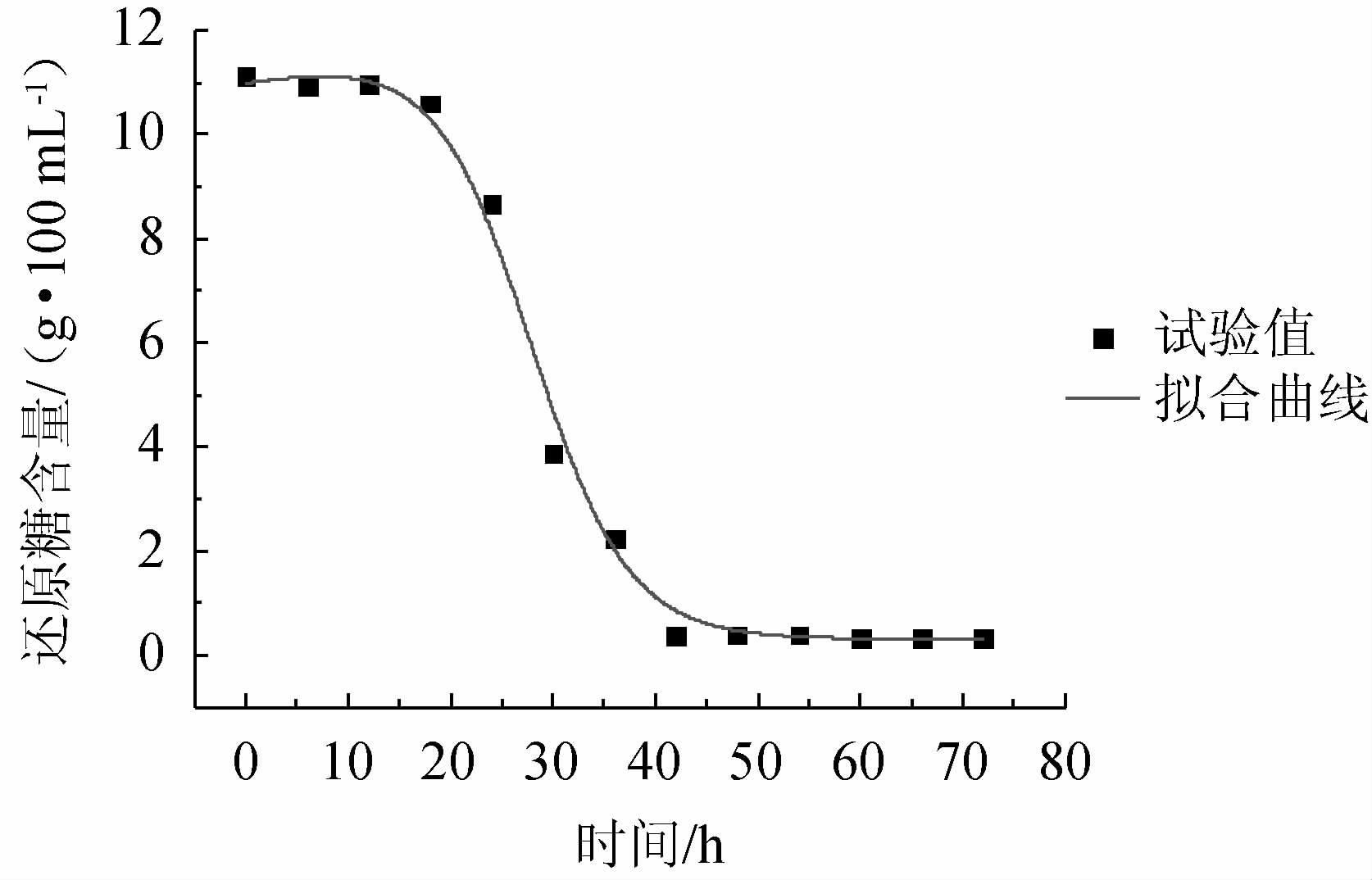
图8 底物消耗动力学模型拟合曲线
Fig.8 Fitting curve of kinetic model of substrate consumption
3 结论
本研究从酱油发酵醪中筛选出1株生香酵母,编号为Flae04,经鉴定为鲁氏接合酵母(Zygosaccharomyces rouxii),该菌株在NaCl浓度为20%时仍可正常生长,可应用于高盐发酵食品中;通过单因素试验与响应面试验优化确定其最适培养条件为培养温度28 ℃、初始pH值5.7、转速181 r/min,在此优化条件下,酵母细胞数为3.33×108个/mL;同时利用Logistic方程与类Luedeking-piret方程分别构建细胞生长和底物消耗动力学模型,相关系数R2分别为0.997和0.995,说明试验值与模型拟合良好,很好地描述了酵母Flae04在生长代谢过程中生物量与还原糖消耗之间的联系,为酵母Flae04的发酵过程控制及其酱油风味改善提供理论参考。
[1]吴婷.酱油发酵工艺条件优化的研究[D].长沙:湖南农业大学,2013.
[2]LIU J,LI D,HU Y,et al.Effect of a halophilic aromatic yeast together withAspergillusoryzae in koji makingon the volatile compoundsand quality of soy sauce moromi[J].Int J Food Sci Technol,2015,50(6):1352-1358.
[3]DEVANTHI P V P,LINFORTH R,ONYEAKA H,et al.Effects of co-inoculation and sequential inoculation of Tetragenococcus halophilus and Zygosaccharomyces rouxii on soysauce fermentation[J].Food Chem,2018,240:1-8.
[4]王靖雯,赵谋明,陈涛,等.高盐稀态酱醪中功能性酵母菌的筛选、鉴定及发酵特性[J].食品科学,2021,42(22):91-97.
[5]ZHAO G,DING L L,HADIATULLAH H,et al.Characterization of the typical fragrant compounds in traditional Chinese-type soy sauce[J].Food Chem,2020,312:126054.
[6]李晨.一株产香酵母的筛选、鉴定及其产香条件的优化研究[D].武汉:武汉轻工大学,2019.
[7]彭东,蒋雪薇,陈幽,等.高盐稀态酱醪中耐盐生香酵母的筛选及生香特性研究[J].食品与发酵工业,2020,46(13):76-84.
[8]谭才邓,王文文,朱美娟,等.1株耐高温高盐生香酵母的选育及特性分析[J].食品与发酵工业,2016,42(3):92-96.
[9]LI Y,DU W,MENG F,et al.Tartary buckwheat protein hydrolysates enhance the salt tolerance of the soy sauce fermentation yeast Zygosaccharomyces rouxii[J].Food Chem,2021,342:128382.
[10]JIANG X W,PENG D,ZHANG W,et al.Effect of aroma-producing yeasts in high-salt liquid-state fermentation soy sauce and the biosynthesis pathways of the dominant esters[J].Food Chem,2021,344:12868.
[11]李学伟,陈强,朱新贵.添加生香酵母改善酱油风味的研究[J].中国酿造,2014,33(3):121-124
[12]WANG J W,ZHAO M M,XIE N Y,et al.Community structure of yeast in fermented soy sauce and screening of functional yeast with potential toenhance the soy sauce flavor[J].Int J Food Microbiol,2022,370:109652.
[13]冯杰.埃切假丝酵母产香机理及其对酱油风味的影响[D].无锡:江南大学,2012.
[14]黄鑫,唐红梅,唐青莲,等.大头菜发酵过程中生香酵母的分离、筛选及鉴定[J].食品研究与开发,2019,40(18):198-203.
[15]BARNETT J A.酵母菌的特征与鉴定手册[M].青岛:青岛海洋大学出版社,1991:188-189.
[16]徐文欢,吴若菡,李采婵,等.传统虾酱中酵母菌分离鉴定及碳源利用特性[J].中国食品学报,2021,21(4):303-309.
[17]李秀婷.食品微生物学实验技术[M].北京:化学工业出版社,2020.
[18]续丹丹,王文平,张欣,等.一株耐盐产香鲁氏接合酵母FA-1的鉴定及其在酱油酿造中的应用[J].中国酿造,2022,41(12):31-39.
[19]王明瑞,侯彦喜,张亚丹.3,5-二硝基水杨酸法测定发酵液中多糖含量[J].现代食品,2020(4):216-222.
[20]BRICKWEDDE A,VAN DEN BROEK M,GEERTMAN J A,et al.Evolutionary engineering in chemostat cultures for improved maltotriose fermentation kinetics in Saccharomyces pastorianus lager brewing yeast[J].Front Microbiol,2017,8:1690.
[21]PERES C M,ALVES M,HERNANDEZ-MENDOZA A,et al.Novel isolates of lactobacilli from fermented Portuguese olive as potential probiotics[J].LWT-Food Sci Technol,2014,59(1):234-246.
[22]余瞻,赵福权,徐成龙,等.红茶菌中细菌纤维素产生菌的筛选、鉴定及其发酵动力学模型构建[J].食品与发酵工业,2021,47(6):92-98.
[23]KASHID M,GHOSALKAR A.Evaluation of fermentation kinetics of xylose to ethanol fermentation in the presence of acetic acid by Pichia stipitis:Modeling and experimental data comparison[J].Indian J Chem Techn,2018,25(1):31-39.
[24]蒋艾廷,李新玲,姜淑娟,等.一株优选酿酒酵母增殖培养条件优化及发酵动力学模型的构建[J].食品科学技术学报,2018,36(1):45-52.
[25]LUEDEKING R,PIRET E L.A kinetic study of the lactic acid fermentation.Batch process at controlled pH[J].Biotechnol Bioeng,2000,67(6):636-644.
[26]陈向东,沈萍.微生物学实验第5版[M].北京:高等教育出版社,2018.
[27]徐成龙,王珍珍,余瞻,等.食用植物酵素中酵母菌的分离鉴定及耐受性研究[J].食品与发酵工业,2021,47(4):80-86.
[28]谭戈,朱新贵,李学伟,等.强化鲁氏接合酵母对酱油品质的影响[J].食品工业科技,2022,43(13):86-93
[29]魏春红,盛艳,吴泽柱.耐高温酒用酵母发酵生长条件的优化[J].食品研究与开发,2017,38(3):169-172.