乳酸菌是一类革兰氏阳性、无芽孢类细菌,包括乳球菌属、乳杆菌属、双歧杆菌属等,生长过程中能够代谢碳水化合物产生乳酸、细菌素、胞外多糖等活性成分[1]。乳酸菌是国际公认的可用于食品发酵的益生菌[2-3],具有抑菌、调节肠道菌群、增强免疫力、促进营养吸收、降低胆固醇等多种功能益处[4-6]。近年来,随着我国消费大众健康意识的增强,消费者逐渐倾向于功能性营养饮食,以食疗的方式增强免疫力、预防疾病的诉求加速了益生菌类产品的发展。然而益生菌类产品发挥健康益处的基本要求是活菌且菌体密度不低于107 CFU/g(或CFU/mL)[7-8]。培养基组成及培养条件的选择对于益生菌的生长至关重要[9-10],因此二者的优化也成为当下提升益生菌菌体密度的常规手段[11-12],如李娜等[13]以吸光度值为响应值,通过单因素、响应面试验优化了植物乳杆菌ZJ316的培养基配方,优化后活菌数提高了3.44倍。
谷糠乳杆菌(Lactobacillus farraginis)是乳杆菌属的一种,具有耐酸性强、生长速度快、发酵温域宽等优点,可作为食品发酵剂[14],也常被应用于饲料贮存、食品防腐等方面[15-17]。实验室前期从我国民间酵素食品中筛选到一株谷糠乳杆菌84-M-Y-7,利用该菌株发酵石斛、葛根、黄芪等中草药,获得了系列功能性药食同源发酵饮品,最大程度的保留了中草药的活性成分,同时改良了传统中草药的风味和口感。故进一步探究该菌株最适培养基成分、培养条件和菌体收集条件,制备高密度菌剂很有必要。
基于此,该研究通过单因素和响应面试验,对谷糠乳杆菌84-M-Y-7的培养基配方及培养条件进行了优化,同时研究了其菌体收集条件,以期得到符合产业开发应用的谷糠乳杆菌84-M-Y-7高密度菌剂,为实现谷糠乳杆菌的产业应用奠定理论基础。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种与试剂
谷糠乳杆菌(Lactobacillus.farraginis)84-M-Y-7,由实验室分离、筛选并保藏于中国微生物菌种保藏管理委员会普通微生物中心(保藏号:CGMCC No.22055)。
乳糖、乙酸钠、磷酸氢二钾、柠檬酸三铵、硫酸镁、硫酸锰、维生素B2、吐温-80,(均为分析纯):北京萃峰科技有限公司;大豆蛋白胨、豆粕粉:市售。
1.1.2 培养基
平板计数培养基、MRS肉汤培养基:北京奥博生物技术有限责任公司。
1.2 仪器与设备
HF160W二氧化碳培养箱:上海力申科学仪器有限公司;DELTA320 pH计:北京海天友诚科技有限公司;spectra MAX190酶标仪:北京科德远扬科技有限公司;BSC-110011A2-X超净工作台:济南鑫贝生物技术有限公司;3K15离心机:济南好来宝医疗器材有限公司。
1.3 方法
1.3.1 菌种活化
谷糠乳杆菌84-M-Y-7菌种保藏于甘油冻存管中(-80℃),菌种按照2%(V/V)的接种量接种于50 mL MRS肉汤培养基中,37 ℃活化培养24 h。
1.3.2 种子液的制备
将活化菌种按照5%(V/V)接种到100 mL MRS肉汤培养基中,37 ℃培养24 h,连续培养3次,制成种子液备用。
1.3.3 菌体量的测定
制备好的种子液按照10%(V/V)的接种量接种到发酵培养基中,37 ℃培养24 h后取0.2 mL置于96孔板中,利用酶标仪在波长600 nm处测定其吸光度值(OD600nm值),得到菌体细胞密度,即菌体量,以OD600nm值反映菌株生长状态。
1.3.4 发酵培养基配方优化
(1)单因素试验优化
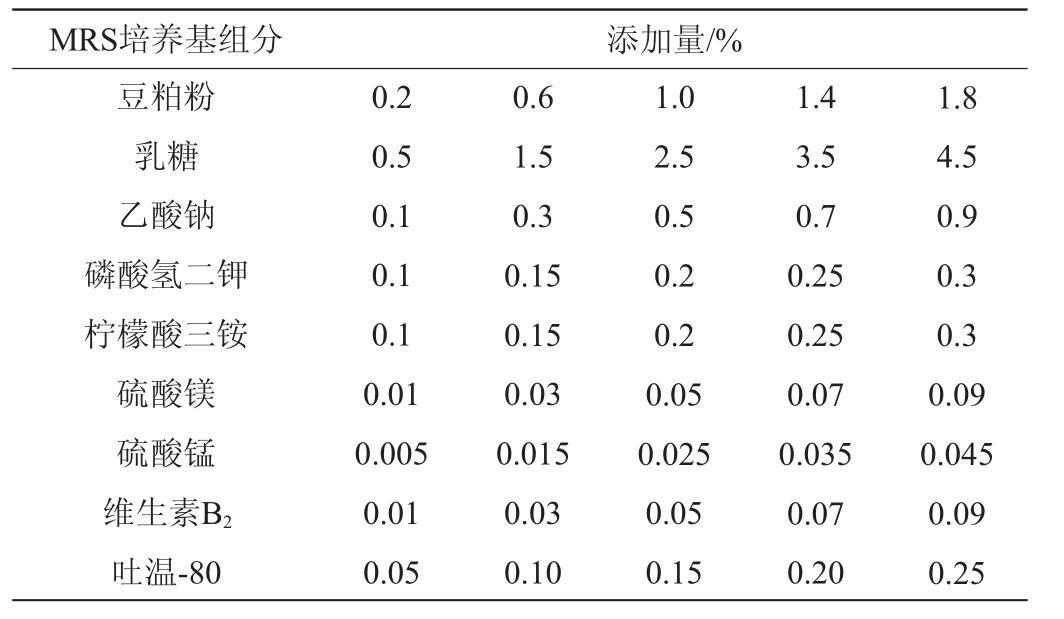
本实验以菌体量为评价指标,通过单因素试验,分别研究MRS肉汤培养基配方中10种组分对谷糠乳杆菌84-M-Y-7生长状态的影响。培养基各组分的添加量详见表1。
表1 培养基各组分添加量设置
Table 1 Design of each component addition of medium
续表
(2)Plackett-Burman(PB)试验设计
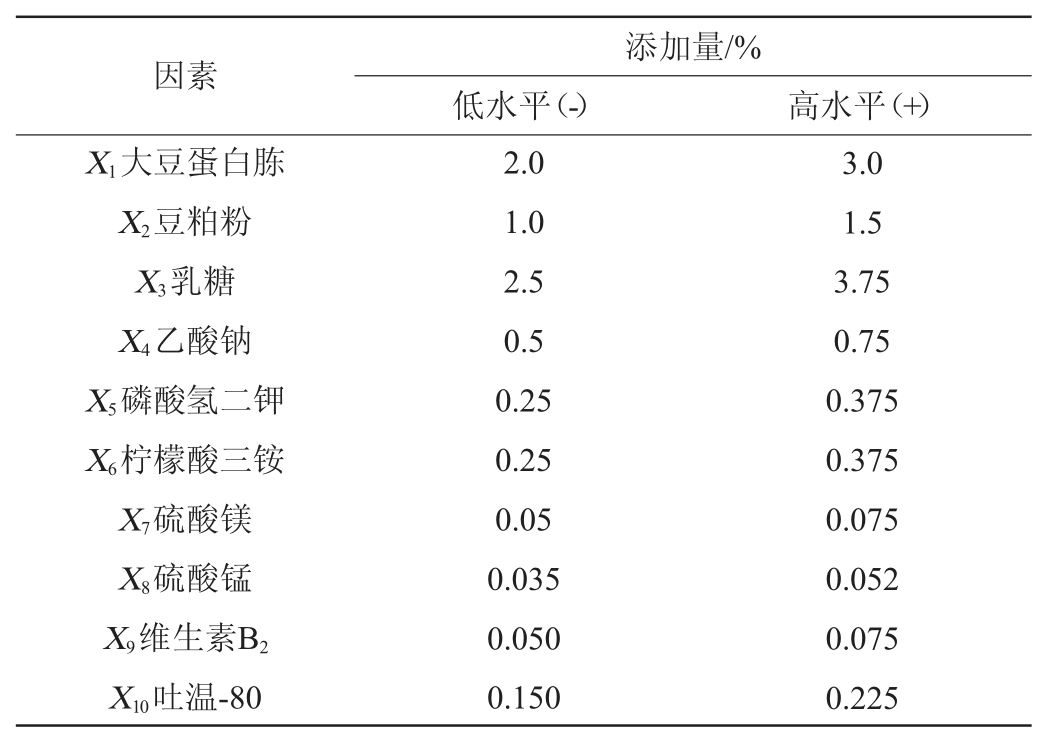
根据单因素试验结果确定的各组分的最佳添加量,考察10种组分对菌体生长影响。每个因素取高和低2个水平(见表2),低水平“-”为单因素试验所得的最佳添加量,高水平“+”为低水平的1.5倍,筛选影响谷糠乳杆菌84-M-Y-7菌体量的重要因素。
表2 发酵培养基配方优化Plackett-Burman试验因素与水平
Table 2 Factors and levels of Plackett-Burman experiments for fermentation medium formula optimization
(3)Box-Behnken试验设计
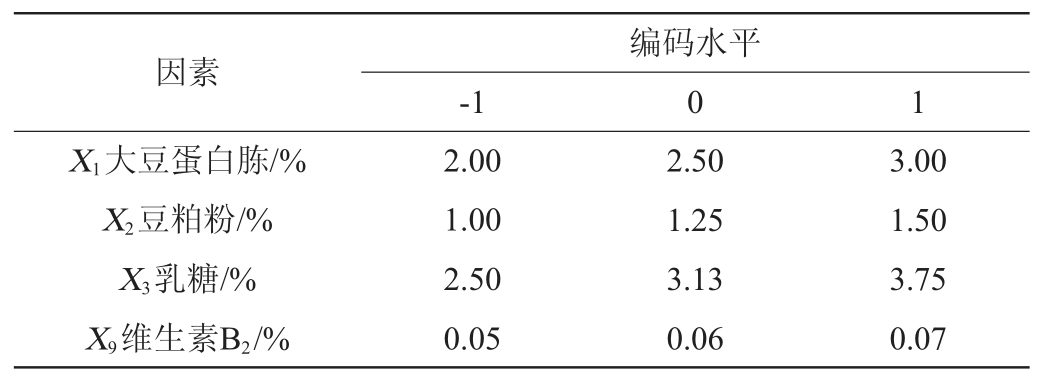
根据PB试验设计结果选择影响谷糠乳杆菌84-M-Y-7生长的4个主要因素。以菌体量作为响应值,设计Box-Behnken试验,确定最佳发酵培养基的配方,试验因素及水平见表3。
表3 发酵培养基配方优化Box-Behnken试验因素与水平
Table 3 Factors and levels of Box-Behnken experiments for fermentation medium formula optimization
1.3.5 谷糠乳杆菌84-M-Y-7培养条件的优化
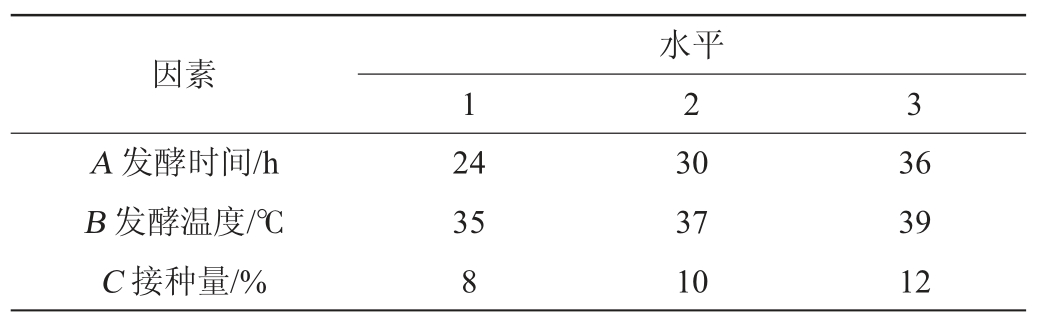
在单因素试验的基础上,选择发酵时间、发酵温度和接种量为影响因素,以菌体量为评价指标,进行3因素3水平的正交试验,优化培养条件,正交试验因素与水平见表4。
表4 谷糠乳杆菌培养条件优化正交试验因素与水平
Table 4 Factors and levels of orthogonal experiments for culture conditions optimization of Lactobacillus farraginis
1.3.6 菌体最佳收集条件的确定
在无菌条件下,将菌液移入无菌离心管中,考察不同离心转速(2 000 r/min、3 000 r/min、4 000 r/min、5 000 r/min、6000r/min)和离心时间(5min、10min、15min、20min、25min)对湿菌体质量和活菌数的影响[18-19],以确定谷糠乳杆菌84-M-Y-7的最佳菌体收集条件。湿菌质量是不同离心条件处理菌液所获的菌体质量(g/mL),活菌数则通过稀释后将菌液涂布在MRS固体培养基平板上进行测定(CFU/mL)。
1.3.7 数据处理
所有试验重复3次,采用Excel 2010记录并计算数据,结果以“平均值±标准差”表示。试验数据利用SPSS17.0软件、Design-Expert 8.0.6响应面软件进行分析并利用GraphPad Prism 7.0软件进行作图。
2 结果与分析
2.1 发酵培养基配方优化单因素试验结果
乳酸菌对培养基组成的要求比较严格,除了碳源、氮源等必需营养物质外,对金属离子、维生素等生长因子的需求也很高[20]。MRS培养基各组分添加量对谷糠乳杆菌84-M-Y-7 菌体量的影响见图1。由图1a-1j可知,随着各组分添加量的增加,所有组分对菌体量影响的变化趋势相同,即先增加后下降,所有的参数均出现峰值,表明合适质量浓度范围内,谷糠乳杆菌84-M-Y-7的生长随之增加。乳酸菌细胞酶系简单[21],而且MRS培养基属于复合氮源培养基,大豆蛋白胨和豆粕粉添加量较低时,营养组分不能满足菌体的繁殖速度[22],添加量过高时,便会影响酶系的表达,影响谷糠乳杆菌84-M-Y-7对营养物质的吸收,乳糖的变化会调整培养基中碳氮比,引起菌株的自溶或者过早死亡[23];金属离子(Na+、Mg2+、Mn2+等)过量会影响菌体酶活性和转录水平的表达,进而抑制菌体生长。乳酸菌不同菌属之间的代谢途径或酶活性存在差异,培养基中影响其生长过程的重要营养因子也会有所不同。
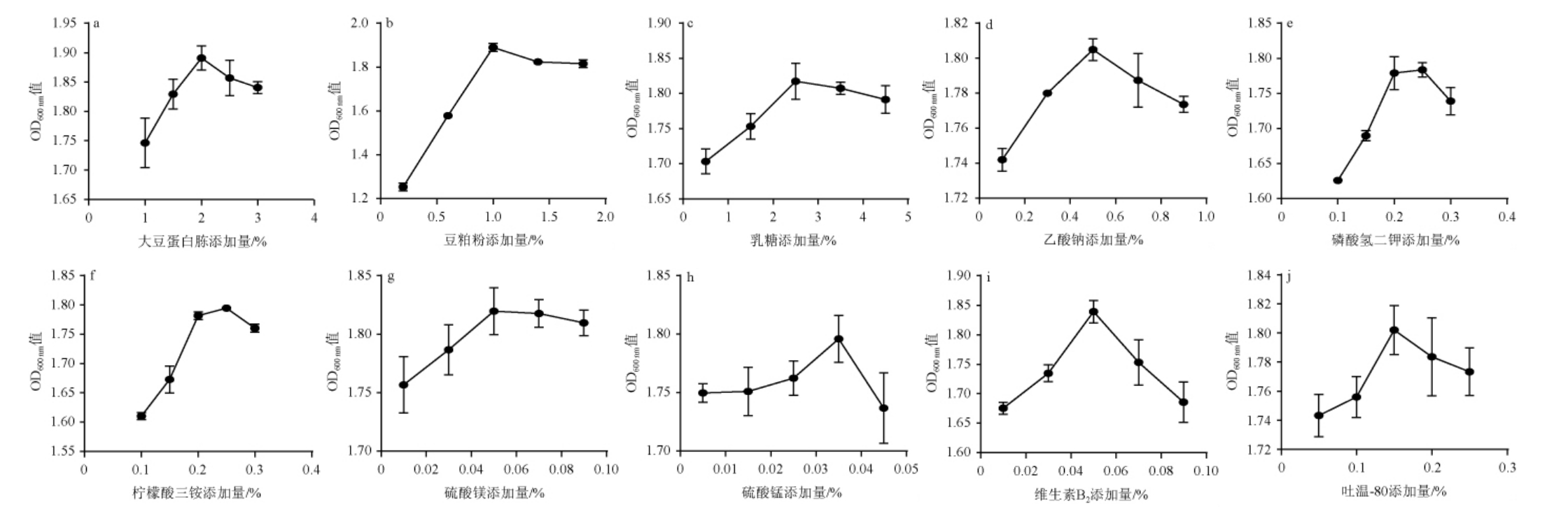
图1 培养基各组分添加量对谷糠乳杆菌菌体量的影响
Fig.1 Effect of each component addition of the medium on the biomass of Lactobacillus farraginis
综上单因素试验可知,培养基配方优化结果为大豆蛋白胨2%、豆粕粉1.0%、乳糖2.5%、乙酸钠0.5%、磷酸氢二钾0.25%、柠檬酸三铵0.25%、硫酸镁0.05%、硫酸锰0.035%、维生素B2 0.05%、吐温-80 0.15%。
2.2 发酵培养基配方优化Placket-Burman试验
本研究通过单因素试验明确10种培养基成分最佳添加量后,通过Placket-Burman设计进一步明确影响谷糠乳杆菌84-M-Y-7菌体量的显著因素。PB试验结果见表5,PB试验结果方差分析见表6。
表5 Plackett-Burman试验设计及结果
Table 5 Design and results of Plackett-Burman experiments
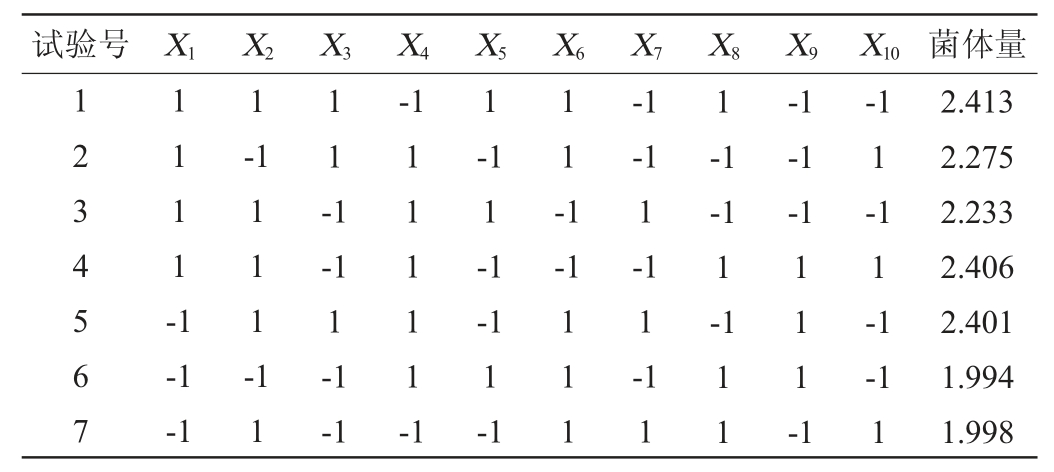
续表
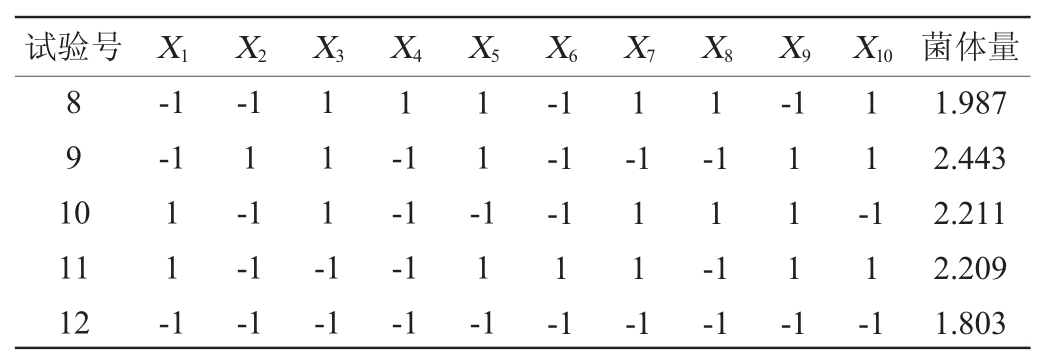
表6 Plackett-Burman试验结果方差分析
Table 6 Variance analysis of Plackett-Burman experiments results
注:“*”表明该变量对响应值的影响显著(P<0.05)。
由表6可知,在10个单因素中,大豆蛋白胨、豆粕粉、乳糖和维生素B2的添加量对谷糠乳杆菌84-M-Y-7的生长影响效应显著(P<0.05),故选择这4个因素进行响应面试验。其他6个因素的影响效应未达到显著,在后续试验中保持单因素试验的MRS培养基水平。
2.3 响应面试验优化发酵培养基配方
2.3.1 Box-Behnken试验结果
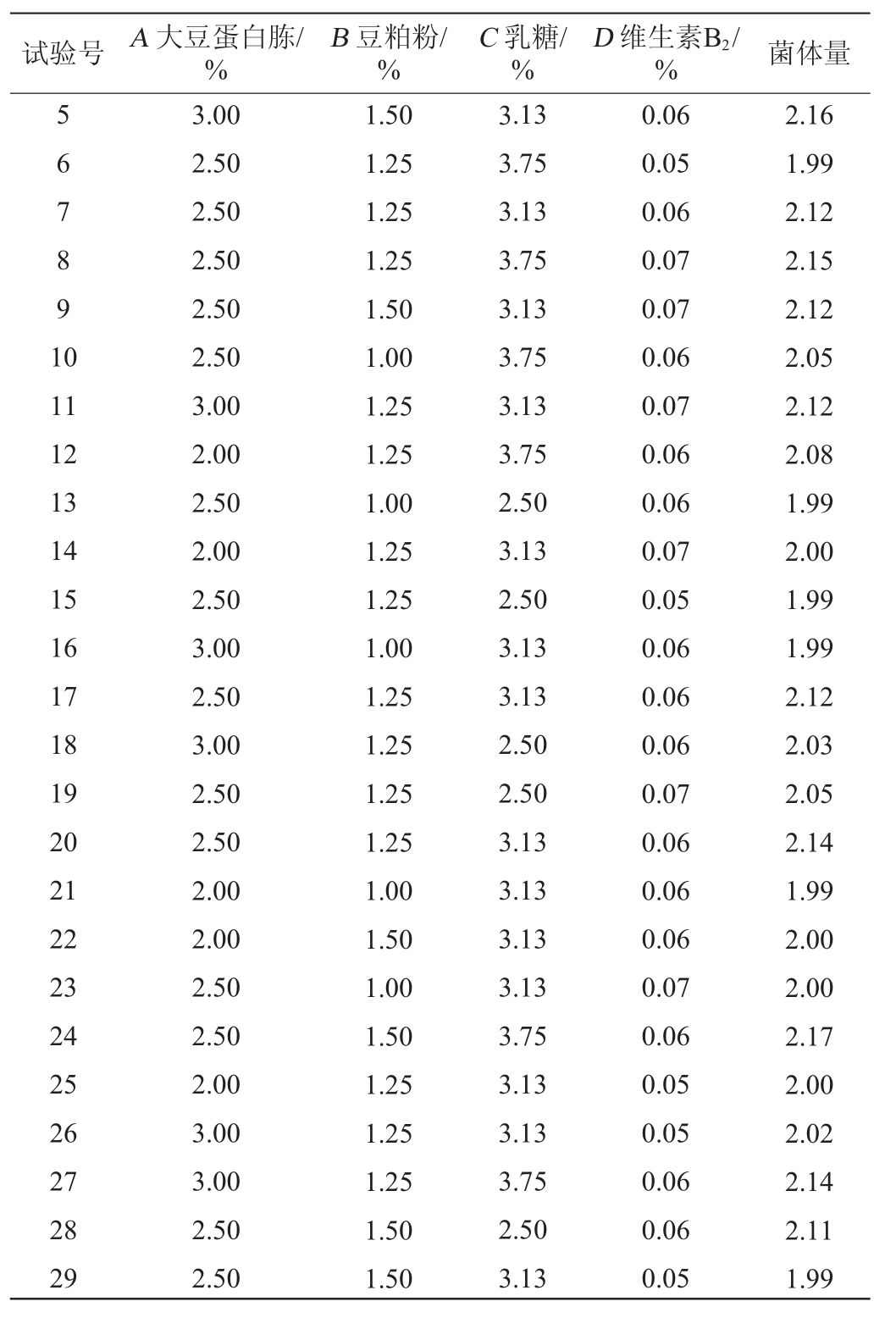
根据单因素试验及Placket-Burman试验结果,选择大豆蛋白胨(A)、豆粕粉(B)、乳糖(C)、维生素B2(D)为评价因素,以菌体量(OD600nm值)(Y)为响应值,通过响应面设计原理,设计4因素3水平的响应面试验,其结果见表7。采用Design-Expert 8.0.6分析软件对所得数据进行回归分析,得到多元二次回归方程为:

表7 发酵培养基配方优化响应面试验设计及结果
Table 7 Design and results of response surface experiments for fermentation medium formula optimization

续表
2.3.2 回归模型方差分析
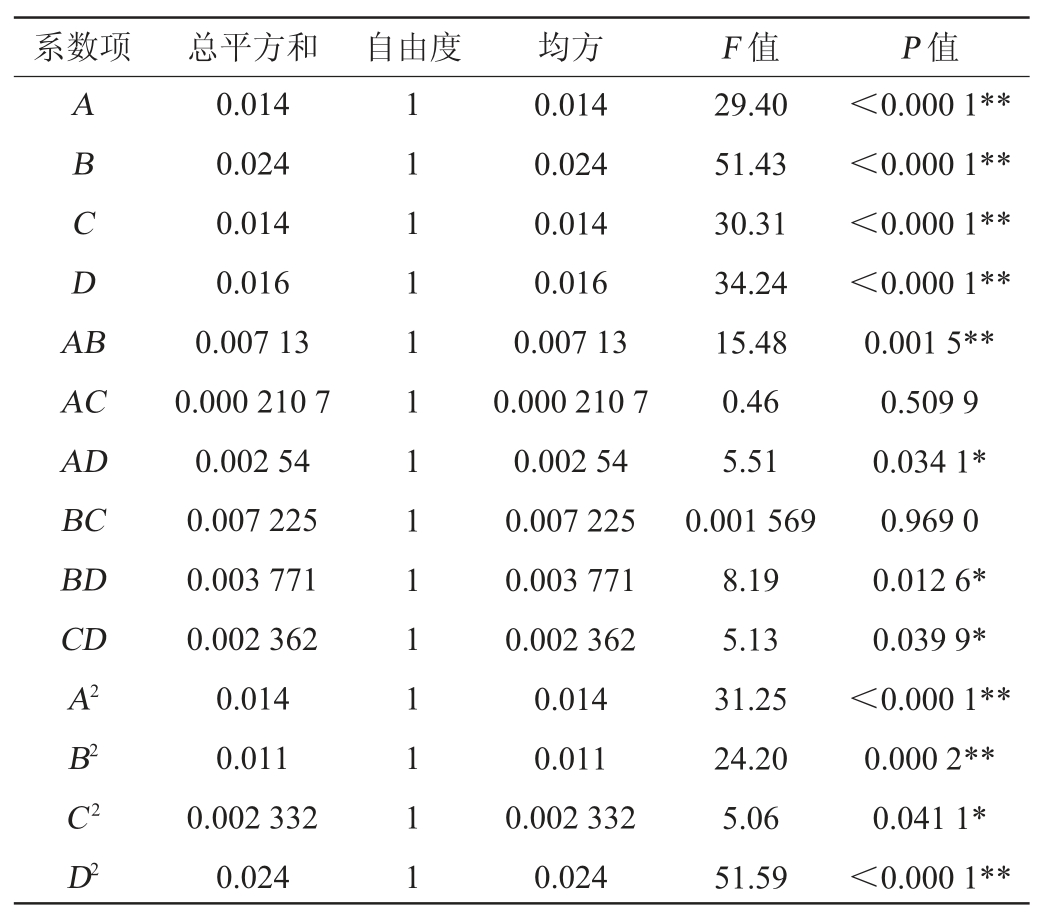
回归模型的显著性分析、失拟显著性分析以及回归系数显著性分析结果见表8。
表8 回归模型方差分析
Table 8 Variance analysis of regression model
续表
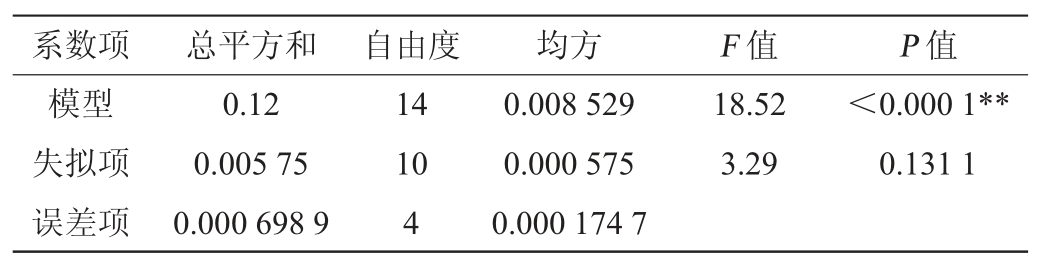
注:“*”表明该变量对响应值的影响显著(P<0.05),“**”表明该变量对响应值的影响极显著(P<0.01)。
由表8可知,回归模型P值<0.01,表明该模型极显著。失拟项P值=0.131 1>0.1,表明该模型拟和良好,即本试验的优化结果具有意义。决定系数R2=0.948 1>0.9,表明该模型数据可靠,试验误差性较小。由P值可知,该模型一次项A、B、C、D,交互项AB,二次项A2、B2、D2对结果影响极显著(P<0.01),交互项AD、BD、CD,二次项C2对结果影响显著(P<0.05)。因此,该模型可用于谷糠乳杆菌84-M-Y-7培养基配方的优化。
2.3.3 响应面分析
通过Design-Expert 8.0.6绘制大豆蛋白胨、豆粕粉、乳糖和维生素B2之间交互作用对菌体量影响的响应面曲线图和等高线,直观地反映出每两组因素之间的交互作用,结果见图2。由图2可知,AB、AD、BD、CD的等高线图呈现椭圆形,表明AB、AD、BD、CD交互作用对谷糠乳杆菌84-M-Y-7的生长影响显著(P<0.05),与方差分析结果一致。

图2 大豆蛋白胨、豆粕粉、乳糖和维生素B2交互作用对谷糠乳杆菌菌体量影响的响应面和等高线
Fig.2 Response surface plots and contour lines of effects of interaction between soybean peptone,soybean meal,lactose and vitamin B2 on the biomass of Lactobacillus farraginis
2.3.4 模型验证试验
根据响应面回归方程得到最佳发酵培养基配方各组分添加量分别为大豆蛋白胨3.02%,豆粕粉1.48%,乳糖3.13%,维生素B20.061%,在此配方下,谷糠乳杆菌84-M-Y-7的OD600nm值理论预测值为2.164。为便于实际操作,将最佳发酵培养基各组分添加量修正为大豆蛋白胨3%,豆粕粉1.5%,乳糖3%,维生素B2 0.06%,在此条件下进行验证试验,测得OD600nm值实际值为2.16,结果在允许误差范围内,证明了回归模型的有效性,以及基于响应面法优化获得的培养基条件参数准确、可靠,具有实用价值。
2.4 谷糠乳杆菌84-M-Y-7培养条件优化
微生物的培养条件也会因菌株个体差异而产生变化。合适的培养条件主要包括对发酵温度、发酵时间、接种量及培养基pH等的调控[24]。在本研究中,结合培养基配方优化结果和实验室前期试验结果,选择发酵时间(A)、发酵温度(B)和接种量(C)3个因素为评价因素,以菌体量为评价指标,进行3因素3水平的L9(33)正交试验,确定谷糠乳杆菌84-M-Y-7的最优培养条件,正交试验结果见表9。
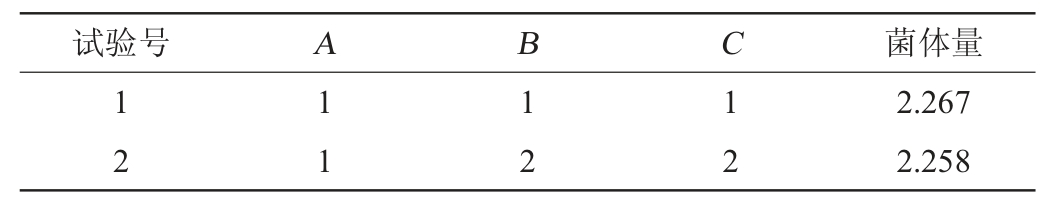
表9 谷糠乳杆菌培养条件优化正交试验结果与分析
Table 9 Results and analysis of orthogonal experiments for Lactobacillus farraginis culture conditions optimization
续表
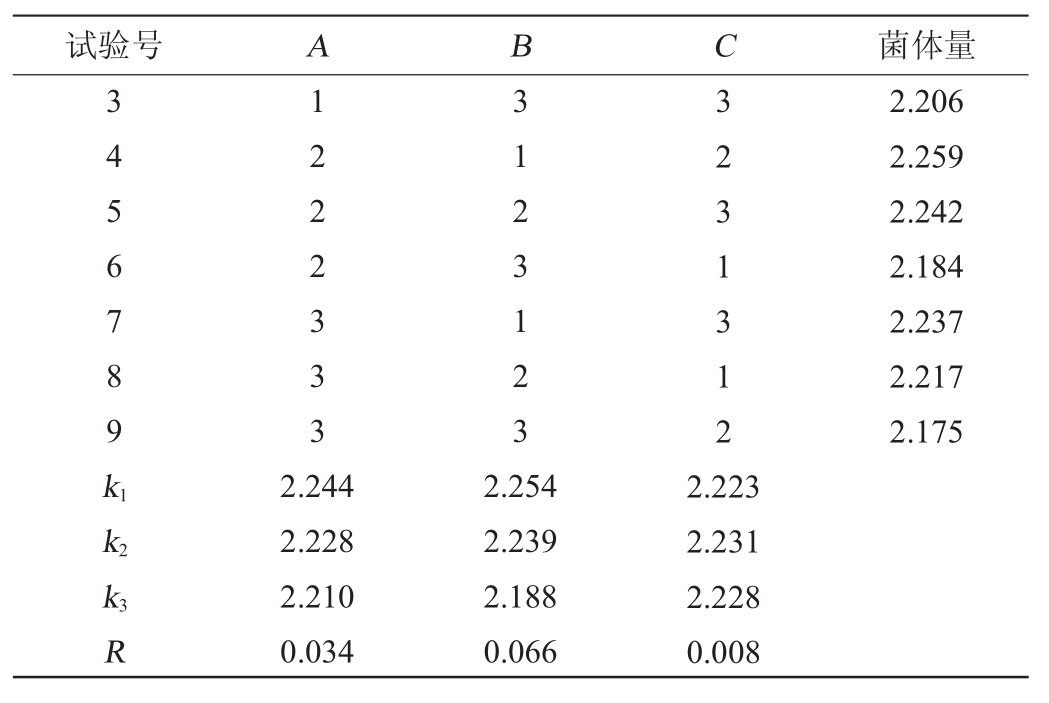
由表9可知,3个因素对谷糠乳杆菌84-M-Y-7的生长情况的影响程度排序为B>A>C,即发酵温度>发酵时间>接种量。极差分析结果表明,谷糠乳杆菌84-M-Y-7的最优培养条件为A1B1C2,即发酵时间24 h,发酵温度35 ℃,接种量10%,谷糠乳杆菌84-M-Y-7的生长情况最好。根据直观分析结果表明,最佳配方为A1B1C1。为获得最佳培养条件,两个配方均进行摇瓶试验,验证试验结果表明,A1B1C2条件下,OD600nm值(2.275)最高,即谷糠乳杆菌84-M-Y-7的最优培养条件为发酵时间24 h,发酵温度35 ℃,接种量10%。
2.5 菌体收集条件优化
离心转速和时间决定菌体收集的效率和菌体的存活率[25]。为了获得更高的湿菌质量及活菌数,考察了不同离心转速和离心时间对菌体存活率的影响,结果见图3。由图3a~3b可知,随着离心转速的增加,湿菌质量逐渐增加,然后趋于平缓,活菌数一直呈下降趋势。当离心转速到达4 000 r/min时,湿菌质量为0.01 g/mL,活菌数达到1.27×107 CFU/mL。故选择4 000 r/min作为最优离心转速。由图3c~3d可知,在最优离心转速(4 000 r/min)条件下,随着离心时间的增加,湿菌质量呈先增加后下降的趋势,而活菌数逐渐下降,然后趋于平缓。当离心时间为15 min时,湿菌质量为0.012 g/mL,活菌数为1.05×107 CFU/mL,与之后时间的数值之间无显著性差异(P>0.05)。因此,选择15 min为最优离心时间。
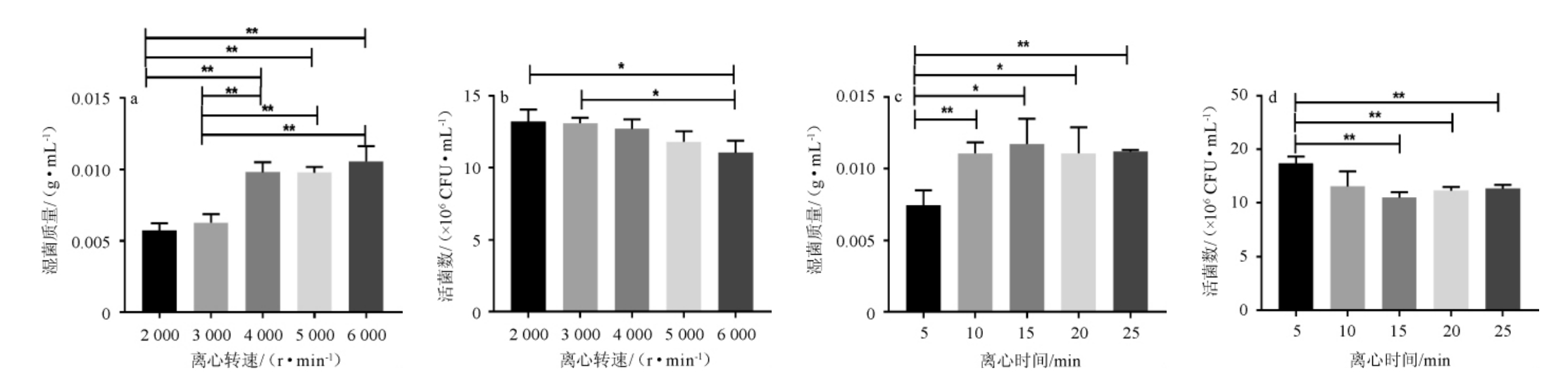
图3 不同离心转速(a,b)和时间(c,d)对谷糠乳杆菌菌体湿菌质量及活菌数的影响
Fig.3 Effects of different centrifugation rotational speed (a,b) and time (c,d) on the wet mass and viable count of Lactobacillus farraginis cells
“*”表示两者之间差异显著(P<0.05);“**”表示两者之间差异极显著(P<0.01)。
3 结论
为提高谷糠乳杆菌84-M-Y-7的产量,本研究以菌体量为评价指标,对其发酵培养基配方及培养条件进行优化,同时以湿菌质量及活菌数为评价指标,得到谷糠乳杆菌84-M-Y-7最佳菌体收集条件。结果表明,谷糠乳杆菌84-M-Y-7最佳培养基配方为大豆蛋白胨3%、豆粕粉1.5%、乳糖3%、维生素B2 0.06%,在此培养基配方下,谷糠乳杆菌84-M-Y-7的菌体量比优化前提高了1.9倍;菌株最适培养条件为:接种量8%、发酵温度35 ℃、发酵时间24 h,在此培养条件下,谷糠乳杆菌84-M-Y-7的菌体密度比优化前提高了2.3倍。最佳菌体收集条件为:4 000 r/min离心15 min,在此条件下,湿菌质量为0.012 g/mL,活菌数为1.05×107CFU/mL。该研究为谷糠乳杆菌84-M-Y-7的产业化开发提供技术支撑。
[1]田良玉.乳酸菌高密度规模发酵工艺优化[D].扬州:扬州大学,2018.
[2]关倩倩,熊涛,谢明勇.植物基食品乳酸菌发酵技术研究进展[J].食品与生物技术学报,2022,41(7):1-11.
[3]段永兰.益生菌在食品中的应用研究进展[J].食品安全导刊,2022(10):125-127.
[4]安江,刘敬科,生庆海,等.乳酸菌发酵杂粮面包品质改善和降糖机理研究进展[J].食品工业科技,2022,43(24):1-10.
[5]陈梓琦,汪彩云,李紫宁,等.乳酸菌的生长特性及其功能性质与应用综述[J].农产品加工,2020(12):80-83.
[6] LIM S M.Antimutagenicity activity of the putative probiotic strain Lactobacillus paracasei subsp.Tolerans JG22 isolated from pepper leaves Jangajji[J].Food Sci Biotechnol,2014,23(1):141-150.
[7]QIN X S,GAO Q Y,LUO Z G.Enhancing the storage and gastrointestinal passage viability of probiotic powder (Lactobacillus plantarum) through encapsulation with pickering high internal phase emulsions stabili zed with WPI-EGCG covalent conjugate nanoparticles[J].Food Hydrocolloid,2021,116:106658.
[8]赖长龙,曹余,杨玉,等.植物乳杆菌发酵动力学及高密度培养研究[J].食品与发酵工业,2022,48(20):137-144.
[9]吴军林,柏建玲,莫树平,等.乳酸菌R8高密度培养的发酵工艺研究[J].现代食品科技,2018,34(2):164-170,251.
[10]张艳丽.乳酸菌的高密度培养及菌剂的制备和应用[D].杭州:浙江工业大学,2016.
[11]RABIYA R,SEN R.Artificial intelligence driven advanced optimization strategy vis-à-vis response surface optimization of production medium:Bacterial exopolysaccharide production as a case-study[J].Biochem Eng J,2022,178:108271.
[12]赵云姣.鼠李糖乳杆菌高密度培养及干燥保存工艺研究[D].邯郸:河北工程大学,2018.
[13]李娜,杨江华,韦宇拓.植物乳杆菌ZJ316高密度发酵条件优化[J].中国酿造,2021,40(5):43-48.
[14]AlI M,SOLTANIAN S,MIRGHAED A T,et al.The potential benefits of Lactobacillus farraginis and Enterococcus durans,isolated from kefir,as probiotic candidates on innate immune responses,expression of some immune genes,and resistance to Lactococcosis disease in juvenile rainbow trout[J].Aquac Res,2021,53:4588-4604.
[15]COSTA D M,CARVALHO B F,BERNARDES T F,et al.New epiphytic strains of lactic acid bacteria improve the conservation of corn silage harvested at late maturity[J].Anim Feed Sci Tech,2021,274:114852.
[16]AKIHITO E,SANAE O.Lactobacillus farraginis sp.nov.and Lactobacillus parafarraginis sp.nov.,heterofermentative lactobacilli isolated from a compost of distilled shochu residue[J].Int J Syst Evol Micr,2007,57:708-712.
[17]BARTKIENE E,BARTKEVICS V,LELE V,et al.Application of antifungal lactobacilli in combination with coatings based on apple processing by-products as a bio-preservative in wheat bread production[J].J Food Sci Technol,2019,56:2989-3000.
[18]于立娟.植物乳杆菌高密度发酵及益生菌片的研制[D].北京:北京农学院,2014.
[19]李娜.植物乳杆菌ZJ316的高密度发酵及高活性菌制剂的初步研究[D].南宁:广西大学,2020.
[20]闫鹏.嗜酸乳杆菌高密度培养及工艺的研究[D].广州:华南理工大学,2011.
[21]KLOPPER K B,BESTER E,DEANE S M,et al.Survival of planktonic and sessile cells of Lactobacillus rhamnosus and Lactobacillus reuteri upon exposure to simulated fasting-state gastrointestinal conditions[J].Probiotics Antimicro,2019,11(2):594-603.
[22]李盼盼,张庆芳,刘春莹,等.鼠李糖乳杆菌LP216高密度发酵培养基优化[J].中国酿造,2022,41(4):87-92.
[23]ALLAM M G M,DARWISH A M G,AYAD E H E,et al. In vivo evaluation of safety and probiotic traits of isolated Enterococcus feacium strain KT712[J].Res J Microbiol,2016,11(6):169-177.
[24]李玉娥,马玲.乳酸菌高密度培养条件优化研究[J].中国酿造,2021,40(9):150-154.
[25]黄莹莹,邢月婷,孟晓瑜,等.离心参数对流式分选后样本的影响研究[J].中国细胞生物学学报,2021,43(10):2001-2008.