褐藻胶是褐藻重要的结构成分,作为细胞壁及细胞间质的填充物质,占褐藻干质量的40%左右[1-3]。褐藻胶寡糖是褐藻胶降解后形成的聚合度在2~20的低分子物质,在医药、食品、日化、饲料和农业方面有广泛的应用[4-6]。
降解褐藻胶的方法主要有物理法、化学法和酶解法。酶解法具有底物专一、反应条件温和等优点,可以定向制备褐藻胶寡糖,相较于物理、化学法是一种理想且环保的方法[7-9]。褐藻胶裂解酶通过β消除机制断裂褐藻胶分子间的1,4-糖苷键催化褐藻胶降解,并在非还原端形成不饱和双键,该双键在波长235 nm处具有强烈吸收峰[10-12]。褐藻胶裂解酶不仅可以降解褐藻胶、定向制备褐藻胶寡糖,而且可以制备海藻原生质体、发酵生产乙醇、降解生物膜等,可应用于食品、农业、制药及能源等方面[13-15]。海洋细菌是获取褐藻胶裂解酶的重要途径,如假单胞菌(Pseudomonas sp.)QD03[16]、固氮菌(Azotobacter vinelandii)[17]、黄杆菌(Flavobacterium sp.)LXA[18]、交替假单胞菌(Pseudoalteromonas sp.)CY24[19]、鞘氨醇单胞菌(Sphingomonas sp.)A1[20]、弧菌(Vibrio sp.)QY102等。本课题组从海南省琼海市海域采集到的腐烂马尾藻中分离出菌株HB161653,经分子鉴定可能为弧菌属(Vibrio sp.)新的分类单元,且具有较好的产褐藻胶裂解酶活性。本研究对该菌产褐藻胶裂解酶的培养基及发酵条件进行优化,以期为褐藻胶裂解酶的规模化生产奠定基础。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种
弧菌(Vibrio sp.HB161653):由本实验室保存。
1.1.2 培养基
活化培养基(2216E琼脂培养基)、种子培养基(2216E液体培养基):青岛海博生物科技有限公司。
初始发酵培养基[21]:海藻酸钠5 g/L,蛋白胨5 g/L,NaCl 20 g/L,K2HPO4 1 g/L,MgSO4 0.5 g/L,pH值为7.0±0.2。
1.1.3 试剂
可溶性淀粉、蔗糖、葡萄糖(均为分析纯)、蛋白胨、酵母粉(均为生化试剂):生工生物工程(上海)股份有限公司;海藻酸钠(分析纯):天津大茂化学试剂厂;尿素、硫酸铵、NaCl、K2HPO4、MgSO4(均分析纯):西陇科学股份有限公司。
1.2 仪器与设备
DK-8AD型电热恒温水槽、GHP-9080型隔水式恒温培养箱:上海一恒科技有限公司;UV-1600型可见分光光度计:上海美普达仪器有限公司;SW-CJ-1FD型超净工作台:苏州安泰空气技术有限公司。
1.3 方法
1.3.1 种子液制备
将保存的弧菌HB161653划线于活化培养基,28 ℃条件下静置培养24 h。从活化平板上挑取单菌落接种于50 mL种子培养基,28℃、180r/min条件下振荡培养24h,制得种子液。
1.3.2 产褐藻胶裂解酶培养基优化
固定初始发酵条件为接种量1.0%、装液量50mL/250mL,28 ℃、180 r/min振荡培养14 h,10 000 r/min、4 ℃离心10 min收集上清液。以褐藻胶裂解酶活力为考察指标,分别考察碳源(添加量均为5 g/L可溶性淀粉、蔗糖、葡萄糖、海藻酸钠)、最佳碳源添加量(2.5 g/L、5.0 g/L、7.5 g/L、10.0 g/L、12.5 g/L),氮源(添加量均为5 g/L蛋白胨、酵母粉、尿素、硫酸铵)、最佳氮源添加量(2.5 g/L、5.0 g/L、7.5 g/L、10.0 g/L、12.5 g/L),NaCl添加量(10 g/L、15 g/L、20 g/L、25 g/L、30 g/L)、K2HPO4添加量(0.05 g/L、0.10 g/L、0.15 g/L、0.20 g/L、0.25 g/L)和MgSO4添加量(0.10 g/L、0.15 g/L、0.20 g/L、0.25g/L、0.30 g/L)对弧菌HB161653产酶的影响。
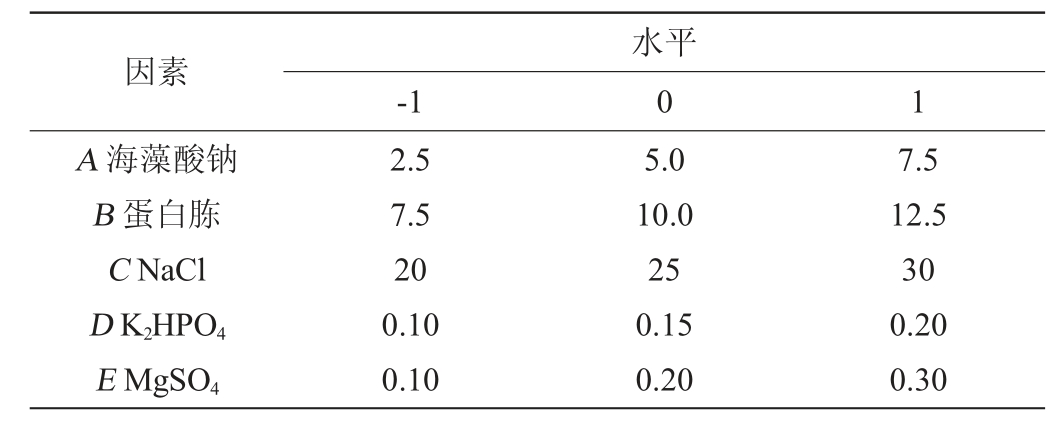
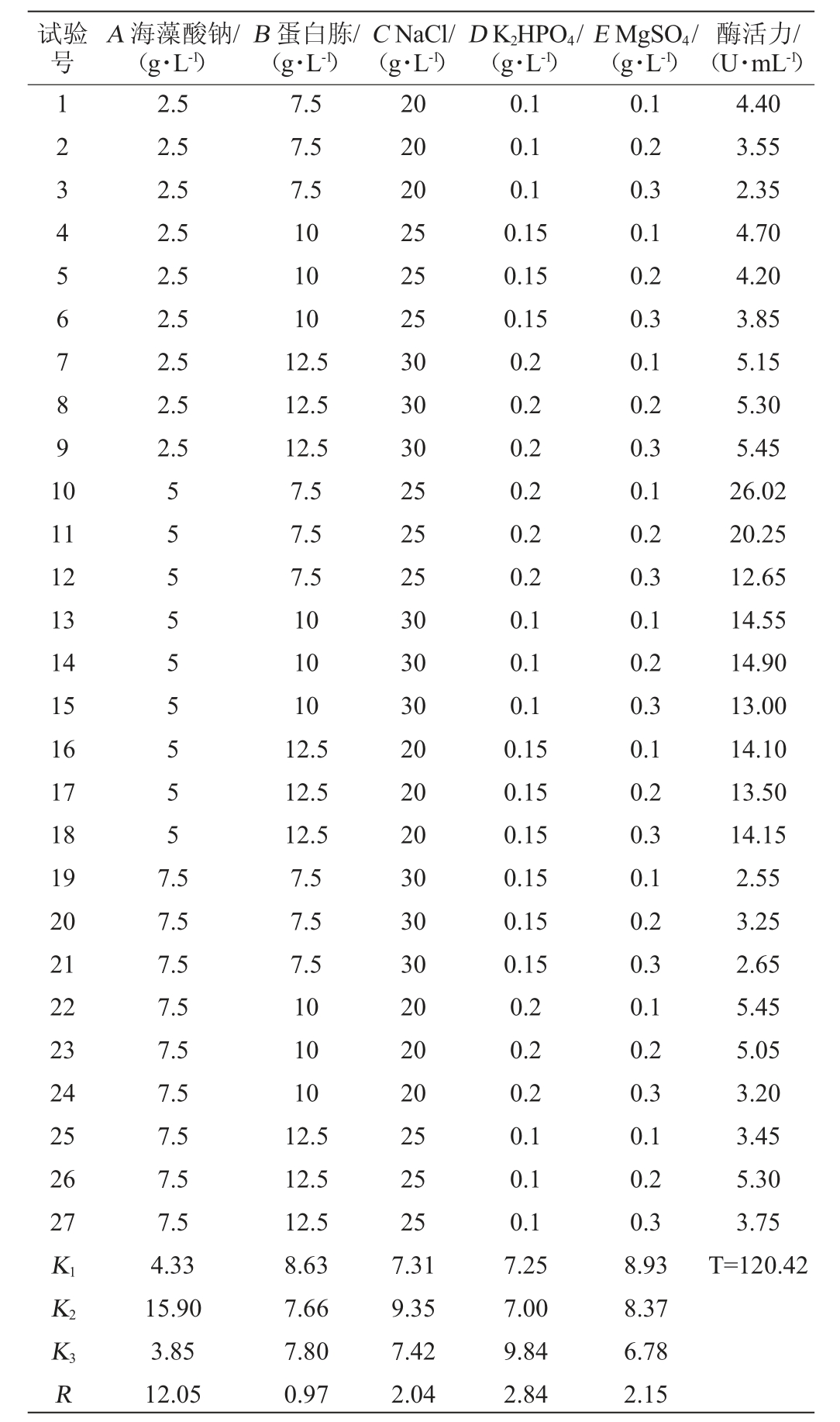
在单因素试验的基础上,进一步以海藻酸钠(A)、蛋白胨(B)、NaCl(C)、K2HPO4(D)和MgSO4(E)添加量为考察因素,设计L27(35)正交试验,正交试验因素与水平如表1所示。
表1 弧菌HB161653产褐藻胶裂解酶培养基组成优化正交试验因素与水平
Table 1 Factors and levels of orthogonal experiments for optimization of alginate lyase production medium composition of Vibrio sp.HB161653 g/L
1.3.3 产褐藻胶裂解酶培养发酵条件优化
在优化产酶培养基基础上分别考察培养基初始pH(5.0、6.0、7.0、8.0、9.0)、接种量(0.5%、1.0%、1.5%、2.0%、2.5%)、发酵温度(22 ℃、25 ℃、28 ℃、31 ℃、34 ℃)对弧菌HB161653产酶的影响。
1.3.4 发酵产酶周期的测定
在优化培养基组成和培养条件下进行发酵,定期取样测定褐藻胶裂解酶活力和发酵液菌体生物量。以发酵时间为横坐标,以褐藻胶裂解酶活力、菌体生物量为纵坐标,确定弧菌HB161653的发酵周期。
1.3.5 测定方法
生物量测定:采用分光光度法,细菌生物量以波长600 nm处的吸光度值表示。
褐藻胶裂解酶活性测定:采用紫外吸收法[22]。取1.8 mL底物(3.0 g海藻酸钠溶于1 L 50 mmol/L磷酸盐缓冲液(pH 7.0)),40 ℃预热5 min,加入0.2 mL待测样品于40 ℃温浴10 min,以灭活酶液为对照,测定反应体系在波长235 nm处的紫外吸收值。在上述酶活性测定方法下,波长235 nm处紫外吸收值每分钟增加0.1的酶量为酶的一个活力单位,U。试验中将最高的酶活性定义为100%,其余条件下的酶活力与最高酶活的比值为相对酶活。
2 结果与分析
2.1 弧菌HB161653产褐藻胶裂解酶培养基组成优化单因素试验
2.1.1 不同的碳源及最适碳源添加量对弧菌HB161653产酶的影响
由图1可知,以葡萄糖、可溶性淀粉和蔗糖为唯一碳源时菌株产酶能力较弱,以海藻酸钠为唯一碳源时酶活最高。因此,选择海藻酸钠作为弧菌HB161653生长的唯一碳源。
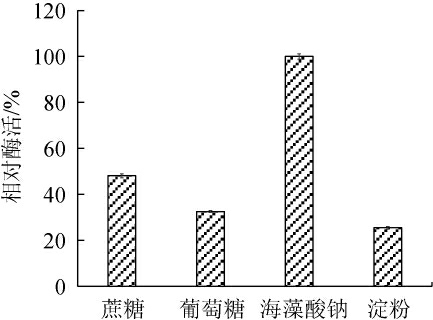
图1 不同碳源对弧菌HB161653产酶的影响
Fig.1 Effect of different carbon sources on enzyme production by Vibrio sp.HB161653
由图2可知,海藻酸钠添加量较低时酶活随着海藻酸钠含量增加而提高,当海藻酸钠添加量为5 g/L时,菌株产酶能力最强;继续增加海藻酸钠添加量,菌株的产酶能力出现下降趋势。这可能是由于海藻酸钠添加量较低时,不能满足菌体正常生长代谢所需导致产酶能力较低;添加量较大时发酵液黏度高,不利于氧气融合和细胞生长。因此,选择发酵培养基的海藻酸钠添加量为5 g/L。
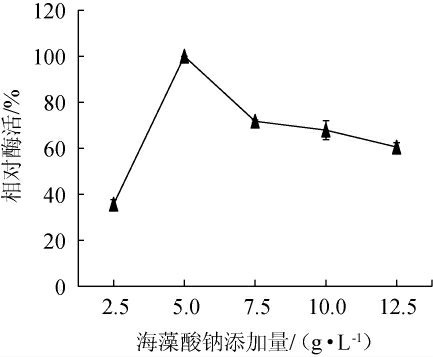
图2 不同海藻酸钠添加量对弧菌HB161653产酶的影响
Fig.2 Effect of different sodium alginate addition on enzyme production by Vibrio sp.HB161653
2.1.2 不同的氮源及最适氮源添加量对弧菌HB161653产酶的影响
由图3可知,几种氮源都可以被菌株HB161653利用,以蛋白胨作为唯一氮源时,菌株的产酶能力最强,酵母粉、硫酸铵次之,尿素最差。因此,选择蛋白胨作为弧菌HB161653生长的唯一氮源。
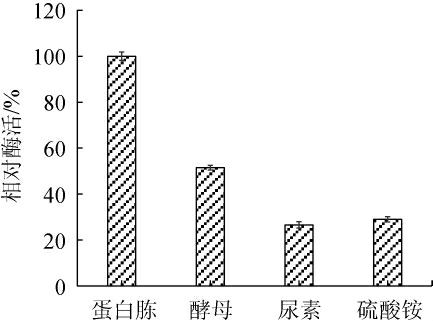
图3 不同的氮源对弧菌HB161653产酶的影响
Fig.3 Effect of different nitrogen sources on enzyme production by Vibrio sp.HB161653
由图4可知,菌株的产酶能力随着蛋白胨添加量的增加而增加,当蛋白胨添加量为10 g/L时达到最大值,之后出现下降趋势,蛋白胨添加量过高或太低时都会影响褐藻胶裂解酶的积累。这可能是由于蛋白胨添加量较低时,不能满足菌体正常生长代谢所需;含量较高时也不利于产酶。因此,选择蛋白胨最佳添加量为10 g/L。
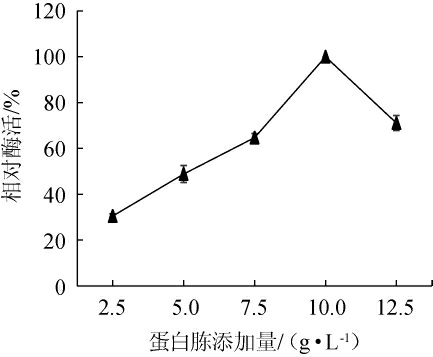
图4 不同蛋白胨添加量对弧菌HB161653产酶的影响
Fig.4 Effect of different peptone addition on enzyme production by Vibrio sp.HB161653
2.1.3 金属离子对弧菌HB161653产酶的影响
由图5可知,当NaCl添加量为25 g/L时产酶量达到最大值,这与海洋中的盐浓度较为接近。当NaCl添加量<25 g/L时,产酶能力呈上升趋势,当NaCl添加量>25 g/L时产酶能力逐渐下降。因此,选择最佳NaCl添加量为25 g/L。
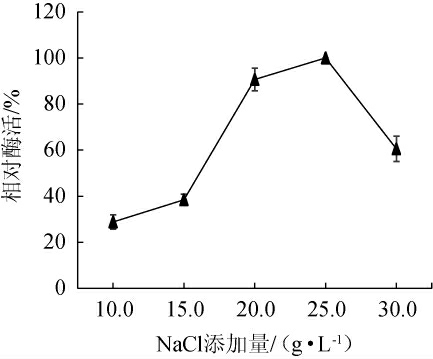
图5 不同NaCl添加量对弧菌HB161653产酶影响
Fig.5 Effect of different NaCl addition on enzyme production by Vibrio sp.HB161653
研究表明,K2HPO4、MgSO4对菌株产酶有促进作用[23]。因而,进一步考察K2HPO4添加量和MgSO4添加量对菌株产酶的影响。由图6可知,当K2HPO4添加量达到0.2 g/L时菌株的产酶能力最强,当K2HPO4添加量>0.2 g/L时,该菌的产酶能力呈逐渐下降趋势;当MgSO4添加量达到0.15 g/L时该菌株的产酶能力最强,当MgSO4添加量>0.15 g/L时,该菌的产酶能力呈逐渐下降趋势。因此,最佳K2HPO4及MgSO4添加量分别为0.2 g/L、0.15 g/L。
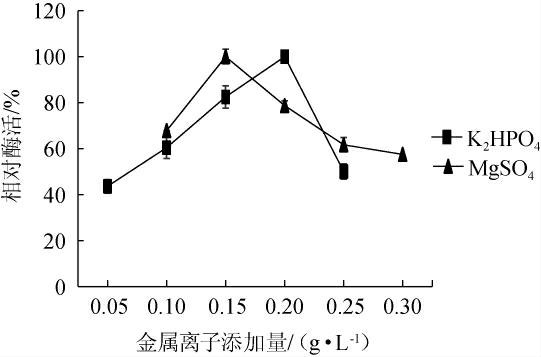
图6 不同K2HPO4、MgSO4添加量对弧菌HB161653产酶影响
Fig.6 Effect of different K2HPO4 and MgSO4 addition on enzyme production by Vibrio sp.HB161653
2.2 弧菌HB161653产褐藻胶裂解酶培养基组成优化正交试验
由表2可以看出,各因素对菌株产酶的影响大小为海藻酸钠>K2HPO4>MgSO4>NaCl>蛋白胨添加量,菌株HB161653产褐藻胶裂解酶的最适组合为A2B1C2D3E1,即发酵培养基组成为海藻酸钠5 g/L、蛋白胨7.5 g/L、NaCl 25 g/L、K2HPO40.2 g/L、MgSO40.1 g/L。在此条件下测得的酶活力为26.02 U/mL。
表2 弧菌HB161653产褐藻胶裂解酶培养基组成优化正交试验结果与分析
Table 2 Results and analysis of orthogonal experiments for optimization of alginate lyase production medium composition of Vibrio sp.HB161653
2.3 弧菌HB161653产褐藻胶裂解酶发酵条件优化
2.3.1 接种量对弧菌HB161653产酶的影响
由图7可知,弧菌HB161653的产酶能力随着接种量的增加而增加,当接种量为1.5%时褐藻胶裂解酶活力最高。接种量超过1.5%,褐藻胶裂解酶活力逐渐下降,可能是由于菌株此时大量繁殖,培养基中营养物质被大量消耗,导致菌株的产酶量下降。因此,确定最佳接种量为1.5%。
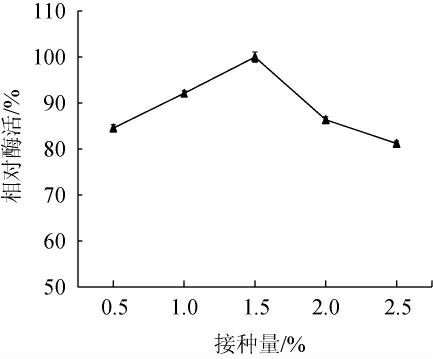
图7 接种量对弧菌HB161653产酶的影响
Fig.7 Effect of inoculum on enzyme production by Vibrio sp.HB161653
2.3.2 培养基初始pH值对弧菌HB161653产酶的影响
pH值影响着细胞膜的稳定性,进而影响细菌的产酶能力[24]。由图8可知,培养基初始pH值为5.0~9.0时,酶活先升高后降低。当培养基初始pH值为7.0时,酶活最高,中性的环境有利于该弧菌产褐藻胶裂解酶。因此,确定最佳培养基初始pH值为7.0。
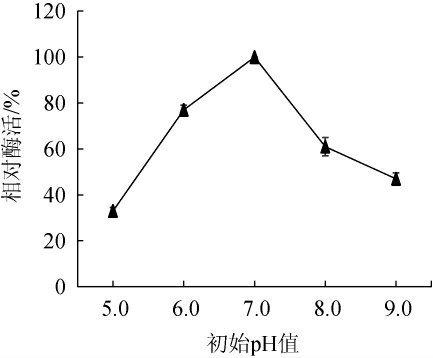
图8 培养基初始pH值对弧菌HB161653产酶的影响
Fig.8 Effect of medium initial pH on enzyme production by Vibrio sp.HB161653
2.3.3 发酵温度对弧菌HB161653产酶的影响
温度对细菌产褐藻胶裂解酶的能力起至关重要的作用,在合适的温度下才能保证菌株产酶的顺利进行[25-26]。由图9可知,发酵温度为28 ℃时产酶最高,发酵温度高于28 ℃时,酶活出现大幅度下降。因此,确定最佳发酵温度为28 ℃。
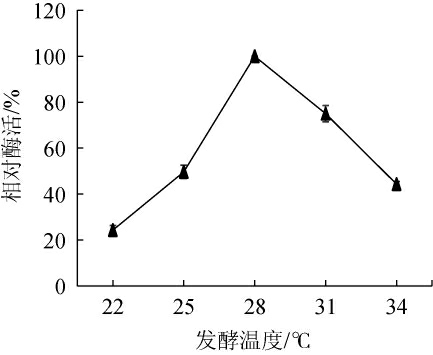
图9 发酵温度对弧菌HB161653产酶的影响
Fig.9 Effect of fermentation temperature on enzyme production by Vibrio sp.HB161653
2.3.4 弧菌HB161653生长及产酶曲线测定
由图10可知,在发酵初期(8~14 h),菌体处于对数生长期,消耗培养基中的营养成分进行生长繁殖,发酵时间为14 h时,菌体生物量达到最大值;发酵时间>14 h之后,菌体的生物量随着时间的延长逐渐下降。在发酵时间为8~12 h时,菌体的产酶能力随着发酵的进行呈快速上升趋势,在发酵时间为12 h时,褐藻胶裂解酶活力达到最高(42.1 U/mL),较优化前(26.0 U/mL)提高了62%。因此,最佳发酵时间为12 h。
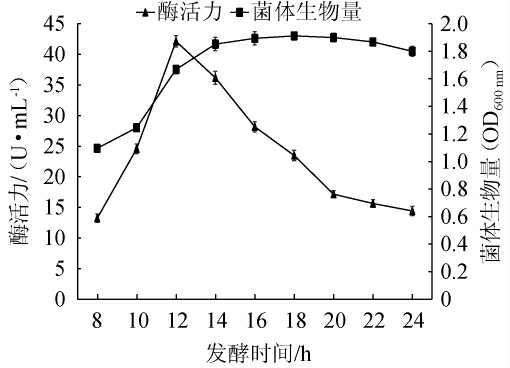
图10 弧菌HB161653的生长及产酶曲线
Fig.10 Growth and enzyme production curves of Vibrio sp.HB161653
3 结论
培养基为细菌的生长与繁殖提供必备的营养物质。本试验通过单因素和正交试验对弧菌HB161653的产酶条件进行优化。最佳产酶培养基组成为海藻酸钠5 g/L,蛋白胨7.5 g/L,NaCl 25 g/L,K2HPO4 0.2 g/L,MgSO4 0.1 g/L;最佳发酵条件为培养基初始pH 7.0,接种量1.5%,发酵温度28 ℃,发酵周期12 h。采用优化后的培养基和发酵条件进行产酶试验,褐藻胶裂解酶活力可达42.1 U/mL,较优化前(26.0 U/mL)提高了62%。本研究对产褐藻胶裂解酶弧菌HB161653的发酵培养基和工艺条件进行研究,以期为褐藻胶裂解酶的生产以及工业化应用提供理论依据。
[1]孟青,江波,周力铖,等.一株产褐藻胶裂解酶的需钠弧菌筛选及酶解产物分析[J].微生物学通报,2022,49(2):421-436.
[2] USOLTSEVA R V,ANASTYUK S D,SHEVCHENKO N M,et al.Polysaccharides from brown algae Sargassum duplicatum: the structure and anticancer activity in vitro[J].Carbohyd Polym,2017,11(1):547-556.
[3] ZHANG Y H,SHAO Y,JIAO C,et al.Characterization and application of an alginate lyase,aly1281 from marine bacterium Pseudoalteromonas carrageenovora ASY5[J].Mar Drugs,2020,18(2):95-111.
[4] MRUDULAKUMARI V U,LEE O K,LEE E Y.Alginate derived functional oligosaccharides: Recent developments,barriers,and future outlooks[J].Carbohyd Polym,2021,267:118158-118175.
[5]傅政,张凤超,李玉姣,等.褐藻胶寡糖生物活性研究进展[J].中国海洋药物,2020,39(5):65-74.
[6]吴哲,任丹丹,梁馨元,等.褐藻胶寡糖的制备分离及生物活性[J].食品安全质量检测学报,2020,11(1):1-7.
[7]阿拉腾珠拉,胡永飞.褐藻寡糖的制备方法及生物活性研究进展[J].生物工程学报,2022,38(1):104-118.
[8]赵婉琳,叶静,张娜,等.褐藻胶降解菌的筛选、鉴定及产酶条件优化[J].微生物学报,2019,59(1):169-180.
[9]吴阳,霍峥,李刚,等.褐藻胶裂解酶研究进展[J].食品工业,2021,42(7):261-266.
[10]汪梓旭,郑志国,鲍时翔,等.褐藻胶裂解酶酶学性质及酶解马尾藻工艺的响应面优化[J].中国酿造,2020,39(2):103-108.
[11]许超,卢明倩,张荣灿,等.响应面法优化海洋弧菌产褐藻胶裂解酶发酵培养基[J].中国酿造,2016,35(12):59-65.
[12]郑志国,黄惠琴,朱军,等.响应面法优化类芽胞杆菌HB172198产褐藻胶裂解酶发酵培养基[J].基因组学与应用生物学,2020,39(1):151-158.
[13]李倩,李悝悝,张付云.褐藻胶降解酶产生菌的筛选与鉴定[J].中国酿造,2019,38(5):63-66.
[14]孙家霞,王海楠,傅政,等.海洋细菌Thalassomonas sp.LD5中新型褐藻胶裂解酶TsAly7C的研究[J].中国海洋药物,2022,41(1):9-16.
[15]孟青.褐藻胶裂解酶产酶菌株挖掘及其催化特性研究[D].无锡:江南大学,2021.
[16]LIN X,FENG H,ZHAO Y,et al.A novel alginate lyase with high activity on acetylated alginate of Pseudomonas aeruginosa FRD1 from Pseudomonas sp.QD03[J].World J Microbiol Biotechnol,2006,22(1):81-88.
[17]GIMMESTAD M,ERTESVAG H,HEGGEST T M,et al.Characterization of three new Azotobacter vinelandii alginate lyases,one of which is involved in cyst germination[J].J Bacteriol,2009,191(15):4845-4853.
[18]AN Q D,ZHANG G L,WU H T,et al.Alginate-deriving oligosaccharide production by alginase from newly isolated Flavobacterium sp.LXA and its potential application in protection against pathogens[J].J Appl Microbiol,2009,106(1):161-170.
[19] DUAN G,HAN F,YU W.Cloning,sequence analysis,and expression of gene alyPI encoding an alginate lyase from marine bacterium Pseudoalteromonas sp.CY24[J].Can J Microbiol,2009,55(9):1113-1118.
[20]MIYAKE O,OCHIAI A,HASHIMOTO W,et al.Origin and diversity of alginate lyases of families PL-5 and-7 in Sphingomonas sp.strain A1[J].J Bacteriol,2004,86(9):2891-2896.
[21]汪梓旭.孤囊马尾藻多糖与寡糖制备工艺优化及其活性评价[D].海口:海南大学,2020.
[22]WANG Y,GUO E W,YU W G,et al.Purification and characterization of a new alginate lyase from a marine bacterium Vibrio sp.[J].Biotechnol Lett,2013,35(5):703-708.
[23]李双,王碧盈,鲍时翔,等.产褐藻胶裂解酶交替单胞菌的发酵优化及alg2951的外源表达[J].基因组学与应用生物学,2020,39(5):2088-2095.
[24]刘彩琴,王楠,陈薇青,等.一株明亮发光杆菌产褐藻胶裂解酶的培养基优化[J].食品工业科技,2017,38(8):156-160.
[25]周敏,冷凯良,王致鹏,等.产褐藻胶裂解酶菌株的筛选及发酵条件优化[J].青岛大学学报(自然科学版),2019,32(1):37-45.
[26]高王宇,黄惠琴,刘敏,等.产褐藻胶裂解酶菌株HB12274的鉴定和发酵优化[J].基因组学与应用生物学,2018,37(10):4365-4371.