谷物类食品是人类的重要食品来源之一,在人类的膳食结构中占有重要地位[1],此外,由于全谷物食品最大程度地保留了谷物中的营养与活性成分,在预防慢性病等多个领域的健康功效得到了充分验证,愈来愈受到消费者的认同和重视[2]。近年来,随着人们生活水平的提高,即食谷物类食品品种越来越多,为了增加产品的色泽,生产企业在生产过程中加入各种各样的色素,以吸引消费者[3-4]。红木素和降红木素是经不同提取溶剂从红木种子中提取得到的食用天然色素[5]。该类色素因其色泽光亮鲜艳、着色力强,受到食品生产企业的青睐[6],广泛应用到食品加工中。为了规范红木素和降红木素的合理使用,我国对该类色素的适用范围和限量进行了明确的规定[7]:用于干酪限量0.6 g/kg;人造奶油限量0.05 g/kg;糖果、果酱、饮料、果冻限量0.6 g/kg;糕点限量0.015 g/kg;肉灌肠类、西式火腿、巧克力限量0.025 g/kg;复合调味料限量0.1 g/kg;膨化食品、面糊、裹粉、煎炸粉限量0.01 g/kg;方便米面制品限量0.012 g/kg;即食谷物类食品限量0.07 g/kg;粉圆限量0.15 g/kg。
食品中关于合成色素的检测报道较多,但关于食用天然色素的检测研究较少[8-12]。目前,国外文献中有关食用天然色素红木素和降红木素的报道大多是从红木种子中提取该类色素的报道[13-15],有关食品中该类色素检测的探讨不多[16-17];国内文献中有关红木素和降红木素检测的基质大多是饮料、奶酪等[18-20],未见有即食谷物类食品中该类色素的检测;在检测标准方面,国内也只有一个进出口食品的检测标准[21]。因此,为了维护消费者权益、推动该天然色素的合理使用,建立即食谷物类食品中红木素和降红木素的快速检测方法显得迫切且必要。
此外,目前用于食品中红木素和降红木素的检测设备主要是液相色谱仪[22-23]、液相色谱串联质谱仪[24]。上述检测设备定性准确度方面尚有不足,不能准确阐明化合物的裂解信息,且对前处理的要求较高,操作繁复、耗时长,不适合样品的批量检测。超高效液相色谱-四级杆-飞行时间质谱(ultra performance liquid chromatography coupled with quadrupole-timeofflightmassspectrometry,UPLC-Q-TOF/MS)仪具有抗干扰能力更强、定性准确度更高的特点[25],如可以在满足化合物检出限的前提下,简化样品前处理操作步骤,则可以大幅提高工作效率。以即食谷物食品为基质,以期建立即食谷物类食品中红木素和降红木素的超高效液相色谱-四级杆-飞行时间质谱检测方法,能准确、简单、快速应用于批量样品的检测。
1 材料与方法
1.1 材料与试剂
即食谷物类食品(饼干、麦片、玉米片、核桃粉、芝麻糊等):市售。
红木素标准物质(CAS号6983-79-5)、降红木素标准物质(CAS号542-40-5)(纯度均≥98%):美国ChromaDex公司;乙腈、甲酸、乙酸铵(色谱纯):美国Tedia公司;实验用水为美国Millipore纯水系统制得的超纯水。
1.2 仪器与设备
1290-6530型超高效液相色谱-四级杆-飞行时间质谱仪(UPLC-Q-TOF MS):美国安捷伦公司;CR22GⅢ日立高速冷冻离心机:日本HITACHI公司;ULTRA-TURRAX T25型均质器、GENIUS 3涡旋混匀器、HS260型多用调速振荡器:德国IKA公司。
1.3 试验方法
1.3.1 标准溶液配制
标准储备液:准确称取相当于50 mg目标待测物的标准品分别于50 mL烧杯中,用甲醇溶解并定量转移至25 mL容量瓶中,用甲醇定容至刻度,配制质量浓度为2 mg/mL的标准储备液,4 ℃避光保存。
标准工作液:实验过程中依据不同待测分析物的定量限,用样品制得的空白提取液逐级稀释标准储备溶液,配制成不同浓度的系列基质标准混合工作液,现用现配。
1.3.2 样品前处理
样品预先打碎混合均匀备用。精确称取2.00 g样品,置于50 mL具塞离心管中,加入10 mL 5%醋酸-乙腈溶液,均质提取1 min,然后置于水平振荡器上振荡30 min,以9 000 r/min冷冻(-2 ℃)离心5 min,取上清液过0.22 μm滤膜,滤液待测。
1.3.3 仪器工作条件
液相色谱条件:ZORBAXSB-C18色谱柱(100mm×2.1mm,3.5 μm);流动相A为乙腈,B为0.1%甲酸水溶液(含5 mmol/L乙酸铵),梯度洗脱程序:0~0.5 min,95%A;0.5~5 min,95%~60%A;5~9 min,60%~5%A;9~14 min,5%A;14~14.1 min,5%~95%A;14.1~18 min;95%A;流速0.3 mL/min;柱温35 ℃;进样量10 μL。
质谱条件:电喷雾离子(electrospray ionization,ESI)源,正离子模式;雾化气压力45 psi;干燥气温度300 ℃;干燥气流速12 L/min;鞘气温度300 ℃;鞘气流速12 L/min;毛细管电压4 500 V;喷嘴电压1 000 V;传输电压110 V;除液电压65 V;扫描范围为50~1 700 m/z,扫描速率为3 spectra/s;数据采集与数据处理(定性分析和定量分析)均采用设备自带软件(version B.04.00)。
1.3.4 数据库的建立
数据谱库一般包括化合物名称、分子式、理论相对分子质量、离子化形式、保留时间、子离子扫描图等信息,化合物名称、分子式、理论相对分子质量可从标准物质证书上获得,离子化形式、保留时间、子离子扫描图均从实验获得。上述实验中已经确定待测分析物的离子化形式为[M+H]+。
保留时间的确定:在上述确定的色谱质谱条件下,配制质量浓度为1 mg/L的标准溶液,进行全扫描并采集数据,依据待测分析物的分子式及理论相对分子质量,确认其色谱峰,进而获得其色谱保留时间。
子离子扫描图的获得:子离子扫描模式下,在Targeted MS/MS界面输入待测物的保留时间,母离子和不同的碰撞能量并采集数据,获得不同碰撞能量下的子离子扫描质谱图,选取碎片离子信息丰富且碎片离子突出的质谱图作为子离子扫描图,与对应的待测物信息相关联并保存。
2 结果与分析
2.1 色谱条件的优化
实验比较了乙腈-水、乙腈-0.1%甲酸水溶液、乙腈-5 mmol/L乙酸铵溶液、乙腈-0.1%甲酸水溶液(含5 mmol/L乙酸铵)四种不同流动相体系下红木素和降红木素的出峰情况,其离子流色谱图见图1。结果表明,红木素和降红木素在酸性体系下的响应高于非酸性体系下的响应,而且峰形也好;体系中加入乙酸铵后目标化合物间及目标化合物与杂峰间的分离度也有所改善,因此,最终选择乙腈-0.1%甲酸水溶液(含5 mmol/L乙酸铵)作为实验用流动相。

图1 红木素(A)及降红木素(B)的总离子流色谱图
Fig. 1 Total ions chromatograms of bixin (A) and norbixin (B)
2.2 质谱条件的优化
实验比较了正、负离子全扫描模式,结果表明,红木素和降红木素在负模式下没有响应,只有在正离子模式下有响应,因而实验采用正离子模式进行扫描。
正离子模式下,目标分析物红木素和降红木素有[M+H]+、[M+Na]+两种离子化形式,且两种化合物[M+H]+离子化形式的响应均高于[M+Na]+离子化的响应,结果见图2。因此实验最终选择[M+H]+离子化形式作为目标化合物的母离子,并用于数据库检索。
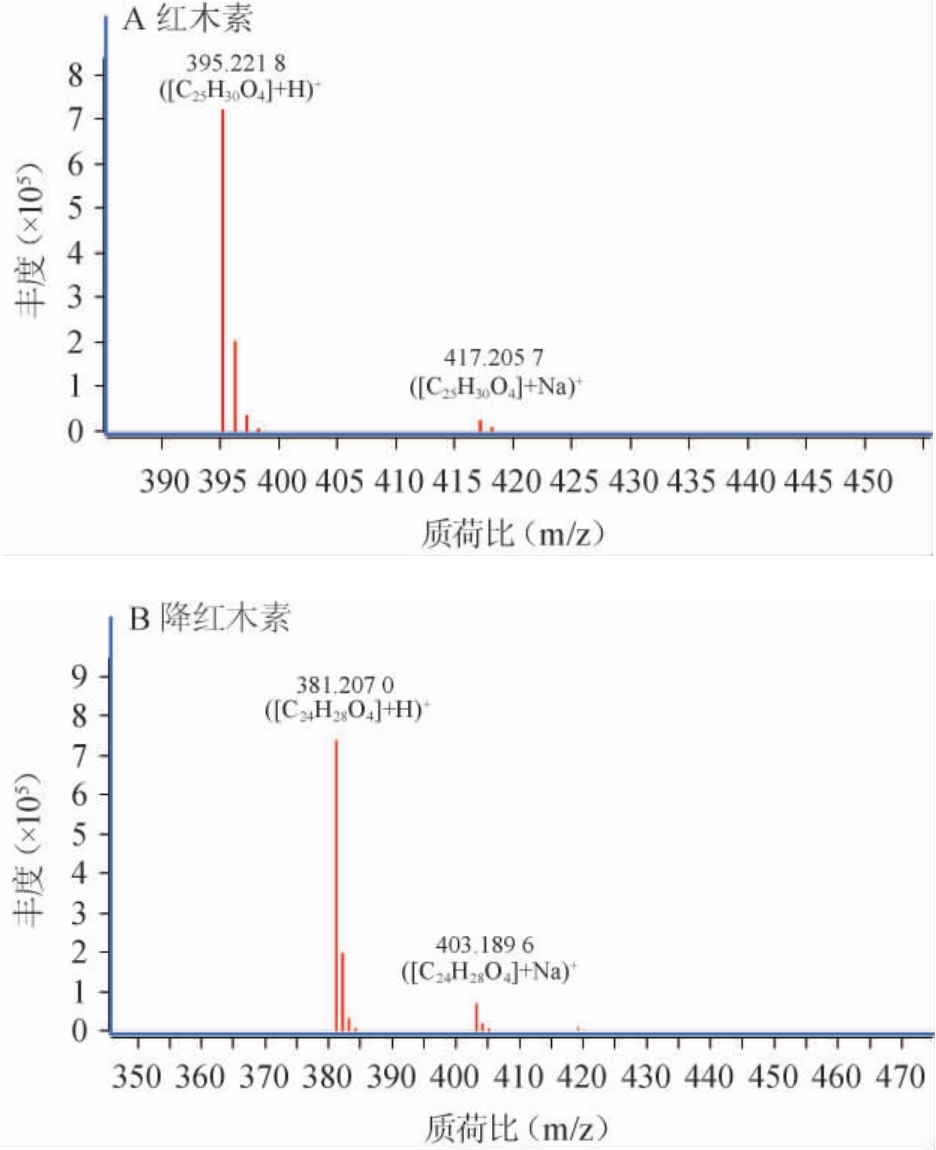
图2 红木素(A)及降红木素(B)不同离子化形式的响应
Fig. 2 Response of bixin (A) and norbixin (B) in different ionic forms
红木素、降红木素的保留时间、理论相对分子质量和特征离子见表1。
表1 红木素、降红木素的保留时间和MS参数
Table 1 Retention time and MS parameters of bixin and norbixin
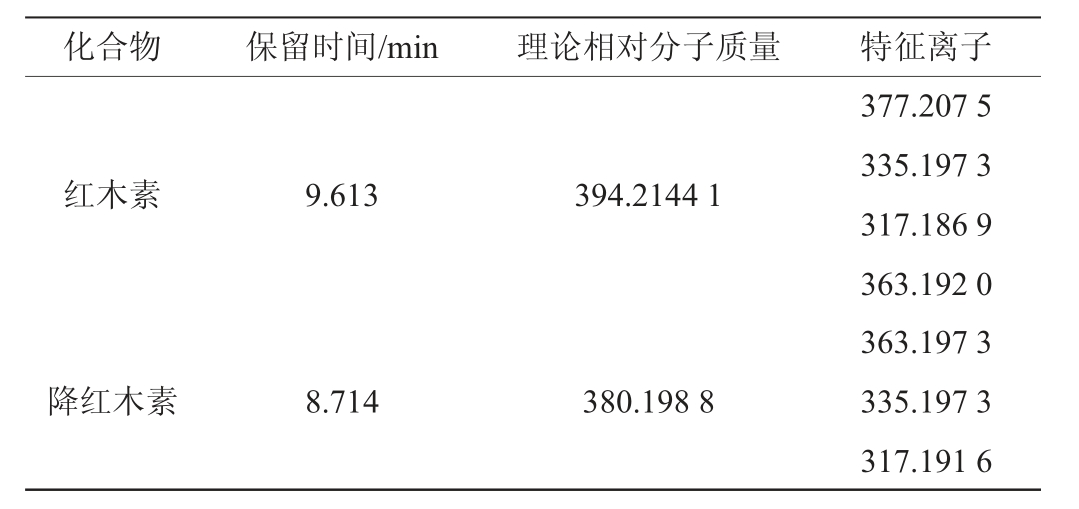
化合物保留时间/min理论相对分子质量特征离子红木素9.613 394.2144 1降红木素8.714 380.198 8 377.207 5 335.197 3 317.186 9 363.192 0 363.197 3 335.197 3 317.191 6
2.3 方法考察
2.3.1 方法的线性和定量限
选取经测定不含有目标化合物的样品,按实验方法进行处理,得到的提取液作为空白基质溶液,用空白基质溶液逐级稀释标准储备液,配制成质量浓度在0.5~70 mg/kg范围内的系列基质混合标准工作溶液,上机测定,以母离子色谱峰面积为纵坐标(Y),质量浓度为横坐标(X)获得目标化合物的线性回归方程。用空白基质溶液逐级稀释标准储备液,直至每种目标化合物的信噪比(S/N)=10,此时对应的化合物质量浓度即为该化合物的定量限(limit of quantitation,LOQ)。红木素、降红木素的线性范围、线性方程、相关系数和定量限见表2。
表2 红木素及降红木素的线性范围、线性方程、相关系数及定量限
Table 2 Linear range, linear equation, correlation coefficient and quantitation limits of bixin and norbixin

化合物线性范围/(mg·kg-1)线性方程相关系数定量限/(mg·kg-1)红木素降红木素1.0~70 0.5~70 Y=6 048.5X+104.23 Y=5481.2X+1233 0.998 5 0.997 6 1.0 0.5
从表2可以看出,两种化合物在1.0~70 mg/kg和0.5~70 mg/kg的质量浓度范围内,相关系数(R)均大于0.99,线性关系良好;此外,两种化合物的定量限分别为1.0 mg/kg和0.5 mg/kg,远远低于其允许使用的限量,完全能够满足快速筛查的需要。
2.3.2 方法回收率和精密度
在经测定不含有待测物质的饼干、全麦片、玉米片3种样品中分别添加1倍、5倍、10倍LOQ和70 mg/kg四个质量浓度水平的加标回收试验,每个加标水平平行做6次,计算其回收率和相对标准偏差(relative standard deviation,RSD),结果见表3。由表3可知,两种化合物的平均加标回收率在71.5%~110.6%之间,相对标准偏差均不高于10.2%。
表3 不同食品中红木素和降红木素的加标回收率和精密度
Table 3 Standard recovery and precision of bixin and norbixin in different foods
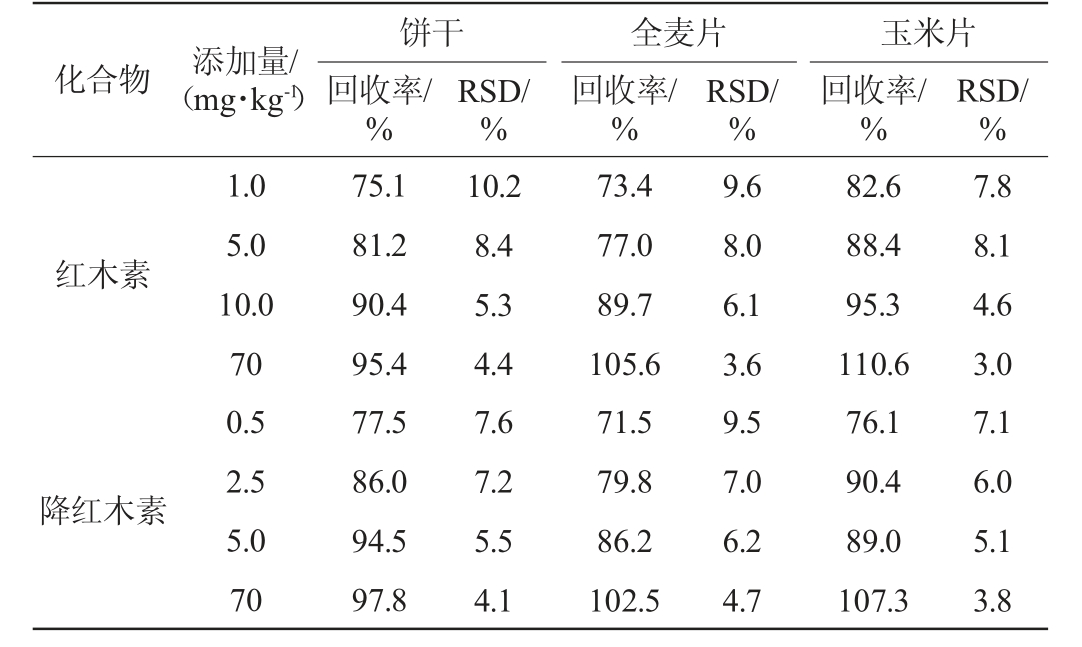
化合物 添加量/(mg·kg-1)饼干回收率/%RSD/%全麦片回收率/%RSD/%玉米片回收率/%RSD/%红木素降红木素1.0 5.0 10.0 70 0.5 2.5 5.0 70 75.1 81.2 90.4 95.4 77.5 86.0 94.5 97.8 10.2 8.4 5.3 4.4 7.6 7.2 5.5 4.1 73.4 77.0 89.7 105.6 71.5 79.8 86.2 102.5 9.6 8.0 6.1 3.6 9.5 7.0 6.2 4.7 82.6 88.4 95.3 110.6 76.1 90.4 89.0 107.3 7.8 8.1 4.6 3.0 7.1 6.0 5.1 3.8
2.3.3 实际样品检测
应用本方法对40件购自超市的饼干、麦片、玉米片、核桃粉、芝麻糊等样品进行检测分析,结果只有一件夹心饼干样品检出降红木素,检出值为3.0 mg/kg。
3 结论
本研究建立了即食谷物食品中红木素和降红木素的超高效液相色谱-四级杆-飞行时间质谱检测法,红木素和降红木素两种化合物分别在1.0~70 mg/kg、0.5~70 mg/kg范围内具有较好的线性关系,相关系数(R)均大于0.99,其定量限分别为1.0 mg/kg、0.5 mg/kg,平均加标回收率在71.5%~110.6%范围内,相对标准偏差(RSD)均不高于10.2%。该方法操作简单、快速、定性准确度高,适用于批量样品的快速筛查,可为食品安全监管提供有效保障。
[1]张京杭.谷物在运动营养食品中的应用——评《运动营养学》[J].粮食与油脂,2021(5):170.
[2]赵梵,郭斐,董笑晨.全谷物食品行业概况和发展趋势[J].现代食品,2018(15):8-12.
[3]王冀宁,涂怡青,王雯熠.食用色素供应链的全过程风险管理研究[J].中国调味品,2021,46(7):171-175.
[4]孙晓莎,任顺成.天然食用色素的研究进展[J].食品研究与开发,2016,37(18):198-201.
[5]陈建白,何美莹,李国华,等.胭脂树橙与降胭脂树橙理化性质比较[J].热带农业科技,2007,30(4):26-28.
[6]黄延春,索全伶,李云霞,等.天然食用红木素[J].中国食品添加剂,2004(3):47-50.
[7]国家卫生和计划生育委员会.GB 2760—2014 食品安全国家标准食品添加剂使用标准[S].北京:中国标准出版社,2014.
[8]张春娥,廖若宇,孙悦,等.液相色谱-串联质谱法测定谷类食品中5种合成着色剂[J].粮油食品科技,2021,29(3):163-169.
[9]周佳,禹洁,朱书强,等.饮料及配制酒中11 种有机合成色素的低共熔溶剂萃取、高效液相色谱法测定[J].分析测试学报,2019,38(11):1358-1363.
[10]张慧敏,刘志,李兆杰,等.高分辨质谱法快速筛查肉制品中28 种着色剂[J].中国食品学报,2020,20(7):229-236.
[11]田晶,李巧玲.近红外光谱法快速检测饮料中的食用合成色素[J].食品科学,2018,39(2):293-297.
[12]张慧敏,鞠玲燕,徐成钢,等.静电场轨道阱高分辨质谱筛查辣椒粉中7 种酸性色素[J].食品研究与开发,2018,39(14):126-131.
[13]BITTENCOURT C,FELICISSIMO M P,PIREAUX J J,et al.ToF-SIMS characterization of thermal modifications of bixin from Bixa orellana fruit[J].J Agr Food Chem,2005,53(16):6195-6200.
[14]SCOTTER M J,CASTLE L,HONEYBONE C A,et al.Method development and analysis of retail foods for annatto food colouring material[J].Food Addit Contam,2002,19(3):205-222.
[15]CHISTÉ R C,YAMASHITA F,GOZZO F C,et al.Simultaneous extraction and analysis by high performance liquid chromatography coupled to diode array and mass spectrometric detectors of bixin and phenolic compounds from annatto seeds[J].J Chromatogr A,2011,1218:57-63.
[16]BARETH A,STROHMAR W,KITZELMANN E.HPLC and spectrophotometric determination of annato in cheese[J]. Eur Food Res Technol,2002,215(4):359-364.
[17] NOPPE H, MARTINEZ S A, VERHEYDEN K, et al. Determination of bixin and norbixin in meat using liquid chromatography and photodiode array detection[J].Food Addit Contam,2009,26(1):17-24.
[18]郑玲,李丽华,李湧,等.高效液相色谱法测定饮料中的胭脂树橙[J].食品研究与开发,2011,32(4):121-123.
[19]陈毓芳,王岚,林海丹,等.高效液相色谱法测定奶酪和人造黄油中胭脂树橙残留[J].中国卫生检验杂志,2011,21(4):778-780.
[20]宁啸骏,杨晋青,俞所银.高效液相色谱法测定巧克力中胭脂树橙的含量[J].食品安全质量检测学报,2020,11(5):1369-1373.
[21]国家质量监督检验检疫总局.SN/T 4394—2015 出口食品中红木素和降红木素的测定液相色谱法[S].北京:中国标准出版社,2015.
[22]林钦.超高效液相色谱法快速检测食品中胭脂树橙的含量[J].福建分析测试,2011,20(3):36-39.
[23]顾艳,杨军丽,宗凌丽,等.固相萃取法测定食品中胭脂树橙的含量[J].现代食品,2017,24(33):103-106.
[24]胡文彦,刘新梅,刘其南,等.超声辅助提取-液相色谱-串联质谱法同时测定马卡龙中人工合成色素与天然色素[J].食品安全质量检测学报,2019,10(9):2678-2683.
[25]李晓娟,彭涛,李重九,等.色谱-飞行时间质谱联用技术的特点及其在食品污染物分析研究中的应用[J].分析测试学报,2012,31(5):628.
