苯乳酸(phenyllactic acid,PLA)也称为2-羟基-3-苯基丙酸或β-苯乳酸,是一种天然有机酸,普遍存在于雪莲花、天麻等多种植物和蜂蜜、发酵牛奶等食品中[1-2]。经研究发现,苯乳酸是一种广谱抑菌性强的生物活性化合物,具有抑制蜡样芽胞杆菌[3]、粪肠球菌[4]、单核细胞增多性李斯特菌[5]等革兰氏阳性细菌,大肠杆菌[6]、阴沟肠杆菌[7]、肠道沙门氏菌[8]等革兰氏阴性细菌和黄曲霉[9]、罗氏青霉[10]、黑曲霉[11]等真菌的能力。作为天然的抑菌剂,由于其具有稳定性强、安全、无害等特点,在食品防腐剂或饲料添加剂等方面具有巨大的应用潜力[12]。
随着苯乳酸应用潜力的不断挖掘[13-15],生物发酵法生产苯乳酸的研究越来越受到重视,提高苯乳酸的产量一直是国内外研究的热点。其中,研究苯乳酸的发酵工艺是提高苯乳酸产量的重要途径之一。WU W Y等[16]对植物乳杆菌(Lactobacillus plantarum)发酵条件和生长营养物质进行优化,发现优化后的样品产苯乳酸的能力是优化前的7.61~13.26倍。张成林等[17]利用植物乳杆菌AB-1在优化培养基中外源添加酵母菌无细胞发酵上清液,使苯乳酸产量相较于优化前增加了60.3%。侯楠楠等[18]在植物乳杆菌BLCC2-0069培养基中添加苯丙酮酸后,发酵液中苯乳酸产量是未添加的3倍。刘周玭等[19]优化重组大肠杆菌的培养条件后,底物苯丙氨酸转化为苯乳酸的转化率为35.2%。李芬等[20]使用亚硝基胍-紫外复合诱变植物乳杆菌LY-78,诱变后苯乳酸产量比诱变前提高了2.89倍。
响应面法因具有准确性高、工作量少和周期短等特点,可以达到提高生产效益的目的[21-22]。本研究以前期研究室筛选得到的植物乳杆菌(Lactobacillus plantarum)BLPC002[23]为生产菌,首先对菌株BLPC002生长曲线进行测定,确定该菌株的接种种龄和培养方式,并通过单因素试验和Box-Behnken试验设计对植物乳杆菌株BLPC002产苯乳酸的发酵工艺条件进行优化。旨在降低生产成本,提高苯乳酸产量,为下一步中试研究提供基础。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种
植物乳杆菌(Lactobacillus plantarum)BLPC002:本实验室筛选保藏。
1.1.2 试剂
蛋白胨、牛肉浸粉、酵母浸粉、琼脂(均为生化试剂):生工生物工程(上海)股份有限公司;苯乳酸、苯丙氨酸标准品(纯度均为98%):德国Sigma公司;甲醇、三氟乙酸(均为色谱纯):德国Merck公司。
1.1.3 培养基
种子培养基采用MRS液体培养基:蛋白胨10.0 g/L,牛肉浸粉10.0 g/L,酵母浸粉5.0 g/L,葡萄糖20.0 g/L,醋酸钠5.0 g/L,柠檬酸氢二铵2.0 g/L,吐温-80 1.0g/L,K2HPO42.0 g/L,MgSO4·7H2O 0.1 g/L,MnSO4·7H2O 0.05 g/L,蒸馏水1.0 L,pH6.2。121 ℃灭菌20 min。
保藏培养基采用MRS固体培养基:在MRS液体培养基的基础上添加琼脂20.0 g/L。
发酵培养基[24]:苯丙氨酸8.3 g/L,蛋白胨10.0 g/L,牛肉浸粉1.8 g/L,酵母浸粉4.0 g/L,葡萄糖30.0 g/L,醋酸钠5.0 g/L,柠檬酸氢二铵2.0 g/L,吐温-80 1.0 g/L,MgSO4·7H2O 0.58 g/L,K2HPO42.0 g/L,MnSO4·7H2O 0.25 g/L,蒸馏水1.0 L,pH6.2。121 ℃灭菌20 min。
1.2 仪器与设备
Waters Alliance e2695高效液相色谱仪(配有紫外-可见光吸收光谱(ultraviolet-visible spectroscopy,UV/VIS)检测器和Empower 3色谱工作站)、Waters SymmetryR C18色谱柱(4.6 mm×250 mm,5 μm):美国Waters公司;UV-6100紫外分光光度计:上海元析仪器有限公司;SW-CJ-2FD双人净化工作台:苏州净化设备有限公司;ZWY-2102C恒温摇床:上海智城分析仪器制造有限公司;NC-MY40超纯水机:重庆隆暾科技有限公司;Biostat A全自动发酵罐:德国赛多利斯集团。
1.3 方法
1.3.1 接种种龄和培养方式的确定
将斜面培养菌种用无菌水洗下后,以2%接种量(V/V)接入装液量为100 mL/500 mL种子培养基中,置于摇床中30 ℃,200 r/min振荡培养,每隔3 h取样,测定菌体浓度(OD600 nm值)和苯乳酸产量,同时对比厌氧(采用不间断通入高纯氮气)振荡培养(30 ℃,200 r/min)的菌体生长情况,根据测定结果,确定最佳接种种龄和培养方式。
1.3.2 菌株BLPC002产苯乳酸发酵工艺优化
(1)单因素试验
接种量对苯乳酸产量的影响:按1%、2%、3%、4%、5%、6%和7%(V/V)的接种量将种子液接入装液量为100 mL/500 mL发酵培养基中,置于摇床中30 ℃、200 r/min振荡培养48 h,检测发酵液中苯乳酸产量,以确定适宜接种量。
发酵时间接种量对苯乳酸产量的影响:将种子液按3%的接种量接入装液量为100 mL/500 mL发酵培养基中,置于摇床中30 ℃、200 r/min分别振荡培养24 h、36 h、48 h、60 h、72 h后,检测发酵液中苯乳酸产量,以确定适宜发酵时间。
发酵温度对苯乳酸产量的影响:将种子液按3%的接种量接入装液量为100 mL/500 mL发酵培养基中,分别置于28 ℃、30 ℃、32 ℃、34 ℃、36 ℃、38 ℃摇床中,200 r/min振荡培养48 h,检测发酵液中苯乳酸产量,以确定适宜的发酵温度。
装液量对苯乳酸产量的影响:将种子液按3%的接种量分别接入装有100 mL、125 mL、150 mL、175 mL、200 mL发酵培养基的500 mL三角瓶中,置于摇床中30 ℃,200 r/min振荡培养48 h,检测发酵液中苯乳酸产量,以确定适宜的装液量。
摇床转速对苯乳酸产量的影响:将种子液按3%的接种量接入装液量为100 mL/500 mL发酵培养基中,置于30 ℃摇床中,分别于100 r/min、150 r/min、200 r/min、250 r/min、300 r/min振荡培养48 h,检测发酵液中苯乳酸产量,以确定适宜的培养转速。
(2)响应面试验
以单因素试验结果为依据,采用Box-Behnken试验设计,以苯乳酸产量为响应值(Y),选择接种量(A)、摇床转速(B)、装液量(C)和发酵温度(D)为响应面分析的自变量因素,对菌株BLPC002发酵产苯乳酸工艺条件进行优化。响应面试验因素及水平见表1。
表1 产苯乳酸发酵工艺优化Box-Behnken试验因素及水平
Table 1 Factors and levels of Box-Behnken experiments for optimization of fermentation process of phenyllactic acid production
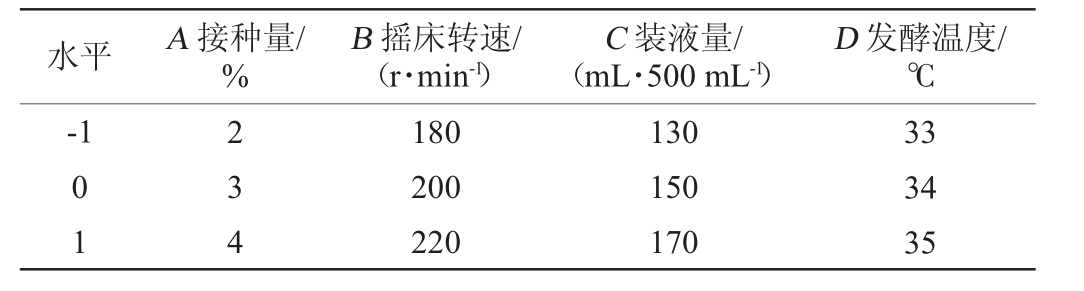
水平A 接种量/%D 发酵温度/℃-1 B 摇床转速/(r·min-1)C 装液量/(mL·500 mL-1)01 234 180 200 220 130 150 170 33 34 35
1.3.3 分析检测
菌体浓度的测定:采用分光光度法。将发酵液稀释至适当浓度后,于波长600 nm处测定其光密度(optical density,OD600nm)值。
苯乳酸的测定:采用高效液相色谱法。参考黄国昌等[25]的方法,WatersSymmetryR C18色谱柱(4.6mm×250mm,5μm),柱温30 ℃,进样量10.0 μL,流速1.0 mL/min,流动相:A相为0.05%三氟乙酸甲醇溶液(V/V),B相为0.05%三氟乙酸溶液(V/V),洗脱程序:0~20 min为A:B由10%线性变化为100%,20~23 min为100%A相,23~25 min保持A:B为10%,检测波长:210 nm。
苯乳酸标准溶液的配制:准确称取苯乳酸标品0.100 0 g,用超纯水溶解后定容至100 mL,配制成1.000 0 g/L的苯乳酸标准溶液。然后从中分别吸取0.5 mL、1.0 mL、2.0 mL、3.0 mL、4.0 mL、5.0 mL用超纯水定容至10.0 mL,分别配制成0.05 g/L、0.1 g/L、0.2 g/L、0.3 g/L、0.4 g/L和0.5 g/L的苯乳酸标准溶液,备用。
发酵液样品的预处理:取发酵液5.0 mL,10 000 r/min离心10 min,上清液经0.22 μm滤膜过滤后即为待测样品。
定性分析:按上述色谱条件分别将苯乳酸标准溶液和发酵液样品进样分析,对比样品中各组分与标准品的出峰保留时间,确定样品中是否含有苯乳酸。
定量分析:将上述各浓度梯度的标准溶液分别进样分析后,以标准溶液质量浓度为横坐标、峰面积为纵坐标建立外标校正曲线,再根据样品的峰面积自动计算出样品中苯乳酸的含量。
2 结果与分析
2.1 接种种龄和培养方式的确定
好氧和厌氧条件下菌株BLPC002的生长曲线见图1。由图1可知,菌株BLPC002的生长过程是典型的分批培养过程中微生物的生长过程,经历了延滞期、对数生长期、稳定期和衰老期四个阶段。其中,发酵时间在0~12 h之间为延滞期,菌体量增长缓慢,主要合成新的酶和细胞增殖所需的各类物质;发酵时间在12~24 h之间为对数生长期,细胞大量增殖,菌体量增长迅速;发酵时间在24~48 h之间为稳定期,产物合成速率加快,但持续时间较短,可能由于葡萄糖的消耗等原因,pH迅速下降,导致菌体内有害产物积累,进入衰亡期。因此,选用对数生长期24 h左右为最佳接种种龄,该生长曲线也为发酵周期的选择提供了一定的参考价值。此外,好氧条件下的菌体生长速度明显高于厌氧条件。培养结束后,对培养液中的苯乳酸产量进行测定发现,厌氧条件下苯乳酸产量均值为0.689 g/L,而好氧条件下苯乳酸产量均值为0.306 g/L,说明厌氧条件有利于苯乳酸的合成,因此,考虑采用兼性厌氧的方式进行苯乳酸的发酵生产,即前24 h内采用好氧方式进行菌体培养,后24 h采用厌氧方式生产苯乳酸。
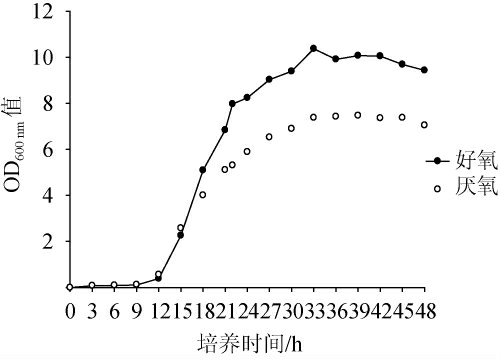
图1 好氧和厌氧条件下菌株BLPC002的生长曲线
Fig. 1 Growth curves of strain BLPC002 under aerobic and anaerobic conditions
2.2 发酵条件优化单因素试验
2.2.1 接种量对苯乳酸产量的影响
接种量对苯乳酸产量的影响见图2。由图2可知,接种量对苯乳酸的产量存在较明显的影响。在一定范围内,随着接种量在1%~3%范围内的增加,苯乳酸产量也随之增加;当接种量为3%时,苯乳酸产量为2.11 g/L;当接种量在3%~5%范围内时,苯乳酸的产量趋于平稳,不再有明显的增长;而当接种量>5%时,苯乳酸产量出现了下降的趋势。这可能是因为当接种量较高时,菌种大量繁殖,但营养物质供应不足,导致苯乳酸产量下降。因此,选择接种量3%为响应面试验优化的中心点。
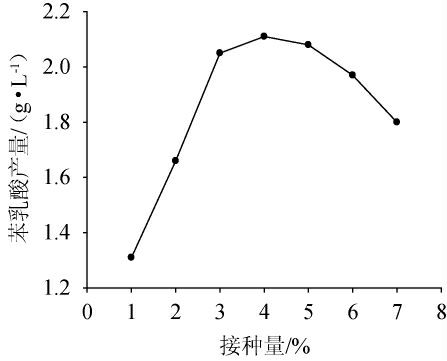
图2 接种量对苯乳酸产量的影响
Fig. 2 Effect of inoculum on phenyllactic acid production
2.2.2 发酵时间对苯乳酸产量的影响
发酵时间对苯乳酸产量的影响见图3。由图3可知,随着发酵时间在24~48 h范围内的增加,苯乳酸产量增幅明显;当发酵时间为48 h时,苯乳酸产量为2.10 g/L;发酵时间超过48 h后,再延长发酵时间,苯乳酸产量变化趋于平稳。因此,选择发酵时间48 h为响应面试验优化的中心点。
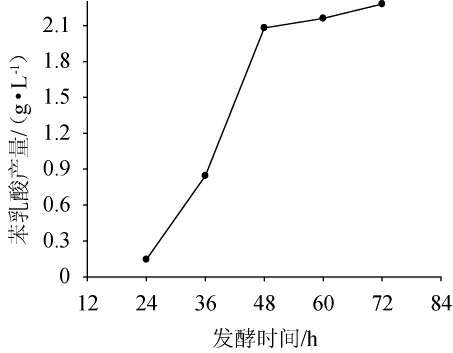
图3 发酵时间对苯乳酸产量的影响
Fig. 3 Effect of fermentation time on phenyllactic acid production
2.2.3 发酵温度对苯乳酸产量的影响
发酵温度对苯乳酸产量的影响见图4。由图4可知,随着发酵温度在28~34 ℃范围内的增加,苯乳酸产量增加;当发酵温度为34 ℃时苯乳酸产量达到最高值,为2.33 g/L;当发酵温度高于34 ℃时,苯乳酸产量急剧下降。其原因可能是,温度过低或过高对菌体生长和代谢合成所需的酶活性都具有不利的影响,导致苯乳酸合成受阻[26]。因此,选择发酵温度34 ℃为响应面试验优化的中心点。
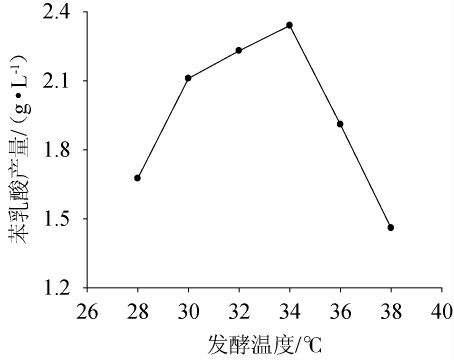
图4 发酵温度对苯乳酸产量的影响
Fig. 4 Effect of fermentation temperature on phenyllactic acid production
2.2.4 装液量对苯乳酸产量的影响
装液量对苯乳酸产量的影响见图5。由图5可知,当装液量为100~150 mL/500 mL时,苯乳酸产量逐渐增加;当装液量为150 mL/500 mL时,苯乳酸产量最高2.27 g/L;当继续增加装液量,苯乳酸产量呈下降趋势。其原因可能是,装液量的多少不仅会影响菌体生长过程中所需的溶氧量,还会影响发酵液中营养物质的传递,从而影响苯乳酸的合成[27]。适当增加装液量有利于菌体的生长,而当装液量过多时,发酵液的传质受到影响,导致苯乳酸产量下降。因此,选择装液量150 mL/500 mL为响应面试验优化的中心点。
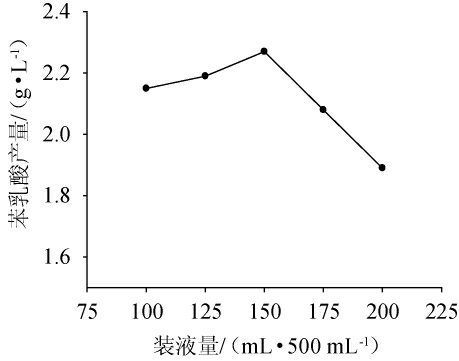
图5 装液量对苯乳酸产量的影响
Fig. 5 Effect of liquid volume on phenyllactic acid production
2.2.5 摇床转速对苯乳酸产量的影响
摇床转速对苯乳酸产量的影响见图6。由图6可知,随着摇床转速在100~200 r/min范围内的增加,苯乳酸产量逐渐增加;当摇床转速为200 r/min时,苯乳酸产量达到最高值,为2.18 g/L;继续增加转速,苯乳酸产量下降。因此,选择转速200 r/min为响应面试验优化的中心点。
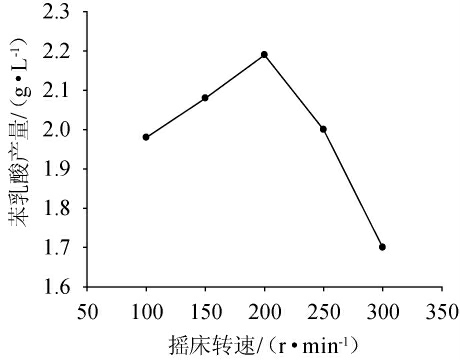
图6 摇床转速对苯乳酸产量的影响
Fig. 6 Effect of shaker speed on phenyllactic acid production
2.3 发酵工艺优化响应面试验结果
2.3.1 Box-Behnken试验结果及回归模型方差分析
结合单因素试验结果,进一步优化菌株BLPC002产苯乳酸发酵工艺。选取接种量(A)、摇床转速(B)、装液量(C)、发酵温度(D)作为影响因子,以苯乳酸产量为(Y)为响应值,设计Box-Behnken试验,试验设计及结果见表2。回归模型方差分析见表3。
表2 产苯乳酸发酵工艺优化Box-Behnken试验设计及结果
Table 2 Design and results of Box-Behnken experiments for optimization of fermentation process of phenyllactic acid production
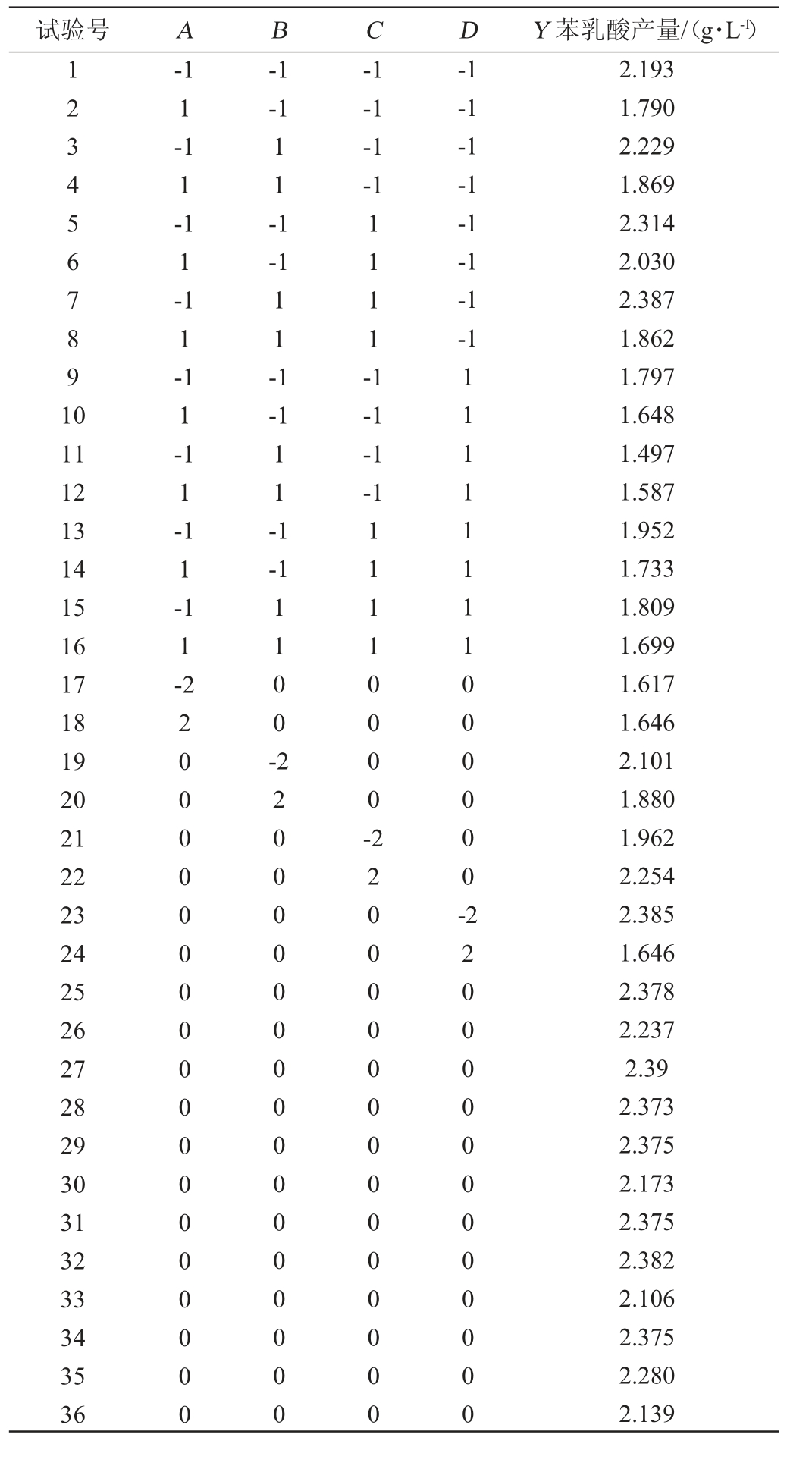
试验号ABCDY 苯乳酸产量/(g·L-1)1234567891 0-1-1 11-1-1-1-1-1-1 1-1 1-1 1-1 1-1 1-1 1-1 1-1 1-2-1 11-1 1111-1-1-1-1-1-1-1-1-1-1 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 11-1-1-1-1-1 2000000000000000000 1100-220000000000000000 11110000-2200000000000000 11111111000000-22000000000000 2.193 1.790 2.229 1.869 2.314 2.030 2.387 1.862 1.797 1.648 1.497 1.587 1.952 1.733 1.809 1.699 1.617 1.646 2.101 1.880 1.962 2.254 2.385 1.646 2.378 2.237 2.39 2.373 2.375 2.173 2.375 2.382 2.106 2.375 2.280 2.139
表3 回归模型方差分析
Table 3 Variance analysis of regression model

注:“**”表示对结果影响极显著(P<0.01);“*”表示对结果影响显著(P<0.05)。
方差来源平方和均方F 值P 值显著性模型ABCDA B********AC AD BC BD CD*A2 B2 C2 D2 15.031 71 11.700 25 2.980 69 10.018 43 63.471 94 0.109 156 0.484 44 6.800 94 0.003 28 1.510 546 0.112 086 74.233 49 17.163 22 7.176 166 14.679 31<0.000 1 0.002 6 0.098 9 0.004 7<0.000 1 0.744 4 0.494 1 0.016 4 0.954 9 0.232 7 0.741 1<0.000 1 0.000 5 0.014 1 0.001 0*******残差失拟项纯误差总和2.711 134 0.150 734 0.038 400 0.129 067 0.817 704 0.001 406 0.006 241 0.087 616 4.22E-05 0.019 460 0.001 444 0.956 345 0.221 113 0.092 450 0.189 113 0.270 541 0.143 399 0.127 143 2.981 675 0.193 652 0.150 734 0.038 400 0.129 067 0.817 704 0.001 406 0.006 241 0.087 616 4.22E-05 0.019 460 0.001 444 0.956 345 0.221 113 0.092 450 0.189 113 0.012 883 0.014 340 0.011 558 1.240 638 0.362 8
用Design Expect 8.0.6软件统计计算,对表2的试验结果进行多元回归拟合,得到各因素水平对苯乳酸产量的二次多项回归模型方程:

由表3可知,上述建立的回归模型极显著(P=0.000 1<0.05),失拟项不显著(P=0.362 8>0.05)。因此,该回归模型高度显著,各试验因子对响应值的影响不是简单的线性关系,而是呈二次抛物面关系。该模型的决定系数R2为90.93%,校正决定系数R2adj=84.88%,表明该模型的预测值和实测值拟合良好,可以很好地解释响应值的变化情况。4个因素对苯乳酸产量影响程度为发酵温度>接种量>装液量>摇床转速。其中,一次项A、C、D,二次项A2、B2、D2达到极显著水平(P<0.01),交互项AD,二次项C2达到显著水平(P<0.05),其他项均不显著。综合数据结果表明,该模型可以较好地反映出菌株BLPC002产苯乳酸发酵工艺中发酵温度、接种量、装液量、摇床转速之间的关系,所得回归方程能较好地预测苯乳酸产量在不同条件下的变化规律。
2.3.2 响应面因子交互作用分析
响应面图和等高线图可以用来直观地表示各变量之间的交互作用及响应值在极点时各自变量的最佳水平。三维响应面图曲面坡度幅度代表响应值的变化幅度,坡度越陡,对响应值影响越大,等高线图为椭圆形代表交互作用强。接种量和发酵温度交互作用对苯乳酸产量影响的响应面和等高线见图7。由图7可知,发酵温度(D)与接种量(A)响应面图曲面坡度明显,等高线为椭圆形,表明二者交互作用对苯乳酸产量影响显著,这与表3的分析结果相符。
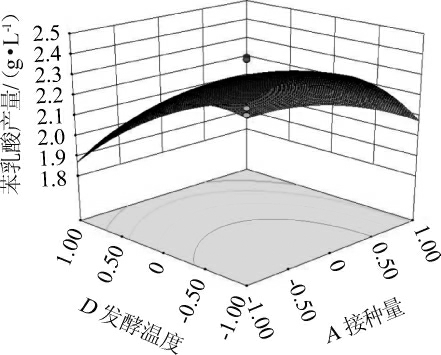
图7 接种量和发酵温度交互作用对苯乳酸产量影响的响应面和等高线
Fig. 7 Response surface plots and contour lines of effects of interaction between inoculum and fermentation temperature on phenyllactic acid production
2.3.3 响应面模型验证试验
通过对回归方程各自变量求极值,得到回归模型预测的最佳编码值为A=-0.589 9,B=0.011 8,C=0.908 1,D=-1.399,对应的实际值为接种量2.410 1%,摇床转速200.236 r/min,装液量168.162 mL/500 mL,温度32.601 ℃。此时,苯乳酸产量预测值为2.566 g/L。考虑到实际操作需要,确定最佳发酵工艺条件分别为接种量2.5%,转速200r/min,装液量170 mL/500 mL,发酵温度33 ℃。在该条件下进行5次平行验证试验,苯乳酸产量实际平均值为2.566 g/L,与预测值接近,说明该模型能准确反映各因素的变化与苯乳酸产量之间的关系,该模型的设计可靠。采用5 L发酵罐以优化后的发酵条件进行验证,苯乳酸产量最高达到2.66 g/L。
3 结论
通过测定植物乳杆菌BLPC002的生长曲线,确定其接种种龄为24 h,培养方式为兼性厌氧,即菌体培养阶段(前24 h)采用好氧方式,苯乳酸生产阶段(后24 h)采用厌氧方式;通过单因素试验和Box-Behnken试验设计确定菌株BLPC002产苯乳酸最佳发酵工艺条件分别为接种量2.5%、摇床转速200 r/min、装液量170 mL/500 mL、发酵温度33 ℃。苯乳酸的产量为2.66 g/L,较优化前提高了1.6倍。后续将对植物乳杆菌BLPC002发酵的pH控制策略和补料工艺进行进一步研究,为苯乳酸生产的中试研究提供参考和依据。
[1]LIU F,WANG F T,DU L H,et al.Antibacterial and antibiofilm activity of phenyllactic acid against Enterobacter cloacae[J].Food Control,2017,84:442-448.
[2]NING Y W,YAN A H,YANG K,et al.Antibacterial activity of phenyllactic acid against Listeria monocytogenes and Escherichia coli by dual mechanisms[J].Food Chem,2017,228:533-540.
[3]NING Y W,FU Y N,HOU L L,et al.iTRAQ-based quantitative proteomic analysis of synergistic antibacterial mechanism of phenyllactic acid and lactic acid against Bacillus cereus[J].Food Res Int,2020,139(3):109562.
[4]WANG F T,WU H H,JIN P P,et al.Antimicrobial activity of phenyllactic acid against Enterococcus faecalis and its effect on cell membrane[J].Foodborne Pathog Dis,2018,15(10):645-652.
[5]SORRENTINO E,TREMONTE P,SUCCI M,et al.Detection of antilisterial activity of 3-phenyllactic acid using Listeria innocuaas a model[J].Front Microbiol,2018,9:1373-1381.
[6]宁亚维,付浴男,何建卓,等.苯乳酸和醋酸联用对大肠杆菌的抑菌机理[J].食品科学,2021,42(3):77-84.
[7]LIU F,SUN Z L,WANG F T,et al.Inhibition of biofilm formation and exopolysaccharide synthesis of Enterococcus faecalis by phenyllactic acid[J].Food Microbiol,2019,86:103344.
[8]RODRÍGUEZ N,SALGADO J M,CORTÉS S,et al.Antimicrobial activity of d-3-phenyllactic acid produced by fed-batch process against Salmonella enterica[J].Food Control,2012,25(1):274-284.
[9] PRADHAN S, ANANTHANARAYAN L, PRASAD K, et al. Anti-fungal activity of lactic acid bacterial isolates against aflatoxigenic fungi inoculated on Peanut kernels[J].LWT-Food Sci Technol,2021,143(4):111104.
[10]MU W M,YU S H,ZHU L J,et al.Recent research on 3-phenyllactic acid,a broad-spectrum antimicrobial compound[J].Appl Microbiol Biotechnol,2012,95(5):1155-1163.
[11] SCHNÜRER J, MAGNUSSON J. Antifungal lactic acid bacteria as biopreservatives[J].Trends Food Sci Tech,2005,16(1-3):70-78.
[12]HUANG C H,CHEN W C,GAO Y H,et al.Production of phenyllactic acid from porphyra residues by lactic acid bacterial fermentation[J].Processes,2021,9(4):678-688.
[13]谢全喜,侯楠楠,王梅,等.高产苯乳酸菌株的筛选及其在豆粕发酵中的应用[J].中国酿造,2021,40(7):65-70.
[14]赵珊,贡汉生,田亚晨,等.苯乳酸-海藻酸钠涂膜保鲜剂的制备及其在甜樱桃保鲜中的应用[J].食品科学,2018,39(11):221-226.
[15]LV X R,MA H H,LIN Y,et al.Antifungal activity of Lactobacillus plantarum C10 against Trichothecium roseum and its application in promotion of defense responses in muskmelon(Cucumis melo L.)fruit[J].J Food Sci Technol,2018,55(9):3703-3711.
[16]WU W Y,DENG G,LIU C J,et al.Optimization and multiomic basis of phenyllactic acid overproduction by Lactobacillus plantarum[J]. J Agric Food Chem,2020,68(6):1741-1749.
[17]张成林,钱怡霖,刘尊英.酵母菌代谢产物对植物乳杆菌AB-1 生产苯乳酸的影响[J].食品研究与开发,2021,42(11):145-151.
[18]侯楠楠,谢全喜,王梅,等.一株高产苯乳酸菌株的安全性评价与发酵工艺优化[J].现代食品科技,2021,37(9):1-9.
[19]刘周玭,王淼.生物转化合成苯乳酸工程菌的培养条件优化[J].工业微生物,2019,49(4):8-15.
[20]李芬,刘晨,田雪娇,等.多种诱变法提高植物乳杆菌产苯乳酸能力的研究[J].黑龙江八一农垦大学学报,2016,28(5):68-72,86.
[21]JIA Q,XIONG C H,CHEN X Y,et al.Optimization of conditions for Cu(II)adsorption on 110 resin from aqueous solutions using response surface methodology and its mechanism study[J].Desalin Water Treat,2013,51(22-24):4613-4621.
[22]袁辉林,康丽华,马海滨.响应曲面法及其在微生物发酵工艺优化中的应用[J].安徽农业科学,2011,39(16):9498-9500,9502.
[23]黄国昌,顾斌涛,黄朝,等.苯乳酸生产菌的筛选及鉴定[J].食品与发酵工业,2018,44(3):97-100.
[24]黄国昌,金丹凤,邱小忠,等.植物乳杆菌BLPC002 产苯乳酸发酵培养基的优化[J].中国酿造,2020,39(7):95-100.
[25]黄国昌,熊大维,黄筱萍,等.高效液相色谱法检测发酵液中苯乳酸和苯丙氨酸含量的研究[J].江西科学,2016,34(5):614-618,702.
[26]陈坚,堵国成.发酵工程原理与技术[M].北京:化学工业出版社,2012:100-101.
[27]韩卫强,王芳,谭天伟,等.接种量和装液量对少根根霉直接发酵生木薯粉生产富马酸的影响[J].北京化工大学学报(自然科学版),2011,38(5):95-99.
