酒是中国饮食文化的重要组成部分,至今已有五千多年历史。有研究表明,机体对酒精摄入没有安全剂量[1-2]。但其他研究发现,适度饮酒能愉悦身心、促进血液循环,但饮酒过度会造成机体损伤[3-4]。酒精滥用和酒精依赖是当前面临的严重问题,人体一次性摄入70~80 g的酒精会引起中毒,达到250~500 g的剂量还会导致死亡。中国的饮酒致死人数世界第一,每年因此致死的人数多达70万[5]。急性醉酒又称急性酒精中毒(acute alcoholism,AAH),一次性过量饮酒会使血液中乙醇含量升高,随后引起头晕、恶心呕吐、昏迷等症状,并伴随着神经、消化、呼吸、心脑血管等系统的损伤[6-7]。酒精主要通过肝脏分解代谢,而多次AAH会引起酒精性肝病的发生[8-9]。近年来AAH的发病率越来越高,且自2019年以来成为除心脑血管及肿瘤外的世界第三大公共卫生问题[10]。
目前,天然化合物在酒精性肝病的治疗中有很大潜力,研究表明一些膳食中的天然成分,如黄酮类化合物、白藜芦醇等具有体外抗氧化活性,可对肝脏起到保护作用[11-13]。老陈醋中含氨基酸、有机酸、多酚、黄酮、川芎嗪、类黑精等活性成分,具有调节血脂、血糖、保护肝脏以及抗肿瘤等功效[14-16]。本实验组前期研究发现山西老陈醋可以抑制小鼠细胞色素P450 2E1(cytochrome P450 2E1,CYP2E1)和还原型烟酰胺腺嘌呤二核苷酸磷酸(nicotinamide adenine dinucleotide phosphate,NADPH)氧化酶活性和Toll样受体4(Tolllike receptor 4,TLR4)诱导的炎症反应,对氧化应激诱导的肝损伤有保护作用[17-18]。目前,国内外关于食醋的醉酒预防作用机制研究相对较少,有待于进一步研究。本试验建立急性醉酒小鼠模型,40只美国癌症研究所(Institute of Cancer Researcch,ICR)小鼠随机分成空白对照组、模型组及低、高剂量山西老陈醋组,并在灌胃4 h后,观察醉酒后小鼠行为学和小鼠肝组织病理学,分别检测血清中乙醇含量及谷草转氨酶(alanine aminotransferase,ALT)、谷丙转氨酶(aspartate aminotransferase,AST)活性和肝组织生化指标(乙醇脱氢酶(alcohol dehydrogenase,ADH)、乙醛脱氢酶(acetalde hydedehydrogenase,ALDH)、过氧化氢酶(catalase,CAT)、超氧化物歧化酶(superoxide dismutase,SOD)和丙二醛(mal ondialdehyde,MDA)。探究山西老陈醋对急性醉酒小鼠的防醉和护肝作用。以期提升传统食醋的保健价值和推动相关功能产品开发。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
实验小鼠(挑选40只体质量在30~34 g的无特定病原体(specific pathogen,SPF)级雄性美国癌症研究所(ICR)小鼠):北京维通利华实验动物技术有限公司。山西老陈醋(酿造食醋,生产许可证号:SC10314012101087):山西紫林醋业股份有限公司;56%vol红星二锅头(食品生产许可证编号:SC11511160310087):北京红星股份有限公司。
1.1.2 试剂
肝素钠:北京索莱宝科技有限公司;血乙醇、谷丙转氨酶(ALT)、谷草转氨酶(AST)、总蛋白定量测定试剂盒(bicinchonininc acid,BCA)法、乙醇脱氢酶(ADH)、乙醛脱氢酶(ALDH)、过氧化氢酶(CAT)、超氧化物歧化酶(SOD)及丙二醛(MDA)试剂盒:南京建成生物工程研究所。
1.2 仪器与设备
CP1502型电子分析天平:上海舜宇恒平科学仪器有限公司;1500型全波长酶标仪:美国Thermo有限公司;UVmini-1240型微量紫外分光光度计:苏州岛津仪器有限公司;Centrifuge 5418 R冷冻离心机:德国Eppendorf有限公司;1X2-1LLJ100普通光学显微镜:日本Olympus有限公司。
1.3 方法
1.3.1 动物分组与处理
小鼠适应性饲养后,按体质量分层后随机分组为空白对照组、模型组及低、高剂量醋组,每组10只。空白对照组小鼠不做处理;模型组小鼠灌胃给予56%vol红星二锅头13 mL/kg;低、高剂量食醋组小鼠在分别灌胃给予山西老陈醋1.25 mg/kg和2.5 mg/kg,30 min后,一次性灌胃给予56%vol红星二锅头13 mL/kg。
1.3.2 急性醉酒小鼠的行为学观察
各组小鼠灌胃白酒后,立刻开始计时并进行翻正反射实验判断小鼠是否醉酒(观察小鼠是否可以保持背部向下30 s,能则判定为醉酒,反之则没醉),并记录醉酒时间(末次灌胃时间-翻正反射消失时间)、醒酒时间(翻正反射消失时间-翻正反射恢复时间)。
1.3.3 肝组织病理形态学观察
各组小鼠末次灌胃4.0 h后,迅速剖取肝脏,冰生理盐水冲洗、擦干后称其质量,拍照;多聚甲醛(4%)固定肝组织,经石蜡包埋后制成切片(5 μm),使用苏木精-伊红(hematoxylin-eosin,HE)染色切片,光镜观察肝脏的病变情况。参考肉眼观察法和脂肪变性评分标准来衡量肝脏组织损伤程度、肝窦充血程度和肝脏细胞空泡化程度等指标[19-20]。
1.3.4 血清和肝脏中指标检测
各组小鼠在末次灌胃0.5 h和4.0 h后处死小鼠,眼球取血后,获得的血液加入抗凝剂肝素钠后在4 ℃、3 000 r/min的条件下离心15 min后取上清液,-80 ℃保存待检。根据试剂盒操作步骤检测0.5 h、4 h血清乙醇含量和4 h血清ALT、AST活性。取4 h后处死的小鼠肝脏,以1∶9比例混入生理盐水进行液氮研磨,在4 ℃,4 500 r/min的条件下离心10 min后取上清液。取上述10%肝匀浆,使用试剂盒检测4.0 h的ADH、ALDH、BCA、MDA、SOD和CAT水平。
1.3.5 数据处理
数据结果均以“平均值±标准差”(X±S)的表示,使用SPSS 26.0软件对数据进行单因素方差分析(analysis of variance,ANOVA),以P<0.05为依据,判断差异是否有统计学意义。
2 结果与分析
2.1 山西老陈醋对急性醉酒小鼠醉酒和醒酒时间的影响
急性酒精中毒后,小鼠由原来行动敏捷、对外界环境的改变反应敏感变为爬行不稳易摔倒,对外界刺激反应迟钝,最终蜷缩瘫倒。本研究将翻正反射消失时间即醉酒时间的长短作为评价药物预防醉酒功效的行为学指标。山西老陈醋对急性醉酒小鼠醉酒、醒酒时间的影响见表1。
由表1可知,与模型组小鼠的醉酒相比,高剂量老陈醋组能显著延长小鼠醉酒时间(P<0.05),将醉酒时间由(27.71±16.27)min延长至(44.00±9.35)min;同时,高剂量老陈醋组能使醉酒小鼠快速从醉酒状态中醒来,缩短醒酒时间(P<0.01),将醒酒时间由原来的(200.29±73.43)min缩短至(121.25±12.71)min。摄入老陈醋后,小鼠由“快醉慢醒”转变为“慢醉快醒”。结果表明山西老陈醋对在小鼠体内的积累的酒精有较好的代谢作用,可以通过延长醉酒时间和缩短醒酒时间起到减弱酒精麻痹,加速醒酒的作用。
表1 山西老陈醋对急性醉酒小鼠醉酒、醒酒时间的影响
Table 1 Effects of Shanxi aged vinegar on drunkenness and sobering time of acute drunkenness mice
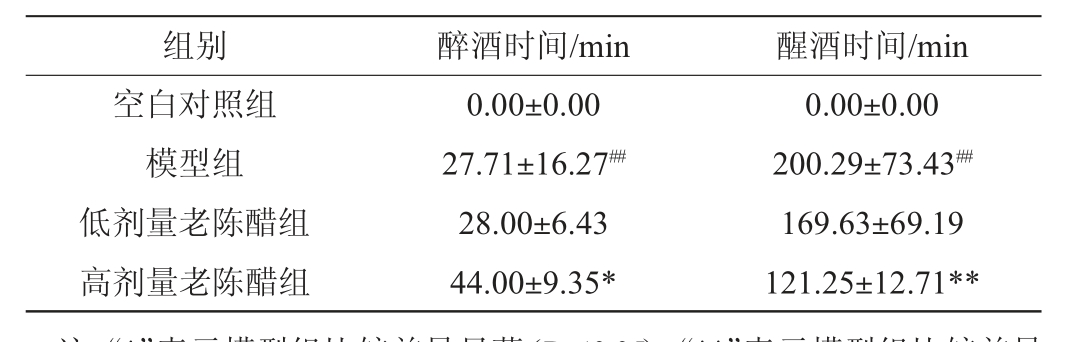
注:“*”表示模型组比较差异显著(P<0.05),“**”表示模型组比较差异极显著(P<0.01),“#”表示与空白组比较差异显著(P<0.05),“##”表示空白组比较差异极显著(P<0.01)。下同。
组别醉酒时间/min醒酒时间/min空白对照组模型组低剂量老陈醋组高剂量老陈醋组0.00±0.00 27.71±16.27##28.00±6.43 44.00±9.35*0.00±0.00 200.29±73.43##169.63±69.19 121.25±12.71**
2.2 山西老陈醋对急性醉酒小鼠酒精含量的影响
肝脏是机体酒精代谢的主要器官,摄入的酒精经胃肠道吸收后分散到血液中,导致血液中的酒精含量上升,之后被输送到肝脏中进行代谢而清除[21]。检测血清中的酒精浓度一方面可以反映乙醇脱氢酶的活性,另一方面可以反映肝损伤程度[22]。山西老陈醋对急性醉酒小鼠血清中酒精含量的影响见表2。
表2 山西老陈醋对急性醉酒小鼠血清中酒精含量的影响
Table 2 Effects of Shanxi aged vinegar on alcohol contents in serum of acute drunkenness mice
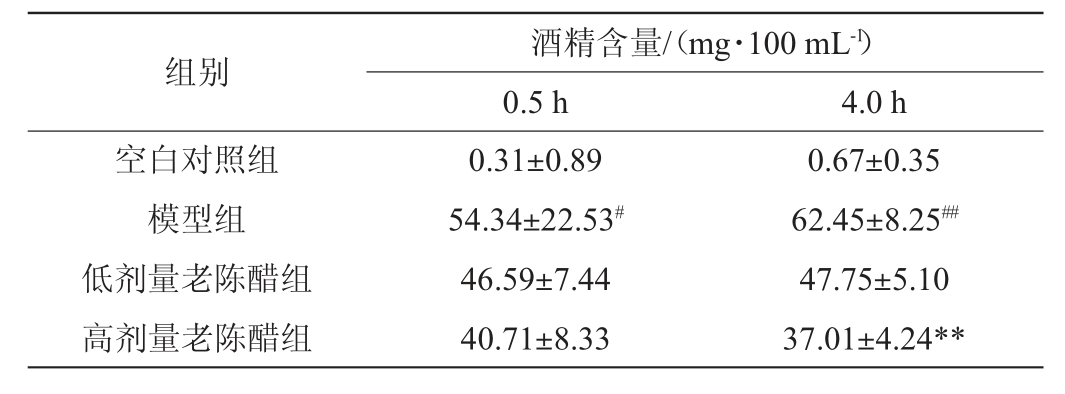
组别空白对照组模型组低剂量老陈醋组高剂量老陈醋组酒精含量/(mg·100 mL-1)0.5 h4.0 h 0.31±0.89 54.34±22.53#46.59±7.44 40.71±8.33 0.67±0.35 62.45±8.25##47.75±5.10 37.01±4.24**
由表2可知,与空白对照组小鼠相比,模型组小鼠血乙醇体积分数在0.5 h显著升高(P<0.05),随着时间延长,在4.0 h时升高更为明显(P<0.01)。与模型组相比,0.5 h的各剂量老陈醋组小鼠的血酒精含量无显著差异(P>0.05),此时老陈醋对血清中酒精含量影响较小;在4.0 h时,高剂量老陈醋组血酒精含量极显著降低(P<0.01),因此,高剂量醋对小鼠血清中酒精含量影响较大。
2.3 山西老陈醋对急性醉酒小鼠ADH、ALDH的影响
ADH和ALDH是体内参与酒精代谢的关键酶,在肝细胞的细胞质及线粒体中广泛存在。乙醇在ADH的作用下分解为乙醛,乙醛在ALDH的作用下分解为乙酸,最终代谢成H2O和CO2,机体通过这种方式降低血液中的酒精浓度[23]。因此ADH和ALDH活性的变化可以直接影响血液中乙醇含量[24]。山西老陈醋对急性醉酒小鼠肝脏ADH、ALDH水平的影响见表3。
表3 山西老陈醋对急性醉酒小鼠肝脏ADH、ALDH水平的影响
Table 3 Effects of Shanxi aged vinegar on ADH and ALDH level in liver of acute drunkenness mice

组别空白对照组模型组低剂量老陈醋组高剂量老陈醋组ADH/(μg·mL-1)ALDH/(μg·mL-1)4.22±1.44 1.65±0.13#4.93±0.74**6.08±1.24**22.42±1.01 15.12±0.82##16.29±0.91 18.6±1.70*
由表3可知,与空白对照组相比,模型组小鼠的ADH含量显著降低(P<0.05),ALDH含量极显著降低(P<0.01)。与模型组相比,各剂量山西老陈醋均极显著提高小鼠ADH活性(P<0.01),低、高剂量老陈醋组的ADH活性分别由(1.65±0.13)μg/mL升至(4.93±0.74)μg/mL、(6.08±1.24)μg/mL;而高剂量老陈醋组的ALDH活性上升较显著(P<0.05),由模型组的(15.12±0.82)μg/mL升至(18.6±1.70)μg/mL,因此,高剂量老陈醋组可显著缓解小鼠的肝损伤。本实验结果表明山西老陈醋可以通过提高ADH和ALDH的活力加快酒精在机体的代谢,降低血液中的酒精含量,起到一定的解酒作用。
2.4 山西老陈醋对急性醉酒小鼠肝组织病理形态学的影响
肝组织病理切片能较直观地观察肝细胞变性坏死、炎细胞浸润等情况,判断肝脏的损伤程度。由图1(a)可知,与空白对照组相比,经酒精处理后的小鼠肝脏出现了明显的病理形态学改变,表现为肝脏表面粗糙、颜色略显泛白等。与模型组相比,经山西老陈醋处理后,上述变化有所缓解,且高剂量老陈醋组缓解效果更明显。
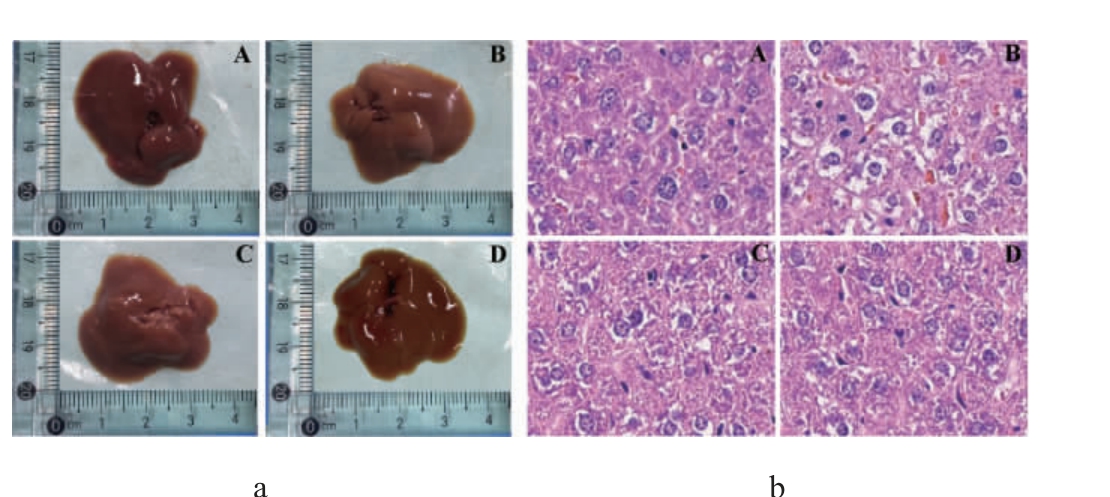
图1 急性醉酒小鼠肝脏组织形态观察(a)与HE染色镜检图(b)
Fig. 1 Liver histomorphology observation (a) and HE staining microscopic examination (b) of acute drunkenness mice
A:空白对照组;B:模型组;C:低剂量老陈醋组;D:高剂量老陈醋组。
由图1(b)可知,空白对照组小鼠的肝脏经过HE染色后肝细胞状态健康,整体无变性、坏死、充血等病变现象。模型组小鼠肝脏细胞出现大面积空泡变性和充血。摄入老陈醋后肝细胞损伤程度得到减轻,以少量空泡变性为主,病变状态得到缓解,以高剂量老陈醋组缓解更为明显。
2.5 山西老陈醋对急性醉酒小鼠肝功酶的影响
ALT和AST是肝中的两种主要的转氨酶,肝细胞受损后这两种酶的活性提高,所以血清中ALT、AST的含量反应了肝脏的健康状况[25-26]。山西老陈醋对急性醉酒小鼠血清中ALT、AST水平的影响见表4。
表4 山西老陈醋对急性醉酒小鼠血清中ALT、AST水平的影响
Table 4 Effects of Shanxi aged vinegar on ALT and AST level in serum of acute drunkenness mice

组别空白对照组模型组低剂量老陈醋组高剂量老陈醋组ALT/(U·g-1)AST/(U·g-1)15.07±1.76 19.93±2.58#16.46±0.78*12.83±3.62**13.15±5.91 24.52±2.80#18.98±0.74*14.22±1.56**
由表4可知,模型组血清中ALT、AST水平较空白对照组显著增高,其含量分别增高至(19.93±2.58)U/g和(24.52±2.80)U/g(P<0.05)。与模型组相比,低剂量老陈醋的摄入显著降低了小鼠血清中ALT、AST水平(P<0.05),其中高剂量老陈醋的摄入使模型组高水平的ALT、AST分别降低至(12.83±3.62)U/g和(14.22±1.56)U/g(P<0.01)。结果表明山西老陈醋对急性醉酒小鼠的肝损伤有一定的保护作用。因此,高剂量的山西老陈醋对急性醉酒小鼠血清中ALT、AST水平影响显著。
2.6 山西老陈醋对急性醉酒小鼠肝脏CAT、SOD和MDA水平的影响
研究表明氧化应激是导致急性酒精肝损伤的发病机制之一[27]。MDA由脂质过氧化产生,MDA水平的提高可干扰抗氧化预防,引起肝脏损伤[28]。另一方面,SOD和CAT主要在机体中起抗氧化作用。SOD和CAT分别在活性氧(reactive oxygen species,ROS)和过氧化氢的催化中起作用,清除体内多余的自由基,将其转变为水和氧排出体外[29-30]。这些抗氧化剂均能保护肝脏免受氧化应激的损害。山西老陈醋对醉酒小鼠肝脏MDA、CAT和SOD水平影响见表5。
表5 山西老陈醋对醉酒小鼠肝脏MDA、CAT和SOD水平影响
Table 5 Effects of Shanxi aged vinegar on MDA, CAT and SOD level in liver of drunkenness mice
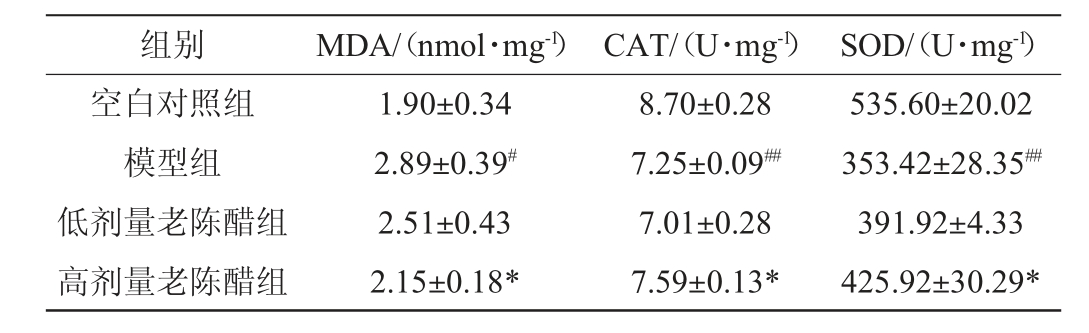
组别MDA/(nmol·mg-1) CAT/(U·mg-1) SOD/(U·mg-1)空白对照组模型组低剂量老陈醋组高剂量老陈醋组1.90±0.34 2.89±0.39#2.51±0.43 2.15±0.18*8.70±0.28 7.25±0.09##7.01±0.28 7.59±0.13*535.60±20.02 353.42±28.35##391.92±4.33 425.92±30.29*
由表5可知,模型组MDA含量相较于空白对照组显著升高至(2.89±0.39)nmol/mg(P<0.05),与模型组相比,各剂量老陈醋组的MDA含量则有所下降,其中高剂量老陈醋组下降最明显(P<0.05),MDA含量由(2.89±0.39)nmol/mg下降至(2.15± 0.18)nmol/mg。模型组CAT和SOD活性较空白对照组显著下降(P<0.01);与模型组相比,高剂量老陈醋组的CAT、SOD活性均显著增强(P<0.05)。CAT含量由(7.25±0.09)U/mg上升至(7.59±0.13)U/mg(P<0.05);SOD含量由(353.42±28.35)U/mg上升至(425.92±30.29)U/mg(P<0.05)。结果表明山西老陈醋可通过减弱急性醉酒小鼠体内的氧化水平,增强抗氧化能力,改善由急性醉酒引起的肝损伤。
3 结论
山西老陈醋是一种健康发酵食品。摄入食醋能够有效改善因急性醉酒引起的醉酒症状,并且能够降低醉酒小鼠的肝功酶活性和氧化应激水平,发挥良好的护肝作用。与模型组相比,高剂量醋组可显著延长醉酒时间至(44.00±9.35)min(P<0.05)、醒酒时间极显著缩短至(121.25±12.71)min(P<0.01);血清中乙醇含量及ALT、AST活性显著降低为(37.01±4.24)mg/100 mL、(12.83±3.62)U/g、(14.22±1.56)U/g;肝组织中乙醇脱氢酶(ADH)活性极显著增加(P<0.01)、乙醛脱氢酶(ALDH)、过氧化氢酶(CAT)和超氧化物歧化酶(SOD)活性显著增加(P<0.05),且丙二醛(MDA)含量显著降低(P<0.05)。食醋组肝脏病变程度减轻,切片显示空泡面积减少。本研究揭示了山西老陈醋能缓解急性醉酒导致的AAH和肝损伤。但对于具有解酒护肝功能的保健山西老陈醋产品的开发仍需要进一步的研究。
[1]杨贵云.饮酒没有健康量[J].当代老年,2019(4):42.
[2]彭文.适量饮酒有益健康?不靠谱[J].百科知识,2018(20):15.
[3]王璐.急诊科治疗急性酒精中毒的临床分析[J].世界最新医学信息文摘,2019,19(31):87.
[4]曹瑞红,雷振河.饮酒与健康之间的关系研究分析[J].酿酒科技,2019(2):135-142.
[5]GRISWOLD M G,FULLMAN N,HAWLEY C,et al.Alcohol use and burden for 195 countries and territories,1990-2016:a systematic analysis for the global burden of disease study 2016[J]. Lancet, 2018, 392(10152): 1015-1035.
[6]LIU X,HOU R L,YAN J J,et al.Purification and characterization of Inonotus hispidus exopolysaccharide and its protective effect on acute alcoholic liver injury in mice[J].Int J Biol Macromol,2019,129:41-49.
[7]吴亚,李艳茹,杨寄镯,等.酒精性肝病发病机制研究现状[J].临床肝胆病杂志,2020,36(12):2822-2825.
[8]SEITZ H K,BATALLER R,CORTEZ-PINTO H,et al.Alcoholic liver disease[J].Nat Rev Dis Primers,2018,4(1):16.
[9]叶松,任凌丽,陈曦,等.王氏保赤丸对急性酒精损伤小鼠醒酒护肝/胃作用及机制研究[J].中国中药杂志,2021(5):1-9.
[10]MARTEN R,AMUL G,CASSWELL S.Alcohol:global health's blind spot[J].Lancet Global Health,2020,8(3):e329-e330.
[11]刘怡菲.软枣猕猴桃解酒护肝作用的研究[J].辽宁林业科技,2019(3):14-16.
[12] TU Y, ZHU S, WANG J, et al. Natural compounds in the chemoprevention of alcoholic liver disease[J].Phytother Res,2019,33(9):2192-2212.
[13]童钰琴,李姝,牛曼思,等.苦荞麸皮总黄酮体外抗氧化活性及体内解酒护肝作用[J].食品工业科技,2020,41(17):314-319,326.
[14]ZHOU Y,TAN F,LI C,et al.White peony(fermented Camellia sinensis)polyphenols help prevent alcoholic liver injury via antioxidation[J]. Antioxidants,2019,8(11):524.
[15] YANG Q Q, ZHANG D, FARHA A K, et al. Phytochemicals, essential oils, and bioactivities of an underutilized wild fruit Cili (Rosa roxburghii)[J].Ind Crop Prod,2020,143:111928.
[16] ZHANG B, XIA T, DUAN W H, et al. Effects of organic acids, amino acids and phenolic compounds on antioxidant characteristic of Zhenjiang aromatic vinegar[J].Molecules,2019,24(20):3799.
[17]XIA T,ZHANG J,YAO J H,et al.Shanxi aged vinegar prevents alcoholic liver injurybyinhibitingCYP2E1 and NADPHoxidase activities[J].J Funct Foods,2018,47:575-584.
[18]XIA T,ZHANG J,YAO J H,et al.Shanxi aged vinegar protects against alcohol-induced liver injury via activating nrf2-mediated antioxidant and inhibiting tlr4-induced inflammatory response[J]. Nutrients, 2018, 10(7):805.
[19]张福利,丁蕾,马旺,等.丹参注射液抑制4-羟基壬烯醛预防酒精性肝病的机制研究[J].浙江中医药大学学报,2016,40(8):579-584.
[20]杨柳,王文地,马允,等.急性酒精性肝损伤模型的考察及验证[J].西北药学杂志,2020,35(3):391-396.
[21]张翼,谭永红,袁吕江,等.葛花提取液成分分析及其抑制小鼠体内酒精吸收实验[J].西南国防医药,2017,27(12):1253-1256.
[22]叶勇,李俊贤,吴英,等.枳椇饮对急性酒精中毒小鼠醒酒作用的实验研究[J].中国中医急症,2019,28(6):1014-1016,1020.
[23]李怡文,刘阳,柳海艳.葛花枳惧子配伍使用对醉酒小鼠体内乙醇代谢过程的影响[J].世界中医药,2017,12(8):1885-1889.
[24]ZHOU T,ZHANG Y J,XU D P,et al.Protective effects of lemon juice on alcohol-induced liver injury in mice[J]. Biomed Res Int,2017, 2017(4):7463571.
[25]李晓宇,李晶,王一博,等.人参皂苷对酒精性肝损伤的保护作用研究[J].药物评价研究,2015,38(5):512-515.
[26] YANG L, LABORITORY D O. The value of aspartate aminotransferase mitochondrial isoenzyme in scrum to patients with alcoholic liver disease[J].Int Lab Med,2016,37(18):2576-2580.
[27]LI L,WU Y F,YIN F Y,et al.Fructose 1,6-diphosphate prevents alcoholinduced liver injury through inhibiting oxidative stress and promoting alcohol metabolism in mice[J].Eur J Pharmacol,2017,815:274-281.
[28]CAO Y W,JIANG Y,ZHANG D Y,et al.The hepatoprotective effect of aqueous extracts of penthorum Chinense pursh again stacute alcohol-induced liver injury is associated with ameliorating hepatic steatosis and reducing oxidative stress[J].Food Funct,2015,6(5):1510-1517.
[29]刘合生,戚向阳,曹少谦,等.杨梅乙醇提取物对小鼠酒精性肝损伤的保护作用[J].中国食品学报,2014,14(8):34-40.
[30]黄颖,谭书明,陈小敏,等.刺梨口服液对急性醉酒小鼠的解酒护肝作用[J].现代食品科技,2019,35(7):18-23.
