醋酸杆菌(Acetobacter aceti,AA)广泛分布于自然界的含糖或酸性物质中,具有快速适应不同生境的典型生物[1-2]。AA是革兰氏阴性或不定、专性需氧菌,形状为椭圆形或杆状,可以单个、成对或成链出现,长0.8~4.5 μm、宽0.4~1.0 μm。醋酸杆菌生长的最适酸碱度pH值为5.0~6.5[3-4]。醋酸菌科按其发育最适温度和特性分为两个主要的属——醋杆菌属(发育适温在30 ℃以上,氧化酒精为乙酸)和葡糖杆菌属(发育适温在30 ℃以下,氧化葡萄糖为葡萄糖酸)[5],通过现代脱氧核糖核酸(deoxyribonucleic acid,DNA)-核糖体核糖核酸(ribosome ribonucleic acid,rRNA)杂交、DNA-DNA杂交和核糖体核糖核酸(ribonucleic acid,RNA)基因序列(5S rRNA、16S rRNA和23S rRNA)技术对醋酸杆菌进行基因分型鉴定,截至目前已经发现55个菌属属于醋酸菌科[6]。在这些菌属中应用较广、研究较成熟的是醋酸杆菌属、葡糖醋酸杆菌属和葡糖酸醋酸杆菌属[6]。
1 醋酸杆菌的有氧呼吸
与许多需氧菌相似,醋酸菌通过有氧呼吸作用来获得维持生理作用的大部分能量[19]。在有氧呼吸中,前体物丙酮酸在柠檬酸循环中被完全氧化成二氧化碳。随后,在柠檬酸循环中形成的还原电子受体穿梭到细胞质膜中[20]。质膜中进行的呼吸链氧化还原的电子载体与电子受体在氧化磷酸化作用下形成水分子,同时将质子从细胞质中排除,产生质子梯度。跨膜三磷酸腺苷酶合酶(transmembrane adenosine triphosphatase synthase,F1F0-ATPase)将质子转移回细胞来平衡这种质子动力,实现三磷酸腺苷(adenosine triphosphate,ATP)的生物合成[21](见图1)。
醋酸杆菌呼吸系统的基本成分由两种周质脱氢酶组成,转氢酶/烟酰胺腺嘌呤二核苷酸磷酸(nicotinamide adenine dinucleotide phosphate,NADP)-泛醌氧化还原酶-依赖性脱氢酶和泛醇氧化酶型的两种末端氧化酶[17]。在氧化过程中,泛醇以其还原形式泛醌(ubiquinone,UQ)穿梭于呼吸蛋白。转氢酶和烟酰胺腺嘌呤二核苷酸(nicotinamide adenine dinucleotide,NADH):泛醌氧化还原酶的反应实现了NADP+和NAD+的再生以及H+的排除。末端氧化酶接受来自泛醌的电子[22],将其转移到电子受体O2形成H2O。
醋酸菌有两个末端泛醇氧化酶,命名为细胞色素bo3泛醇氧化酶和细胞色素bd喹啉氧化酶[23]。细胞色素bo3泛醇氧化酶催化电子的接受进而产生质子动力,而细胞色素bd喹啉氧化酶将泛醇再氧化为泛醌,从而快速再生泛醌,有助于呼吸链或氧化发酵进一步反应[7]。此外,研究发现在氧化葡糖杆菌中,细胞色素bd喹啉氧化酶在低酸碱度下特别活跃[24-25],这表明细胞色素bo3泛醇氧化酶可能在早期生长阶段作为主要的末端氧化酶,当培养物的酸碱度接近中性,在氧化发酵过程中产生大量氧化产物而导致酸碱度降低时,细胞色素bd喹啉氧化酶变得活跃以维持氧化发酵的进行[26]。
表1 醋酸杆菌的菌属及种的数量概况
Table 1 Overview of the number of genus and species of Acetobacter aceti
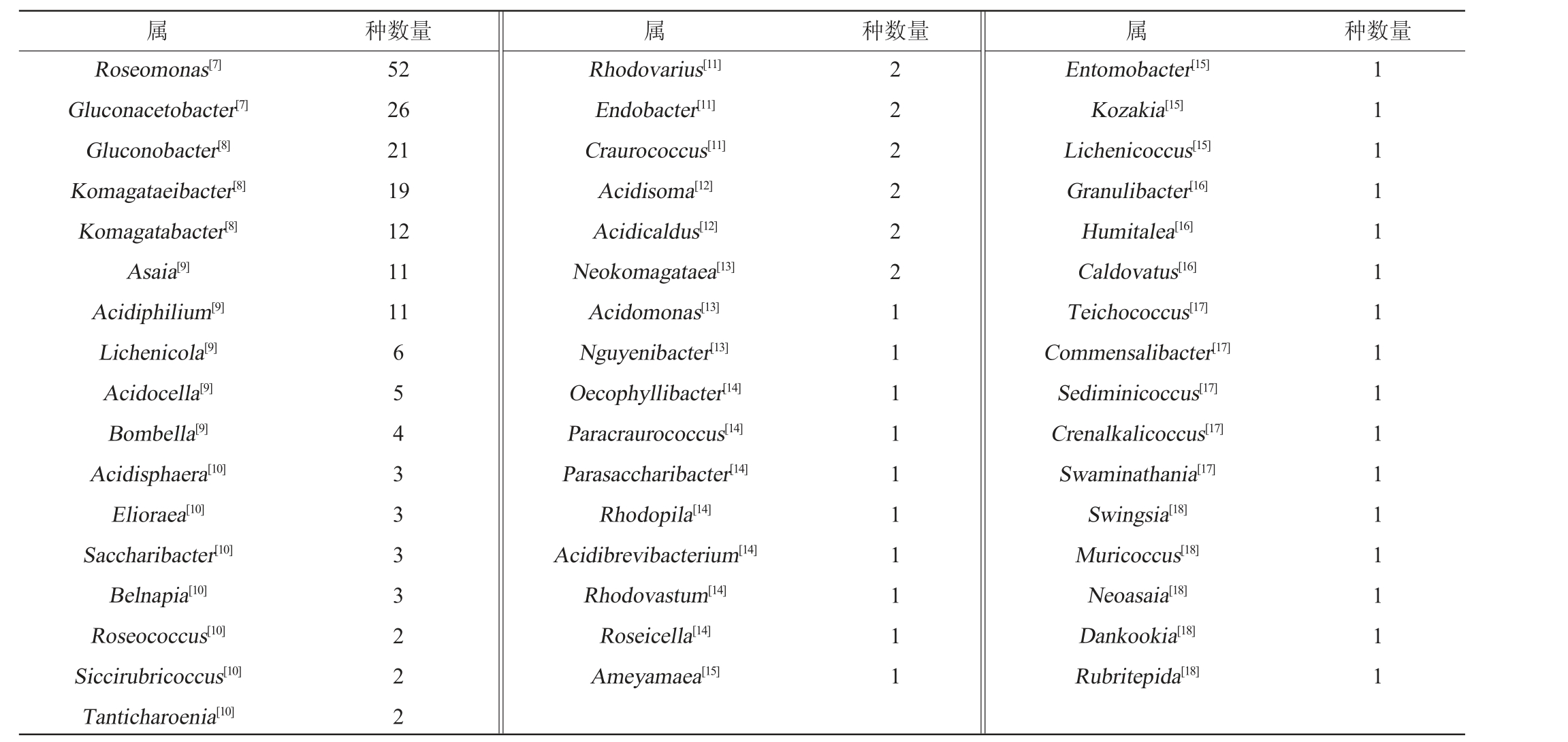
属种数量属种数量属种数量Roseomonas[7]Gluconacetobacter[7]Gluconobacter[8]Komagataeibacter[8]Komagatabacter[8]Asaia[9]Acidiphilium[9]Lichenicola[9]Acidocella[9]Bombella[9]Acidisphaera[10]Elioraea[10]Saccharibacter[10]Belnapia[10]Roseococcus[10]Siccirubricoccus[10]Tanticharoenia[10]52 26 21 19 12 11 11 6543333222 Rhodovarius[11]Endobacter[11]Craurococcus[11]Acidisoma[12]Acidicaldus[12]Neokomagataea[13]Acidomonas[13]Nguyenibacter[13]Oecophyllibacter[14]Paracraurococcus[14]Parasaccharibacter[14]Rhodopila[14]Acidibrevibacterium[14]Rhodovastum[14]Roseicella[14]Ameyamaea[15]2222221111111111 Entomobacter[15]Kozakia[15]Lichenicoccus[15]Granulibacter[16]Humitalea[16]Caldovatus[16]Teichococcus[17]Commensalibacter[17]Sediminicoccus[17]Crenalkalicoccus[17]Swaminathania[17]Swingsia[18]Muricoccus[18]Neoasaia[18]Dankookia[18]Rubritepida[18]1111111111111111
2 醋酸杆菌的有氧代谢
有氧代谢是底物不完全氧化、使反应液中累积了不完全氧化生成物的发酵形式[27]。氧化发酵是一种“溢出代谢”,与通过有氧呼吸将底物完全氧化成二氧化碳和水相比,氧化发酵节省了能量[3,6,28]。醋酸杆菌是能进行氧化发酵的突出菌,通常醋酸杆菌将乙醇、碳水化合物和糖醇氧化成各种相应的产物,如有机酸、醛和酮。氧化发酵过程中氧气的浓度深刻影响发酵的速率和生产率[21]。酸性产品在其低酸碱度的环境中使醋酸杆菌比竞争微生物更具优势。
醋酸杆菌的氧化发酵是通过呼吸链进行的,该呼吸链与上面提及的有氧呼吸氧化还原电子载体类似(见图1)。在这个过程中,电子被泛醌引导到末端氧化酶的分子氧中,而质子被提取出来以产生质子动力。这种质子动力可以被ATPase利用。值得一提的是,参与氧化发酵呼吸链中的脱氢酶会结合特异性底物如乙醇、碳水化合物和糖醇,与还原的电子载体NADH相反[7,9-11,21]。这些酶含有一个辅基,通常是吡咯喹啉醌-酒精脱氢酶(pyrroloquinoline quinonealcohol dehydrogenase, PQQ-ADH),醌蛋白和醌蛋白细胞色素c复合物或黄素腺嘌呤二核苷酸依赖性脱氢酶((flavin adenine dinucleotide-dependent dehydrogenase,FAD-ADH);黄素蛋白-细胞色素c复合物)。这些脱氢酶的细胞色素亚单位负责将电子转移到泛醌,从而将泛醌还原成泛醇[29]。
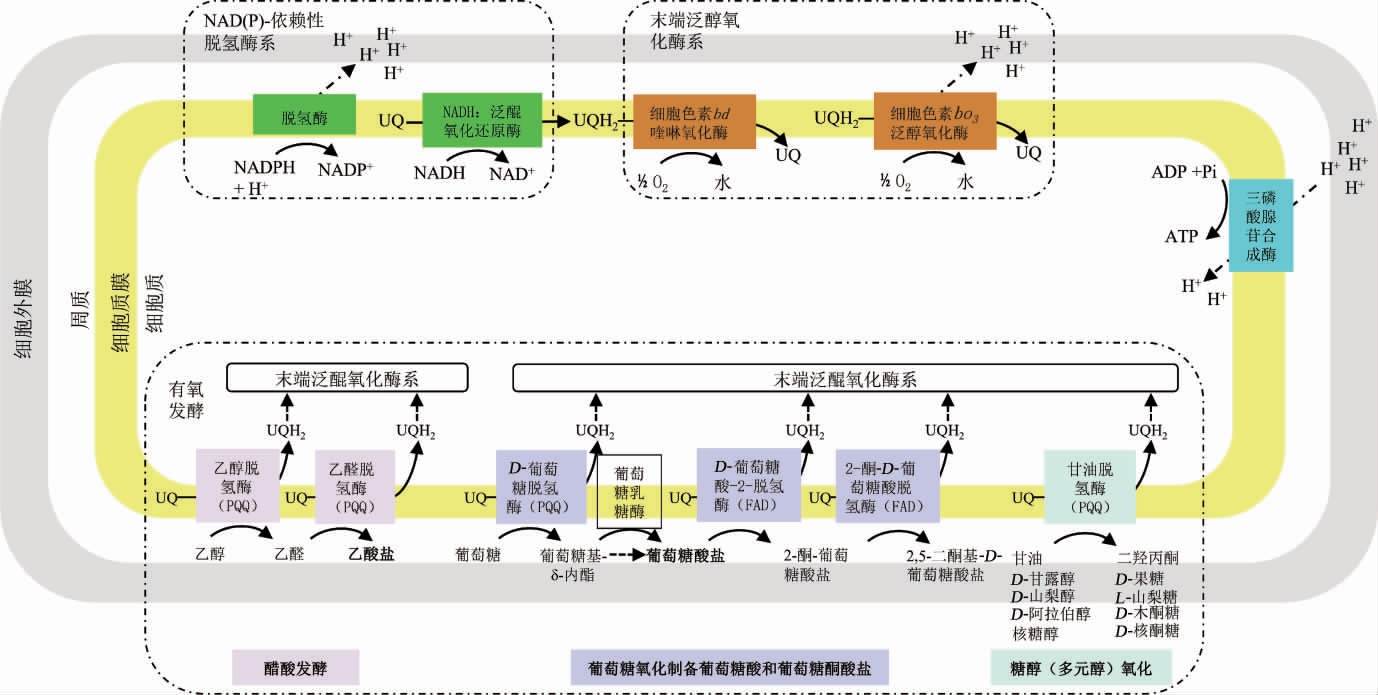
图1 醋酸杆菌的氧化发酵过程与路径
Fig. 1 Process and pathway of oxidative fermentation of Acetobacter aceti
2.1 乙醇氧化
醋酸杆菌最著名的氧化发酵反应之一是从乙醇生产乙酸(醋)。Acetobacter和Komagataeibacter都具有很强的生产乙酸的能力,并且这两个属都表现出对乙醇和乙酸的高抗性,这是满足食醋工业生产的重要特征[30-31]。乙醇首先PQQ-ADH氧化成乙醛,乙醛进一步被乙醛脱氢酶(acetaldehyde dehydrogenase,ALDH)氧化成乙酸。值得关注的是ALDH对存在的氧气水平敏感,当氧气浓度过低或过高时,它的活性就会下降,使乙醛在培养基中积累,降低乙酸的产率[31]。乙醇被完全氧化和耗尽时,Acetobacter,Gluconacetobacter和Komagataeibacter可以同化乙酸,并利用三羧酸循环(tricarboxylic acid cycle,TCA)和乙醛酸分流将其完全氧化成二氧化碳和水,这就是众所周知的乙酸盐“过度氧化”,这在食醋生产中是不利的[15,24,29]。
2.2 碳水化合物氧化
醋酸菌中的葡糖杆菌(Gluconobacter)特别擅长碳水化合物和糖醇氧化。醋酸杆菌首先通过吡咯喹啉醌-葡糖脱氢酶(pyrroloquinoline quinone-glucose dehydrogenas,PQQGDH)将D-葡萄糖氧化成D-葡糖酸-δ-内酯,然后自发地或通过位于细胞质膜中的葡糖酸内酯酶氧化产生D-葡糖酸盐。D-葡萄糖酸盐可以被其他周质脱氢酶进一步转化为酮葡萄糖酸盐[16]。它可以被含果糖二磷酸钠的葡萄糖酸脱氢酶氧化成2-酮-D-葡萄糖酸盐(2-keto-D-gluconate,2-KGA),或者被吡咯喹啉醌-甘油脱氢酶(pyrroloquinoline quinoneglycerol dehydrogenase,PQQ-GLDH)氧化成5-酮-D-葡萄糖酸盐(5-KGA)。葡萄糖浓度、酸碱度和氧化水平等因素会影响赤霉素与酮葡糖酸盐的产量和比例[32-33]。如果要最大限度地提高葡萄糖酸的产量,就不希望将谷氨酸进一步氧化成酮葡糖酸盐。此外,虽然大多数醋酸菌在TCA中可以将底物完全氧化为CO2和H2O,但在葡糖杆菌中,由于缺乏琥珀酰辅酶a合成酶和琥珀酸脱氢酶,这种循环是不完全的。碳水化合物和糖醇氧化产物的生成使得醋酸菌能够迅速消耗竞争微生物的碳源,同时由于酸性产物积累所产生的低pH值,也抑制了竞争微生物的生理活动[34]。
3 醋酸杆菌的解酒护肝作用
当人体大量饮酒,酒精代谢量小于摄入量时,酒精就会在体内短时间大量蓄积,使肝脏乙醇脱氢酶(ethanol dehydrogenase,ADH)、谷胱甘肽巯基转移酶(glutathione sulfotransferase,GST),谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)的含量显著降低,对肝脏产生直接损伤作用。其机制主要涉及乙醇的代谢产物乙醛的生理损伤,氧缺乏、氧应激、自由基的损伤以及还原性辅酶异常引起代谢紊乱等方面[35]。
人体摄入的酒精经一系列消化器官进行体循环,胃和肠道吸收的酒精经血液循环进入肝脏,约90%的酒精在肝脏代谢(见图2)。乙醇对人体的损伤不仅仅是其自身,还在于过量的酒精扰乱人体脂质代谢,进而产生体表发热、脸红、眩晕甚至脑溢血等危及生命的风险[36]。在肝脏,乙醇主要通过ADH酶的酶解作用代谢成乙醛(过氧化氢酶、微粒体氧化酶以及黄嘌呤氧化酶仅代谢约20%)。当过度摄入乙醇导致ADH活性增加,产生过量的NADH,刺激机体丙酮酸代谢,丙酮酸含量的降低导致葡萄糖分解率增加,降低了血液中血糖含量(引起低血糖,甚至死亡)、提高了乳酸的含量。乙醇代谢产生的乙醛通过肝细胞线粒体内的ALDH催化脱氢生成乙酸[37]。过度产生的乙醛累积引起中枢神经系统功能障碍以及Flush(脸部潮红)现象。同时由乙醛代谢产生的乙酸会以乙酰辅酶A(acetyl coenzyme A,A-CoA)的形式参与TCA。而在此过程中H+浓度过高,促进了肝脏脂肪酸的合成,过量脂肪合成,形成将军肚[38]。已有研究表明,醋酸菌产品具有解酒护肝的作用,具体的作用机制也逐渐被关注。
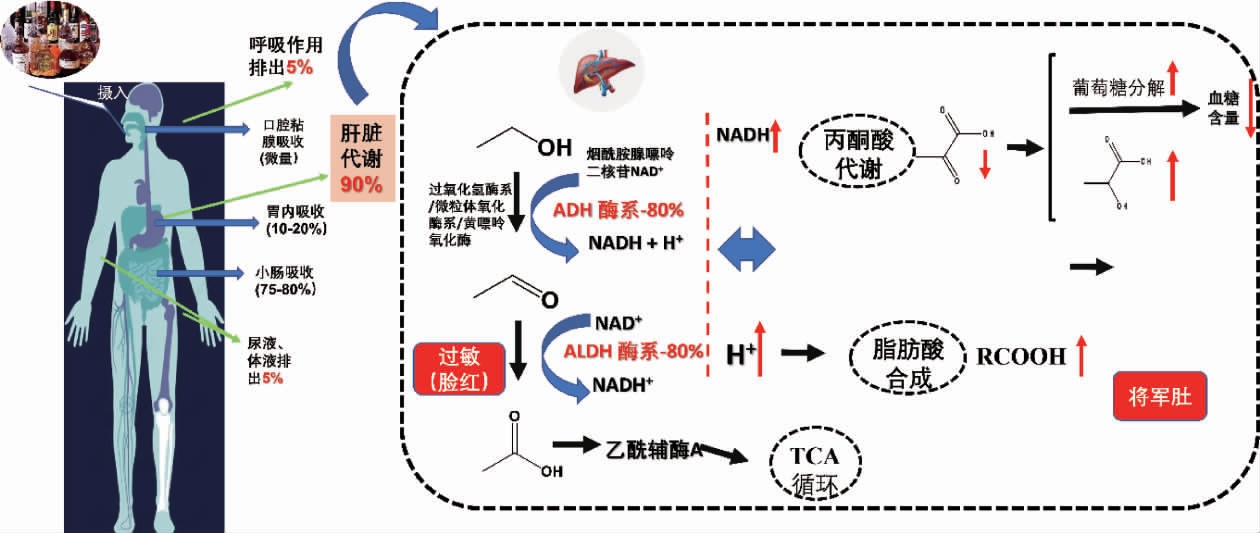
图2 酒精在人体内消化代谢途径及酒精中毒机制
Fig. 2 Digestion and metabolism pathway of alcohol in human body and mechanism of alcoholism
3.1 促进乙醇在胃部氧化
前面介绍已经提到,醋酸杆菌在低酸碱度的条件下PQQ-ADH和ALDH酶依然具有酶活性,胃部是食物消化代谢的场所,正常pH值在0.9~1.8,此时醋酸杆菌与乙醇一同摄入便可以在胃部进行部分乙醇代谢,减缓肝脏的代谢压力和脂质累积进而起到解酒护肝的作用。NOMURA Y等[19]在麻醉大鼠的胃中注射体积分数为5%乙醇协同冻干醋酸菌悬液发现醋酸菌协同组大鼠血中乙醇浓度低于对照组(P<0.05)。NISHIYAMA H等[34]研究发现,具有ADH 和ALDH 活性的醋酸菌粉末与乙醇同时摄入可降低人体呼气和血液中的乙醇浓度。
3.2 调节肝脏脂质代谢
该假说认为具有ADH和ALDH 活性的醋酸杆菌进入机体促进肝脏的乙醇和乙醛的代谢,调节了脂质代谢酶环境,减缓了NADH和乳酸对肝脏的损伤[40-45]。陈小雪等[46]探究不同剂量醋酸杆菌对急性酒精摄入小鼠肝损伤影响,发现15 mg/kg和45 mg/kg的醋酸菌粉末(人体等效剂量1.2 mg/kg和3.6 mg/kg醋酸杆菌)可有效降低肝脏甘油三酯(triglyceride,TG)和总胆固醇(total cholesterol,TC)含量并显著降低了转氨酶的含量。清野慧至等[17]通过14 dC57BL/6J小鼠摄入酒精协同醋酸杆菌实验发现,醋酸杆菌抑制了转氨酶的升高和脂质的堆积、改善肝脏纤维化,达到了解酒效果。
3.3 调节机体氧化应激
细菌蛋白表达的整体变化研究表明ALDH在暴露于环境和化学应激状态下表达会上调,这种上调是细菌的应激反应途径。亚砷酸盐(As3+)暴露通过破坏柠檬酸循环和释放未结合的Fe2+诱导氧化应激,然后通过芬顿反应诱导活性氧(reactive oxygen species,ROS)的产生[47]。假单胞菌暴露于亚砷酸盐会导致几种蛋白质的上调,包括预测的乙醛脱氢酶家族1P蛋白家族1(acetaldehyde dehydrogenase-protein family-1,ALDH1P1),当暴露于斑铜矿石(Cu5FeS4)时,硫杆菌上调未知的ALDH(ALD1Q1)(NCBI基因ID:198283897)[48]。田思敏等[49]研究发现,使用日本丘比株式会社“YOITOKI”醋酸杆菌胶囊(醋酸杆菌45 mg/胶囊,人体推荐量2粒/日)对急性酒精摄入小鼠氧化应激状态具有调节作用,显著提高了还原型谷胱甘肽的含量。JIANG X等[50]灌胃小鼠醋酸杆菌协同28%酒精发现显著降低了丙二醛(malondialdehyde,MDA)含量、提高了超氧化物歧化酶(superoxide dismutase,SOD)和谷胱甘肽转移酶的含量,改善了氧化应激水平。因此可以假设当酒精过度摄入引起机体氧化应激时,同时可以激活醋酸菌中的ALDH对氧化应激的应激反应,促进醛类物质的生成与代谢,协同达到保护肝脏的作用。
4 结论与展望
本文对醋酸杆菌生理代谢过程、解酒护肝疗效、解酒途径进行相关综述并对解酒机制进行归纳与总结。发现醋酸杆菌解酒护肝效果体现在醋酸杆菌中PQQ-ADH和ALDH酶及其显著的催化乙醇氧化作用中。醋酸菌科属种较多,其中醋酸杆菌属和葡糖醋酸杆菌属已有深入研究,无论是醋酸菌的培养基质、菌种贮藏还是剂型研究都较为完整,而对醋酸菌有氧代谢涉及的酶相关基因水平研究还不够透彻。对于醋酸杆菌解酒机制,主要是从乙醇脱氢酶与乙醛脱氢酶入手,虽然相关研究比较少,研究程度也比较浅,但是由于具体的分子机制牵涉广泛,还需要各方面专家学者联合研究以期找到醋酸杆菌解酒护肝是否通过脱氢酶作用机制,为临床指导安全用药及相关研究提供参考意义。
[1]FUKAMI H,KOBAYASHI S,TACHIMOTO H,et al.Effect of continuous ingestion of acetic acid bacteria on memory retention and the synaptic function in aged rats[J].Biosci Biotech Biochem,2010,74(7):1498-500.
[2] HAGHSHENAS B, NAMI Y, ABDULLAH N, et al. Potentially probiotic acetic acid bacteria isolation and identification from traditional dairies microbiota[J]. Int J Food Sci Technol,2015,50(4):1056-1064.
[3]HAGHSHENAS B,NAMI Y,ABDULLAH N,et al.Anticancer impacts of potentially probiotic acetic acid bacteria isolated from traditional dairy microbiota[J].LWT-Food Sci Technol,2015,60(2):690-697.
[4]INAGAWA H,NISHIZAWA T,KOCHI C,et al.Pollen allergy suppression effect by the oral administration of acetic acid bacteria (Gluconacetobacter hansenii)[J].Anticancer Res,2019,39(8):4511-4516.
[5]石庆叠,何星,卢红梅,等.赤水晒醋醋醅中醋酸菌的筛选和发酵特性研究[J].食品与发酵工业,2021,47(14):223-228.
[6] HOU X X, LIU H L, WEI S Z, et al. Roseomonas selenitidurans sp. nov.,isolated from urban soil,and emended description of Roseomonas frigidaquae[J].Int J Syst Evolut Microbiol,2020,70(11):5937-5942.
[7]JIN R,SU J,LIU H,et al.Description of Belnapia rosea sp.nov and emended description of the genus Belnapia [J].Int J Syst Evolut Microbiol,2012,62(3):705-709.
[8]NISHIJIMA M,TAZATO N,HANDA Y,et al.Gluconacetobacter tumulisoli sp.nov.,Gluconacetobacter takamatsuzukensis sp.nov and Gluconacetobacter aggeris sp.nov.,isolated from Takamatsuzuka Tumulus samples before and during the dismantling work in 2007[J].Int J Syst Evolut Microbiol,2013,63(11):3981-3988.
[9]孙大鹏,周伟平.乙醛脱氢酶2 与酒精性肝脏疾病的研究进展[J].腹部外科,2020,33(1):86-89.
[10]YAMADA Y,YUKPHAN P,MURAMATSU Y,et al.Subdivision of the genus Gluconacetobacter Yamada, Hoshino and Ishikawa 1998: the proposal of Komagatabacter gen. nov., for strains accommodated to the Gluconacetobacter xylinus group in the alpha-Proteobacteria[J].Ann Microbiol,2012,62(2):849-859.
[11]MALIMAS T,YUKPHAN P,TAKAHASHI M,et al.Asaia lannaensis sp.nov., a new acetic acid bacterium in the Alphaproteobacteria[J].Biosci Biotechn Biochem,2008,72(3):666-671.
[12]NOH H J.Lichenicola cladoniae gen.nov.,sp.nov.,a member of the family Acetobacteraceae isolated from an Antarctic lichen[J]. Int J Syst Evolut Microbiol,2020,70(11):5918-5925.
[13] DE ROOS J, DE VUYST L. Acetic acid bacteria in fermented foods and beverages[J].Curr Opin Biotechnol,2018,49(1):115-119.
[14]GOMES R J,BORGES M F,ROSA M F,et al.Acetic acid bacteria in the food industry:systematics,characteristics and applications[J].Food Technol Biotechnol,2018,56(2):139-151.
[15] KAO L, LIU T H, TSAI T Y, et al. Beneficial effects of the commercial lactic acid bacteria product, Vigiis 101, on gastric mucosa and intestinal bacterial flora in rats[J].J Microbiol Immunol Infect,2020,53(2):266-273.
[16] LEBLANC J G, CHAIN F, MARTIN R, et al. Beneficial effects on host energy metabolism of short-chain fatty acids and vitamins produced by commensal and probiotic bacteria[J].Microbial Cell Factor,2017,16(1):79.
[17]清野慧至,栗原仁,松冈亮辅,等.醋酸菌对C57BL/6J 小鼠的酒精性肝损伤的影响研究[J].中国酿造,2018,37(8):28-31
[18] NAKAMURA S, MITSUNAGA F. Anti-Allergic effect of para-probiotics from non-viable acetic acid bacteria in ovalbumin-sensitized mice[J].Food Nutr Sci,2018,9(12):1376-1385.
[19]NOMURA Y,YAMAMOTO M,FUSHIKI T.Effect of acetic acid bacterium on ethanol oxidation in vivo[J]. Biosci Biotechn Biochem, 1997, 61(2):365-366.
[20]SAICHANA N,MATSUSHITA K,ADACHI O,et al.Acetic acid bacteria:A group of bacteria with versatile biotechnological applications[J].Biotechnol Adv,2015,33(6):1260-1271.
[21] LYNCH K M, ZANNINI E, WILKINSON S, et al. Physiology of acetic acid bacteria and their role in vinegar and fermented beverages[J].Compreh Rev Food Sci Food Safety,2019,18(3):587-625.
[22]SENGUN I Y,KARABIYIKLI S.Importance of acetic acid bacteria in food industry[J].Food Control,2011,22(5):647-656.
[23]SINGH S,BROCKER C,KOPPAKA V,et al.Aldehyde dehydrogenases in cellular responses to oxidative/electrophilic stress[J].Free Rad Biol Med,2013,56(1):89-101.
[24]阳飞,覃凌云,张华山,等.醋酸菌分类及其应用研究进展[J].中国调味品,2015,40(10):112.
[25] VACCHINI V, GONELLA E, CROTTI E, et al. Bacterial diversity shift determined by different diets in the gut of the spotted wing fly Drosophila suzukii is primarily reflected on acetic acid bacteria[J].Environ Microbiol Report,2017,9(2):91-103.
[26] GAO L, WU X, ZHU C, et al. Metabolic engineering to improve the biomanufacturing efficiency of acetic acid bacteria:advances and prospects[J].Crit Rev Biotechnol,2020,40(4):522-538.
[27]GULLO M,LA CHINA S,FALCONE P M,et al.Biotechnological production of cellulose by acetic acid bacteria: current state and perspectives[J].Appl Microbiol Biotechn,2018,102(16):6885-6898.
[28] MATSUTANI M, YAKUSHI T. Pyrroloquinoline quinone-dependent dehydrogenases of acetic acid bacteria[J]. Appl Microbiol Biotechn, 2018,102(22):9531-9540.
[29]冯静,施庆珊,欧阳友生,等.醋酸菌多相分类研究进展[J].微生物学通报,2009,36(9):1390-1396.
[30] AMANO S, INAGAWA H, NAKATA Y, et al. Oral administration of lipopolysaccharide of acetic acid bacteria protects pollen allergy in a murine model[J].Anticancer Res,2015,35(8):4509-4514.
[31]CLEENWERCK I,VOS P D.Polyphasic taxonomy of acetic acid bacteria:an overview of the currently applied methodology[J]. Int J Food Microbiol,2008,125(1):2-14.
[32] GULLO M, VERZELLONI E, CANONICO M. Aerobic submerged fermentation by acetic acid bacteria for vinegar production: Process and biotechnological aspects[J].Process Biochem,2014,49(10):1571-1579.
[33]尹良爽,庞良俊,朱文礼.饮酒相关遗传及基因研究进展[J].安徽医学,2018,39(6):764-766.
[34] NISHIYAMA H, WATANABE S, OKUYAMA Y, et al. Effect of acetic acid bacteria containing food on ethanol concentration in expiration and blood while healthy adult males drinking[J]. J New Remed Clin, 2017,66(3):250-258.
[35]管咏梅,许攀,沈倩,等.葛根解酒的研究进展[J].中国实验方剂学杂志,2021,27(2):210-217.
[36] RAMIREZ-BAHENA M, TEJEDOR C, MARTIN I, et al. Endobacter medicaginis gen. nov., sp nov., isolated from alfalfa nodules in an acidic soil[J].Int J Syst Evolut Microbiol,2013,63(5):1760-1765.
[37]TSUCHIYA Y,BAN M,KISHI M,et al.Safety and efficacy of oral intake of ceramide-containing acetic acid bacteria for improving the stratum corneum hydration: A randomized, double-blind, placebo-controlled study over 12 weeks[J].J Oleo Sci,2020,69(11):1497-1508.
[38] QIU X, ZHANG Y, HONG H. Classification of acetic acid bacteria and their acid resistant mechanism[J].AMB Express,2021,11(1):1-15.
[39] WU J J, MA Y K, ZHANG F F, et al. Biodiversity of yeasts, lactic acid bacteria and acetic acid bacteria in the fermentation of"Shanxi aged vinegar",a traditional Chinese vinegar[J].Food Microbiol,2012,30(1):289-297.
[40] CUI M, ZHANG M, WU J, et al. Marine polysaccharides from Gelidium pacificum Okamura and Cereus sinensis reveal prebiotic functions[J].Int J Biol Macromol,2020,164(1):4381-90.
[41]QI Y,CHEN L,GAO K,et al.Effects of Schisandra chinensis polysaccharides on rats with antibiotic-associated diarrhea[J].Int J Biol Macromol,2019,124(1):627-634.
[42]SONG M,ZENG J,JIA T,et al.Effects of sialylated lactulose on the mouse intestinal microbiome using Illumina high-throughput sequencing[J].Appl Microbiol Biotechn,2019,103(21-22):9067-9076.
[43]ZENG J,SONG M,JIA T,et al.Immunomodulatory influences of sialylated lactuloses in mice[J].Biochem Biophys Res Commun,2019,514(2):351-357.
[44] PELUZIO M D C G, MARTINEZ J A, MILAGRO F I. Postbiotics:Metabolites and mechanisms involved in microbiota-host interactions[J].Trend Food Sci Technol,2021,108(1):11-26.
[45]姜欣欣.木葡糖醋杆菌对酒精肝损伤的保护作用及机制研究[D].西安:陕西师范大学,2019.
[46]陈小雪,田思敏,程永强.含醋酸菌粉末的食品对ICR 小鼠的酒精性肝损伤的影响[J].食品与发酵工业,2020,46(13):114-118.
[47] PARVATIYAR K, ALSABBAGH E M, OCHSNER U A, et al. Global analysis of cellular factors and responses involved in Pseudomonas aeruginosa resistance to arsenite[J].J Bacteriol,2005,187(14):4853-4864.
[48]FERRAZ L F,VERDE L C,VICENTINI R,et al.Ferric iron uptake genes are differentially expressed in the presence of copper sulfides in Acidithiobacillus ferrooxidans strain LR[J].Anton Leeuw,2011,99(3):609-617.
[49]田思敏,陈小雪,韩北忠.醋酸菌粉末对ICR 小鼠的酒精性肝脂质蓄积和氧化应激的影响研究[J].中国酿造,2020,39(4):28-31.
[50] JIANG X, LIN D, SHAO H, et al. Antioxidant properties of Komagataeibacter hansenii CGMCC 3917 and its ameliorative effects on alcoholinduced liver injury in mice[J].CyTA-J Food,2019,17(1):355-364.
