中国白酒的特点为制曲酿酒,自古就有“曲乃酒之骨”之说[1]。中国白酒制曲历史十分悠久,《书经·说命篇》记载:“若作酒醴,尔惟曲蘖”,曲蘖即是我国最原始的酒曲,可以说是酒曲的起源,大曲是重要的微生物群落载体,综合物系、酶系、菌系于一体[2-3]。清香型大曲根据其生产工艺可定义为中低温大曲,其中包含霉菌、酵母菌、细菌等各类微生物,在白酒酿造过程中起糖化、发酵、酯化等作用[4-5]。其中,清香型大曲的酯化作用体现在大曲中酯化酶在白酒酿造过程中催化各种有机酸与乙醇结合、脱水生成相应的酯类化合物[6],酯类物质在清香型白酒中具有增加白酒香气、柔和度、醇厚度等作用,是影响白酒品质的重要因素,因此,大曲的酯化力水平即成为判断大曲质量的重要指标之一[7-8]。
沈才洪等[9]经实验研究认为,大曲酯化力是指制曲过程中大曲微生物所代谢的酯化酶催化酸醇合成乙酯类物质的能力,其中曲块曲心部位表现出酯化力显著大于曲皮部位。汤有宏等[10]根据酯化酶特性从酯化温度、酯化时间、加曲量、底物浓度角度研究并确定了测定浓香型大曲酯化力的最佳条件。倪雪[11]分别用总酯法和色谱分析法对凤香型大曲酯化力进行测定,经过反复实验,最终确定了数据准确、操作简易、适合凤香型大曲酯化力的检测方法。
轻工行业标准QB/T 4257—2011《酿酒大曲通用分析方法》中规定,在规定的试验条件下,大曲中酯化酶催化游离有机酸与乙醇合成酯,再用皂化法测定所生成的总酯(以己酸乙酯计),表示其酯化力[12]。该标准分析方法中以己酸与乙醇为主要反应试剂,进行酯化反应,并最终测定总酯(以己酸乙酯计)含量。而清香型白酒中酯类化合物以乙酸乙酯为主,己酸乙酯反而成为清香型白酒中的“杂质”成分,是不允许出现的[13-14]。清香型大曲中的酯化酶主要为催化合成乙酸乙酯的酶类[15]。根据前期实验研究发现,大曲中催化合成己酸乙酯的酯化酶与催化合成乙酸乙酯的酯化酶通常并非同一种酶类。因此清香型大曲酯化力的测定,应以其中的酶类催化合成乙酸乙酯的能力进行衡量更为准确。
本研究以清香型大曲为催化剂,以乙酸、乙醇为主要反应试剂,对影响酯化反应的不同条件进行试验、分析,并最终确定了适合清香型大曲酯化力测定的最优方法。酯化力是衡量清香型酿酒大曲质量优劣的关键性指标之一,研究并确定适宜清香型大曲的酯化力测定方法具有十分重要的现实意义,该方法的确定能够更好的应用于生产实践,更为准确的对大曲质量做出判定,能够指导大曲生产的顺利进行,从而对清香型白酒生产具有积极的促进作用。
1 材料与方法
1.1 材料与试剂
清香型白酒大曲HX-1:北京红星股份有限公司;不同批次清香型白酒大曲L-1、L-2:山西兰花青酒业有限公司;不同批次清香型白酒大曲Z-1、Z-2:山西宗酒酒业有限公司。
乙酸、无水乙醇、氢氧化钠、硫酸(均为分析纯):北京化工厂。
1.2 仪器与设备
LA230S电子天平:德国赛多利斯公司;DHP-9272电热恒温培养箱、DHG-9245A电热鼓风干燥箱:上海一恒科学仪器有限公司;Q10A电陶炉:广东新功电器有限公司;DZKW-4电子恒温水浴锅:北京中兴伟业仪器有限公司。
1.3 试验方法
1.3.1 大曲酯化力测定方法
制备酯化样品:于250 mL锥形瓶中加入25.0 mL无水乙醇,再加入75 mL蒸馏水,稍微振荡后,再分别加入不同体积乙酸,充分混匀。再称取相当于绝干HX-1大曲样品质量25.00 g,精确至0.01 g,加入锥形瓶中,摇匀后用塞子塞上,置于不同温度恒温培养箱内保温酯化。同时以不添加大曲样品酯化反应液作为空白对照试验。
其他操作及结果计算均按照QB/T 4257—2011《酿酒大曲通用分析方法》规定方法[12]执行。酯化力单位定义:每50 g大曲在一定温度下,经过一定时间催化有机酸和乙醇合成有机酸乙酯的毫克数为一个单位,符号为U,以mg/50 g表示。
1.3.2 测定条件优化单因素试验
分别向100 mL酯化反应体系中加入不同体积(0.6 mL、0.8 mL、1.0 mL、1.2 mL、1.5 mL)乙酸,将锥形瓶置于不同温度(28 ℃、30 ℃、32 ℃、35 ℃、37 ℃)恒温培养箱内,保温酯化不同时间(4 d、5 d、6 d、7 d、8 d),酯化反应结束后,测定并计算大曲试样的酯化力。
1.3.3 测定条件优化正交试验
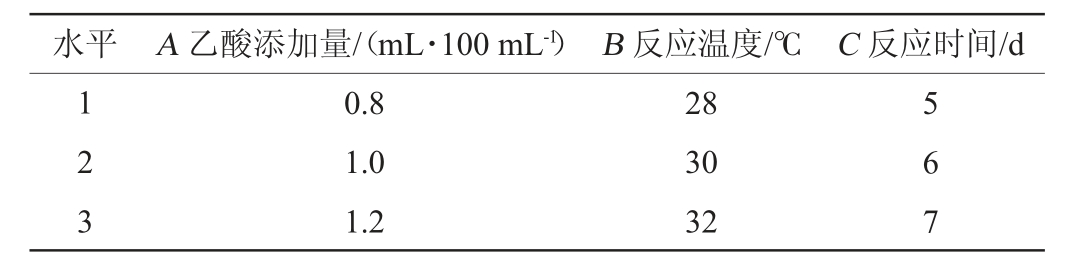
以乙酸添加量、反应温度、反应时间为评价因素,以酯化力为评价指标,对酯化反应条件采用L9(34)正交试验进行优化,试验因素与水平见表1。
表1 测定条件优化正交试验因素与水平
Table 1 Factors and levels of orthogonal experiments for determination conditions optimization
1.3.4 方法精密度考察
取同一大曲粉样品充分混合均匀后,均分为6份,分别按照优化后实验方法检测各份样品的酯化力,计算结果相对标准偏差(relative standard deviation,RSD)。
1.3.5 数据分析
试验操作均重复3次,进行正交试验及方差分析,确定数据差异的显著性(P<0.05)。
2 结果与分析
2.1 不同底物添加量对测定结果的影响
分别向100 mL酯化反应体系中加入不同体积乙酸,将锥形瓶置于35 ℃恒温培养箱内,保温酯化7 d,测定并计算大曲试样的酯化力,结果见图1。
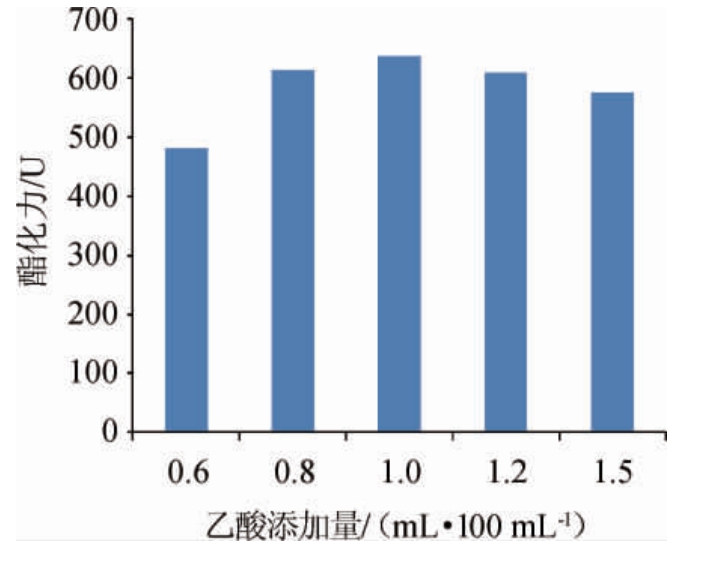
图1 不同乙酸添加量对测定结果的影响
Fig.1 Effect of different acetic acid addition on detection result
由图1可知,当乙酸添加量由0.6 mL/100 mL增加至0.8 mL/100 mL时,所测得大曲酯化力升高,继续增加乙酸添加量,则酯化力无明显升高迹象。向100 mL反应体系中加入乙酸量为0.6 mL/100 mL时,测得大曲酯化力结果明显低于其他,分析原因为反应体系中乙酸量不足导致,当增加乙酸添加量至0.8~1.5 mL/100 mL时,酯化力测定结果相差较小,说明反应体系中底物已充足,可满足酯化反应充分进行。因此,确定最佳乙酸添加量为0.8~1.2 mL/100 mL。
2.2 不同反应温度对测定结果的影响
向100 mL酯化反应体系中加入1.2 mL乙酸,分别将锥形瓶置于不同温度条件下,保温酯化7 d,测定并计算大曲试样的酯化力,结果见图2。
由图2可知,随着反应温度升高,所测得大曲酯化力随之升高,当反应温度高于32 ℃时,继续升高反应温度,所测酯化力反而逐渐降低。酯化反应温度为28 ℃时所测大曲酯化力略低,而35 ℃以上反应温度测得大曲酯化力更低,说明酯化反应温度过高、过低均不利于清香型大曲中酯化酶催化合成乙酸乙酯,温度过低时酯化反应进行缓慢,温度过高则易导致酯化酶活力降低,甚至失活。30 ℃与32 ℃条件下测得大曲酯化力结果较高,大曲中酯化酶充分发挥作用。因此,确定30 ℃为酯化酶最适催化温度。
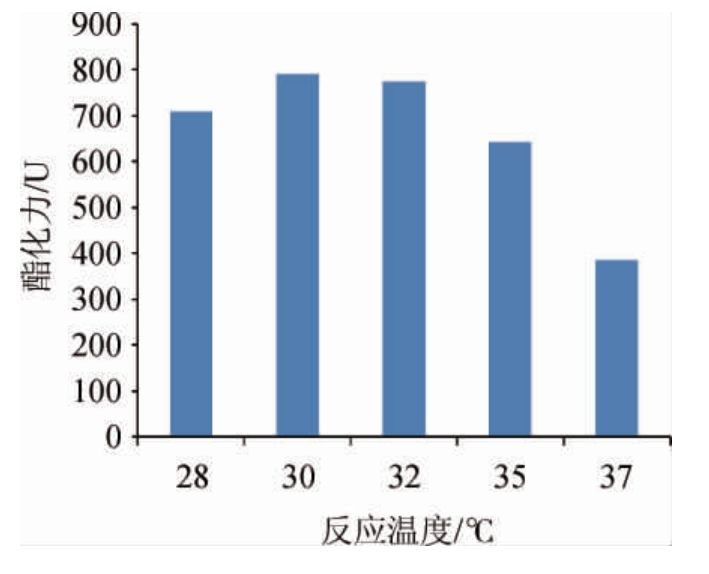
图2 不同酯化温度对测定结果的影响
Fig.2 Effect of different esterification temperature on detection result
2.3 不同反应时间对测定结果的影响
向100 mL酯化反应体系中加入1.2 mL乙酸,将锥形瓶置于32 ℃恒温培养箱内,分别保温酯化不同时间,测定并计算大曲试样的酯化力,结果见图3。
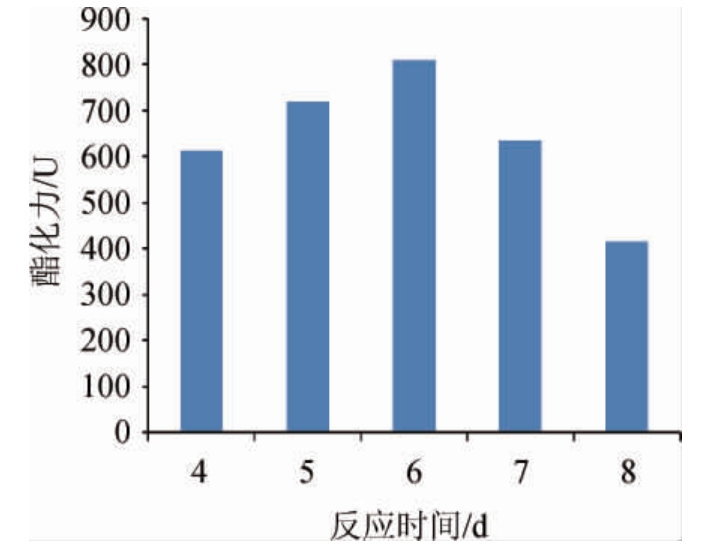
图3 不同酯化时间对测定结果的影响
Fig.3 Effect of different esterification time on detection result
由图3可知,酯化反应初始,随着反应时间在4~6 d范围内延长,大曲酯化力增加,当反应时间至6 d时,酯化反应得以充分进行,酯化力达到最高,继续延长反应时间,所测得大曲酯化力降低。据相关研究表明,酯化过程存在可逆性,酯化酶既可以催化酯类的合成,也可以分解已经形成的酯类物质[16],故酯化反应时间并非越长越好,应在酯类合成量达到最高时及时终止反应,避免由于酯类分解导致测量误差。因此,选择6 d为最佳酯化反应时间。
2.4 正交试验分析
为得出最优试验条件,在单因素试验的基础上对乙酸添加量、反应温度、反应时间进行正交试验分析,正交试验结果及分析见表2。
表2 测定条件优化正交试验结果与分析
Table 2 Results and analysis of orthogonal experiments for determination conditions optimization
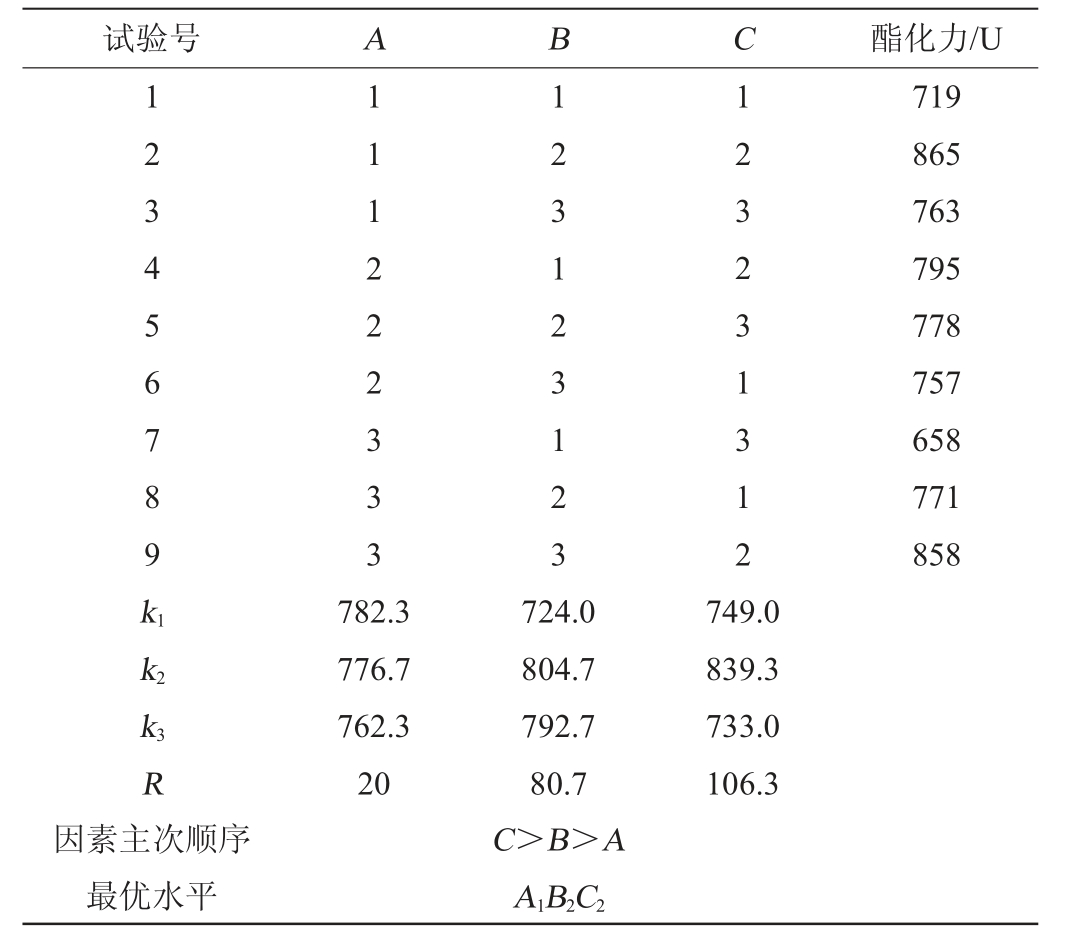
根据极差分析结果可知,清香型大曲酯化最佳测定反应条件组合为A1B2C2,即向100 mL反应体系中加入0.8 mL分析纯乙酸,将锥形瓶置于30 ℃条件下保温酯化6 d。根据方差分析(表3)可知,反应时间对酯化力测定具有显著影响(P<0.05),而乙酸添加量及反应温度对酯化力影响不显著。
表3 测定条件优化正交试验结果方差分析
Table 3 Variance analysis of the orthogonal experiments results for determination conditions optimization
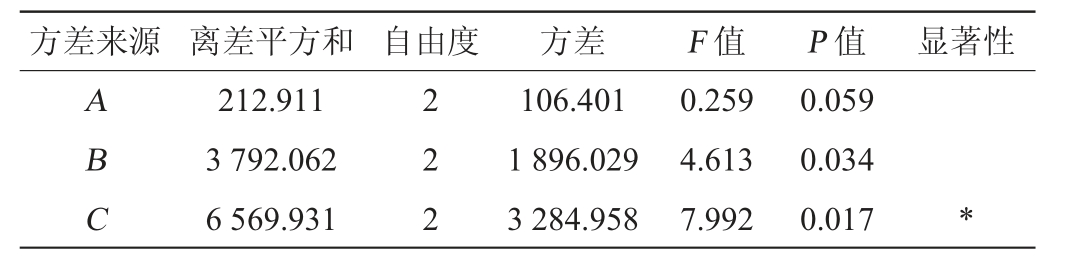
注:“*”表示影响显著(P<0.05)。
以最佳测定条件进行验证试验,测得清香型大曲酯化力为898 U。本方法优化后的酯化反应体系为酯化过程提供充足的反应底物、最适宜酯化温度及酯化时间,酯化反应足够彻底,所测定大曲酯化力达到试验中最高水平。
2.5 方法精密度考察
取同一大曲粉样品充分混合均匀后,均分为6份,分别按照优化后实验方法检测各份样品的酯化力,检测结果并计算相对标准偏差(RSD),结果如表4所示。
表4 酯化力检测方法的相对标准偏差
Table 4 Relative standard deviation of the determination method for the esterification ability

经测定,本试验方法的相对标准偏差为3.1%,符合标准QB/T 4257—2011《酿酒大曲通用分析方法》要求(不超过10%)。
2.6 清香型大曲酯化力分析
应用以上酯化力检测方法对不同来源的清香型大曲进行检测,结果见图4。
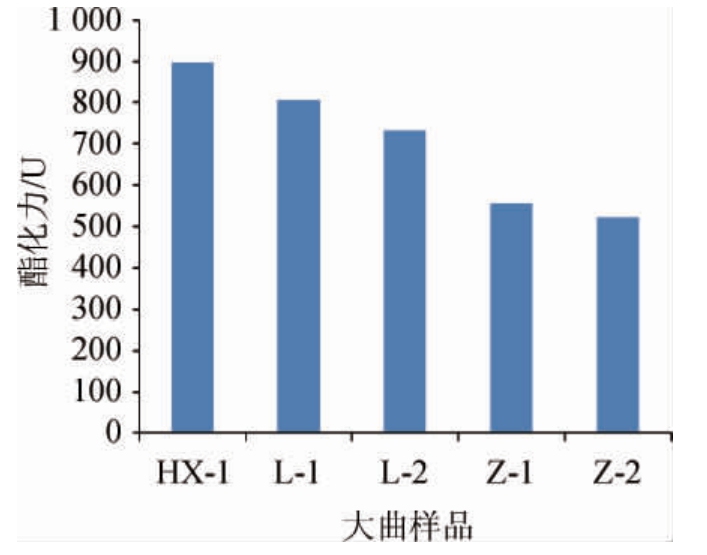
图4 不同清香型大曲酯化力检测结果
Fig.4 Esterification determination results of different light-flavor Baijiu Daqu
由图4可知,红星二锅头清香型大曲酯化力为898 U,与不同来源大曲酯化力差异明显,主要原因为制曲工艺不同导致大曲酯化力不同。
大曲酯化力与制曲工艺及制曲环境因素密切相关,根据清香型大曲制曲工艺不同,可分为清茬曲、红心曲和后火曲[18-19]。三种大曲曲坯相同,主要差异为制曲过程工艺条件控制不同[20]。其中,后火曲在潮火期、干火期、后火期等各个阶段曲块温度均高于清茬曲;而红心曲在整个制曲培养过程中持续保持曲块品温上升,升温时间长,降温幅度小[21-22]。清香型大曲培养过程的实质即是通过对培养环境温度、氧气、水分的调节控制从而达到对大曲块中微生物种类及数量的选择。在培养过程中,扩大大曲中有益微生物的种群、数量,淘汰不利微生物,使曲块更有利于白酒酿造过程的进行[23-24]。
经相关研究表明,清茬曲酯化力水平较高,明显高于红心曲和后火曲[25]。主要原因为不同制曲环境与制曲工艺导致大曲中微生物菌群组成结构存在较大差异性,清茬曲中含有丰富的酵母菌属、霉菌属等产酯化酶类微生物,更有利于提高大曲整体酯化力水平[26-27]。
3 结论
本研究依据标准QB/T 4257—2011《酿酒大曲通用分析方法》中规定的大曲检测方法,根据清香型大曲的特殊性质,通过实验进一步对清香型大曲酯化力测定过程中酯化反应底物及酯化反应条件做出了分析优化。最终确定以乙酸代替标准中规定的己酸,乙酸添加量为0.8 mL/100 mL,酯化反应温度为30 ℃,酯化反应时间为6 d。在此反应条件下可使清香型大曲中的酯化酶充分发挥催化作用,得出更为接近真实值的酯化力结果。
经过近两年的检测应用实践,应用本方法测定的清香型大曲酯化力,能更为科学、客观的反映出清香型大曲中酯化酶催化合成乙酸乙酯的能力,为进一步研究清香型大曲提供了可行途径,对清香型白酒质量控制及提升具有重要意义。
[1]路星,相里加雄.汾酒大曲与普通清香型大曲酿酒性能对比[J].酿酒,2014,41(4):53-57.
[2]傅金泉.《天工开物·曲糵》读后感[J].酿酒科技,2015(11):142-145.
[3]栾春光,郝建国,江伟,等.不同工艺清香型大曲理化指标差异与微生物菌群结构的相关性研究[J].酿酒,2021,48(1):43-48.
[4]徐秋硕,陈亚祥,石凤,等.不同大曲对清香基酒产质量影响的研究[J].酿酒,2021,48(1):116-119.
[5]乔晓梅.清香大曲糖化力酯化力功能及真菌群落结构分析[D].临汾:山西师范大学,2015.
[6]徐希望,王剑芳,夏培禹,等.大曲酯化力的测定方法探讨[J].酿酒,2005,32(6):69-70.
[7]刘小改,马美荣,周林艳,等.高产乙酸乙酯酵母菌筛选及固态发酵应用研究[J].中国酿造,2020,39(10):79-83.
[8]樊文毅.论清香型大曲酒的质量控制[J].山西食品工业,1994(4):30-32.
[9]沈才洪,应鸿,许德富,等.大曲酯化力的探讨[J].酿酒科技,2005(3):17-20.
[10]汤有宏,王志强,唐林,等.大曲酯化力测定参数的探讨与优化[J].酿酒,2015,42(5):54-57.
[11]倪雪.凤香型大曲酯化力的测定方法探讨[J].酿酒,2015,42(3):70-72.
[12]中华人民共和国工业和信息化部.QB/T 4257—2011 酿酒大曲通用分析方法[S].北京:中国标准出版社,2011.
[13]程伟,彭兵,汪焰胜,等.清香型酒醅中一株产乙酸乙酯酵母菌的筛选及其应用性能分析[J].酿酒,2018,45(5):43-47.
[14]刘阳,薛正莲,黄祖耀,等.中高温大曲中产酯酶细菌的筛选[J].中国酿造,2012,31(8):99-102.
[15]唐取来,李晶晶,郭学武,等.清香型大曲酯化酶活力的研究[J].中国酿造,2017,36(1):35-38.
[16]范光森,吴秋华,刘朋肖,等.脂肪酶在白酒酯类化合物合成中的作用研究进展[J].中国食品学报,2021,21(1):351-360.
[17]臧青民,马春兰,王端,等.正交设计优化超声波辅助提取广西犁头草中总黄酮的工艺[J].广州化工,2021,49(8):74-77.
[18]张敏,张锦华.清香型白酒酒曲中核心真菌发酵特性的研究[J].酿酒科技,2020(3):17-23.
[19]马茹菲,马玉帛,佟世生,等.不同清香型大曲理化生化指标和挥发性成分分析[J].酿酒科技,2019(3):70-75.
[20]李增胜.汾酒大曲生产发展史[J].酿酒科技,2005(2):85-86.
[21]赵景龙.浅谈清香型酒三种大曲的差异性[J].酿酒,2000(5):43-44.
[22]熊子书.中国三大香型白酒的研究(三)清香·杏花村篇[J].酿酒科技,2005(7):17-21.
[23]叶光斌,王彩虹,王毅,等.清香型大曲细菌群落结构的比较分析[J].食品与机械,2015,31(3):11-15.
[24]李奇,相里加雄.汾酒三种大曲酿酒性能对比分析[J].酿酒科技,2011(4):63-64.
[25]栾春光,郝建国,江伟,等.不同工艺清香型大曲理化指标差异与微生物菌群结构的相关性研究[J].酿酒,2021,48(2):43-48.
[26]范文来,徐岩.大曲酶系研究的回顾与展望[J].酿酒,2000(3):35-40.
[27]乔晓梅.清香大曲糖化力酯化力功能及真菌群落结构分析[D].临汾:山西师范大学,2015.