玛咖(Lepidium meyenii Walp.)为十字花科独行菜属一年生或两年生草本植物,原产于高海拔南美安第斯山地区,我国自20世纪初引种,在云南、西藏、新疆和四川等地种植,2011年被中国卫生部批准为新食品原料[1-3]。目前以玛咖作为原料已经开发生产了47种保健食品,其中与中药配伍的有27种,同时还有多项专利对玛咖进行研究[4]。而玛咖作为配制酒原料也已得到普遍应用。玛咖中的化学物质如氨基酸[5-6]、玛咖酰胺和玛咖烯类[7]、芥子油苷和异硫氰酸酯类[8]、生物碱[9]、黄酮[10]等都已有相应的研究进展。玛咖中含有丰富的皂苷类物质,是有效的活性成分之一,作为配制酒中的原材料应用愈加广泛。玛咖中含有丰富的皂苷类物质,是有效的活性成分之一,作为配制酒中的原材料应用愈加广泛。
皂苷类物质研究方法多为高效液相色谱法及高效液相色谱质谱法[11-20],但目前针对玛咖及其配制酒中总皂苷含量测定的研究较少,不能有效的表征该类产品中总皂苷的含量水平。现有的测定总皂苷标准方法有4项[21-24],其中保健食品中总皂苷的检测方法主要为《保健食品理化及卫生指标检验与评价技术指导原则(2020年版)》,采用Amberlite-XAD-2大孔树脂(或D-101大孔树脂)纯化样品总皂苷[23];普通食品多引用T/AHFIA 004—2018《食品中总皂苷含量的测定分光光度法》,采用XAD-2大孔树脂分离纯化[24]。比较已有的方法可以看出,总皂苷的纯化分离均使用树脂填充柱,在检测过程中由于手工填柱导致可重现性和准确度均偏低,操作时间偏长。因此本实验拟采用SPEC18柱作为固相萃取方式进行玛咖酒中总皂苷的纯化分离,通过方法确认来考察该方法的可行性。以期建立一种准确性、重复性高,操作性强的玛咖酒试样中总皂苷检测方法。
1 材料与方法
1.1 材料与试剂
玛咖酒(52% vol):泸州老窖养生酒业有限责任公司;人参皂苷Re标准品(纯度>98%):中国药品生物制品检定所;Amberlite-XAD-2大孔树脂:美国Sigma化学公司;D101大孔吸附树脂:成都市科龙化工试剂厂;甲醇(色谱纯):美国Thermo Fisher公司;中性氧化铝(100~200目)、乙醇、香草醛、冰乙酸、高氯酸等(均为分析纯):国药集团化学试剂有限公司;试验用水均为一级水。
1.2 仪器与设备
U-3900紫外可见分光光度计:日本HITACHI公司;MPEva GS平行浓缩仪:睿莱博仪器(广州)有限公司;CPA225D电子天平:德国赛多利斯公司;SPE-12固相萃取装置:上海安谱科学仪器有限公司;SPEC18柱(500 mg填料,3 mL):天津博纳艾杰尔科技有限公司。
1.3 方法
1.3.1 人参皂苷标准储备溶液溶液配制
称取人参皂苷Re标准品10.0 mg于10 mL容量瓶中,用甲醇溶解并定容。
1.3.2 最大吸收波长测定及标准曲线绘制
分别取0、0.05mL、0.075mL、0.100mL、0.150mL、0.175mL、0.200 mL人参皂苷Re标准溶液于10 mL比色管中,60 ℃氮吹至干。加0.2 mL 5%香草醛冰醋酸溶液,0.8 mL高氯酸后于60 ℃水浴中保温10 min,自来水冷却后加入5 mL冰乙酸,混匀后以试剂空白为参比,用系列标准溶液全波段扫描确定最大吸收波长后,测定系列标准溶液吸光度值。以人参皂苷Re质量浓度(C)为横坐标,吸光度值(A)为纵坐标,绘制标准曲线。
1.3.3 大孔树脂填充柱及SPEC18柱预处理
大孔树脂填充柱:取适量Amberlite-XAD-2大孔树脂和D101大孔吸附树脂适量于烧杯中,使用无水乙醇浸泡(覆盖树脂2.5~5.0 cm),缓慢搅拌树脂1 min以充分混合,静置2 h。倒出乙醇,用一级水冲洗,直至无醇味。然后再用等量的无水乙醇洗涤,充分混合静置20 min,再用一级水洗至无醇味,备用。用10 mL玻璃注射器作层析管,分别装入柱高3 cm预处理过的D101大孔吸附树脂和Amberlite-XAD-2大孔树脂,用一级水洗至无醇味后,加入柱高1 cm中性氧化铝。先用25 mL体积分数70%的乙醇洗柱,再用25 mL水洗柱,弃去洗脱液,待上样。
SPEC18柱:取20 mL一级水淋洗SPEC18柱,然后用20 mL甲醇进行活化,再用20 mL一级水平衡,待水与柱筛板近平时上样。
1.3.4 大孔树脂填充柱及SPEC18柱分离能力比较
取玛咖酒试样20 mL于50 mL蒸发皿中,60 ℃水浴上挥干,5 mL水溶解后洗脱至10 mL容量瓶中,定容为样品提取液。
树脂填充柱分离:取样品提取液2 mL注入填充柱中保留20 min,先用25 mL水洗柱,控制流速1.5~2.0 mL/min,弃去洗脱液,再用25 mL体积分数70%的乙醇洗脱,控制流速1.5~2.0 mL/min,收集洗脱液于蒸发皿中,60 ℃水浴挥干,测定(同1.3.2中标准溶液测定方法)。
SPEC18柱分离:取样品提取液2 mL注入预先处理的SPEC18柱中,保留20 min后控制流速在1滴/s流出,待测液与柱筛板近平时加入10 mL水淋洗SPEC18柱,弃去流出液。加入6 mL体积分数70%的乙醇洗脱SPEC18柱,收集洗脱液于蒸发皿中,60 ℃水浴挥干,测定(同1.3.2中标准溶液测定方法)。
1.3.5 检测方法优化及确认
洗脱液浓度对皂苷含量影响:分别取6组提取液2 mL注入预先处理的SPEC18柱中,保留20 min后控制流速在1滴/s流出,待测液与柱筛板近平时加入10 mL水淋洗SPEC18柱,弃去流出液。分别加入6 mL体积分数为70%、75%、80%、85%、90%、95%的乙醇洗脱SPEC18柱,收集洗脱液于蒸发皿中,60 ℃水浴挥干,测定(同1.3.2中标准溶液测定方法)。
方法检出限:参考GB/T 27417—2017《合格评定化学分析方法确认和验证指南》中检出限目视评价法[25]。以52% vol的浓香型白酒为空白基质添加已知浓度的标准品溶液,配制成5个质量浓度梯度(5.5mg/L、5.0mg/L、4.5mg/L、4.0mg/L、3.0 mg/L)的人参皂苷Re溶液,进行检测,每个浓度的平行测试次数7次。以正好不能检出目标组分的浓度为参考,将其上一个正好能被检出的浓度作为检出限参考值。计算该浓度下7组测定值平均值m¯及总标准偏差S,检出限即为m¯+3S。
方法正确度:以52% vol的浓香型白酒为空白基质,配制成人参皂苷Re质量浓度分别为5 mg/L、15 mg/L、50 mg/L。分别取上述6组溶液20 mL于水浴锅60 ℃挥干,5 mL水溶解后洗脱至10 mL容量瓶中定容。取2 mL提取液于已预处理的SPEC18柱保留20 min后控制流速在1滴/秒流出,待测液与柱筛板近平时加入10 mL一级水淋洗SPEC18柱,弃去流出液。加入6 mL(95%)乙醇洗脱SPEC18柱,收集洗脱液于10 mL比色管中,60 ℃氮吹至干,显色测定。以平行试验的均值与加入浓度后测定值比较。
方法精密度:分别取6组玛咖酒样各20 mL,60 ℃水浴挥干,用5 mL水溶解后洗脱至10 mL容量瓶中定容。于SPEC18柱净化后60 ℃氮吹至干(同正确度实验方法),显色测定。计算相对标准偏差(relative standard deviation,RSD)(n=6)。
方法加标回收率:分别取3组玛咖酒样各20 mL,每组加标量的质量浓度分别为5 mg/L、10 mg/L、25 mg/L,于水浴锅60 ℃挥干,5 mL水溶解后洗脱至10 mL容量瓶中定容。SPEC18柱净化后测定(同正确度实验方法)。其回收率计算方式为回收率=(标准加入测定值-本底值)/标准加入值×100%。
2 结果与分析
2.1 最大吸收波长及标准曲线
按照1.3.2方法进行试验,通过全波段扫描该方法最大吸收波长为560 nm,绘制标准曲线见图1。由图1可知,以人参皂苷Re质量浓度(C)为横坐标,吸光度值(A)为纵坐标绘制标准曲线,得到线性回归方程A=4.457 2C-0.0.052 0(R2=0.990 1),线性范围0~0.20 mg/mL。
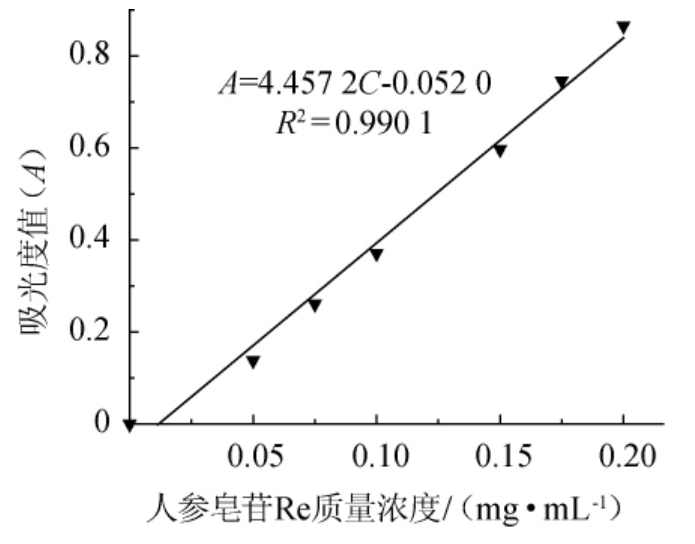
图1 人参皂苷Re的标准曲线
Fig.1 Standard curve of ginsenoside Re
2.2 树脂填充柱和SPEC18柱测定结果比较
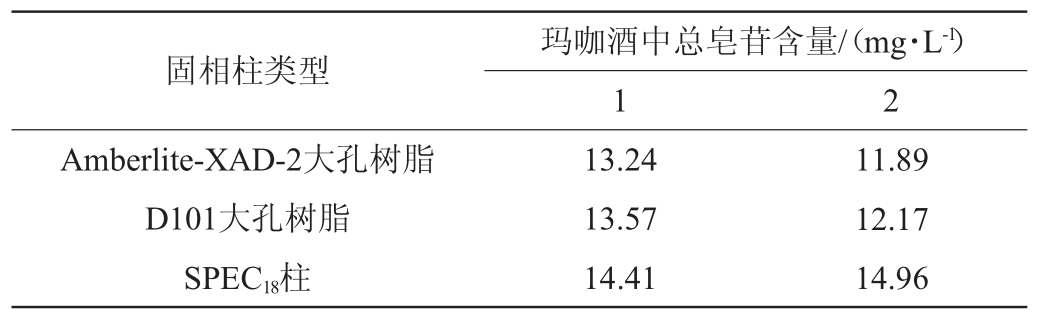
按照1.3.4的方法进行两次平行试验,比较不同方式固相萃取纯化分离总皂苷的差异,结果见表1。由表1可知,填充柱测定值结果相对偏小且相对标准偏差大于10%,而SPEC18柱结果值稳定且纯化分离结果较好。同时在试验过程中发现填充柱容易出现柱塌陷,流速难以控制,不同批次之间回收结果差异大。因此选用SPEC18柱作为固相萃取纯化柱具有良好的实用性和高效性。
表1 树脂填充柱和SPEC18柱总皂苷测定结果比较
Table 1 Comparison of total saponins determination results between resin packed column and SPEC18 column
2.3 检测方法优化及确认结果
2.3.1 洗脱液浓度对检测结果的影响
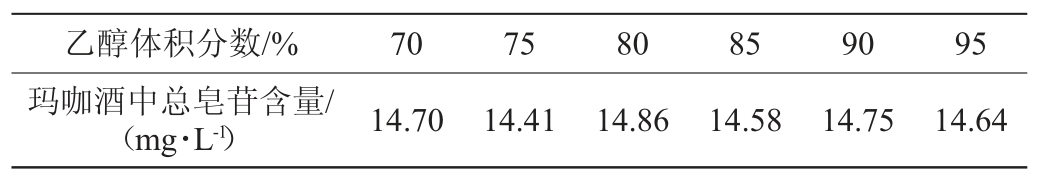
按照洗脱液浓度对皂苷含量影响的方法进行试验,考察乙醇洗脱液浓度对总皂苷检测结果的影响,结果见表2。由表2可知,70%~95%乙醇体积分数下总皂苷含量无明显差异,而在试验中发现转移至蒸发皿水浴挥干和比色管中氮吹两种方式下,氮吹法更为稳定且不需再显色后再转移,因此选择体积分数95%的乙醇作为洗脱剂以达到快速氮吹至干的目的。
表2 乙醇洗脱液体积分数对总皂苷测定结果的影响
Table 2 Effect of ethanol elution volume fraction on total saponins determination results
2.3.2 方法检出限
根据试验结果可知,空白基质质量浓度>5 mg/L以上的阳性检出率为100%,空白基质质量浓度<5 mg/L的阳性检出率为0%,测定值平均值为4.07 mg/L,计算总标准偏差S为0.18,因此检出限为4.6 mg/L。
2.3.3 方法正确度
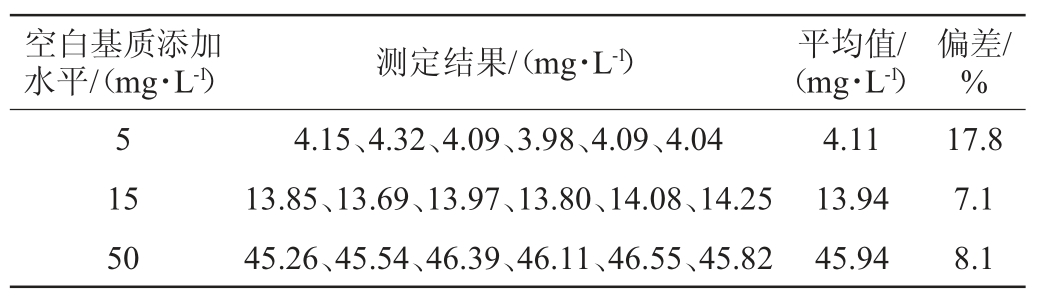
方法的正确度试验测定结果见表3。由表3可知,检出限、中值(1~10倍检出限)、高值(10倍检出限)3水平下空白基质加标后平均值与加标浓度比较偏差分别<20%、<10%,均在可信任区间范围内,由此可证明该方法系统误差较小。
表3 方法正确度试验测定结果
Table 3 Determination results of method accuracy
2.3.4 方法精密度
方法的精密度试验测定结果见表4。由表4可知,对总皂苷精密度试验的数据进行处理,可得相对标准偏差(RSD)(n=6)为2.24%。试验表明,该方法测定总皂苷含量具有较好的可重复性。
表4 方法精密度试验测定结果
Table 4 Determination results of method precision

2.3.5 方法加标回收率
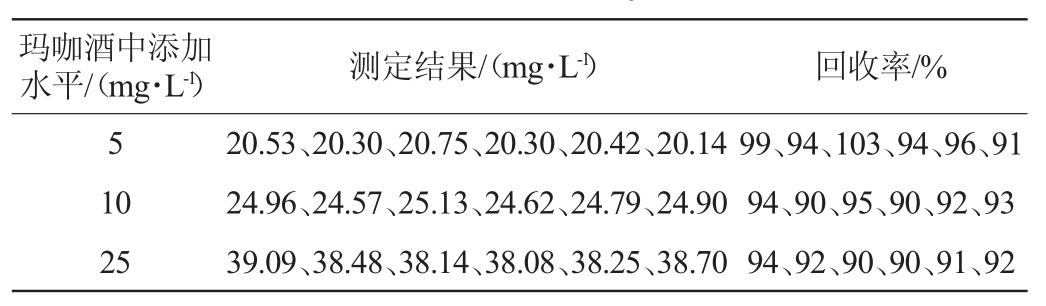
按照回收率方法进行试验,结果如表5所示。试验表明,以玛咖酒中总皂苷含量(平均值15.60 mg/L)为基础值,3水平下回收率均在90%~103%之间,满足GB/T 27417—2017中1~100 mg/kg质量浓度下回收率偏差要求90%~110%[12]。该方法测定总皂苷含量偏倚度小具有较高的准确性。
表5 方法的加标回收率试验结果
Table 5 Results of standard recovery rate of the method
3 结论
该实验对玛咖酒试样中总皂苷含量测定的前处理方法进行优化,并考察该方法的可行性。结果表明,玛咖酒试样采用SPEC18柱纯化,选用体积分数95%的乙醇作为洗脱剂;人参皂苷Re吸光度值与其质量浓度呈良好的线性关系(R2=0.990 1),线性范围0~0.20 mg/mL;方法检出限为4.6 mg/L;方法正确度的偏差在5 mg/L添加水平<20%、在15 mg/L及50 mg/L添加水平均<10%,符合要求;精密度实验结果相对标准偏差(RSD)为2.24%;加标回收率在90%~103%。建立的玛咖酒试样中总皂苷检测方法正确度及精密度高,适用于该产品总皂苷含量的测定。
[1]许敏,王兆杰,杨少杰,等.玛咖的化学成分和生物活性研究进展[J].食品研究与开发,2017,38(1):193-199.
[2]中华人民共和国卫生部.关于批准玛咖粉作为新资源食品的公告[EB/OL].http://www.gov.cn/zwgk/2011-06/16/content_1885915.htm,2011-05-18.
[3]万文婷,张志鹏,谭晓蕾,等.玛卡云南主产区发展现状调查[J].中国现代中医药,2015,17(7):726-729.
[4]李爱民,王淳,张建军,等.玛咖的现状研究与分析[J].中华中医药杂志,2018,33(1):244-248.
[5]崔耀天,赵乐荣,于建伟,等.玛咖中总游离氨基酸的提取纯化工艺研究[J].食品科技,2017,42(12):235-238.
[6]WANG Z Q,ZHAO Q M,ZHONG X T,et al.Comparative analysis of maca(Lepidium meyenii)proteome profiles reveals insights into response mechanisms of herbal plants to high-temperature stress[J].BMC Plant Biol,2020,20(1):1066-1077.
[7]付玲,陈芮.玛咖酰胺及玛咖烯的研究进展[J].化工管理,2019(1):55-56.
[8]杰布,拉琼,罗布,等.拉萨玛咖营养成分及功效成分芥子油苷的分析[J].食品工业,2017,38(4):302-304.
[9]代宏哲,高续春,徐伟洲,等.玛咖总生物碱提取和检测及药理活性研究进展[J].中国新药杂志,2018,27(15):1744-1752.
[10]高玉梅,和堂香,魏金超,等.玛咖中黄酮类化合物的研究进展[J].云南化工,2020,47(6):9-11.
[11]中华人民共和国农业部.NY/T 1842—2010 人参皂甙的测定[S].北京:中国农业出版社,2010.
[12]中华人民共和国卫生部.GB/T 22996—2008 人参中多种人参皂甙含量的测定[S].北京:中国标准出版社,2009.
[13]国家药典委员会.中华人民共和国药典[S].北京:中国医药科技出版社,2015.
[14]中国营养保健食品协会.T/CNHFA 001—2021 人参稀有皂苷的含量测定[S].北京:中国标准出版社,2021.
[15]孙媛,田秀秀,丁江生.三七不同药用部位中人参皂苷Rg3 的含量测定[J].现代中医药,2021,41(2):29-34.
[16]徐文武,谢涛,吕东峰,等.一测多评法同时测定红参中11 种人参皂苷的含量[J].中草药,2021,52(7):2099-2105.
[17]李占鹰,袁丽君,涂星,等.HPLC 测定人参-天麻药对不同配比中的人参皂苷Re[J].华西药学杂志,2019,34(6):610-612.
[18]祝洪艳,蒋然,何忠梅,等.不同乌天麻炮制品中天麻素、天麻苷元和天麻多糖的含量分析[J].中国药学杂志,2017,52(23):2062-2065.
[19]徐怡,张晓南,苏钛,等.竹节参中皂苷含量测定方法的建立[J].云南中医中药杂志,2020,41(1):69-73.
[20]李耀华,陆峥琳,魏江存,等.瑶药三角风中常春藤皂苷元含量测定方法建立[J].辽宁中医药大学学报,2020,22(1):69-72.
[21]白鸿.保健食品功效成分检测方法[M].北京:中国轻工业出版社,2002:113-115.
[22]吉林省质量技术监督局.DB22/T 2478—2016 人参中人参总皂苷的测定重量法[S].北京:中国标准出版社,2016.
[23]国家市场监督管理总局.保健食品理化及卫生指标检验与评价技术指导原则(2020 年版)[S].北京:国家市场监督管理总局,2020.
[24]安徽省食品行业协会.T/AHFIA 004—2018 食品中总皂苷含量的测定分光光度法[S].北京:中国标准出版社,2018.
[25]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 27417—2017 合格评定化学分析方法确认和验证指南[S].北京:中国标准出版社,2017.