白酒是中国的国酒,是一种历史悠久的蒸馏酒,因其独特的固态酿造方式成为我国传统酿造食品中的典范,在中国饮食文化中占有重要地位[1-2]。传统白酒酿造是以富含淀粉基质的高粱、玉米和大米等为原料,采用边糖化边发酵的“双边发酵”方式协同进行,再经过蒸馏、勾调和贮存等过程酿制的富含千种风味物质的酒精类饮品[3]。在白酒酿造过程中,“双边发酵”中的糖化和发酵协调一致、有序进行是白酒酿造成功的关键,决定了白酒的出酒率和丰富度[4]。如糖化作用不足,原料中的淀粉转化为可发酵的糖量不充分,从而影响酵母的发酵,导致原料利用率差,出酒率低[5]。高产淀粉酶菌株往往具有高糖化作用,对于提高白酒出酒率和缩短白酒酿造周期具有重要的作用。为此,有研究者针对白酒酿造环境中高产淀粉酶菌株开展了研究,获得了多株具有提高白酒出酒率等应用潜力的优良菌株[6]。众所周知,霉菌是重要的淀粉酶产生菌株,在白酒酿造糖化过程中发挥一定作用,是众多研究者筛选白酒酿造环境中高产淀粉酶的重要关注菌群,这也是有关白酒酿酒中高产淀粉酶菌株相关研究主要集中于霉菌的原因[7]。然而,在白酒酿造过程中,细菌菌群具有更高的丰度和多样性,是白酒酿造更为有力的主导者,加强白酒酿造环境中细菌功能的研究将会有助于白酒品质的进一步提升,尤其是对其所产酶能力的探究[8]。因此,已有研究者将研究白酒酿酒环境中高产淀粉酶的菌株聚焦于细菌,筛选出多株高产淀粉酶的细菌[9-10]。
酱香型白酒是白酒的基本香型之一,具有“酱香突出,幽雅细腻,酒体醇厚,回味悠久,空杯留香”的酒体风格,深受消费者的喜爱[11]。其中,以茅台为代表的酱香型白酒因其独特的品质而广受好评,因此,在1975年“八大名酒进北京”时,北京华都酿酒食品有限责任公司沿袭和创新了茅台酱香型白酒的酿造工艺,开启了一段南酱北传的历史传奇,成为北派酱香的先河,也奠定了华都在北派酱香中的历史地位。但毕竟南北方的气候和环境差异很大,微生物区系也有较大差异[12],因此,以华都为代表的北派酱香型白酒在酿造过程上也因地制宜进行了创新,从而酿造出了独具一格的北派酱香型白酒,如“下沙”时间段相比茅台酿造工艺的“下沙”时间段后移,以此将酿造好酒的3~5轮次安排在最接近南方炎热且潮湿气候的7~9月;冬季寒冷季节通过供暖系统提高酿造环境温度等。为进一步提升北派酱香白酒的品质,北京华都酿造食品有限责任公司尝试通过挖掘酿造环境中微生物的功能,以白酒酿造驱动力-微生物作为进一步深化改革的靶点。因此,本研究正是基于此,采用平板涂布方法结合淀粉琼脂筛选培养基透明圈法从其酿造环境(大曲、酒醅和窖泥)中筛选高产淀粉酶菌株,并通过形态和细胞观察、生理生化试验结合分子生物学方法对其进行鉴定,同时探究其在不同条件下的菌体生长情况分析其生长特性和环境耐受性,以此进一步解决因冬季寒冷,入窖温度低,糖化作用低的问题。本研究将有助于了解华都酿造食品有限责任公司白酒酿造环境中产淀粉酶细菌微生物情况,为后续利用功能微生物强化方法提高其出酒率提供优良菌株。
1 材料与方法
1.1 材料与试剂
1.1.1 材料与试剂
大曲、酒醅和窖泥:2020年8月取自北京华都酿酒食品有限责任公司酿造车间;可溶性淀粉:美国Sigma公司;细菌基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:北京索莱宝科技有限公司;3,5-二硝基水杨酸(3,5-dinitrosalicylicacid,DNS):国药集团化学试剂有限公司;淀粉酶(2万U/mL):上海麦克林生化科技有限公司;糖化酶(10万U/mL):上海阿拉丁生化科技股份有限公司;其他试剂均为国产生化试剂或分析纯。
1.1.2 培养基
LB固体培养基:氯化钠10 g/L,蛋白胨10 g/L,酵母浸粉5 g/L,琼脂粉20 g/L,自然pH值,121 ℃灭菌20 min。
淀粉琼脂筛选培养基:牛肉膏3 g/L,氯化钠5 g/L,胰蛋白胨10 g/L,琼脂粉20 g/L,可溶性淀粉20 g/L,自然pH值,121 ℃灭菌20 min。
发酵培养基:可溶性淀粉1 g/L,蛋白胨1 g/L,(NH4)2SO4 0.25 g/L,MgSO4 0.02 g/L,FeSO4·7H2O 0.002 5 g/L,KH2PO4 0.3 g/L,CaCl2·6H2O 0.025 g/L,自然pH值,121 ℃灭菌20 min,FeSO4·7H2O灭菌后过膜加入。
高粱酶解液培养基:参照FAN G S等[13]方法进行制备。
1.2 仪器与设备
BSA124S电子天平、PB-10 pH计:赛多利斯科学仪器有限公司;YQX-SG46-280S立式高压蒸汽灭菌锅:上海博迅实业有限公司医疗设备厂;BCN-1360型生物洁净工作台:北京东联哈尔仪器公司;LHS-100CL恒温恒湿培养箱:上海一恒仪器设备有限公司;TU-19紫外-可见分光光度计:北京普析通用仪器有限责任公司;CKX41-F32FL倒置荧光显微镜:日本OLYMPUS公司;Tprofessional 聚合酶链式反应(polymeras chain reaction,PCR)仪:德国Biometra公司;Microfuge2R离心机:北京田林恒泰科技有限公司;TSQTM8000 evo三重四级杆气质联用(gaschromatography-massspectrometry,GC-MS)仪:美国ThermoFisherScientific公司;ZQZY-C8V振荡培养箱:上海知楚仪器有限公司。
1.3 实验方法
1.3.1 菌株的筛选和分离
用无菌水将曲粉、窖泥或酒醅样品稀释成10-5、10-6和10-7的菌悬液,取100 μL菌悬液涂布于LB平板上,倒置培养于30 ℃,随时观察并挑取菌落形态特征明显不同的单菌落,采用分区划线法进行分离纯化,纯化菌株保藏于4 ℃备用。
1.3.2 产淀粉酶菌株的筛选
将筛选得到的菌株分别点种于淀粉琼脂筛选培养基上,于30 ℃倒置培养48 h,用少量碘液铺平平板后,静置1 min,观察菌落周围有无透明圈,若有透明圈,则表明菌株能产生淀粉酶根据透明圈直径(D2)与菌落直径(D1)的比值(D2/D1)的大小判断菌株产淀粉酶的能力。
1.3.3 菌株的鉴定
形态观察:将高产淀粉酶菌株接种至LB固体培养基上,30 ℃条件下培养2 d后进行菌落形态观察;挑取LB平板上单菌落少量菌体,涂布并固定在载玻片上,进行革兰氏染色及芽孢染色,采用油镜(10×100倍)观察,记录细胞形态情况[14]。
生理生化实验:菌株生理生化分析参照《伯杰细菌鉴定手册》[15],包括糖发酵、碳源同化、氮源同化、淀粉水解试验、甲基红试验、吲哚试验、尿素试验、硫化氢试验、牛奶石蕊试验、V.P.试验、明胶液化试验和柠檬酸盐试验。
分子生物学鉴定:采用细菌基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒提取初筛获得的高产淀粉酶菌株的基因组DNA,并以该DNA为模板,采用通用引物27F(5'-AGAGTTTGATCCTGGCTCAG-3')和1492(5'-GGTTACCTTGTTACGACTT-3')进行16S rRNA基因的PCR扩增。PCR反应体系为:37.5 μL双蒸水(ddH2O),4 μL脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTPs),1 μL上游引物(27F),1 μL下游引物(1492R),1 μL总DNA,0.5 μL Taq DNA聚合酶,5 μL 10×Buffer。PCR反应条件为:94 ℃预变性10 min;94 ℃变性30 s,55 ℃退火30 s,72 ℃延伸30 s,循环35次;72 ℃再延伸10 min。将PCR产物进行1%琼脂糖凝胶电泳检测后送至北京诺赛基因组研究中心有限公司测序,测序结果在美国国家生物技术信息中心(national center for biotechnology information,NCBI)上进行基本局部比对搜索工具(basic local alignment search tool,BLAST)同源性比对,使用MEGA 7.0生物学软件对近似序列进行比对分析,利用邻接(neighbor-joining,NJ)法构建系统发育树。
1.3.4 菌株生物学特性研究
菌株生物学特性研究参照之前研究报道[16],主要包括生长温度范围、pH值范围、乙醇耐受性、葡萄糖耐受性、NaCl耐受性和己酸耐受性。
1.3.5 菌株产淀粉酶测定
菌株于LB液体培养基中进行活化(37 ℃、180 r/min条件下培养18 h)后,按照1%(V/V)的接种量接种于发酵培养基中于37 ℃、180 r/min条件下培养5 d,每天测定淀粉酶活力和生物量。
淀粉酶活力采用DNS法进行测定[17],淀粉酶活力单位定义为:在上述反应条件下,每分钟生产1 μmol葡萄糖所需要的酶量为一个酶活单位(U/mL)。
生物量采用分光光度计于波长600 nm处测定吸光度值(OD600nm值)。
1.3.6 菌株产香特性
菌株按照1.3.5中方法进行活化后,接种于高粱酶解液中进行产香特性分析,培养条件为37 ℃、180 r/min培养48 h,采用顶空固相微萃取-气质联用(solid-phase micro-extractiongas chromatography-mass spectrometry,SPME-GC-MS)法检测其所产挥发性风味物质。参照FAN G S等[18]的方法并采取一定修改测定菌株在高粱酶解液中培养所产挥发性成分,具体参数如下:发酵液装入顶空瓶中50 ℃平衡30 min,采用50/30 μm DVB/CAR/PDMS萃取头吸附30 min,于气相色谱高温气化室解吸5 min后进行气质分析。
GC条件:毛细管色谱柱为DB-WAX(30 m×0.32 mm×0.25 μm),不分流进样,进样口温度为250 ℃,载气为氦气(He),流速为1mL/min,程序升温:40℃,保留3min,以2℃/min的速率升至100 ℃,保留5 min,再以2 ℃/min升至150 ℃,稳定3 min,最后以10 ℃/min升至280 ℃,稳定6 min。
MS条件:电子电离(electronic ionization,EI)源,电子能量70 eV,扫描范围35~400 amu,离子源温度250 ℃,接口温度250 ℃。
定性定量方法:通过质谱解析与NIST 11谱库和文献保留指数比对确定各化合物结构,并采用四辛醇作为内标进行内标半定量法计算各化合物的含量。
1.3.7 数据处理
每组试验进行三个平行,数据采用“平均值±标准差”表示,利用Excel 2016处理试验数据。
2 结果与分析
2.1 产淀粉酶菌株筛选
通过梯度稀释结合平板涂布方法先后从大曲、酒醅和窖泥样品中分离出127株菌株(分别编号为2-1~2-15,3-1~3-25,4-1~4-25,5-1~5-8,7-1~7-19,12-1~12-19,17-1~17-16;其中从大曲中筛选获得16株,从酒醅中分离获得96株,窖泥样品中分离出15株)。将上述127株菌分别接种到淀粉琼脂筛选培养基中培养48 h后,用碘液染色,观察有无透明圈,代表菌株结果见图1。测定每株菌株形成的透明圈直径和菌落直径,并计算两者的比值,试验结果见表1。
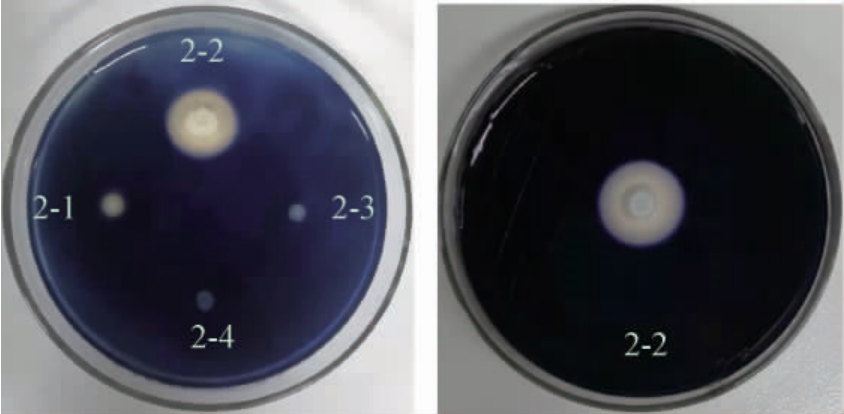
图1 淀粉酶产生菌株的筛选
Fig.1 Screening of amylase-producing bacteria
表1 分离菌株透明圈直径与菌落直径比
Table 1 Transparent circle diameter and colony diameter ratio of isolated strains

续表

由表1可知,在所筛选菌株中,将近40%菌株能产生透明圈,这可能与生长环境有关,是富含淀粉的酿造环境选择和富集的结果。在这些能产生透明圈的菌株中,其比值差异比较大,表明其所产淀粉酶活力存在一定差异,这主要是由于不同菌株的遗产特性决定的,也正是这些微生物之间存在类似于淀粉酶活力等生物活性的差异,才会促使不同白酒酿造微生物菌群之间巧妙的有机结合,相互促进、协调和制衡,形成符合其酿造工艺特有的菌群演替规律,最终获得对应酿造环境和生产工艺的产品[19]。相比茅台酒厂,北京华都酿酒食品有限责任公司酿造车间中高产淀粉酶的菌株相对较少,其比值达到1.50以上的菌株仅9株,其中,以菌株2-2的比值为最大,为2.25,为此将其确定为本研究的目标菌株[20]。
2.2 菌株2-2的鉴定
2.2.1 菌株2-2的形态特征
由图2a可知,菌株2-2在LB鉴定平板上的生长菌落呈白色不透明状,表面褶皱,边缘不规则,内部湿润不易挑起;由图2b可知,菌株2-2革兰氏染色结果呈阳性;由图2c可知,显微镜下菌株2-2细胞形态为杆状,链状排列,可形成芽孢,呈椭圆形,两端钝圆,芽孢囊不膨大,属典型细菌特征。根据菌株2-2的菌落形态和细胞形态初步确定菌株2-2为芽孢杆菌属(Bacillus sp.)。
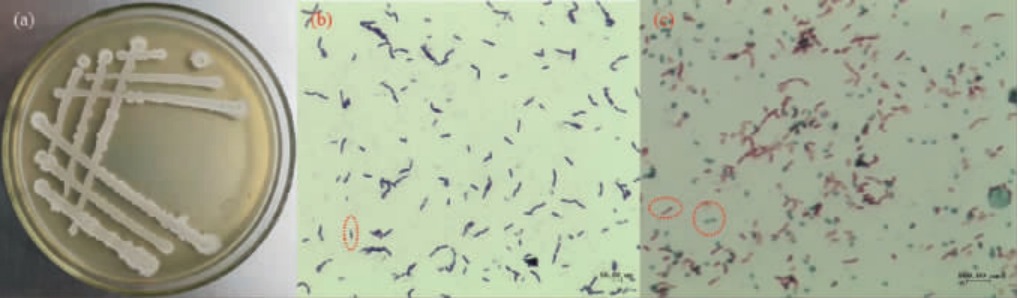
图2 菌株2-2在LB培养基上菌落形态特征(a)及细胞形态特征(b,c)
Fig.2 Colony morphological characteristics on LB culture medium (a)and cell morphological characteristics (b and c) of strain 2-2
2.2.2 菌株2-2的生理生化试验结果
从表2可以看出,菌株2-2能利用葡萄糖、蔗糖、麦芽糖发酵产酸不产气,但不能利用乳糖、半乳糖、棉子糖、甘露糖、山梨糖、木糖和海藻糖产酸或产气;碳源同化试验表明该细菌能利用葡萄糖、蔗糖、乳糖、半乳糖、麦芽糖、可溶性淀粉、棉子糖、甘露糖、山梨糖、木糖和海藻糖等碳源生长;氮源同化试验结果表明,该细菌能利用尿素、硝酸钾、硫酸铵、L-苯丙氨酸和L-赖氨酸作为唯一氮源进行生长;硫化氢试验、吲哚试验、甲基红试验和柠檬酸盐试验均为阴性反应;V.P.试验、淀粉水解试验、尿素酶试验和明胶水解试验均为阳性反应,石蕊牛乳试验表明该细菌能够产生蛋白酶水解牛乳且具有还原性,能够使石蕊还原。根据《伯杰细菌鉴定手册》,该细菌与解淀粉芽孢杆菌(Bacillus amyloliquefaciens)的生理特性相似度最高,初步认为菌株2-2属于解淀粉芽孢杆菌(Bacillus amyloliquefaciens)。
表2 菌株2-2的生理生化特征
Table 2 Physiological and biochemical characteristics of strain 2-2

注:“+”为结果阳性,“-”为结果阴性,“w”为结果弱阳性。
2.2.3 菌株2-2的分子生物学鉴定
菌株2-2的系统发育树见图3。由图3可知,菌株2-2与解淀粉芽孢杆菌(Bacillus amyloliquefaciens)及贝莱斯芽孢杆菌(Bacillus velezensis)AJAS1的16S rDNA序列同源性最高,相似度达到99%。综合菌落形态、细胞形态、生理生化和分子生物学的试验结果,菌株2-2被鉴定为解淀粉芽孢杆菌(Bacillus amyloliquefaciens)。

图3 基于16S rDNA序列菌株2-2的系统发育树
Fig.3 Phylogenetic tree of strain 2-2 based on 16S rDNA sequences
2.3 菌株2-2生物学特性分析
2.3.1 生长温度
白酒酿造时温度范围变化较大,温度的适当升高有利于糖化的进行,但过高的温度也会导致细胞代谢能力的降低,影响酶的活性[21]。
由图4可知,菌株2-2在25~50 ℃的温度范围内都可以生长,在30~40 ℃的温度范围内长势良好,且其最适生长温度为30 ℃。这表明菌株2-2能够很好的适应糖化过程中温度的变化,切合北方地区白酒酿造环境中温度的变化,表明其在北方地区的白酒酿造过程中具有很好的实际应用价值。
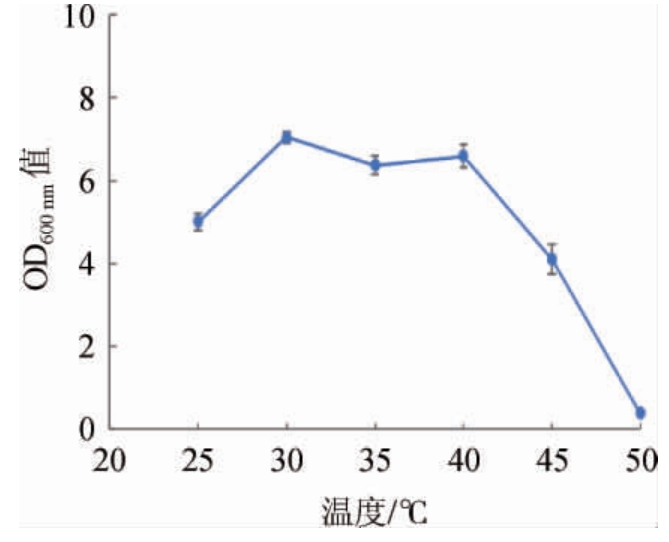
图4 菌株2-2在不同温度下的生长情况
Fig.4 Growth situation of strain 2-2 at different temperature
2.3.2 生长pH值
环境pH值会对菌株的生长代谢产生一定影响[22]。在白酒发酵过程中,原料中的淀粉和蛋白质等营养物质的分解会产生有机酸、氨类化合物或其他产物,从而导致酿造环境pH的变化[23],这就要求菌株具有较为宽广的pH值适应范围,从而适应发酵过程中pH值的变化。由图5可知,菌株2-2在pH值4~10的范围内都可以生长,且在pH值5~9时生长旺盛,有较好的pH值适应性。因此可以在白酒酿造环境中存活且发挥其糖化作用。
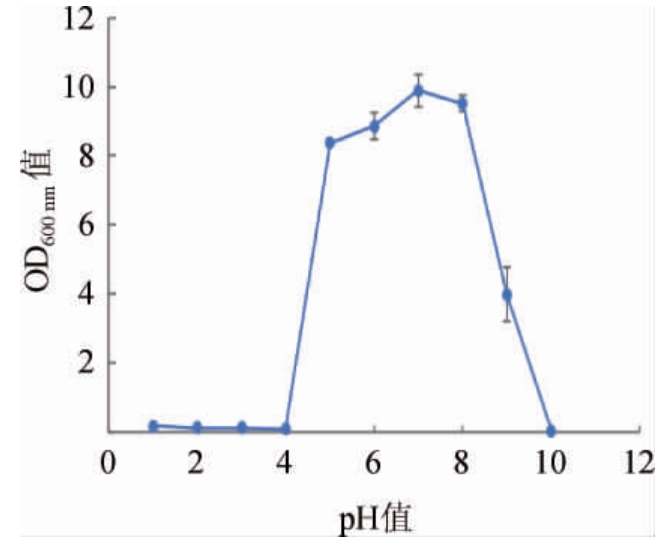
图5 菌株2-2在不同pH值下的生长情况
Fig.5 Growth situation of strain 2-2 at different pH
2.3.3 乙醇耐受性
菌株的耐乙醇能力在发酵白酒的过程中是非常重要的,因为白酒酿造过程中产生的乙醇会抑制细胞的正常代谢,对其繁殖也会造成一定程度的影响[24]。由图6可知,随着乙醇体积分数的增加,菌株2-2的生长速率下降,但在乙醇体积分数为12%时,菌株2-2还能够生长,说明其具有较高的耐乙醇能力。在乙醇体积分数10%的范围内,菌株2-2都有很好的生长,这使得该菌株能够更好的在酿造环境中发挥作用,发挥糖化力,从而有利于出酒率的提升。
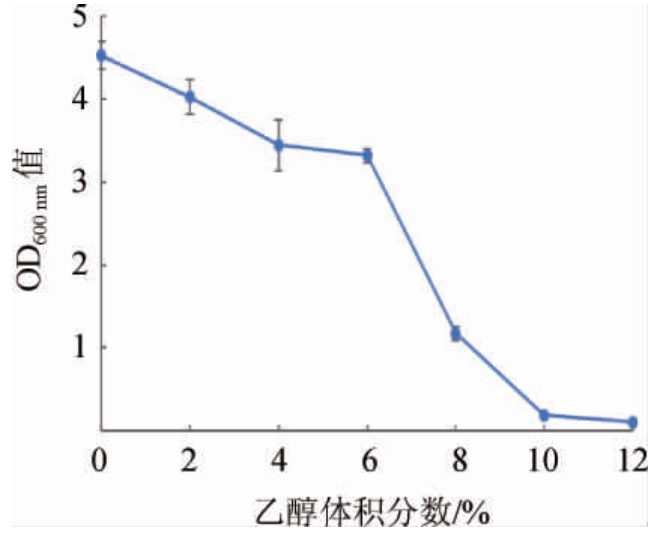
图6 菌株2-2的乙醇耐受性
Fig.6 Ethanol tolerance of strain 2-2
2.3.4 葡萄糖耐受性
淀粉酶在白酒酿造过程中主要起糖化作用,水解酿造原料中的淀粉为后续的发酵生产乙醇提供原料,但是过高浓度的糖产生的高渗透压会导致细胞内水分的流失,对菌株自身具有一定的危害作用[25],因此能够适应高糖环境的菌株对于糖化过程是有利的。由图7可知,随着葡萄糖质量分数在0~80%的范围内增加,逐渐形成的高渗透压会对细菌细胞产生抑制作用,从而导致生长速率的下降,但菌株2-2在葡萄糖质量分数为70%时还可以生长,表明具有较强的葡萄糖耐受性,这一特征进一步表明了其在白酒酿造中具有潜在的提高白酒产率的应用价值。
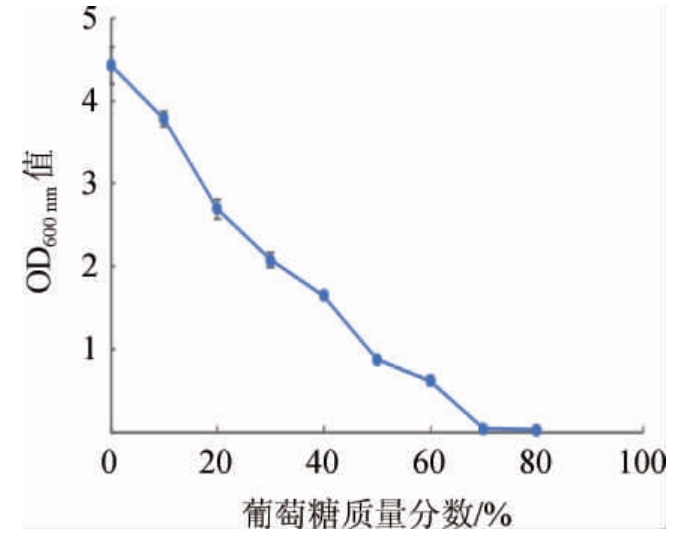
图7 菌株2-2的葡萄糖耐受性
Fig.7 Glucose tolerance of strain 2-2
2.3.5 NaCl耐受性
NaCl浓度越高,产生的渗透压越大,从而会引起细胞内水分活度、细胞结构及组成成分的变化,甚至会降低细胞中酶的活性。微生物的种类不同,其所能适应的渗透压也不同,具有高渗透压耐受性的微生物细胞内会形成多种具有特殊功能的酶,来适应环境的变化[26-27]。由图8可以看出,随着NaCl质量分数在0~30%的范围内增加,菌株2-2生长速率会受到一定程度的抑制,但其耐受NaCl的质量分数可以达到15%,说明菌株2-2具有较好的耐盐性。这可能是在复杂的白酒酿造环境中自然选择而来的,有利于其快速适应白酒酿造环境。
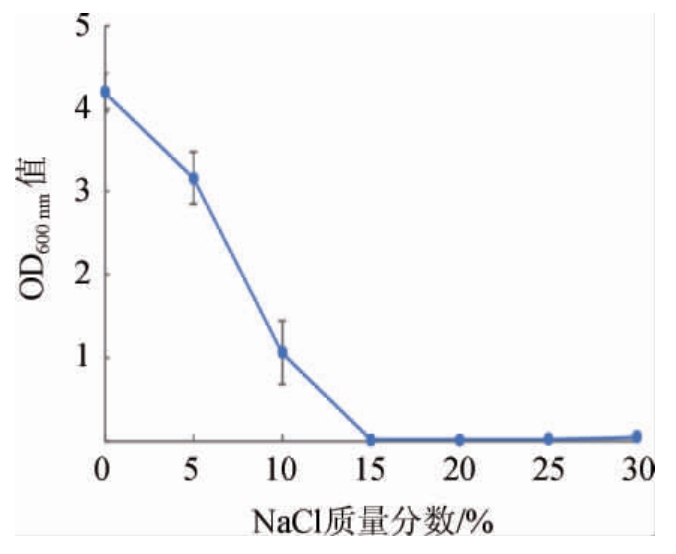
图8 菌株2-2的NaCl耐受性
Fig.8 NaCl tolerance of strain 2-2
2.3.6 己酸耐受性
白酒在酿造过程中会产生很多风味物质,如醇类、酯类等,其中短链有机酸物质在这一过程中会大量积累,同时酸类也是产生酯类的前体物质,但有机酸含量过高也会对细胞产生毒害作用,从而影响到白酒的品质,基于此考察了菌株的己酸耐受性。由图9可知,己酸体积分数<0.02%时,有利于菌株2-2的生长,但是随着己酸添加量的增加,其生长受到影响,当己酸体积分数为0.06%时,菌株已不能生长,由此可见,该菌株具有一定的己酸耐受性,可能在白酒酿造中发挥着将己酸转化为己酸乙酯的作用。
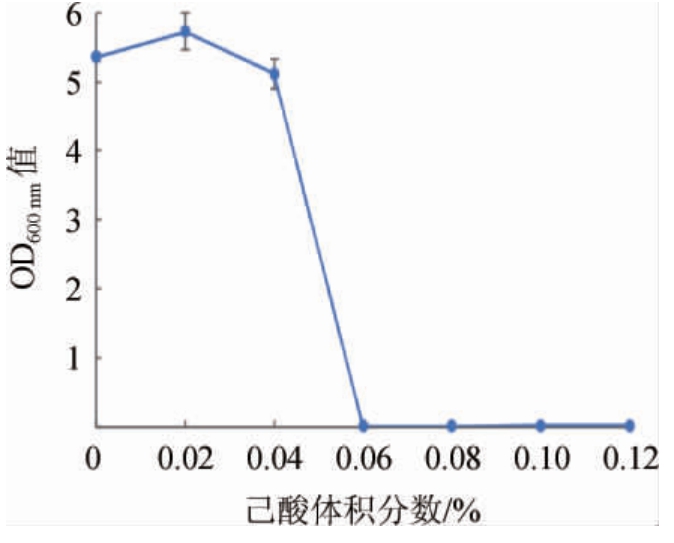
图9 菌株2-2的己酸耐受性
Fig.9 Caproic acid tolerance of strain 2-2
2.4 菌株2-2的产酶特性
菌株2-2在37 ℃的条件下培养5 d,每隔24 h取样进行酶活测定和生物量测定,产酶结果如图10所示。由图10可知,淀粉酶的活力随着发酵时间的延长先增加后降低,在第3天达到最大值,为18.7 U/mL。由图10亦可知,前2 d菌体生长较慢,可能处于延迟期,因此产酶较弱,第3天时菌体生长较快,产酶能力也随之加强,在第3天到第4天时,菌体量迅速增加。通过比较菌体量和淀粉酶活力的变化,在菌体量较高时,淀粉酶活力反而降低,这可能是由于该菌株所产蛋白质酶所致,也正是由于微生物所产酶系的不断变化才产生了不同香型和品质特性的白酒。另外,该酒厂中所产淀粉酶菌株活力相对较低,这也表明了其采用“下沙”时间后移,冬季采暖等措施的科学性。
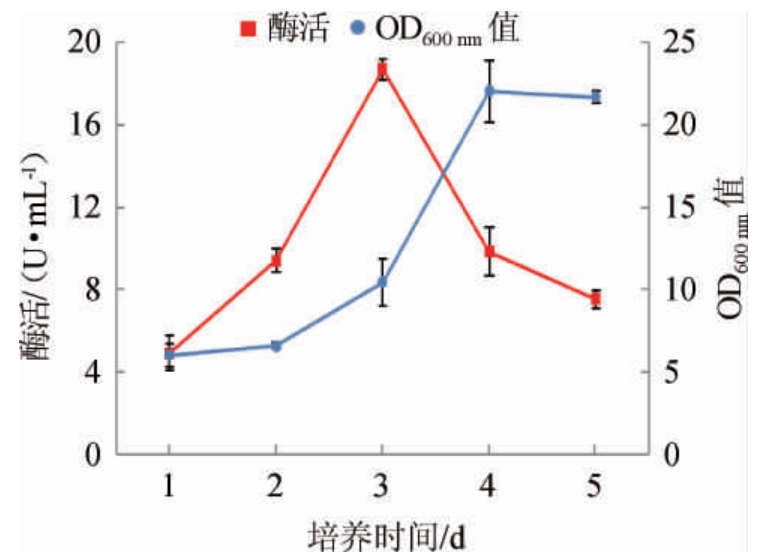
图10 菌株2-2的产酶曲线和生长曲线
Fig.10 Enzyme production curve and growth curve of strain 2-2
2.5 菌株2-2的产香特性
通过对产香特性分析发现,菌株2-2可以产生乙醇、苯乙醇、正己醇、2-甲基-3-戊醇、4-辛醇、异辛醇、5-甲基-5-壬醇、α-松油醇、糠醇、(2S,3S)-(+)-2,3-丁二醇、香叶醇七种醇类物质,其中苯乙醇、正己醇均为酱香型白酒骨架成分[28];酮类物质主要有3-羟基-2-丁酮、1-丁醇2-庚酮、2-羟基-3-戊酮和大马士酮,其中3-羟基-2-丁酮的浓度达到0.35 mg/L,它是合成4-甲基吡嗪的前体物质,而吡嗪类物质是酱香型白酒中的重要风味物质[29],同时在该菌株的产香实验中也检测到了2,5-二甲基吡嗪;此外还可以产生丁酸、异丁酸等有机酸类物质和对乙烯基愈疮木酚、苯酚两种酚类物质,对酱香型酒体风味也有较大的贡献。
3 结论
本研究从北方酱香型白酒大曲中获得一株产淀粉酶的细菌菌株,通过形态学观察、生理生化试验和分子生物学分析综合鉴定为解淀粉芽孢杆菌(Bacillus amyloliquefaciens),该菌株在25~45 ℃和pH 5~9的范围内都能良好生长,同时还具有12%的乙醇耐受性、15%的NaCl耐受性和70%的葡萄糖耐受性;在37 ℃的条件下培养3 d淀粉酶活力最高,达到18.7 U/mL。综上可见,该细菌对于北方酱香型白酒酿造具有很好的实际应用意义。
[1]LIU H L,SUN B G.Effect of fermentation processing on the flavor of Baijiu[J].J Agric Food Chem,2018,66(22):5425-5432.
[2]吴继红,黄明泉,郑福平,等.健康白酒的研究进展[J].食品科学技术学报,2019,37(2):17-23.
[3]王柏文,吴群,徐岩,等.中国白酒酒曲微生物组研究进展及趋势[J].微生物学通报,2021,48(5):1737-1746.
[4]信春晖,马冬梅,王万伟,等.白酒酿造浅说(一)[J].酿酒,2014,41(6):32-38.
[5]邓皖玉,许永明,程伟,等.润粮工艺对酱香型白酒生产的影响[J].酿酒科技,2021(1):36-41,49.
[6]潘菲.高糖化力霉菌的筛选及其对特香型白酒酿造出酒率和风味的影响[D].南昌:南昌大学,2018.
[7]王鹏昊,关统伟,邓奥宇,等.酒曲中高产蛋白酶和α-淀粉酶霉菌菌株的筛选与分子鉴定[J].酿酒科技,2016(6):61-64,71.
[8]FAN G S,FU Z L,TENG C,et al.Effects of aging on the quality of roasted sesame-like flavor Daqu[J].BMC Microbiol,2020,20(1):67.
[9]刘延波,张世凯,赵志军,等.高产淀粉酶细菌的分离鉴定及产酶条件优化[J].食品与机械,2020,36(1):65-71.
[10]曹振华,李富强,闫培勋,等.窖泥中高产淀粉酶细菌的分离和鉴定[J].酿酒,2020,47(6):39-44.
[11]孙时光,左勇,张晶,等.酱香型白酒中的风味物质及功效[J].中国酿造,2017,36(12):10-13.
[12]JIN G Y,ZHU Y,XU Y.Mystery behind Chinese liquor fermentation[J].Trends Food Sci Tech,2017,63:18-28.
[13]FAN G S,SUN B G,XU D,et al.Isolation and identification of high-yield ethyl acetate-producing yeast from Gujinggong Daqu and its fermentation characteristics[J].J Am Soc Brew Chem,2018,76(2):117-124.
[14]李秀婷.食品微生物学实验技术[M].北京:化学工业出版社,2020:26-31.
[15]布坎南R E,吉本斯N E.伯杰细菌鉴定手册[M].北京:科学出版社,1984:744.
[16]FAN G S,CHENG L J,FU Z L,et al.Screening of yeasts isolated from Baijiu environments for 2-phenylethanol production and optimization of production conditions[J].3 Biotech,2020,10(6):275.
[17]HAN P,ZHOU P,HU S Q,et al.A novel multifunctional alpha-amylase from the thermophilic fungus Malbranchea cinnamomea:Biochemical characterization and three-dimensional structure[J].Appl Biochem Biotechnol,2013,170(2):420-435.
[18]FAN G S,TENG C,XU D,et al.Enhanced production of ethyl acetate using co-culture of Wickerhamomyces anomalus and Saccharomyces cerevisiae[J].J Biosci Bioeng,2019,128(5):564-570.
[19]印丽,邱树毅,曹文涛,等.酱香型白酒核心产区大曲的酶系分析[J].现代食品科技,2021,37(3):89-96.
[20]翁庆北,赵维娜,万晴姣,等.茅台酒曲中产淀粉酶细菌分离及性质[J].贵州师范大学学报(自然科学版),2005(2):20-22.
[21]黄永光.酱香型白酒酿造中Aspergillus hennebergii 及其分泌酸性蛋白酶的研究[D].无锡:江南大学,2014.
[22]付肖蒙,王鹏飞,郝爱丽,等.高耐性酿酒酵母的筛选及其耐受性研究[J].中国酿造,2017,36(10):23-26.
[23]贾丽艳,郭晋田,刘帅,等.清香型白酒发酵过程中微生物及理化指标的变化规律[J].中国食品学报,2020,20(8):162-167.
[24]吴健,何伟,王建成,等.酿酒酵母与产香酵母发酵特性及其相互作用规律[J].食品与发酵工业,2020,46(20):78-87.
[25]邢晓莹,刘毅,霍乃蕊,等.山西老陈醋中优良酵母菌株筛选及其在木枣果酒发酵中的应用[J].中国酿造,2021,40(3):64-72.
[26]范光森,许岱,富志磊,等.古井贡酒曲中酵母的分离及其产香挥发性风味物质分析[J].中国食品学报,2018,18(7):220-229.
[27]詹建立,易霞.耐盐细菌研究进展及多样性分析[J].高师理科学刊,2020,40(12):52-56,61.
[28]王荣钰,赵金松,苏占元,等.酱香型白酒关键酱香风味物质研究现状[J].酿酒科技,2020(6):81-86.
[29]李俊,王震,郭晓关,等.基于全二维气相飞行时间质谱联用法分析贵州酱香型白酒挥发性风味成分[J].酿酒科技,2016(12):102-106.