牛蒡(Arctium lappc L.)属菊科(Compositae)牛蒡属植物,是一种典型的药食同源植物[1],具有降血压、降血脂、抗病毒、抗肿瘤等作用[2]。牛蒡口味独特,是东南亚特别是日本人喜爱的餐桌佳品,甚至有“东洋参”之说[3]。牛蒡主要分布在温热带地区,我国大部分地区都可种植[4],目前,江苏省徐州市种植面积最多,大约占全国种植面积的70%。随着牛蒡产量增加,化学肥料和农药大规模使用,造成牛蒡品质下降、土壤板结、生态环境破坏[5]。生物有机肥可以改变上述弊端,其中含有固氮菌、解磷菌、解钾菌、生防菌等,由于大量的益生菌的存在既能促进牛蒡对N、P、K等营养的吸收又能抵御病虫害的侵袭,提高了产品品质,改善了环境。近年来,生物有机肥成为现代农业的研究热点之一[6]。
植物内生固氮菌是指定植于宿主植物体内,与宿主联合固定空气中氮素,为宿主植物提供氮素的微生物[7]。根据固氮菌是否定植于植物体内,可将固氮菌分为内生固氮菌和根际固氮菌。目前,内生固氮菌在禾本科植物中发现较多,小麦、玉米、水稻、甘蔗等体内都发现固氮能力较强的固氮菌[8]。但是,到目前为止很少发现牛蒡内生固氮菌的研究报道。本研究利用无氮培养基从牛蒡根内分离、筛选具有固氮能力可人工培养的体内固氮菌,通过形态观察、生理生化特性测定和16S rDNA鉴定对其进行菌种鉴定,并对其培养条件进行优化,以期为用于牛蒡根内固氮菌的资源开发和牛蒡专用生物有机肥的制备提供支持。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
在徐州市丰县牛蒡标准化种植基地采集牛蒡的根,采集后装入无菌塑料袋密封。
1.1.2 培养基
改良阿斯贝(Ashby)无氮培养基[9]:MgSO4·7H2O 0.2 g/L、CaSO4 0.1 g/L、KH2PO4 0.2 g/L、CaCO3 5.0 g/L、NaCl 0.2 g/L、葡萄糖10.0 g/L、琼脂18 g/L、蒸馏水1 000 mL,pH 7.0~7.2。115 ℃高压蒸汽灭菌20 min。
1.1.3 试剂
MgSO4·7H2O、CaCO3、KH2PO4、CaSO4、葡萄糖(均为分析纯):格里斯医药化学技术有限公司;柠檬酸、甘露醇、L-酪氨酸、L-苯丙氨酸、L-组氨酸、L-亮氨酸(均为分析纯):北京市津同乐泰化工产品有限公司;细菌基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:北京Solarbio公司。其他试剂均为国产分析纯或生化试剂。
1.2 仪器与设备
BX43/53生物显微镜:北京瑞科中仪科技有限公司;VD-850台式超净工作台:杭州旭清科技有限公司;HZ-124/85S半微量电子天平:上海诺宣科学仪器有限公司;XW-80A旋涡混合仪:广森实验器材有限公司;LH-PYX3M生化培养箱:常州金南仪器制造有限公司;HNY-200B恒温摇床:上海乔跃电子科技有限公司;TDZ24离心机:青岛诺凯达机械制造有限公司;UV2800S紫外分光光度计:上海力辰仪器科技有限公司。
1.3 方法
1.3.1 牛蒡根预处理及消毒
清洗:采集来的牛蒡根首先用流水冲洗掉根表面的泥土,然后再用流水冲洗30 min,最后用无菌水清洗3~5次。
表面消毒[10]:先把牛蒡根放在体积分数75%乙醇中浸泡10 min,取出后用无菌水冲洗3次,接着用0.1%升汞浸泡1 min,取出后再用无菌水冲洗3~5次。
1.3.2 牛蒡根内生固氮菌分离、筛选
在超净工作台上,将表面消毒完的牛蒡根用无菌剪刀剪碎,放入灭过菌的研钵中,加入适量的磷酸缓冲盐溶液,研磨30 min。取0.1 mL研磨的汁液均匀的涂布在改良的阿斯贝(Ashby)无氮培养基上,28 ℃倒置黑暗培养,12 h后每6 h观察1次。根据观察,选择生长速度快、菌落饱满的不同菌落,在新的固体培养基上划线分离纯化。
1.3.3 菌株的鉴定
形态观察:借助显微镜进行菌株的形态特征观察。
生理生化特性鉴定:主要进行了V-P试验、脲酶试验、甲基红反应试验、吲哚反应试验、接触酶试验、产氨试验、产H2S试验、硝酸盐还原试验、氧化酶试验等,具体方法参考文献[11-14]。
16S rDNA序列分析[15-17]:利用细菌基因组提取DNA试剂盒提取纯化菌株的DNA。使用通用引物27F:5'-AGAGTTTGATCCTGGCTCAG-3',1492R:5'-GGTTACCTTGTTACGACTT-3'。通过聚合酶链式反应(polynerase chain reaction,PCR)克隆菌株基因组DNA的16S rDNA基因。PCR扩增体系20 μL:10×PCR缓冲液2 μL,模板DNA 20 μL,脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphates,dNTPs)(10 mmol/L)0.45 μL,20 μg/L上、下游引物各0.25 μL,Taq DNA聚合酶0.4 μL(浓度5 U/μL),加双蒸水(ddH2O)至终体积。PCR扩增程序:95 ℃预变性5 min;95 ℃变性30 s,55.5 ℃退火45 s,72 ℃延伸2 min,共35个循环;72 ℃最后延伸10 min。回收琼脂糖凝胶PCR克隆片段链接到T载体,送至南京世和基因生物技术有限公司进行基因测序,测序结果和美国国立生物技术信息中心(national center for biotechnology information,NCBI)的GenBank数据库采用基本局部比对搜索工具(basic local alignment search tool,BLAST)进行序列相似性比对分析,利用Mega 6软件进行发育进化树的构建,分析固氮菌株的分类学地位。
1.3.4 乙炔还原活性的测定[18-20]
将分离得到的纯种菌株培养在液态改良阿斯贝(Ashby)无氮培养基中,把对数生长期的菌株培养液加入到密封的100 mL的培养容器中,接着将容器中10%空气置换成高纯乙炔气体,28 ℃、240 r/min培养24 h后用气相色谱检测容器中乙烯的浓度[12],计算乙烯生成速率[nmol/(mL·min)],来反映乙烯还原活性。
1.3.5 固氮菌株培养条件优化
将分离筛选鉴定后的固氮菌株接种到液态改良阿斯贝(Ashby)无氮培养基进行培养,进行Plackett-Burman试验设计如表1,以菌种生长量OD600nm值为响应值,以培养温度、初始pH值、培养时间、接种量、摇床转速、装液量(250 mL摇瓶)、葡萄糖添加量、混菌培养柠檬酸废弃物添加量8个因素为因变量。接着进行Box-Behnken响应面优化试验[21],从而得出固氮菌株的最优培养条件。
表1 固氮菌株培养条件优化Plackett-Burman试验设计
Table 1 Plackett-burman tests design for culture conditions optimization of nitrogen-fixing becteria

2 结果与分析
2.1 牛蒡根内生固氮菌的分离、筛选及鉴定
2.1.1 固氮菌株乙炔还原活性测定结果
表征菌株固氮能力强弱的最重要的指标之一就是乙炔还原活性,牛蒡根经过表面消毒、研磨、分离和筛选,最终在改良阿斯贝(Ashby)无氮固体培养基上得到116个纯菌落,其培养24 h时的乙炔还原活性见图1。由图1可知,菌株NF-008、NF-024、NF-072、NF-096、NF-112的乙炔还原活性较高,其中菌株NF-112还原活性最高,乙烯生成速率为682.27 nmol/(mL·min)。
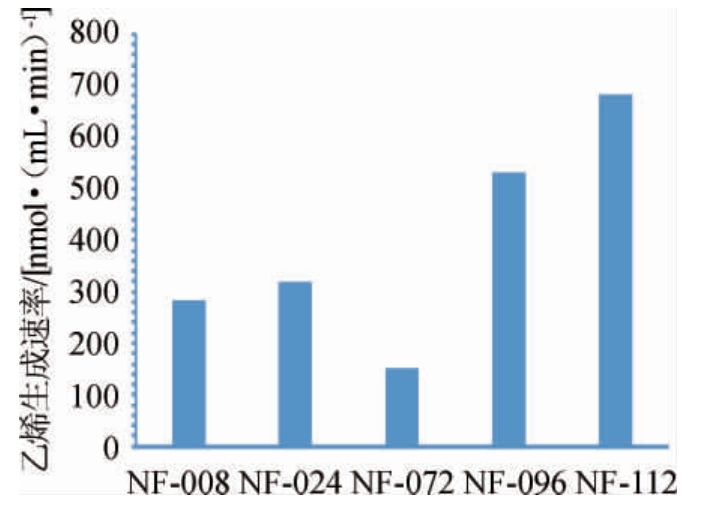
图1 固氮菌株的乙炔还原性
Fig.1 Acetylene reducibility of nitrogen-fixation strains
2.1.2 固氮菌株形态观察及生理生化特性测定结果
(1)菌株形态学观察
菌株NF-112的菌落形态和显微形态见图2。由图2可知,菌株NF-112的革兰氏染色呈阴性,显微镜下呈棒状,大小约(0.6~1.0)μm×(1.2~2.0)μm,单生或成对、成短链存在,菌株有荚膜、菌毛,无鞭毛,无芽孢。
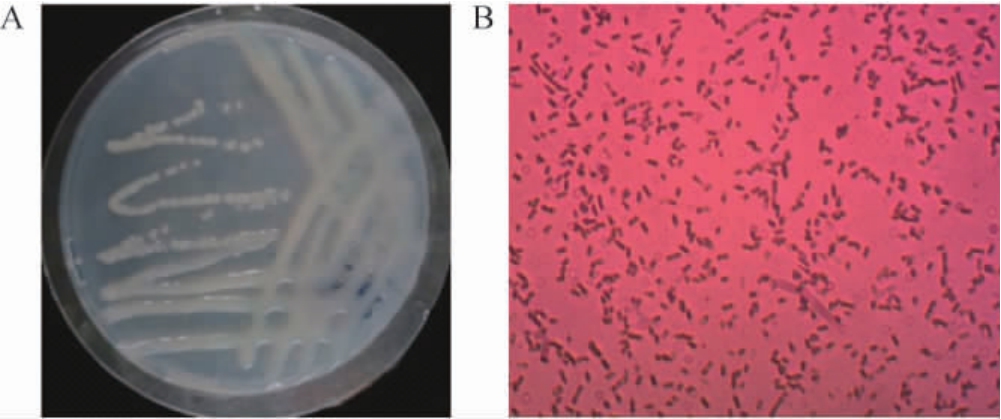
图2 菌株NF-112的菌落(A)及细胞(B)形态
Fig.2 Colony (A) and cell (B) morphology of strain NF-112
(2)生理生化试验
菌株NF-112的生理生化特性特性见表2。
表2 菌株NF-112生理生化特性
Table 2 Physiological-biochemical characteristics of strain NF-112

注:“+”表示结果呈阳性,“-”表示结果呈阴性。
由表2可知,菌株NF-112可以以葡萄糖、乳糖、半乳糖、蔗糖作碳源,以L-酪氨酸作氮源,但不能以淀粉、柠檬酸、甘露醇作为碳源,不能以L-苯丙氨酸、L-组氨酸、L-亮氨酸作为氮源;V-P试验不显示红色,表明菌株NF-112不具有丙酮酸脱羧酶;脲酶试验显示红色为阳性,表明菌株NF-112代谢过程中产丙酮酸脱羧酶;甲基红反应不显红色,呈阴性;吲哚反应显红色,呈阳性,表明菌株NF-112代谢过程中能产生色氨酸酶。接触酶试验无气泡产生,呈阴性;氧化酶试验不变色,呈阴性;产氨试验出现黄色沉淀,呈阳性;产H2S试验不变色,呈阴性;硝酸盐还原试验无颜色改变,呈阴性。
2.1.3 菌株NF-112的16S rDNA基因鉴定结果
菌株NF-112的16S rDNA琼脂糖凝胶电泳图见图3。从图3可以看出,菌株NF-112的PCR扩增产物在1.5 kbp处有一条明亮的条带,说明基因片段纯度较高,DNA长度大约是1.5 kbp。经检测,菌株NF-112的16S rDNA长度为1 488 bp。将测序结果和NCBI数据库进行比对,从NCBI数据库中选取与菌种NF-112同源性大约95%作为模式菌种,通过邻接法(neighbor-joining,NJ)构建系统进化树,结果见图4。从图4可以看出,菌株NF-112与克雷伯菌属(Klebsiella)的亲缘关系最近,相似性都>99%。根据菌株NF-112的菌落特征、显微观察特征、生理生化特性以及16S rDNA序列分析结果,将菌株NF-112鉴定为肺炎克雷伯氏菌(Klebsiellapneumoniae)。
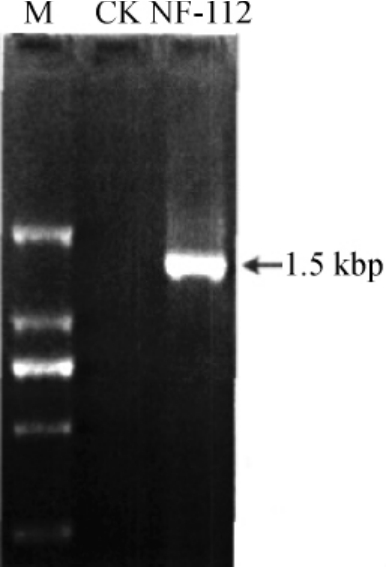
图3 菌株NF-112的16S rDNA基因的PCR扩增产物的琼脂糖凝胶电泳图
Fig.3 Agarose gel electrophoresis electrophoretogram of 16S rDNA gene of strain NF-112 by PCR amplification
M为Marker,CK为空白对照。

图4 菌株NF-112的16S rDNA系统进化树
Fig.4 16S rDNA phylogenetic tree of strain NF-112
2.2 响应面法优化菌株NF-112培养条件
2.2.1 影响菌株NF-112培养关键因素的确定
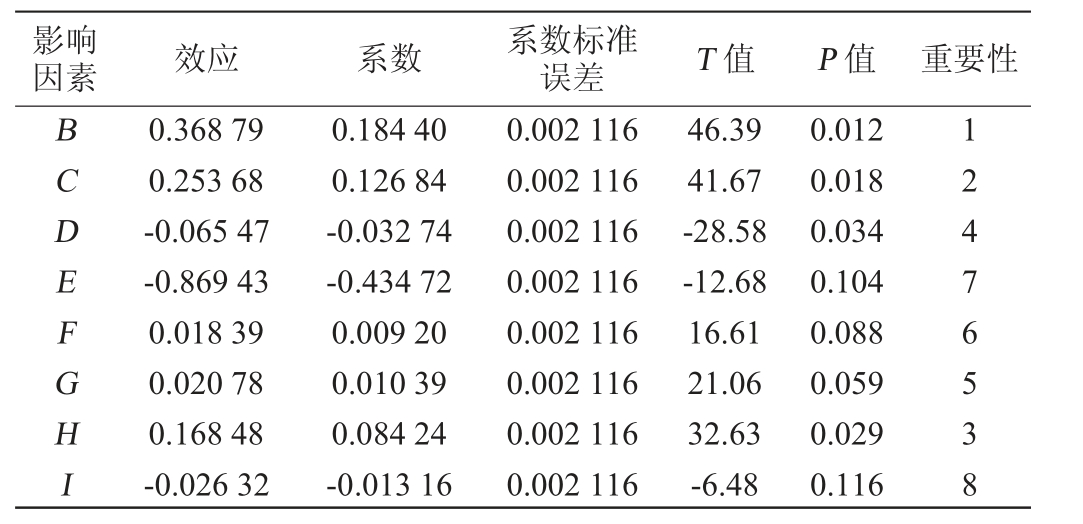
对影响菌株NF-112培养的8个因素进行Plackett-Burman试验设计,利用软件Minitab 15对试验结果进行分析,试验分析的结果见表3,显著性分析结果见表4。从表3和表4可以看出,影响菌种NF-112培养生产8个因素的顺序为:B(培养温度)>C(初始pH值)>H(葡萄糖添加量)>D(培养时间)>G(摇床转速)>F(装液量)>E(接种量)>I(废弃物添加量),其中对培养过程影响较显著的因素有3个,分别为B(培养温度)、C(初始pH值)、H(葡萄糖添加量)。
表3 菌株NF-112培养条件优化的Plackett-Burman试验设计及结果
Table 3 Plackett-Burman tests design and results for culture conditions optimization of strain NF-112
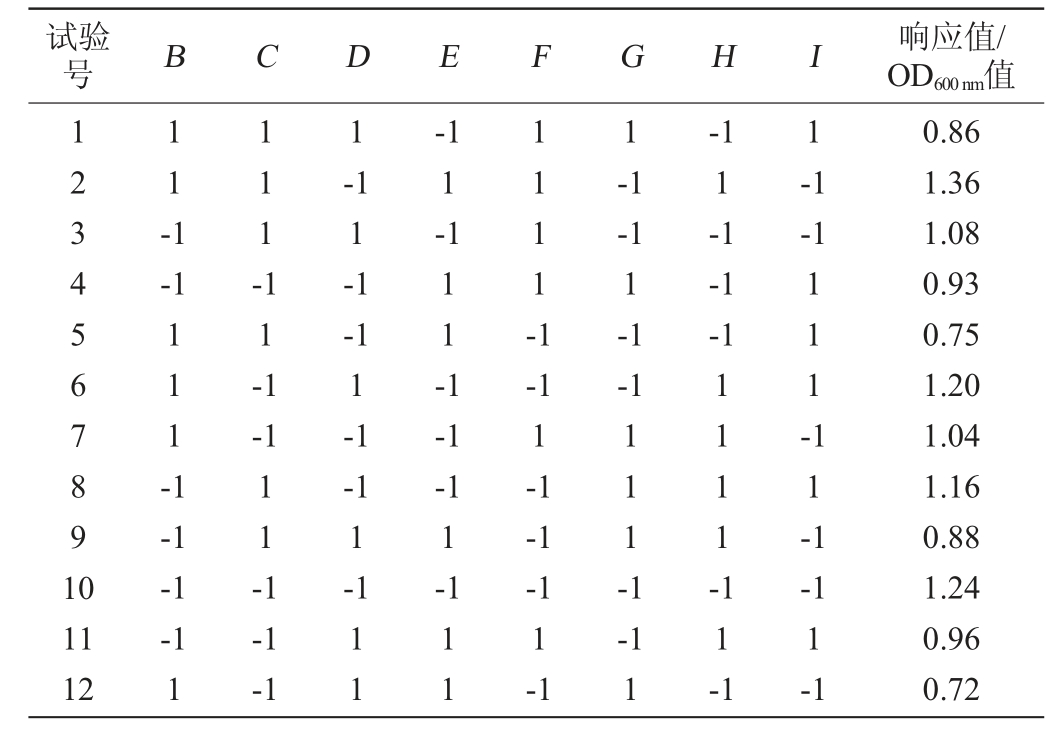
表4 Plackett-Burman试验显著性分析
Table 4 Significance analysis of Plackett-Burman experiments
2.2.2 菌株NF-112培养条件的优化
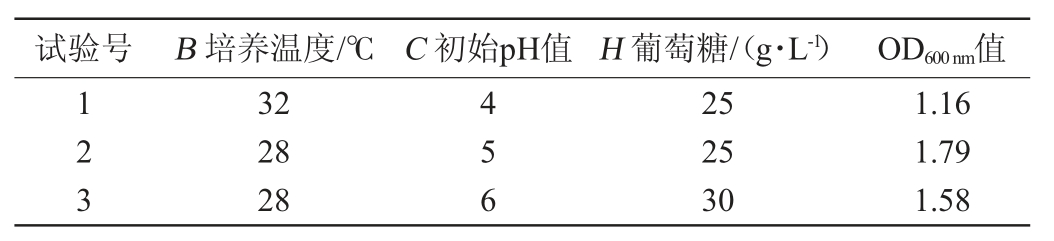
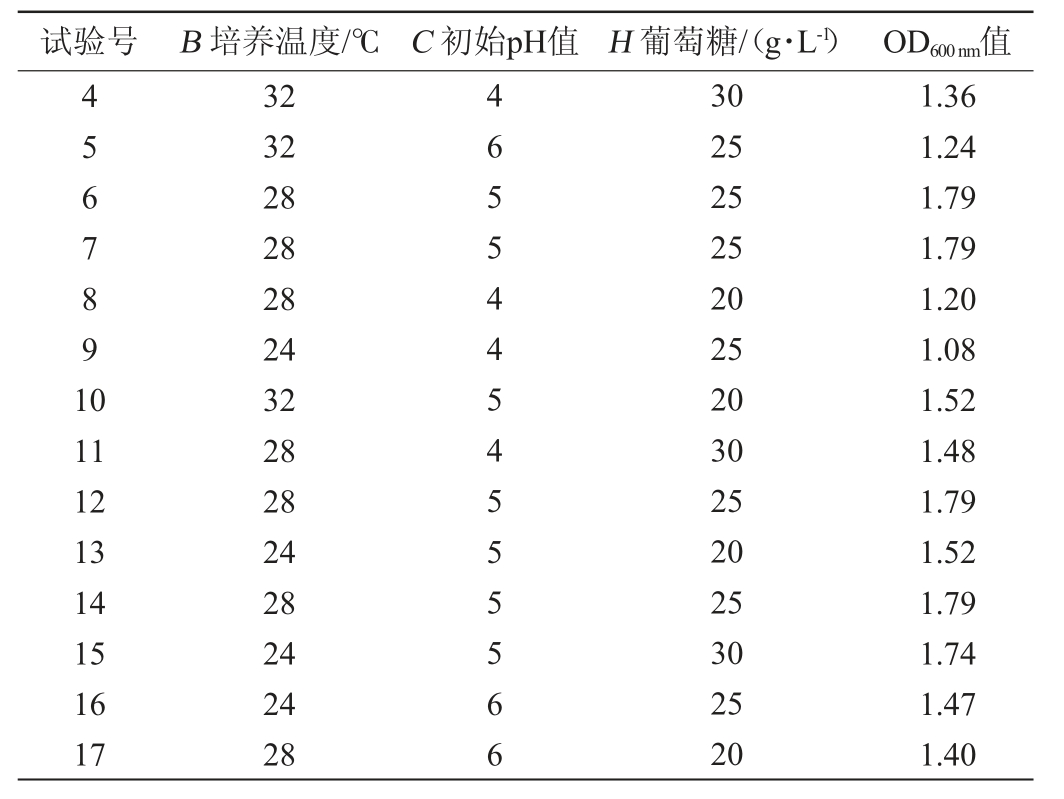
以培养温度、初始pH值和葡萄糖添加量为自变量,以OD600nm值为响应值,进行菌株NF-112培养条件优化3因素3水平的Box-Behnken试验设计[22],结果见表5。
使用统计软件Design Expert 8.0.6对表5结果进行多元回归拟合[23-26],所得二次多项式回归方程为:
表5 菌株NF-112培养条件优化Box-Benhnken试验设计及结果
Table 5 Design and results of Box-Benhnken tests for culture conditions optimization of strain NF-112
续表
2.2.3 回归模型方差分析
回归模型的方差分析结果见表6。
表6 回归模型方差分析
Table 6 Variance analysis of regression model

由表6可知,模型极显著(P<0.01),失拟项不显著(P>0.05),表明回归模型的拟合度较好。模型的决定系数R2=0.924 6,校正决定系数R2adj=0.911 6,表明所建模型和实际情况拟合程度高,可以真实反映3个因素对OD600nm值的影响。一次项B、C,交互项BC和二次项B2、C 2对结果影响极显著(P<0.01);二次项H2对结果影响显著(P<0.05);其他项相对结果影响不显著(P>0.05)。
2.2.4 响应面图的分析
初始pH值、培养温度、葡萄糖添加量交互作用对菌株NF-112培养液OD600nm值影响的响应面及等高线见图6。
从图6可以看出,B(培养温度)和C(初始pH值)2个因素交互作用对菌株NF-112培养的OD600nm值影响极显著(P<0.01),其余两组间交互作用不显著(P>0.05),这和回归模型方差分析结果一致。
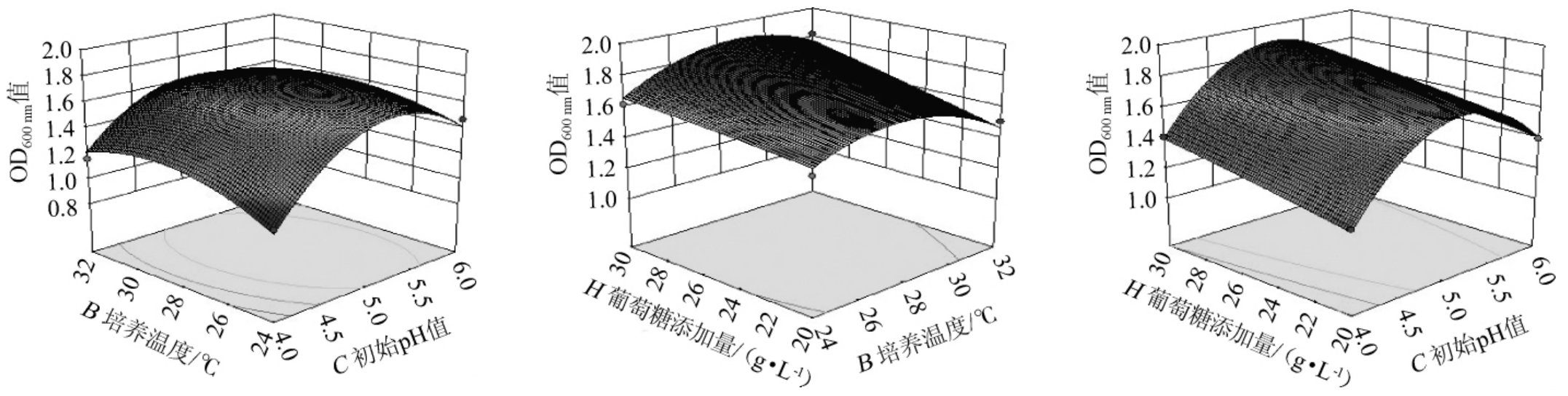
图5 各因素交互作用对菌株NF-112 OD600nm值影响的响应面及等高线
Fig.5 Response surface plots and contour lines of effect of interaction between each factors on OD600 nm value of strain NF-112
2.3 验证性试验
使用软件Design Expert 8.0.6对二次多项式回归方程求解,求得菌株NF-112培养最优条件为:初始pH值5.32、培养温度27.7 ℃、葡萄糖添加量26.2 g/L,预测OD600nm值为1.68。考虑实际成本及技术情况,最终确定最优处理条件为:初始pH值5.3、培养温度28 ℃、葡萄糖添加量26 g/L。在此最优培养条件下,OD600nm值为1.76,与预测值接近,说明回归模型和实际情况可以较好的拟合。
3 结论
固氮菌能通过自身的代谢系统把空气中无机氮转化为有机氮,可以为植物的生长提供氮素。该研究利用改良阿斯贝(Ashby)无氮选择培养基初筛和乙炔还原法复筛从牛蒡的根系中筛选出固氮能力较强的菌株NF-112,通过菌落特征和显微特性观察、生理生化特性测定及16S rDNA序列分析,初步鉴定为肺炎克雷伯氏菌(Klebsiella pneumoniae)。并且利用响应面方法研究了菌株NF-112的最优培养条件,最终确定最优培养条件为:初始pH值5.3、培养温度28 ℃、葡萄糖添加量26 g/L。在此最佳培养条件下,OD600nm值可达到1.76。本研究说明除了豆科和禾本科植物之外,其他植物体内也存在固氮微生物,为固氮微生物的工业化生产提供理论和技术支撑,也为下一步牛蒡专用生物有机肥的制备提供固氮菌剂。
[1]徐孝梁.牛蒡根有效成分工业化提取技术研究及牛黄饮料的制备[D].济南:齐鲁工业大学,2015.
[2]伏卉,杜丽君,牛先前,等.牛蒡保健饮料加工研究[J].食品研究与开发,2015,36(19):98-101.
[3]赵凯,马维红,赵娜,等.牛蒡提取物防治心血管疾病作用机制的研究现状[J].山东医药,2015,55(14):96-98.
[4]任媛媛,高晓光,祁琪,等.牛蒡多酚提取护色和提取工艺条件的优化研究[J].食品工业科技,2016,37(21):265-268.
[5]武兴友.微生物菌肥对农业生产的影响及研究趋势分析[J].中国果菜,2018(4):138-142.
[6]马鸣超,姜昕,曹凤明,等.生物有机肥生产菌种安全分析及管控对策研究[J].农产品质量与安全,2019(6):57-61.
[7]王琦,李文涛,张沛东,等.鳗草根际固氮菌的分离鉴定及培养条件的筛选[J].中国水产科学,2017,24(4):791-801.
[8]翟超男.内生固氮菌在海滨雀稗中的多样性和生理功能研究[D].广州:华南农业大学,2016.
[9]许沛东,赵艳,张晓波,等.草地早熟禾根际固氮菌的培养[J].草业科学,2014,31(6):1033-1038.
[10]尹坤,阳洁,顾文杰.岑溪药用野生稻高效内生固氮菌分离及促生特性[J].微生物学通报,2015,42(8):1482-1491.
[11]XING Y X,WEI C Y,MO Y,et al.Nitrogen-fixing and plant growth promoting ability of two endophytic bacterial strains isolated from sugarcane stalks[J].Suger Tech,2016,18(4):373-379.
[12]葛江丽,施汉钰,刘桂棋,等.水稻根际固氮菌分离及最适培养条件研究[J].东北农业科学,2018,43(4):53-56.
[13]马文彬,姚拓,王国基,等.根际促生菌筛选及其接种剂对箭筈豌豆生长影响的研究[J].草业学报,2014,23(5):241-248.
[14]李海云,姚拓,张榕,等.红三叶根际促生菌中具生防效果菌株筛选、鉴定及特性研究[J].植物营养与肥料学报,2018,24(3):743-750.
[15]李琬,刘淼,张必弦,等.植物根际促生菌的研究进展及其应用现状[J].中国农学通报,2014,30(24):1-5.
[16]李建宏,李雪萍,马文文,等.东祁连山高寒草地几种禾本科牧草根际促生菌研究[J].草业学报,2016,25(11):173-177.
[17]甄莉娜,王润梅,杨俊霞,等.丛枝菌根真菌与氮肥对羊草生长的影响[J].中国草地学报,2018,40(3):49-54.
[18]刘旭艳,石凤翎,刘昊,等.接种根瘤菌对苜蓿生长及土壤养分的影响[J].中国草地学报,2016,38(6):45-52.
[19]SUAREZ C,CARDINALE M,RATERING S,et al.Plant growth-promoting effects of Hartmannibacter diazotrophicus,on summer barley (Hordeum vulgare L.)under salt stress[J].Appl Soil Ecol,2015,95:23-30.
[20]AHEMAD M,KIBRET M.Mechanisms and applications of plant growth promoting rhizobacteria:Current perspective[J]. J King Saud Univ Sci,2014,26(1):1-20.
[21]SHRIVASTAVA P,KUMAR R.Soil salinity:A serious environmental issue and plant growth promoting bacteria as one the tools for its alleviation[J].Saudi J Biol Sci,2015,22(2):123-131.
[22]SHARMA S,KULKARNI J,JHA B.Halotolerant rhizobacteria promote growth and enhance salinity tolerance in peanut[J].Front Microbiol,2016,7:01600.
[23]LIU X L,LI X Y,LI Y,et al.Plant growth promotion properties of bacterial strains isolated from the rhizosphere of the Jerusalem artichoke(Helianthus tuberosus L.)adapted to salt-alkaline soils and their effect on wheat growth[J].Can J Microbiol,2017,63(3):228-237.
[24]COUTINHO B G,LICASTRO D,MENDONCA-PRECIATO L,et al.Plant-influenced gene expression in the rice endophyte Burkholderia kururienses M130[J].Mol Plant Microbe Interact,2015,28(1):10-21.
[25]李达,姜媛媛,周洋,等.饲用枯草芽孢杆菌高密度培养培养基的优化[J].东北农业科学,2016,41(2):104-108.
[26]王广慧,李士慧,梁婷,等.响应面优化超声波辅助复合酶法提取杏鲍菇黄铜[J].东北农业科学,2018,43(1):45-50.