鲊广椒又称鲊辣椒,通常是以大米面或玉米面、新鲜红辣椒碎和适量食盐为主要原料,经均匀混合后密封发酵制作而成的一种特色谷物发酵制品,烹饪后口感酸辣酥脆,在我国华中和西南地区有较广的食用人群[1]。有研究指出,微生物类群对鲊广椒的品质形成具有较大的影响[2-3],因而对鲊广椒的微生物多样性进行解析则极为必要。王玉荣等[2]采用第二代高通量测序技术对湖北省宜昌市当阳地区鲊广椒中细菌多样性进行了解析,结果发现乳酸杆菌属(Lactobacillus)、魏斯氏菌属(Weissella)和戊糖片球菌属(Pediococcus)等乳酸菌为其中主要的优势菌属,同时葛东颖等[4]研究发现,接种乳酸菌纯种发酵后能明显提升鲊广椒的酸味品质。值得一提的是,本研究团队前期从湖北省宜昌市当阳地区和恩施土家族苗族自治州鲊广椒中各分离鉴定出了一株乳酸杆菌新物种,分别命名为鲊广椒乳酸杆菌(L.zhachilii)[5]和恩施乳酸杆菌(L.enshiensis)[6]。由此可见,鲊广椒中可能蕴含了较为丰富和独特的乳酸菌菌群资源,加之不同地区的鲊广椒其微生物类群可能存在一定的差异[7],因而对不同地区鲊广椒中乳酸菌资源进行收集,同时对其微生物类群进行解析,对后续传统谷物发酵食品的产业化推动具有一定的作用。
虽然发酵食品中蕴含的部分微生物菌株无法在实验室条件下分离得到[8],但传统微生物学手段目前依旧是进行微生物菌株分离和鉴定的常用方法。第二代测序技术的出现弥补了传统微生物学手段的不足,可对发酵食品中可培养和不可培养微生物的类群进行全面解析,实现了不同样品间微生物群落的平行比较[9],该技术在辣椒酱[10]、泡菜[11]和腐乳[12]等发酵食品微生物群落结构解析中有着广泛的应用。由此可见,将两种技术相结合用于谷物发酵食品的微生物类群解析是较为可行的。
湖北省宜昌市秭归县位于长江上游末端,当地居民制作的鲊广椒以玉米面为主,目前有关该地区鲊广椒细菌多样性的研究还未见报道。本研究在采用传统微生物学方法对秭归地区鲊广椒中乳酸菌进行分离和鉴定的基础上,进一步采用MiSeq高通量测序技术对其细菌多样性进行解析,以期为后续我国传统谷物发酵食品的产业化推动提供数据支撑。
1 材料与方法
1.1 材料与试剂
鲊广椒样品:纳入本研究的14份鲊广椒样品均于2019年1月采集于湖北省宜昌市秭归县(E110°18'~111°0',N30°38'~31°11')的橘颂市场和山水龙城市场,所有样品均以玉米为主要原料且在当地制作和销售,发酵时间在25~30 d,分别编号为ZG1~ZG14。
MRS培养基、LB培养基:青岛海博生物技术有限公司;Axygen清洁试剂盒:康宁生命科学吴江有限公司;DNeasy mericon Food Kit 脱氧核糖核酸(deoxyribonucleic acid,DNA)基因组提取试剂盒:德国QIAGEN公司;10×Buffer、脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphates,dNTPs)Mix和DNA聚合酶:北京全式金生物技术有限公司;引物338F/806R和M13F(-47)/M13R(-48):天一辉远(武汉)生物科技有限公司;大肠杆菌(Escherichia coli)Top10:湖北文理学院鄂西北传统发酵食品研究所自制。
1.2 仪器与设备
DG250型厌氧工作站:英国DonWhitley公司;VeritiFAST梯度聚合酶链式反应(polymerase chain reaction,PCR)仪:美国ABI公司;164-5050基础电泳仪:美国BIO-RAD公司;UVPCDS8000凝胶成像分析系统:美国Protein Simple公司;Illumina MiSeq PE250高通量测序平台:美国Illumina公司;R920型机架式服务器:美国DELL公司。
1.3 方法
1.3.1 乳酸菌的分离鉴定
采用倍比稀释涂布法对鲊广椒中疑似乳酸菌菌株进行初分离,继而通过平板划线法对分离株进行纯化,将过氧化氢酶阴性且革兰氏阳性的菌株做成甘油管于-80 ℃保藏[4]。后续菌株DNA的提取、PCR扩增、清洁和连接转化均参照葛东颖等[4]的方法进行操作。将扩增成功的阳性克隆子送至天一辉远(武汉)生物科技有限公司进行测序,返回的序列在美国国家生物信息中心(national center for biotechnology information,NCBI)网站进行比对[13],并完成系统发育树的构建。
1.3.2 宏基因组DNA的提取、PCR扩增和高通量测序
鲊广椒宏基因组DNA的提取:每份鲊广椒样品分别称取2 g,参照基因组提取试剂盒说明方法提取总DNA。
PCR扩增和高通量测序:使用添加barcode(核苷酸标签)的引物338F/806R对鲊广椒中细菌16S rRNA V3-V4区进行PCR扩增,扩增体系和程序均参照沈馨等[14]的方法。扩增完成后,将扩增产物寄至上海美吉生物医药科技有限公司测序。
1.3.3 序列质控和生物信息学分析
反馈回的序列fq文件,参照沈馨等[14]的方法对序列进行拼接和质控,将质控合格的fasta序列文件上传至QIIME1分析平台进行生物信息学分析。采用两步UCLUST法(100%和97%相似度)进行序列归并和构建操作分类单元(operational taxonomic units,OTU)[15],删除含有嵌合体序列的OTU[16],选择余下OTU代表性序列在SILVA[17]、RDP[18]和Greengenes[19]数据库中进行序列比对,并在门和属水平注释其分类学地位。
1.3.4 数据处理
使用R软件构建系统发育树,使用Excel2016绘制瀑布图,使用Origin2017软件绘制柱形图。
2 结果与分析
2.1 鲊广椒中乳酸菌分离鉴定及其多样性分析
经倍比稀释后的样品厌氧培养36~48 h后,在含有1.0% CaCO3的MRS固体平板中可观察到已形成较多单菌落。本研究将菌落周围存在透明圈、革兰氏染色呈阳性和过氧化氢酶呈阴性的菌株初步判定为乳酸菌,共分离得到了43 株疑似乳酸菌菌株。部分分离株菌落形态及细胞形态见图1。
由图1A可知,分离的部分菌株其菌落颜色均呈现白色或乳白色,表面光滑湿润,且周围均有透明圈形成。图A1和A3中的菌落透明圈明显要比图A2中的透明圈透明程度更大,这表明不同菌株其产酸的能力有所差异。由图1B可知,分离菌株的细胞形态均属于短杆状。各乳酸菌分离株的系统发育树见图2。
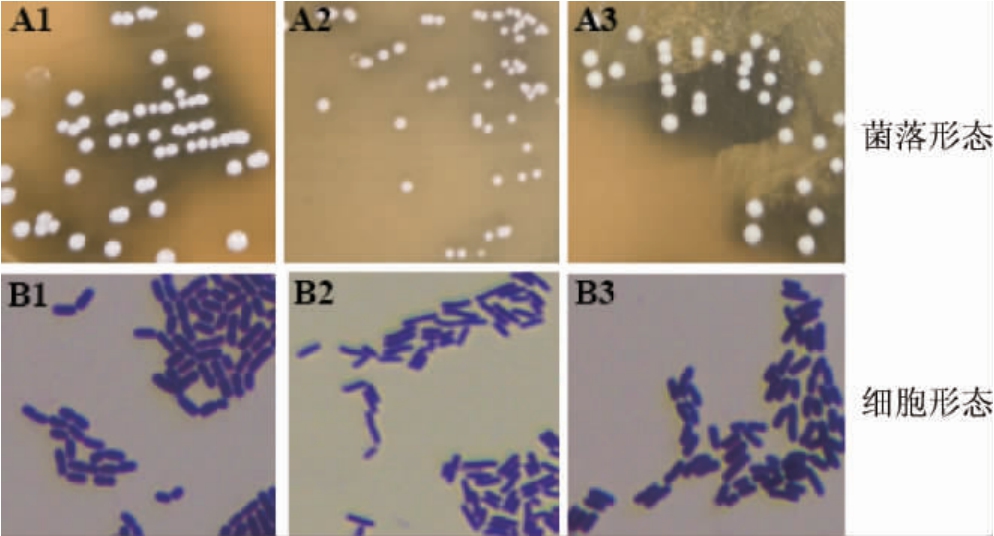
图1 部分疑似乳酸菌分离株的菌落形态(A)及细胞形态(B)
Fig.1 Colony morphology (A) and cell morphology (B) of some suspected lactic acid bacteria strains
A1和B1分别为菌株HBUAS56187的菌落形态和细胞形态;A2和B2分别为菌株HBUAS56163的菌落形态和细胞形态;A3和B3分别为菌株HBUAS56193的菌落形态和细胞形态。细胞形态放大了1 000 倍。
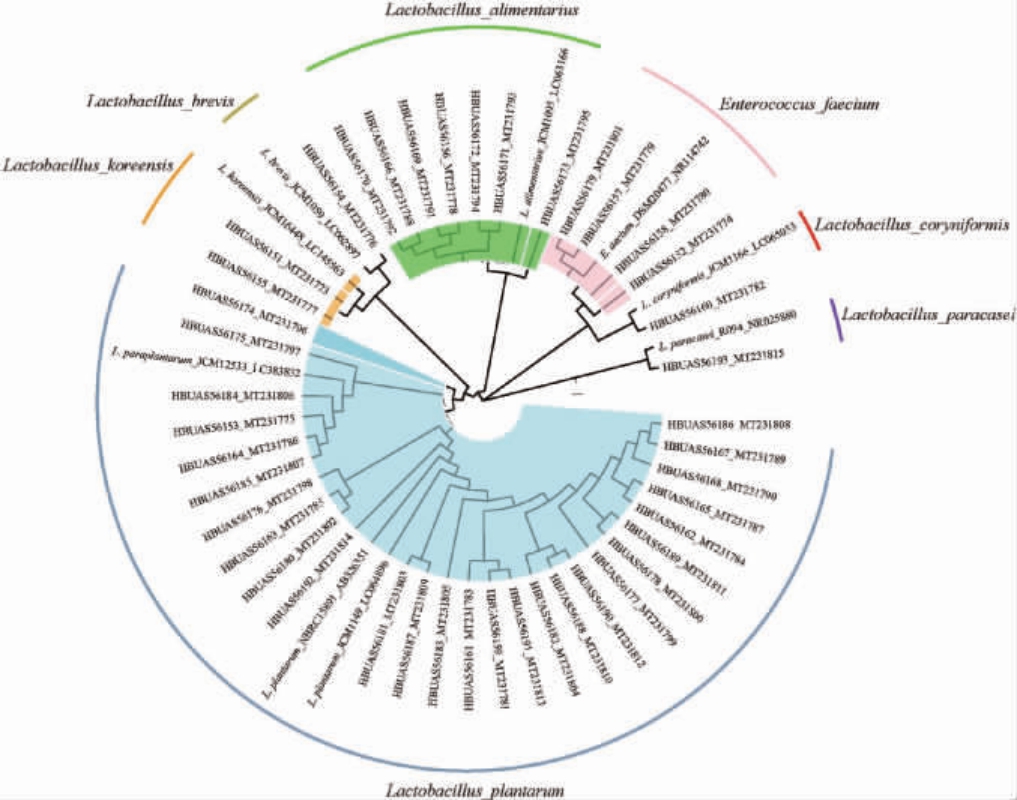
图2 乳酸菌分离株的系统发育树
Fig.2 Phylogenetic tree of isolated lactic acid bacteria strains
由图2可知,43株分离株中有27株鉴定为植物乳杆菌群,其中21株鉴定为植物乳杆菌(Lactobacillus plantarum),6株鉴定为副植物乳杆菌(L.paraplantarum),其余分离株中7株鉴定为消化乳杆菌(L.alimentarius),4株鉴定为屎肠球菌(Enterococcus faecium),2株鉴定为韩国乳杆菌(L.koreensis),各有1 株鉴定为短乳杆菌(L.brevis)、棒状乳杆菌(L.coryniformis)和副干酪乳杆菌(L.paracasei)。由此可见,秭归地区鲊广椒中的乳酸菌分离株主要隶属于乳酸杆菌属(Lactobacillus)和屎肠球菌属(Enterococcus)。分离株中各乳酸菌类群的构成情况见图3。
由图3可知,L.plantarum是秭归地区鲊广椒中的优势乳酸菌,相对含量达60.47%;其次是L.alimentarius、E.faecium和L.koreensis,相对含量分别为16.28%、9.30%和4.65%;L.brevis、L.coryniformis、L.paraplantarum和L.paracasei相对含量最低,均为2.33%。在对湖北省荆州地区鲊广椒乳酸菌类群进行解析时,本研究团队亦发现L.plantarum为其优势菌种[4],这与本研究结果相同。有研究发现乳酸菌对谷物发酵食品的营养特性及抗营养因子具有一定影响,ROGER T等[20]研究发现L.plantarum A6能够降低发酵玉米糊中单宁成分的含量,而部分L.brevis则可以提高玉米糊中还原糖或淀粉的含量。
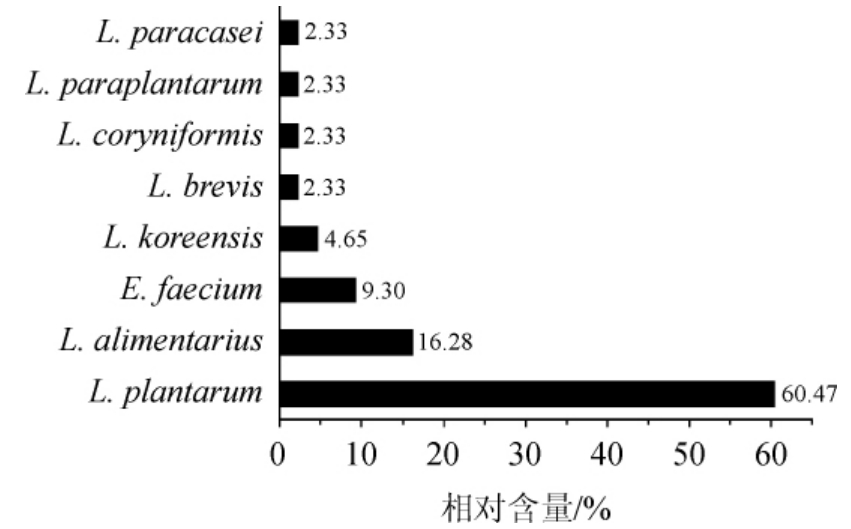
图3 乳酸菌分离株中各类群的构成情况
Fig.3 Composition of various groups among lactic acid bacteria strains
2.2 基于门和属水平的鲊广椒细菌多样性分析
在对鲊广椒中乳酸菌分离鉴定的基础上,本研究采用MiSeq高通量测序[21]进一步对样品中细菌的多样性进行了解析。因有4个样品微生物基因组提取质量偏低,不符合建库要求,故仅对10个样品进行了高通量测序。MiSeq结果显示,10个鲊广椒经测序共得到了201 854条高质量序列,每个样品平均含有20 185条,有效序列经97%相似度划分后得到了6 404个OTU,每个样品平均含有796个OTU。本研究将平均相对含量大于1.0%的门和属定义为优势门和属[22],10 个鲊广椒的优势门相对含量见图4。
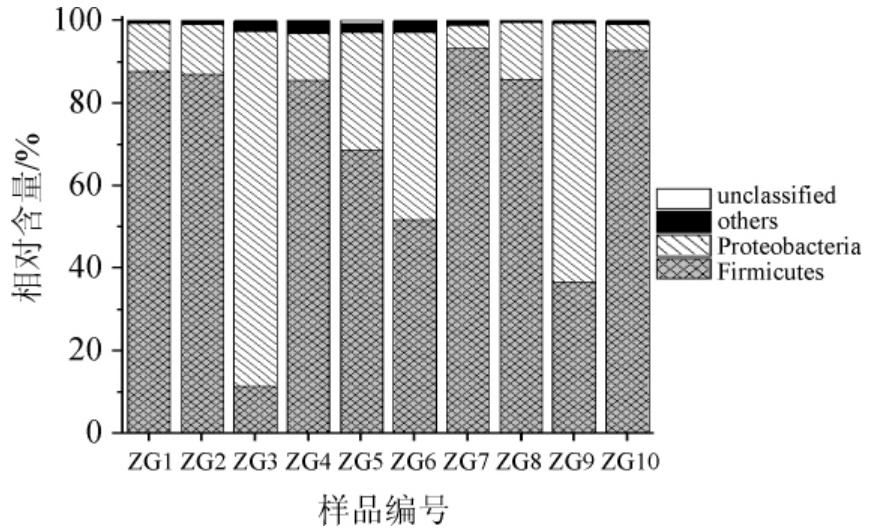
图4 鲊广椒中优势细菌门的相对含量
Fig.4 Relative contents of dominant bacterial phyla in Zha-chili
由图4可知,硬壁菌门(Firmicutes)和变形菌门(Proteobacteria)为鲊广椒中的优势细菌门,其平均相对含量分别为70.02%和28.38%。在样品ZG3和ZG9中Proteobacteria为相对含量最高的优势门,相对含量分别为86.13%和62.62%;而在其余8 个样品中Firmicutes为相对含量最高的优势门,其相对含量范围在51.64%~93.30%之间。由此可见,各鲊广椒的细菌类群可能存在一定的差异,而这种差异在门水平上就有所体现。本研究进一步对鲊广椒中优势属的相对含量进行了分析,结果见图5。
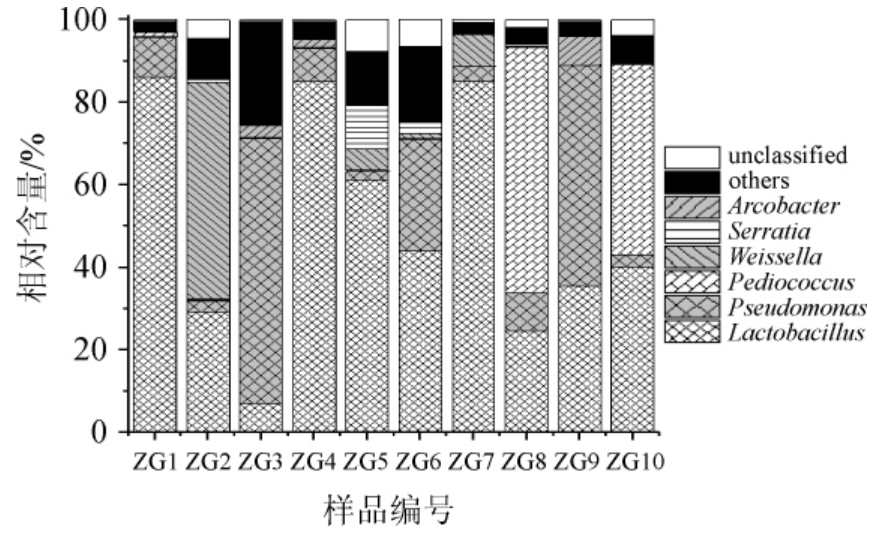
图5 鲊广椒中优势细菌属的相对含量
Fig.5 Relative contents of dominant bacterial genera in Zha-chili
由图5可知,隶属于Firmicutes的Lactobacillus(47.85%)、Pediococcus(13.29%)和Weissella(1.81%),隶属于Proteobacteria的假单胞菌属(Pseudomonas)(21.31%)、沙雷菌属(Serratia)(1.80%)和弓形杆菌属(Arcobacter)(1.54%)为鲊广椒中的优势属,其中Lactobacillus、Pediococcus和Weissella均为乳酸菌,累计含量达到62.95%。由此可见,秭归鲊广椒中蕴含着较为丰富的乳酸菌资源。由图5亦可知,在样品ZG3和ZG9中Pseudomonas的含量较高,分别为64.16%和53.37%。有大量研究表明Pseudomonas是发酵食品中的一类微生物污染物,防止Pseudomonas污染是提高食品安全性的重要方面[23-24]。除此之外,鲊广椒中还含有少量的Serratia,WANG X Q等[25]的研究指出粘质沙雷氏菌(Serratia marcescens)会导致玉米作物患有轮纹斑病,因而鲊广椒中含有少量Serratia的原因极有可能是农户制作鲊广椒时使用的原料中夹杂了部分患有轮纹斑病的玉米作物。
2.3 基于OTU水平的鲊广椒细菌多样性分析
本研究将平均相对含量大于1.0%的OTU定义为优势OTU[22],鲊广椒中优势OTU的相对含量见图6。
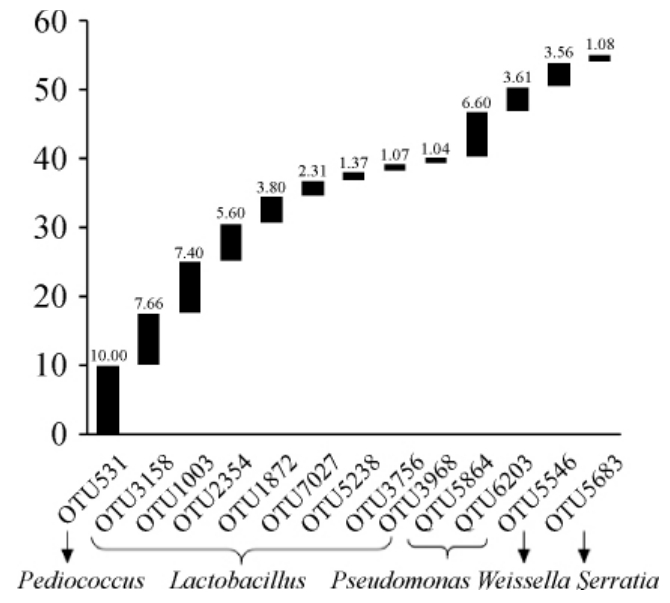
图6 鲊广椒中优势操作分类单元(OTU)的相对含量
Fig.6 Relative contents of dominant operational taxonomic unit in Zha-chili
由图6可知,测序的10个鲊广椒中共含有13个优势OTU,平均累计相对含量达到55.10%,其中OTU531被鉴定为Pediococcus,平均相对含量为10.00%;OTU3158、OTU1003、OTU2354、OTU1872、OTU7027、OTU5238、OTU3756和OTU 3968均被鉴定为Lactobacillus,平均累计含量达30.25%;OTU5864和OTU6203被鉴定为Pseudomonas,平均累计含量为10.21%;OTU5546和OTU5683分别被鉴定为Weissella和Serratia,平均相对含量为3.56%和1.08%。综上所述,各鲊广椒样品中乳酸菌的平均累计相对含量达到43.81%。由此可见,乳酸菌是鲊广椒中的核心类群,但Pseudomonas在所有样品中均占有一定的比例,这也进一步说明在后续鲊广椒产业化推动进程中积极开展具有优良发酵特性乳酸菌的筛选,同时通过加强原料质量的监管和生产环境的改良,积极探索提升鲊广椒食用安全品质的路径是极为必要的。
3 结论
本研究采用传统生物学方法和MiSeq高通量测序技术分别对秭归鲊广椒中乳酸菌和细菌多样性进行了解析。结果显示,分离的乳酸菌菌株主要隶属于Lactobacillu和Enterococcus,且L.plantarum为其中的优势菌种。高通量测序结果显示,鲊广椒中主要的细菌类群为隶属于Firmicutes的Lactobacillus和Pediococcus以及隶属于Proteobacteria的Pseudomonas。由此可见,秭归鲊广椒中蕴含着较为丰富的乳酸菌资源,同时也含有一定量的条件致病菌。
[1]尚雪娇,雷炎,代凯文,等.当阳地区鲊广椒品质的评价[J].食品研究与开发,2018,39(24):33-38.
[2]王玉荣,沈馨,董蕴,等.鲊广椒细菌多样性评价及其对风味的影响[J].食品与机械,2018,34(4):25-30.
[3]王玉荣,代凯文,沈馨,等.鲊广椒真菌多样性及其对滋味品质影响的评价[J].食品科学,2018,39(18):173-178.
[4]葛东颖,王玉荣,向凡舒,等.荆州地区鲊广椒乳酸菌多样性解析及其分离株发酵特性的评价[J].中国食品添加剂,2019,30(4):72-79.
[5]ZHANG Z D,HOU Q C,WANG Y R,et al.Lactobacillus zhachilii sp.nov.,a lactic acid bacterium isolated from Zha-Chili[J].Int J Syst Evol Microbiol,2019,69(8):2196-2201.
[6]ZHANG Z,WANG Y,HOU Q,et al. Lactobacillus enshiensis sp.nov.,a novel arsenic-resistant bacterium[J].Int J Syst Evol Microbiol,2020,70(5):2580-2587.
[7]李娜,张苗苗,舒娜,等.咸丰和当阳地区鲊广椒细菌群落结构差异性研究[J].中国酿造,2020,39(10):48-53.
[8]SUN X D,LYU G Z,LUAN Y S,et al.Analyses of microbial community of naturally homemade soybean pastes in Liaoning province of China by Illumina MiSeq sequencing[J].Food Res Int,2018,111(9):50-57.
[9]DEREAKHSHANI H,TUN H M,KHAFIPOUR E.An extended single-index multiplexed 16S rRNA sequencing for microbial community analysis on MiSeq Illumina platforms[J].J Basic Microbiol,2016,56(3):321-326.
[10]武亚婷,杜木英,何欢欢,等.基于高通量测序技术分析新疆不同地区自然发酵辣椒酱微生物群落多样性[J].食品与发酵工业,2019,45(21):221-228.
[11]LIANG H P,YIN L G,ZHANG Y H,et al.Dynamics and diversity of a microbial community during the fermentation of industrialized Qingcai paocai,a traditional Chinese fermented vegetable food,as assessed by Illumina MiSeq sequencing,DGGE and qPCR assay[J].Ann Microbiol,2018,68(2):111-122.
[12]石黎琳,牟方婷,李安,等.基于高通量测序技术分析腐乳自然发酵过程微生物多样性[J].中国酿造,2021,40(2):144-149.
[13]PRUITT K D,TATIANA T,MAGLOTT D R.NCBI reference sequence(RefSeq):a curated non-redundant sequence database of genomes,transcripts and proteins[J].Nucleic Acids Res,2007,35:61-65.
[14]沈馨,王艳,代凯文,等.基于Miseq 高通量测序技术的辣椒酱核心细菌类群研究[J].食品研究与开发,2018,39(10):151-157.
[15]CALLAHAN B J,MCUMURDIE P J,HOLMES S P.Exact sequence variants should replace operational taxonomic units in marker-gene data analysis[J].ISME J,2017,11(12):2639-2643.
[16]HAAS B J,GEVERS D,EARL A M,et al.Chimeric 16S rRNA sequence formation and detection in Sanger and 454-pyrosequenced PCR amplicons[J].Genome Res,2011,21(3):494-504.
[17]YILMAZ P,PARFREY L W,YARZA P,et al.The SILVA and"all-species living tree project (LTP)" taxonomic frameworks[J]. Nucleic Acids Res,2014,42:643-648.
[18]COLE J R,WANG Q,FISH J A,et al.Ribosomal database project:Data and tools for high throughput rRNA analysis[J].Nucleic Acids Res,2014,42(1):633-642.
[19]ANUKAM K C.Effects of ampicillin on the gut microbiome of an adult male as determined by 16S rRNA V4 metagenomics sequencing and green genes bioinformatics suite[J].J Adv Microbiol,2017,7(4):1-18.
[20]ROGER T,LÉOPOLD T N,FUNTONG M C M.Nutritional properties and antinutritional factors of corn paste(Kutukutu)fermented by different strains of lactic acid bacteria[J].Int J Food Sci,2015:502910.
[21]SHARMA G.Pros and cons of different sampling techniques[J].Int J Appl Res,2017,3(7):749-752.
[22]ZHANG J C,GUO Z,XUE Z S,et al.A Phylo-functional core of gut microbiota in healthy young Chinese cohorts across lifestyles,geography and ethnicities[J].ISME J,2015,9(9):1979-1990.
[23]MASKE B L,PEREIRA G V M,NETO D P C,et al.Presence and persistence of Pseudomonas sp.during Caspian sea-style spontaneous milk fermentation highlights the importance of safety and regulatory concerns for traditional and ethnic foods[J].Food Sci Technol,2020(10):1-11.
[24]OLMO A,CALZADA J,NUÑEZ M.The blue discoloration of fresh cheeses:A worldwide defect associated to specific contamination by Pseudomonas fluorescens[J].Food Control,2018,86(4):359-366.
[25]WANG X Q,BI T,LI X D,et al.First report of corn whorl rot caused by Serratia marcescens in China[J].J Phytopa,2015,163(11-12):1059-1063.