益生菌是指一类活的微生物,当摄取足够数量时,对宿主产生一种或多种特殊且确切的功能性健康益处[1-2],这与当前通用的联合国粮农组织(food and agriculture organization of the united nations,FAO)和世界卫生组织(world health organization,WHO)对益生菌的定义相近[3]。2010年4月,卫生部印发了初版可食用菌种名单,包括双歧杆菌属(Bifidobacterium)、乳杆菌属(Lactobacillus)、链球菌属(Streptococcus)在内的三个菌属大类的21种菌种,随后对名单进行了多次更新及丰富。截止2017年12月,明确可以用于食品的益生菌已有10个属共计35种。目前,国内市场益生菌菌株90%以上被国外公司所垄断,国内主要由江南大学的陈卫院士和内蒙古农业大学的张和平老师团队进行益生菌筛选,筛选菌株大多通过生理生化实验、16S rDNA测序、全基因测序来进行鉴定,选育的益生菌多属双歧杆菌属(Bifidobacterium)、乳杆菌属(Lactobacillus)、链球菌属(Streptococcus)、乳球菌属(Lactococcus)、芽孢杆菌属(Bacillus)等[4-5]。作为益生菌必须要满足两个条件,一是能够在人体胃肠道内存活,具有耐酸、耐胆盐能力,以及分解胆固醇和抗氧化性等重要的益生功能[6];二是可以高密度培养,收集大量菌体,益生菌的高密度培养技术需要优化一系列相关的工艺参数来对发酵过程进行严格的控制。植物乳杆菌(Lactobacillus plantarum)属于乳杆菌属,革兰氏阳性、厌氧或兼性厌氧、最适生长温度为30~35 ℃,常见于乳品、奶油、肉类、发酵果蔬中,也存在于人的肠道内[7]。研究表明,植物乳杆菌(L.plantarum)具有调节肠道菌群、改善乳糖不耐受、提高免疫力、降低胆固醇、降低血压、清除自由基抗氧化等功效[8-11]。于长青等[12]对两株植物乳杆菌进行紫外线诱变处理后,得到了2株具有强降胆固醇能力同时性能较稳定的突变菌株,胆固醇的降解率分别为48.7%和44.2%。张凤敏等[13]从发酵食品中分离出2株能耐受1 mmol/L过氧化氢的植物乳杆菌,试验显示细胞浓度为109 CFU/mL的L1001完整细胞与无细胞提取物的DPPH自由基(1,1-diphenyl-2-picrylhydrazylradical,DPPH·)清除率分别为36.2%和37.9%。由于植物乳杆菌(L.plantarum)在调节肠道微生物、维护人体健康方面的影响,其在食品发酵、乳品工业、医疗保健等领域都有广泛应用[14-15]。本研究为获得性能优良的益生菌生产菌株,通过乳酸菌的溶钙圈筛选,耐酸、耐胆盐检测及体外抗氧化和分解胆固醇能力测试进行了菌株的选育;对筛选菌株进行16S rRNA基因测序及生理生化特性鉴定;采用正交试验优化培养基配方和发酵条件,并对发酵特性研究,实现菌体高密度发酵,为其在益生菌产业中的应用奠定基础。
1 材料与方法
1.1 材料与试剂
菌株:分离于山西维尔生物乳制品有限公司生牛乳储藏罐中。
脱氧核糖核酸(deoxyribonucleic acid polymerase,DNA)聚合酶、T4DNA连接酶、脱氧核糖核酸三磷酸(deoxy-ribonucleosidetriphosphate,dNTP)、MgCl2、ExTaqDNA聚合酶、DNA Marker、克隆载体pMD18-T、DNA胶回收试剂盒、DMEGA细菌DNA提取试剂盒:大连Takara公司;牛胆酸钠(分析纯):北京Solarbio科技有限公司。其他试剂均为进口或国产分析纯。
MRS培养基、LB培养基:赛默飞世尔科技(中国)有限公司;MRS碳酸钙培养基:MRS 培养基中加入20 g/L的碳酸钙;高胆固醇MRS培养基:MRS 培养基中加入0.1 g/L的胆固醇及3 g/L的牛胆酸钠。
1.2 仪器与设备
BJ-2CD超净工作台、YXQ-70A立式压力蒸汽灭菌器、SPX-150B-Z生化培养箱:上海博迅医疗生物仪器股份有限公司;FE28-standard PH计:瑞士梅特勒-托利多公司;MTV-1漩涡振荡器:杭州奥盛仪器有限公司;H1850R冷冻离心机:湖南湘仪实验室仪器开发有限公司;Minispin plus高速离心机:德国艾本德股份公司;DK-8D电热恒温水浴槽:常州诺基仪器有限公司;UV-1500紫外分光光度计:上海美析仪器有限公司;Masterecycler nexus GX2聚合酶链式反应(polymerase chain reaction,PCR)仪:德国艾本德股份公司;C-32 厌氧培养盒:日本三菱瓦斯化学株式会社。
1.3 方法
1.3.1 乳酸菌初筛
从山西维尔生物乳制品有限公司生牛乳储藏罐中收集残余牛乳于无菌三角瓶中,用灭菌生理盐水将牛乳样品稀释至10-5,取原液、10-1、10-3、10-5各0.1 mL涂布MRS碳酸钙培养基平板,35 ℃厌氧培养盒培养48 h,挑选溶钙圈比较大的单菌落,重复划线分离,挑选单菌落用200 mL/L甘油管-80 ℃保藏备用[16]。
1.3.2 耐酸菌株筛选
将初筛的菌株按活菌数2×1010 CFU/mL的接种量接种于装有MRS液体培养基的试管中,35 ℃静置培养24 h,6000r/min离心8 min,收集菌体,灭菌生理盐水洗涤3次,最后悬浮为108 CFU/mL的菌悬液。调灭菌MRS液体培养基pH值为2.5,取10 mL分装试管。将调好菌浓度的菌悬液按1%(V/V)的量加入其中,混匀,37 ℃水浴放置。分别于0、2 h取1 mL用生理盐水做系列10倍稀释,取10-1、10-3、10-5各0.1 mL涂MRS 琼脂平板,35 ℃厌氧培养48 h,进行菌落计数,计算菌株耐酸生长率,其计算公式如下:
1.3.3 耐胆盐菌株筛选
分别配制含有0.5 g/L、1.0 g/L、2.0 g/L牛胆酸钠的MRS液体培养基,将各菌株以活菌数2×1010 CFU/mL的接种量依次接入以上培养基中35 ℃、16 h传代培养驯化,最后再接入MRS液体培养基中35 ℃培养24 h,6 000 r/mim离心8 min,收集菌体,灭菌生理盐水洗涤3次,最后悬浮为108 CFU/mL的菌悬液,取1 mL用生理盐水做系列10倍稀释,取10-1、10-3、10-5各0.1 mL涂布含有3.0 g/L牛胆酸钠和不含牛胆酸钠的MRS琼脂培养基平板,35 ℃厌氧培养48 h,进行菌落计数,计算菌株耐胆盐生长率,其计算公式如下:
1.3.4 抗氧化能力测试
(1)清除1,1-二苯基-2-三硝基苯肼自由基能力的测定
分别取1×108 CFU/mL、1×109 CFU/mL、1×1010 CFU/mL的细胞悬液2 mL,加入1 mL DPPH·溶液(0.2 mmol/L,以无水乙醇溶解),混合均匀,置于室温下避光反应30 min,6 000 r/min离心8 min,取上清,测定样品在波长517 nm处的吸光度值Ai,测3次取平均值。对照组样品以等体积蒸馏水代替细胞悬液,以等体积蒸馏水和无水乙醇混合液作参比[17-18]。DPPH·清除率计算公式如下:
式中:A0为对照组吸光度值;Ai为样品组吸光度值。
(2)清除羟自由基能力的测定
在10 mL具塞试管中依次加入1 mL FeSO4水溶液(5 mmol/L)、1 mL水杨酸-乙醇溶液(5 mmol/L)、1mL H2O2水溶液(3 mmol/L),混合均匀后向上述体系中加入1×108、1×109、1×1010 CFU/mL的细胞悬液2 mL,用双蒸水补齐至刻度,37 ℃水浴15 min,6 000 r/min离心8 min,以双蒸水作参比,在波长510 nm下测定吸光度A值,吸光度值数据平行测定3 次[13]。·OH清除率计算公式如下:
式中:A0为对照样品的吸光度值,Ax为加入待测乳酸菌细胞悬液的吸光度值。
1.3.5 分解胆固醇能力测试
挑选菌株经MRS培养基活化后,以活菌数5×1010CFU/mL的接种量接种于高胆固醇MRS-CHOL培养基中,35 ℃培养24 h,培养液6 000 r/min 离心8 min,取上清液,采用邻苯二甲醛比色法测定胆固醇含量[12,19]。胆固醇分解率计算公式如下:
式中:A0为未接菌对照的吸光度值,A为菌体培养后培养液的吸光度值。
1.3.6 乳酸菌鉴定
乳酸菌的形态学观察和生理生化实验:菌株的生理生化鉴定参照《常见细菌鉴定手册》和《微生物分类学》,观察各菌株的形态特征,并对菌株进行生理生化实验,对筛选菌株进行初步的分类鉴定[20]。
分子生物学鉴定:使用OMEGA细菌DNA提取试剂盒对培养菌株进行DNA提取,使用细菌16S rRNA通用引物F 5'-AGAGTTTGATCCTGGCTCAG-3';R 5'-AAGGAGGTGATCCAGCCGCA-3'进行聚合酶链式反应(polymerase chain reaction,PCR),纯化后的PCR回收产物与pMD18-T Vector连接,转化感受态细胞E.coli DH5α,质粒提取后由金唯智公司进行DNA序列的测定。将测得的DNA序列提交到GenBank美国国家生物技术信息中心(national center of biotechnology information,NCBI)进行基本局部比对,搜索工具(basic local alignment search tool,BLAST)。应用NCBI数据库的BLAST程序对序列进行聚类、应用Mega软件做基因序列系统发育树。
1.3.7 高密度发酵培养基优化正交试验
以MRS培养基为种子液,在MRS培养基配方的基础上,以磷酸氢二钾(A),柠檬酸氢二胺(B),乙酸钠(C),葡萄糖(D)添加量作为影响因素,在MRS原有添加量的基础上,上下浮动设定不同的水平,以生物量(OD600nm值)为评价指标设计正交试验,20 mL/L接种量,35 ℃条件下静置培养24 h,优化发酵培养基配方[21]。
1.3.8 高密度发酵条件优化正交试验
以MRS培养基为种子液,以优化后的发酵培养基为发酵液,以接种量(E)、发酵温度(F)、起始pH值(G)、溶氧量(H)作为影响因素,在植物乳杆菌常规培养条件的基础上,上下浮动设定不同的水平,以生物量(OD600nm值)为评价指标设计正交试验,优化发酵条件[22-23]。
2 结果与分析
2.1 乳酸菌的初筛
使用MRS碳酸钙培养基,从生牛乳储罐残余牛乳中分离出88株乳酸菌,编号为SX1~SX88,其中溶钙圈较大的乳酸菌菌株,纯化后用20%的甘油管保存,进行下一步的筛选,部分菌株的溶钙圈情况见图1。
图1 筛选乳酸菌的溶钙圈
Fig.1 Calcium dissolving circle of screened lactic acid bacteria
2.2 耐酸菌株筛选
作为益生菌菌株,要能够耐胃酸,才能进一步到达肠道起到益生作用,通常胃液pH值为1.3~1.8,饭后由于食物中和、稀释,胃内pH值会达到3.5,因此通过耐酸实验,筛选耐酸菌株。88株菌中,在pH 2.5的培养液中处理2 h,稀释到10-5仍可在MRS 琼脂平板生长的菌株共12株,其耐酸生长率见表1。
表1 筛选菌株的耐酸生长率
Table 1 Acid resistant growth rate of screened strains
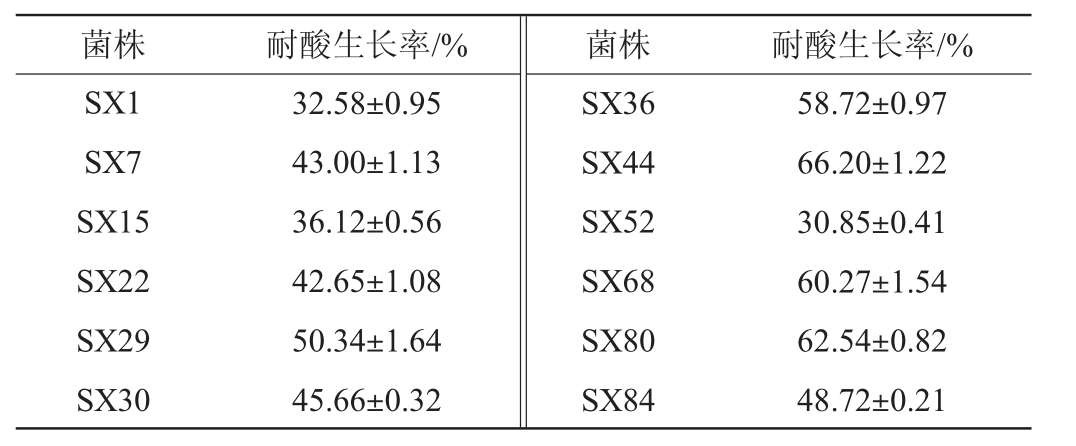
由表1可知,筛选到的12株产酸菌株耐酸生长率都在30%以上,其中菌株SX36、SX44、SX68、SX80的耐酸生长率最高,为58.72%~66%.20。因此,选择耐酸比较好的4株菌SX36、SX44、SX68、SX80进行下一步的实验。
2.3 耐胆盐菌株筛选
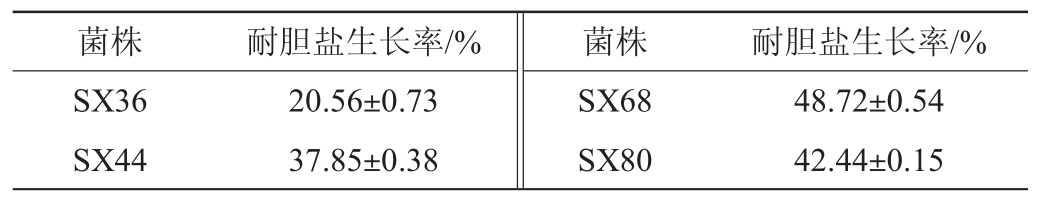
对其中耐酸比较好的4株菌SX36、SX44、SX68、SX80进行耐胆盐筛选,4株菌的耐胆盐生长率见表2。由表2可知,菌株SX36的耐胆盐生长率为20.56%,菌株SX44、SX68、SX80的耐胆盐生长率在37.85%~48.72%。因此,选择耐胆盐比较好的3株菌SSX44、SX68、SX80进行下一步的实验。
表2 筛选菌株的耐胆盐生长率
Table 2 Bile salt tolerance growth rate of screened strains
2.4 抗氧化能力测定
对其中耐酸、耐胆盐比较好的3株菌SX44、SX68、SX80进行抗氧化能力测定,3株菌的抗氧化能力见图2。
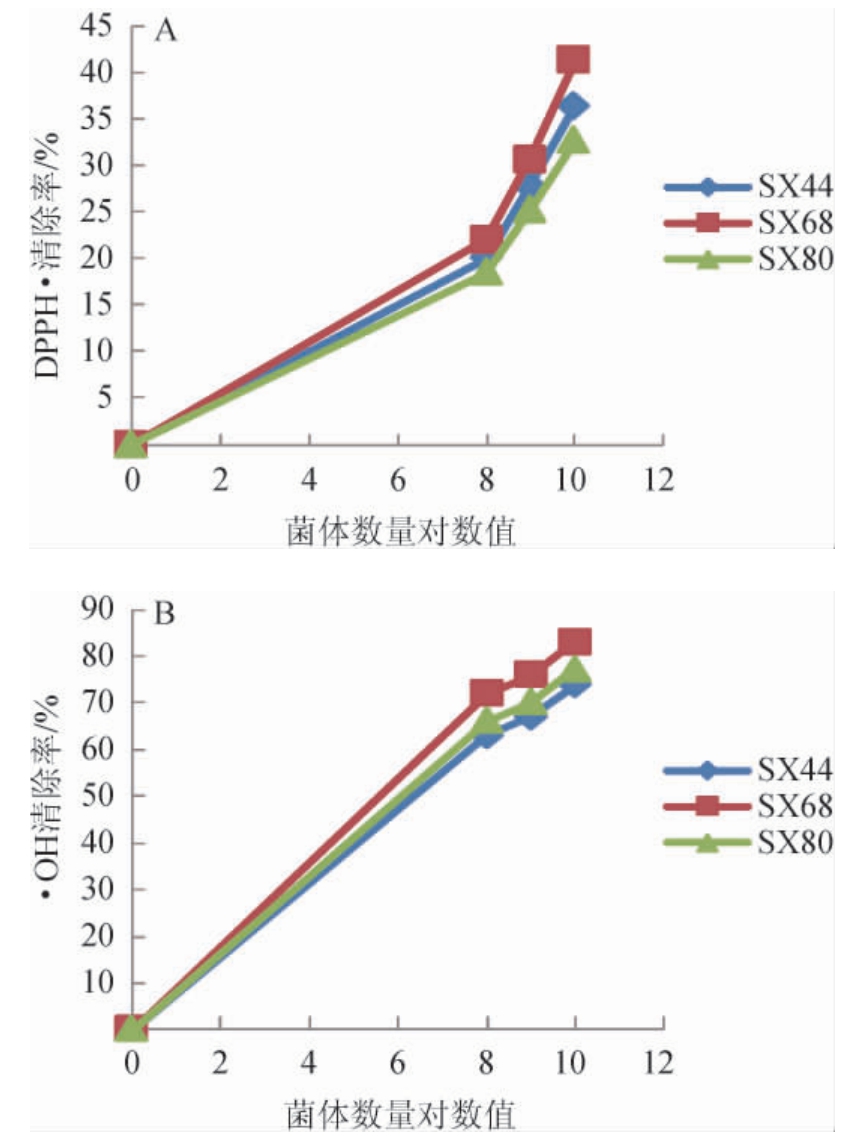
图2 筛选菌株对DPPH·(A)及·OH(B)的清除率
Fig.2 Scavenging rates of screened strains on DPPH·(A) and·OH (B)
由图2可知,3株菌在菌体浓度达到1010 CFU/mL的情况下,DPPH·清除率可以达到32.7%以上,·OH清除率可以达到73.8%以上,其中菌株SX68的DPPH·清除率为41.3%,·OH清除率为83.0%。提高菌体浓度,DPPH·和·OH的清除率有可能会再提高,考虑到实际应用中菌体在体内浓度,确定以1010 CFU/mL菌体浓度下菌株SX68的抗氧化能力最强。
2.5 分解胆固醇能力测定
对其中耐酸、耐胆盐比较好的3株菌SX44、SX68、SX80进行分解胆固醇能力测定,3株菌的分解胆固醇能力见图3。
由图3可知,菌株SX68的胆固醇分解能力最强,可以达到45.7%,菌株为初筛获得,如经过菌株驯化和诱变选育,分解胆固醇能力可能会进一步加强。综合上述试验对筛选到的SX68菌株进行菌种鉴定。
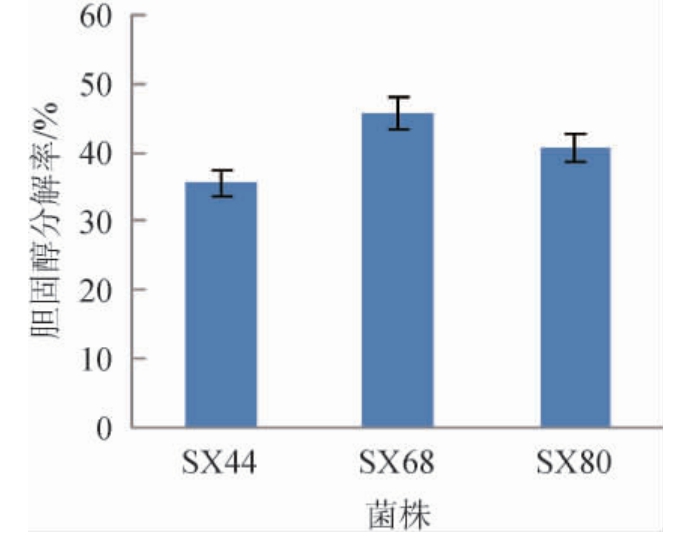
图3 筛选菌株的胆固醇分解率
Fig.3 Cholesterol decomposition rate of screened strains
2.6 菌株SX68的鉴定
2.6.1 形态学观察
菌株SX68的菌落及菌体形态见图4。由图4a可知,菌株SX68的菌落直径约1~3 mm左右,凸起,呈圆形,表面光滑,细密,白色。由图4b可知,菌株SX68的菌体形态呈短杆状、成短链,革兰氏染色为阳性,无芽孢,产酸,兼性厌氧。从菌落及细胞形态初步判断菌株SX68为乳杆菌属(Lactobacillus)。
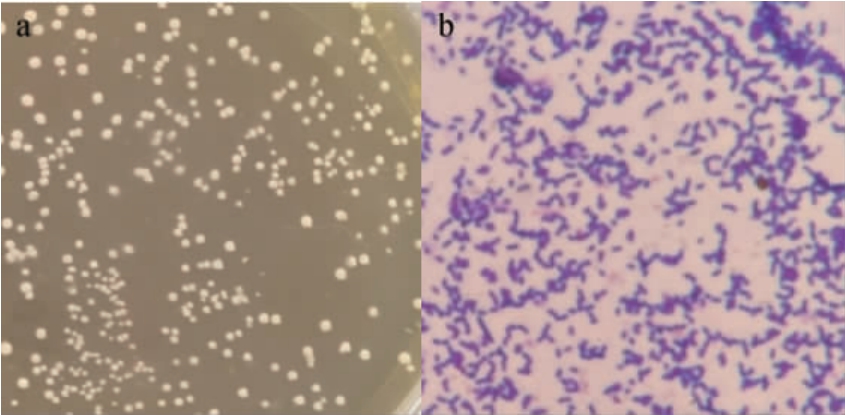
图4 菌株SX68的菌落(a)及菌体(b)形态
Fig.4 Colony (a) and cell (b) morphology of strain SX68
2.6.2 生理生化特性
由表3可知,菌株SX68过氧化氢酶、氧化酶、淀粉水解、明胶液化试验结果呈阴性,以及甲基红实验结果呈阳性,进一步验证了菌株SX68为乳杆菌属(Lactobacillus)。
表3 菌株SX68的生理生化特性
Table 3 Physiological and biochemical characteristics of strain SX68

注:“+”表示结果为阳性,“-”表示结果为阴性。
2.6.3 分子生物学鉴定
菌株SX68的16S rRNA基因测序后在GenBank(NCBI)的16S ribosomal RNA sequences(Bacteria and Archaea)数据库进行BLAST 比对,序列相似性在98.65%以上的菌株有6株,比对结果见表4。应用NCBI数据库的BLAST工具寻找相似菌株,并通过BLAST程序对序列进行聚类、应用Mega软件做基因序列系统发育树见图5。
表4 菌株SX68的16S rRNA基因序列比对结果
Table 4 16S rRNA gene sequence alignment results of strain SX68
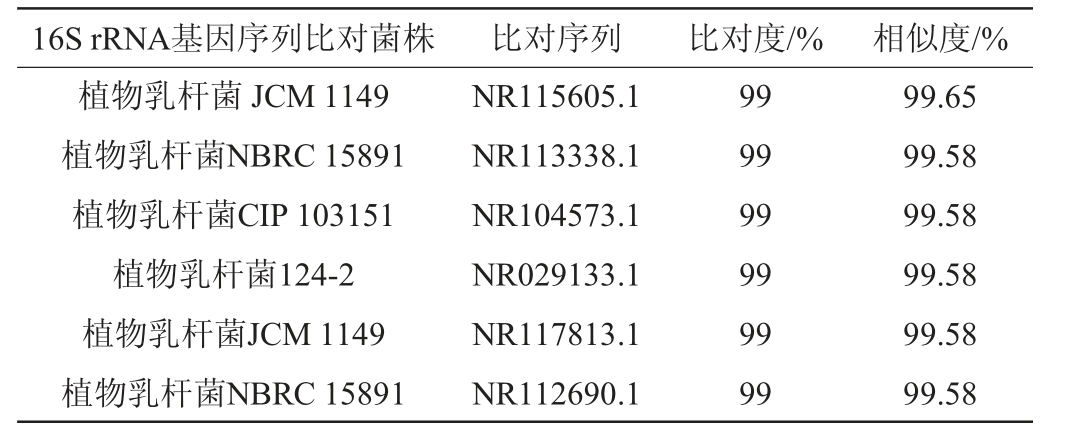
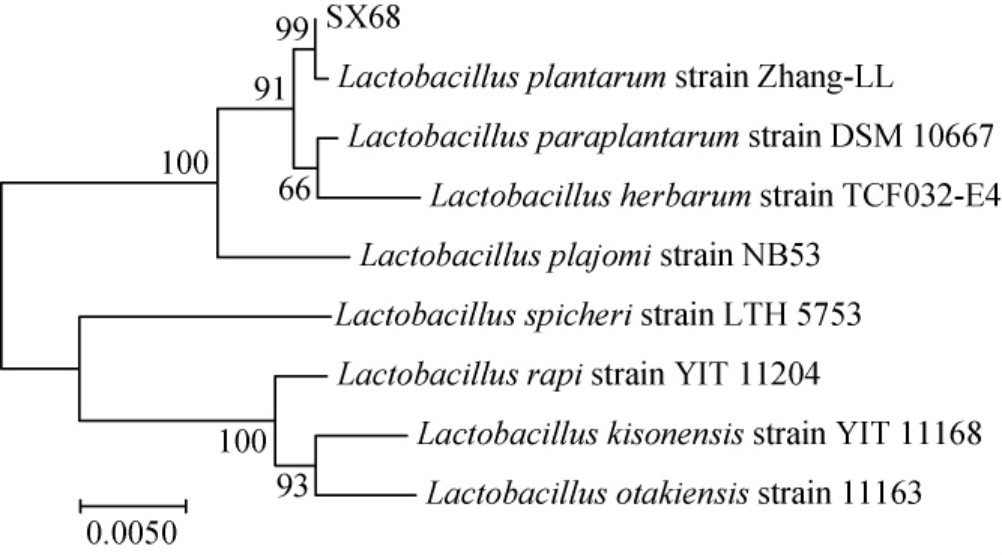
图5 菌株SX68基于16S rRNA 基因序列系统发育树
Fig.5 Phylogenetic tree of strain SX68 based on 16S rRNA gene sequence
由表4可知,菌株SX68 与Lactobacillus plantarum模式株JCM 1149序列相似性99.58%,亲缘关系密切。由图5可知,菌株SX68属于厚壁菌门(Firmicutes),和植物乳杆菌Zhang-LL、9714等亲缘关系密切,亲缘距离差异在0.000 4以内。结合形态特征、生理生化特性和16S rRNA 基因序列分析,将菌株SX68鉴定为植物乳杆菌(Lactobacillus plantarum)。
2.7 高密度发酵培养基配方优化
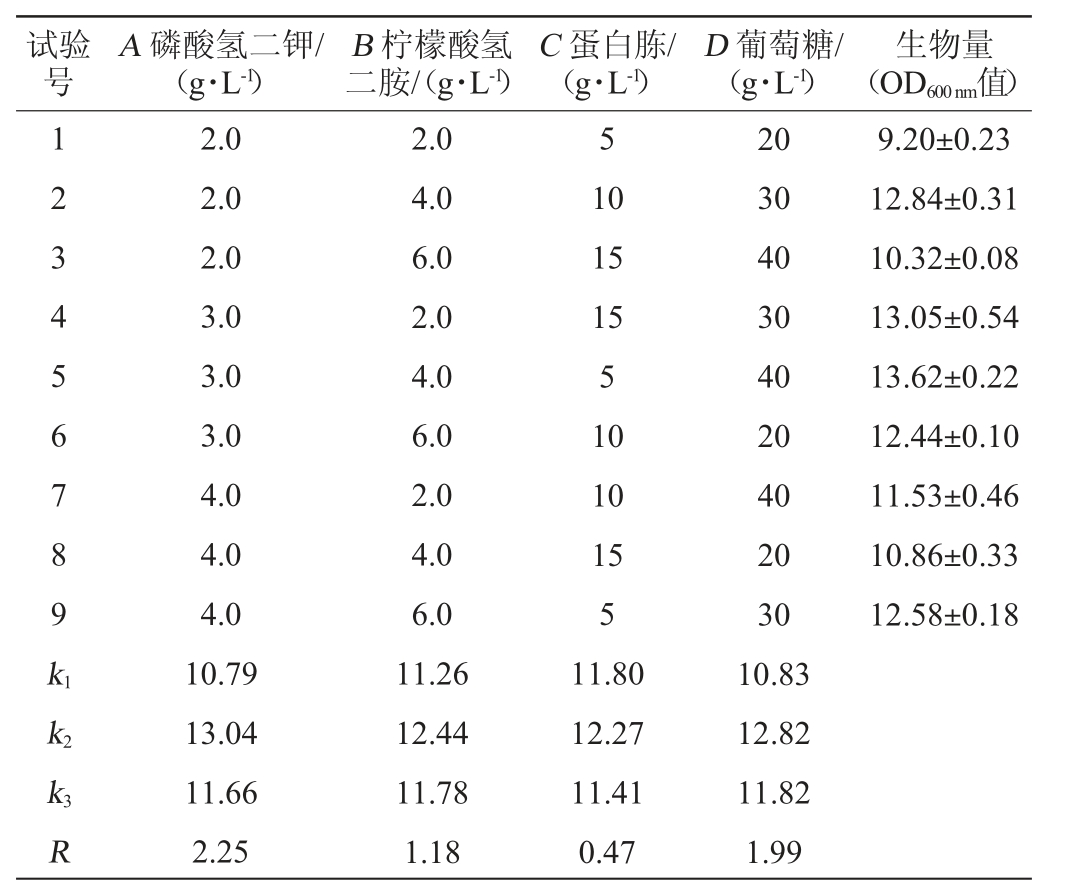
在MRS培养基配方的基础上,以生物量(OD600nm值)为评价指标,以磷酸氢二钾(A),柠檬酸氢二胺(B),乙酸钠(C),葡萄糖(D)添加量为影响因素,设计正交试验确定菌株SX68的发酵液配方,正交试验结果见表5。
由表5可知,不同因素对菌株高密度培养影响大小依次为:磷酸氢二钾>葡萄糖>柠檬酸氢二胺>蛋白胨,其最佳添加量为磷酸氢二钾3.0 g/L,葡萄糖30 g/L,柠檬酸氢二胺4 g/L,蛋白胨10 g/L。确定最优培养基配方组合为A2B2C2D2,即最佳添加量为磷酸氢二钾3.0 g/L,葡萄糖30 g/L,柠檬酸氢二胺4 g/L,蛋白胨10 g/L。培养基组成为蛋白胨10 g/L,牛肉膏10 g/L,酵母提取物5 g/L,K2HPO4 3 g/L,柠檬酸氢二胺4 g/L,乙酸钠5 g/L,葡萄糖30 g/L,吐温80 1 mL/L,MgSO4·7H2O 0.58 g/L,MnSO4·4H2O 0.25 g/L,pH 6.4。用此培养基摇瓶发酵,最高OD600nm值可达14.13,平板活菌计数,活菌量可达1.5×1012 CFU/mL。
表5 发酵培养基配方优化正交试验结果与分析
Table 5 Results and analysis of orthogonal tests for fermentation medium formula optimization
2.8 高密度发酵条件优化
在10 L发酵罐单因素试验基础上,以生物量(OD600nm值)为评价指标,以接种量(E)、发酵温度(F)、起始pH值(G)、溶氧量(H)作为影响因素,正交试验结果与分析见表6。
表6 发酵条件优化正交试验结果与分析
Table 6 Results and analysis of orthogonal tests for fermentation conditions optimization
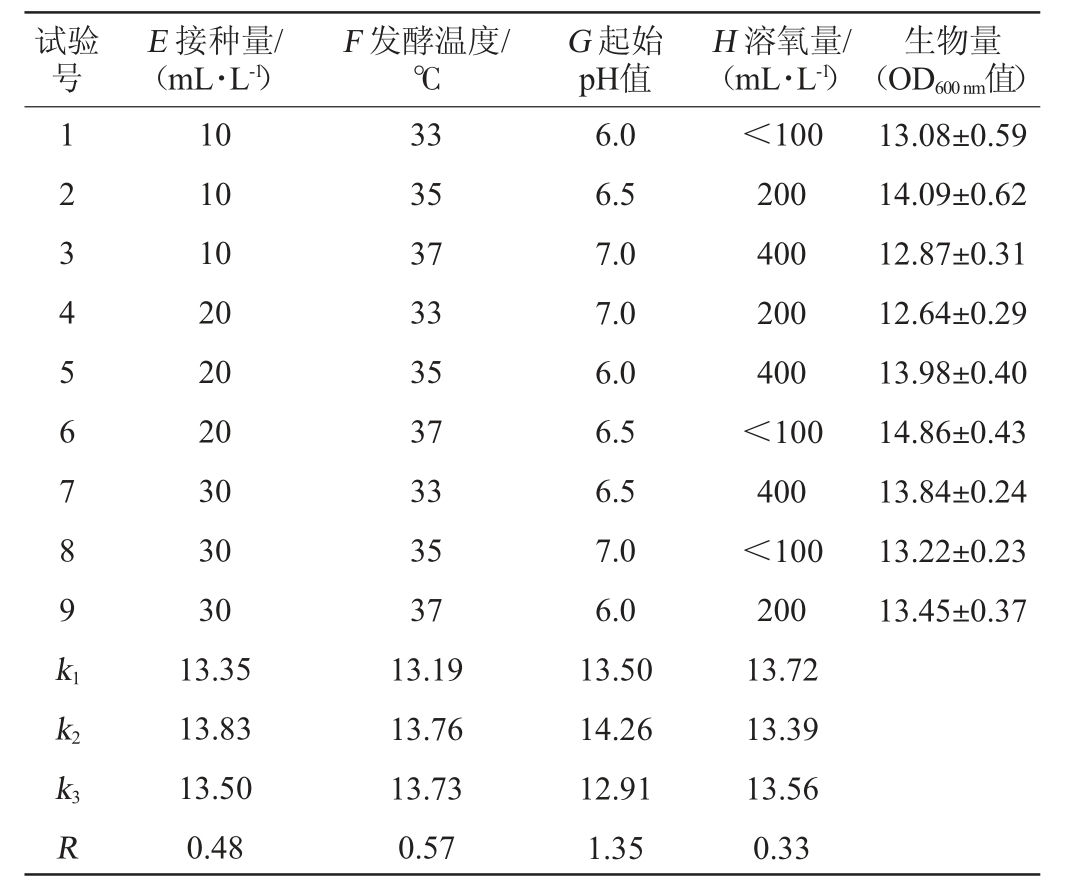
由表6可知,不同因素对菌株高密度培养影响大小依次为:起始pH值>发酵温度>接种量>溶氧量,其最佳发酵条件组合为E2F2G2H1,即起始pH值6.5,发酵温度35 ℃,接种量20 mL/L,溶氧量<100 mL/L。确定最优发酵条件为:起始pH 6.5,发酵温度35 ℃,接种量20 mL/L,溶氧量<100 mL/L,搅拌转速50 r/min,罐压0.03 MPa。在最佳发酵培养基配方及发酵条件下,最高OD600nm值可达15.68,活菌数可达9.6×1012 CFU/mL。
3 结论
本研究筛选到的植物乳杆菌(Lactobacillus plantarum)SX68,pH 2.5条件下处理2 h耐酸生长率可达60.27%,耐3 g/L胆盐生长率可达48.72%;在菌体浓度达到1010 CFU/mL的情况下,DPPH·清除率可达41.3%,羟自由基清除率可达83.0%,胆固醇分解能力可达45.7%。具有很好的耐酸、耐胆盐胁迫能力和较强的抗氧化、分解胆固醇益生功效。
菌株SX68优化培养基配方为:蛋白胨10 g/L,牛肉膏10 g/L,酵母提取物5 g/L,磷酸氢二钾3 g/L,柠檬酸氢二胺4 g/L,乙酸钠5 g/L,葡萄糖30 g/L,MgSO4·7H2O 0.58 g/L,吐温80 1 mL/L,MnSO4·4H2O 0.25 g/L,pH 6.4;优化发酵条件为:起始pH 6.5,发酵温度35 ℃,接种量20 mL/L,溶氧量<100 mL/L,搅拌转速50 r/min,罐压0.03 MPa。此优化条件下,最高发酵生物量(OD600nm值)可达15.68,活菌数可达9.6×1012 CFU/mL,较文献报道的109 CFU/mL提高了1 000倍[24-26],较王秋萍[27]报道的1.92×1012 CFU/mL提高了5倍。本研究为菌株SX68用于益生菌生产奠定了基础。
[1]中国食品科学技术学会益生菌分会.益生菌的科学共识[J].中国食品学报,2020,20(5):303-307.
[2]张彦位,路江浩,鄢梦洁,等.益生菌对微生态系统的改善作用及其应用研究进展[J].食品工业科技,2021,42(4):369-380.
[3]CROWLEY S,MAHONY J,VAN SINDEREN D.Current perspectives on antifungal lactic acid bacteria as natural bio-preservatives[J]. Trends Food Sci Tech,2013,33(2):93-109.
[4]赵龙玉.益生乳酸菌的筛选及其在食品加工上的应用研究[D].济南:山东农业大学,2015.
[5]AHN H,KIM J,KIM W J.Isolation and characterization of bacteriocin-producing Pediococcus acidilactici HW01 from malt and its potential to control beer spoilage lactic acid bacteria[J].Food Control,2017,80(1):59-66.
[6]武万强,王琳琳,赵建新,等.植物乳杆菌生理特性及益生功能研究进展[J].食品与发酵工业,2019,45(1):1-8.
[7]王水泉,包艳,董喜梅,等.植物乳杆菌的生理功能及应用[J].中国农业科技导报,2010,12(4):49-55.
[8]肖仔君,钟瑞敏,陈惠音,等.植物乳杆菌的生理功能与应用[J].中国食品添加剂,2005,16(2):87-89.
[9]马千里,刘冬,顾瑞霞.植物乳杆菌的益生特性及其在乳制品中的应用[J].中国奶牛,2014,32(1):36-40.
[10]丁诗瑶,雷文平,刘成国,等.不同来源植物乳杆菌的益生特性研究[J].中国乳品工业,2021,49(1):20-24.
[11]孙雯娟,张波,李大魁,等.益生菌制剂的发展现状与临床应用进展[J].中国医院药学杂志,2015,35(9):850-857.
[12]于长青,张丽娜,邓旭明.降胆固醇植物乳杆菌的紫外诱变选育[J].微生物学通报,2008,35(9):1461-1465.
[13]张凤敏,田丰伟,陈卫,等.具抗氧化活性乳酸菌的筛选[J].中国乳品工业,2007,35(2):4-7.
[14]刘冠兰,冯勋,朱文韬,等.复合益生菌粉对人体肠道菌群多样性的作用[J].兰州大学学报(医学版),2021,47(1):8-14.
[15]靳志强,王延样.植物乳杆菌在人体肠道的益生特性[J].中国乳品工业,2007,35(9):30-34.
[16]王春光,张雪,李达.酸菜来源植物乳杆菌的分离鉴定与耐受性研究[J].食品科技,2010,35(10):35-38.
[17]辛国芹,辛国民,徐海燕,等.一株植物乳杆菌的分离鉴定及特性研究[J].江西农业学报,2012,24(8):77-80.
[18]马爽,张雪,张莉,等.益生性植物乳杆菌的体外抗氧化活性研究[J].中国乳品工业,2013,41(4):10-14.
[19]肖琳琳,董明盛.干酪乳杆菌KM-16 的筛选及其降胆固醇活性研究[J].中国乳品工业,2003,31(6):7-8.
[20]张纪忠.微生物分类学[M].上海:复旦大学出版社,1990:93-109.
[21]金玉洁,何国庆.植物乳杆菌ZU018 增殖培养基的优化[J].食品工业科技,2020,41(14):94-99.
[22]赵巍,付丽,王欣,等.不同发酵条件对植物乳杆菌生长的影响[J].饲料工业,2014,35(22):44-48.
[23]张广敏,王炜,张晓琳,等.植物乳杆菌高密度增殖发酵条件的研究[J].新疆农业科学,2009,46(3):643-650.
[24]张瑶,李啸,潘冬瑞.Box-Benhnken 设计优化植物乳杆菌培养基[J].天津农业科学,2013,19(7):1-5.
[25]王帅.植物乳杆菌培养及冻干技术研究[D].西安:陕西科技大学,2016.
[26]杨加怀.植物乳杆菌299 高密度培养及冷冻干燥保护的研究[D].天津:天津科技大学,2015.
[27]王秋萍.高密度益生菌发酵技术优化及益生菌冰淇淋的研制[D].天津:天津商业大学,2019.