耐甲氧西林金黄色葡萄球菌(methicillin-resistant Staphylococcus aureus,MRSA)是引起医院感染的多重耐药菌[1-3],自首次分离出MRSA以来,其临床检出率逐年上升,MRSA能引起心内膜炎、脑膜炎和败血症等危重的致死性疾病[2-5],MRSA感染已被公认为世界三大最难解决的感染性疾病之一。随着抗生素的滥用,MRSA耐药率不断升高,唐克文等[6]研究表明,MRSA对克林霉素和红霉素的耐药率逐渐增高,因此,MRSA的多重耐药性一直受到密切关注。虽然不断有新的抗MRSA感染药物被发现和研究,体外药敏试验也显示出较好的抗MRSA活性,但其疗效和安全性尚需验证[7-8],这使得人类需更加重视抗耐药菌株的药物开发研究。
微生物是药物先导化合物最重要的来源[9],有研究从广西涠洲岛礁栖珊瑚、海绵和海藻等样品中分离获得5种具有丰富代谢产物及抗MRSA活性的菌株[10]。还有研究筛选到一株对MRSA具有较强的抑制作用且稳定性好的枯草芽孢杆菌(Bacillus subtilis)SC-2,并提取到对耐药鲍曼不动杆菌、大肠杆菌、幽门螺旋杆菌等常见的致病菌具有抗菌活性的化合物[11]。这些抗菌活性物质的发现为本研究提供了理论依据。红树林因其特殊的生态环境、周期性的海水侵袭、河口有机质的沉积和落叶的腐败作用而富含有机质和腐殖质,蕴含了丰富的微生物资源[12]。有研究从南海海桑根际土壤筛选出一株抗MRSA活性较强的真菌,并追踪分离到具有显著抗菌活性的天然产物嗜氮酮[13]。因此,本研究从红树林根部土壤中筛选出具有抗MRSA活性的菌株,根据形态学观察、生理生化试验及16S rDNA基因序列分析对其进行鉴定,采用不同的培养基优选抑菌物质生成条件;以有机溶剂分离纯化抑菌物质物质,采用气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)分析抑菌物质化学成分,以期获得抗MRSA活性物质,为开发治疗MRSA感染的药物提供新的思路。
1 材料与方法
1.1 材料与试剂
1.1.1 样品和菌株
土壤样品:海南省红树林根部土壤;指示菌株耐甲氧西林金黄色葡萄球菌(methicillin-resistant Staphylococcus aureus,MRSA):本实验室提供。
1.1.2 化学试剂
革兰氏染色液试剂盒HB8278:青岛高科技工业园海博生物有限公司;细菌脱氧核糖核酸(deoxyribonucleic acid,DNA)试剂盒(D3350-01)、淀粉酶、胰凝乳蛋白酶、胰蛋白酶、胃蛋白酶、链霉蛋白酶、蛋白酶K(酶活均为1 mg/mL):上海古朵生物科技有限公司。
1.1.3 培养基
LB(Luria-Bertani)液体培养基:蛋白胨10 g/L,酵母粉5 g/L,NaCl 10 g/L。LB固体培养基:LB液体培养基中加琼脂16 g/L。
淀粉培养基:蛋白胨10 g/L,牛肉膏5 g/L,NaCl 5 g/L,可溶性淀粉10 g/L。
缓冲葡萄糖蛋白胨培养基:蛋白胨5 g/L,葡萄糖5 g/L,NaCl 5 g/L。
尿素培养基:蛋白胨1 g/L,NaCl 5 g/L,葡萄糖1 g/L,磷酸二氢钾2 g/L,0.4%酚红溶液3 mL,琼脂20 g/L,20%尿素溶液100 mL。
克氏双糖铁琼脂培养基(g/L):乳糖10 g/L,葡萄糖1 g/L,氯化钠5 g/L,柠檬酸铁铵0.5 g/L,硫代硫酸钠0.5 g/L,琼脂12 g/L,酚红0.025 g/L。
营养琼脂(nutrient agar,NA)培养基:牛肉浸膏3g/L,酵母浸膏1 g/L,胰蛋白胨5 g/L,葡萄糖20 g/L。
水解酪蛋白(Mueller-Hinton,MH)培养基:牛肉膏5 g/L,淀粉1.5 g/L,酪蛋白水解物17.5 g/L。
ZS培养基:蛋白胨10 g/L,酵母粉5 g/L,NaCl 10 g/L,牛肉膏5 g/L。
葡萄糖酵母牛肉膏(ager yeast dextrose,AYDA)培养基:葡萄糖10 g/L,牛肉膏80 g/L,酵母粉5 g/L。
Landy培养基:葡萄糖20 g/L,L-谷氨酸5 g/L,KH2PO4 1 g/L,KCl 0.5 g/L,MgSO4·7H2O 0.5 g/L,酵母抽提物1 g/L,MnSO45mg/L,CuSO4·5H2O0.16mg/L,FeSO4·7H2O0.15mg/L,L-苯丙氨酸2 mg/L。
金氏培养基(Kings Medium B,KMB):蛋白胨20 g/L,MgSO4·7H2O2.5g/L,K2HPO4·3H2O1.5g/L,甘油20g/L。
牛肉蛋白胨酵母(beef peptone yeast,BPY)培养基:牛肉膏5 g/L,胰蛋白胨10 g/L,酵母浸膏5 g/L,葡萄糖5 g/L,NaCl 5 g/L。
酵母浸出粉胨葡萄糖(yeast extract peptone dextrose,YPD)培养基:酵母膏10 g/L,蛋白胨20 g/L,葡萄糖20 g/L。
胰蛋白胨大豆琼脂培养基(trypcasein soy agar,TSA):胰蛋白胨17 g/L,大豆蛋白胨3 g/L,NaCl 5g/L,K2HPO4·3H2O 2.5 g/L,葡萄糖2.5 g/L。
上述培养基灭菌条件均为121 ℃、20 min。
明胶培养基:牛肉膏蛋白胨液100 mL,明胶15 g/L。112.6 ℃灭菌30 min。
1.2 仪器与设备
GI54DS型全自动高压灭菌锅:南京傲然生物科技有限公司;Microfuge 20R型高速离心机:美国Beckman Coulter Inc公司;HF-safe-1500LC(A2)型生物安全柜:上海力申科学仪器有限公司;JAN-26台式高速冷冻离心机:美国BECKMAN COULTER公司;Core ML型旋转蒸发仪:德国Heidolph Hei-VAP公司;ME204E型电子分析天平:METTLER TOLEDO集团;TONE 96G型梯度聚合酶链反应(polymerase chain reaction,PCR)仪:德国耶拿Biomentra公司;BSD-YX 2400型温控回旋立式双层摇床:上海博讯实业有限公司;JY04S-3E型凝胶成像分析系统:北京君意东方电泳设备有限公司;Ni-U+DS-Ri2型正置荧光显微镜:日本Nikon公司。
1.3 方法
1.3.1 抗MRSA活性菌株的筛选
从平板挑取一环指示菌MRSA接种于5mL LB液体培养基中,37 ℃、180 r/min条件下振荡培养18~24 h,采用平板倾注法[14],将MRSA病原菌种子液接种至LB 固体培养基中,倒平板,晾干备用。
从海南省红树林根部土壤随机取9份样品,每份土样分别取11 g与10 mL无菌水混合,37 ℃、180 r/min条件下振荡15 min,静置5 min后,吸取上层清液按10倍梯度稀释法稀释至10-2、10-3、10-4倍浓度,各取100 μL涂布于上述混有MRSA菌液的培养皿中,37 ℃恒温培养5 d,观察各土壤样品菌株有无抑菌圈,测量并比较抑菌圈大小,以抑菌圈直径大小评判抑菌活性强弱,筛选出抑菌圈最大即抗MRSA活性强的菌株。
1.3.2 筛选菌株鉴定
形态学观察及生理生化反应测定:参考东秀珠等[15]编著的《常见细菌系统鉴定手册》,观察、分析菌落形态、生长特性,通过革兰氏染色、鞭毛染色、芽孢染色和各生化试验对菌株进行检测、鉴定,方法参考《微生物学实验》[16]。
分子生物学鉴定:利用16S rDNA基因序列分析的方法对筛选菌株进一步鉴定。以筛选菌株基因组DNA为模板,采用通用引物27F(5'-AGAGTTTGATCCTGGCTCAG-3')和1492R(5'-GGTTACCTTGTTACGACTT-3')扩增16S rDNA。PCR扩增体系:EXTaq酶0.25 μL,10×Buffer 5 μL,脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTP)4 μL,MgCl2 4 μL,模板DNA 2 μL,27F 1 μL,1492R 1 μL,双蒸水(ddH2O)32.75 μL。PCR扩增条件为:95 ℃5 min;94 ℃60 s;55 ℃60 s;72 ℃90 s;循环30次,延伸72 ℃10 min。PCR扩增完成后通过1%琼脂糖凝胶检测扩增产物,将获得的特异性DNA送往华大基因科技股份有限公司进行测序,提交序列至GenBank数据库,获得序列号。将测序结果在美国国家生物技术信息中心(national center of biotechnology information,NCBI)网站进行基本局部比对搜索工具(basic local alignment search tool,BLAST)比对,使用Mega7.0建立发育树获得亲缘远近关系。
1.3.3 筛选菌株产抑菌物质培养基的优选
配制LB、MH、NA、Landy、ZS、KMB、BPY、AYDA、YPD、TSA培养基,从平板挑取筛选抗MRSA活性菌株分别接种至装液量为50 mL/250 mL的上述培养基中,每组设3个重复,37 ℃,200 r/min 振荡培养24 h。将培养液于12 000 r/min离心10 min,取上清液,用0.22 μm膜过滤,收集滤液备用。采用平板倾注法,将MRSA病原菌种子液接种至LB 固体培养基中,在上述平板上分别均匀打孔,孔径为8 mm,每孔分别接入200 μL的上述各种备用滤液,每组设3个重复,37 ℃恒温箱培养24 h,以上述培养基作为相应培养基培养菌株NEL-002后发酵液滤液为抑菌对照组,利用抑菌物质不断溶解经琼脂扩散形成不同浓度梯度,在扩散过程中浓度逐渐减少,直到抑菌物质浓度与细菌对该种抑菌物质的最高耐受浓度相同,此时抑菌物质不再扩散,即形成抑菌圈,以显示其抑菌作用[17-18],通过抑菌圈大小以判断其是否具有抑菌能力,判定标准:抑菌圈≤7 mm为无抑菌作用,抑菌圈直径>7 mm为有抑菌作用,抑菌圈直径7~10 mm为钝敏,抑菌圈直径11~20 mm为中敏,抑菌圈直径>20 mm为高敏。比较不同孔径中滤液抗MRSA活性的敏感性差异,确定筛选抗MRSA活性菌株的最适发酵培养基。
1.3.4 抑菌物质的分离纯化
从平板挑取1环筛选抗MRSA活性菌株接种至装液量为50 mL/250 mL LB液体培养基中,37 ℃、200 r/min振荡培养24 h,发酵液于12 000 r/min 离心10 min,取上清液,分别用乙酸乙酯、石油醚、正丁醇对上清液进行反复3次的萃取,分别将得到的有机相减压蒸干,得到的沉淀1 mL加入二甲基亚砜(dimethyl sulfoxide,DMSO)充分溶解,通过0.22 μm细菌过滤器除菌,收集滤液备用。采用平板倾注法,将MRSA病原菌种子液接种至LB 固体培养基中,倒平板,晾干备用,再在上述平板上分别均匀打孔,孔径为8 mm,每孔分别接入200 μL的上述各种备用滤液,每组设3个重复,37 ℃培养24 h,以乙酸乙酯、石油醚、正丁醇、DMSO为对照组,测量抑菌圈大小,比较不同孔径中滤液抗MRSA活性的差异,确定筛选抗MRSA活性菌株抑菌物质的分离纯化方法,并以此方法粗提发酵液,用二甲基亚砜充分溶解,作为样液,4 ℃保存备用。
1.3.5 抑菌物质的化学成分分析
抗MRSA活性菌株抑菌物质GC-MS分析[19-20]。GC条件:DB25 交联石英毛细管柱(30 m×0.25 mm),柱温为40 ℃,进样温度为250 ℃,柱压为49.7 kPa,载气为高纯度氦气(He),柱流量为1 mL/min,载气流量3 mL/min,进样量0.5 μL,分流比20∶1。MS条件:电子电离(electronic ionization,EI)源,电子能量70 eV,离子源温度为230 ℃,四级杆温度为150 ℃,传输线温度250 ℃,扫描质量范围为20~500 amu。定性定量方法:将各组分的相对保留指数与文献[21-22]中真实化合物的相对保留指数进行比较,并与美国国家标准技术研究所(national institute of standards and technology,NIST)98文献数据中的相对保留指数进行比较进行定性,采用面积归一法对各组分进行定量。
1.3.6 抑菌物质稳定性研究
热稳定性:将1.3.4中制备的抑菌物质粗提液,在40 ℃、50 ℃、60 ℃、70 ℃、80 ℃、90 ℃、100 ℃、121 ℃的不同温度下处理20 min,对照组在37℃温度下处理20 min,每处设置3个重复,过滤后用圆盘扩散法[23]测定其抑菌活性,37 ℃避光恒温培养48 h后测量抑菌圈直径,以对照组(CK)的抑菌圈大小为活性100%,计算各温度下的相对活性。
酸碱稳定性:将1.3.4中制备的抑菌物质粗提液,调节pH值至1~12,对照组为原液pH值,每处设置3个重复,过滤后采用圆盘扩散法测定其抑菌活性,37 ℃恒温培养48 h后测量抑菌圈大小,以对照组(CK)的抑菌圈大小为活性100%,计算各pH组的相对活性。
蛋白酶稳定性:将1.3.4中制备的抑菌物质粗提液,分别加入淀粉酶、胰凝乳蛋白酶、胰蛋白酶、胃蛋白酶、链霉蛋白酶、蛋白酶K,酶的终质量浓度为1 mg/mL,对照组不加任何蛋白酶,每处设置3个重复,过滤后采用圆盘扩散法测定其活性,37 ℃的恒温培养48 h后测量抑菌圈大小。以对照组的抑菌圈大小为活性100%,计算各蛋白酶处理组的相对活性,通过对蛋白酶敏感性判断抑菌物质是否含有蛋白类化合物,其活性是否容易被蛋白酶破坏[24]。
1.3.7 最低抑菌浓和最低杀菌浓度测定
最低抑菌浓度(minimal inhibitory concentration,MIC)和最低杀菌浓度(minimal bactericidal concentration,MBC)测定:将1.3.4中制备的抑菌物质粗提液,用LB液体培养基稀释至质量浓度为2 000 μg/mL,再依次稀释为1 000 μg/mL、500 μg/mL、250 μg/mL、125 μg/mL、62.5 μg/mL、31.25 μg/mL、15.62 μg/mL、7.81 μg/mL。采用96孔板法,设置3个重复,以含等量DMSO(5%)的LB液体培养基作对照,37 ℃恒温静置培养24 h后,观察并统计结果,阴性孔显示清亮,阳性孔显示混浊,MIC值为96孔板上横排中未有混浊的最后一孔所对应的浓度。
读取MIC值结果后,分别移取各组药物阴性孔液体50 μL,涂布于LB固体培养基,37 ℃恒温静置培养24 h;读取菌落个数,分别计算对应孔内细菌数量,能够杀死>99.9%初始细菌含量(<100 CFU/mL)的最低药物浓度为MBC。
2 结果与分析
2.1 抗MRSA活性菌株的筛选
37 ℃恒温静置培养5 d后,结果见图1。由图1可知,筛选出5株抗MRSA活性菌株,得到抗MRSA生长能力最强的菌株,编号NEL-002,抑菌圈直径约为(28.77±0.42)mm,其他4株抗MRSA活性菌株的抑菌圈直径<10 mm,抑菌活性较弱,不作为后续研究对象。
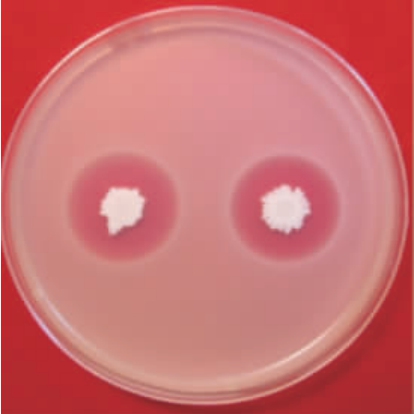
图1 菌株NEL-002抗耐甲氧西林金黄色葡萄球菌活性
Fig.1 Activity of methicillin-resistant Staphylococcus aureus of strain NEL-002
2.2 菌株NEL-002的鉴定
2.2.1 形态学观察
菌株NEL-002在LB固体培养基,37 ℃恒温静置培养18 h,菌株NEL-002的形态特征见图2。
由图2A可知,菌落生长茂盛,似圆形、乳白色,不透明,边缘形态不规则,表面粗糙、较干燥。由图2B可知,经革兰染色,在显微镜下观察到菌体呈紫色,为革兰阳性菌。由图2C可知,经鞭毛染色,在显微镜下观察发现菌体端生鞭毛1根。由图2D可知,经芽孢染色,在显微镜下观察到红色的菌体和绿色的芽孢。
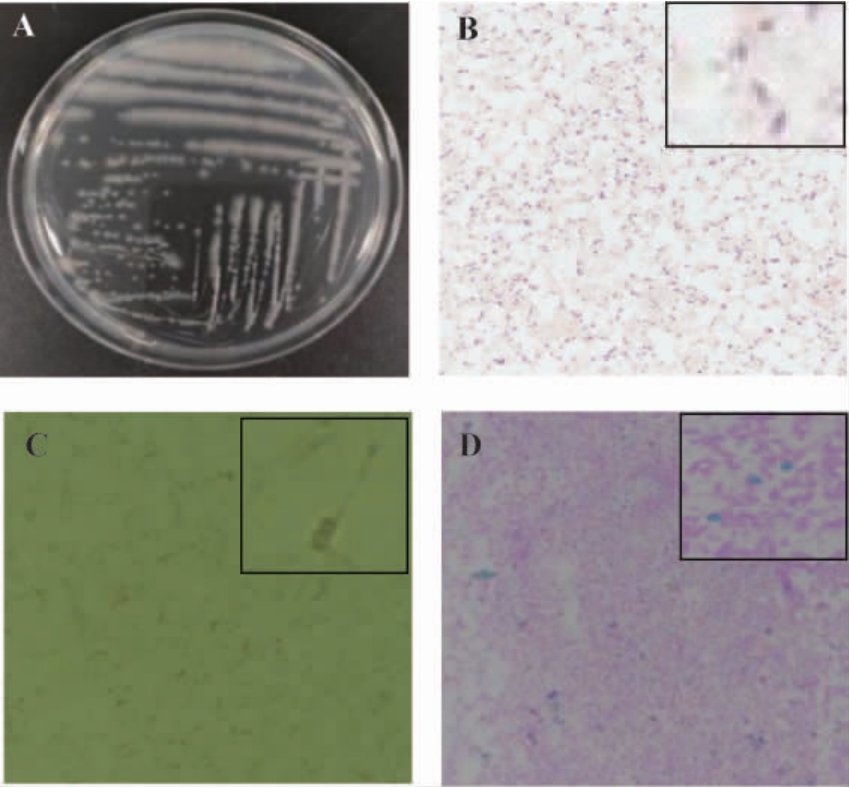
图2 菌株NEL-002的形态特征
Fig.2 Morphological characteristics of strain NEL-002
A:菌落形态;B:革兰氏染色;C:鞭毛染色;D:芽孢染色。
2.2.2 菌株NEL-002生理生化特征
菌株NEL-002其生理生化特征结果见表1。由表1可知,V-P试验阳性、M.R.试验阴性说明该菌株分解利用葡萄糖产生乙酰甲基甲醇,过氧化氢酶试验阳性符合革兰阳性菌特征,淀粉酶试验、尿素酶试验阳性,说明该菌株不产生淀粉酶和尿素酶,不能分解利用淀粉和尿素,明胶液化试验、硫化氢试验阴性,说明该菌株不能分解氨基酸。
表1 菌株NEL-002的部分生理生化特征
Table 1 Some physiological and biochemical characteristics of strain NEL-002
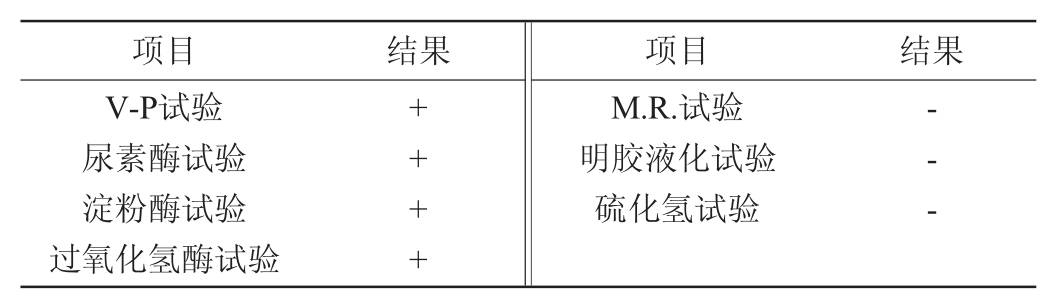
注:“+”表示结果呈阳性;“-”表示结果呈阴性。
2.2.3 菌株NEL-002分子生物学鉴定
菌株NEL-002的16S rDNA PCR扩增产物经1%琼脂糖凝胶电泳分析,结果如图3所示,扩增条带在1 000~2 000 bp之间,说明重组质粒构建成功,可回收扩增产物,连接转化,筛选阳性克隆,进行测序和序列分析。经基因测序,提交序列数据至Genbank,序列号为MN640828。使用Mega 7.0建立发育树结果如图4所示,综合NCBI的BLAST搜索,细菌的16S rDNA 进行比对,结果显示菌株NEL-002与萎缩芽孢杆菌同源性达到99%,菌株NEL-002被鉴定为萎缩芽孢杆菌(Bacillus atrophiae)。
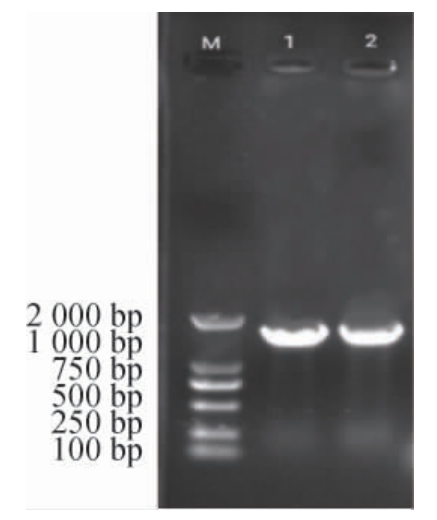
图3 菌株NEL-002基于16S rDNA序列PCR扩增产物电泳结果
Fig.3 PCR amplification product electrophoresis results of strain NEL-002 based on 16S rDNA sequence
M:DNA Marker DL2000;1、2:菌株NEL-002、16S rDNA序列PCR扩增产物。
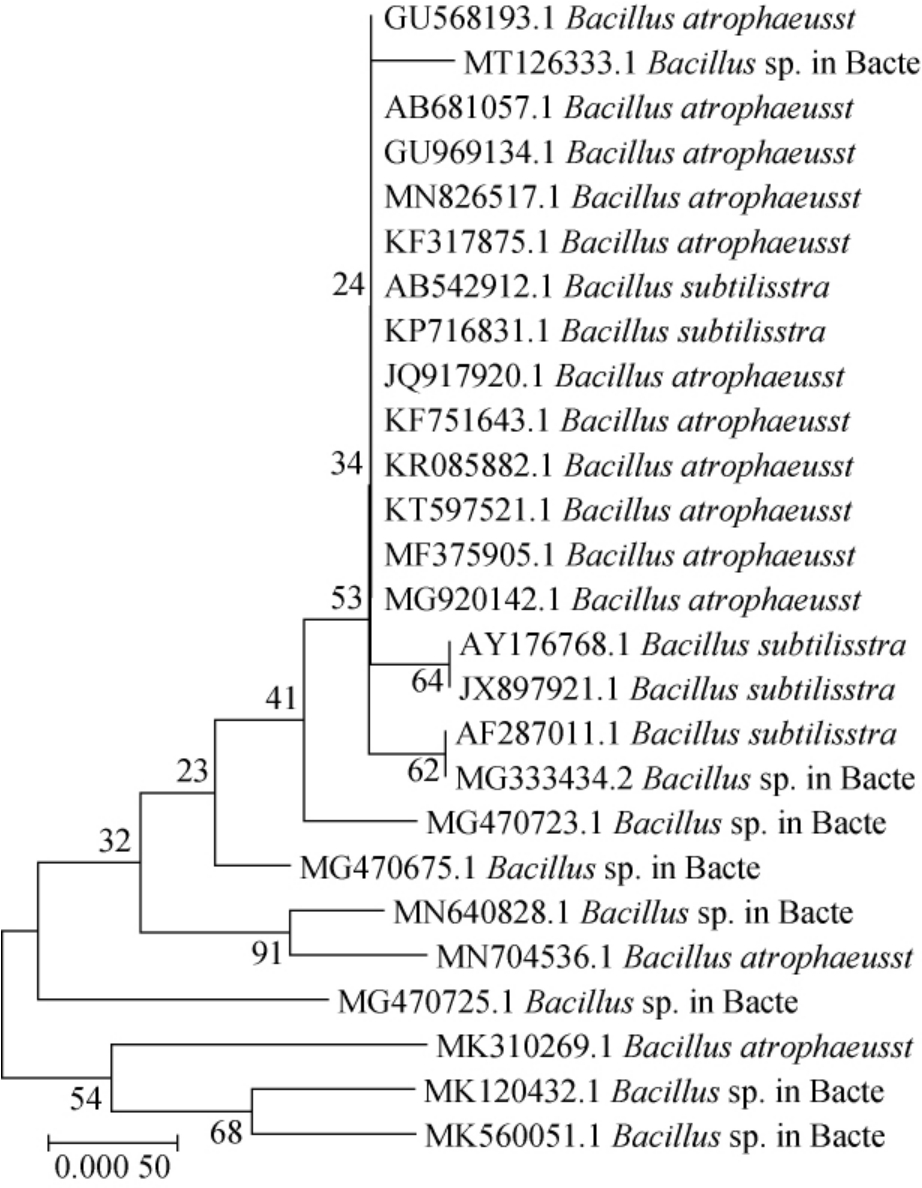
图4 菌株NEL-002基于16S rDNA基因序列构建的系统发育树
Fig.4 Phylogenetic tree of strain NEL-002 based on 16S rDNA sequences
2.3 菌株NEL-002活性物质研究
2.3.1 最适发酵培养基的筛选
用不同培养基对菌株NEL-002培养,观察其抗菌活性,结果见图5。
由图5可知,菌株NEL-002在TSA、YPD培养基上抑菌圈直径<7 mm无抑菌活性,在BPY、AYDA培养基上抑菌圈直径在7~10 mm,为钝敏,有微弱抑菌活性,在KMB、ZS、Landy、NA培养基上抑菌圈直径在11~20 mm,为中敏,抑菌活性较强,在MH、LB培养基上抑菌圈直径>20 mm,为高敏,抑菌活性强,其中在LB液体培养基抑菌圈直径为(25.91±0.38)mm,较其他培养基抗菌活性最强,对照组未出现抑菌圈,无抑菌活性。因此,选用LB液体培养基培养菌株NEL-002。
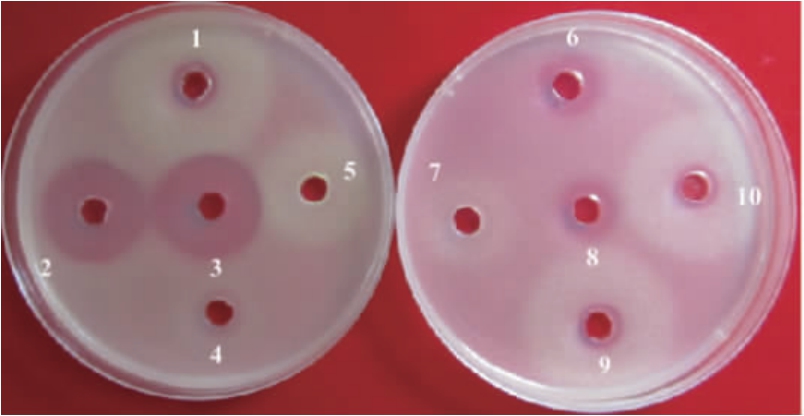
图5 不同发酵培养基对菌株NEL-002抑菌活性的影响
Fig.5 Effects of different fermentation media on antibacterial activity of strain NEL-002
1:ZS培养基;2:MH培养基;3:LB培养基;4:BPY培养基;5:YPD培养基;6:Landy培养基;7:TSA培养基;8:NA培养基;9:AYDA培养基;10:KMB培养基。
2.3.2 抗菌活性物质的分离纯化
分别采用石油醚、乙酸乙酯、正丁醇3种有机溶剂对菌株NEL-002发酵上清液进行萃取,石油醚萃取物抗菌活性最强,抑菌圈直径为(25.48±0.01)mm,正丁醇萃取物抑菌圈直径为(17.70±0.00)mm,乙酸乙酯萃取物抑菌圈直径为(17.70±0.02)mm抗菌活性较低,对照组各有机溶剂及DMSO未出现抑菌圈,无抑菌活性。因此,选用石油醚粗提物进行后续实验。
2.3.3 菌株NEL-002抑菌物质化学成分分析
采用气相色谱-质谱联用技术(GC-MS)分析了该菌株粗提物中可能具有抗MRSA活性的化合物,结果见表2。由表2可知,在粗提物中共鉴定出3种已知化合物,包括邻苯二甲酸二丁酯、十甲基环戊硅氧烷和十二甲基环六硅氧烷,与文献[25-26]报道的邻苯二甲酸二丁酯、十甲基环戊硅氧烷和十二甲基环六硅氧烷相关信息基本一致。
表2 菌株NEL-002抑菌物质粗提物主要成分
Table 2 Main components of crude extract of antibacterial material from strain NEL-002

2.3.4 菌株NEL-002活性物质稳定性分析
由图6可知,粗提物经不同温度处理20 min后,在40~80 ℃的温度范围内随着温度的升高,抑菌活性无明显差异,抑菌圈直径均在18.00 mm以上,90 ℃开始抑菌活性随温度升高开始降低,加热至121℃,抑菌圈直径为(9.26±0.05)mm,相对活性49.34%。说明石油醚粗提物不耐高温,但在温度40~80 ℃范围内粗提物热稳定性良好。
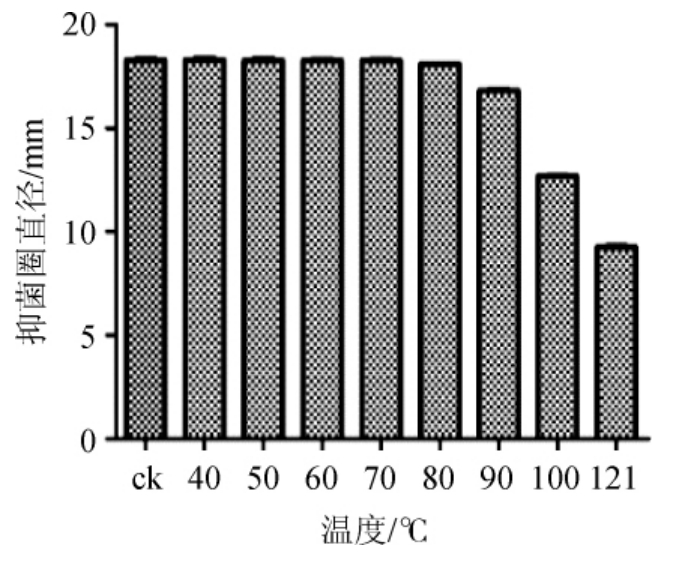
图6 菌株NEL-002粗提活性物质热稳定性
Fig.6 Thermal stability of the crude extracts from strain NEL-002
由图7可知,粗提物经不同pH值处理后,pH值在5~10时,抑菌圈直径较大,在碱性条件pH值为8时抑菌圈直径最大,约为(17.87±0.02)mm,pH值在1~4抑菌圈直径较小,与对照组相比抑菌活性降低,相对活性均在62.27%以上,而pH值在11~12条件下无抑菌活性,说明提取菌株NEL-002的粗提物在pH值在5~10范围内稳定性良好。
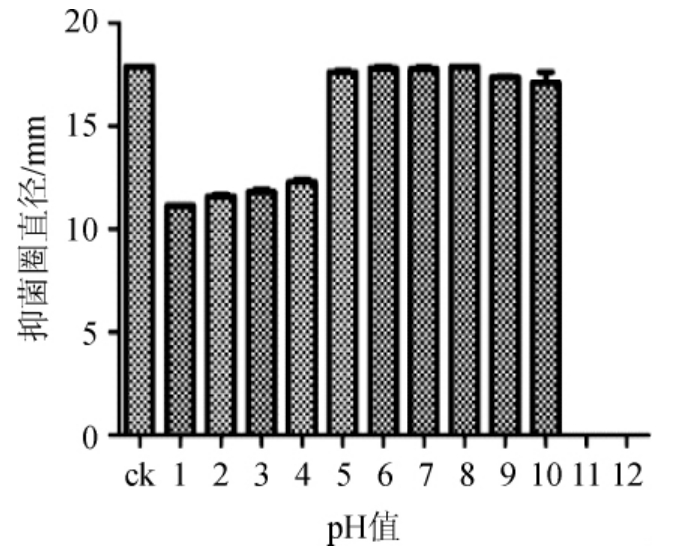
图7 菌株NEL-002粗提活性物质酸碱稳定性
Fig.7 Acid and alkali stability of the crude extracts from strain NEL-002
由图8可知,分别用淀粉酶、胰凝乳蛋白酶、胰蛋白酶、胃蛋白酶、链霉蛋白酶、蛋白酶K处理30 min培养后,抗菌活性均较稳定,说明菌株NEL-002产生的抗菌物质对上述蛋白酶不敏感,不易被酶破坏其活性。
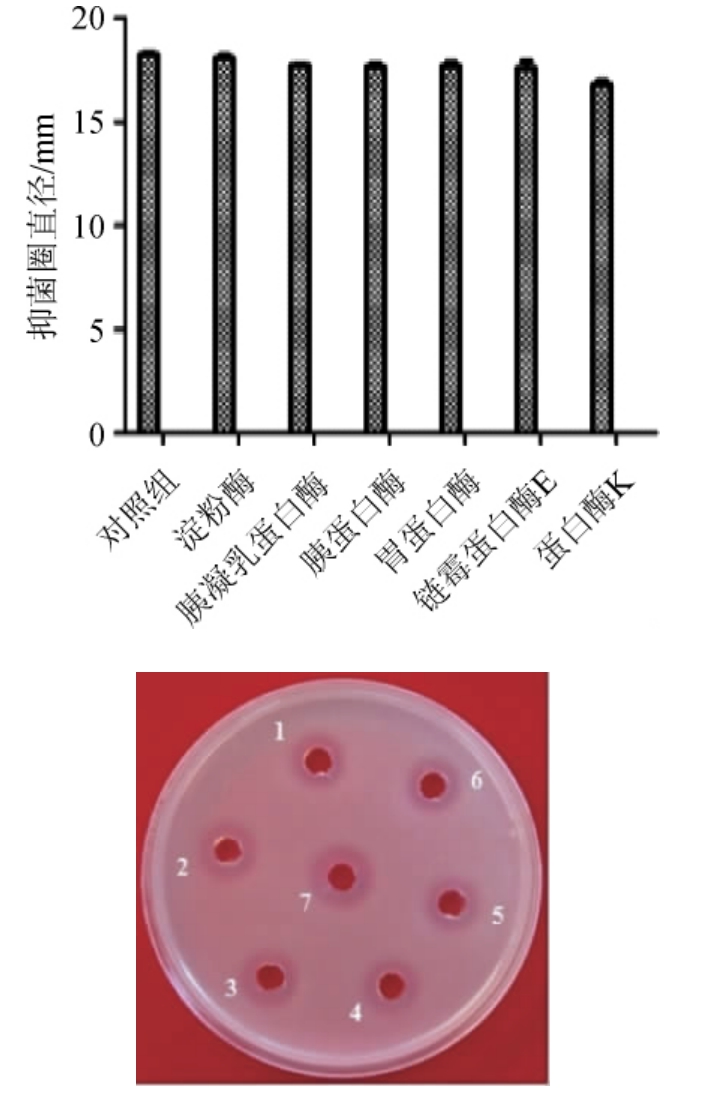
图8 不同蛋白酶对菌株NEL-002发酵液抑菌活性的影响
Fig.8 Effect of different protease on antibacterial activity of strain NEL-002
1:胰凝乳蛋白酶;2:胃蛋白酶;3:链霉蛋白酶E;4:蛋白酶K;5:胰蛋白酶;6:淀粉酶;7:CK。
2.4 最低抑菌浓度及杀菌浓度
采用微量稀释法测定,菌株NEL-002粗提活性物质的MIC和MBC,结果如图9所示。在96孔板上横排阴性孔中最后一孔所对应的浓度即最低抑菌浓度(MIC)为62.5 μg/mL。菌落计数为0的平板所对应的阴性孔浓度,即菌株NEL-002粗提活性物质能够拮抗MRSA菌生长的最低杀菌浓度(MBC)为500 μg/mL。
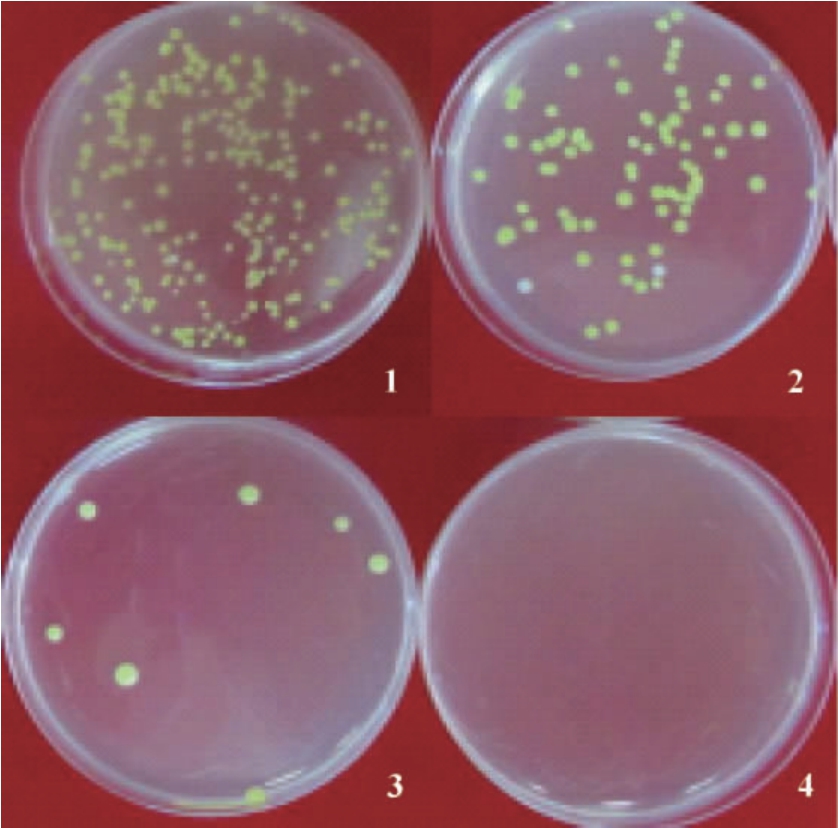
图9 菌株NEL-002粗提活性物质最低抑菌浓度及最低杀菌浓度
Fig.9 Minimum inhibitory concentration and minimum bactericidal concentration of the crude extracts from strain NEL-002
1:62.5 μg/mL;2:125 μg/mL;3:250 μg/mL;4:500 μg/mL。
3 结论
本研究对红树林根部土壤拮抗微生物进行研究,对土壤悬浮液处理、分离筛选得到具有抗MRSA活性的菌株NEL-002,经细菌形态观察、生理生化特性及16S rDNA 序列分析等方法鉴定该菌株为萎缩芽孢杆菌(Bacillusatrophiae)。菌株NEL-002采用LB液体培养基得到发酵液经石油醚萃取粗体物抗MRSA菌活性最强,且在40~80 ℃、pH在5~10较稳定,对多种蛋白酶不敏感;最低抑菌质量浓度为62.5 μg/mL,最低杀菌质量浓度为500 μg/mL。GC-MS鉴定出抗菌活性物质为十甲基环戊硅氧烷、十二甲基环六硅氧烷及邻苯二甲酸二丁酯。
[1]陈方圆,马笑雪,蔡景钰,等.多重耐药性金黄色葡萄球菌(MRSA)的临床药物治疗及耐药机制研究[J].微生物学杂志,2010,1(1):71-74.
[2]顾国威,李尔凡,申冬梅.耐甲氧西林金黄色葡萄球菌的临床分布及耐药性分析[J].临床合理用药杂志,2021,14(13):171-173.
[3]孙盼盼,菅记涌,解泽强,等.2009—2019 年北京世纪坛医院金黄色葡萄球菌临床感染分布及耐药性分析[J].现代预防医学,2021,48(7):1305-1309.
[4]王敏.耐甲氧西林金黄色葡萄球菌分子流行病学及临床感染特征的研究[D].北京:中国人民解放军军事医学科学院,2017.
[5]蔡玉华,胥振国,刘修树,等.白术提取物及其在抗耐甲氧西林金黄色葡萄球菌方面的初步应用[J].齐齐哈尔医学院学报,2018,39(15):1740-1743.
[6]唐克文,李从荣,汪倩钰.2016~2018 年某重症监护病房耐甲氧西林金黄色葡萄球菌的分布特点和耐药变迁[J].广西医学,2020,42(3):315-318,333.
[7]吕玮.耐药革兰阳性球菌感染的诊治[J].中国医刊,2013,48(10):8-10.
[8]BASSETTI M,CARNELUTTI A,CASTALDO N,et al.Important new therapies for methicillin-resistant Staphylococcus aureus[J].Expert Opin Pharmaco,2019,20(18):2317-2334.
[9]王高学,高鸿涛,付维法,等.蕈状芽孢杆菌代谢产物增强小鼠免疫力活性物质的分离、鉴定[J].微生物学通报,2009,36(6):858-864.
[10]卢护木,詹振宇,李蜜,等.涠洲岛珊瑚礁海洋真菌的分离鉴定及其抗MRSA 活性筛选[J].广西科学,2020,27(5):520-525.
[11]邹远军.抗多重耐药性金黄色葡萄球菌(MRSA)菌株SC-2 的物质基础研究[D].重庆:重庆理工大学,2017.
[12]刘颖,洪葵,庄令,等.红树林样品不经分离的微生物群体培养物生物活性研究[J].微生物学报,2007,47(1):110-114.
[13]沈南星.南海红树根际土壤真菌的分离、筛选与抗菌活性物质研究[D].扬州:扬州大学,2019.
[14]刘颖,罗绮淇,林秀源,等.湛江硇洲岛全缘马尾藻共附生抗菌活性菌的筛选与多样性分析[J].现代食品科技,2014,30(3):13-17,6.
[15]东秀珠,蔡妙英.常见细菌系统鉴定手册[M].北京:科学出版社,2001:364-398.
[16]咸洪泉,郭立忠,李树文.微生物学实验[M].北京:高等教育出版社,2018:16-23.
[17]苏德模,马绪荣.药品微生物学及检验技术[M].北京:华龄出版社,2007:498.
[18]叶生梅,尹为想,程其国.地衣芽孢杆菌BLy 产抑菌物质培养条件优化[J].安徽工程大学学报,2017,32(5):5-9.
[19]李钦,王引权,张慧,等.基于气相色谱-质谱联用技术的道地与近道地产区当归挥发油化学组分分析[J].甘肃中医药大学学报,2021,38(1):29-32.
[20]JASIM H,HUSSEIN A O,HAMEED I H,et al.Characterization of alkaloid constitution and evaluation of antimicrobial activity of Solanum nigrum using gas chromatography mass spectrometry(GC-MS)[J].J Pharmacogn Phytother,2015,7(4):56-72.
[21]TASWAR AHSAN,et al.Extraction and identification of bioactive compounds (eicosane and dibutyl phthalate) produced by Streptomyces strain KX852460 for the biological control of Rhizoctonia solani AG-3 strain KX852461 to control target spot disease in tobacco leaf[J].AMB Express,2017,7(1):1-9.
[22]南措吉,李毛加,张金魁,等.藏药止泻木子挥发油超临界提取工艺、GC-MS 分析及抑菌活性研究[J].湖南师范大学(自然科学学报),2020,43(2):64-68.
[23]SHARIFI-RAD J,ALFATEMI S M H,MIRI A,et al.Exploration of phytochemical and antibacterial potentiality of Anagallis arvensis L.extract against methicillin-resistant Staphylococcus aureus(MRSA)[J].British Biotechnol J,2015,10(2):1-8.
[24]杨艳红,余瑛,胡永强,等.解淀粉芽孢杆菌AF1 发酵液的抗菌活性与抗菌机理[J].生物技术通报,2017,33(9):223-230.
[25]陈志宇.抗MRSA 活性蜚蠊肠道球孢链霉菌WA5-2-37 次级代谢产物的初步研究[D].广州:广东药科大学,2019.
[26]杨鼎超.山苍子内生真菌多样性及其挥发性物质研究[D].南昌:江西农业大学,2018.