辣椒酸又称为辣椒红酸汤,是贵州黔东南地区苗族、侗族等民族常见的传统发酵食品。辣椒酸以辣椒为主要原材料,经传统自然发酵而成,是制作凯里红酸汤的半成品;可与番茄红酸汤按照一定比例混合,经二次发酵便可制成凯里红酸汤[1]。研究发现,酸汤具有生津止渴、清热解毒、健脾开胃和促进消化等功能[2]。在黔东南地区有着“三天不吃酸,走路打串串”的说法[3]。凯里地区为酸汤主要食用地区,有着悠久的历史。2012年,经国家质检总局批准,“凯里红酸汤”正式成为地理标志保护产品。
目前,酸汤中微生物研究渐渐成为热点。如酸汤中优势微生物分离[4-5],酸汤中微生物多样性分析[6-8]、乳酸菌发酵酸汤品质变化研究[9],酸汤微生物发酵风味物质检测[10],酸汤微生物发酵工艺研究[11-12],酸汤口服液和饮料产品开发利用[13-14]、酸汤对高脂血症大鼠血脂以及肠道影响[13,15]、微生态制剂对断奶仔猪肠道微生物影响[16]等。本研究借助发展成熟的Illumina MiSeq高通量测序技术,对凯里传统发酵辣椒酸及其工业化成品进行研究。利用乳酸菌常用MRS培养基从辣椒酸中筛选优势乳酸菌,以期为研究酸汤发酵工艺以及酸汤产品开发奠定基础。
1 材料与方法
1.1 材料与试剂
5份传统发酵成熟阶段的辣椒酸样品:从凯里市东门街农贸市场、金玉农贸市场、开发区农贸市场以及鸭塘镇农贸市场采集,分别编号为ST8、ST11、ST17、ST23和ST25;某品牌辣椒酸样品1份(对照):市售,出厂前已进行灭活处理,编号为ST21。每个样品采集时取30 mL,装入50 mL无菌离心管,并置于便携式冰盒中进行携带。样品随即运至昆明理工大学生命科学与技术学院应用微生物实验室于4 ℃冰箱暂存待用。
脱氧核糖核酸(deoxyribonucleic acid,DNA)提取裂解缓冲液,TE缓冲液[24];玻璃珠(直径212~300 mm):美国Sigma公司;PremixExTaqTM(2×):日本TaKaRa公司;QIAquick gel Extraction Kit试剂盒:德国Qiangen公司;MRS培养基:北京鼎国生物技术有限公司;蔗糖、乙二胺四乙酸(ethylene diamine tetraacetic acid,EDTA)、琼脂糖:上海生工生物工程有限公司;甘油:天津试剂三厂。上述试剂均为分析纯或生化试剂。
1.2 仪器与设备
SX-300高压灭菌锅:日本TOMY Digital Biology公司;GHP-9160恒温培养箱:上海一恒科学仪器有限公司;SWCJ-1FD超净工作台:苏净安泰公司;ABI 7200 聚合酶链式反应(polymerase chain reaction,PCR)仪:美国ABI公司;Roche_454罗氏GS-FLX测序仪:瑞士Roche公司;Labnet230V EU涡旋仪:美国Labnet公司;SIGMA 3-18K高速离心机:德国Sigma公司;YP1002N电子天平:上海恒平科学仪器有限公司;ADW-B纯水仪:美国艾科浦国际有限公司;GL-3250A磁力搅拌器:麒麟贝尔仪器制造有限公司;Ultrospec 2100 pro紫外分光光度计:安玛西亚(中国)有限公司。
1.3 方法
1.3.1 辣椒酸样品细菌宏基因组DNA提取
称取辣椒酸样品500 mg,参考文献[17]的方法进行改良[18],对样品细菌总基因组DNA进行提取。将提取的DNA置于-20 ℃冰箱中保存待用。
1.3.2 细菌16S rDNA目的基因扩增和高通量测序
使用细菌16S rDNA通用引物,扩增高变区V2-V4区域。引物序列如下:
338F(5'-ACTCCTACGGGAGGCAGCAG-3')
806R(5'-GGACTACHVGGGTWTCTAAT-3')
以1.3.1中提取DNA为模板,对细菌16S rDNA V2-V4区进行PCR扩增。PCR扩增体系:Premix ExTaqTM聚合酶10 μL,模板基因组DNA0.5 μL,目的基因上下游引物各1 μL,双蒸水(ddH2O)8 μL。PCR扩增程序:95 ℃预变性5 min;95 ℃变性30 s,56 ℃退火1 min,72 ℃延伸15 s,循环30次后;72 ℃延伸5 min。
吸取上述PCR扩增产物5 μL,用去离子水稀释10倍,按照原反应条件进行5个循环,以减少PCR产物的非特异性扩增[19]。PCR产物用QIAquick gel Extraction Kit试剂盒进行纯化回收,并使用分光光度计定量,使用Illumina Miseq高通量测序技术对PCR产物进行测序[20]。
1.3.3 测序结果分类鉴定
根据barcode将测序序列分配到对应样品中,去除barcode以及引物序列得到有效序列。使用mothur v1.43.1软件包Miseq SOP进行序列拼接,去除质量欠佳序列,保留长度大于400 bp的序列。运用mothur v1.43.1软件classify.seqs命令进行分析,结合Silva的SSU rRNA序列数据库V138分类信息进行分析[21],得到序列分类数据。
1.3.4 α多样性指数分析
使用mothur中classify.seq命令获得样品中微生物群落结构,使用rarefaction.single命令得到微生物Chao1和ACE等指数。以序列相似度为97%划分可操作分类单元(operational taxonomic unit,OTU)。根据以上结果计算样品ACE指数、Chao1指数、Shannon指数以及Coverage等。并根据Rarefaction文件绘制Rarefaction曲线。
1.3.5 辣椒酸中乳酸菌分离
采用倍比稀释涂布法分离辣椒酸中的乳酸菌。在超净工作台中吸取辣椒酸样品1 mL,经无菌生理盐水梯度稀释后,吸取20 μL稀释度为10-6的稀释液涂布于MRS琼脂平板表面。待菌液吸收后,将平板倒置于恒温培养箱中35 ℃静置培养24 h。观察培养菌落形态,挑取具有不同形状、大小以及颜色的单菌落进行2~3次划线分离。结合过氧化氢实验和革兰氏染色实验,选取过氧化氢阴性、革兰氏染色阳性的菌株,加入30%甘油置于-80 ℃冰箱保存[22]。
1.3.6 辣椒酸中乳酸菌分子生物学鉴定
以改良十六烷基三甲基溴化铵(cetyltrimethylammonium bromide,CTAB)法提取1.3.5中分离到的乳酸菌基因组DNA,利用细菌16S rRNA通用引物进行PCR扩增。
引物序列:F27(5'-AGAGTATGATCATGGCTCAG-3'),R1492(5'-TACGGTTACCTTGTTACGACTT-3')
扩增体系:Ex Taq 25.0 μL,F27和R1492引物各1.0 μL,DNA模板2.0 μL,ddH2O 21.0 μL。按照程序95 ℃热变性30 s;60 ℃变性1 min,72 ℃延伸150 s,循环35次后;72 ℃延伸10 min。以便得到足够数量的目的DNA分子。
采用双脱氧链终止法进行序列测定。所得测序核苷酸序列提交美国国家生物信息中心(national center for biotechnology information,NCBI)数据库(http://www.ncbi.nlm.nih.gov/BLAST),利用基本局部比对搜索工具(basic local alignment search tool,BLAST)与Genebank中已知的16S rDNA核苷酸序列进行同源性比较,当被检菌株核苷酸序列与参考菌株同源性大于97%时,即确定为同一个菌种[23]。
1.3.7 乳酸菌代表菌株系统发育分析
选取样品ST8中分离的ST8-4、ST8-7、样品ST11中分离的ST11-7、样品ST17中分离的ST17-2、以及样品ST23中分离的ST23-10、ST23-11和ST25-1作为代表菌株。将代表菌株的16S rDNA核苷酸测序结果登录NCBI网站进行BLAST序列同源性比对,选取同源性较高的菌株构建系统发育树。
2 结果与分析
2.1 样品序列信息和α多样性分析
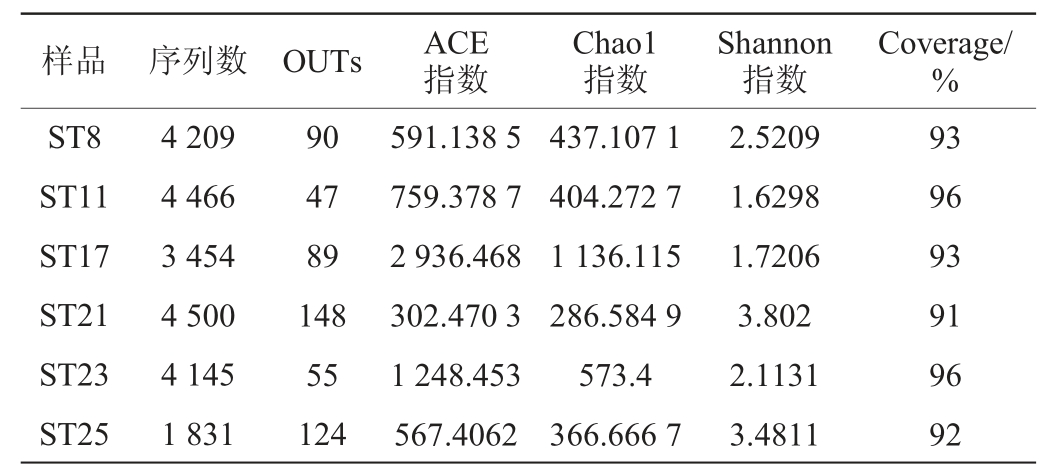
由表1可知,6个辣椒酸样品(ST8、ST11、ST17、ST21、ST23、ST25)由Illumina MiSeq测序共得到22 605个有效序列,553个OTUs其Coverage分别为93%、96%、93%、91%、96%和92%,样品覆盖度比较高,均在90%以上。样品ST17的ACE指数和Chao1指数最高,分别为2 936.468和1 136.115;说明其物种丰度最高。ST21的序列数、OTUs数目以及Shannon指数最高,分别为4 500、148和3.802;说明其物种多样性在所有样品中最高。可见,各个样品之间微生物多样性以及丰度存在一定差异。
表1 不同样品中细菌菌群的α多样性指数
Table 1 Alpha diversity index of bacterial community in different samples
根据Rarefaction数据绘制Rarefaction稀释曲线,结果见图1。当cutoff值为0.03时,样品ST17曲线处于上升趋势。但从表1的Coverage可看出,样品中细菌序列的覆盖度达到了90%以上。说明该样品在发酵过程中起主要作用的微生物已得到分析,物种测序深度已经足够。其余5个辣椒酸样品Rarefaction稀释曲线趋于平缓,说明其测序深度充分,基本可覆盖到样品中的所有物种。
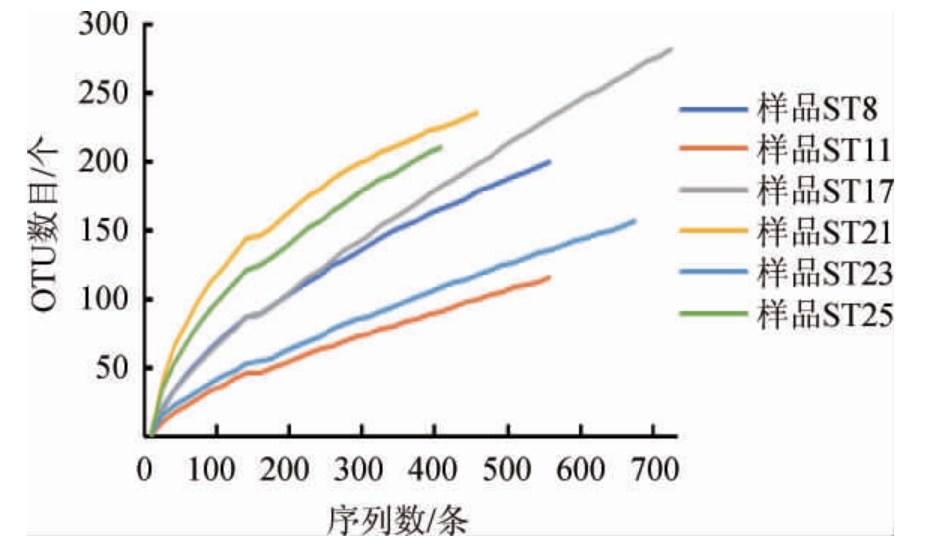
图1 序列相似度为97%细菌Rarefaction评估
Fig.1 Rarefaction evaluation of bacteria with 97% sequence similarity
2.2 门水平细菌多样性分析
从门水平对辣椒酸中细菌群落多样性进行分析,结果见图2。从图2可知,辣椒酸中优势细菌门依次为厚壁菌门(Firmicutes)、变形菌门(Proteobacteria)、类杆菌门(Bacteroidota)和Actinobacteriota,平均相对含量分别为77.9%、19.59%、1.21%和0.95%;其余细菌门相对含量均<0.1%。
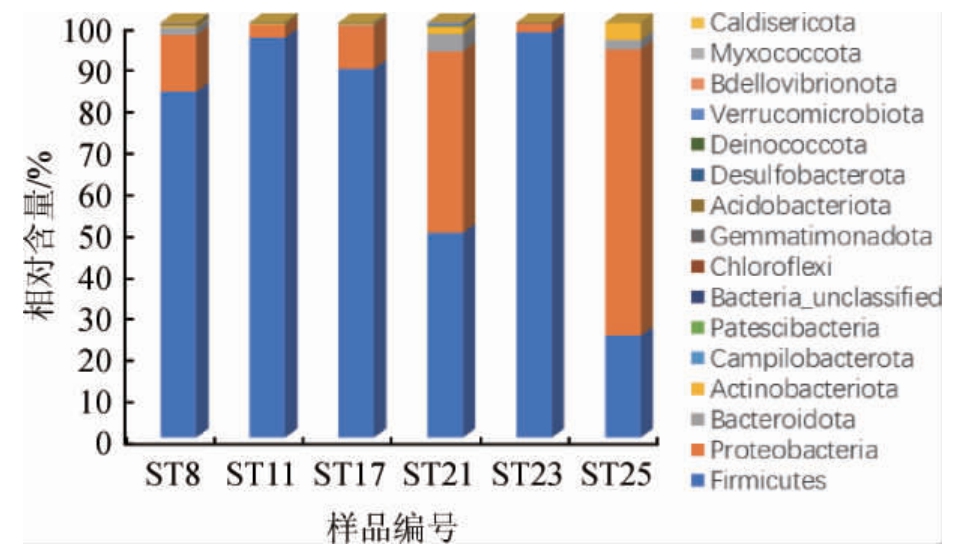
图2 基于门水平辣椒酸中细菌群落结构分析
Fig.2 Analysis of bacterial community structure in peper acid based on phylum level
其中厚壁菌门(Firmicutes)在样品ST11和ST23中占绝对优势,相对含量分别为95.19%和97.66%。该细菌门在样品ST8和ST17中相对含量也较高,为83.33%和88.66%;在样品ST21中相对含量稍低,为49.38%;除了在样品ST25中,厚壁菌门(Firmicutes)在每个样品中相对含量均超过或接近50%。可见厚壁菌门(Firmicutes)为辣椒酸中的优势菌门。样品ST25中,厚壁菌门(Firmicutes)相对含量为24.54%,在所有样品中含量最低;而变形菌门(Proteobacteria)在该样品中相对含量为69.01%,在所有样品中含量最高。样品ST8、ST17和ST21中变形菌门(Proteobacteria)相对含量也比较高,分别为13.66%、10.41%和43.71%;另外两个样品ST11和ST23中相对含量最低,分别为3.03%和2.01%。可见变形菌门(Proteobacteria)细菌门在不同辣椒酸中相对含量差异很大。
王琪琪等[6]对辣椒红酸汤(即辣椒酸)中微生物多样性研究发现,厚壁菌门(Firmicutes)、蓝藻细菌门(Cyanobacteria)和变形菌门(Proteobacteria)为样品中的优势菌门。而本研究也发现了大量蓝藻细菌门(Cyanobacteria)的序列,但考虑到其序列为叶绿体的[24],即辣椒酸发酵时加入新鲜红辣椒所致。因此,并未归为样品细菌门当中。
2.3 属水平细菌多样性分析
从属水平对辣椒酸中细菌群落多样性进行分析,见图3。总体上,辣椒酸样品中相对含量>1%的属有乳酸杆菌(Lactobacillus)、假单胞菌属(Pseudomonas)、肠杆菌属属(Enterobacter)、Lelliottia、芽孢杆菌属(Bacillus)、葡萄球菌属(Staphylococcus)和寡养单胞菌属(Stenotrophomonas),一共7个属,平均相对含量分别为72.02%、5.59%、3.97%、5.30%、1.64%、1.07%和1.02%。可见,各样品中乳酸杆菌属(Lactobacillus)相对含量最高。单个样品中,样品ST8、ST11、ST17、ST21和ST23,乳酸杆菌属(Lactobacillus)为优势菌属,相对含量分别为67.74%、95.09%、83.95%、38.34%和95.01%。从乳酸杆菌属(Lactobacillus)的相对含量可看出,样品ST11(95.09%)和ST23(95.01%)中该细菌属占绝对优势,样品ST17(83.95%)次之,样品ST25(1.81%)中最低。而假单胞菌属(Pseudomonas)和Lelliottia细菌属在样品ST25中相对含量较高,分别为27.23%和11.79%,该样品的细菌多样性和丰度比较分散。从以上数据可以看出乳酸杆菌(Lactobacillus)和假单胞菌属(Pseudomonas)为辣椒酸中的优势菌属,与王琦琦等[6]研究结果一致。
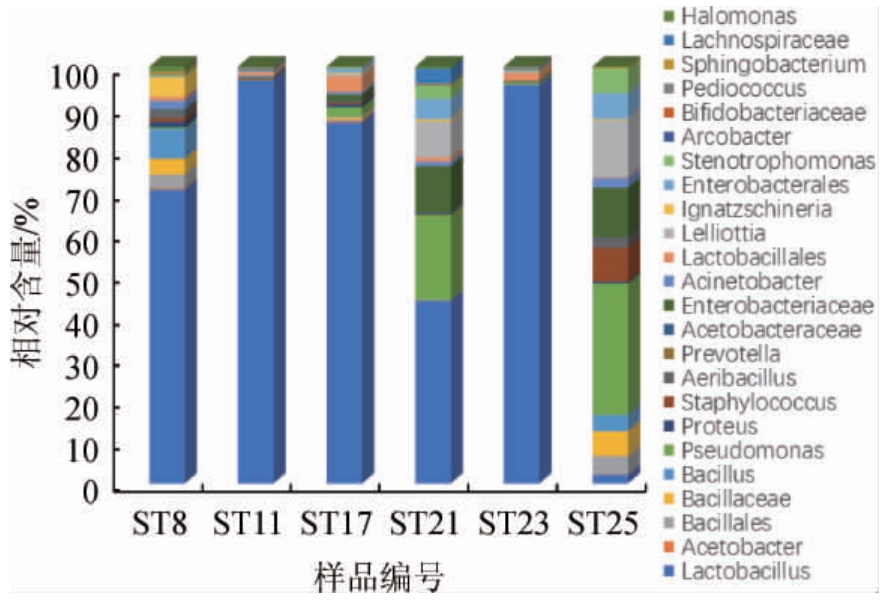
图3 基于属水平辣椒酸中细菌群落结构分析
Fig.3 Analysis of bacterial community structure in peper acid based on genus level
乳酸杆菌属(Lactobacillus)作为乳酸菌中最大的一个属,在人和动物肠道中维持着肠道的微生态平衡。同时有研究表明酸汤在改善胃肠道方面具有保健功能[4]。在辣椒酸样品中,存在着大量的假单胞菌属(Pseudomonas)和少量的葡萄球菌属(Staphylococcus)。报道指出,隶属于金黄色葡萄球菌属(Staphylococcus aureus)[25]和铜绿假单胞菌属(Pseudomonas aeruginos)[26]部分“种”对人体产生一定的条件致病性。因此,在制作传统发酵酸辣椒时需注意生产环境的影响作用。
2.4 乳酸菌鉴定结果
结合Illumina MiSeq高通量测序数据,在分析辣椒酸样品属分类水平细菌多样性时发现乳酸菌相对含量很高。为进一步探明辣椒酸中的优势乳酸菌类群,利用MRS合成培养基对辣椒酸样品中乳酸菌进行分离培养,结果表明,从辣椒酸样品中一共分离出了43株细菌。分别为34株乳酸菌、6株芽孢杆菌和3株葡萄球菌,分别占分离菌株的79.07%、13.95%和6.98%。其中分离出的植物乳杆菌(Lactobacillus plantarum)最多,一共20株,该菌被认为是影响泡菜感官品质的重要菌之一[27];其他分别为副干酪乳杆菌(Lactobacillus paracasei)5株、枯草杆菌(Bacillus sp.)4株、干酪乳杆菌(Lactobacillus casei)3株、短乳杆菌(Lactobacillus brevis)和白色芽孢杆菌(Bacillus albus)各2株。戊糖乳杆菌(Lactobacillus pentosus)、乳酸杆菌(Lactobacillus sp.)、葡萄球菌(Staphylo coccus sp.)、免培养葡萄球菌(Uncultured Staphylococcus sp.)、假肠膜明串珠菌(Leuconostoc pseudomesenteroides)、巴氏葡萄球菌(Staphylococcus pasteuri)和免培养乳酸杆菌(Uncultured Lactobacillus)各1株。根据各样品名称,将其对应分离的菌株进行命名,其鉴定结果见表2。
表2 筛选菌种鉴定结果
Table 2 Identification results of screened strains
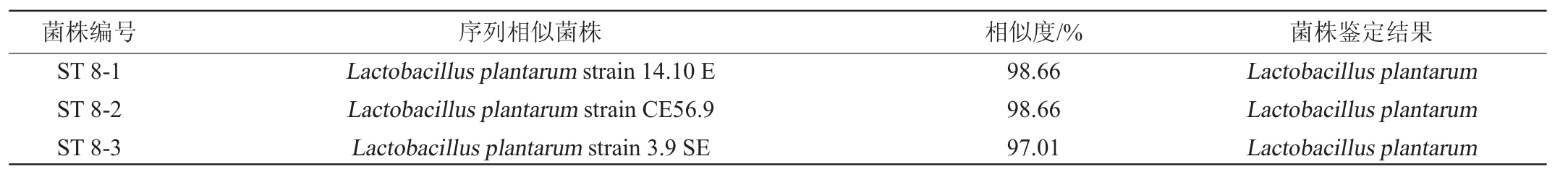
样品ST8中分离出植物乳杆菌(Lactobacillus plantarum)14株,戊糖乳杆菌(Lactobacillus pentosus)1株。向凡舒等[28]从酸豇豆中分离得到12株植物乳杆菌(Lactobacillus plantarum)占分离菌株的92.3%,该菌在蔬菜发酵过程中起到重要的作用。徐莉等[29]研究发现植物乳杆菌(Lactobacillus plantarum)可有效抑制酸汤中杂菌的生长,可缩短发酵反应进程,影响酸汤风味。田永峰[4]从红酸汤中分离出4株杆菌,研究发现乳杆菌影响酸汤的营养价值和风味。在酸汤发酵后期乳杆菌产生大量乳酸,可迅速降低发酵环境的pH,抑制其他菌群生长,乳杆菌成为最后的优势菌群。
样品ST11中分离出植物乳杆菌(Lactobacillusplantarum)6株,乳酸杆菌(Lactobacillus sp.)、葡萄球菌(Staphylococcus sp.)、免培养葡萄球菌(Uncultured Staphylococcus sp.)和假肠膜明串珠菌(Leuconostoc pseudomesenteroides)各1株。其中葡萄球菌(Staphylococcus sp.)和免培养葡萄球菌(Uncultured Staphylococcussp.)多数为非致病菌,但少数可导致疾病。提示传统发酵食品中潜藏着一定的食品安全风险,需引起重视。
样品ST17分离出植物乳杆菌(Lactobacillus plantarum)2株。样品ST21为工业化辣椒酸成品,未分离出乳酸菌。显然产品在出厂前进行了活菌灭活处理[30],用以保持产品风味稳定性和常温保存时延长产品货架期。样品ST23中分离出副干酪乳杆菌(Lactobacillus paracasei)5株、干酪乳杆菌(Lactobacillus casei)3株、巴氏葡萄球菌(Staphylococcus pasteuri)和免培养乳酸杆菌(Uncultured Lactobacillus)各1株;样品ST25分离出芽孢杆菌(Bacillus sp.)4株,白色芽孢杆菌(Bacillus albus)2株。从以上辣椒酸中微生物分离结果可看出,不同样品中分离出的细菌种类和数量基本都不相同。不同微生物在辣椒酸发酵时产生不同的产物,造就了辣椒酸的不同风味。
续表

2.5 代表菌株系统发育分析
将随机挑选同一个菌种名称的菌株作为代表菌株ST8-4、ST8-7、ST11-7、ST11-10、ST17-2、ST23-10、ST23-11和ST25-1菌株的16S rRNA核苷酸序列提交NCBI数据库进行同源性比对,并构建系统发育树,如图4所示。发现菌株ST8-7与植物乳杆菌(Lactobacillus plantarum)8m-21呈现出较高的相似度;菌株ST8-4与戊糖乳杆菌(Lactobacillus pentosus)CE14.15呈现出较高的相似度;菌株ST11-7和ST11-10与乳酸杆菌(Lactobacillus sp.)THK-W4呈现出较高的相似度;菌株ST17-2与短乳杆菌(Lactobacillus brevis)gp107呈现出较高的相似度;菌株ST23-10h与副干酪乳杆菌(Lactobacillus paracasei)呈现出较高的相似度;菌株ST23-11与副干酪乳杆菌(Lactobacillus paracasei)6664呈现出较高的相似度;菌株ST25-1与枯草杆菌(Bacillus sp.)Pg 15呈现出较高的相似度。
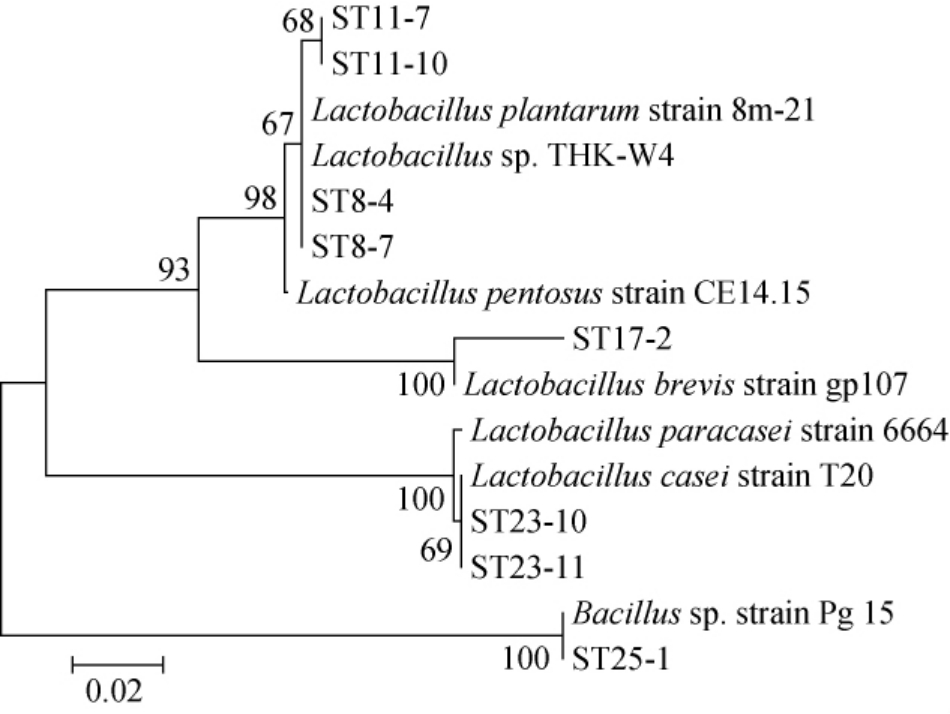
图4 代表菌株基于16S rRNA基因序列构建的系统发育树
Fig.4 Phylogenetic tree of representative strains based on 16S rRNA gene sequence
3 结论
本研究结合Illumina MiSeq高通量测序技术和传统纯培养技术对凯里地区辣椒酸中微生物群落多样性进行分析。发现凯里地区辣椒酸中优势门为厚壁菌门(Firmicutes)和变形菌门(Proteobacteria),所占比例最大的优势属为乳酸杆菌属(Lactobacillus)。利用MRS培养基,采用纯培养技术分离出的细菌多为乳酸杆菌,部分为芽孢杆菌以及少数葡萄球菌;且不同样品分出的细菌种类基本不同。可能与辣椒酸生产环境以及生产工艺的不同相关。纯培养分离的细菌当中以植物乳杆菌(Lactobacillusplantarum)为主。由此可见,凯里地区辣椒酸中含有丰富的乳酸菌资源,有待进一步的开发利用。
[1]鲁杨,王楠兰,李贤,等.凯里红酸汤主要营养和功能成分的分析研究[J].食品研究与开发,2019,40(7):163-166.
[2]石敏,袁玮.“酸汤”发酵过程中酸度的动态变化[J].凯里学院学报,2007(3):30-31.
[3]张璇.贵州“红酸汤”半成品中微生物区系的研究[D].重庆:西南大学,2011.
[4]田永峰.贵州苗族发酵型酸汤中功能性乳酸菌的筛选[D].贵阳:贵州大学,2008.
[5]后立琼.苗族酸汤中乳酸菌的分离鉴定及发酵动力学模型研究[D].雅安:四川农业大学,2012.
[6]王琪琪,田界先,潘宗东,等.基于Illumina MiSeq 分析贵州凯里酸汤独特风味的优势菌群[J].食品与发酵工业,2020,46(14):40-47.
[7]肖甜甜,冯子娟,邱树毅,等.苗家白酸汤中微生物群落多样性研究及其优势微生物的筛选[J].食品与发酵科技,2021,57(1):1-11.
[8]田亚.贵州米酸汤优势微生物与品质特性的相关性研究[D].贵阳:贵州大学,2020.
[9]郑莎莎,胡萍.利用乳酸菌发酵红酸汤的品质变化研究[J].中国调味品,2019,44(8):65-70.
[10]田亚,王晓宇,杨欣,等.贵州米酸汤发酵过程中风味品质的研究[J].中国调味品,2020,45(5):94-99.
[11]韦明明.番茄酸汤发酵过程分析及混菌发酵工艺研究[D].南京:南京农业大学,2016.
[12]张东亚,徐俐.响应面法优化复合型红酸汤乳化工艺[J].包装与食品机械,2017,35(4):19-23.
[13]鲁青松.凯里红酸汤口服液开发及功能性评价[D].贵阳:贵州大学,2019.
[14]石敏,王美,袁玮,等.凯里米酸汤饮料工艺研究[J].凯里学院学报,2016(3):119-122.
[15]曲子晗.凯里红酸汤对高脂血症大鼠肠道影响[D].贵阳:贵州医科大学,2020.
[16]张滔滔.酸汤微生态制剂对断奶仔猪应激及肠道微生物的影响[D].贵阳:贵州大学,2020.
[17]SCHMIDT T M,DELONG E F,PACE N R.Analysis of a marine picoplankton community by 16S rRNA gene cloning and sequencing[J]. J Bacteriol,1991,173(14):4371-4378.
[18]李晓然,刘晓峰,张海燕,等.利用高通量测序分析云南两个地区豆豉微生物群落的多样性[J].现代食品科技,2014,30(12):61-67.
[19]THOMPSON J R,MARCELINO L A,POLZ M F.Heteroduplexes in mixed-template amplifications:formation,consequence and elimination by'reconditioning PCR'[J]. Nucleic Acids Res,2002,30(9):2083-2088.
[20]尚云,柳陈坚,刘祥祥,等.基于高通量测序分析结肠息肉患者肠道细菌群落结构[J].昆明理工大学学报(自然科学版),2018,43(2):71-78.
[21]SCHLOSS P D,WESTCOTT S L,RYABIN T,et al.Introducing mothur:open-source,platform-independent,community-supported software for describing and comparing microbial communities[J].Appl Environ Microbiol,2009,75(23):7537-7541.
[22]代程洋,陈江红,郭壮,等.枣阳酸浆水来源乳酸菌对泡菜及泡菜水发酵品质的影响[J].中国酿造,2019,38(5):54-58.
[23]GOEBEL B M,STACKEBRANT E.Cultural and phylogenetic analysis of mixed microbial populations found in natural and commercial bioleaching environments[J].Appl Environ Microbiol,1994,6(5):1614-1621.
[24]张海燕,柳陈坚,刘祥祥,等.基于高通量测序分析老面细菌多样性[J].食品工业科技,2016,37(15):145-149.
[25]THOMER L,SCHNEEWIND O,MISSIAKAS D.Pathogenesis of Staphylococcus aureus bloodstream infections[J]. Annu Rev Pathol,2016,11:343-364.
[26]MAYER-HAMBLETT N,RETSCH-BOGART G,KLOSTER M,et al.Azithromycin for earlypseudomonas infection in cystic fibrosis.The optimize randomized trial[J].Am J Resp Crit Care,2018,198(9):1177-1187.
[27]XIA Y J,LIU X F,WANG G Q,et al.Characterization and selection of Lactobacillus brevis starter for nitrite degradation of Chinese pickle[J].Food Control,2017,78:126-131.
[28]向凡舒,黄怡,陈小艳,等.建始地区酸豇豆盐水细菌多样性及乳酸菌分离鉴定[J].中国酿造,2020,39(10):61-65.
[29]徐俐,戴岳宗.乳酸菌对酸汤中亚硝酸盐变化研究[J].中国调味品,2009,34(5):43-46.
[30]曾荣妹,韩琳,黄平.贵州红酸汤火锅调料的研究进展及工业化进程[J].食品与发酵科技,2014,50(5):72-75.