酿酒酵母(Saccharomyces cerevisiae)作为重要的模式生物[1],在遗传学和分子生物学研究中都有重要的应用。然而酿酒酵母细胞壁呈甘露聚糖-蛋白质-葡聚糖的三明治结构[2-4],非常坚韧,难以破碎,导致胞内遗传物质难以释放[5],干扰核糖核酸(ribonucleic acid,RNA)的提取。而在进行Northern印迹及杂交分析、转录组分析、信使核糖核酸(messenger ribonucleic acid,mRNA)纯化用于体外构建互补脱氧核糖核酸(complementary deoxyribonucleic acid,cDNA)文库等分子生物学研究时,都需要高质量的RNA。因此,获得高纯度、高质量、完整性好的RNA是酵母进行分子生物学研究的基础。虽然研究学者已经建立了多种生物特异性RNA分离和提取方法[6-8],开发了多种RNA分离和提取试剂盒[9-10],如十六烷基三甲基溴化铵(hexadecyltrimethylammonium bromide,CTAB)法[11]、改进总RNA提取试剂(Trizol)法[12-13]、甲酰胺法[14]等,但不同方法在提取效果、试剂组成和操作步骤等方面都存在差异,从而使RNA提取的效果也不尽相同。
虽然有研究通过不同破壁方法来提高RNA的提取效率,如易弋等[15]在提取酵母菌总RNA的试验中认为反复冻融和液氮研磨是较为有效且简便的酵母菌破壁方法。商安全等[16]通过在Trizol试剂溶液中加钢珠匀浆振荡辅助破壁,提取的白假丝酵母菌总RNA浓度好、质量高,提取效果优于溶菌酶法,尚鲜见将不同提取RNA方法放在同一体系下进行比较,因此,本研究选择试剂盒法、Trizol 法、热酚法3种方法提取酿酒酵母总RNA,为解决破壁问题,选用酵母破壁酶辅助破壁,并进行菌体用量的条件优化,比较了不同方法提取酿酒酵母总RNA的效果,以期为酵母总RNA的提取提供参考。
1 材料与方法
1.1 材料与试剂
酿酒酵母(Saccharomyces cerevisiae)GGSF16:广西科技大学发酵工程研究所;RNA提取酚(分析纯)、酵母破壁酶溶液:北京索莱宝科技有限公司;Trizol试剂:赛默飞世尔科技公司;RNA提取试剂盒(非酵母专用总RNA提取试剂盒):市售;焦炭酸二乙酯(分析纯):上海吉至生化科技有限公司;三氯甲烷(分析纯):成都市科龙化工试剂厂;异丙醇(分析纯):西陇科学股份有限公司。
0.1%焦炭酸二乙酯(diethyl pyrocarbonate,DEPC)处理水:取1 mL DEPC溶液,用超纯水定容至1 L,处于振荡状态下过夜放置,121 ℃灭菌40 min;三羟甲基甲胺基乙磺酸溶液(2-(tris(hydroxymethyl)methylamino)ethane-1-sulphonic acid,TES):取1 mL 1 mol/L的三(羟甲基)氨基甲烷(Tris(hydroxymethyl)aminomethane,Tris-HCl)(pH为7.5),2 mL 0.5 mol/L的乙二胺四乙酸(ethylene diamine tetraacetic acid,EDTA)(pH为8.0),5 mL 10%的十二烷基硫酸钠(sodium dodecyl sulfate,SDS),用0.1% DEPC处理水定容至100 mL备用。
0.01mol/L磷酸盐缓冲溶液(phosphate buffered solution,PBS):称取氯化钠8.0 g,氯化钾0.2 g,磷酸氢二钠1.44 g,磷酸二氢钾0.24 g,加0.1% DEPC处理水溶解并定容至1 L,pH调至7.4,121 ℃灭菌20 min。
酵母浸出粉胨葡萄糖(yeast extract peptone dextrose,YPD)培养基:青岛高科技工业园海博生物技术有限公司。
1.2 仪器与设备
H2100R低温高速离心机:湖南湘仪离心机仪器有限公司;HH 系列数显恒温水浴锅:金坛市科析仪器有限公司;B-500超微量分光光度计:上海元析仪器有限公司;JY02S紫外分析仪:北京君意东方电泳设备有限公司;LDZH-100KBS立式压力蒸汽灭菌器:上海申安医疗器械厂;DYY-6D电泳仪:北京市六一仪器厂;ZWYR-C2402C叠式恒温调速摇床:上海智诚分析仪器制造有限公司。
1.3 方法
1.3.1 实验器材预处理
在本次试验中,所有实验器材均用0.1%的DEPC水过夜浸泡,121 ℃灭菌40 min。在整个实验操作中始终佩戴一次性手套,并及时更换,以避免RNA污染。
1.3.2 酿酒酵母细胞培养
接种酿酒酵母GGSF16于100 mL YPD液体培养基中,30 ℃、160 r/min培养10 h,得到种子液。按10%种子液接种至YPD液体培养基中,30 ℃、160 r/min继续培养至OD600nm值为1.0,得到酵母菌GGSF菌悬液。
1.3.3 不加酵母破壁酶处理下三种方法的比较
(1)试剂盒法
取750 μL酵母菌菌悬液,4 ℃、12 000 r/min条件下离心2 min,弃去培养基,利用试剂盒法提取酵母总RNA。TaKaRa试剂盒提取过程详见其说明书。产物用于电泳分析或-80 ℃保存。
(2)Trizol法
取750 μL酵母菌菌悬液,4 ℃、12 000 r/min条件下离心2 min,弃去培养基。在菌体中加入750 μL Trizol溶液,冰浴5 min后加入150 μL三氯甲烷,剧烈振荡15 s,冰浴2~3 min,4 ℃、12 000 r/min条件下离心15 min。取水相至另一个离心管,并加入500 μL的异丙醇,上下颠倒,混匀后冰浴10 min,4 ℃、12 000 r/min条件下离心10 min,弃上清。在白色沉淀中加入1 mL体积分数为75%乙醇,上下颠倒混匀,4 ℃、7 500r/min条件下离心5 min,弃上清。在室温下晾晒5 min后加50 μL的0.1% DEPC处理水溶解。产物用于电泳分析或-80 ℃保存。
(3)热酚法
取750 μL酵母菌菌悬液,4 ℃、12 000 r/min条件下离心2 min,弃去培养基。在菌体中加入1 mL PBS重悬,4 ℃、12 000 r/min条件下离心2 min,弃上清。加入400 μL TES溶液和400 μL RNA提取酚,剧烈振荡混匀后65 ℃水浴10 min,期间每隔2 min混匀一次,冰浴5 min后,4 ℃、12 000 r/min条件下离心15 min。将水相转移至新的离心管中,加入400 μL RNA提取酚/三氯甲烷/异丙醇(25∶24∶1,V/V)抽提一次,4 ℃、12 000 r/min条件下离心15 min。将水相转移至新管,加入1/10体积的乙酸钠和2倍体积的无水乙醇,冰浴3 min,4 ℃、12 000 r/min条件下离心5 min,弃上清。用1 mL体积分数为75%乙醇洗涤,上下颠倒混匀,4 ℃、7 500 r/min条件下离心5 min,弃上清。在室温下晾晒5 min后加50 μL的0.1% DEPC处理水溶解。产物用于电泳分析或-80 ℃保存。
1.3.4 酵母破壁酶处理下三种方法的比较
在1.5 mL离心管中分别加入100 μL、250 μL、500 μL、750 μL、1.0 mL、1.5 mL、3.0 mL的酵母菌菌悬液,4 ℃、12 000 r/min条件下离心2 min,弃去培养基。在离心管中加入25 μL的酵母破壁酶溶液,30 ℃培养45 min。利用1.3.3中所述的3种方法分别提取酵母总RNA。
1.3.5 总RNA浓度及纯度检测
利用超微量分光光度计测定总RNA溶液在波长260 nm和280 nm处的吸光度值(A260nm和A280nm),并计算总RNA的浓度,并以A260nm/A280nm,A260nm/A230nm的大小判断RNA样品纯度。
1.3.6 总RNA完整性检测
取1 μL提取得到的RNA,加入1 μL的上样缓冲液和4 μL的0.1% DEPC处理水混匀后加入到1%凝胶的加样孔中,于1×TBE缓冲液中180 V电泳10 min。电泳完成后,用紫外分析仪进行分析。
2 结果与分析
2.1 不加酵母破壁酶提取酵母总RNA
取750 μL酿酒酵母培养液,按1.3.3所述的3种方法分别提取总RNA,并进行浓度、纯度和电泳分析,结果分别见表1和图1。
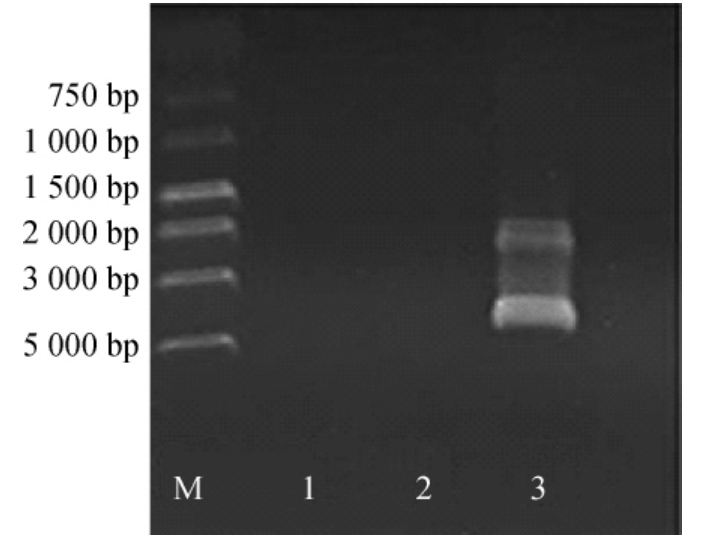
图1 不同方法提取酵母总RNA电泳图
Fig.1 Electrophoretogram of total RNA extracted from yeast by different methods
M为Marker;1为试剂盒法;2为Trizol法;3为热酚法。
表1 不同提取方法获得的RNA浓度和纯度
Table 1 RNA concentration and purity obtained by different extraction methods

由表1可知,试剂盒法和Trizol法提取的RNA核酸浓度低,且A260nm/A280nm和A260nm/A230nm均<2.0,这说明酵母菌细胞壁较厚,直接用裂解液处理不容易破坏酵母菌的细胞壁,从而无法释放细胞内容物,需要借助外力来辅助破壁,提高酵母菌总RNA的提取效率。
由图1可知,泳道1和泳道2中没有出现条带。采用热酚法提取的RNA浓度很高,A260nm/A280nm和A260nm/A230nm均在2.0左右,说明RNA中很少有蛋白质、盐类等杂质的污染。电泳图显示泳道3有两条明显的条带,条带美观且清晰,没有明显的小分子弥散带,且28S rRNA和18S rRNA条带亮度接近2∶1。结果表明,热酚法是一种适用于酵母菌RNA提取的方法。
2.2 酵母破壁酶对于酵母总RNA提取结果的影响
2.2.1 试剂盒法
取不同菌体量的酿酒酵母培养液,按1.3.4所述的试剂盒法提取总RNA,并进行浓度、纯度和电泳分析,结果见分别见表2和图2。
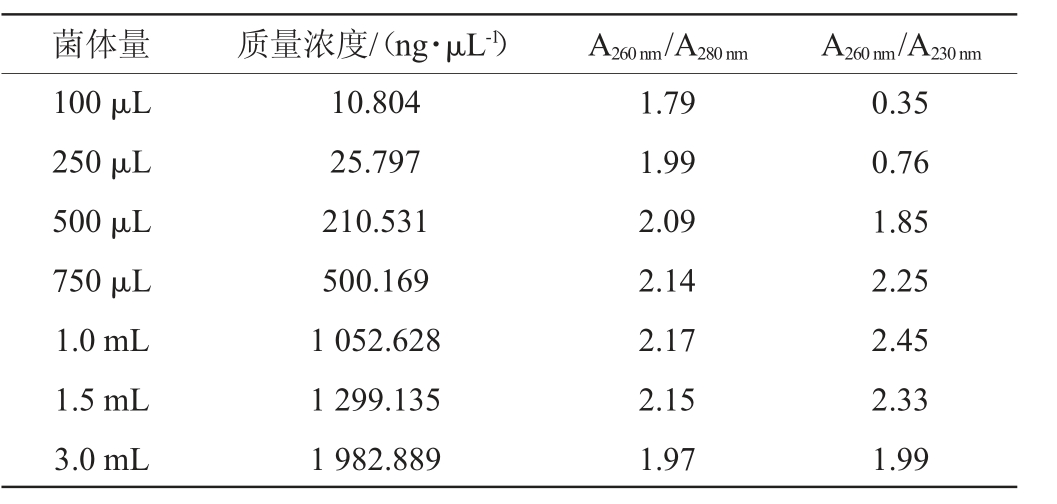
由表2可知,菌体量≥750 μL时得到的核酸质量浓度较高均在500 ng/μL以上,A260nm/A280nm在2.0左右的范围,说明RNA中蛋白质污染小,A260nm/A230nm在2.0左右的范围,说明RNA的纯度较高,盐类的污染较小。
表2 破壁酶辅助试剂盒法获得的RNA浓度和纯度
Table 2 Concentration and purity of RNA obtained by lyticase assisted with kit method
由图2可知,泳道4、5、6、7有两条较为明显的条带,但也有明显的小片段RNA的弥散带。菌体量≤500 μL时得到的核酸浓度较低,A260nm/A230nm过小,杂质污染严重,导致泳道1、2、3没有任何可见的条带。
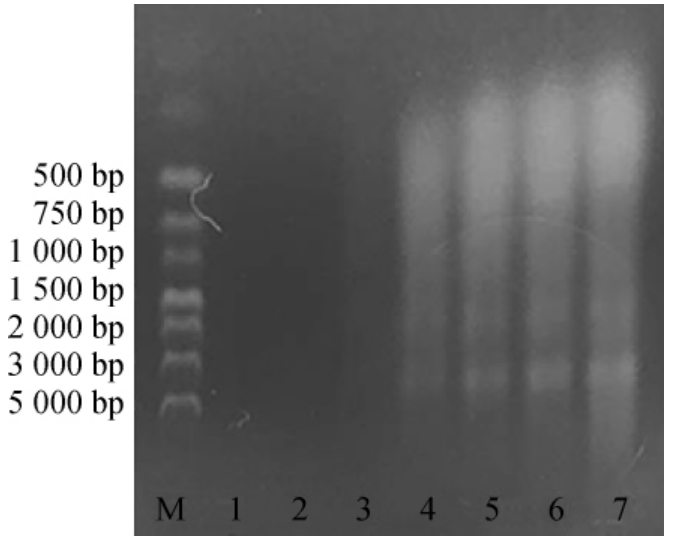
图2 破壁酶辅助试剂盒法提取酵母总RNA电泳图
Fig.2 Electrophoretogram of total RNA extracted from yeast by lyticase assisted with kit method
M为Marker;泳道1~7:菌体使用量分别为100 μL,250 μL,500 μL,750 μL,1.0 mL,1.5 mL,3.0 mL。
结果表明,加入酵母破壁酶后利用试剂盒法可以破除酵母菌的细胞壁,菌体量≥750 μL的提取效果较好。原因可能是由于菌体量过少导致酵母释放出的RNA少,提取效果不佳。
2.2.2 Trizol法
取不同菌体量的酿酒酵母培养液,按1.3.4所述的Trizol法提取总RNA,并进行浓度、纯度和电泳分析,结果分别见表3和图3。
由表3可知,菌体量在750 μL时得到的核酸质量浓度较高为1 056.967 ng/μL,A260nm/A280nm为2.07,说明RNA中蛋白质污染小。由图3可知,泳道4中有较亮的28S rRNA和18S rRNA条带,并伴有轻微的降解。菌体量>750 μL之后,核酸浓度较高,但在电泳图中对应的泳道5、6、7中的RNA降解严重,说明酵母破壁酶虽然可以有效的破坏酵母细胞壁,提高RNA的提取效率,但是菌体量过大,所释放出的大量胞内物也会影响RNA的提取质量。
表3 破壁酶辅助Trizol法获得的RNA浓度和纯度
Table 3 Concentration and purity of RNA obtained by lyticase assisted with Trizol method
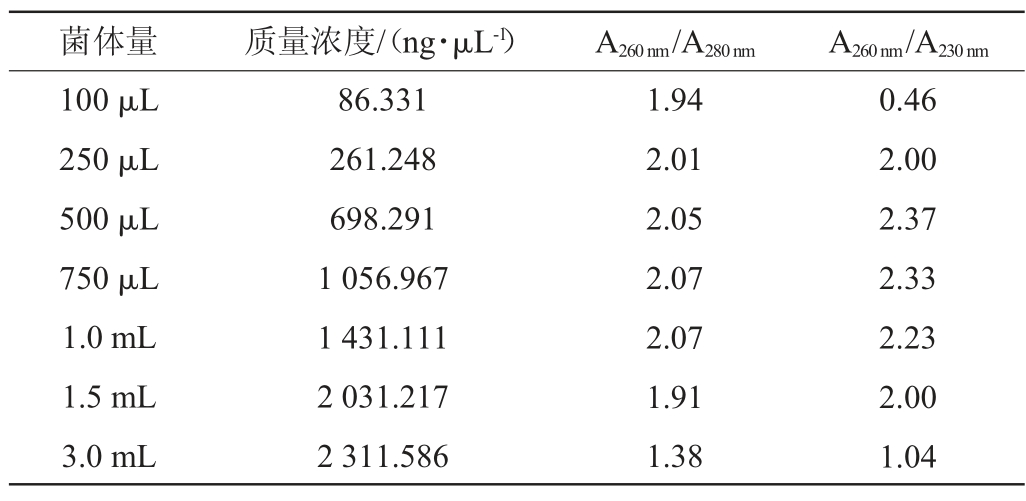
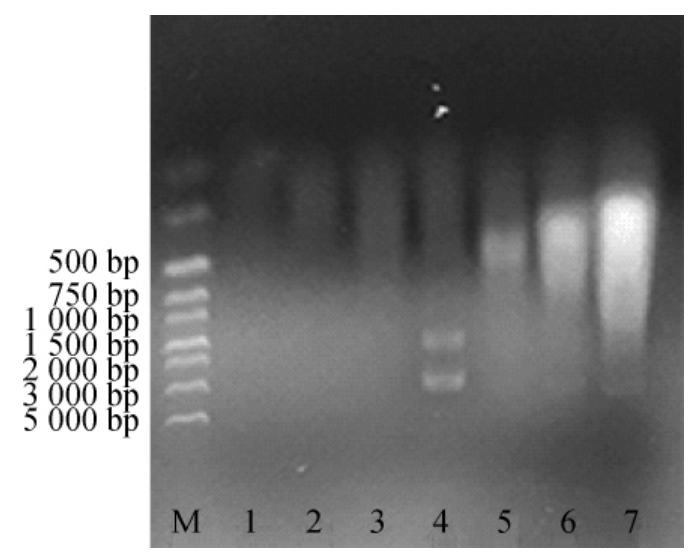
图3 破壁酶辅助Trizol法提取酵母总RNA
Fig.3 Electrophoretogram of total RNA extracted from yeast by lyticase assisted with Trizol mrthod
M为Marker;泳道1~7:菌体使用量分别为100 μL,250 μL,500 μL,
750 μL,1.0 mL,1.5 mL,3.0 mL。
2.2.3 热酚法
取不同菌体量的酿酒酵母培养液,按1.3.4所述的热酚法提取总RNA,并进行浓度、纯度和电泳分析,结果分别见表4和图4。
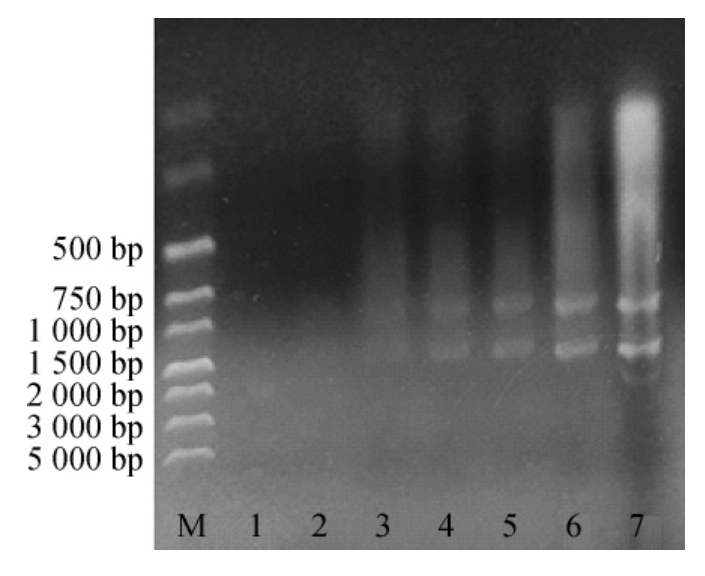
图4 破壁酶辅助热酚法提取酵母总RNA电泳图
Fig.4 Electrophoretogram of total RNA extracted from yeast by lyticase assisted with hot-phenol method
M为Marker;泳道1~7:菌体使用量分别为100 μL,250 μL,500 μL,750 μL,1.0 mL,1.5 mL,3.0 mL。
表4 破壁酶辅助热酚法获得的RNA浓度和纯度
Table 4 Concentration and purity of RNA obtained by lyticase assisted with hot-phenol method
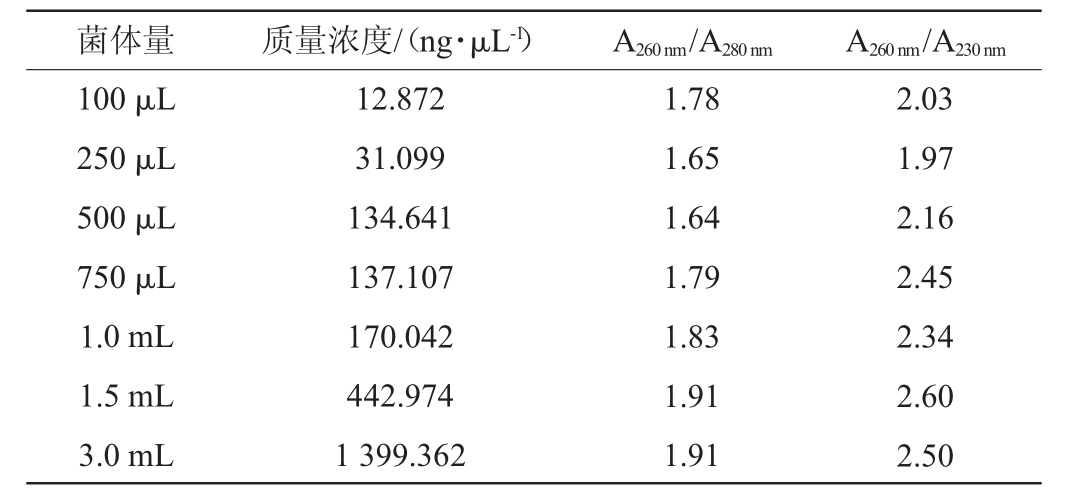
由表4可知,除了3.0 mL菌体量,其余菌体量的核酸浓度均不高,在500 ng/μL以下;不同菌体量下测得的RNA中A260nm/A280nm均在2.0以下,说明RNA中有蛋白质污染。
由图4也验证了这种观点,泳道4、5、6、7都出现了28S rRNA和18S rRNA条带,但仍有降解现象,其中泳道6、7降解较严重,泳道3依稀可以看到两条条带,但降解比较严重,泳道1、2 没有出现任何条带。结果表明,加入酵母破壁酶后利用热酚法提取酵母总RNA可获得较好的效果,但不如不添加破壁酶直接使用热酚法提取。
3 讨论
本研究比较了3种常用的总RNA提取方法,结果表明,用热酚法提取酿酒酵母总RNA的效果较好,RNA完整性高,可能原因是用RNA提取酚进行抽提后,再使用氯仿进行再次的抽提,使酵母细胞壁在能很好的被破碎的同时还能使RNA分离的更彻底。张琰等[17]认为用改良热酸性酚法是提取白色念珠菌早期生物膜RNA的理想方法。本研究中,在加酶条件下使用热酚法提取得到的RNA浓度和纯度都很低,究其原因,可能是在加酶后的温浴过程中,细胞内容物已经释放,导致RNA酶水解RNA,从而影响RNA的提取质量。
本研究尝试了用市售普通总RNA提取试剂盒提取酿酒酵母总RNA,没有得到理想的结果。试剂盒的说明书一般指出本产品适合提取植物组织、动物组织、悬浮细胞、细菌、酵母细胞的总RNA。但事实上直接使用试剂盒提取酵母总RNA的效果并不好,需要一些辅助破壁的方法[18-19]配合使用来提高RNA的提取效果。龙燕等[20]使用溶菌酶搭配专门的酵母RNA提取试剂盒可以提取到高质量的热带假丝酵母总RNA。本课题组也曾使用TaKaRa酵母菌专门的总RNA提取预处理试剂配合试剂盒提取酵母总RNA,也能得到高质量的RNA,不足之处是费用偏高。本研究加入酵母破壁酶后,虽然核酸浓度大大增加,但只有在菌体量大的情况下才有28S rRNA和18S rRNA条带,且条带出现降解,可能是由于使用酶进行破壁会延长RNA的提取时间,从而导致后续的提取效果不佳。
Trizol法是一种常用的总RNA提取方法[21],但本研究发现此方法也不适合直接用于提取酿酒酵母总RNA,也需要配合一些辅助破壁的方法来提高提取效果。潘琤等[22]通过液氮研磨改进Trizol法提取的白色念珠菌总RNA质量高,完整性优于Trizol法和超声粉碎法。本研究采用的是酵母破壁酶溶液进行的破壁,用Trizol法只有在750 μL菌体量下才能提取到RNA,但并未提取到高质量的RNA,猜测酶解法破壁虽然条件比较温和,但受温度、处理时间、pH等条件的影响,从而对RNA的抽提产生影响,因此,要想获得此方法下完整性高的RNA,还需要对酶解条件进行更加深入的探索。
4 结论
研究表明,普通的总RNA提取试剂盒和Trizol法不适合直接用于酿酒酵母总RNA的提取,但通过添加酵母破壁酶,可以提高提取效果。采用热酚法提取酿酒酵母总RNA,菌体量为750 μL时得到的RNA质量浓度为1 759.602 ng/μL,A260nm/A280nm为2.06,A260nm/A230nm为2.27,达到后续分子生物学实验的要求。该方法不用加酵母破壁酶,减少了操作时间,且具有操作简单、成本低、高质、高效等优点,有较高的使用价值。
[1]HALL M N,LINDER P.The early days of yeast genetics[J].Bioessays,1994,16(11):857-863.
[2]张明芳.啤酒酵母细胞壁环境压力应答机制研究进展[J].生物工程学报,2019,35(7):1214-1221.
[3]MOLON M,WOZNICKA O,ZEBROWSKI J.Cell wall biosynthesis impairment affects the budding lifespan of the Saccharomyces cerevisiae yeast[J].Biogerontology,2018,19:67-79.
[4]QUEIROZ M G,ELSZTEIN C,MORAIS M.The effects of the Ncw2 protein of Saccharomyces cerevisiae on the positioning of chitin in response to cell wall damage[J]. Anton Leeuw,2020,113:265-277.
[5]GARCÍA R,BOTET J,RODRÍGUEZ-PEÑA J M,et al.Genomic profiling of fungal cell wall-interfering compounds:identification of a common genesignature[J].BMC Genomics,2015,16:683-102.
[6]TONI L S,GARCIA A M,JEFFREY D A,et al.Optimization of phenolchloroform RNA extraction[J].Methodsx,2018,30(5):599-608.
[7]SASANO Y,KARIYA T,USUGI S,et al.Molecular breeding of Saccharomyces cerevisiae with high RNA content by harnessing essential ribosomal RNA transcription regulator[J].AMB Express,2017,7:32-42.
[8]VILLA-RODRIGUEZ E,IBARRA-GAMEZ C,SANTOS-VILLALOBOS S.Extraction of high-quality RNA from Bacillus subtilis with a lysozyme pretreatment followed by the Trizol method[J].J Microbiol Meth,2018,147:14-16.
[9]冷秋思,屈燕,刘伟,等.绿绒蒿属植物不同RNA 提取方式的比较分析[J].分子植物育种印刷版,2019,17(14):4643-4647.
[10]吴小英,陈玉容,侯杰,等.南药益智果实的总RNA 提取方法比较研究[J].时珍国医国药,2018,271(3):766-768.
[11]庞宏光,许建锋,张江红,等.杜梨不同组织总RNA 提取方法比较及质量分析[J].果树学报,2018,35(S1):68-72.
[12]WEI Z M,LI S G,LIU M,et al.A simple and high quality method for isolation and extraction of total RNA of Pholiota adipose[J].Asian Agr Res,2018,10(1):44-48.
[13]黄国文,管天球,赵雨云,等.油茶叶片总RNA 提取的改良Trizol 试剂法及比较[J].分子植物育种,2018,16(18):5920-5926.
[14]SHEDLOVSKIY D,SHCHERBIK N,PESTOV D G.One-step hot formamide extraction of RNA from Saccharomyces cerevisiae[J].RNA Biology,2017,14(12):1722-1726.
[15]易弋,容元平,程谦伟,等.不同破壁方法提取酵母菌总RNA 的比较[J].食品科学,2011,32(11):161-164.
[16]商安全,魏军,王微微,等.改良破壁法提取白假丝酵母菌总RNA 的应用评价[J].临床检验杂志,2016,34(7):552-554.
[17]张琰,马鸣,虞丽华,等.改良热酸酚法提取白色念珠菌早期生物膜总RNA 的研究[J].口腔生物医学,2010,1(2):15-17.
[18]相晨曦,王安利,廖绍安,等.不同破壁方法获取海洋毕赤酵母提取物及其应用[J].华南师范大学学报,2018,50(6):66-73.
[19]吕天琪,杜超,曹小彦,等.锁掷酵母破壁技术的研究[J].中国酿造,2017,36(12):88-91.
[20]龙燕,杨升.几种提取热带假丝酵母总RNA 方法比较[J].实验技术与管理,2012,29(9):54-56.
[21]李照熙,杨瑞,靳树胜,等.影响Trizol 提取RNA 质量的因素分析[J].新乡医学院学报,2016,33(8):653-656.
[22]潘琤,魏昕,刘卫红.改进Trizol 法提取白色念珠菌总RNA 初探[J].临床口腔医学杂志,2007,23(9):531-533.