余甘子(Phyllanthus emblica L.)别名喉甘子、庵罗果、牛甘果等,属大戟科叶下珠属植物,广泛分布于我国西南等地区,其果实入口微涩,回味甘甜,故名余甘[1-3]。余甘子果实具有清热利咽,生津止渴,润肺化痰等功能,主要用于治疗感冒发热、咳嗽、咽痛、白喉、烦热口干[4-6],降糖、调节血脂代谢等作用显著[7]。余甘子是联合国卫生组织指定为全世界推广种植的3种保健植物之一,且在17个国家的传统药物体系中使用[8],为药食两用植物。
目前,余甘子植物的研究主要集中在余甘子果实、叶中总黄酮、多酚物质的提取[9-10];余甘子抗氧化、护肝、调节血脂及抗癌等药理作用的研究[11-13]。研究表明,余甘子中主要的生物活性成分之一是水解单宁[14],余甘子多酚具有抗氧化、抑菌、调节免疫、降血糖、抗病毒和肿瘤等作用[15-18]。但关于余甘子果核有效成分的提取工艺及抗氧化活性研究鲜见报道。
余甘子果核占干果质量的40%左右,在临床应用中并未严格区分余甘子果肉和余甘子,2020年版《中国药典》也仅收载了余甘子,并未对其果肉有所规定[15]。但是在产地加工时,部分余甘子会经过去核的方法净制后再流通进入市场或应用于临床。为了更好地开发和完善余甘子植物的综合利用,使废弃的余甘子果核得到充分利用,减少资源浪费,试验采用超声波辅助法提取余甘子果核多酚,并通过正交试验设计优化余甘子果核多酚的提取工艺条件,并研究余甘子果核多酚对羟基自由基(·OH)及1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)自由基(DPPH·)的清除作用考察其抗氧化活性,以期为余甘子果核在食品保健和药用开发方面的应用提供依据。
1 材料与方法
1.1 材料与试剂
余甘果:2020年7月采摘于广西崇左市江州区;
单宁酸(纯度≥99%)、维生素C(vitamin C,VC)、福林酚、丙酮、DPPH等实验试剂均为国产分析纯。
1.2 仪器与设备
FW100型高速万能粉碎机:天津市泰斯特仪器有限公司;722型紫外可见分光光度计:上海舜宇恒平科学仪器有限公司;SG2200HPT型超声波清洗仪:上海冠特超声仪器有限公司;SHZ-D型电热恒温鼓风干燥箱:上海福玛实验设备有限公司。
1.3 试验方法
1.3.1 余甘子果核多酚的提取
参考文献[19]的方法,对余甘子果核进行预处理:将采摘的余甘果洗净自然晾干,人工对果实、果核进行分离,果核洗净后放置于60 ℃恒温干燥箱中烘干,粉碎,过60目筛即得余甘子果核粉末。用石油醚以1∶4料液比(g∶mL)在70 ℃油浴条件下对余甘子果核粉末进行脱脂、除色处理,回流4 h,抽滤,再放置60 ℃干燥箱中干燥,即得脱脂脱色的余甘子果核粉末原料,于常温条件下密封避光保存以备用。
称取已脱脂脱色的1.000 0 g余甘子果核粉末加入一定量丙酮溶液,于一定条件下超声辅助提取,抽滤,所得滤液用蒸馏水定容至100 mL容量瓶中,即得余甘子果核多酚提取液,待用。
1.3.2 余甘子果核多酚提取工艺优化单因素试验
以余甘子果核多酚得率为评价指标,分别考察提取剂(体积分数70%丙酮、体积分数70%乙醇、体积分数70%乙醇(1%盐酸)酸性溶液、蒸馏水)、丙酮体积分数(50%、60%、70%、80%、90%)、料液比(1∶20、1∶30、1∶40、1∶50、1∶60(g∶mL))、提取时间(10 min、20 min、30 min、40 min、50 min)、提取温度(20 ℃、30 ℃、40 ℃、50 ℃、60 ℃)对余甘子果核多酚得率的影响。
1.3.3 余甘子果核多酚提取工艺优化正交试验
在单因素试验的基础上,选取丙酮体积分数(A)、料液比(B)、提取时间(C)及提取温度(D)为4个考察因素,以余甘子果核多酚得率为评价指标,设计L9(34)正交试验优化余甘子果核多酚提取工艺。正交试验因素与水平见表1。
表1 余甘子果核多酚提取工艺优化正交试验因素与水平
Table 1 Factors and levels of orthogonal experiments for polyphenols from Phyllanthus emblica L.kernel extraction technology optimization

1.3.4 测定方法
余甘子果核多酚得率的测定:参考文献[20]的方法,配制不同浓度梯度的单宁酸标准溶液,采用福林酚显色法,显色后分别测定它们在波长760 nm处的吸光度值,以单宁酸溶液的质量浓度(x)为横坐标,吸光度值(y)为纵坐标,绘制标准曲线,拟合得回归方程:y=93.780 4x+0.079 6,R2=0.999 0。
根据单宁酸标准曲线绘制方法显色后测定余甘子果核多酚提取液在波长760 nm处的吸光度值。用标准曲线方程计算相关浓度,根据下式计算余甘子果核多酚的得率:
式中:Y为余甘子果核多酚的得率,%;WR为脱脂原料的质量,g;C为通过标准曲线方程求出的质量浓度,mg/mL;V1为提取液的总体积,mL;V2为测定时量取的提取液体积,mL。
余甘子果核多酚抗氧化性的测定:在正交试验优化得到的最佳工艺条件下提取余甘子果核多酚,以抗坏血酸为阳性对照,参照文献[21-22]的方法,分别测定余甘子果核多酚对·OH及DPPH·的清除能力,以对应清除率为参考指标评价余甘子果核中多酚的抗氧化活性。
1.3.5 数据处理
所有实验重复3次取均值,采用Origin8.5软件进行数据处理和图片绘制。
2 结果与分析
2.1 单因素试验结果
2.1.1 提取溶剂对余甘子果核多酚得率的影响
如图1所示,不同提取剂提取余甘子果核多酚对应得率由大到小顺序为:70%丙酮>70%乙醇(1%盐酸)>70%乙醇>蒸馏水,以体积分数70%的丙酮作为提取剂时提取得到的余甘子果核多酚得率最大,为4.58%。原因是丙酮极性与多酚物质相近,相似相溶原理使得其提取率相对较高,因此,确定丙酮溶液为余甘子果核多酚的最佳提取溶剂。

图1 提取溶剂对余甘子果核多酚得率的影响
Fig.1 Effect of extracting agent on extraction rate of polyphenols from Phyllanthus emblica L.kernel
2.1.2 丙酮体积分数对余甘子果核多酚得率的影响
如图2所示,余甘子果核多酚的提取率随着丙酮体积分数的逐渐增大先缓慢升高后显著降低。当丙酮体积分数为80%时对应得率最大为5.60%,继续增大丙酮体积分数,则脂溶性物质溶出增多,使得多酚的得率下降[20]。因此,选取的最佳丙酮体积分数为80%。
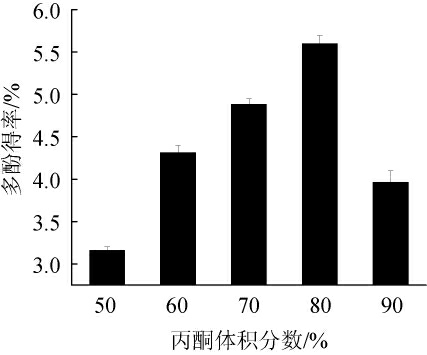
图2 丙酮体积分数对余甘子果核多酚得率的影响
Fig.2 Effect of acetone volume fraction on extraction rate of polyphenols from Phyllanthus emblica L.kernel
2.1.3 料液比对余甘子果核多酚得率的影响
如图3所示,随着料液比的变化余甘子果核多酚得率先升高后缓慢降低,当料液比为1∶30 g/mL对应的多酚得率最大为5.90%,原因可能是适当增大提取剂用量可利于余甘子果核多酚的溶出,但提取剂用量过大会导致其他杂质溶出也增多,从而导致多酚得率下降[23],且不利于后续浓缩处理。因此,选取的最佳料液比为1∶30(g∶mL)。
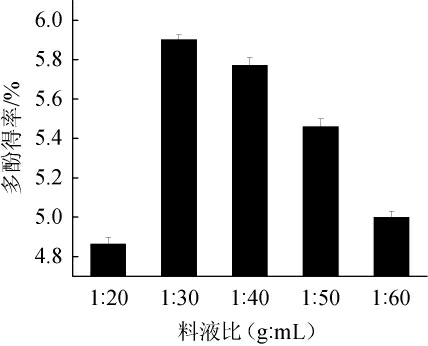
图3 料液比对余甘子果核多酚得率的影响
Fig.3 Effect of solid and liquid ratio on extraction rate of polyphenols from Phyllanthus emblica L.kernel
2.1.4 提取时间对余甘子果核多酚得率的影响
余甘子果核多酚得率随着提取时间的增加先升高后降低,超声提取20 min对应的余甘子果核多酚得率最大6.19%,此时继续增加提取时间则部分多酚物质被氧化耗损或者被分解结构被破坏,导致其得率降低[24]。因此,选取的最佳提取时间为20 min。

图4 提取时间对余甘子果核多酚得率的影响
Fig.4 Effect of extraction time on extraction rate of polyphenols from Phyllanthus emblica L.kernel
2.2.5 提取温度对余甘子果核多酚得率的影响
如图5所示,随着提取温度的升高余甘子果核多酚得率先升高后降低,在50 ℃时多酚得率达到最高(6.98%)。原因是低温不利于酚类物质的溶出,但温度较高会使部分多酚氧化和降解,导致多酚得率降低[25]。因此,选取的最佳提取温度为50 ℃。
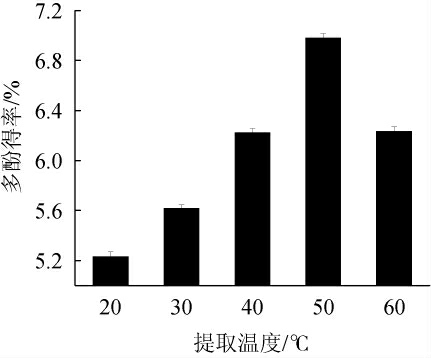
图5 提取温度对余甘子果核多酚得率的影响
Fig.5 Effect of extraction temperature on extraction rate of polyphenols from Phyllanthus emblica L.kernel
2.3 正交试验结果
以单因素试验结果为基准,按表1的因素水平L9(34)正交试验,优化余甘子果核多酚提取工艺,试验结果见表2,方差分析结果见表3。
由表2可知,影响余甘子果核多酚得率的因素主次顺序为D(提取温度)>A(丙酮体积分数)>B(料液比)>C(提取时间),试验得到的余甘子果核多酚最佳提取工艺条件组合为A1B3C3D1,即丙酮体积分数70%、料液比1∶40(g∶mL)、提取温度40 ℃及提取时间30 min。按上述的最佳提取工艺条件进行3次平行试验,余甘子果核多酚得率的平均值为7.37%。由表3可知,料液比和提取温度对结果影响显著(P<0.05)。
表2 余甘子果核多酚提取工艺优化正交试验结果与分析
Table 2 Results and analysis of orthogonal experiments for polyphenols from Phyllanthus emblica L.kernel extraction technology optimization

表3 正交试验结果方差分析
Table 3 Variance analysis of orthogonal experiments results
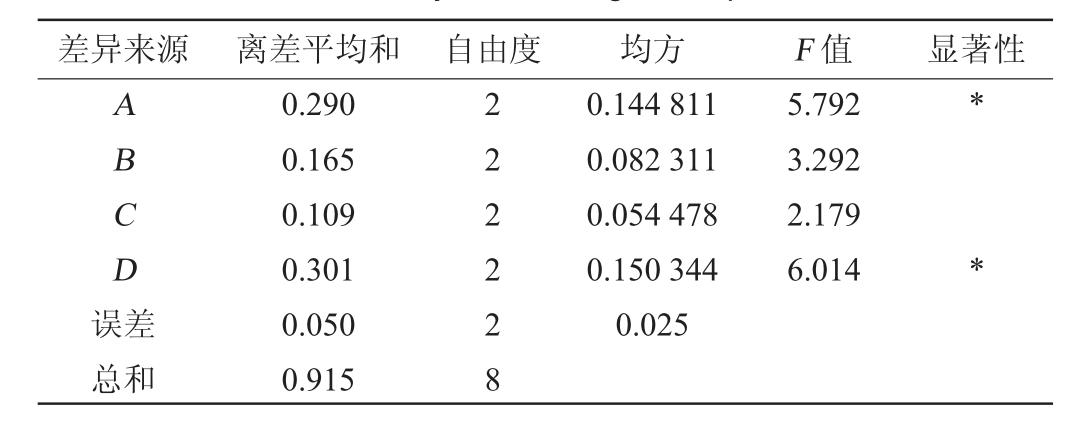
注:F0.05(2,8)=4.46,F0.01(2,8)=8.86;“*”表示因素对结果影响显著
(P<0.05),“**”表示因素对结果影响极显著(P<0.01)。
2.4 余甘子果核多酚的抗氧化性
2.4.1 余甘子果核多酚清除·OH的活性
由图6可知,余甘子果核多酚对·OH的清除效果与样品浓度呈正相关。余甘子果核多酚质量浓度由1.0 mg/mL增大至3.0 mg/mL时,则对·OH的清除率由46.06%增大至84.44%,略小于同质量浓度的VC对·OH的清除率,对应的半抑制浓度(half inhibitory concentration,IC50)值(清除率达50%时所需的浓度)为1.2 mg/mL,表明余甘子果核多酚清除·OH效果较显著,具有良好的抗氧化性。
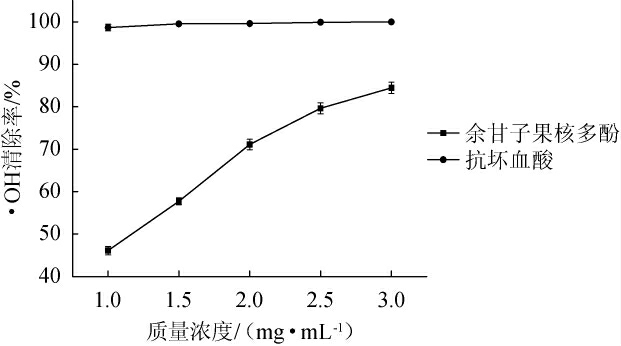
图6 余甘子果核多酚对·OH的清除效果
Fig.6 Scavenging effect of polyphenols from Phyllanthus emblica L.kerenl on·OH
2.4.2 余甘子果核多酚清除DPPH·的活性
由图7所示,随着余甘子果核多酚浓度的不断增大,对DPPH·的清除作用也逐渐增强,清除效果与多酚样品浓度呈正相关。当多酚质量浓度为0.05 mg/mL时,对DPPH·的清除率为80.53%(同浓度VC对DPPH·的清除率为97.07%),表明余甘子果核多酚具有一定的抗氧化性。
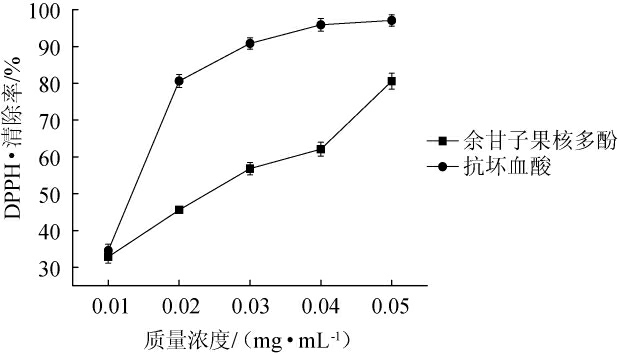
图7 余甘子果核多酚对DPPH·的清除效果
Fig.7 Scavenging effect of polyphenols from Phyllanthus emblica L.kernel on DPPH·
3 结论
经正交试验设计优化得到超声波辅助法提取余甘子果核多酚的最佳提取工艺条件为丙酮70%、1∶40(g∶mL)料液比、提取温度40 ℃及提取时间30 min,对应多酚的得率为7.37%。
余甘子果核多酚的浓度越大,清除·OH及DPPH·的效果越显著,清除能力与多酚样品浓度呈正相关的量效关系,且对·OH的清除作用较强。当余甘子果核多酚质量浓度为3.0 mg/mL时,对·OH的清除率达84.44%,IC50值为1.2 mg/mL。结果表明余甘子果核多酚具有良好的抗氧化活性,可开发作为天然抗氧化剂应用于食品、药品等领域。后续可采用大孔吸附树脂对余甘子果核多酚物质做进一步的分离纯化,并深入探究余甘子果核多酚的抗氧化活性与各有效成分之间的量效关系,为余甘子果核的合理开发和深加工提供依据。
[1]国家药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2020:186-187.
[2]WU J J,XU Y B,ZHU B,et al.Characterization of an arabinogalactan from the fruit hulls of Ficus pumila Linn.and its immunomodulatory effect[J].J Funct Food,2020,73:104091.
[3]黄浩洲,冉飞,谭庆刍,等.药食同源品种余甘子综合开发利用策略与思路[J].中国中药杂志,2021,46(5):1034-1042.
[4]LU C C,YANG S H,HSIA S M,et al.Inhibitory effects of Phyllanthus emblica L.on hepatic steatosis and liver fibrosis in vitro[J].J Funct Food,2016,20:20-30.
[5]杨冰鑫,刘晓丽.余甘子总多酚的提取及其抗氧化活性研究[J].食品工业科技,2019,40(16):151-155,162.
[6]唐仕荣,宋慧,陈尚龙,等.不同方法提取余甘子多酚的抗氧化活性及其指纹图谱分析[J].中国食品添加剂,2018(8):90-97.
[7]陈文雅,钟振国,张雯艳.余甘子叶的化学成分与药理作用研究概况[J].广西中医药大学学报,2016,19(3):82-83,93.
[8]杜丽娟,苏秀芳,黄成银.余甘子叶总黄酮的超声波法提取工艺优化及其抗氧化能力研究[J].食品与机械,2020,36(3):185-189,193.
[9]李洁,王沂雯,郑涵予,等.余甘子多酚微波-热水浸提工艺的优化及其pH 稳定性[J].江苏农业学报,2020,36(3):733-742.
[10]赵春草,符晓晖,杨清云,等.余甘子总酚提取纯化工艺的研究[J].中成药,2020,42(6):1410-1415.
[11] YADAV S S,SING M K,SINGH P K,et al.Traditional knowledge to clinical trials:A review on therapeutic actions of Emblica officinalis[J].Biomed Pharmacother,2017,93:1292-1302.
[12] ZHANG N,HU Y,DING C C,et al.Salvianolic acid B protects against chronic alcoholic liver injury via SIRT1-mediated inhibition of CRP and ChREBP in rats[J].Toxicol Lett,2017,267:1-10.
[13]吴玲芳,张家莹,李师,等.藏药余甘子抗肿瘤作用进展[J].世界科学技术-中医药现代化专题讨论,2016,18(7):1177-1181.
[14]YANG B R,LIU P Z.Composition and biological activities of hydrolyzabletannins of fruits of Phyllanthus emblica[J].J Agric Food Chem,2014,62(3):529-541.
[15]罗传红,黄胜杰,胡琪琪,等.去核对余甘子药材质量的影响[J].中国实验方剂学杂志,2021,27(9):147-156.
[16] LUO W,ZHAO M M,YANG B,et al.Identification of bioactive compounds in Phyllenthus emblica L.fruit and their free radical scavenging activities[J].Food Chem,2009,114(2):499-504.
[17] DHALE D A,MOGLE U P.Phytochemical screening and antibacterial activity of Phyllanthus emblica(L.)[J].Sci Res Rep,2011,1(3):138-142.
[18] ZHAO T J,SUN Q,MARQUES M,et al.Anticancer properties of Phyllanthus emblica (Indian gooseberry)[J].Oxid Med Cell Longev,2015,2015:950890.
[19]许建本,苏秀芳,莫耀芳.超声波辅助法提取假苹婆树叶总黄酮及其清除羟自由基能力[J].食品工业科技,2018,39(23):199-202,209.
[20]郑燕菲,张强,蓝亮美,等.单性木兰枝多酚提取工艺及抗氧化性研究[J].食品与机械,2020,36(5):175-181.
[21]吕亭亭,杨志华,陶娟,等.泡桐花总黄酮的提取工艺优化及抗氧化活性[J].中国酿造,2021,40(1):197-202.
[22]田明杰,谭宏渊,叶帆宇,等.福白菊总黄酮的微波辅助提取工艺优化及其抗氧化活性研究[J].中国酿造,2020,39(1):170-174.
[23]李利华.正交实验法优选花椒多酚的超声波辅助提取工艺[J].中国调味品,2018,43(4):1-3,27.
[24]胡会刚,赵巧丽.菠萝皮渣多酚的提取分离及其抗氧化活性评价[J].食品科技,2020,45(1):286-293.
[25]许海棠,田程飘,赵彦芝,等.百香果叶总酚的提取工艺优化、抗氧化活性及其抑制α-葡萄糖苷酶活性[J].食品工业科技,2019,40(20):223-227,236.