我国是农业大国,是生产和使用农药最多的国家,随着现代农业生产中农药的广泛使用,大量农药经挥发、富集等方式残留于环境中。在20世纪50~80年代有机氯农药(organochlorine pesticides,OCPs)由于其防治农作物病虫害效果好,被大量使用[1-3]。OCPs由于氯苯结构较稳定,在环境中难于被降解,并且能够在动物和人体内蓄积从而导致各类神经、免疫、生殖以及遗传性疾病[4,5],虽然我国已对其禁用多年,但近年来世界各地仍然在土壤,水,以及人类的食物当中都能检测到痕量的农药残留及其代谢产物[6]。
白酒是以高粱、小麦等粮食为主要原料经发酵、蒸馏而成[7],虽然经过发酵、蒸馏过程,减少了农药的残留量,但仍有残留在酒中的风险,同时白酒成分中大部分是乙醇和水[8],我国饮用水卫生标准[9]中对六六六、滴滴滴、七氯、林丹等有机氯农残进行了相应的限量标准,水中的有机氯农药残留对白酒的食品安全也存在潜在的风险。我国目前尚未有白酒中农药残留限量的相关规定,因此,有必要建立一种快速准确的检测方法,为白酒中有机氯农残的风险评估提供技术支持。
目前,国内外对有机氯农残的检测的方法有很多,主要有气相色谱法(gas chromatography,GC)[1,10-11]、气相色谱质谱法(gas chromatography mass spectrometry,GC-MS)[12]和气相色谱-三重四级杆质谱法(gas chromatography-triple quadruple mass spectrometry,GC-MS/MS)[13-14]。针对白酒中农残的检测方法的报道却较少,文献报道的分析方法多采用固相萃取法(solid-phase extraction,SPE)[15-16],分散固相萃取(dispersive solid phase extraction,D-SPE)[17]或者凝胶渗透色谱(gel permeation chromatography,GPC)净化法[18],由于白酒中的有机氯农药含量低,基质本底复杂,且分析前常需要较复杂的前处理方法净化,再经浓缩后上样分析,操作繁琐耗时,灵活性不强,且前处理设备和装置价格也相对较高。本研究尝试采用直接进样法来测定白酒中的有机氯农残,重点考察了色谱柱对直接进样的耐受力[19],并通过GC-MS/MS对仪器参数进行优化,采用多反应监测(multiple reaction monitoring,MRM)扫描模式对白酒样品进行分析,避免了使用单离子监测(single ion monitoring,SIM)扫描模式引起的相同分子质量的不同分子结构的干扰,以期建立一种直接进样测定白酒中的有机氯农药残留的分析方法。
1 材料与方法
1.1 材料与试剂
20余种白酒样品(包括浓香型、酱香型、清香型、米香型等):市售。
有机氯农药标准品:α-六六六、β-六六六、γ-六六六、δ-六六六、五氯硝基苯、七氯、艾氏剂、四氯苯酞、狄氏剂、异狄氏剂、双对氯苯基三氯乙烷(dichlorodiphenyltrichloroethane,DDT)(P,P'-滴滴涕)、O,P'-滴滴涕(O,P'-DDT)、1,1-双(对氯苯基)-2,2-二氯乙烯(1,1-bis(chlorophenyl)-2,2-dichloroethylene,DDE)(P,P'-滴滴伊)、1,1-二氯-2,2-双(对氯苯基)乙烷(1,1-dichloro-2,2-bis(p-chlorophenyl)ethane,DDD)(P,P'-滴滴滴);质量浓度为100 μg/mL的单标准溶液:中国标准物质中心;乙酸乙酯(色谱纯):赛默飞世尔科技有限公司。
1.2 仪器与设备
7890A-7000C气相色谱质谱联用仪、电子电离(electron ionization,EI)源:安捷伦科技有限公司。
1.3 方法
1.3.1 有机氯农残混合标液的配制
准确量取质量浓度为100 μg/mL的14种单标准溶液各100 μL于10 mL的棕色容量瓶中,加入8 600 μL乙酸乙酯,混匀后得质量浓度为1 μg/mL的混合标准储备液;混合标准工作液的配制:采用逐级稀释法配制不同浓度的有机氯农残混合标准工作液,用空白基质的白酒将有机氯农残混标储备液稀释成1 μg/L、2 μg/L、4 μg/L、7 μg/L、10 μg/L的混合标准工作液。
1.3.2 气相色谱条件
色谱柱:HP-5MS毛细管柱(30 m×250 μm×0.25 μm);载气为氦气(He)(纯度≥99.999%),流速1 mL/min;进样方式:脉冲不分流进样;进样量:1 μL;柱温:起始温度40 ℃,保持1 min,以30 ℃/min升至180 ℃,保持0.5 min,以2 ℃/min升至200 ℃,保持0.5 min,再以5 ℃/min升至280 ℃保持1 min;进样口温度:250 ℃;辅助加热温度280 ℃。
1.3.3 质谱条件
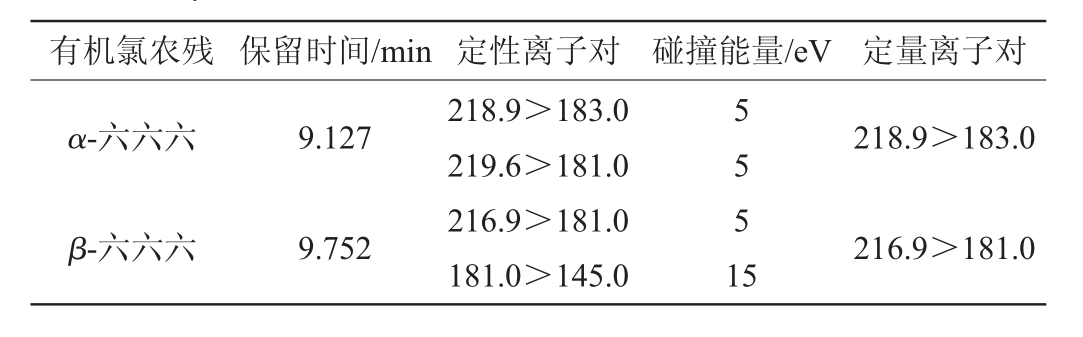
采用电子电离(EI)源多反应监测(MRM)模式,溶剂延迟:5 min,离子源温度:230 ℃,四级杆1温度:150 ℃,四级杆2温度:150 ℃。具体有机氯农药保留时间,离子参数及碰撞能量见表1。
表1 14种有机氯农药的保留时间及离子参数
Table 1 Retention time and ionic parameters of 14 organochlorine pesticides
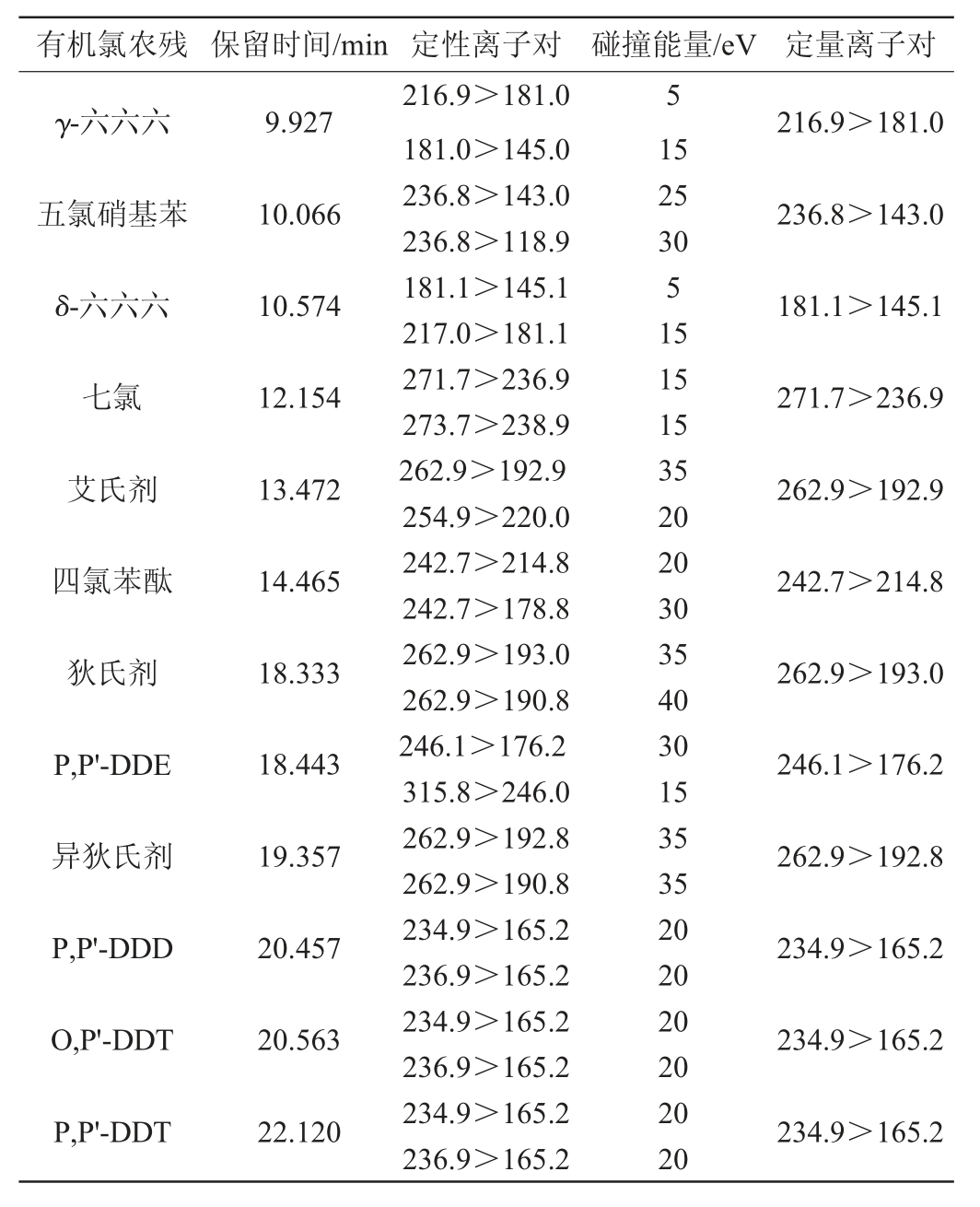
续表
1.3.4 数据处理
本方法采用外标法定量,按梯度添加一定量的有机氯农残的标准品(对照品)于空白溶剂中制成对照样品,与未知试样平行地进行样品处理并检测。不同浓度的标准品进样,以峰面积为值绘制成标准曲线,从而推算出未知试样中被测组分浓度进行定量。
2 结果与分析
2.1 有机氯标样色谱图
有机氯标样MRM色谱图见图1,结果表明,各相邻色谱峰分离情况良好。

图1 有机氯标样多反应监测色谱图
Fig.1 Multiple reaction monitoring chromatogram of organochlorine standard sample
1:α-六六六;2:β-六六六;3:γ-六六六;4:五氯硝基苯;5:δ-六六六;6:七氯;7:艾氏剂;8:四氯苯酞;9:狄氏剂;10:P,P'-DDE;11:异狄氏剂;12:P,P'-DDD;13:O,P'-DDT;14:P,P'-DDT。
2.2 仪器条件优化
2.2.1 气相条件优化
有机氯农残是弱极性,高沸点的化合物(绝大多数200℃以上),研究将进样口温度设置为250 ℃便于物质汽化,因其沸点较高,出峰时间靠后,故加快了柱温箱的升温时间,以30 ℃/min升至180 ℃,这样将缩短了整个样品的出峰时间,同时白酒的成分较为复杂,多为中等极性以及强极性的物质,研究采用HP-5MS非极性色谱柱,能避免白酒中的多数复杂成分对有机氯的干扰,在第一个有机氯农残出峰时,柱温已达180 ℃,此时白酒中的大多数干扰物都已避开,因为白酒中的成分多为低沸点的化合物,只有少数沸点较高的化合物可能对直接进样方法有干扰,如肉豆蔻酸乙酯,其出峰的时间和五氯硝基苯完全重合(见图2),其可通过质谱条件进行进一步优化。
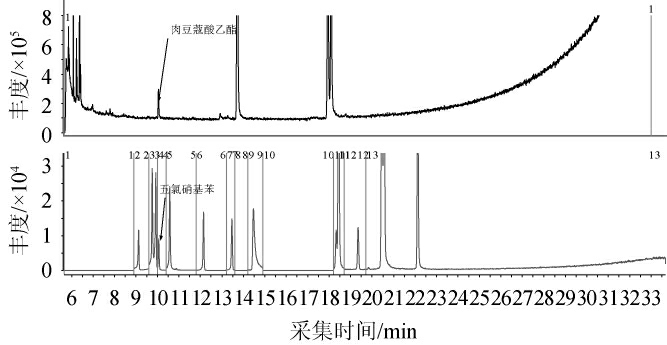
图2 空白基质SCAN图和空白基质加标多反应监测色谱图
Fig.2 SCAN of blank matrix and multiple reaction monitoring chromatogram of blank matrix adding standards
2.2.2 质谱条件优化
根据有机氯农残的特性,首先对高浓度的有机氯农残标样进行全扫描,确定了各物质的保留时间后,逐个分析其质谱图,选择响应较强,干扰较小的母离子进行子离子扫描,设置对应的电离能,在不同的电离情况下确定各个化合物响应最佳的碎片离子以及电离能量。由于直接进样,白酒中部分成分会对待测物有干扰,通过MRM的采集方法的特性,即使保留时间重合,也能根据不同物质的特征离子进行分离,实验为了得到更高的灵敏度,对质谱的增益进行了一定的调节,增益因子可以增加仪器的响应,样品浓度较低可通过增大增益因子来增强响应,对部分低响应的有机氯的增益因子进行了调节,在保证目标组分完全检测到的情况下,尽可能提高仪器的检出限,同时将各目标组分尽可能单独设置一个扫描通道,即可避开白酒中的复杂基质对农药残留的干扰,优化条件下样品经直接进样结果见图3。结果表明,14种有机氯农药均能得到较好的分离。
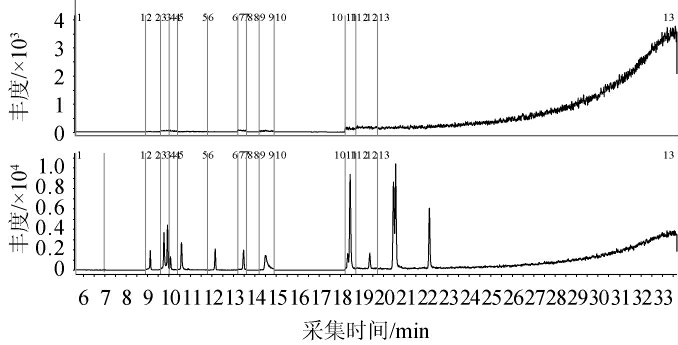
图3 空白基质与空白基质加标色谱图
Fig.3 Chromatogram of blank matrix and blank matrix adding standards
2.3 回归方程、线性范围和检出限
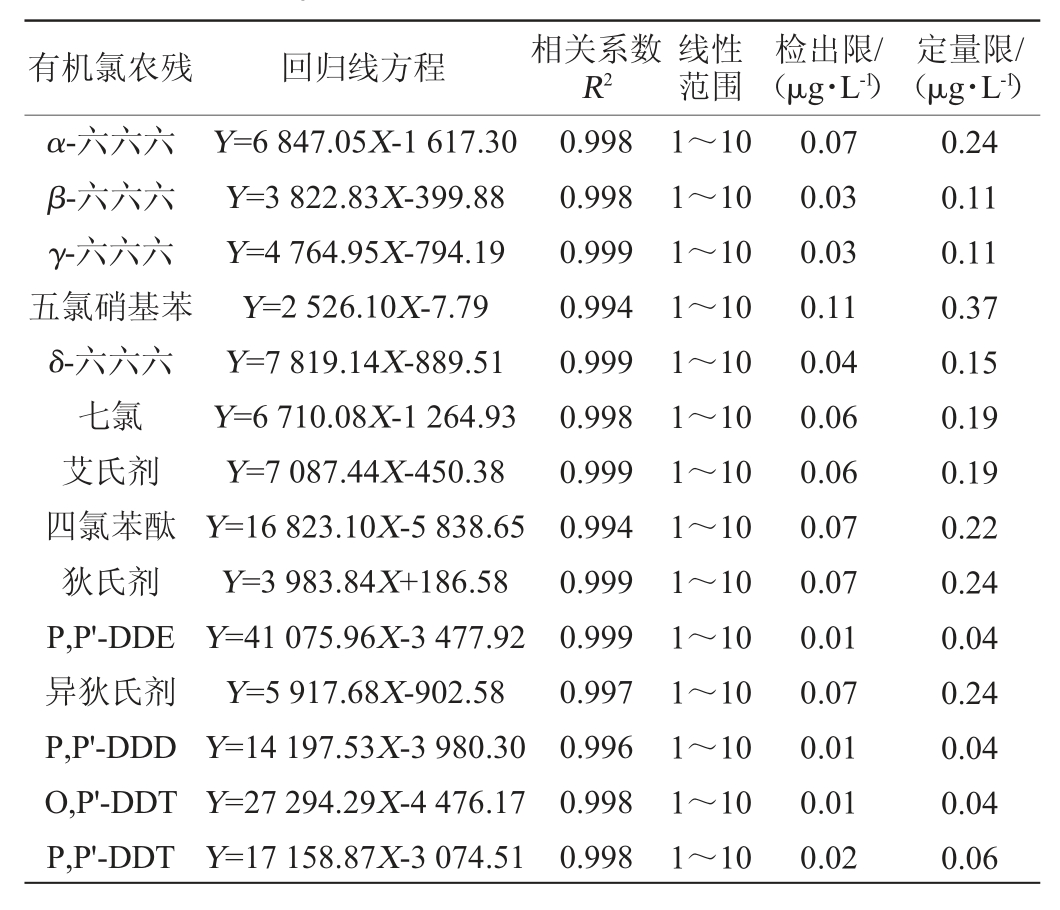
取标准系列溶液按上述条件进行进样分析,分别以每种标样的峰面积(Y)为纵坐标和质量浓度(X,μg/L)为横坐标绘制标准曲线,利用1 μg/L的添加浓度水平为依据,特征离子质量色谱峰性噪比(singnalto noise ratio,SNR)=3计算检出限(limit of detection,LOD),SNR=10计算定量限(limit of quantitation,LOQ),结果见表2。结果表明,在1~10 μg/L范围内,待测物线性良好,相关系数R2均在0.99以上。
表2 标准曲线、相关系数、线性范围及检出限和定量限
Table 2 Standard curve,correlation coefficient,linear range,detection limit and quantitation limit
2.4 方法精密度及回收率试验
分别向空白酒样中添加0.002 mg/L、0.005 mg/L和0.008 mg/L的有机氯农药混合标样,进行加标回收试验,每个浓度水平平行测定6次。利用保留时间和特征离子的丰度比定性,采用峰面积外标法定量,计算回收率及相对标准偏差,结果见表3。结果表明,在3个浓度水平上,有机氯农药的平均回收率80.88%~115.28%,相对标准偏差在2.7%~11.1%之间,符合农药多残留分析要求。
表3 14种有机氯农药的回收率及精密度试验
Table 3 Recovery and precision tests of 14 organochlorine pesticides

注:“ND”代表未检出。
2.5 前处理方法的比较
对于白酒中的农药残留检测方法,王蓉等[15]建立了白酒中8种有机氯农药残留检测的GC-MS法,该法用Florisil固相萃取柱对样品进行前处理,该法在0.05 mg/L和0.5 mg/L两个添加水平下的回收率在81.0%~106.3%之间,方法的最低检出限在0.4~1.2 μg/L之间;姜利等[18]建立了GC-MS/MS测定白酒中滴滴涕和六六六残留的分析方法,样品经旋蒸去除酒精,经二氯甲烷+丙酮(4∶1,V/V)进行萃取,有机相通过凝胶渗透色谱进行净化和浓缩,该方法的检出限为0.2~1.0 μg/L。
对比发现,固相萃取虽然对农残进行了富集,但同时其也浪费了大量的有机溶剂、时间及人工成本,小柱的成本较高,活化、洗脱的试剂对环境也造成了相应的污染,而直接进样在避免复杂基质的干扰下,减少了样品的预处理过程,操作简单、省时省力,节约成本。本研究采用直接进样测定白酒中的14种有机氯农残,该法在0.002 mg/L、0.005 mg/L和0.008 mg/L水平下进行加标回收试验有机氯农药的平均回收率80.88%~115.28%,方法的检出限为0.01~0.11 μg/L之间低于国标的食品中农药最大残留限量要求[20]。
2.6 基质效应
基质效应的存在会对目标组分的信号产生增强或者抑制效应,基质效应(ME=B/A,A为纯溶剂中农药的响应值,B为样品基质中添加的相同含量农药的响应值),比值在0.9和1.1之间,表示基质效应可以忽略,大于1.2为基质效应增强,小于0.9为基质效应减弱[21-23]。我国白酒共有12种香型,其中浓香型、酱香型、清香型、米香型为四大基本香型,独立存在于各白酒之中,其余8种香型是在这四种基本香型的基础上衍生而来[24-25],因此本方法选用了四种基本香型的白酒空白代表(即浓香型、酱香型、米香型、清香型)作为基质配制标样,同时和纯溶剂乙酸乙酯配标作对比,结果见图4。

图4 异狄氏剂在不同香型白酒中的基质效应
Fig.4 Matrix effects of endrin in different flavor of Baijiu
结果表明,α-六六六、七氯、艾氏剂的基质效应可以忽略,异狄氏剂在清香型白酒中的基质效应可以忽略,在浓香型、酱香型、米香型白酒中的基质效应为增强,其它有机氯农残在四种不同香型白酒的基质中均为基质增强效应。尽管白酒的复杂基质对有机氯农残的响应有较大的影响,但并不影响方法对白酒中有机氯的筛查,为彻底消除基质效应,在对不同香型的白酒进行定量测定时,应该用相应香型的白酒进行基质配标准曲线。
2.7 样品检测分析
运用本方法对市售20余种白酒进行样品分析,均未检出目标分析物,这可能和白酒的酿造工艺相关。韩永涛[26]研究了从原粮到白酒的过程中各农药的迁移规律,结果表明供试农药的残留水平随着白酒酿造进程而不断降低,润糁过程对农药残留的去除效果与农药本身的蒸汽压有关,蒸汽压越高,去除效果越明显,蒸糁过程持续高温使农药残留降低22%~83%,发酵过程对农药的降解率在36%~76%之间,这说明白酒酿造工艺能显著降低白酒中农药残留水平。
3 结论
建立了GC-MS直接进样检测白酒中14种有机氯的检测方法,在拟定的实验条件下,14种有机氯农残得到了较好的分离,分析方法的检测限、回收率和灵敏度均满足痕量农残分析技术要求。本方法的检出限为0.01~0.11 μg/L,其检出限远低于其在食品中的残留限量,回收率和灵敏度也满足痕量农药残留分析技术要求,该方法的建立对白酒农药残留方法的制定及白酒中农药残留风险性评估具有十分重要的意义。
[1]王晓春,梁丽,周焕英.基于QuEChERS 净化/气相色谱法测定蔬菜及水果中16 种有机氯农药残留[J].分析测试学报,2021,40(3):401-405.
[2]田浩.有机氯农残检测方法及相关技术进展[J].科学技术创新,2017(5):45.
[3]夏静雪,李洒,李鹏飞.气相色谱串联质谱法测定水中多种有机氯农残[J].广州化工,2019,47(19):90-93.
[4]MOUSTAFA A,MOUSTAFA K,ATEF M,et al.Analysis of organochlorine pesticides residues in fish from Edko Lake(North of Egypt)using eco-friendly method and their health implications for humans[J].Toxicol Res,2021,38:1-9.
[5]YIN S J,SUN Y,YU J H,et al.Prenatal exposure to organochlorine pesticides is associated with increased risk for neural tube defects[J].Sci Total Environ,2021,770:145284-145284.
[6]ZHOU Q X,WU Y L,SHENG X Y,et al.Magnetic polyamidoamine dendrimers for magnetic separation and sensitive determination of organochlorine pesticides from water samples by high-performance liquid chromatogra-phy[J].J Environ Sci,2021,102:64-73.
[7]沈怡方.白酒生产技术全书[M].北京:中国轻工业出版社,2015:1-10.
[8]钱冲,廖永红,刘明艳,等.不同香型白酒的聚类分析和主成分分析[J].中国食品学报,2017,17(2):243-255.
[9]中华人民共和国卫生部,中国国家标准化管理委员会.GB 5749—2006生活饮用水卫生标准[S].北京:中国标准出版社,2006.
[10]严朝朝,魏文婉,伍佳慧,等.基质固相分散萃取-气相色谱法测定土壤中有机氯农药含量[J].化工环保,2021,41(2):235-240.
[11]LI G J,ZHANG X,LIU T T,et al.Dynamic microwave-assisted extraction combined with liquid phase microextraction based on the solidification of a floating drop for the analysis of organochlorine pesticides in grains followed by GC[J].Food Sci Hum Wellness,2021,10(3):375-382.
[12]王贵双,高丽华,赵俊平,等.固相萃取-气相色谱-质谱法测定粮谷中17 种有机氯和拟除虫菊酯农药残留[J].中国酿造,2010,29(11):165-170.
[13]李志,冉茂乾,张馨允,等.QuEChERS-GC-MS/MS 法同时测定刺梨中15 种有机氯农药残留[J].中国酿造,2020,39(3):166-171.
[14]钱冲,胡光辉,张梅,等.气相色谱-三重四级杆质谱法测定人参中22种有机氯农残[J].食品安全质量检测学报,2020,11(6):1736-1742.
[15]王蓉,袁东,付大友,等.气相色谱质谱法测定白酒中的有机氯农药残留[J].酿酒科技,2007(12):102-104.
[16]李俊,王震,庞宏宇,等.白酒中多种拟除虫菊酯类农药检测方法[J].酿酒科技,2013,233(11):98-100.
[17]袁河,王莉,楼小华,等.一种测定白酒中100 种农药残留的方法CN106248854A[P].2016-12-21.
[18]姜利,侯素丽,汤有宏,等.凝胶渗透GC-QQQ 法测定白酒中六六六与滴滴涕农药残留[J].分析仪器,2016(2):41-45.
[19]周琛,陈汉哲,苏婷,等.直接进样气相色谱-质谱法快速测定酒中氨基甲酸乙酯[J].现代预防医学,2016,43(4):715-721.
[20]中华人民共和国国家卫生和计划生育委员会.GB 2763—2019 食品安全国家标准食品中农药最大残留限量[S].北京:中国标准出版社,2019.
[21]王贵双,高丽华,孙晶,等.基质效应对气相色谱-质谱法测定粮谷中17 种有机氯和拟除虫菊酯农药残留影响的研究[J].中国酿造,2012,31(11):169-172.
[22]宋淑玲,饶竹,马晓东,等.不同基质中有机氯农药提取技术及发展趋势[J].分析测试学报,2011,30(1):108-114.
[23]易盛国,侯雪,韩梅,等.气相色谱-串联质谱法检测蔬菜农药残留基质效应与基质分类的研究[J].西南农业学报,2012,25(2):537-543.
[24]杨柳.中国白酒香型划分回顾与反思[J].酿酒科技,20163(5):115-116.
[25]张治刚,张彪,赵书名.中国白酒香型演变及发展趋势[J].中国酿造,2018,37(2):15-18.
[26]韩永涛.高粱酿酒过程中农药残留迁移规律及风险评估研究[D].北京:中国农业大学,2017.