酵母是一类包括酿酒酵母(Saccharomyces cerevisiae)和非常规酵母在内的能发酵糖类的多种单细胞真核微生物的总称,主要分布在偏酸性含糖量较高的环境中[1],其中酿酒酵母是工业生产中重要的微生物类群,它们可合成的天然产物超过100种[2],广泛应用于食品、医药保健、轻工、能源化工和生命科学等多个领域,尤其是在发酵食品和啤酒、葡萄酒等酒精类产品的发酵方面具有重要的作用[3],现如今全世界酒精年产量已超过一亿t[4]。
酿酒酵母在发酵过程中,尤其是在果酒生产中,经常会遇到强酸性、高糖、高酒精环境,这对酵母的耐酸性能提出了很高的要求。目前,国外科研工作者通过基因重组技术以获取耐酸性较强且产量高的酿酒酵母[5-6],但是基因重组技术获得的耐酸性能不够稳定。国内研究人员通常选择传统的筛选方法对酿酒酵母进行选育,同时对酿酒酵母耐酸机理展开研究[7],并将其应用于白酒和果酒的生产[8-10]。获得的酿酒酵母对于糖的利用能力、酒精生产能力、高糖和高酒精环境耐受性能等方面虽然有了很大的进步[11-12],但是对于耐酸性的高产菌株筛选工作仍有待进一步深化。
本研究采用酸性选择培养基、氯化三苯基四氮唑(triphenyltetrazolium chloride,TTC)显色法、杜氏小管发酵法从实验室保藏的87株酿酒酵母(Saccharomyces cerevisiae)中筛选出耐酸性强的优良菌株,并测定其最适生长条件、耐受性及发酵性能,以期为后续果酒酿造工作研究提供优质的菌种[13-14]。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
87株酿酒酵母(Saccharomyces cerevisiae)(编号为SC-1~SC-87):为前期研究利用皂素废水发酵酒精时筛选并保存于本实验室的具有一定耐酸性的实验菌株[15]。
1.1.2 培养基
酵母浸出粉胨葡萄糖(yeastextractpeptonedextrose,YPD)培养基[16]:酵母浸粉10.0 g,蛋白胨20.0 g,溶于900 mL蒸馏水中,121 ℃高压蒸汽灭菌20 min;另取葡萄糖20.0 g溶于100 mL蒸馏水中,115 ℃高压蒸汽灭菌15 min后与上述溶液混匀,pH自然。如配制固体培养基另加入20.0 g琼脂粉。
WL营养琼脂(wallerstein laboratory nutrient agar,WL)培养基[17]:酵母浸粉4.0 g,蛋白胨5.0 g,KH2PO4 0.55 g,KCl 0.425 g,CaCl2 0.125 g,MgSO4·7H2O 0.125 g,FeCl3 0.002 5 g,MnSO40.002 5 g,琼脂粉20.0 g,加入溴甲酚绿22.0 mg,121 ℃高压蒸汽灭菌20 min;另取葡萄糖50.0 g溶于100 mL蒸馏水中,115 ℃高压蒸汽灭菌15 min后与上述溶液混匀,pH自然。
TTC培养基[18]:TTC上层培养基:葡萄糖0.5 g,琼脂粉15.0 g,121 ℃高压蒸汽灭菌20 min,待冷却后加入TTC 0.5 g。TTC下层培养基:蛋白胨10.0 g,酵母浸粉7.5 g,KH2PO45.0 g,MgSO4·7H2O 2.0 g,柠檬酸1.35 g,氨苄青霉素1.0 g,琼脂粉30.0 g,溶于900 mL蒸馏水中,121 ℃高压蒸汽灭菌20 min;另取葡萄糖50.5 g溶于100 mL蒸馏水中,115 ℃高压蒸汽灭菌15 min后与上述溶液混匀,pH 4.0。
1.1.3 主要试剂
酵母浸粉、蛋白胨、葡萄糖、琼脂粉、乳酸、无水乙醇、KH2PO4、KCl、CaCl2、MgSO4·7H2O、FeCl3、MnSO4、NaCl:国药集团化学试剂有限公司;溴甲酚绿:上海源叶生物科技有限公司;氨苄青霉素:北京索莱宝科技有限公司。实验所用试剂均为分析纯或生化试剂。
1.2 仪器与设备
YJ-VS-1型单人垂直超净工作台:无锡一净净化设备有限公司;LDZX-50L型高压蒸汽灭菌锅:上海申安医疗器械厂;DHP-9602电热恒温培养箱:上海一恒科学仪器有限公司;BS-2E型恒温振荡培养箱:常州恒隆仪器有限公司;UV-1900i型紫外-可见分光光度计:岛津企业管理(中国)有限公司;ME204型电子分析天平、FE22型pH计:梅特勒-托利多国际贸易(上海)有限公司;PAL-1糖度仪:广州市爱宕科学仪器有限公司;A8964酒精计:上海阿拉丁生化科技股份有限公司。
1.3 试验方法
1.3.1 酿酒酵母菌株的活化
在无菌环境下分别挑取实验室保藏的87株酿酒酵母,接种到YPD固体斜面培养基上,于28 ℃培养24 h;挑取上述菌株移接入100 mL YPD液体培养基中,于28 ℃静置培养24 h;再移接入100 mL YPD液体培养基中,于28 ℃、160 r/min振荡培养24 h作为种子液,备用。
1.3.2 优良耐酸酿酒酵母菌株的筛选
用乳酸调节YPD液体培养基pH值为2.0,按5%(V/V)的接种量接入酿酒酵母种子液,于28 ℃、160 r/min振荡培养24 h后,取菌悬液划线于WL固体培养基,于28 ℃恒温培养24 h,挑取生长状况较好的典型的单菌落,接种到YPD固体斜面保藏,用于后续筛选[19]。
TTC显色法筛选[20-21]:用接种环挑取酿酒酵母菌株在TTC下层培养基表面连续划线,于28 ℃培养48 h,将融化并冷却至45~50 ℃的TTC上层培养基倒入TTC下层培养基表面,于28 ℃培养3 h后,观察培养基显色情况,从中筛选出产酒精能力较强的菌株。
杜氏小管发酵法筛选[22]:取0.5 mL酿酒酵母种子液于装有10 mL YPD液体培养基的试管中,倒置放入杜氏小管,并避免杜氏小管内有气体存在,密封后于28 ℃静置培养,每隔12 h观察并记录杜氏小管内产气情况,筛选出生长和发酵性能较好的菌株。
1.3.3 优良耐酸酿酒酵母菌株生长特征的测定
最适生长温度:按5%(V/V)的接种量将酿酒酵母种子液接种于100mLYPD液体培养基中,分别于不同温度(22℃、24 ℃、26 ℃、28 ℃、30 ℃、32 ℃)、160 r/min条件下振荡培养,每组平行三份,以不加菌的YPD液体培养基为对照,培养24 h后使用紫外-可见分光光度计在波长600 nm处测定菌液的OD600nm值。
最适生长pH值:用乳酸调节YPD液体培养基的pH值为3.0、3.2、3.4、3.6、3.8、4.0、4.2、4.4、4.6、4.8、5.0,按5%(V/V)的接种量将酿酒酵母种子液接种于100 mL不同pH值的YPD液体培养基中,在最适温度、160 r/min条件下振荡培养,每组平行三份,培养24 h后测定菌液的OD600nm值。
生长曲线的测定[23]:按最适pH值配制YPD液体培养基,按5%(V/V)的接种量将酿酒酵母种子液接种于100 mL YPD液体培养基中,在最适温度、160 r/min条件下振荡培养,每组平行三份,每2 h取样测定菌液的OD600nm值,以发酵时间(x)为横坐标,OD600nm值(y)为纵坐标绘制生长曲线。
1.3.4 优良耐酸酿酒酵母菌株耐受性的测定
乙醇耐受性测定:按体积比在YPD液体培养基中加入6%、8%、10%、12%、14%、16%、18%无水乙醇,按5%(V/V)的接种量将酿酒酵母种子液接种于100 mL YPD液体培养基中,在最适培养环境下培养48 h后测定菌液的OD600nm值。
盐耐受性能测定[24]:在YPD液体培养基中加入NaCl,使培养基中NaCl含量为10 g/L、30 g/L、50 g/L、70 g/L、100 g/L、150 g/L、200 g/L,按5%(V/V)的接种量将酿酒酵母种子液接种于100 mL YPD液体培养基中,在最适培养环境下培养一周,并观察菌株是否有生长。
糖耐受性能测定[24]:调整YPD液体培养基中葡萄糖的质量浓度分别为200 g/L、300 g/L、400 g/L、500 g/L、600 g/L,按5%(V/V)的接种量将酿酒酵母种子液接种于100 mL YPD液体培养基中,在最适培养环境下培养一周,并观察菌株是否有生长。
1.3.5 优良耐酸酿酒酵母菌株发酵性能的测定[25]
按5%(V/V)的接种量将酿酒酵母种子液接种于100 mL YPD液体培养基中,称质量后在最适培养条件下振荡培养,每24 h称一次质量,按国家标准GB/T 15038—2006《葡萄酒、果酒通用分析方法》测定发酵力、总糖、总酸、挥发酸含量及酒精度。
1.3.6 数据分析
采用Excel 2019对数据进行整理和作图,数据结果以“平均值±标准差”表示。
2 结果与分析
2.1 优良耐酸酿酒酵母菌株的筛选
2.1.1 酿酒酵母菌株耐酸性能的测定
从87株酿酒酵母中筛选得到5株耐酸性能较好的酿酒酵母菌株,分别为菌株SC-6、SC-15、SC-19、SC-55、SC-62,其生长情况见表1。
表1 酿酒酵母菌株耐酸性能的测定结果
Table 1 Determination results of acid tolerance of Saccharomyces cerevisiae strains

注:“+++”表示菌落生长良好;“++”表示菌落生长中等;“+”表示菌落生长差。
2.1.2 酿酒酵母菌株产酒精能力的测定
5株酿酒酵母菌株的产酒精能力见表2。由表2可知,菌株SC-6、SC-15、SC-62的产酒精能力相对较强。
表2 5株酿酒酵母菌株产酒精能力的测定结果
Table 2 Determination results of alcohol production capacity of 5 Saccharomyces cerevisiae strains
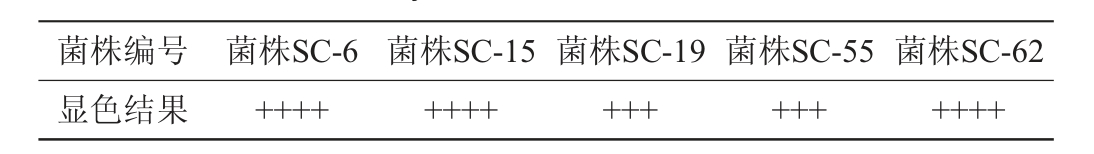
注:“++++”表示颜色为深红色;“+++”表示颜色为红色;“++”表示颜色为粉红色;“+”表示颜色为浅粉色;“-”表示无颜色变化。
2.1.3 酿酒酵母菌株产气能力的测定
5株酿酒酵母菌株的产气情况见表3。
表3 5株酿酒酵母菌株产气能力的测定结果
Table 3 Determination results of gas production capacity of 5 Saccharomyces cerevisiae strains

注:“++++”表示杜氏小管充满CO2气体;“+++”表示杜氏小管中充有1/2 CO2气体;“++”表示杜氏小管中充有1/3 CO2气体;“+”表示杜氏小管中充有1/4 CO2气体。
由表3可知,菌株SC-15和SC-62的产气能力最强,在24 h时已经使杜氏小管中充有一半气体,在36 h时杜氏小管中已经充满CO2气体。结合TTC显色实验结果,故选择菌株SC-15和SC-62为优良耐酸酿酒酵母菌株。
2.2 优良耐酸酿酒酵母菌株的生长特征
2.2.1 最适生长温度的测定结果培养温度对酿酒酵母SC-15和SC-62生长的影响见图1。
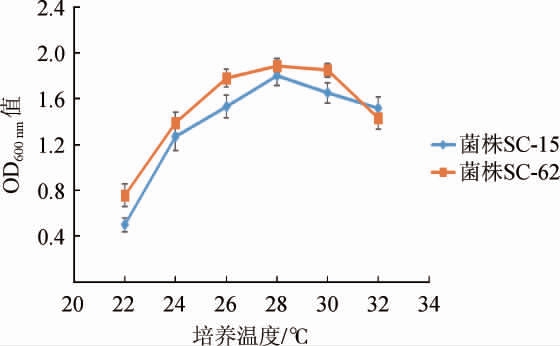
图1 培养温度对两株酿酒酵母菌株的影响
Fig.1 Effects of culture temperature on 2 Saccharomyces cerevisiae strains
由图1可知,酿酒酵母SC-15和SC-62均在28 ℃时生长最好,OD600nm值达到最大,分别为1.80和1.89。菌株SC-62在26~32 ℃的范围内OD600nm值均高于菌株SC-15,尤其是在30 ℃时,菌株SC-62的OD600nm值与28 ℃时变化不明显,呈现出更强的温度适应能力。综上,菌株SC-15和SC-62的最适生长温度均为28 ℃,且菌株SC-62的温度适应能力更强。
2.2.2 最适生长pH值的测定结果
培养基初始pH对酿酒酵母SC-15和SC-62生长的影响见图2。

图2 初始pH值对两株酿酒酵母菌株的影响
Fig.2 Effects of initial pH value on 2 Saccharomyces cerevisiae strains
由图2可知,pH值变化对两株菌生长的影响存在差异,菌株SC-15在初始pH值为3.8~4.8之间生长良好,有较宽的pH值适应范围,其最适pH值为4.4,而菌株SC-62在初始pH值为3.6~4.4之间生长旺盛,最适pH值为4.0。在pH值3.0~4.2范围内,菌株SC-62的OD600nm值高于菌株SC-15,说明菌株SC-62具备更强的耐酸特性。综上,菌株SC-15和SC-62的最适生长pH值分别为4.4、4.0,且菌株SC-62具备更强的耐酸特性。
2.2.3 生长曲线的测定结果
酿酒酵母SC-15和SC-62的生长曲线见图3。

图3 两株酿酒酵母菌株的生长曲线
Fig.3 Growth curves of 2 Saccharomyces cerevisiae strains
由图3可知,两株酿酒酵母菌株的生长规律类似,菌株SC-15在发酵0~14 h时生长速度较慢,为延滞期;在发酵14~22 h时进入迅速生长的对数期,之后进入稳定期。与菌株SC-15相比,菌株SC-62的延滞期相对更短,在第12小时时进入对数期,达到稳定期后的OD600nm值也稍高。在生产中延滞期短的菌株适应能力更强,可在短时间内形成数量优势,减少染菌机会同时减少副产物的形成,并有利于提高发酵效率。
2.3 优良耐酸酿酒酵母菌株的耐受性
2.3.1 耐乙醇性能的测定结果
酿酒酵母SC-15和SC-62的耐乙醇性能见图4。
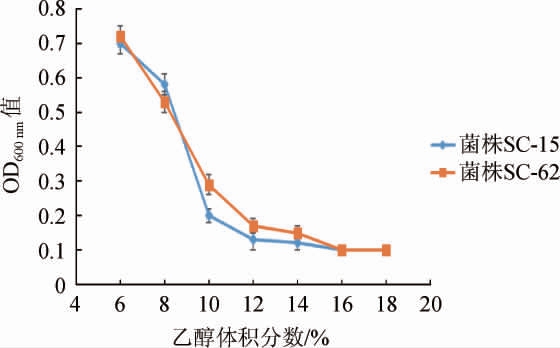
图4 两株酿酒酵母菌株耐乙醇性能的测定结果
Fig.4 Determination results of alcohol tolerance of 2 Saccharomyces cerevisiae strains
由图4可知,乙醇体积分数在6%~8%时,两株酿酒酵母生长状况均良好;当乙醇体积分数>12%之后,两株菌株受到较大的抑制,OD600nm值急剧下降;当乙醇体积分数>16%之后,两株菌株的OD600nm值与刚接种时相同,说明酿酒酵母在此环境中被完全抑制。与菌株SC-15相比,菌株SC-62的耐乙醇性能较好,且优于李彦芹等[24-25]研究菌株的耐受性。
2.3.2 耐盐性能测定结果
酿酒酵母SC-15和SC-62的耐盐性能见表4。
表4 两株酿酒酵母菌株耐盐性能的测定结果
Table 4 Determination results of salt tolerance of 2 Saccharomyces cerevisiae strains

注:“+”表示有菌体生长;“-”表示无菌体生长。下同。
由表4可知,两株酿酒酵母均能在NaCl质量浓度≤70g/L的YPD液体培养基中生长,当NaCl质量浓度为100 g/L时,菌株SC-62仍可生长,可见菌株SC-62具有良好的耐盐性能。
2.3.3 耐糖性能测定结果
酿酒酵母SC-15和SC-62的耐糖性能见表5。
表5 两株酿酒酵母菌株耐糖性能的测定结果
Table 5 Determination results of sugar tolerance of 2 Saccharomyces cerevisiae strains
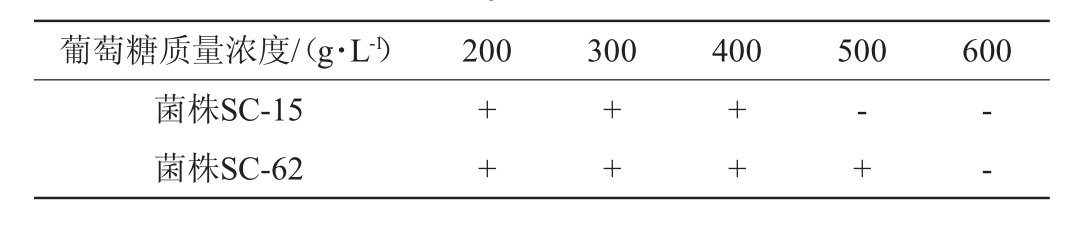
由表5可知,菌株SC-15在葡萄糖质量浓度≤400 g/L的YPD液体培养基中生长,而菌株SC-62具有相对更好的耐糖性能,可在葡萄糖质量浓度≤500 g/L的YPD液体培养基中生长。
2.4 优良耐酸酵母菌株发酵性能测定结果
酿酒酵母SC-15和SC-62的发酵性能见表6。
表6 两株酿酒酵母菌株发酵性能的测定结果
Table 6 Determination results of fermentation performance of 2 Saccharomyces cerevisiae strains

由表6可知,菌株SC-62具有更高的发酵力[5.93 g CO2/(100 mL·24 h)],高于杨宽等[25]的研究结果,说明此菌株能充分利用培养基中的糖转化为酒精,发酵后酒精度达到7.55%vol,达到了用于果酒发酵的要求,产生的挥发酸含量(0.61 g/L)也低于国标GB 15037—2006《葡萄酒》中规定的葡萄酒中挥发酸含量≤1.2 g/L的限值,综合性能优于菌株SC-15,相比实验室保存的原有菌株,菌株SC-62具备更好的耐酸、耐糖性能,同时具有延滞期短、可适应较宽的温度范围等优点,发酵力强,具备一定的应用价值[15]。
3 结论
本研究采用酸性选择培养基、TTC显色法、杜氏小管发酵法从实验室保藏的87株酿酒酵母(Saccharomyces cerevisiae)中筛选得到2株耐酸性强的优良菌株,其中菌株SC-62综合性能优于菌株SC-15,最适生长温度、pH分别为28 ℃、4.0,可耐受乙醇体积分数14%、NaCl 100 g/L、葡萄糖500 g/L,具有发酵力[5.93 g CO2/(100 mL·24 h)]强,酒精产量(7.55%vol)高,延滞期(12 h)短、适应性强等优点。
[1]何国庆,贾英民,丁立孝.食品微生物学[M].[第3 版].北京:中国农业大学出版社,2016:10-40.
[2]张云丰,何丹,卢欢,等.代谢工程改造酿酒酵母底盘细胞[J].科学通报,2021,66(3):310-318.
[3]范婷婷,王慕瑶,李俊,等.酵母生物多样性开发及工业应用[J].生物工程学报,2021,37(3):806-815.
[4]ZAZULYA A,SEMKIV M,DMYTRUK K,et al.Adaptive evolution for the improvement of ethanol production during alcoholic fermentation with the industrial strains of yeast Saccharomyces cerevisiae[J].Cytol Genet,2020,54(5):398-407.
[5] WAWRO A.Improvement of acetic acid tolerance in Saccharomyces cerevisiae by novel genome shuffling[J].Appl Biochem Microbiol,2021,57(2):180-188.
[6]TSAI S Y,HSU Y C,SHU C M,et al.Synchronization of isothermal calorimetry and liquid cultivation identifying the beneficial conditions for producing ethanol by yeast Saccharomyces cerevisiae fermentation[J].J Therm Anal Calorim,2020,142(2):829-840.
[7]张国顺,洪青,刘智,等.一株特耐酸酵母R1 的分离及其耐酸机理研究[J].微生物学报,2004,44(5):631-635.
[8]卢君,山其木格,唐平,等.耐酸酵母菌株的筛选及其在酱香白酒酿造过程中的应用研究[J].酿酒科技,2019(10):106-111.
[9]葛隐,唐圣云,赵东,等.五粮液窖池中耐酸性酿酒酵母菌的分离与筛选[J].中国酿造,2010,29(8):130-133.
[10]胡佳星,袁文艳,杨小冲,等.耐酸酵母菌株在沙棘果酒中的应用研究[J].中国酿造,2018,37(5):71-75.
[11] GALLONE B,STEENSELS J,PRAHL T,et al.Domestication and divergence of Saccharomyces cerevisiae beer yeasts[J].Cell,2016,166(6):1397-1410.e1316.
[12]VILELA J,VILELA L,RAMOS C L,et al.Physiological and genetic characterization of indigenous Saccharomyces cerevisiae for potential use in productions of fermented maize-based-beverages[J].Braz J Microbiol,2020,51(3):1297-1307.
[13] KISHKOVSKAYA S A,TANASHCHUK T N,SHALAMITSKIY M Y,et al.Natural yeast strains of Saccharomyces cerevisiae that are promising for sherry production[J].Appl Biochem Microbiol,2020,56(3):329-335.
[14]FERNANDES A M O,GARCIA N F L,FONSECA G G,et al.Evaluation of the fermentative capacity of Saccharomyces cerevisiae CAT-1 and BB9 strains and Pichia kudriavzevii BB2 at simulated industrial conditions[J].Indian J Microbiol,2020,60(4):494-504.
[15]耿海波,安丽平.皂素废水酒精发酵条件的研究[J].河北化工,2011,34(8):44-45,50.
[16]白玉峰,张文霞,田亚楠,等.宁夏贺兰山东麓降L-苹果酸葡萄酒酵母的筛选[J].中国酿造,2021,40(1):49-54.
[17]方月月,解文利,潘肇仪,等.生姜猕猴桃自然酒精发酵醪微生物多样性研究[J].中国酿造,2020,39(12):125-129.
[18]李凯,王金晶,李永仙,等.红芯火龙果酒酿酒酵母的筛选及鉴定[J].食品与发酵工业,2019,45(5):115-120.
[19]杨小冲,陈忠军,赵洁,等.紫外诱变选育耐酸酵母菌株及其特性研究[J].中国酿造,2017,36(10):109-113.
[20]陈忠军,杨小冲,赵洁,等.具高乙醇耐受力酵母菌的选育及其在猕猴桃果酒中的应用[J].食品工业科技,2018,39(2):141-145,151.
[21]王犁烨,陈新军,卢丕超,等.紫外诱变选育高产酒精及酸的酿酒酵母[J].中国酿造,2019,38(1):104-108.
[22]王犁烨,王浩臣,马珊,等.常压室温等离子体选育高产酒精及酸的酿酒酵母[J].食品与机械,2019,35(5):26-31.
[23]苏艳秋,朱卫华,吴鹏,等.耐高温、耐酸产酒精酵母的筛选与鉴定[J].微生物学杂志,2009,29(2):43-47.
[24]李彦芹,崔海灏,李春青,等.耐酸酵母的分离鉴定及在丢糟发酵中的应用[J].河北大学学报(自然科学版),2016,36(5):517-523.
[25]杨宽,张帅,王柱华,等.香格里拉葡萄酒产区野生酿酒酵母的分离鉴定和发酵性能研究[J].食品研究与开发,2020,41(14):83-91.