大头菜(Brassica iuncea)原产于我国,隶属于芸苔属一年生草本植物,栽培面积约100万hm2,具有极其丰富的茎用、叶用和根用等价值[1]。腌制大头菜叶以根用大头菜的绿叶为主要原料,并辅以食盐、姜末和大蒜等发酵制成,经过清洗切断、晒干脱水、辅料混合和厌氧发酵等过程[2-3]。在腌制过程中,芥菜叶中的硫代葡萄糖苷和氨基酸等,在酸和酶的作用下生成芥子油等挥发性风味物质,赋予成品独特的香味[4]。研究报道显示,大头菜叶腌制一般为自然发酵,叶片表面附着的微生物起主要作用,包括乳酸球菌、乳酸杆菌、酵母菌和肠膜明串珠菌等有益微生物[5]。目前,对于大头菜叶腌制的研究主要集中在发酵工艺优化[6]、减少食盐用量[7-8]和挥发性风味物质的研究[9]以及提取物抗氧化上等[10-13],而对于腌制大头菜叶中微生物多样性的研究却相对较少。
随着测序技术的广泛应用,Illumina MiSeq 高通量测序技术快速发展,以其快速高效等特点,成为微生物群落多样性解析的主要工具[14],目前广泛应用于发酵食品中微生物多样性解析[15-18]。周森等[19]利用Illumina MiSeq 高通量测序技术对来自5个地区的11份清香型大曲中微生物进行研究,发现清香型大曲中细菌微生物多样性丰富,真菌则以扣囊覆膜酵母为优势真菌;玛依乐·艾海提等[20]利用高通量测序技术研究发现南疆传统酸奶中厚壁菌门(Firmicutes)和子囊菌门(Ascomycota)分别为优势细菌门和真菌门。蔡怀依等[21]利用Illumina MiSeq 高通量测序技术对新鲜年糕内细菌多样性进行研究,发现年糕内生细菌优势菌属为玫瑰色半光合菌属(Roseateles)、芽孢杆菌属(Bacillus)和寡养单胞菌属(Stenotrophomonas)。
本研究以湖北省来凤县腌制大头菜叶样品为研究对象,采用Illumina MiSeq高通量测序技术,以细菌16S rRNA和真菌18S rRNA为靶点,对腌制大头菜叶中细菌和真菌微生物群落结构和多样性进行了解析。本研究通过对腌制大头菜中微生物的研究,以期为后续腌制大头菜叶品质提升、纯种发酵及安全评价提供理论依据和数据支撑。
1 材料与方法
1.1 材料与试剂
LB培养基:青岛海博生物技术有限公司;QIAGEN DNeasy mericon Food Kit 脱氧核糖核苷酸(deoxyribo nucleic acid,DNA)基因组提取试剂盒:德国QIAGEN公司;脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphates,dNTPs)混合液、FastPfu Fly DNA聚合酶、5×TransStartTM FastPfu Buffer:北京全式金生物技术有限公司。
1.2 仪器与设备
SW-CJ-2D型双人单面净化工作台:苏州安泰空气技术有限公司;ND-2000C微量紫外分光光度计:美国Thermo公司;Veriti FAST梯度聚合酶链式反应polymerase chain reaction,PCR)仪:美国ABI公司;DYY-12电泳仪:北京六一仪器厂;UVPCDS8000凝胶成像分析系统:美国ProteinSimple公司;Illumina MiSeq高通量测序平台:美国Illumina公司;R920机架式服务器:美国Dell公司。
1.3 方法
1.3.1 样品采集
从恩施土家族苗族自治州来凤县北门菜市场和金凤市场采集腌制大头菜叶样品3份,分别标记为LF1、LF2、LF3,置于含有冰袋的采样箱中运回实验室,-20 ℃保存备用。
1.3.2 样品微生物宏基因组DNA的提取
称取2.0 g腌制大头菜叶样品,按照QIAGEN DNeasy mericon Food Kit DNA基因组提取试剂盒说明书步骤对样品DNA进行提取。
1.3.3 细菌16S rRNA的PCR扩增
使用加入成对核苷酸标签(barcode)的引物,参照文献[22]中的PCR扩增体系和条件对细菌16S rRNA V3-V4区进行PCR扩增。PCR扩增体系:5×PCR缓冲液4 μL,dNTPs混合液(2.5 mmol/L)2 μL,正反向引物(5 μmol/L)各0.8 μL,DNA聚合酶(5 U/μL)0.4 μL,DNA模板10 ng,补充双蒸水(ddH2O)至20 μL。PCR扩增条件:95 ℃预变性3 min;95 ℃变性30 s,55 ℃退火30 s,72 ℃延伸45 s,循环30 次;72 ℃再延伸10 min。
1.3.4 真菌18S rRNA序列扩增
加入成对核苷酸标签(barcode)的引物,对真菌18SrRNA V3-V4区进行PCR扩增,PCR扩增体系及条件同1.3.3。
1.3.5 高通量测序及生物信息学分析
将经1.0%琼脂糖凝胶电泳检测成功的PCR产物,送至上海美吉生物医药科技有限公司进行测序,使用Illumina MiSeq PE300高通量测序平台进行测序。将返回序列拼接后进行质控[23],对齐和去除引物。参照沈馨等[24]的分析流程,使用QIIME(V1.70)平台对质控后合格的序列进行物种分析和多样性评价。1)使用PyNAST软件对序列进行对齐;2)按照97%和100%相似度对序列进行两步UCLUST法构建操作分类单元(operationaltaxonomicunits,OTU)矩阵;3)使用ChimeraSlayer软件将含有嵌合体的OTU进行筛选与去除;4)挑选OTU代表性序列,使用RDP、SILVA和GREE-NGENE 3 个数据库进行同源性比对,明确不同水平的分类学地位;5)计算Chao1指数、Shannon指数和发现物种数,进而对微生物群落的多样性和丰度进行评价。
1.3.6 多元统计学分析
使用柱状图表示样品中优势细菌门和真菌门构成及相对含量;使用热图对优势细菌属和真菌属间相关性进行可视化处理;使用R软件(V3.6.2)对文中的图进行绘制。
2 结果与分析
2.1 序列丰度和多样性分析
对纳入本研究的3 份腌制大头菜叶样品的16S rRNA和18S rRNA高通量测序结果的不同分类学地位进行数量统计,结果如表1所示。
表1 腌制大头菜叶样品测序结果及不同分类学地位数量统计
Table 1 Sequencing results and quantitative statistics in different taxonomic status of pickled kohlrabi leaves samples
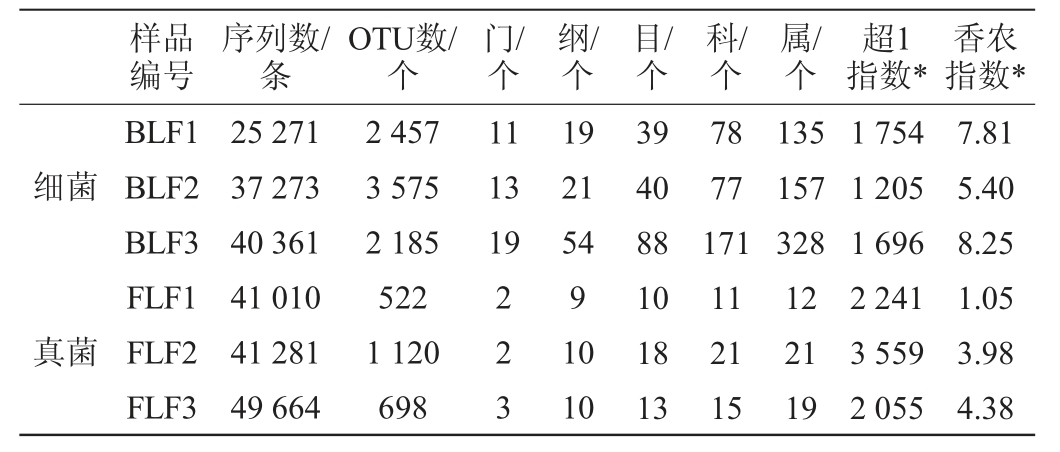
注:*表示计算细菌超1指数和香农指数时,样品测序量均在测序量为24010条;计算真菌超1指数和香农指数时,样品测序量均在40010条。
由表1可知,3 个样品共产生102 905 条高质量16S rRNA序列,平均每个样品产生34 301 条;共产生131 955 条高质量18S rRNA序列,平均每个样品产生43 985 条。按照97%和100%的相似度对序列进行划分后分别得到8 217个细菌OTU和2 340 个真菌OTU。
当细菌测序量达到24 010 时,样品BLF1的超1指数最高为1 754,样品BLF3的香农指数最高为8.25;当真菌测序量达到40 010 时,样品FLF2的超1指数最高为3 559,样品FLF3的香农指数最高为4.38。由此可见,3 号样品细菌和真菌菌落较其他2个样品具有较高的物种多样性。值得一提的是,细菌菌落香农指数均高于真菌,而超1指数均低于真菌,说明腌制大头菜叶中细菌群落多样性较高且分布均匀,而真菌的群落结构多样性和分布均匀性均不如细菌,可能与密封发酵中的厌氧环境对真菌生长抑制以及腌制大头菜制作环境的差异有关[25]。
2.2 基于不同分类地位的微生物菌群种类及平均相对含量分析
腌制大头菜叶样品中细菌和真菌优势门(相对含量>1%)种类及平均相对含量如图1所示。
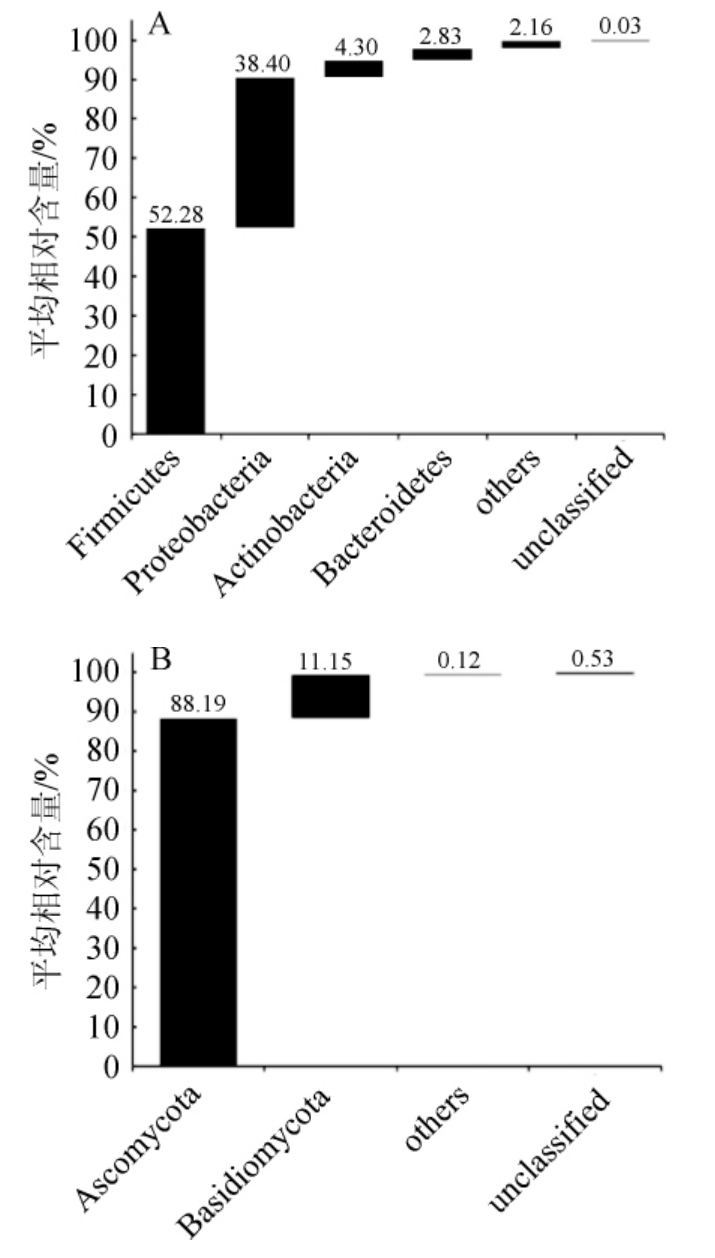
图1 腌制大头菜叶细菌(A)和真菌(B)优势门平均相对含量分析
Fig.1 Average relative contents of bacteria (A) and fungi (B) dominant phylum of pickled kohlrabi leaves
others表示相对含量<1%的菌门。
3个腌制大头菜叶样品在门的分类水平上,注释到明确分类地位的分别有20个细菌门和3个真菌门,其中平均相对含量>1%的细菌门有4个,分别为硬壁菌门(Firmicutes,52.28%)、变形菌门(Proteobacteria,38.40%)、放线菌门(Actinobacteria,4.30%)和拟杆菌门(Bacteroidetes,2.83%);平均相对含量>1%的真菌门有2个,分别为子囊菌门(Ascomycota,88.19%)和担子菌门(Basidiomycota,11.15%)。
本研究进一步对腌制大头菜叶样品中细菌和真菌优势属(相对含量>1%)的种类及平均相对含量进行了统计,结果如图2所示。

图2 腌制大头菜叶细菌(A)和真菌(B)优势属平均相对含量分析
Fig.2 Average relative contents analysis of bacteria (A) and fungi (B)dominant genera of pickled kohlrabi leaves
在属的分类水平上,注释到明确分类地位的细菌属和真菌属分别有382个和31个。
由图2(A)可知,腌制大头菜叶样品中优势细菌属有12个,分别为乳酸杆菌属(Lactobacillus,22.45%)、假单胞菌属(Pseudomonas,10.97%)、樱桃样芽胞杆菌属(Cerasibacillus,10.58%)、肠杆菌属(Enterobacter,8.29%)、枝芽孢杆菌属(Virgibacillus,6.44%)、不动杆菌属(Acinetobacter,6.06%)、芽孢杆菌属(Bacillus,2.50%)、魏斯氏菌属(Weissella,2.08%)、欧文氏菌属(Erwinia,1.65%)、气单胞菌属(Aeromonas,1.42%)、鞘脂单胞菌属(Sphingomonas,1.09%)和乳球菌属(Lactococcus,1.02%)。由图2(B)可知,腌制大头菜叶样品中优势真菌属有8 个,分别为接合酵母属(Zygosaccharomyces,55.29%)、德巴利氏酵母属(Debaryomyces,9.33%)、隐球菌属(Cryptococcus,7.97%)、假丝酵母属(Candida,6.83%)、枝孢属(Cladosporium,6.70%)、曲霉菌属(Aspergillus,4.23%)、毕赤酵母属(Pichia,1.57%)和节菌属(Wallemia,1.07%)。由图2亦可知,细菌属和真菌属分别有5.04%和5.40%的属不能注释到明确的分类地位。
值得一提的是,接合酵母属(Zygosaccharomyces)在样品FLF1中含量高达91.95%,与其他样品存在较明显差异,且隐球菌属(Cryptococcus)在样品FLF3中相对含量为22.06%,而在FLF1和FLF2中仅含有0.24%和1.62%,进一步证明,不同大头菜样品中真菌菌群分布不均匀。
2.3 OTU统计分析
据统计,样品中细菌和真菌OTU总数分别为7 510个和1 959个,而3个样品共有的OTU分别为143个和88个。本研究进一步统计了样品中平均相对含量大于1%的核心OTU构成及平均相对含量,结果如图3所示。
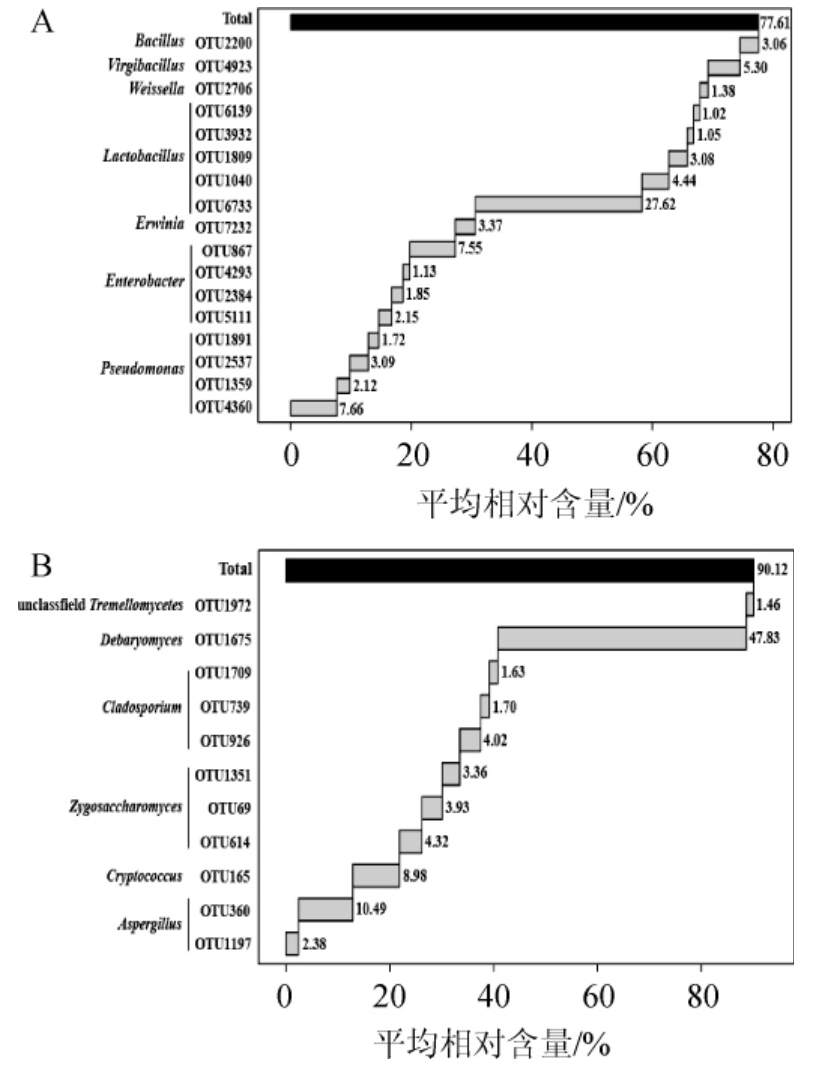
图3 腌制大头菜叶细菌(A)和真菌(B)核心OTU平均相对含量分析
Fig.3 Average relative content analysis of bacteria (A) and fungi (B)core OTU of pickled kohlrabi leaves
由图3(A)可知,3个样品中核心细菌OTU有17个,其中有5个隶属于乳酸杆菌属(Lactobacillus),4个隶属于肠杆菌属(Enterobacter)、4个隶属于假单胞菌属(Pseudomonas)、1个隶属于枝芽孢杆菌属(Virgibacillus)、1个隶属于芽孢杆菌属(Bacillus)、1个隶属于魏斯氏菌属(Weissella)。由图3(B)可知,3个样品中核心真菌OTU有11个,其中有3个隶属于枝孢属(Cladosporium)、3 个隶属于接合酵母属(Zygosaccharomyces)、2个隶属于曲霉菌属(Aspergillus)、1个隶属于德巴利氏酵母属(Debaryomyces)、1个隶属于隐球菌属(Cryptococcus)和一个仅鉴定到纲的银耳纲(Tremellomycetes)。
此外,细菌OTU867(隶属于肠杆菌属)在样品BLF2含量达到21.32%,在样品BLF1和BLF3中含量仅为0.03%和1.30%;真菌OTU1675(隶属于德巴利氏酵母属)在样品FLF1和FLF2中含量高达92.57%和48.12%,而在样品FLF3中仅含2.80%。由此可见,虽然细菌和真菌的核心OTU在所有样品中均存在,但是在每个样品中的含量却存在明显的差异[26],进一步证明自然发酵蔬菜中微生物的群落结构和多样性受制作环境的影响,进而影响发酵蔬菜的品质。
2.4 核心细菌属和真菌属相关性分析
本研究共发现12个核心细菌属和8个核心真菌属,其相关性热图如图4所示。

图4 腌制大头菜叶细菌和真菌优势属相关性分析
Fig.4 Correlation analysis of bacteria and fungi dominant genera of pickled rutabaga leaves
由图4可知,曲霉菌属(Aspergillus)与假单胞菌属(Pseudomonas)和枝孢属(Cladosporium)与魏斯氏菌属(Weissella)呈显著正相关(P<0.05),而其他优势细菌属和真菌属之间相关性均不显著(P>0.05)。由此可见,腌制大头菜叶中部分真菌和细菌之间存在着明显的共生关系,这种共生关系对发酵蔬菜的品质有什么样的影响还需要进一步的研究。
3 结论
本研究利用Illumina MiSeq第二代测序技术对3 个腌制大头菜叶样品进行微生物多样性研究后发现,共鉴定出20 个细菌门,优势细菌门有4个,分别为硬壁菌门(Firmicutes)、变形菌门(Proteobacteria)、放线菌门(Actinobacteria)和拟杆菌门(Bacteroidetes);鉴定出3个真菌门,优势真菌门仅有2 个,分别为子囊菌门(Ascomycota)和担子菌门(Basidiomycota)。优势细菌属分别为隶属于硬壁菌门的乳酸杆菌属(Lactobacillus)、樱桃样芽孢杆菌属(Cerasibacillus)、枝芽孢杆菌属(Virgibacillus)、芽孢杆菌属(Bacillus)、魏斯氏菌属(Weissella)和乳球菌属(Lactococcus);隶属于变形菌门的假单胞菌属(Pseudomonas)、肠杆菌属(Enterobacter)、不动杆菌属(Acinetobacter)、欧文氏菌属(Erwinia)、气单胞菌属(Aeromonas)和鞘脂单胞菌属(Sphingomonas)。优势真菌属分别为隶属于子囊菌门的接合酵母属(Zygosaccharomyces)、德巴利氏酵母属(Debaryomyces)、假丝酵母属(Candida)、枝孢属(Cladosporium)、曲霉菌属(Aspergillus)和毕赤酵母属(Pichia);隶属于担子菌门的隐球菌属(Cryptococcus)和节菌属(Wallemia)。结果表明,由于是自然发酵,制作环境的不同造成腌制大头菜叶样品中间微生物多样性差异较高,密闭发酵的方式造成样品中细菌群落物种种类和分布的均匀性高于真菌。
[1]许庆方,董宽虎,王保平,等.芥菜叶青贮的研究[J].饲料博览,2010(6):44-45.
[2]杨媛,蔡丽,刘淑晶,等.芥菜抗芜菁花叶病毒种质资源的鉴定与评价[J].华中农业大学学报,2019,38(2):65-67,69-72.
[3]NEUPANE R C,SHRESTHA A K,REGMI R,et al.Effect of pest exclusion net (PEN) on the sustainable production of late season broad leaf mustard(BLM)in Chitwan,Nepal[J].J Agr Sci Tech,2018,8(5):315-322.
[4]王洁,杨晓宾,王婧,等.几种叶用芥菜发芽期耐盐性鉴定与分析[J].浙江农业科学,2019,60(11):2028-2030,2033.
[5]李文青,卿泉,唐清苗,等.发酵芥菜工艺及品质变化研究进展[J].中国酿造,2019,38(12):1-4.
[6]侯爱香,王一淇,姜辉,等.基于Plackett-Burman 的湖南芥菜发酵菌种高密度培养条件优化[J].湖南农业大学学报(自然科学版),2017,43(16):669-675.
[7]周美琪,周其德,田赛莺,等.低盐腌制对缙云梅干菜加工品质的影响[J].核农学报,2018,32(8):1562-1571.
[8]任爱清,徐生可,周亚君,等.菜干低盐腌制过程中品质影响因子的动态变化[J].浙江农业科学,2020,61(7):1414-1417.
[9]罗耀华,刘晓鸣,李月,等.不同芥菜的滋味及挥发性成分变化规律[J].食品科技,2018,43(9):90-94.
[10]SHEN Q,JIANG J,WANG M T,et al.Volatile compounds and antioxidant properties of pickled and dried mustard as influenced by different cooking methods[J].J Food Process Pres,2019,43(4):e13918.
[11]张新,张有做.绍兴梅干菜提取物抗氧化活性研究[J].食品与发酵科技,2017,53(6):75-80.
[12]沈清,楼乐燕,尹培,等.5 种梅干菜的酚类化合物及抗氧化能力比较分析[J].食品科学,2018,39(12):212-218.
[13]黄师荣,李豪杰,戴杰辉,等.九头芥梅干菜提取物抗菌活性及其在猪肉保鲜中的应用[J].现代食品科技,2014,30(10):58-62,101.
[14]CAPORASO J G,LAUBER C L,WALTERS W A,et al.Ultra-high-throughput microbial community analysis on the Illumina HiSeq and MiSeq platforms[J].Int Society Microb Ecol,2012,6(8):1621-1624.
[15] GUO Z,WANG Y R,XIANG F S,et al.Bacterial diversity in pickled cowpea(Vigna unguiculata[Linn.]Walp)as determined by Illumina MiSeq sequencing and culture-dependent methods[J].Curr Microbiol,2021,78:1286-1297.
[16]陈梦娟,蒋立文,徐元昊,等.利用Illumina MiSeq 测序分析手筑茯砖茶发酵及干燥阶段真菌群落多样性[J].食品科学,2020,41(2):126-132.
[17]CHEN M,QIN Y,DENG F,et al.Illumina MiSeq Sequencing reveals microbial community succession in salted peppers with different salinity during preservation[J].Food Res Int,2021,143(1):110234.
[18]王琪琪,田界先,潘宗东,等.基于Illumina MiSeq 分析贵州凯里酸汤独特风味的优势菌群[J].食品与发酵工业,2020,46(14):40-47.
[19]周森,胡佳音,崔洋,等.应用高通量测序技术解析清香型大曲微生物多样性[J].中国食品学报,2019,19(6):244-250.
[20]玛依乐·艾海提,西热娜依·阿布力克木,努尔古丽·热合曼.应用高通量测序法检测南疆传统酸奶中微生物多样性[J].食品科学,2018,39(20):126-131.
[21]蔡怀依,雷丽萍,娄永江,等.基于高通量测序分析年糕菌群结构和优势菌属[J].中国粮油学报,2018,33(8):112-118.
[22]尚雪娇,王玉荣,杨江,等.应用Illumina MiSeq 高通量测序技术解析梅干菜中细菌多样性.中国酿造,2019,38(1):140-144.
[23]王旭辉,徐鑫,宝哲,等.高通量测序分析新疆沼液中发酵微生物的多样性[J].农业工程学报,2019,35(5):219-225.
[24]沈馨,王艳,代凯文,等.基于Miseq 高通量测序技术的辣椒酱核心细菌类群研究[J].食品研究与开发,2018,39(10):151-157.
[25]郭倩倩,卢彪.基于高通量测序不同生产工艺晴隆酸菜细菌多样性分析[J].中国酿造,2019,38(8):73-76.
[26]陈善义,李菁菁,林俭,等.基于高通量测序的不同产地和部位自然醇化片烟真菌群落结构分析[J].烟草科技,2018,51(4):12-19.