米酒又称醪糟,是以糯米为原料,经液化、糖化和发酵而成的中国传统酿造酒之一[1],主要分布在我国湖北省、广西壮族自治区和四川省等地区[2],其营养丰富,具有开胃提神、抗氧化和抗衰老等多种功效[3]。米酒主体香气成分为乙酸乙酯、乳酸乙酯和β-苯乙醇,主要由微生物在米酒酿造过程中代谢生成[4]。米酒的品质与米酒曲的微生物群落息息相关,因而有“曲为酒之骨”的说法[5-6]。米酒曲的制作通常是在开放的环境内完成,因而其微生物菌群较为丰富,包含细菌、真菌和霉菌三个类群,其中霉菌分泌的酶可以加速谷物中的淀粉和蛋白质等物质的转化,糖分在酵母菌的代谢下可进一步生成乙醇,而以乳酸菌为代表的细菌类群则对米酒滋味品质的形成具有重要作用[7-8]。
近年来,关于米酒曲中微生物多样性的研究卓有成效。向凡舒等[9]对湖北省建始地区米酒曲微生物群落进行研究,结果发现细菌以假单胞菌属(Pseudomonas)、片球菌属(Pediococcus)、魏斯氏菌属(Weissella)、芽孢杆菌属(Bacillus)、肠杆菌属(Enterobacter)、泛菌属(Pantoea)、克雷伯菌属(Klebsiella)和乳球菌属(Lactococcus)为主;真菌以淀粉霉属(Amylomyces)、复膜孢酵母属(Saccharomycopsis)和威克汉姆酵母属(Wickerhamomyces)为主;杨春敏等[10]对海南省山兰米酒曲的微生物多样性进行分析,结果发现真菌主要以根霉属(Rhizopus)、假丝酵母属(Candida)、布勒掷孢酵母属(Bullera)、拟青霉属(Simplicillium)、曲霉属(Aspergillus)和赤霉属(Gibberella)为主,其中Rhizopus是酒曲中优势真菌属;蔡海莺等[11]对12种不同来源的酒曲进行筛选和分离得到46株细菌和54株真菌,真菌主要为酵母属(Saccharomyces)、毕赤酵母属(Pichia)及根霉属(Rhizopus)等。这些研究均表明米酒曲中存在丰富的微生物群落。米酒曲的质量与地理和气候等息息相关,不同地区的酒曲中微生物可能存在差异,然而对于不同地区米酒曲真菌多样性比较的研究较少。
作为发酵食品微生物多样性解析强有力的手段之一,Illumina MiSeq高通量测序技术具有通量高和价格相对较低的优点,已被广泛应用于腐乳[12-13]、白酒[14]、泡菜[15]以及酸汤[16]等发酵制品的微生物类群分析中。本研究以采集自广西壮族自治区南宁市和湖北省孝感市的米酒曲为研究对象,采用Illumina MiSeq高通量测序技术对米酒曲中真菌多样性进行解析,以期为酒曲的复配和改善米酒品质提供数据支撑与理论依据。
1 材料与方法
1.1 材料与试剂
脱氧核糖核酸(deoxyribonucleic acid,DNA)基因组提取试剂盒:德国QIAGEN公司;10×聚合酶链式反应(poly merase chain reaction,PCR)缓冲液、脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTPs)Mix:宝生物工程(大连)有限公司;引物ITS4R/ITS3F:武汉天一辉远生物科技有限公司。
1.2 仪器与设备
ND-2000C微量紫外分光光度计:美国NanoDrop公司;Veriti 96孔梯度PCR仪:美国ABI公司;CR21N高速冷冻离心机:日本HITACHI公司;Fluor Chem FC3化学发光凝胶成像系统:美国ProteinSimple公司;Illumina MiSeq高通量测序平台:美国Illumina公司。
1.3 方法
1.3.1 样本采集
南宁米酒曲:采集自广西壮族自治区南宁市(107°45′~108°51′E,22°13′~22°32′N);孝感米酒曲:采集自湖北省孝感市(113°19′~114°35′E,30°23′~31°52′N)。每个地区采集米酒曲样本10个,合计采集20个。所有米酒曲均以糯米为原料且添加5%母曲自然发酵而成,均不添加辣蓼草等中草药,均无虫眼,形状均为圆形,无异味、无霉斑且储藏时间在2~4个月之间,均为家庭自制成品。
1.3.2 Illumina高通量测序
按照DNA提取试剂盒中的方法对研磨碎的米酒曲样本进行宏基因组DNA提取,以其为模板,使用引物ITS3F(5'-GCATCGATGAAGAACGCAGC-3')/ITS4R(5'-TCCTCCGCTTATTGATATGC-3')参照文献[17]中的方法对真菌引物内转录间隔区(internal transcribed spacer,ITS)2区基因序列进行PCR扩增。将合格的PCR扩增产物送至上海美吉生物医药科技有限公司进行Illumina MiSeq高通量测序。
1.3.3 生物信息学分析
首先对序列进行拼接和质控[18]。使用QIIME(V1.9.1)分析平台对质控后的序列进行分析[19-20],利用PyNAST软件[21]将序列标准化和对齐,接着使用两步UCLUST法构建操作分类单元(operational taxonomic units,OTU)矩阵[22],然后对每个OTU的代表性序列使用UNITE数据库进行同源性比对[23],以97%和100%的相似度进行OTU划分,将所有样本中都存在的某一OTU定义为核心OTU。对同一测序深度下的4种α多样性指数(香农指数、辛普森指数、超1指数、发现物种数)进行分析,同时基于UniFrac距离[24]使用主坐标分析(principal co-ordinates analysis,PCoA)对2个地区米酒曲的真菌类群进行β多样性解析。
1.3.4 数据处理
使用曼-惠特尼秩和检验(Mann-Whitney)和多元方差分析(multivariate analysis of variance,MANOVA)对2个地区米酒曲的差异性进行分析;采用Excel 2016进行数据处理;采用在线网页(https://www.omicstudio.cn/tool/24)绘制主成分分析(principal component analysis,PCA)图;利用R软件(V4.0.3)的waterfall软件包绘制瀑布图;使用Origin 8.5绘制其他图。实验均重复3次,结果以“平均值±标准差”的形式表示。
2 结果与分析
2.1 不同地区米酒曲真菌类群α多样性的比较分析
采用Illumina高通量测序技术分别对南宁和孝感地区20个米酒曲样本进行测序,共得到高质量序列1 072 821条,平均每个样本53 641条。当测序深度为23 010条序列时,采用Mann-Whitney检验对2个地区米酒曲样本的α多样性指数(香农指数、辛普森指数、超1指数、发现物种数)进行显著性分析,结果见图1。
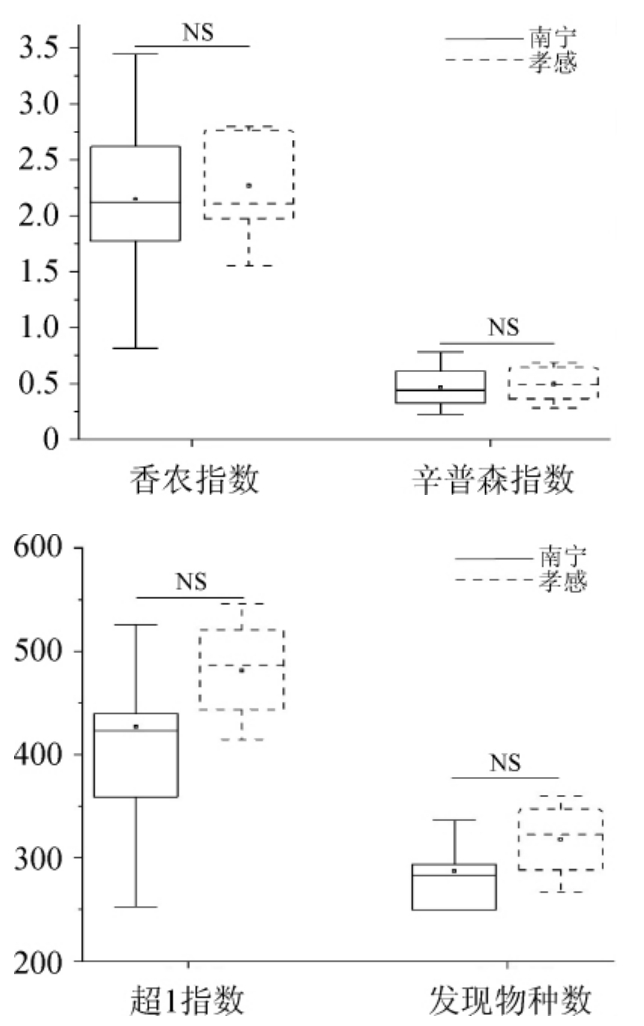
图1 不同地区米酒曲真菌菌群的α多样性指数比较分析结果
Fig.1 Comparative analysis results of α diversity indexes of fungi community in rice-wine Jiuqu from different regions
NS表示无统计学差异(P>0.05)。
由图1可知,2个地区米酒曲样本的α多样性指数差异均不显著(P>0.05)。由此说明,2个地区米酒曲真菌的丰富度和物种多样性并无显著性差异。
2.2 基于OTU水平不同地区米酒曲真菌类群的分析
以97%和100%的相似度进行OTU划分后,共得到1 648个OTU,南宁米酒曲样本划分得到(379±189)个OTU,孝感米酒曲样本划分得到(428±37)个OTU,各OTU出现次数统计结果见图2。
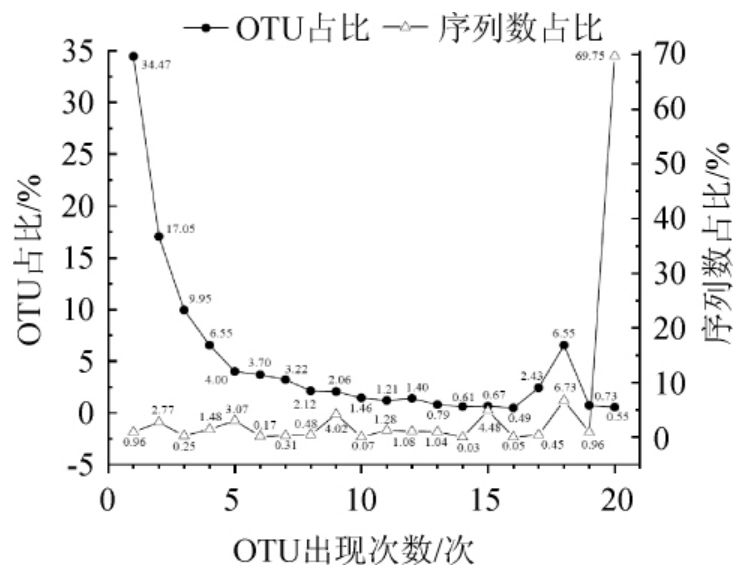
图2 OTU出现次数统计分析结果
Fig.2 Statistical analysis results of OTU occurrence number
由图2可知,各样本中的OTU分布不尽相同,随着OTU出现次数的增加,其所含OTU数占总OTU数的比例整体上呈现逐渐下降的趋势,而所含序列数占总序列数的比例则呈现相反的趋势。由图2亦可知,出现20次的OTU占总OTU数的比例仅为0.55%,而其所含序列数占到总序列数的69.75%,这说明不同地区米酒曲样本共有大量相同的真菌菌群,虽然各样品特有真菌类群的物种数较多但其在各样本的含量少。值得一提的是,1 648个OTU中核心OTU仅有9个,其相对含量瀑布图见图3。
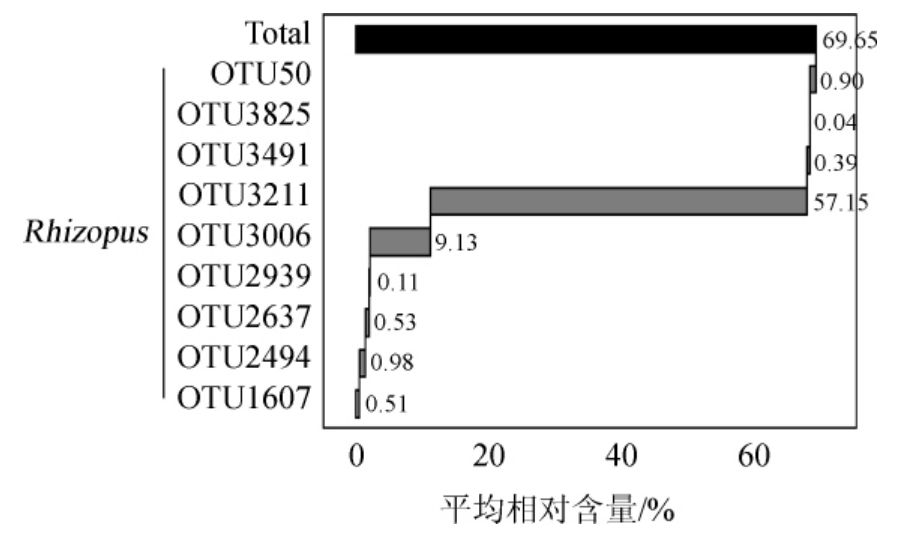
图3 核心OTU相对含量的瀑布图
Fig.3 Waterfall plot of relative content of core OTU
由图3可知,核心OTU及其平均相对含量分别为OTU50(0.90%)、OTU3825(0.04%)、OTU3491(0.39%)、OTU3211(57.15%)、OTU3006(9.13%)、OTU2939(0.11%)、OTU2637(0.53%)、OTU494(0.98%)和OTU21607(0.51%),这9个OTU均隶属于根霉属(Rhizopus),这也进一步说明Rhizopus是2个地区米酒曲中的优势真菌属。
2.3 不同地区米酒曲真菌类群β多样性的比较分析
采用基于加权和非加权的UniFrac距离对2个地区米酒曲中真菌类群的β多样性进行解析,结果见图4。
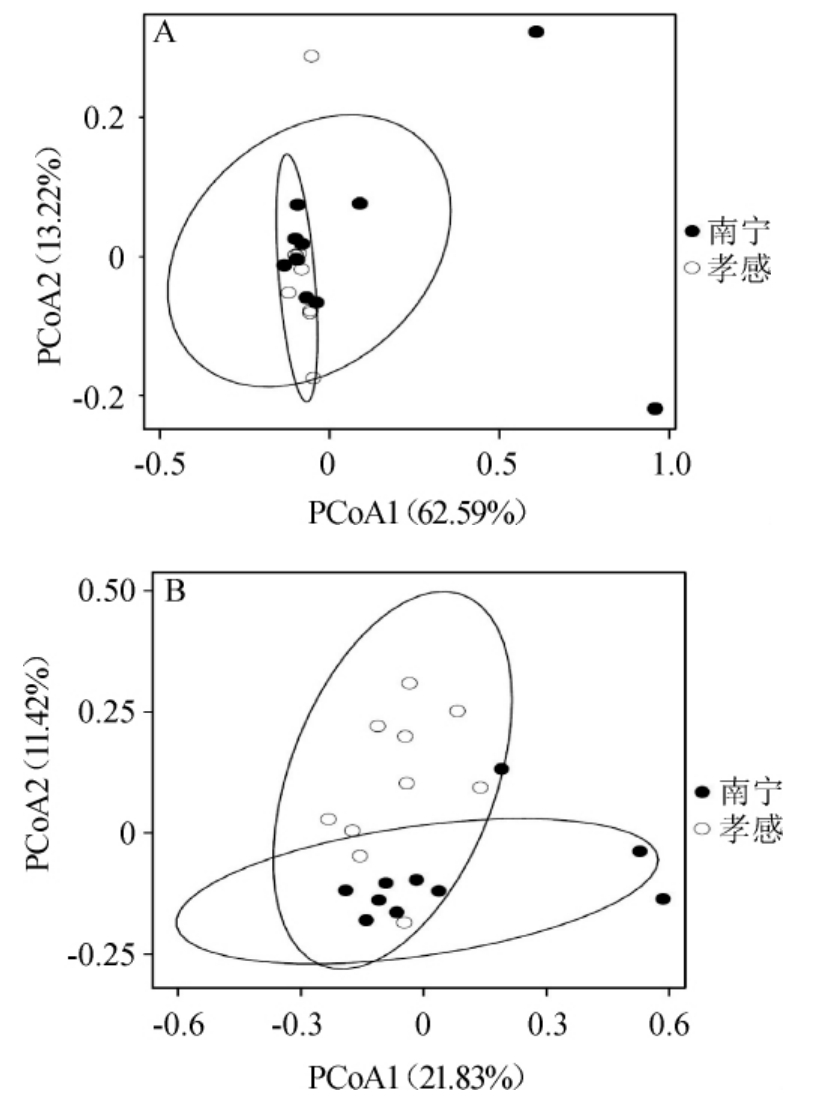
图4 基于加权距离(A)和非加权距离(B)的主坐标分析
Fig.4 Principal coordinate analysis based on weighted distance (A)and unweighted distance (B)
由图4A可知,在考虑物种丰度的情况下,2个地区的米酒曲在空间排布上交叠明显,且经多元方差分析发现,2个地区米酒曲真菌群落结构差异不显著(P>0.05)。由图4B可知,在仅考虑真菌种类而不考虑其丰度的情况下,2个地区的米酒曲在空间排布上较分散,其中南宁地区的样本主要位于Y轴负方向,而孝感地区样本主要位于Y轴正方向,且经多元方差分析发现,2个地区米酒曲真菌群落结构差异显著(P<0.05)。由此说明,2个地区米酒曲真菌类群的差异可能主要体现在一些低丰度的OTU上。
2.4 不同地区米酒曲真菌菌群结构分析
在门和属水平上,南宁地区米酒曲中的真菌类群可被鉴定为5个门和63个属,孝感地区米酒曲可被鉴定为4个门和23个属,不同地区米酒曲的真菌菌群结构见图5。
由图5A可知,毛霉菌门(Mucoromycota)在南宁和孝感地区米酒曲中的平均相对含量分别为78.58%和91.90%,子囊菌门(Ascomycota)的平均相对含量分别为21.18%和8.08%。由此可见,Mucoromycota和Ascomycota为2个地区米酒曲中的优势真菌门,经Mann-Whitney检验发现其在南宁、孝感地区米酒曲中的平均相对含量差异显著(P<0.05)。
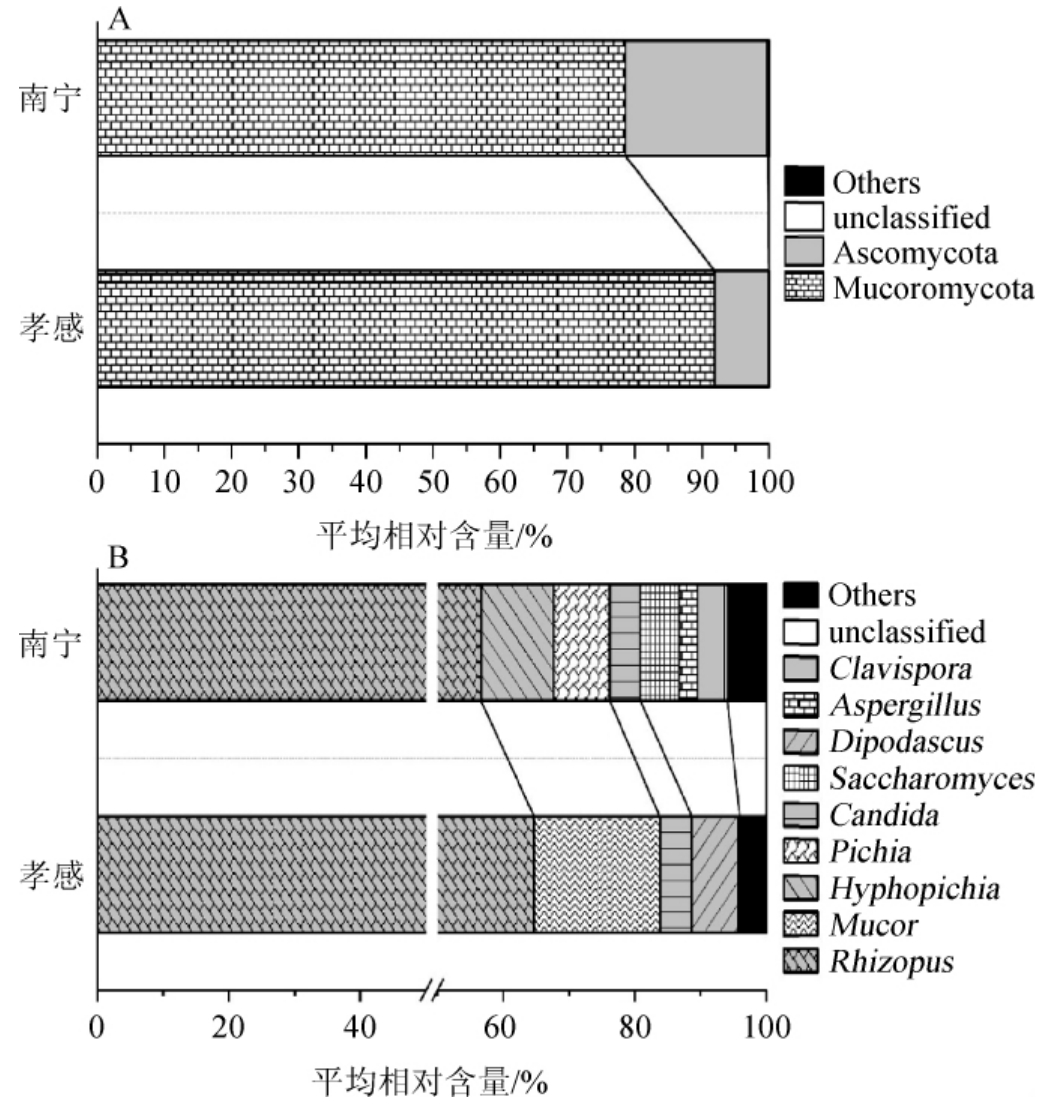
图5 基于门(A)和属(B)水平南宁和孝感地区米酒曲的真菌群落结构
Fig.5 Fungal community structure of rice-wine Jiuqu from Nanning and Xiaogan based on phylum (A) and genus (B) level
Others:平均相对含量<1%的真菌。
由图5B可知,南宁地区米酒曲中的优势真菌属分别为根霉属(Rhizopus)(78.29%)、丝孢毕赤酵母属(Hyphopichia)(5.52%)、毕赤酵母属(Pichia)(4.27%)、酵母菌属(Saccharomyces)(2.95%)、假丝酵母属(Candida)(2.33%)、枝包酵母属(Clavispora)(2.06%)和曲霉属(Aspergillus)(1.40%);而孝感地区米酒曲中的优势真菌属分别为Rhizopus(82.32%)、毛霉属(Mucor)(9.58%)、双足囊菌属(Dipodascus)(3.53%)和Candida(2.45%)。由此可见,2个地区的米酒曲优势真菌属均以Rhizopus为主,这与图3结果一致。已有研究结果表明,Rhizopus是米酒曲中最主要的微生物,不仅具有较强的糖化能力、酒化能力同时还能产生各种有机酸,可显著影响米酒的风味和质量[25]。周金虎等[26]从4种甜酒曲中筛选出了一株高产淀粉酶的米根霉(Rhizopus oryzae);姚淑敏等[27]对湖南韶山、湘潭和祁东、福建福州以及浙江丽水和兰溪6种甜酒曲进行真菌多样性分析亦发现,样本主要真菌类群均包含Rhizopus。
经Mann-Whitney检验发现,Aspergillus在南宁地区米酒曲中的平均相对含量显著偏高(P<0.05),而Mucor在孝感地区米酒曲中的平均相对含量显著偏高(P<0.01)。由此可见,2个地区的米酒曲真菌类群存在一定差异。王丹丹等[28]对孝感凤窝米酒曲的真菌多样性研究发现,孝感凤窝米酒曲中优势真菌为淀粉霉属(Amylomyces)、小克银汉霉属(Cunninghamella)、毛霉属(Mucor)、Saccharomycopsis、Aspergillus、Candida、拟威尔酵母属(Cyberlindnera)和接合酵母属(Zygosaccharomyces)。由此可见,不同地区的米酒曲其真菌类群可能存在一定的差异。
3 结论
本研究通过Illumina MiSeq高通量测序技术对广西省南宁地区和湖北省孝感地区米酒曲真菌类群的多样性进行分析比较,结果表明,2个地区米酒曲真菌丰富度和物种多样性均无显著性差异(P>0.05),米酒曲中共有9个核心OTU,所含序列数占总序列数的69.75%,经鉴定均隶属于根霉属(Rhizopus)。2个地区米酒曲的优势真菌门均为毛霉菌门(Mucoromycota)和子囊菌门(Ascomycota),优势真菌属均以Rhizopus为主,真菌类群的差异可能主要体现在一些低丰度的OTU上。
[1]张洋洋,张伟国,徐建中,等.米酒液态发酵过程中理化指标和风味物质变化规律[J].东北农业大学学报,2020,51(12):79-89.
[2]王婉君,赵立艳,汤静.新型米酒产品研究与开发进展[J].中国酿造,2018,37(5):1-4.
[3]温承坤,陈孝,王奕芳,等.米酒功能性成分研究进展[J].中国酿造,2019,38(12):5-8.
[4]吴轩德.筛选多菌种发酵提升米酒特征香气物质含量的研究[D].广州:华南理工大学,2018.
[5]宁亚丽,吴跃,何嫱,等.基于高通量测序技术分析朝鲜族传统米酒及其酒曲中微生物群落多样性[J].食品科学,2019,40(16):107-114.
[6]王菲,钟小丹,戴彩霞,等.原料米和酒曲对米酒滋味品质影响的评价[J].食品研究与开发,2017,38(20):80-84.
[7]李泽洋,伍时华,龙秀锋,等.米酒糖化菌的分离筛选鉴定及其性能研究[J].食品与发酵工业,2021,47(4):188-194.
[8]任丽霞.甜酒曲微生物群落结构分析及八二曲的改良研究[D].上海:上海应用技术大学,2020.
[9]向凡舒,朱媛媛,邓风,等.建始地区米酒曲细菌和真菌多样性研究[J].食品工业科技,2021,42(1):126-131.
[10]杨春敏,黄建初,查丽艳.海南山兰米酒酒曲微生物多样性分析[J].食品工程,2019,26(4):44-48.
[11]蔡海莺,张婷,沈灵智,等.甜米酒酒曲微生物分离和菌种鉴定[J].食品研究与开发,2019,40(24):204-210.
[12]WAN H,LIU T,SU C,et al.Evaluation of bacterial and fungal communities during the fermentation of Baixi sufu,a traditional spicy fermented bean curd[J].J Sci Food Agr,2020,100(4):1448-1457.
[13]石黎琳,牟方婷,李安,等.基于高通量测序技术分析腐乳自然发酵过程微生物多样性[J].中国酿造,2021,40(2):144-149.
[14]胡晓龙,余苗,王康丽,等.浓香型白酒窖泥微生物群落多样性及理化因素对其影响[J].食品研究与开发,2021,42(2):178-185.
[15] TANG Y,ZHOU X,HUANG S,et al.Microbial community analysis of different qualities of pickled radishes by Illumina MiSeq sequencing[J]. J Food Safety,2019,39(2):e12596.
[16]肖甜甜,冯子娟,邱树毅,等.苗家白酸汤中微生物群落多样性研究及其优势微生物的筛选[J].食品与发酵科技,2021,57(1):1-11.
[17]陈怡,刘洋,蒋立文,等.基于高通量测序分析不同浏阳豆豉中真菌的多样性[J].中国酿造,2020,39(11):66-70.
[18]GUO Z,WANG Y,XIANG F,et al.Bacterial diversity in pickled cowpea(Vigna unguiculata[Linn.]Walp)as determined by Illumina MiSeq sequencing and culture-dependent methods[J].Curr Microbiol,2021,78(2):1286-1297.
[19] DU R,GE J,ZHAO D,et al.Bacterial diversity and community structure duringfermentationofChinesesauerkrautwith Lactobacilluscasei 11MZ-5-1 by Illumina Miseq sequencing[J].Lett Appl Microbiol,2018,66(1):55-62.
[20]CAPORASO J G,KUCZYNSKI J,STOMBAUGH J,et al.QIIME allows analysis of high-throughput community sequencing data[J].Nat Methods,2010,7(5):335-336.
[21] CAPORASO J G,BITTINGER K,BUSHMAN F D,et al.PyNAST:Aflexible tool for aligning sequences to a template alignment[J]. Bioinformatics,2010,26(2):266-267.
[22]CALLAHAN B J,MCMURDIE P J,HOLMES S P.Exact sequence variants should replace operational taxonomic units in marker-gene data analysis[J].ISME J,2017,11(12):2639.
[23]KÕLJALG U,LARSSON K H,ABARENKOV K,et al.UNITE:a database providing web-based methods for the molecular identification of ectomycorrhizal fungi[J].New Phytol,2005,166(3):1063-1068.
[24]LOZUPONE C,LLADSER M E,KNIGHTS D,et al.UniFrac:an effective distance metric for microbial community comparison[J]. ISME J,2011,5(2):169-172.
[25]康宪.传统桂林甜酒曲微生物协同作用及应用研究[D].广州:华南农业大学,2016.
[26]周金虎,陈茂彬,毛志海,等.甜酒曲中一株高产淀粉酶根霉的筛选与鉴定[J].酿酒科技,2019(1):37-40.
[27]姚淑敏,陈璐,闫华文.应用PCR-DGGE 方法研究甜酒曲中真菌多样性[J].中国酿造,2016,35(11):44-48.
[28]王丹丹,沈馨,董蕴,等.孝感凤窝酒曲真菌多样性评价[J].中国酿造,2017,36(11):38-42.