白酒根据香型主要分为12种,清香型白酒是其中的一种,以山西汾酒为代表。白酒不仅历史文化悠久,同时其独特的生产发酵工艺还赋予了白酒以酯类为主体的复合香味[1-2]。清香型白酒的主体香味物质是乙酸乙酯和乳酸乙酯,主要合成途径分别是酵母菌代谢与酸和醇在酯化酶作用下的化学合成,这两种途径都需要微生物的参与[3]。清香型白酒发酵阶段包括大茬发酵和二茬发酵两个阶段[4],不同发酵阶段的发酵工艺均存在差异。因此,不同发酵条件下酒醅中微生物群落结构存在差异,对酒的品质也会造成一定的影响。
高通量测序(high-throughput sequencing,HTS)技术具有成本低、通量高和结果准确的优势[5],广泛应用于渣豆酱[6]、豆豉[7]、大头菜[8]、酸奶[9]以及各种香型白酒[10-12]发酵基质的微生物类群解析。陈雪等[13]对陕西凤香型白酒发酵过程中的微生物群落结构进行研究发现,发酵过程中共检测出216个属,其中细菌属183个、真菌属33个,酒醅中微生物真菌以Naumovozyma、根霉属(Rhizopus)、热子囊菌属(Thermoascus)、曲霉属(Aspergillus)、假丝酵母属(Canndida)、Pseudeurotium、复膜孢酵母属(Saccharomycopsis)、毕赤酵母属(Pichia)和酵母属(Saccharomyces)为主,细菌以乳杆菌属(Lactobacillus)、芽孢杆菌属(Bacillus)、片球菌属(Pediococcus)和链霉菌属(Streptomyces)为主;张双燕等[14]对北京某清香型酒厂大曲中微生物多样性进行研究发现,细菌中优势菌是乳酸菌,真菌中优势菌属是Canndida、Aspergillus、毛霉属(Mucor)、维克汉姆酵母属(Wickerhamomyces)等;雷振河[15]分析了山西清香型白酒大曲及酒醅中微生物多样性,结果发现大曲中优势真核微生物主要包括Aspergillus、Thermoascus、Rhizopus、嗜热真菌属(Thermomyces)和Canndida;酒醅中真菌主要包括Canndida和Pichia。这些研究均表明不同地区清香型白酒酿造微生物类群存在一定的差异,加之生态环境和制作工艺存在差异,其生产的白酒品质与风格也会有所差别。
本研究采用Illumina MiSeq高通量测序技术对湖北省石花酿酒股份有限公司的清香型白酒大茬和二茬酒醅中真菌多样性及群落结构进行比较分析,以期更加全面地了解大茬和二茬酒醅中真菌类群,为湖北襄阳地区酿酒微生物资源挖掘和后续白酒的发酵调控提供一定理论参考依据。
1 材料与方法
1.1 材料与试剂
1.1.1 样品
酒醅:湖北省石花酿酒股份有限公司酿造车间。以高粱为主要原料,经粉碎、高温润糁、糊化和出甑加浆后,按照粮食干质量的10%接入低温大曲,入缸发酵28 d,此时所取样品即为大茬酒醅。大茬酒醅出缸拌辅料装甑蒸馏后,加入等质量低温大曲入缸发酵21 d,此时所取样品即为二茬酒醅。
1.1.2 试剂
脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:德国QIAGEN公司;Fast Pfu Buffer、Fast Pfu Fly DNA聚合酶(酶活5 U/μL)、脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTPs)Mix、5×TransStartTM:北京全式金生物技术有限公司;引物ITS4R/ITS3F、6×Loading Buffer:武汉天一辉远生物科技有限公司。
1.2 仪器与设备
Veriti 96孔梯度聚合酶链式反应(polymerase chain reaction,PCR)仪:美国ABI公司;ND-2000C微量紫外分光光度计:美国Nano Drop公司;Fluor Chem FC3型化学发光凝胶成像系统:美国Protein Simple公司;Illumina MiSeq高通量测序平台:美国Illumina公司;CR21N高速冷冻离心机:日本HITACHI公司。
1.3 实验方法
1.3.1 样品采集
于湖北省石花酿酒股份有限公司酿造车间选取20个地缸,其中10个为大茬发酵缸,10个为二茬发酵缸,地缸深度均为1.2 m,使用土壤采样器深入酒醅表面约0.6 m处取样品约500 g,将大茬酒醅样品依次编号为DC1~DC10,二茬酒醅样品依次编号为EC1~EC10。
1.3.2 宏基因组DNA提取、PCR扩增及Illumina MiSeq高通量测序
参照试剂盒方法提取酒醅的宏基因组DNA,以其为模板,采用引物ITS4R(5'-TCCTCCGCTTATTGATATGC-3')和ITS3F(5'-GCATCGATGAAGAACGCAGC-3')对酒醅中真菌的内部转录间隔区(internal transcribed spacer,ITS)2区基因序列进行PCR扩增,PCR扩增体系及扩增条件参照文献[16]。采用1%琼脂糖凝胶电泳对PCR扩增产物进行检测,将检验合格的PCR扩增产物送至上海美吉生物医药科技有限公司进行Illumina MiSeq高通量测序。
1.3.3 序列质控和生物信息学分析
参照文献[17]中的方法进行质控,使用QIIME(version 1.9.1)分析平台[18]对质控后的序列进行分析。采用PyNAST[19]软件将序列对齐,按97%和100%相似性构建操作分类单元(operational taxonomic units,OTU)矩阵[20],然后对每个OTU的代表性序列利用UNITE数据库进行同源性比对[21]。
1.3.4 多元统计分析及图表绘制
本研究对最小测序深度下的发现物种数和香农指数等α多样性指标进行分析,同时基于UniFrac距离[22]使用主坐标分析(principal co-ordinates analysis,PCoA)对2种酒醅的真菌类群进行β多样性分析。使用曼-惠特尼秩和(Mann-Whitney)检验对单个指标在2种酒醅中的差异性进行分析,使用多元方差分析(multivariate analysis of variance,MANOVA)对2种酒醅样品真菌群落结构的差异性进行分析。使用Excel 2016进行数据处理,使用R软件(v3.6.3)的Ggpubr和ggplot2软件包绘制小提琴图,使用Ggplot2和Reshape2软件包绘制气泡图,使用Waterfall软件包绘制瀑布图,使用Origin 8.5绘制其他图,部分数据采用“平均值±标准差”形式进行展示。
2 结果与分析
2.1 大茬及二茬酒醅样品间α多样性分析
本研究采用Illumina MiSeq高通量测序技术对20个酒醅样品检测共产生988 381条有效序列,平均每个样品的有效序列为49 419条。在97%的相似度下,10个大茬酒醅样品划分了(2 297±197)个OTU,10个二茬酒醅样品划分了(1 828±398)个OTU。使用小提琴图对2种酒醅样品的α多样性进行比较分析,结果见图1。
物种多样性指数和香农指数分别用来评估样本中微生物的丰度和多样性[23]。由图1可知,当测序深度达到34 010条序列时,大茬和二茬酒醅真菌类群发现物种数分别为(1 796±115)种和(1 497±107)种,香农指数分别为4.97±0.50和3.70±0.27,经Mann-Whitney检验发现两者差异均极显著(P<0.001),这说明大茬酒醅中真菌的丰富度和多样性均高于二茬酒醅。
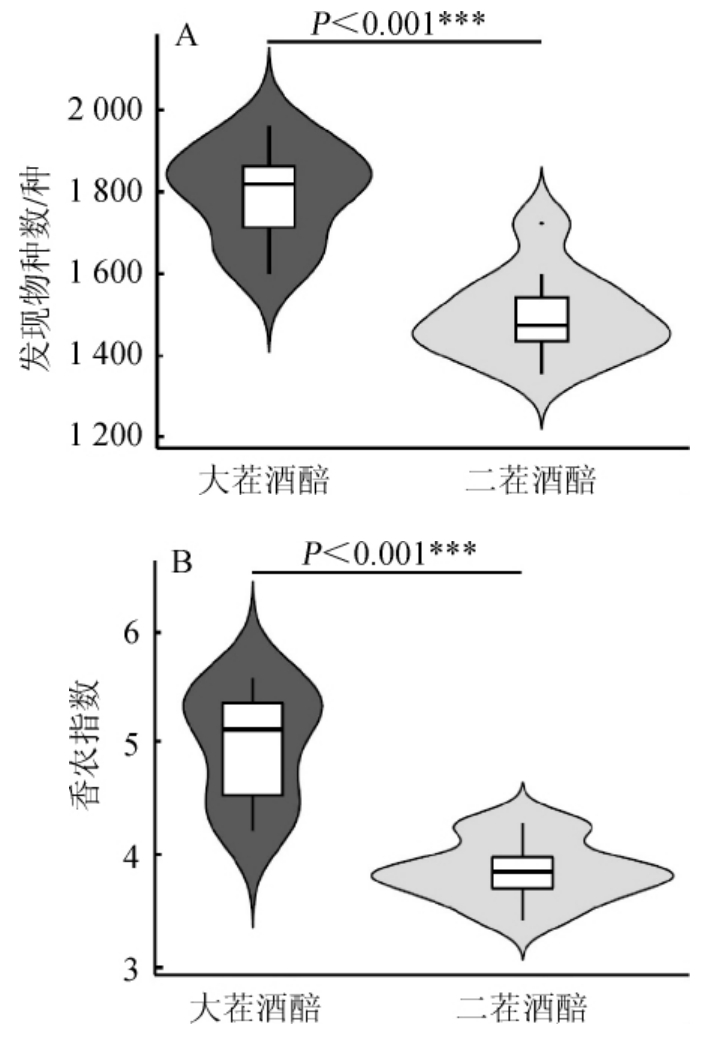
图1 酒醅样品发现物种数(A)和香农指数(B)比较的小提琴图
Fig.1 Violin diagram of comparison of observed species number (A)and Shannon index (B) of fermented grains samples
“***”表示差异极显著(P<0.001)。下同。
2.2 大茬及二茬酒醅样品间β多样性分析
β多样性可反映不同环境中物种组成的相异性或物种沿环境梯度的更替速率[29]。基于UniFrac距离的加权和非加权主坐标分析对20个酒醅样品进行空间排布,结果见图2。
由图2A可知,将真菌相对含量和遗传进化关系均纳入分析范畴时,第一主成分和第二主成分的累计方差贡献率高达95.02%,大茬酒醅样本分布在第一、三和四象限,二茬酒醅样本集中分布在第二象限,2种样本间无交叠现象。由图2B可知,在仅考虑真菌类群遗传进化关系而不考虑各真菌相对含量时,第一主成分的方差贡献率为17.24%,第二主成分的方差贡献率为5.83%,大茬酒醅样本分布在第二和第三象限,二茬酒醅样本分布在第一和第四象限。由此可定性认为2种酒醅样本间真菌群落存在较大差异,且大茬酒醅真菌类群的组间差异要大于二茬酒醅。本研究进一步采用欧式距离对2种酒醅群落结构组内差异进行计算,结果见图3。
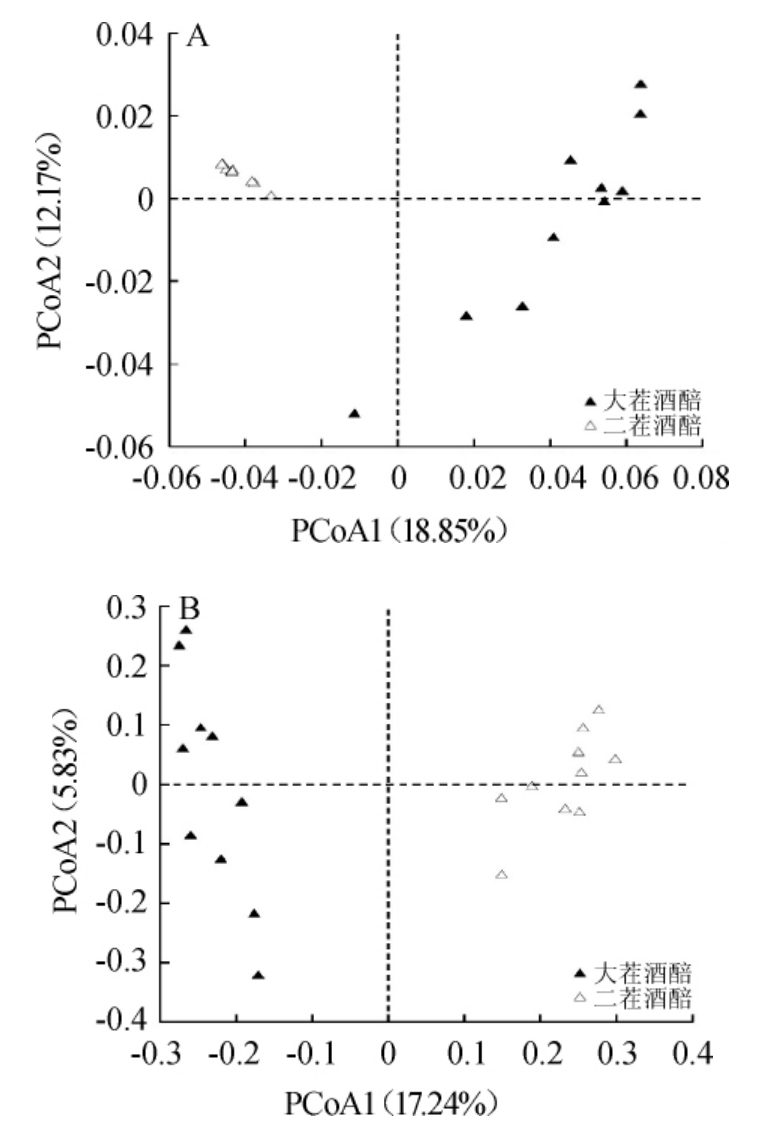
图2 基于加权(A)和非加权(B)的UniFrac距离酒醅样品的主坐标分析
Fig.2 Principal coordinate analysis of fermented grains samples based on weighted (A) and unweighted (B) UniFrac distance
由图3可知,大茬酒醅组内各样本间的欧式距离为0.044±0.010,而二茬酒醅组内各样本间的欧式距离为0.010±0.002,这可定量证明大茬酒醅样本组内差异性要比二茬酒醅样本大。采用MANOVA检验亦发现,大茬酒醅样品和二茬酒醅样品真菌群落结构整体上存在极显著差异(P<0.001),这与主坐标分析结果一致。
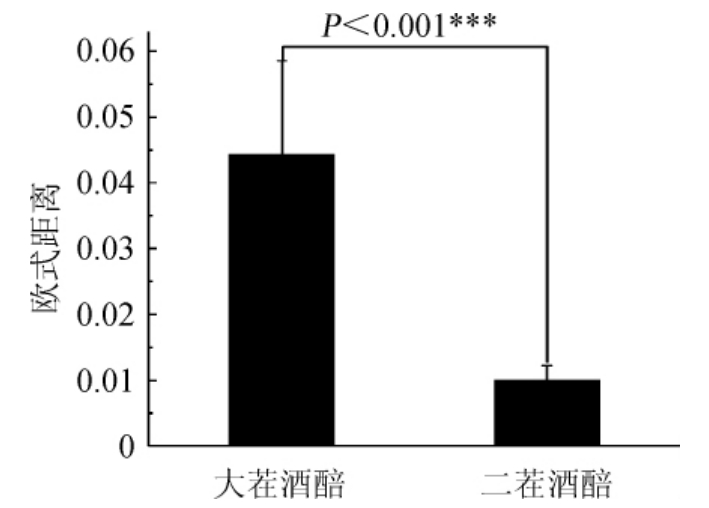
图3 基于欧式距离酒醅样品真菌群落结构组间差异分析
Fig.3 Analysis of between-group differences in fungal community structure of fermented grains samples based on Euclidean distance
2.3 基于OTU水平酒醅样品真菌类群分析
经两步UCLUST划分共得到17 543个OTU,将所有样品中都存在的某一OTU定义为核心OTU。对样品中OTU出现次数和核心OTU相对含量进行分析,结果见图4。
由图4A可知,本研究中核心OTU共有134个,仅占总OTU数的0.76%,包含序列数856 136条,占总序列的86.62%。由此可见,大茬酒醅和二茬酒醅样品中共有大量的核心OTU真菌类群。由图4B可知,平均相对含量>1.00%的核心OTU有6个,包含序列数占总序列数的68.85%,但OTU数仅占总OTU数的0.03%,分别为OTU6804(17.41%)、OTU4028(38.25%)、OTU4343(1.04%)、OTU1926(1.01%)、OTU1903(1.01%)和OTU12648(10.13%),其中OTU6804隶属于热子囊菌属(Thermoascus),OTU4028和OTU4343隶属于酵母属(Saccharomyces),OTU1926隶属于曲霉属(Aspergillus),OTU1903隶属于汉逊酵母属(Hanseniaspora),OTU12648隶属于覆膜孢酵母属(Saccharomycopsis),由此可见Saccharomyces、Thermoascus、Aspergillus、Hanseniaspora 和Saccharomycopsis是襄阳地区清香型白酒酒醅中的优势真菌。值得一提的是,有23个OTU仅存在于大茬酒醅样品中,有1个OTU仅存在于二茬酒醅样品中,其累计包含序列占总序列数的比例分别为2.36%和0.04%,其中17个鉴定为散囊菌目(Eurotiales)的分类单元,4个鉴定为酵母菌目(Saccharomycetales)的分类单元,1个鉴定为散囊菌纲(Eurotiomycetes)的分类单元,2个仅能鉴定为Ascomycota的分类单元。
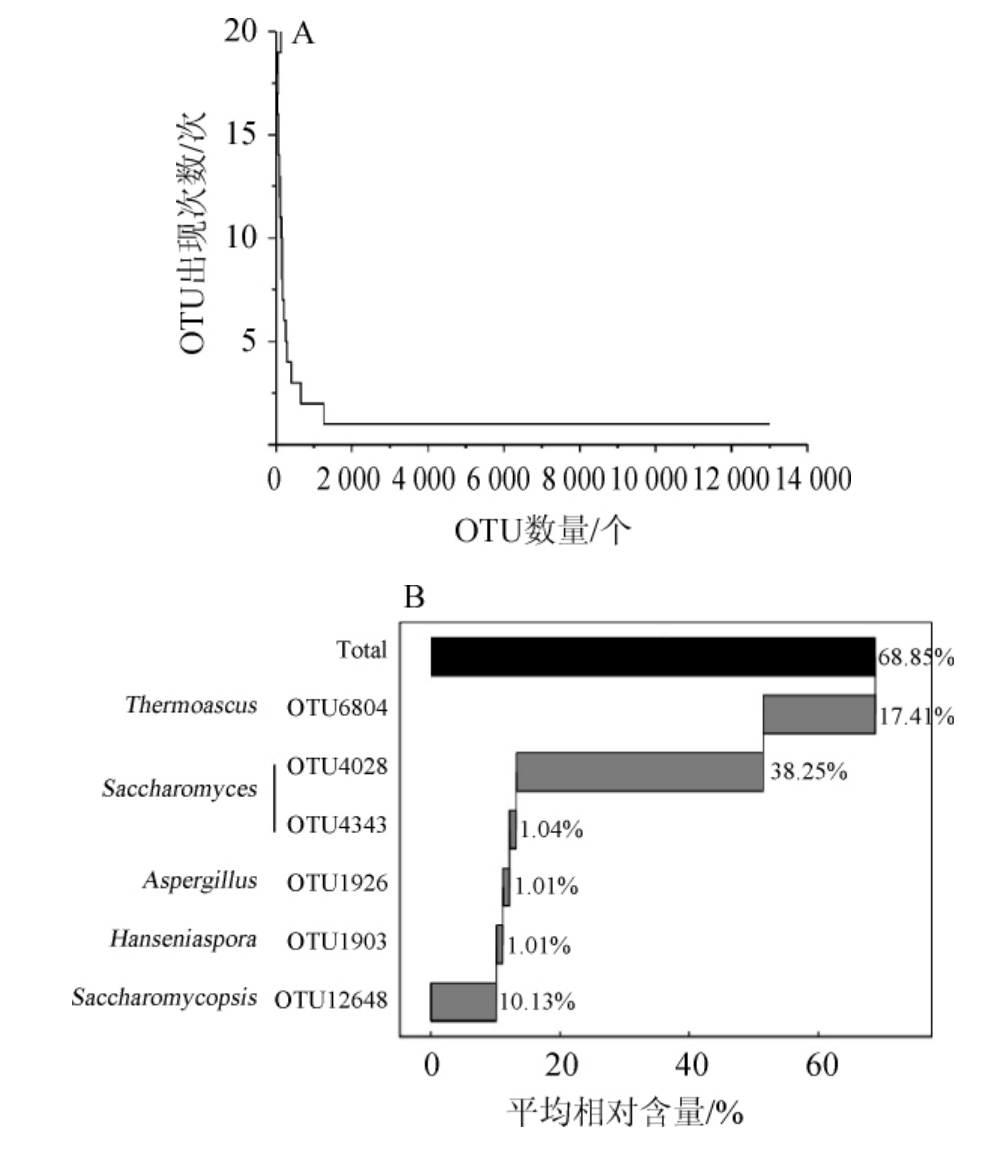
图4 酒醅样品OTUs出现次数阶梯图(A)和核心OTUs相对含量瀑布图(B)
Fig.4 Ladder plot of OTUs occurrence frequency (A) and waterfall plot of the relative content of core OTUs (B) of fermented grains samples
2.4 基于门和属分类学地位酒醅样品的真菌类群分析
将平均相对含量>1.00%的真菌门或属定义为优势真菌门或属,将平均相对含量<1.00%的门或属归并为“others”,将不能鉴定到门或者属水平的序列归并为“unclassified”。本研究中鉴定的真菌类群为3个门和32个属,其中优势门仅1个,优势属有5个。基于门和属水平的2种酒醅真菌类群的分析结果见图5。
由图5A可知,大茬酒醅和二茬酒醅的优势真菌门均为子囊菌门(Ascomycota),平均相对含量分别为99.82%和99.97%。经Mann-Whitney检验发现,采集的2种酒醅样品在门水平上差异均不显著(P>0.05)。有研究表明,子囊菌门不仅是清香型酒醅中优势真菌种群[24],同样也是浓香型[25]、酱香型白酒[26]及多种发酵食品中的主要真菌种群。
由图5B可知,大茬酒醅中平均相对含量>1.00%的真菌属分别为Thermoascus(33.77%)、Saccharomycopsis(22.60%)、Saccharomyces(13.51%)、Leiothecium(9.34%)、Aspergillus(4.19%)和Hanseniaspora(1.62%),二茬酒醅中为Saccharomyces(84.64%)、Saccharomycopsis(1.42%)和Thermoascus(1.30%)。经Mann-Whitney检验发现,2种酒醅样品中优势真菌属含量均呈现极显著差异(P<0.001)。由图5B亦可知,Thermoascus和Saccharomycopsis平均相对含量在大茬酒醅中显著偏高(P<0.01),而Saccharomyces平均相对含量在二茬酒醅中显著偏高(P<0.01)。襄阳地区大茬酒醅和二茬酒醅样品真菌类群存在较大差异的原因,可能与原料和制作工艺的不同有关[27]。
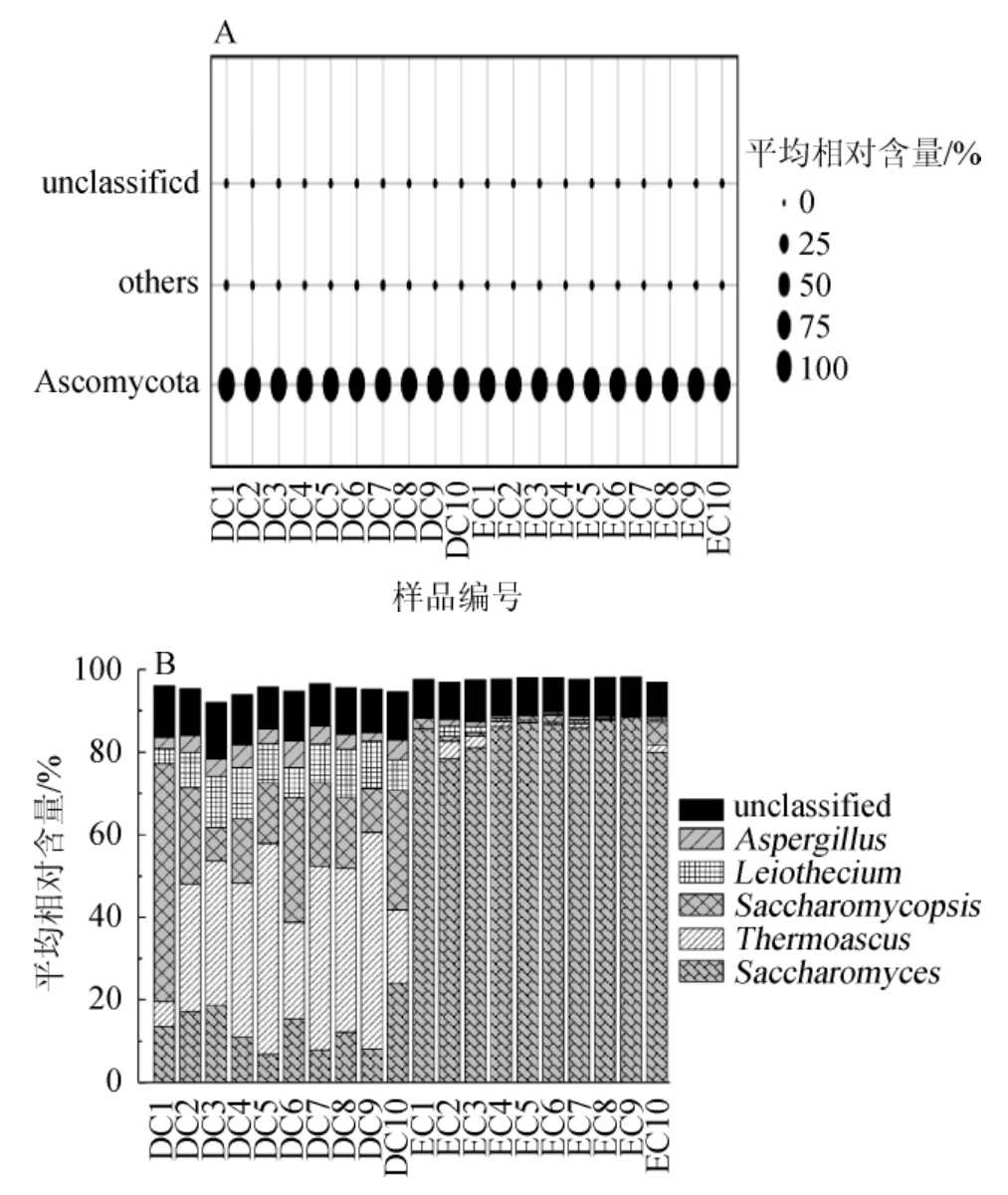
图5 基于门(A)和属(B)分类学地位酒醅样品的真菌类群分析
Fig.5 Fungal community analysis of fermented grains samples based on the taxonomic status of phylum (A) and genus (B)
大茬酒醅和二茬酒醅的发酵周期一般为21~28 d,大茬酒醅发酵温度遵循“前缓升、中挺、后缓落”的原则,由于二茬酒醅酸度较大,发酵温度和大茬酒醅有所差别,一般遵循“前紧、中挺、后缓落”的原则。有研究表明,霉菌是具有糖化力的主要微生物,使酒曲具有发酵和生香的特殊香味[28]。贾丽艳等[29]研究了山西杏花村汾酒大茬酒醅和二茬酒醅发酵过程中的真菌群落结构,结果发现在发酵过程中真菌的种类和数量随着发酵时间和环境的影响而变化,其中大茬酒醅发酵过程中Saccharomycopsis、Saccharomyces和Candida为优势种群,二茬酒醅中Saccharomycopsis、Hanseniaspora、青霉属(Penicillium)、Aspergillus、范氏酵母属(Vanderwaltozyma)和有孢圆酵母属(Torulaspora)为主要优势菌群,该研究与本研究结果有所差别,可能是由于原料、制作工艺和地域气候环境等综合因素不同造成的。
3 结论
采用Illumina MiSeq高通量测序技术对石花清香型白酒大茬和二茬酒醅中真菌的群落结构和多样性进行分析。结果表明,大茬酒醅的发现物种数和香农指数与OTU数较高,丰富度和多样性均高于二茬酒醅,且2种酒醅真菌类群存在明显的差异。2种酒醅共有大量的核心OTU(134个)。在门水平上,2种酒醅的优势真菌门均为子囊菌门(Ascomycota),平均相对含量分别为99.82%和99.97%。在属水平上,大茬酒醅中优势真菌属为热子囊菌属(Thermoascus)(33.77%)、腹膜孢酵母属(Saccharomycopsis)(22.60%)、酵母属(Saccharomyces)(13.51%)、Leiothecium(9.34%)曲霉菌属(Aspergillus)(4.19%)和汉逊酵母属(Hanseniaspora)(1.62%),二茬酒醅中优势真菌属为(Saccharomyces)(84.64%)、Saccharomycopsis(1.42%)和Thermoascus(1.30%)。由此可见,虽然共有部分真菌类群,但2种酒醅真菌群落结构存在明显的差异。
[1] YIN X,YOSHIZAKI Y,KURAZONO S,et al.Characterization of flavor compounds in rice-flavor baijiu,a traditional Chinese distilled liquor,compared with Japanese distilled liquors,awamori and kome-shochu[J].Food Sci Technol Res,2020,26(3):411-422.
[2]XIE J,TIAN X F,HE S G,et al.Evaluating the intoxicating degree of liquor products with combinations of fusel alcohols,acids,and esters[J].Molecules,2018,23(6):1239.
[3]曹苗文,相里加雄,徐炳璋,等.功能型曲在清香型白酒生产中的应用[J].食品与发酵工业,2020,46(5):134-139.
[4]章克昌.酒精与蒸馏酒工艺学[M].北京:中国轻工业出版社,2017:465-472.
[5] SCHIRMER M,IJAZ U Z,D'AMORE R,et al.Insight into biases and sequencing errors for amplicon sequencing with the Illumina MiSeq platform[J].Nucleic Acids Res,2015,43(6):e37-e37.
[6]向凡舒,张振东,望诗琪,等.基于MiSeq 高通量测序技术渣豆酱微生物类群研究[J].中国酿造,2020,39(9):48-52.
[7]倪慧,王玉荣,尚雪娇,等.龙山地区干豆豉真菌多样性研究[J].食品研究与开发,2020,41(4):27-31.
[8]吴进菊,曾瑞萍,张俊毅,等.高通量测序分析大头菜发酵过程中真菌的多样性[J].食品科学,2020,41(10):75-80.
[9]马才仁卓玛,白玛普赤,次仁潘多,等.高通量测序技术对西藏林芝传统发酵酸奶及酪乳细菌多样性研究[J].中国酿造,2020,39(11):116-119.
[10]ZHENG Q,LIN B,WANG Y,et al.Proteomic and high-throughput analysis of protein expression and microbial diversity of microbes from 30-and 300-year pit muds of Chinese Luzhou-flavor liquor[J].Food Res Int,2015,75(9):305-314.
[11]胡晓龙,王康丽,余苗,等.浓香型酒醅微生物菌群演替规律及其空间异质性[J].食品与发酵工业,2020,46(10):66-73.
[12]罗方雯,黄永光,涂华彬,等.基于高通量测序技术对茅台镇酱香白酒主酿区域酵母菌群结构多样性的解析[J].食品科学,2020,41(20):127-133.
[13]陈雪,张永利,闫宗科,等.凤香型酒醅微生物群落演替及其与理化指标的相关性分析[J].食品科学,2020,41(22):200-205.
[14]张双燕,廖永红,纪南,等.基于高通量测序技术分析北京清香型大曲微生物多样性[J].中国酿造,2016,35(11):49-53.
[15]雷振河.采用高通量测序技术分析清香型白酒酿造微生物[J].食品与发酵工业,2015,41(9):164-167.
[16]陈怡,刘洋,蒋立文,等.基于高通量测序分析不同浏阳豆豉中真菌的多样性[J].中国酿造,2020,39(11):66-70.
[17]王玉荣,杨成聪,葛东颖,等.扩增区域对鲊广椒细菌MiSeq 测序的影响[J].食品科学,2019,40(10):134-140.
[18]CAPORASO J G,KUCZYNSKI J,STOMBAUGH J,et al.QIIME allows analysis of high-throughput community sequencing data[J].Nat Methods,2010,7(5):335.
[19] CAPORASO J G,BITTINGER K,BUSHMAN F D,et al.PyNAST:a flexible tool for aligning sequences to a template alignment[J]. Bioinformatics,2010,26(2):266-267.
[20]CALLAHAN B J,MCMURDIE P J,HOLMES S P.Exact sequence variants should replace operational taxonomic units in marker-gene data analysis[J].ISME J,2017,11(12):2639.
[21]KÕLJALG U,LARSSON K H,ABARENKOV K,et al.UNITE:a database providing web-based methods for the molecular identification of ectomycorrhizal fungi[J].New Phytol,2005,166(3):1063-1068.
[22]LOZUPONE C,LLADSER M E,KNIGHTS D,et al.UniFrac:an effective distance metric for microbial community comparison[J]. ISME J,2011,5(2):169-172.
[23]杨国平,叶敏霞,张荣,等.基于高通量测序的鼠类肠道细菌群落多样性分析[J].中华卫生杀虫药械,2021,27(2):148-153.
[24]LI X R,MA E B,YAN L Z,et al.Bacterial and fungal diversity in the traditional Chinese liquor fermentation process[J]. Int J Food Microbiol,2011,146(1):31-37.
[25]ZHANG W X,QIAO Z W,TANG Y Q,et al.Analysis of the fungal community in zaopei during the production of Chinese Luzhou-flavour liquor[J].J I Brewing,2007,113(1):21-27.
[26] WU Q,CHEN L Q,XU Y.Yeast community associated with the solid state fermentation of traditional Chinese Maotai-flavor liquor[J].Int J Food Microbiol,2013,166(2):323-330.
[27]甄攀.汾酒发酵过程之酒醅化学成分变化规律[J].酿酒,2016,42(1):83-86.
[28]马红玉.清香型白酒酒醅测定及核心真菌特性研究[D].太原:山西大学,2019.
[29]贾丽艳,田宇敏,王晓勇,等.传统清香型白酒发酵过程中真菌群落结构及其动态演替[J].中国食品学报,2020,20(10):303-308.