白酒是我国的传统酒种,以粮谷为主要原料,发酵而成的蒸馏酒,历史悠久,在漫长的发展过程中形成了独特的工艺和种类丰富的风味[1]。白酒酿造过程中所产生的独特风味是多种微生物共同作用的结果,而大曲是发酵过程中微生物的主要来源之一[2]。大曲不仅作为原料,也起到网罗环境中微生物的作用,是白酒的酿造动力源,有利于酿造过程中生成酶和风味物质成分[3]。同时大曲中含有丰富的兼性可培养微生物,为白酒酿造提供了大量产香微生物,对白酒中酯类、醛类、醇类等有机物的形成有着直接作用[4],并且对白酒的风味形成也至关重要[5]。
大曲中的微生物主要有细菌和真菌,真菌对于大曲的质量以及白酒风味的形成具有重要的作用。酵母菌是大曲主要功能微生物菌群之一,在大曲酒的发酵过程中起主导作用[6]。酵母不仅能发酵糖类产生乙醇,而且能代谢产生丰富的风味成分,如生香酿酒酵母(Saccharomyces cerevisiae)和假丝酵母(Candida)等;而毕赤酵母(Pichia pastoris)在不同发酵条件下,可以产生醇、酯、酸等多种风味物质,从而影响白酒的产品味感和风味特征[7-8]。白酒发酵过程中酵母菌具有多样性,不同种类酵母菌的耐热性、耐酒精性、耐酸性和发酵力也都不同[9]。
大曲中的霉菌不仅是形成曲表穿衣、保证曲体排水顺畅从而避免大曲酸败的主要菌类[10],而且赋予大曲糖化、液化、蛋白分解等各种水解能力及酯化能力,对白酒的风格形成起到了重要作用[11]。在发酵伊始,霉菌所产生的酶在发酵过程中有糖化的作用,将淀粉质原料在一定条件下全部或部分转化为葡萄糖等可发酵性糖,以供酵母菌和细菌利用[12],其次大曲中的霉菌可产生丰富的淀粉酶、蛋白酶、纤维素酶、酯化酶、果胶酶等酶系,不同的霉菌所产生的酶不同,这些酶系在酿酒的过程中产生积极的作用[13]。
由于微生物的各种生理代谢功能只能在可培养的条件下研究,纯种培养技术可以得到微生物菌株,再对其形态结构和遗传特性进一步认识,有利于丰富微生物的物种多样性[14]。目前采用可培养技术对中原浓香型白酒大曲微生物物种多样性的研究较少,本研究通过传统微生物培养技术从赊店老酒大曲中得到纯种真菌菌株,对获得的纯种菌株进行菌种鉴定,最后构建系统发育树对大曲中酵母菌和霉菌进行整体分析,以便于准确认识赊店老酒大曲可培养真菌多样性,丰富了中原地区浓香型白酒的真菌菌种资源库,为真菌资源的有效开发和利用奠定基础。
1 材料与方法
1.1 材料与试剂
1.1.1 实验材料
大曲:河南赊店老酒股份有限公司。
1.1.2 主要试剂
蔗糖、葡萄糖、无水乙醇、硫酸镁、琼脂:天津市科密欧化学试剂有限公司;氯化钠:西陇化工股份有限公司;磷酸二氢钾、50%甘油、硝酸钠、磷酸氢二钾:天津市德恩化学试剂有限公司;氯化钾:郑州派尼化学试剂厂;硫酸亚铁:国药集团化学试剂有限公司;酵母浸粉:英国Oxoid公司;酵母膏、蛋白胨:北京奥博星生物技术有限责任公司;氯霉素、链霉素:北京博奥拓达科技有限公司;1.0%琼脂糖:厦门太阳马生物工程有限公司;0.5×三羟甲基氨基甲烷硼酸电泳缓冲液(Tris-borate electrophoresis buffer,TBE):广州赛国生物科技有限公司;溶壁酶(酶活200 U/mg):上海源叶生物科技有限公司;SanTaqPCRMix预混液:北京康为世纪生物科技有限公司;酵母基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒、DNA Marker:天根生化科技(北京)有限公司;引物:上海英骏生物技术有限公司。实验所用试剂均为分析纯或生化试剂。
1.1.3 培养基
豆芽汁富集培养基:黄豆芽10 g,水100 mL,煮沸30 min,过滤后补足失水,加水400 mL,葡萄糖25 g,121 ℃灭菌20 min。
酵母浸出粉胨葡萄糖(yeast extract peptone dextrose,YEPD)培养基:葡萄糖20 g/L,蛋白胨20 g/L,酵母浸粉10 g/L,琼脂20 g/L,pH值自然,121 ℃灭菌20 min。
马铃薯葡萄糖琼脂(potato dextrose agar,PDA)培养基:去皮马铃薯200 g/L,葡萄糖20 g/L,琼脂20 g/L,115 ℃灭菌20 min。
PDA液体培养基:去皮马铃薯200 g/L,切成小块,加水1 000 mL加热搅拌30 min,过滤除去固形物并补足失水,加入葡萄糖20 g,加热充分溶解,121 ℃灭菌20 min。
高盐查氏培养基:硝酸钠2 g/L,磷酸二氢钾1 g/L,硫酸镁0.5 g/L,氯化钾0.5 g/L,硫酸亚铁0.01 g/L,氯化钠60 g/L,蔗糖30 g/L,琼脂20 g/L,121 ℃灭菌20 min
孟加拉红培养基:蛋白胨5 g/L,葡萄糖10 g/L,磷酸氢二钾1 g/L,硫酸镁0.5 g/L,琼脂20 g/L,氯霉素0.1 g,121 ℃灭菌20 min。
1.2 仪器与设备
LDZM-60KCS立式压力蒸汽灭菌器:上海申安医疗器械厂;ZQLY-300S恒温培养摇床:上海精宏试验设备有限公司;MQD-B3R振荡培养箱、DHP-9162电热恒温培养箱:上海一恒科学仪器有限公司;LQ-C3002电子天平:上海瑶新电子科技有限公司;SW-CJ-2F型双人双面净化工作台:苏州净化设备有限公司;3-18KS高速冷冻离心机:美国Sigma公司;DYY-2C电泳仪:北京六一生物科技有限公司;Labcycler梯度聚合酶联式反应(polymerase chain reaction,PCR)仪:德国SensoQuest公司;WD-9403F紫外分光光度仪、CX31型生物显微镜:奥林巴斯(中国)有限公司。
1.3 方法
1.3.1 真菌菌株的分离纯化
从赊店老酒优质大曲的曲心和曲皮按照1∶1的比例,分别取样5 g。并混合研磨成粉[16]。取混合均匀的曲粉10 g(无菌条件下)于90 mL无菌水中150 r/min、28 ℃振荡30 min。待混合液静置后,取5 mL上清液与100 mL豆芽汁富集培养基混合均匀,28 ℃、200 r/min摇床培养48 h。分别取10-2~10-6梯度稀释液100 μL于YEPD培养基及PDA培养基(含2%链霉素)涂布,每个梯度三个平行,其中YEPD平板培养基于28 ℃条件下培养48 h,PDA培养基于28 ℃条件下培养3~5 d。挑取长势良好的单菌落接种到PDA培养基固体平板中,反复划线纯化获得纯菌株。观察稀释涂布平板分离得到的单菌落,根据菌落特征及镜检结果,挑选相应的单菌落反复接种3~4次直至获得纯种菌落。对实验过程中的特殊菌落做好特征记录。将纯化后的菌落制成种子液,与50%灭菌甘油按1∶1(V/V)注入冻存管混匀,保存在-20 ℃冰箱。
1.3.2 形态学观察
用PDA培养基和孟加拉红培养基筛选霉菌,用YEPD培养基筛选酵母,对分离得到的酵母菌和霉菌观察并记录菌落形状、颜色、透明度、边缘、质地、湿润程度等菌落特征,以及霉菌菌株的分生孢子梗着生情况、孢子形态与颜色等特征,并对所有菌株初步分类,结合镜检结果将形态和培养特征高度一致的归为一类,对特殊形态的菌株特别标记。
1.3.3 分子生物学鉴定
将所获得的真菌接种于PDA液体培养基,28℃、120r/min条件下振荡培养约18 h,取1 mL菌液于已灭菌的离心管中离心,得到菌体沉淀后,按照Ezup柱式酵母基因组DNA提取试剂盒说明书提取真菌基因组DNA,并于1%琼脂糖凝胶电泳观察目的基因条带,所获基因组DNA保存在-20 ℃冰箱中备用。
以提取的基因组DNA为模板对分离酵母菌株的26S rDNA(D1/D2)区基因序列进行PCR扩增。PCR反应体系为50 μL,其中SanTaq PCRMix预混液25 μL、通用引物NL1(5'-GCATATCAATAAGCGGAGGAAAAG-3')和NL4(5'-GGTCCGTGTTTCAAGACGG-3')各2μL、DNA模板2μL、双蒸水(ddH2O)19 μL。PCR扩增程序:94 ℃预变性5 min;94 ℃变性40 s,53 ℃退火45 s,72 ℃延伸45 s,35个循环,72 ℃延伸10 min,4 ℃终止反应。
以提取的基因组DNA为模板对分离霉菌菌株的18S rDNA基因序列进行PCR扩增。PCR反应体系为50 μL,其中SanTaqPCR Mix预混液25 μL、通用引物ITS1(5'-TCCGTAGGTGAACCTGCGG-3')和ITS4(5'-TCCTCCGCTTATTGATATGC-3')各2 μL,DNA模板2 μL、双蒸水(ddH2O)19 μL。PCR扩增程序:94 ℃预变性6 min,94 ℃变性45 s,53 ℃退火45 s,72 ℃延伸120 s,30个循环,72 ℃延伸10 min,4 ℃终止反应。
取3 μL扩增产物经1%琼脂糖凝胶电泳检测产量和特异性,电泳条件:电压110 V,时间30 min,将PCR产物送至生工生物工程(上海)有限公司进行测序。
将测序所得的特定真菌菌株序列结果,在美国国家生物技术信息中心(national center for biotechnology information,NCBI)上通过局部序列排比检索基本工具(basic local alignment search tool,BLAST)程序进行同源序列比较与分析,初步确定受试菌株的分类地位,用MEGA 7.0软件进行多序列比对,采用邻接(neighbor-joining,NJ)法构建系统发育树[15]。
2 结果与分析
2.1 真菌的分离纯化和菌落形态观察
从赊店老酒优质大曲中分离纯化得103株霉菌,根据菌落形态特征的不同将霉菌分为35类,编号为LQMJ1~LQMJ35,部分菌株菌落的形态及镜检结果见图1,霉菌菌落特征描述结果见表1。分离纯化得到45株酵母菌,编号为SDJM1~SDJM45,部分酵母代表菌株的菌落特征及镜检图结果见图2、菌落形态具体描述结果见表2。
表1 赊店老酒大曲可培养霉菌的形态特征
Table 1 Morphological characteristics of culturable molds in Shedianlaojiu Daqu

表2 分离酵母菌的形态特征
Table 2 Morphological characteristics of isolated yeasts
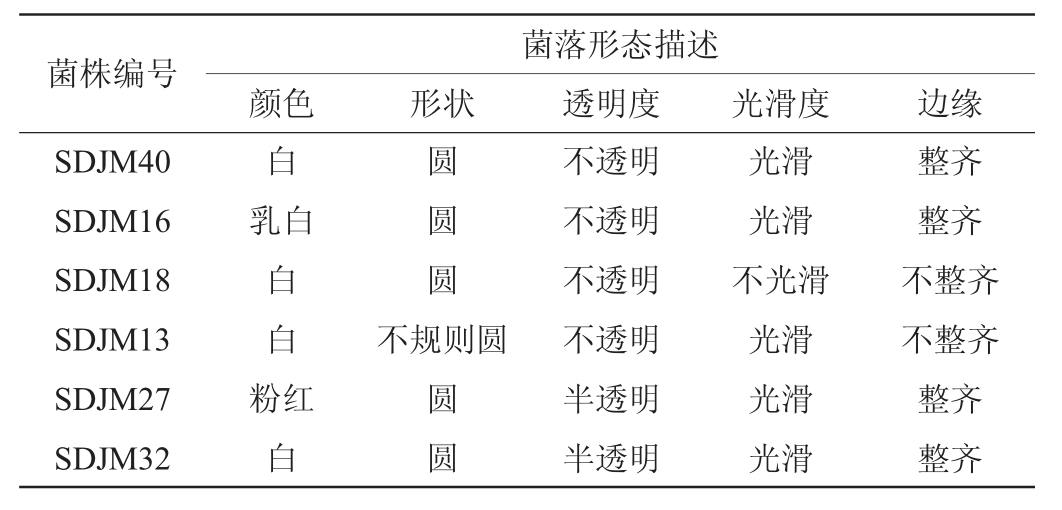

图1 部分霉菌菌落及孢子形态
Fig.1 Colonies and spore morphology of some molds
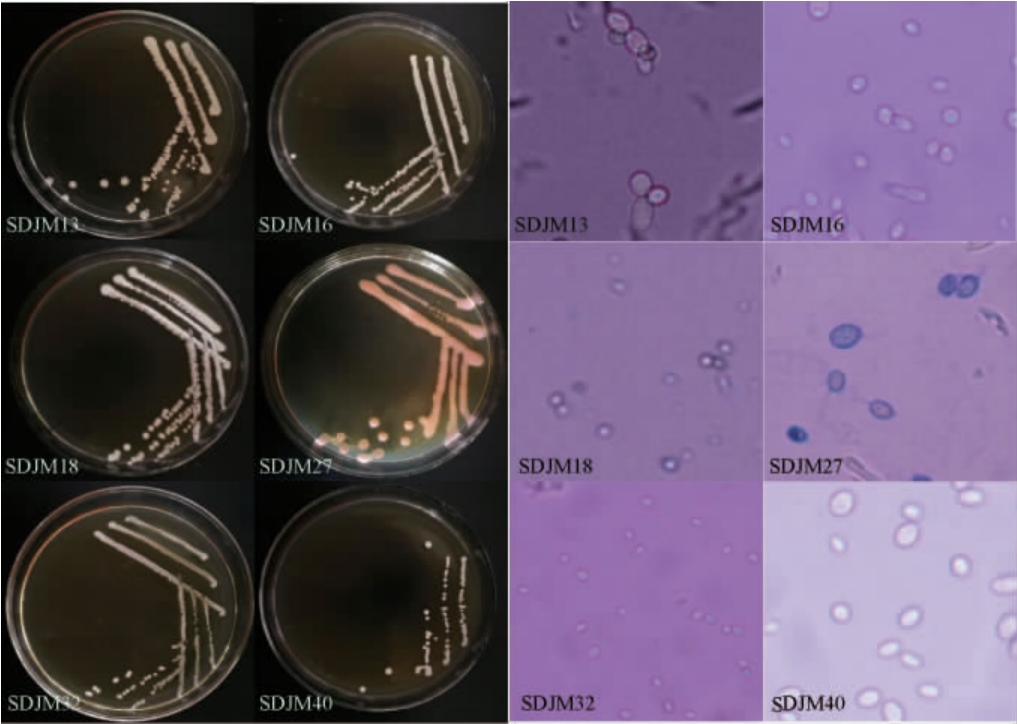
图2 部分酵母菌的菌落及细胞形态
Fig.2 Colonies and cell morphology of some yeasts
2.2 真菌分子生物学鉴定
2.2.1 酵母菌PCR扩增结果
通过酵母DNA提取试剂盒获得酵母DNA,用引物NL1/NL4对酵母26S rDNA序列扩增,琼脂糖凝胶结果见图3,都得到600 bp大小片段,与预期产物大小一致。
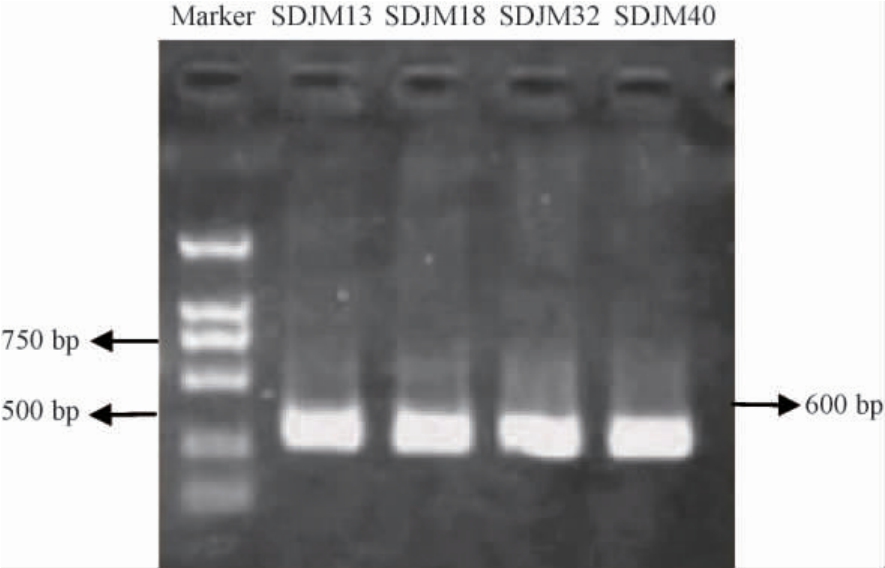
图3 部分酵母基因片段的PCR扩增产物电泳图
Fig.3 Electrophoresis of PCR amplification products of some yeasts gene fragments
2.2.2 霉菌PCR扩增结果
利用酵母试剂盒提取霉菌DNA,用引物ITS1和ITS4对霉菌进行18S rDNA序列扩增,琼脂糖凝胶结果见图4,都得到550 bp大小片段,均与预期产物大小一致。
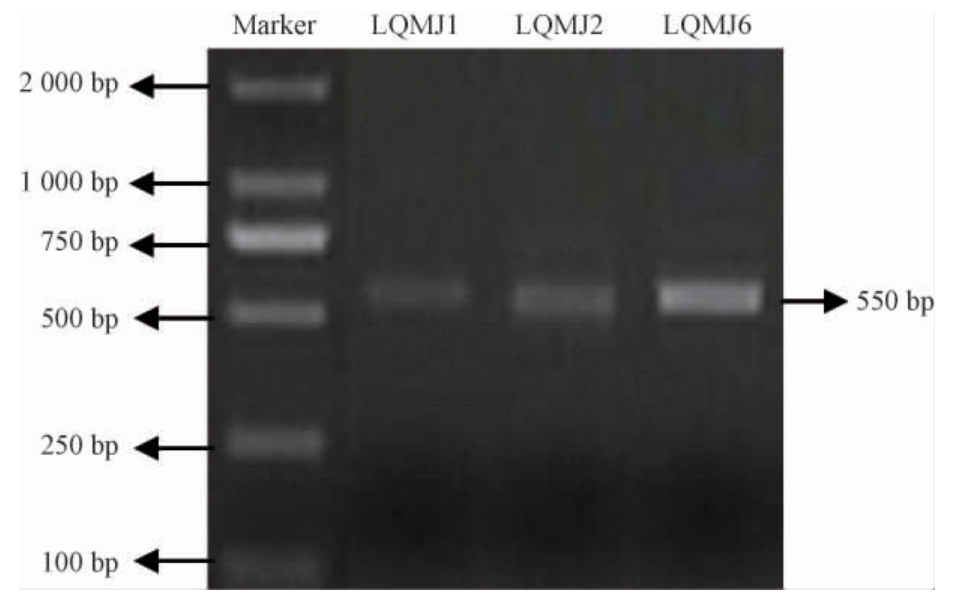
图4 部分霉菌基因片段的PCR扩增产物电泳图
Fig.4 Electrophoresis of PCR amplification products of some molds gene fragments
2.3 分离菌株的系统发育树分析
根据所得26S rDNA基因序列和18S rDNA基因序列,在NCBI上通过BLAST程序进行同源序列比较与分析,构建酵母菌及霉菌系统发育树,结果分别如图5和图6所示,结合45株酵母的菌落形态观察结果和细胞形态观察结果,确认从赊店老酒大曲中分离得到6株酵母菌,分别为酿酒酵母(Saccharomyces cerevisiae)、异常威克汉姆酵母(Wicker hamomyces anomalus)、扣囊复膜酵母(Saccharomycopsis fibuligera)、发酵毕赤酵母(Pichia fermentans)、胶红酵母(Rhodotorula mucilaginosa)及光滑假丝酵母(Candida glabrata)。35株霉菌经18S rDNA鉴定得到4个霉菌菌属,分别为根霉属(Rhizopus)、横梗霉属(Lichtheimia)、曲霉属(Aspergillus)和毛霉属(Mucor)。
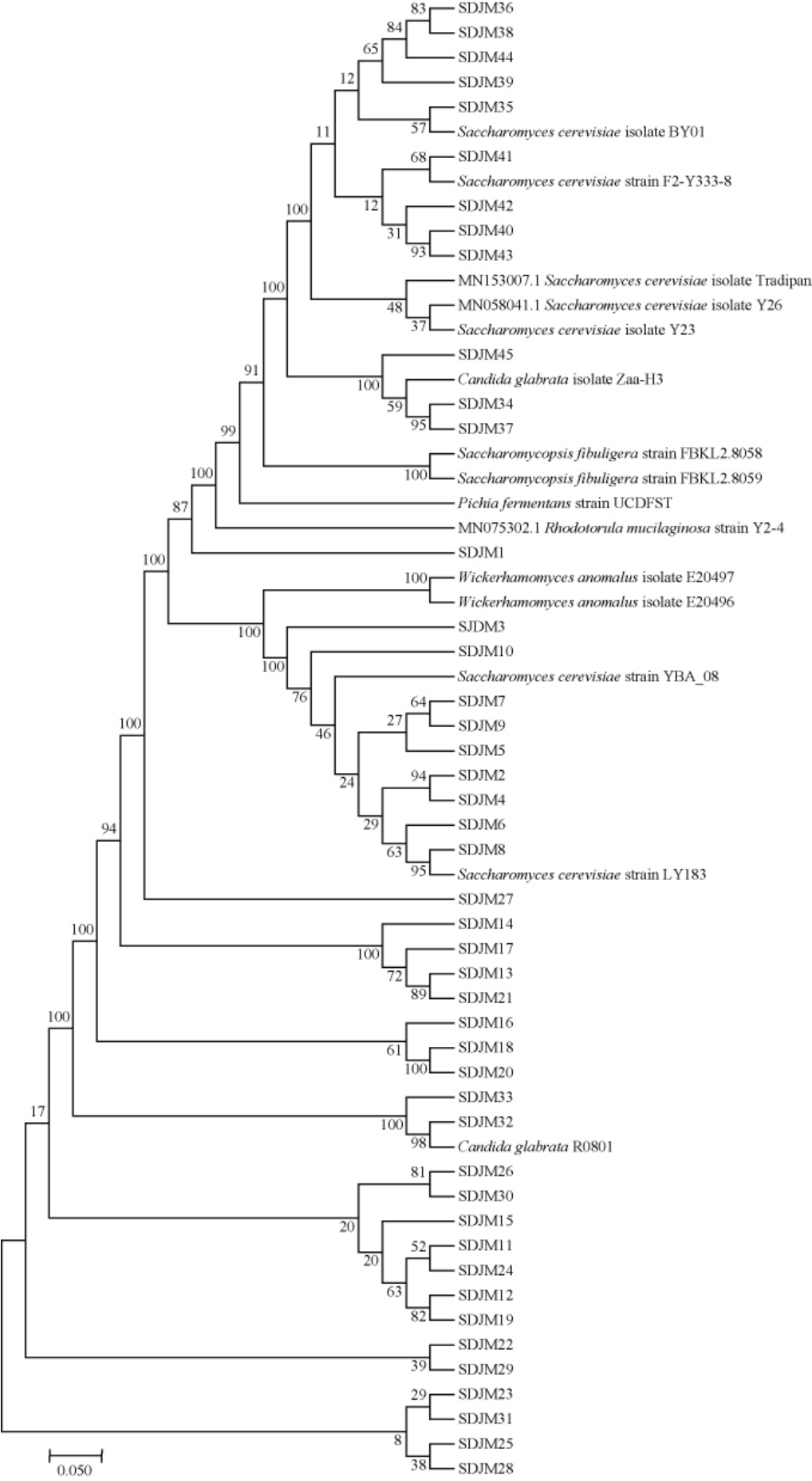
图5 基于26S rDNA序列45株酵母菌的系统发育树
Fig.5 Phylogenetic tree of 45 yeasts based on 26S rDNA sequences
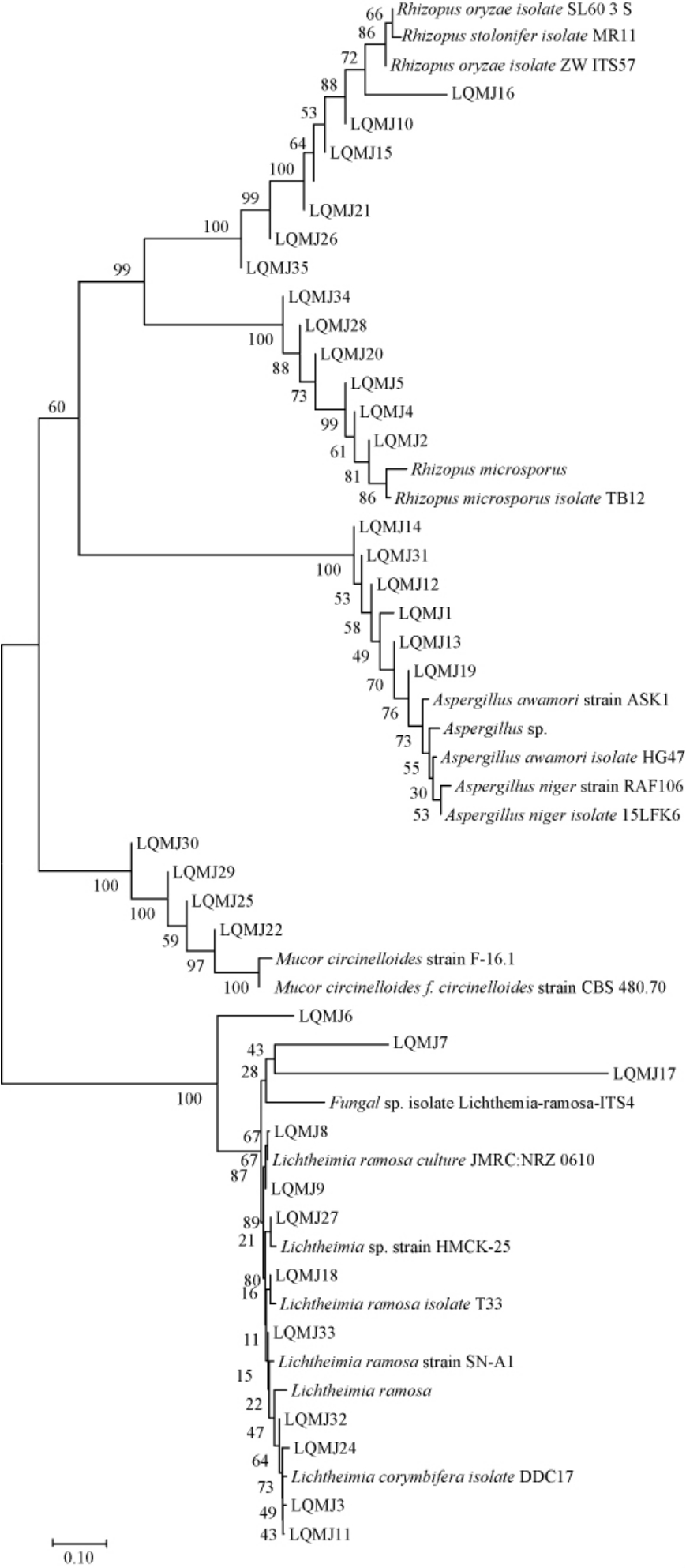
图6 基于18S rDNA序列35株霉菌系统发育树
Fig.6 Phylogenetic tree of 35 molds based on 18S rDNA sequences
2.4 真菌的种群数量分析
6种酵母所占总量比例见图7a。由图7a可知,45株酵母中,酿酒酵母(Saccharomyces cerevisiae)占71%、胶红酵母(Rhodotorula mucilaginosa)占2%、发酵毕赤酵母(Pichia fermentans)占9%、扣囊复膜酵母(Saccharomycopsis fibuligera)占5%、光滑假丝酵母(Candida glabrata)占11%、异常威克汉姆酵母(Wickerhamomyces anomalus)占2%。4种霉菌属所占总量比例见图7b。由图7b可知,筛选的霉菌经DNA分子鉴定最终确认根霉属(Rhizopus)和横梗霉属(Lichtheimia)数量较多,其中根霉属(Rhizopus)占37%、横梗霉属(Lichtheimia)占33%、曲霉属(Aspergillus)占18%、毛霉属(Mucor)占12%。
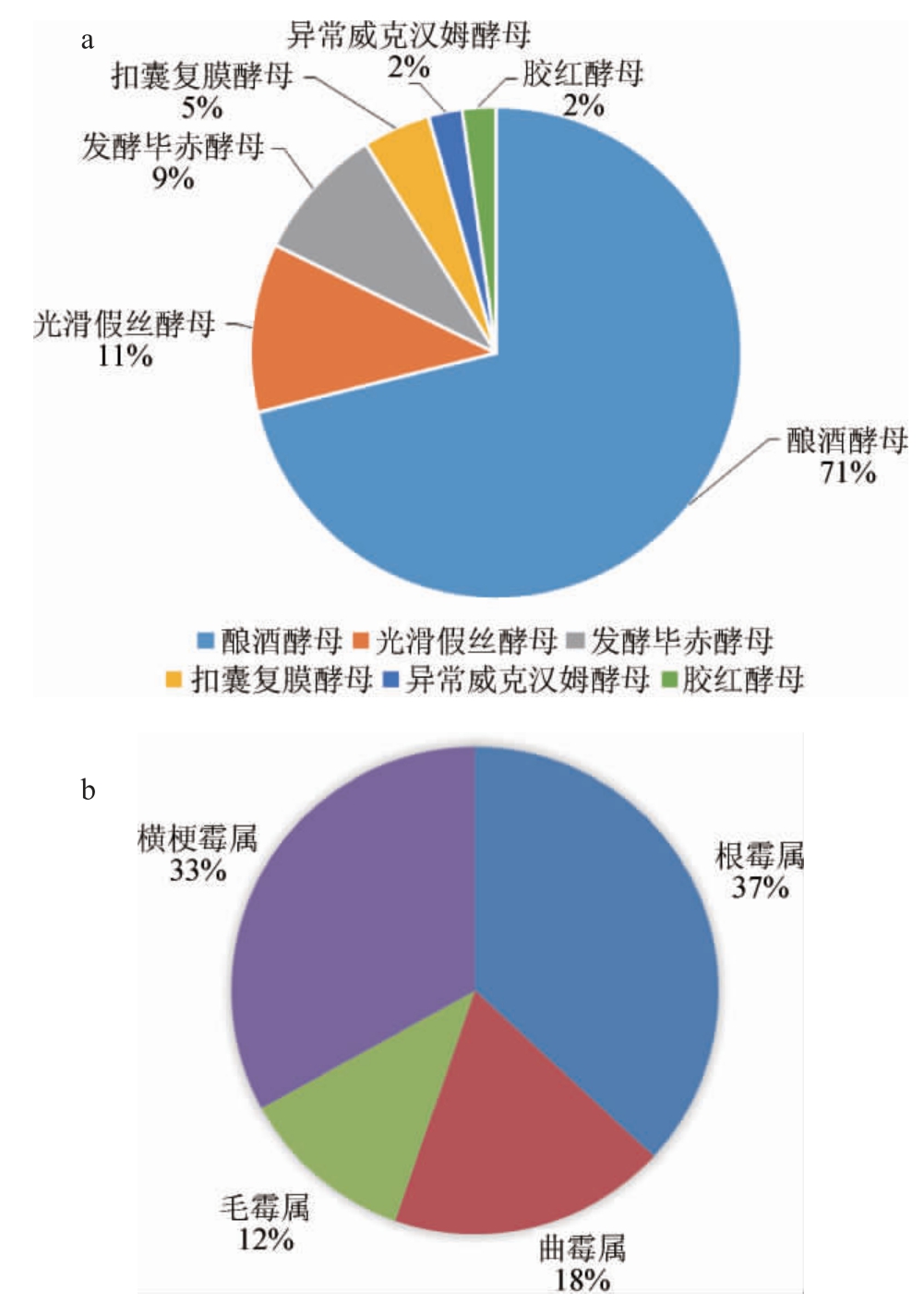
图7 6种酵母(a)及4种霉菌属(b)所占总量比例
Fig.7 Proportion of 6 kinds of yeasts(a)and 4 kinds of molds(b)in total
3 讨论
白酒酿造处于一个开放的环境,相对于其他酒种具有一定的区域性,不同地区的微生物资源不同,酿造出的白酒风格也不同。张杰等[17]在宋河酒厂高温大曲中分离鉴定出假丝酵母(Candida)、三角酵母(Trigonopsis)、红冬孢酵母(Rhodos poridium)等3个酵母属。罗惠波等[18]从泸州老窖浓香大曲中分离得出酿酒酵母(Saccharomyces cerevisiae)、德巴利氏酵母(Debaryomyces)、异常威克汉姆酵母(Wickerhamomyces anomalus)和锁掷酵母(Sporidiololus pararoseus)4个酵母属。刘宏媛等[19]以泸州老窖大曲为样本,使用传统培养分离方法得到2株酵母菌,经过菌落特征观察和显微镜观察后,利用Biolog微生物自动鉴定系统对2株酵母进行鉴定,确认它们分别为佛罗伦萨结合酵母(Zygosaccharomyces florentine)和伯顿丝孢毕赤酵母(Pichia burtoni)。徐占成等[20]以剑南春大曲为研究对象,利用聚合酶链式反应-变性梯度凝胶电泳研究得出剑南春大曲中酵母主要分布在酿酒酵母(Saccharomyces cerevisiae)、东方伊萨酵母(Issatchenkia orientalis)、汉逊酵母(Hansenula)、假丝酵母(Candida)和毕赤酵母(Pichia)5个属。本实验中发现的6个酵母菌属与其他浓香型白酒相比处于较高水平,由此可以看出,不同地区白酒大曲酵母菌的种类有很大区别,正因为这些不同,构成了各个白酒品牌的风味特色。
酿酒酵母(Saccharomyces cerevisiae)是大曲中分布最为广泛的酵母菌属,能够将糟醅中的淀粉发酵为酒精,在白酒发酵过程中起着至关重要的作用。企业从酿酒生产中分离筛选出功能突出的产酒酵母强化发酵,能够节约粮食、提高出酒率、降低成本[21]。除了生产酒精外,酵母菌的代谢作用还能够赋予白酒层次复杂的香味[22-23]。产酯酵母(产香酵母)的种类和数量对白酒的质量有着极大的影响,产酯酵母也成为了近年来白酒功能菌的研究热点。本实验中发现的产香酵母种类丰富,如毕赤酵母(Pichia)、光滑假丝酵母(Candida glabrata)、扣囊复膜酵母(Saccharomycopsis fibuligera)、异常威克汉姆酵母(Wickerhamomyces anomalus)等,为白酒提供了复杂有层次的香味。异常威克汉姆酵母(Wickerhamomyces anomalus)能够产生丰富的香味物质,有吡嗪类物质、苯乙醇、愈创木酚等[24]。扣囊复膜酵母(Saccharomycopsis fibuligera)能够使醇类物质和酯类物质含量提高,如使乙酸乙酯、乙酸异戊酯及其他产物呈现清灵果香[25]。
从赊店老酒大曲中分离筛选的霉菌属也在白酒的酿造过程中发挥着非常重要的作用。如根霉(Rhizopus)能产生一些酶类,如淀粉酶、果胶酶、脂肪酶等,能将淀粉近乎理论值地转化为葡萄糖[26],在酿酒过程中用做糖化菌,在发酵过程中也能产生乙酸乙酯、丙酸乙酯、正丙醇等芳香性成分,从而影响酒的品质。曲霉(Aspergillus)是大曲中产酶能力较强的一类微生物,自身能够分泌葡萄糖氧化酶、糖化酶和蛋白酶,对于白酒的口感和质量起着至关重要的作用[27]。毛霉(Mucor)具有极其丰富的酶系,针对蛋白酶而言,就能产出酸性蛋白酶、碱性蛋白酶以及中性蛋白酶,可以合成端肽酶、分泌内肽酶,是一种天然的复合酶系[28]。另外,毛霉在生长过程中产生分解蛋白质的酶系能代谢积累乙酸和甘油等,对大曲的品质有一定的积极影响,这对曲酒的发酵进程具有非常重要的作用。
4 结论
本研究采用传统培养分离法,研究了赊店老酒优质大曲中真菌的物种多样性,通过传统培养分离方法共得到45株酵母菌、103株霉菌,对其进行形态学观察和分子生物学鉴定,结果表明,大曲中共鉴定出6株酵母菌和4个霉菌属。6株酵母菌分别为:酿酒酵母(Saccharomyces cerevisiae)占71%、异常威克汉姆酵母(Wickerhamomyces anomalus)占2%、扣囊复膜酵母(Saccharomycopsis fibuligera)占5%、发酵毕赤酵母(Pichia fermentans)占9%、胶红酵母(Rhodotorula mucilaginosa)占2%、光滑假丝酵母(Candida glabrata)占11%。4个霉菌属分别为:根霉属(Rhizopus)占37%、横梗霉属(Lichtheimia)占33%、曲霉属(Aspergillus)占18%、毛霉属(Mucor)占12%。研究结果表明,赊店老酒优质大曲中含有丰富的真菌资源,为中原浓香型白酒的酿造微生物研究奠定了基础。
[1]郜希璐.白酒窖泥中酵母菌的分离鉴定及发酵特性研究[D].天津:天津大学,2009.
[2]敞颜,赵辉,凌宏志.传统白酒发酵微生物的研究进展[J].食品工业科技,2019,31(9):425-427.
[3]ZHENG X W,TABRIZI M R,NOUT M J R,et al.Daqu-a traditional Chinese liquor fermentation starter[J].J I Brewing,2011,117(1):82-90.
[4]LE V D,ZHENG X W,CHEN J Y,et al.Characterization of volatile compounds in Fen-Daqu a traditional Chinese liquor fermentation starter[J].J I Brewing,2012,118(1):107-113.
[5]WU Q,XU Y,CHEN L.Diversity of yeast species during fermentative process contributing to Chinese Maotai-flavour liquor making[J].Lett Appl Microbiol,2012,55(4):301-307.
[6]祝云飞,黄治国,邓杰,等.浓香型大曲中一株酵母菌的分离鉴定及其挥发性产物分析[J].四川理工学院学报(自然科学版),2016,29(1):7-11.
[7]罗方雯,黄永光,涂华彬.茅台镇酱香白酒不同酿造区域可培养酵母种群结构多样性分析[J].食品科学,2020,41(12):143-149.
[8]陈美竹,邱树毅,胡宝东,等.酱香型白酒酿造体系中酵母菌研究进展[J].中国酿造,2015,34(6):5-10.
[9]刘婷婷,曾驰,杨团元,等.白云边酒优势酵母菌的分离鉴定及其发酵特征分析[J].中国酿造,2013,32(12):116-120.
[10]常强,吴再节,孙伟,等.不同培养温度对大曲微生物种群变化影响的研究[J].现代食品,2019,(12):63-65,78.
[11]胡承,邬捷锋,沈才洪,等.浓香型(泸型)大曲的研究及其应用[J].酿酒科技,2004(1):33-36.
[12]牛帅科.羊羔酒大曲中微生物多样性研究[D].石家庄:河北科技大学,2013.
[13]李绍亮,李学思,候小歌,等.宋河酒曲中主要霉菌的鉴定及其产酶特性的研究[J].酿酒,2016,43(6):24-29.
[14] LI J X,LIU C.Progress on methods for increasing microbial culturability[J].Adv Microbiol,2016,5:1-8.
[15]李艳,董振玲,牟德华.羊羔美酒大曲中酵母菌多样性及分子鉴定[J].食品科学,2014,35(5):144-149.
[16]孔维兵,王晓丹,班世栋,等.酱香型大曲中酵母的分离与鉴定[J].酿酒,2015,42(1):57-62.
[17]张杰,侯小歌,王俊英,等.高温大曲中酵母菌的分离、鉴定及耐高温性[J].中国酿造,2011,30(11):112-114.
[18]罗惠波,杨晓东,杨跃寰,等.浓香型大曲中可培养真菌的分离鉴定与系统发育学分析[J].现代食品科技,2013,29(9):2047-2052.
[19]刘宏媛,李光辉,罗惠波,等.大曲中酵母菌的分离及Biolog 微生物系统分析鉴定[J].食品与发酵科技,2011,47(1):1-3.
[20]徐占成,唐清兰,刘孟华,等.剑南春大曲曲药真菌群落结构的分析[J].酿酒,2015,42(4):13-16.
[21]胡帮超,刘国英,董琪,等.白酒酿造中功能性酵母菌的研究及应用[J].酿酒,2017,44(2):13-18.
[22]李兵,张超,王玉霞,等.白酒大曲功能微生物与酶系研究进展[J].中国酿造,2019,38(6):7-12.
[23]侯小歌,王俊英,李学思,等.浓香型白酒糟醅及窖泥产香功能菌的研究进展[J].微生物学通报,2013,40(7):1257-1265.
[24]明红梅,郭志,周健,等.浓香型大曲中产香微生物的筛选及鉴定[J].现代食品科技,2015,31(4):186-191.
[25]罗小叶,邱树毅,陆安谋,等.酱香大曲产香酵母的分离及鉴定[J].食品与发酵工业,2016,42(12):26-31.
[26]刘金梅,张凤英.根霉在发酵工业与环境科学中的研究进展[J].生物技术通报,2013(11):26-33.
[27]路怀金,刘通讯,赵谋明,等.2 株米曲霉的特色酶系对酱油理化指标及品质的影响[J].中国食品学报,2021,21(5):230-237.
[28]罗惠波,杨晓东,杨跃寰,等.浓香型大曲中可培养真菌的分离鉴定与系统发育学分析[J].现代食品科技,2013,29(9):2047-2052.