酒精工业作为国民经济发展的重要支柱产业,在酿酒、医药卫生、新能源等方面发挥着至关重要的作用[1-2]。人们对酒精溶液的研究已有较长历史,早期以酒精质量检测为主[3-5],近十几年来,随着燃料乙醇产业的发展,人们开始关注不同浓度乙醇燃烧热值的差异原因;在食品产业方面,人们希望利用简便快捷的方法鉴别出发酵酒和配制酒[6],然而,这些都与乙醇溶液的微观结构有关[7-8]。因此,各国学者将红外光谱、拉曼光谱、荧光光谱和X-射线衍射等多种光谱学技术结合起来,开展对乙醇-水溶液微观结构的研究[9-15]。尽管国内外学者采用实验和理论模拟方法相结合对乙醇-水溶液微观结构做了大量研究[16-17],但至今仍未得到统一的结论,特别是乙醇-水溶液微观结构变化对食品质量的影响鲜有报道。
水分活度表示食品中水逸出的程度,间接反映食品中自由水数量,与食品保藏时间密切相关[18]。电导率表示液体溶液的导电能力,受到液体中乙醇浓度和离子数量的影响[19]。声速值表示声音在溶液中的传播速度,与溶液微观结构的疏密程度有关[20]。本实验通过测定乙醇溶液不同质量浓度和时间声速、水分活度和电导率的变化,结合乙醇溶液分子基团振动频率的响应、探究乙醇溶液宏观物理参数与微观结构的相互关系,以期更好地阐明乙醇溶液物理特性的变化机制。
1 材料与方法
1.1 材料与试剂
乙醇(99.99%)(优级纯):天津市富宇精细化工有限公司;氯化钠、尿素(均为分析纯):天津市东丽区天大化学试剂厂。
1.2 仪器与设备
DSA48密度声速仪(density and sound velocitymeter,DSV):奥地利安东帕有限公司;HD-4水分活度测量仪(water activity meter,WAM):上海精密仪器仪表有限公司;FT-NIR傅里叶变换近红外光谱(near infrared spectrometer,NIR)仪:美国Perkin Elmer公司;EC 214电导率仪(conductivity meter,CM):上海加惠仪器仪表有限公司;LCQ液相色谱-质谱联用仪:美国Finnigan公司;HP 1100高效液相色谱系统:美国惠普公司。
1.3 实验方法
1.3.1 样品处理
乙醇溶液(不加尿素)组:乙醇体积分数分别为5%、14%、38%和45%(20 ℃);
乙醇溶液(加尿素)组,添加尿素0.5 g/100 mL:乙醇体积分数分别为5%、14%、38%和45%(20 ℃)。由于溶质的介入会影响溶液中分子间的氢键网络结构,尿素作为生物体内常见的小分子有机渗透剂,加入尿素破坏乙醇溶液中乙醇分子与水分子的氢键作用,探究乙醇分子与水分子氢键作用对乙醇溶液物理特性的影响[21]。
1.3.2 声速的测定
利用密度声速仪测定不同体积分数乙醇样品在贮藏不同时间(5 d、15 d、30 d和60 d)的声速[22]。
1.3.3 水分活度的测定
利用水分活度仪测定不同体积分数乙醇样品在贮藏不同时间(5 d、15 d、30 d和60 d)的水分活度[23]。水分活度仪开机预热30 min,利用配制24 h饱和氯化钠溶液进行仪器校正,测定时把测量样品放置在20 ℃恒温槽中,保持测量溶液温度一致。
1.3.4 电导率的测定
利用电导率仪测定不同体积分数乙醇样品在贮藏不同时间(5 d、15 d、30 d和60 d)的电导率[24]。电导率仪开机预热30 min,利用0.1%KCl溶液进行校正,把测量样品放置在20 ℃恒温槽中,保持测量溶液温度一致。
1.3.5 近红外光谱的测定
利用傅里叶变换近红外光谱仪测定不同体积分数乙醇样品贮藏不同时间(5 d和60 d)以及添加尿素不同体积分数乙醇样品在贮藏5 d的近红外光谱。光谱采集参数:仪器信号能量为5 eV,参比材料为石英比色皿,光程为1 mm,扫描分辨率16 cm-1,扫描次数为32次。对光谱数据进行移动窗口平均平滑处理,提高谱图的信噪比;以马氏距离为指标对光谱数据进行筛选,剔除异常光谱数据[25]。
1.3.6 数据统计分析
使用SPSS软件版本16.0处理数据,结果均表示为平均值±标准偏差(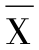 ±SD),通过单因素方差分析(analysisof variance,ANOVA)对数据进行统计学分析,进行最小显著性差异(least significant difference,LSD)法检验,P<0.05表示数据差异显著。
±SD),通过单因素方差分析(analysisof variance,ANOVA)对数据进行统计学分析,进行最小显著性差异(least significant difference,LSD)法检验,P<0.05表示数据差异显著。
2 结果与分析
2.1 乙醇体积分数和贮存时间对乙醇溶液声速的影响
由图1可知,对于不同体积分数乙醇溶液,随着贮存时间增加,声速变化完全不同。乙醇体积分数为5%、38%和45%总体呈现下降趋势,乙醇体积分数为14%在贮存时间内变化较小。对于不同贮存时间,4种体积分数乙醇溶液(5%、14%、38%和45%)声速变化趋势基本一致,即随着乙醇体积分数增加,声速呈现先上升后下降的趋势,乙醇体积分数为38%的声速最高。由于液体没有剪切弹性,只能纵波形式传播,在线性声学条件下,溶液的声速由溶液本身的体积弹性模量和密度决定,介质的弹性模量愈大,密度愈小,声速愈大[26]。乙醇溶液密度随乙醇体积分数增加呈线性下降,说明乙醇声速变化主要由体积弹性模量引起的,而体积弹性模量强弱取决于分子结构[27],可见,不同体积分数乙醇溶液微观结构存在显著差异(P<0.05)。
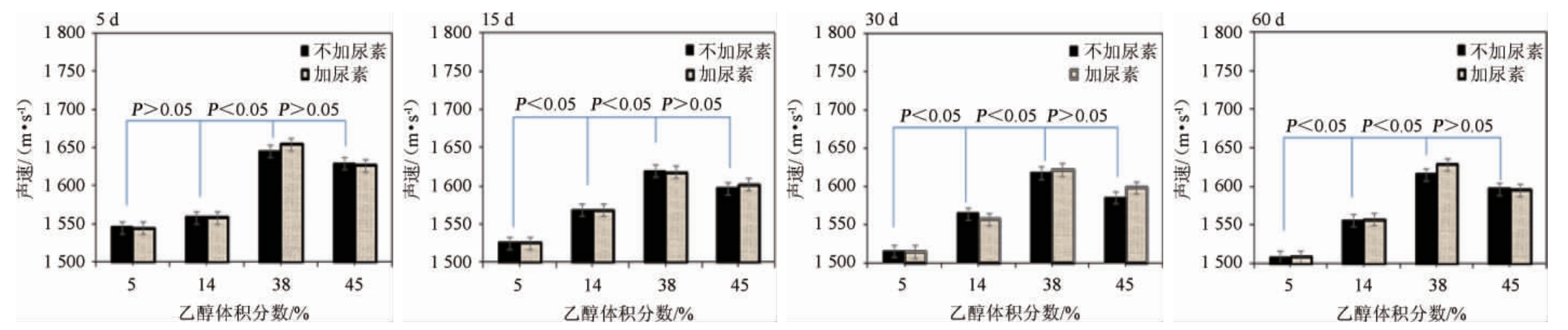
图1 4个贮存时间不同体积分数乙醇溶液的声速值
Fig.1 Sound velocity of ethanol solutions of different concentration for 4 storage time
尽管尿素添加能够破坏乙醇溶液分子结构的氢键作用,导致乙醇溶液声速变化,但这种变化不具有统计学意义(P>0.05),对声速变化趋势无影响,说明尿素添加只是破坏了部分氢键,还有许多氢键维持着乙醇溶液不同的空间结构。
2.2 乙醇体积分数和贮存时间对乙醇溶液水分活度的影响
由图2可知,对于体积分数为5%和14%的乙醇溶液,在贮存时间水分活度的变化趋势基本一致。第5天开始急剧上升,15 d后急剧下降,即乙醇分子与水分子形成更加稳定的结构。对于体积分数为38%和45%的乙醇溶液,在贮存时间水分活度变化趋势基本一致,第5天开始急剧上升,与38%相比45%体积分数乙醇溶液上升速率更快。15 d均达到最高,然后缓慢下降。说明高浓度乙醇溶液,形成空间稳定结构的速度更慢,而且在形成稳定结构过程中,存在着水分子氢键的断裂和重新结合,有自由水释放和结合的变化[28]。在不同贮存时间,4种体积分数乙醇溶液(5%、14%、38%和45%)的相关关系基本一致,水分活度值差异均不显著(P>0.05),但低浓度组(5%和14%)和高浓度组(38%和45%)乙醇溶液间水分活度值存在显著差异(P<0.05)。说明高浓度乙醇溶液乙醇分子与水分子形成更多的共价键,使溶液中自由水含量降低,这和水分活度基本理论是一致的。
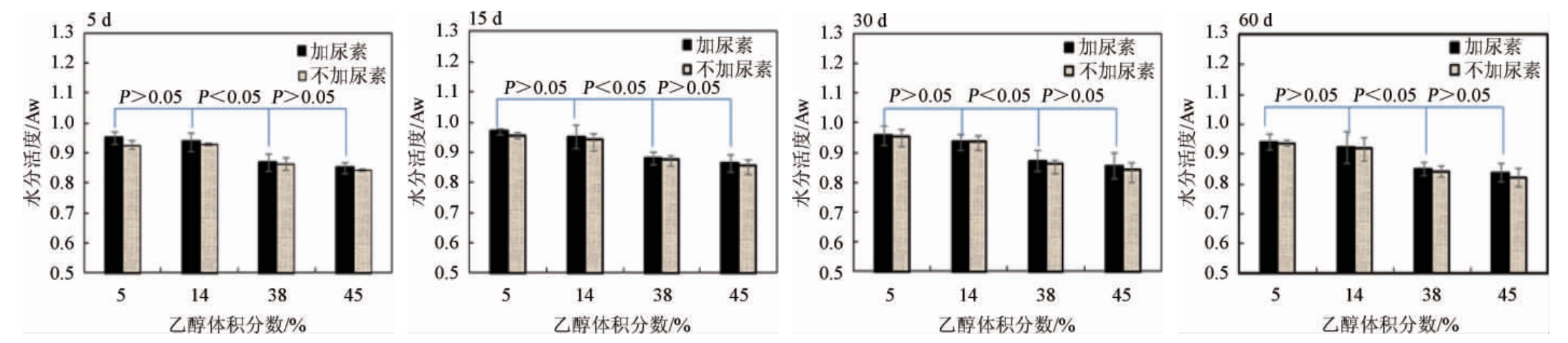
图2 4个贮存时间不同体积分数乙醇溶液的水分活度
Fig.2 Water activity of ethanol solutions of different concentration for 4 storage time
2.3 乙醇体积分数和贮存时间对乙醇溶液电导率的影响
由图3可知,对于体积分数为5%和14%的乙醇溶液,随着贮存时间的增加,电导率先缓慢下降,15 d和30 d无明显变化,30 d后开始转为上升,60 d电导率回到起点。对于体积分数为38%和45%的乙醇溶液,随着贮存时间的增加,电导率先急剧上升,再急剧下降,30 d后开始转为上升,60 d电导率又回到起点。在不同贮存时间,4种体积分数乙醇溶液的电导率基本保持相同线性关系。乙醇溶液体积分数从5%、14%到38%,电导率始终保持下降趋势(P<0.05),乙醇溶液体积分数为38%和45%时电导率差异不显著(P>0.05)。
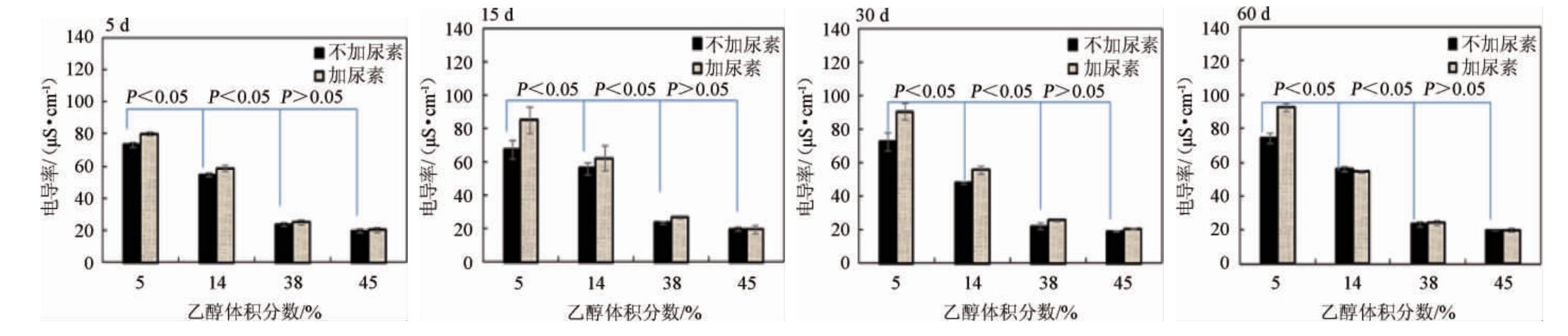
图3 4个贮存时间不同体积分数乙醇溶液的电导率
Fig.3 Conductivity of ethanol solutions of different concentration for 4 storage time
由此说明,随着贮存时间的增加,乙醇分子与水分子的结构不断发生着变化,电导率下降后又上升,空间结构从疏松到致密,再到疏松稳定,体积分数38%和45%乙醇溶液电导率无显著差异。
2.4 不同贮存时间乙醇溶液的近红外光谱图
图4为贮存时间5 d和60 d,不同体积分数乙醇溶液的近红外光谱图,由图4可知,波长960 nm处为非键合羟基伸缩振动二级倍频吸收峰,该处吸收峰为氢键的研究提供重要的信息;波长1 190 nm处为甲基二级倍频吸收峰;波长1 460~1 600 nm处宽吸收峰为氢键键合的醇,归为羟基的分子内键合;波长1 701 nm和1 732 nm处为甲基吸收峰;波长1 762 nm处为亚甲基一级倍频吸收峰,表示-CH2的对称伸缩振动。
从图4短波区可见,波长960 nm处,体积分数5%和14%乙醇溶液吸收峰强于38%和45%,说明体积分数5%和14%乙醇空间结构游离羟基多于38%和45%,38%和45%更多的羟基与周围水分子形成了氢键,可以证实,5%和14%羟基挂在外侧,体积分数越高,羟基越多,和38%(或45%)的外层结构完全不同。波长1 190 nm和1 701 nm两处甲基吸收峰显示乙醇体积分数越高,吸收峰越强,这符合高浓度乙醇溶液甲基基团多的规律[25]。在波长1 732 nm 吸收峰处,体积分数5%和14%乙醇溶液没有吸收峰,更说明与38%(或45%)微观结构不同。1 762 nm处为亚甲基一级倍频吸收峰处,随着乙醇体积分数越低,吸收峰强度越强,且明显发生蓝移(向波长增大方向移动),说明低浓度时CH-基团与水分子发生作用,导致-CH2伸缩振动频率随浓度降低发生进一步蓝移。
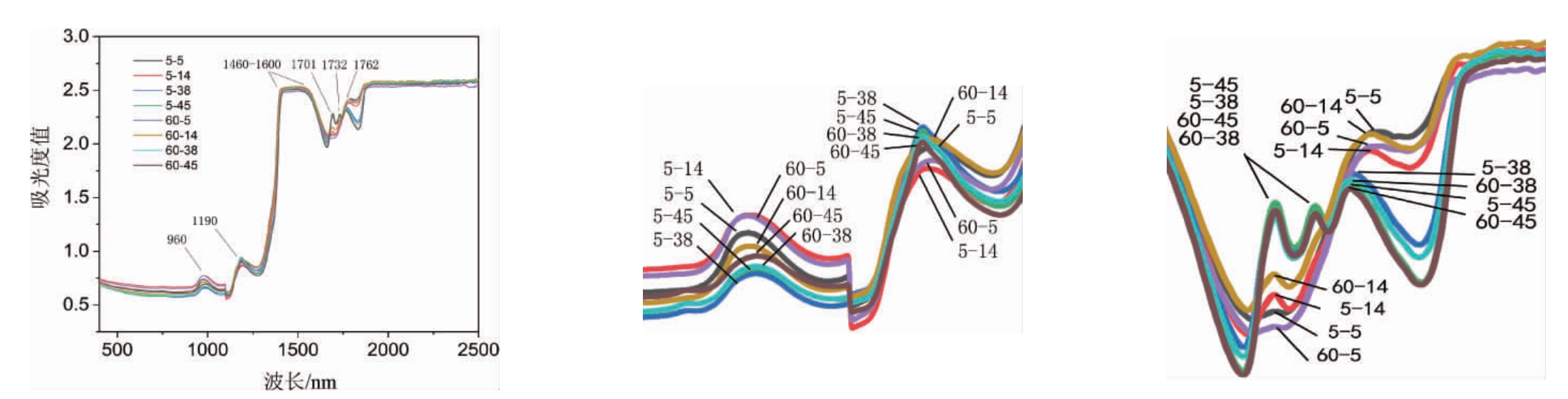
图4 5 d和60 d对照组不同体积分数乙醇溶液红外光谱及短波区和长波区谱图
Fig.4 Infrared spectra and the short-wave and long-wave regions spectra of different concentrations ethanol solutions of the control group for 5 d and 60 d
从图5短波区可见,960 nm吸收峰处,体积分数为5%和14%乙醇溶液加尿素破坏氢键,却导致非键合羟基较少,又因为尿素添加对亚甲基上的氢键影响不大(1 762 nm处吸收峰无明显变化),推测尿素更多是破坏了水之间氢键,造成水多聚体产生较多空洞,这可能提高溶液导电性能。1 701 nm和1 732 nm处为甲基吸收峰,体积分数为5%和14%乙醇溶液均未出现双峰现象,而体积分数为38%和45%均出现双峰现象,同前面的结论一样,证明乙醇体积分数>38%,乙醇微观结构发生显著变化,在1 732 nm吸收峰通常是线型C-H化合物在一级倍频区最强的谱带,亚甲基发生扭摆弯曲,实验组添加尿素吸收峰强度没有改变,更加证实了高浓度乙醇溶液笼状稳定结构的猜想。
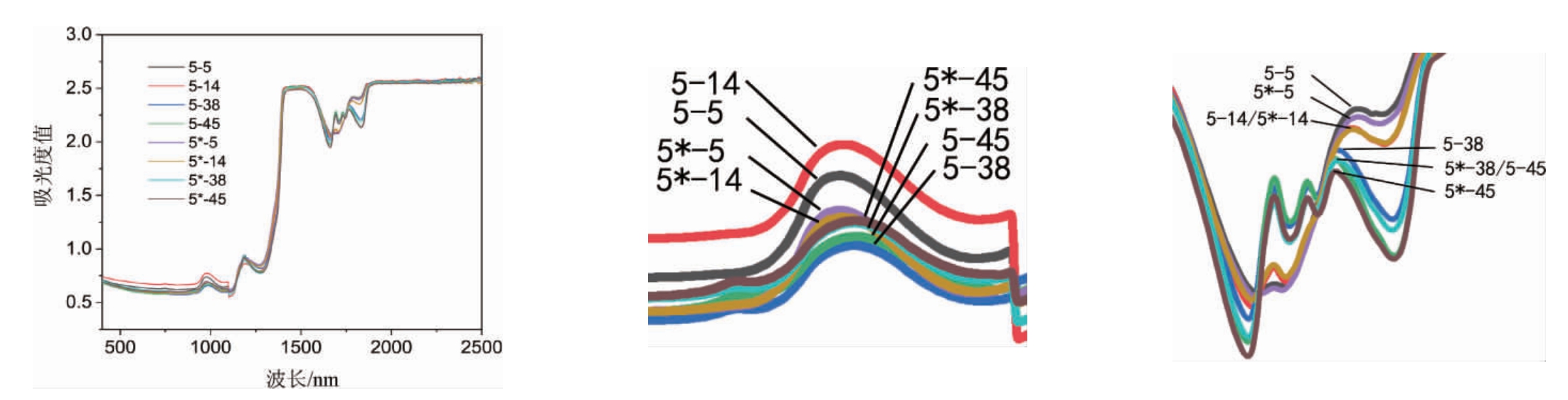
图5 5 d实验组和对照组不同体积分数乙醇溶液红外光谱及短波区和长波区谱图
Fig.5 Infrared spectra and the short-wave and long-wave regions spectra of different concentrations ethanol solutions of the experimental group and control group for 5 d
3 讨论
测定4种体积分数乙醇溶液的声速,结果表明,随着乙醇体积分数增加,声速呈现先上升后下降的趋势,体积分数38%乙醇溶液声速最高。根据声速值的定义可知,不同浓度乙醇溶液微观结构存在差异,体积分数38%附近正好是乙醇-水分子微观结构发生改变的区域,这与吴斌[11]的结论一致。
测定4种体积分数乙醇溶液的水分活度,结果表明,体积分数越高,水分活度越低,说明自由水含量越低,说明乙醇分子和水分子形成结合共价键。随着贮存时间延长,4种乙醇溶液变化趋势不一致,体积分数5%和14%乙醇溶液水分活度呈下降趋势,体积分数38%和45%乙醇溶液水分活度贮存15 d达到最高值,说明高浓度乙醇溶液形成稳定空间结构的过程更漫长,推测分子间氢键形成可能存在前后关系或持续变化,乙醇-水分子的空间微观结构更加稳定和致密。尿素添加能够破坏一部分氢键作用,但对乙醇-水分子微观结构无显著影响。
测定4种体积分数乙醇溶液的电导率和近红外光谱,5%、14%和38%差异显著(P<0.05),38%和45%差异不显著(P>0.05),说明体积分数5%、14%和38%空间微观结构差异较大,体积分数为38%和45%结构微观结构差别不大。随着贮存时间延长,4种体积分数乙醇溶液的电导率均出现先下降后上升的趋势,表明乙醇溶液微观结构不断发生变化;体积分数为38%和45%乙醇溶液再次表现出近似一致的变化趋势,也说明两种乙醇溶液微观结构近似。这与DIXIT S等[29]对甲醇-水溶液的红外光谱分析一致。这一结论可以用于酒类发酵年份和真假酒类鉴别,为酒类饮品智能化管理提供了新的方法。
4 结论
通过测定乙醇溶液宏观物理参数,发现这些物理参数的变化规律,并利用NIR从微观结构水平解释乙醇溶液物理参数与氢键作用的相互关系。结果表明,声速值与乙醇体积分数并不存在线性关系。加入尿素,对不同体积分数乙醇溶液声速值影响不同,但不会影响任何乙醇溶液的总体变化趋势。乙醇体积分数越高,水分活度越低。随着乙醇体积分数的增加,4种体积分数乙醇溶液电导率呈下降趋势。随着贮存时间的延长,乙醇溶液微观结构不断变化。尽管本论文仅用NIR解释氢键作用略显匮乏,但从乙醇分子微观结构去解释乙醇产品质量特性,在食品领域具有较好的创新价值,具有重要的理论意义。
[1]KAPPATOS T,GORDON M H,BIRCH G G.Solution properties of vanillin and diacetyl in aqueous-ethanol solutions[J].Food Chem,1996,57(2):275-282.
[2]YASIN M H M,MAMAT R,YUSOP A F,et al.Fuel physical characteristics of biodiesel blend fuels with alcohol as additives[J]. Procedia Eng,2013,53(53):701-706.
[3]COCCIA A,INDOVINA P L,PODO F,et al.PMR studies on the structures of water-ethyl alcohol mixtures[J].Chem Phys,1975,7(1):30-40.
[4]NISIH,TAKAHASHI N,MATSUMOTO S,et al.Hydrogen-bonded cluster formation and hydrophobic solute association in aqueous solutions of ethanol[J].Chem Phys,1995,99(1):462-468.
[5] HARRIS K R,NEWITT P J,DERLACKI Z L.Alcohol tracer diffusion,density,NMR and FTIR studies of aqueous ethanol and 2,2,2-trifluoroethanol solutions at 25 ℃[J].Chem Soc,1998,94(14):1963-1970.
[6]赵勃,王永胜,李冲伟.沙枣替代部分玉米生产乙醇条件的优化[J].中国酿造,2019,38(8):152-156.
[7]YING P,ZHENG Y R,LI Z J,et al.Kaplan,Ethanol-induced coacervation in aqueous gelatin solution for constructing nanospheres and networks:Morphology,dynamics and thermal sensitivity[J].J Colloid Interface Sci,2021,582(2):610-618.
[8] SANGEETHA T,KANNAN P P,KARTHUCK K K,et al.Classical/nonclassical hydrogen bonds in xylene-ethanol solution:FTIR and theoretical approach[J].J Mol Liq,2020,312,1134-1140.
[9]王喆,刘洋,李先芝,等.在线近红外光谱在保健酒酒精度检测上的应用[J].食品工业科技,2016,37(21):291-293.
[10]ZHANPEISOV N U,TAKANASHI S,KAJIMOTO S,et al.On the origin of the Raman band shifts for H-bonded complexes of normal alcohols and 2-butoxyethanol with water:A theoretical DFT and MP2 study[J].Chem Phys Lett,2010,491(4-6):151-155.
[11]吴斌.荧光和拉曼光谱法研究乙醇-水溶液中的氢键作用和团簇结构[D].南京:南京理工大学,2011.
[12]KOCK F V C,ROCH T C,ARA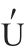 JO G M,et al.Time-domain NMR:A novel analytical method to quantify adulteration of ethanol fuel with methanol[J].Fuel,2019,258:10.1016/j.fuel.2019.116158.
JO G M,et al.Time-domain NMR:A novel analytical method to quantify adulteration of ethanol fuel with methanol[J].Fuel,2019,258:10.1016/j.fuel.2019.116158.
[13]HARADA M,NAKAMURA T,YANO K.Evaluating the internal structure of monodispersed mesoporous silica spheres by small-angle X-ray scattering[J].J Colloid Int Sci Comm,2019,33:10.1016/j.colcom.2019.100203.
[14]MILLARE J C,BASILIA B A.Dispersion and electrokinetics of scattered objects in ethanol-water mixtures[J].Fluid Phase Equilibr,2019,481:44-54.
[15]SISCO E,ROBINSON E L.Determination of ethanol concentration in alcoholic beverages by direct analysis in real time mass spectrometry(DARTMS)[J].Forensic Chem,2020,18:10.1016/j.forc.2020.100219.
[16]FAIZULLIN D A,KONNOVA T A,HAERTLÉ T,et al.Secondary structure and colloidal stability of beta-casein in microheterogeneous water-ethanol solutions[J].Food Hydrocoll,2017,63:349-355.
[17]LI F B,MEN Z W,LI S,et al.Study of hydrogen bonding in ethanol-water binary solutions by Raman spectroscopy[J]. Spectrochim Acta A,2018,189:621-624.
[18]林祉延.水活度用于食品质量与安全控制的研究进展[J].食品安全导刊,2019(36):86.
[19]龚英.金属盐—有机溶剂—水体系电导性和电转换性研究[D].大连:大连理工大学,2019.
[20]杨燕婷,王敏,周莹,等.超声光栅测量溶液中超声声速与浓度关系研究[J].实验技术与管理,2011,28(7):32-35.
[21]方衡鑫.基于氢键弛豫的有机/无机渗透剂水合作用机理研究[D].湘潭:湘潭大学,2019.
[22]PARKE S A,BIRCH G G.Solution properties of ethanol in water[J].Food Chem,1999,67(3):241-246.
[23]李敬,苏红,张晓梅,等.不同水分活度降低剂对大菱鲆即食制品的影响[J].食品科学,2017,38(22):269-274.
[24]李冲伟,宋福强,宋永,等.酒精发酵过程中电导率变化趋势解析[J].食品科学,2015,36(21):105-110.
[25] SCHOCK T,HUSSEIN M,HITZMANN B,et al.Influence of dissolved carbon dioxide on the sound velocity and adiabatic compressibility in aqueous solutions with saccharose and ethanol[J]. Mol Liq,2012,175(175):111-120.
[26]郭启凯,郭敏强,李超,等.乙醇-水溶液体系声速反常现象的机理分析[J].大学物理,2012,31(11):47-65.
[27]PEDRO B,SHANICA B,MARIELA M,et al.Partial molar volumes and isentropic compressions of sugar alcohols in aqueous solutions from 15 ℃to 40 ℃at atmospheric pressure[J].Food Chem,2019,280(280):805-811.
[28] SALTZMAN A,HOUSER H,LANGREHR M,et al.Nonpolar solute cononsolvency in ethanol/water mixtures-Connections to solvent structure[J].J Mol Liq,2019,298:10.1016/j.molliq.2019.111944.
[29]DIXIT S,POON W C K,CRAIN J.Hydration of methanol in aqueous solutions:a Ramans Spectroscopic study[J].J Phys-Condens Mat,1999,12:323-328.