红枣(Ziziphus jujuba Mill.)是李科枣属植物,枣果原产自中国[1]。红枣中含有丰富的有机酸、氨基酸[2]、维生素、矿物质和微量元素,以及大量的多糖、总酚、总黄酮类化合物[3]、环磷酸腺苷[4]、皂苷[5]等,具有抗衰老、抗肿瘤、护肝等的作用[6]。而红枣含糖量较高,并不适宜低糖人群食用,因此利用技术手段降低红枣含糖量就成为新的研究趋势。乳酸菌具有维持胃肠道菌群平衡、调节消化免疫系统、调节血糖等作用。采用乳酸菌发酵果汁可降低单糖含量,丰富产品口感,防止腐败,生成新的营养物质,从而提高保健价值[7]。余偲等[8]利用乳酸菌产γ-氨基丁酸的特点,生产出一种具有功能性成分的红枣乳酸菌饮品;周春峰等[9]利用复合乳酸菌发酵红枣,减少了自由基,提高了抗氧化活性。
代谢组学是以生物样品中的低分子质量代谢产物(如有机酸、脂肪酸、氨基酸、糖等)为研究对象,通过高通量检测和数据处理,进行信息整合及生物标记物鉴定的科学[10],由于气相色谱-质谱(gas chromatography-mass spec trometry,GC-MS)技术成本较低,具有重复性好、分辨率高、基体效应小的优点[11],已被广泛用于发酵食品中代谢物的定性和定量测定。如陈中等[12]利用嗜酸乳杆菌(Lactobacillus acidophilus)和植物乳杆菌(Lactobacillus plantarum)发酵西瓜汁,利用GC-MS技术测定主要挥发性物质,对比了不同乳酸菌发酵特性的差异;杨立启[13]采用GC-MS法比较了植物乳杆菌、嗜酸乳杆菌和副干酪乳杆菌发酵蜜桔的挥发性成分差异,以及三种乳酸菌对呈香呈味方面的作用。上述研究均表明基于气相色谱-质谱联用的代谢物分析有助于了解发酵产品的代谢物差异。
然而,目前关于发酵枣汁的报道主要集中经过发酵后风味物质变化,对发酵过程中代谢产物的差异以及动态变化的研究较少,本研究采用GC-MS结合多元统计分析方法,对发酵红枣汁在不同发酵阶段差异代谢物进行全面的鉴定与分析,以期深入了解发酵过程中风味形成、营养物质产生的潜在机制,为红枣乳酸菌发酵产品的功能性研发及其产业化发展提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
干红枣(Ziziphus jujube):宁夏同心路市场采购;嗜酸乳杆菌(Lactobacillus acidophilus):宁夏固原农家采集浆水,无菌离心管采样带回实验室,放于实验室4 ℃保存。
1.1.2 化学试剂
氯仿(色谱纯):北京沃凯生物科技有限公司;吡啶(色谱纯)、甲氧胺盐酸盐(分析纯)、L-2氯苯丙氨酸(分析纯):上海阿达玛斯试剂有限公司;双三甲基硅烷基三氟乙酰胺(bistrimethylsilane trifluoroacetamide,BSTFA)(1%三甲基氯硅烷(trimethylchlorosilane,TMCS))硅烷化试剂:美国Regis公司;甲醇、乙腈(均为色谱纯):美国Fisher Scientific公司;果胶酶(500 U/mg):上海源叶生物有限公司。
1.1.3 培养基
MRS肉汤培养基:青岛高科技工业园海博生物技术有限公司。
1.2 仪器与设备
BXM-30R立式压力蒸汽灭菌器:上海博讯实业有限公司;LRH-250生化培养箱:广东省医疗器械厂;Y66静音真空高速破壁机:九阳股份有限公司;Wonbio-96c多样品冷冻研磨仪:上海万柏生物科技有限公司;NewClassicMFMS105DU New Classic MS电子天平:瑞士METTLER TOLEDO公司;Centrifuge 5424 R高速冷冻离心机、(100~1 000)μL、(20~200)μL手动单道移液器:德国Eppendorf公司;JXDC-20氮吹仪:上海净信实业发展有限公司;8890B-5977B气相色谱-质谱联用仪:美国Agilent公司;TH2-D恒温振荡器:上海叶拓仪器仪表有限公司。
1.3 方法
1.3.1 菌株活化
将嗜酸乳杆菌在MRS固体培养基上进行划线后放入恒温培养箱,37 ℃条件下培养24 h,挑取固体培养基上的单菌落转接到MRS液体培养基中,经过两次MRS液体培养基继代培养进行扩培。
1.3.2 发酵枣汁的制备
将干红枣清洗干净、去核、切块,将清洗后的红枣按料液比1∶6(g∶mL)加水,在90 ℃条件下预煮20 min可使红枣充分软化,冷却到室温后,打浆机破碎,加入0.15%果胶酶,装入已灭菌的锥形瓶,进行巴氏杀菌,根据单因素响应面优化的发酵条件,按4%(V/V)接种量接入事先活化好的嗜酸乳杆菌,37 ℃条件下恒温培养12 h。将上述发酵汁放置-80 ℃,备用[14]。
1.3.3 发酵枣汁预处理
称取50 mg发酵枣汁样本,放入1.5 mL EP管中,加入40 μL内标(L-2-氯-苯丙氨酸0.3 mg/mL),加入360 μL冷甲醇,匀浆,冰水浴中超声提取30 min,加入200 μL的氯仿和400 μL的纯水,涡旋1 min,冰水浴中超声提取30 min,10 000 r/min、4 ℃条件下离心10 min,取400 μL上清液,室温挥干后衍生化。
1.3.4 不同发酵阶段枣汁中挥发性化合物分析
采用气相色谱质谱(GC-MS)联用仪对发酵枣汁进行代谢组学分析。
分别设置0 h(记为FJ-0 h)、18 h(记为FJ-18 h)、22 h(记为FJ-22 h)的不同发酵时间,并设置未发酵组(记为UFJ)及质控样品组(记为QC),每组样品采样5次,全部上机进行分析。
气相色谱条件:HP-5MS(5%-苯基)-甲基聚硅氧烷毛细管柱(30 m×0.25 mm×0.25 μm);进样量1 μL;不分流进样;载气:高纯氦气(He);流速1.0 mL/min;进样口温度260 ℃;程序升温:初始温度60 ℃,8 ℃/min 的速度升至310 ℃,并维持6 min。
质谱条件:电离方式为电子电离(electron ionization,EI)源;离子源温度230 ℃;四极杆温度150 ℃,电子能量70 eV;扫描类型:全扫描模式。
1.3.5 代谢物定性定量分析
GC-MS的原始数据经MassHunter软件进行预处理,导出CSV格式的三维数据矩阵,三维矩阵包括的信息有:样品信息、代谢物名称和质谱响应强度,内标峰以及任何已知的假阳性峰(包括噪音、柱流失和衍生物化试剂峰)均从数据矩阵中去除,并进行去冗余和峰合并。用峰面积归一化法对样本质谱峰的响应强度进行归一化,得到归一化后的数据矩阵。采用MassHunter workstation Quantitative Analysis(v10.0.707.0)软件进行代谢物注释、数据预处理等,最终得到代谢物列表及数据矩阵,结合T检验和正交偏最小二乘法-判别分析(orthogonal-partial least squares-discriminant analysis,O-PLS-DA)筛选出代谢物。进一步采用通路分析、关联分析、聚类分析等高级分析对代谢的生物学信息进行挖掘。
1.3.6 数据处理
筛选出的显著性代谢差异物根据其质荷比、保留时间(retention time,RT)和二级碎片信息通过Progenesis QI软件在HMDB(http://www.hmdb.ca/),ECMDB(http://ecmdb.ca/),YMDB(http://www.ymdb.ca/)与KEGG(http://www.kegg.jp/),Chem-spider(http://www.chemspider.com/)等数据库进行检索,确定其结构。
2 结果与分析
2.1 多元统计分析
主成分分析(principal component analysis,PCA)得分图的聚散程度反映了样本代谢物的相近程度,即发酵过程中代谢物的聚类情况,代谢水平越接近的点在得分图上越接近[15]。将未发酵枣汁、嗜酸乳杆菌发酵枣汁0 h、18 h、22 h进行PCA,结果见图1。由图1可知,样品PCA中模型对X变量差异解释能力R2为0.651>0.5,表明模型的拟合准确性好,且得分图的所有样品均在椭圆内,说明分析的样品中没有异常值。随着发酵时间的延长,由于代谢物之间的相互作用,产生酸等各种风味物质,导致未发酵、0 h和18 h样本之间存在明显分离。而发酵18 h和22 h后的样本在得分图上区分不明显,可能是原料中的糖基本被消耗,代谢物变化缓慢。
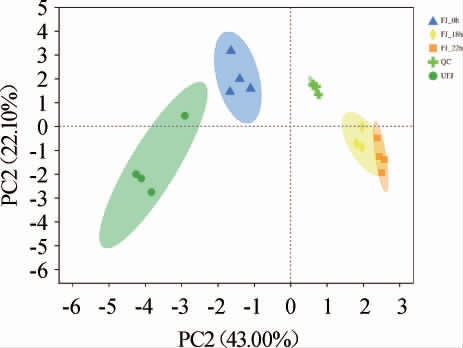
图1 不同发酵阶段代谢物主成分分析结果
Fig.1 Results of principle component analysis for metabolites in different fermentation stages
2.2 嗜酸乳杆菌发酵枣汁过程中挥发性成分O-PLS-DA结果
对嗜酸乳杆菌发酵枣汁过程中的挥发性成分进行主成分分析和聚类分析,可将发酵分为四个阶段:未发酵、0 h、18 h、22 h。因此将发酵过程中的样品进行归类,利用O-PLS-DA进行分析,可以得出发酵枣汁各阶段的主要呈味香气成分,不同发酵时间O-PLS-DA得分结果见图2。由图2可以看出,此模型共提取4个预测成分,这4个预测成分的累计统计量所建模型对X矩阵的解释能力R2为0.788,说明该模型对挥发性成分矩阵的解释能力R2为0.788;所建模型对Y矩阵的解释能力R2为0.998,说明该模型对发酵过程中样品矩阵的解释能力R2为0.998;模型的预测能力Q2为0.978。通常R2和Q2>0.50拟合准确性较好,>0.4即可接受,预测该模型在本实验中的拟合准确性极高。
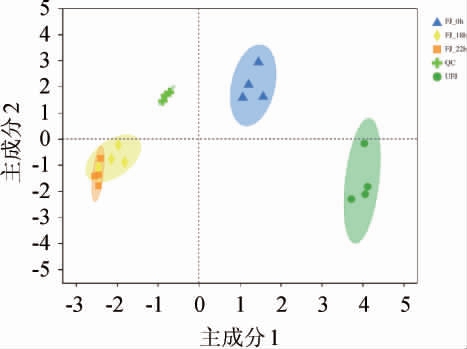
图2 不同发酵阶段代谢物正交偏最小二乘法-判别分析结果
Fig.2 Results of orthogonal partial least squares-discriminant analysis for metabolites in different fermentation stages
2.3 差异代谢物筛选与分析
基于O-PLS-DA模型分析结果,将P值<0.05的代谢物作为后发酵阶段的差异代谢物,结果共鉴定出29种显著差异代谢物。其中有机酸4种,苯环化合物3种,酯类物质2种,有机杂环化合物2种,碳氧化合物1种,其他种类化合物15种。不同发酵阶段差异代谢物含量如表1所示。
表1 枣汁不同发酵阶段差异代谢物
Table1 Different metabolites of jujube juice in different fermentation stages
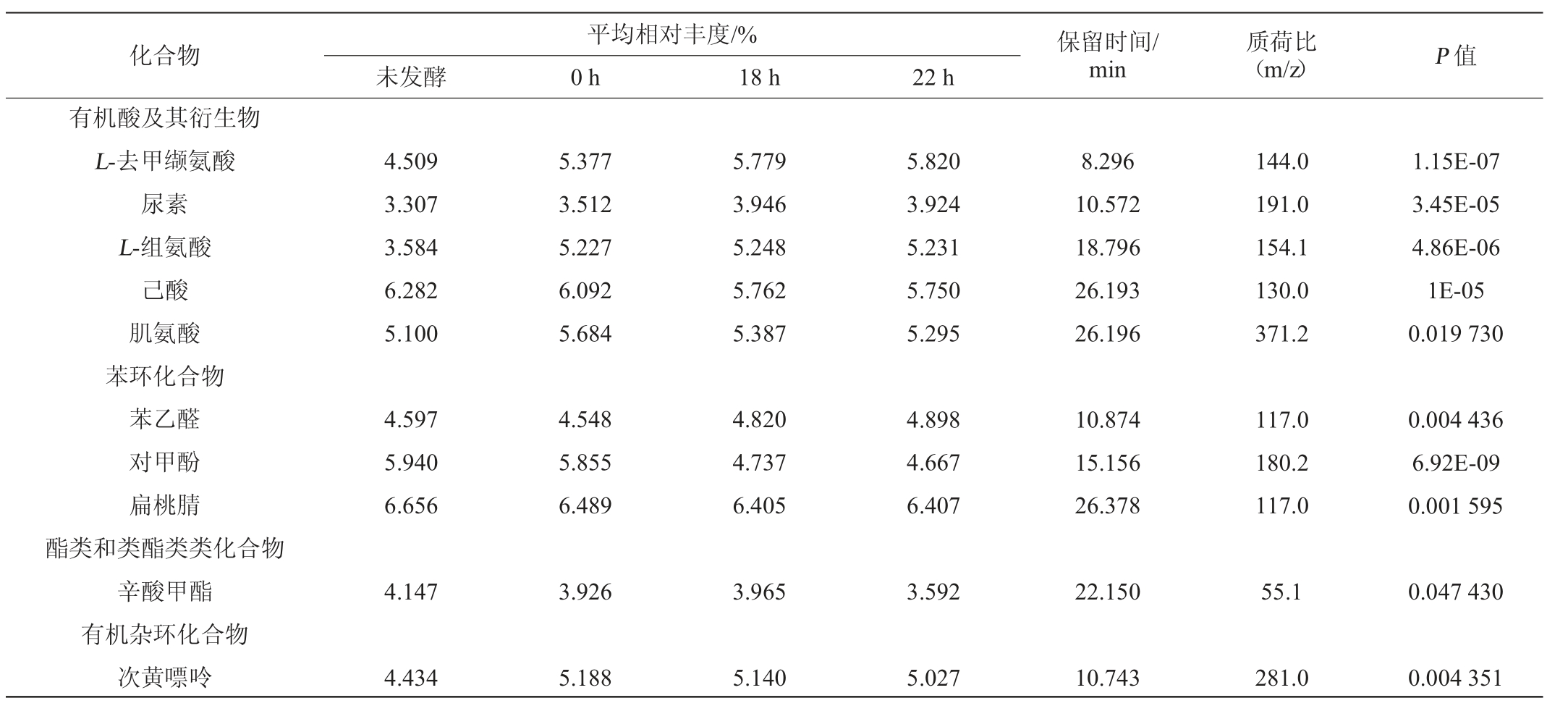
续表

差异代谢物在不同阶段相对丰度变化的聚类分析见图3,左侧为代谢物聚类的树状图,右侧为代谢物的名称,同一代谢物在不同时间段,蓝色表示表达量降低,红色表示表达量升高。由图3可知,随着发酵时长增长,代谢物表达量逐渐增加,18 h和22 h代谢物表达相似。
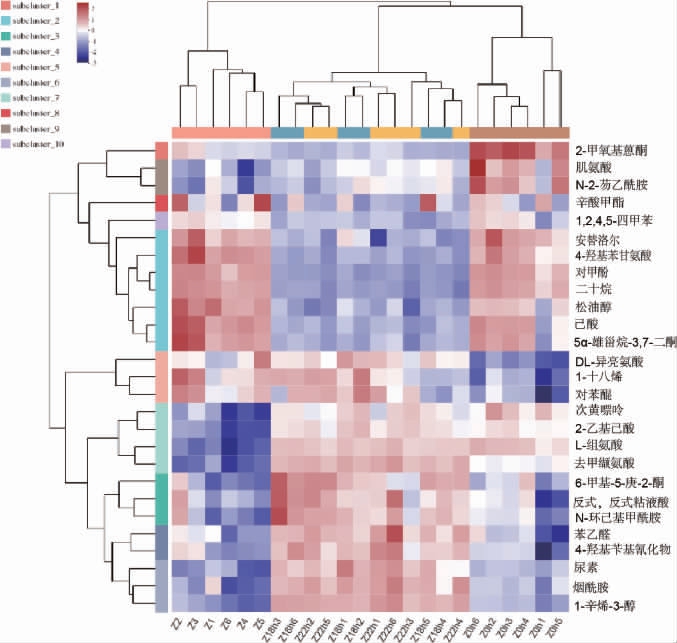
图3 枣汁不同发酵阶段差异代谢物聚类分析
Fig.3 Cluster analysis of differential metabolites of jujube juice in different fermentation stages
Z:未发酵枣汁;Z0:接菌0 h发酵枣汁;Z18:接菌18 h发酵枣汁;Z22:接菌22 h发酵枣汁。
在发酵乳发酵过程中产生的酸类化合物主要来源于脂肪分解、蛋白质水解等代谢途径[16]。有机酸在风味方面更显较大。由图3可知,通过嗜酸乳杆菌与红枣协同发酵可产生更多具有酸败气味[17]的己酸,在发酵过程中己酸含量逐渐降低,说明通过嗜酸乳杆菌发酵可减弱不良气味,有利于风味的提升。
风味物质方面,在发酵过程中,辛酸甲酯的含量由高降低,辛酸甲酯具有柑香与酒香味[18]。另外发现一种与3-苯乳酸类似的物质苯乙醛,它是一种具有浓郁玉簪花香气的风味物质[19],在发酵初期阶段相对含量提高,赋予发酵产品独特风味,它通过苯丙氨酸代谢途径产生,苯丙氨酸代谢途径与酚类化合物合成有关。对甲酚具有臭味,在发酵过程中含量下调。松油醇具有花香,是常见香料,经过发酵后,含量降低。1-辛烯-3-醇具有蘑菇、薰衣草、玫瑰和干草的香气[20],在发酵枣汁产品挥发性成分中常见,随着发酵时间延长,相对丰度增加。1-十八烯是一种马铃薯苗所具有的挥发性物质,在发酵过程中代谢被抑制。这些香气物质通过发酵在发酵产品所含浓度增加,促进了良好风味的形成。
氨基酸具有缩短发酵时间赋予了发酵产品更多的营养物质的作用[21]。虽然氨基酸并非发酵乳的挥发性风味物质,但作为挥发性化合物的前体物质,能够进一步转化成醇类、醛类、酯类和硫化物等物质,且对发酵产品的滋味具有的较大贡献[22]。去甲缬氨酸、L-组氨酸在发酵过程中上调。肌氨酸在发酵过程中含量降低,与甘氨酸代谢有关。
2.4 关键代谢物分析
为了深入了解发酵枣汁发酵阶段潜在代谢途径,进行差异代谢物的代谢途径分析,结果见图4。由图4可知,通路分析结果显示共获得26个途径,基于重要性分析,对关键代谢途径进行筛选,筛选出12条在嗜酸乳杆菌发酵红枣过程重要的代谢通路,这些途径包括:组氨酸代谢、苯乙烯降解、烟酸和烟酰胺代谢、精氨酸生物合成、甲苯降解、苯丙氨酸代谢、阿特拉津降解、嘌呤代谢、甘氨酸、丝氨酸和苏氨酸代谢、苯甲酸降解、精氨酸和脯氨酸代谢、嘧啶代谢。其中重要的代谢物分别为L-组氨酸、去甲缬氨酸、尿素、次黄嘌呤、褪黑素、烟酰胺。
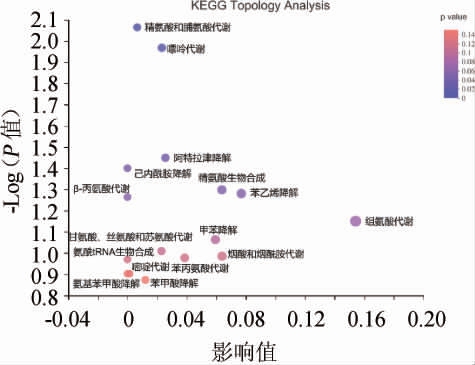
图4 枣汁不同发酵阶段差异代谢物京都基因与基因组百科全书拓扑学分析气泡图
Fig.4 Bubble chart of Kyoto encyclopedia of genes and genomes topological analysis of differential metabolites of jujube juice in different fermentation stages
影响值:表示通路中代谢物在通路中的相对重要性的大小;-log10(P 值):代谢物参与通路的富集显著性大小。
L-组氨酸作为氨基酸代谢的重要产物,在红枣发酵过程中参与了其中6条KEGG代谢通路,分别为β-丙氨酸代谢、组氨酸代谢、氨酰tRNA生物合成、植物次生代谢产物的生物合成、组氨酸和嘌呤生物碱的生物合成。其中重要的代谢物分别为L-组氨酸、去甲缬氨酸、尿素、次黄嘌呤。肌肽通过β-丙氨酸代谢生成L-组氨酸和β-丙氨酸,肌肽具有调节血糖的功效。在接菌后产生此代谢通路,猜测嗜酸乳杆菌可能通过分解乳酸菌中肌肽产生L-组氨酸。
去甲缬氨酸是一种非蛋白源性支链氨基酸,非蛋白质氨基酸在生物体内可参与储能、形成跨膜离子通道和充当神经递质,乳酸菌具有较强的精氨酸代谢能力,通过精氨酸脱亚胺途径可产生尿素[23]。尿素作为代谢过程中的终产物,在发酵过程中注释到8条KEGG代谢通路,包括精氨酸、脯氨酸、嘌呤、嘧啶、甘氨酸、丝氨酸、苏氨酸、苯丙氨酸代谢通路、阿特拉津降解。
次黄嘌呤氧化酶氧化次黄嘌呤生成黄嘌呤,进一步氧化黄嘌呤生成尿素。黄嘌呤氧化酶在催化多种不同底物的氧化时,除了生成产物尿酸之外,还形成超氧自由基和过氧化氢[24]。接菌0 h次黄嘌呤含量升高,尿素含量升高,黄嘌呤氧化酶含量增加,菌株自身可能具有产次黄嘌呤氧化酶的作用,随着发酵时间增长,次黄嘌呤表达丰度降低,产生的代谢物对黄嘌呤氧化酶有抑制作用。
褪黑素是一种强氧化剂强,有超强的抗氧化清除能力,具有抗衰老、调节睡眠、抗肿瘤等作用。在参与色氨酸代谢过程中,4个连续酶促反应生成褪黑素。随着发酵时间增长,枣汁中的pH降低。pH偏酸会提高褪黑素水平[25]。研究证明,褪黑素含量少,多酚、黄酮等抗氧化物质含量增加。YU Z等[26]研究发现,在甜樱桃果实发育周期内,褪黑素含量与丙二醛含量呈现出反比的关系。乳酸菌具有提高多酚、黄酮物质等抗氧化物质含量的作用。为开发功能性发酵产品提供依据。
烟酰胺参与生物体内糖原分解、脂类代谢及各种物质的氧化作用[27],是一种潜在抗氧化性物质,注释到一条代谢通路为烟酸和烟酰胺代谢。随着发酵时间增加,含量增加,说明通过嗜酸乳杆菌的发酵,抗氧化能力被逐渐提高。
3 结论
本研究采用GC-MS技术对嗜酸乳杆菌发酵红枣汁各阶段的代谢物进行分析。结果表明,在未发酵、发酵0 h、18 h、22 h这4个时间点中有12条代谢通路具有重要作用,其中筛选出关键代谢物为L-组氨酸、去甲缬氨酸、尿素、次黄嘌呤、褪黑素、烟酰胺。辛酸甲酯、苯乙醛、松油醇、1-辛烯-3-醇、1-十八烯作为呈香作用的酯类物质和醛类物质随着发酵时间增加对乳酸菌饮料特殊风味形成发挥重要作用。烟酰胺、褪黑素等具有强抗氧化能力的物质,为产品功能性开发提供依据,去甲缬氨酸、L-组氨酸、肌氨酸、肌肽等有机酸、氨基酸、多肽类等生物活性物质的含量变化为益生菌饮料的生产提供一定的技术支撑和理论指导。
[1]郭佳欣,张培基,刘丁玉,等.常压室温等离子体诱变选育高产核黄素枯草芽孢杆菌[J].食品与发酵工业,2020,46(4):28-33.
[2]冯新光,吕吉鸿,郭泽峰,等.中国不同产地红枣的组分分析与评价[J].中国酿造,2012,31(9):30-33.
[3]CHENG D,ZHU C Q,CAO J K,et al.The protective effects of polyphenols from jujube peel(Ziziphus jujube Mill)on isoproterenol-induced myocardial ischemia and aluminum-induced oxidative damage in rats[J].Food Chem Toxicol,2012,50(5):1302-1308.
[4]PAREEK S.Nutritional composition of jujube fruit[J].Emir J Food Agric,2013,25(6):463-470
[5]刘子祯,姜蕊,刘伟锐,等.红枣叶中三萜皂苷的提取工艺和含量测定研究[J].食品研究与开发,2016,37(1):57-59.
[6]靳玉红,李志西,乔艳霞,等.红枣乳酸发酵饮料的抗氧化活性[J].西北农林科技大学学报(自然科学版),2016,44(1):199-205.
[7] HOU Y P,GAO J L,GU L.Effects of agaro-oligosaccharide treatment on postharvest quality of cherry tomatoes during cold storage[J].J Food Process Pres,2015,39(6):949-955.
[8]余偲,赵育,张晶,等.红枣汁乳酸菌发酵生产γ-氨基丁酸的研究[J].西北农业学报,2020,29(2):266-275.
[9]周春峰,郭倩,吕行,等.红枣汁/饮料发酵过程中抗氧化活性变化的研究[J].河南农业大学学报,2019,53(6):973-977.
[10]王鹏飞,王倩倩,李先恩,等.GC-MS 技术在延胡索块茎代谢产物研究中的应用[J].植物学报,2012,47(2):149-154.
[11]KOPKA J.Current challenges and developments in GC-MS based metabolite profiling technology[J].J Biotechnol,2006,124(1):312-322.
[12]陈中,徐柳柳,林伟锋.两种乳杆菌发酵西瓜汁挥发性风味物质的研究[J].现代食品科技,2016,32(3):291-299.
[13]杨立启.益生菌发酵柑橘全果汁中抗氧化活性和挥发性物质研究[D].杭州:浙江工业大学,2019.
[14]陆冉冉,刘慧燕,潘琳,等.响应面法优化乳酸片球菌TK530 发酵红枣浆工艺[J].南方农业学报,2020,51(9):2245-2253.
[15]CEBOLLERO E,CARRASCOSA A V,GONZALEZ R.Evidence for yeast autophagy during simulation of sparkling wine aging:a reappraisal of the mechanism of yeast autolysis in wine[J]. Biotechnol Progr,2005,21(2):614-616.
[16] CURIONI P M G,BOSSET J O.Key odorants in various cheese types as determined by gas chromatography-olfactometry[J].Int Dairy J,2002,12(12):959-984.
[17]徐亦秀,张慜,孙金才.固相微萃取与气质联用法分析杨梅汁饮料中不良风味成分[J].食品与生物技术学报,2012,31(10):1057-1061.
[18]沈燕飞.乳酸菌发酵苹果原浆过程中的基本组分与抗氧化活性变化[D].杭州:浙江工业大学,2019.
[19]校大伟,成春雷,张金,等.苯乙醛合成研究进展[J].化学试剂,2008,30(12):899-902.
[20]王娟,赵江,陈见容,等.红枣杜仲复合饮料的配方优化及其风味物质分析[J].食品工业科技,2019,40(2):215-222.
[21]王越男,米智慧,李常坤,等.植物乳杆菌P-8 发酵乳的代谢物图谱[J].中国食品学报,2021,21(1):236-245.
[22]陈洁,赵建新,陈卫,等.中温发酵酸乳的游离氨基酸、脂肪酸和感官特性的研究[J].食品与发酵工业,2008,34(7):28-33.
[23]方若思.传统黄酒发酵中氨基甲酸乙酯产生的代谢规律及抑制方法研究[D].杭州:浙江大学,2017.
[24]王成华,邢新会.黄嘌呤氧化酶的研究进展及其发展前景[J].广西科学,2017,24(1):15-24.
[25]ARNAO M B,HERNÁNDEZ-RUIZ J.Chemical stress by different agents affects the melatonin content of barley roots[J].J Pineal Res,2009,46(3):295-299.
[26] ZHAO Y,TAN D X,LEI Q,et al.Melatonin and its potential biological functions in the fruits of sweet cherry[J].J Pineal Res,2013,55(1):79-88.
[27]李倩,权博文,常虹,等.扁桃属植物的化学成分及药理作用研究进展[J].中国药房,2020,31(21):2683-2688.