葡萄酒酿造过程中会产生大量副产物(葡萄皮渣),占鲜果质量的25%左右,每年产生的葡萄皮渣超过900万t[1]。葡萄皮渣中含有丰富的脂质、蛋白质、膳食纤维和多种酚类物质,尤其是其中的酚类物质具有抗氧化、抗炎、抑菌及抗癌等多种生物活性[2]。葡萄皮渣中的酚类物质主要分布在葡萄籽中,葡萄籽中的酚类物质主要是黄烷-3-醇类[3-4]。然而,目前酿酒葡萄皮渣主要被用作植物肥料[5]、牲畜饲料[6-7],甚至被当作废弃垃圾,这些处理方式会造成土壤酸化、板结以及生态环境污染等负面影响,同时也导致了资源的严重浪费。
目前,植物基质中多酚化合物的提取主要采用有机溶剂提取法,或者是借助物理方法辅助提取。然而有机溶剂提取法存在许多缺点,如较高挥发性、毒性、可燃性以及较低生物降解率等。低共熔溶剂(deep eutectic solvents,DESs)是一类环境友好的新型绿色溶剂,其通常由氢供体(hydrogenbonddonor,HBD)和氢受体(hydrogenbondacceptor,HBA)组成,溶剂熔点比其中任一组分的熔点都低,因此在室温下能以液态形式稳定存在[8]。相比有机溶剂,DESs易于合成、成本低、稳定性好、不易挥发、可生物降解、绿色环保,近年来引起越来越多的人关注,并广泛应用于天然产物的提取研究中[9-10]。焦晓波等[11]合成了4种DES溶剂用来提取芝麻渣中的芝麻蛋白,相比传统的碱溶酸沉法,其中醋酸钠和尿素形成的DES对芝麻蛋白的提取纯度较高,说明DESs可以作为一种绿色新型的植物蛋白提取溶剂。周萍等[12]利用DESs提取桑葚果渣中的花色苷,发现草酸-氯化胆碱对桑葚果渣花色苷的提取率最高,经大孔树脂分离后,回收率达到92.76%。孙悦等[13]采用超声辅助低共熔溶剂法,优化提取甘草中多糖的工艺条件,在含水量为40%,物质的量比为1∶3的氯化胆碱-异丙醇溶剂,提取温度39 ℃、料液比1∶50(g∶mL)、超声时间30 min、超声功率250 W条件下,对多糖的提取率高达8.31%。
本研究首先合成不同的DESs,采用合成的DESs结合超声辅助法提取赤霞珠葡萄籽多酚,分析不同DESs对葡萄籽的酚类化合物提取及体外抗氧化活性的影响,为酿酒葡萄皮渣中多酚的高效提取及基于多酚的酿酒葡萄废弃物资源化利用奠定基础。
1 材料与方法
1.1 材料与试剂
赤霞珠葡萄皮渣(手动分离得到赤霞珠葡萄籽,置于烘箱内,50 ℃烘干48 h,经粉碎、过筛(18目),避光储存在-80 ℃冰箱,待用):由宁夏贺兰山东麓保乐力加酒厂提供;没食子酸、氯化胆碱、脯氨酸、甜菜碱、甘油、乳酸、三乙二醇、乙酰丙酸、乙二醇、1,3-丁二醇、1,4-丁二醇(均为分析纯):上海阿拉丁生化科技股份有限公司;丁香酸、儿茶素、表儿茶素、没食子酸、原花青素B1、原花青素B2(均为色谱纯):上海阿拉丁生化科技股份有限公司;甲醇(MeOH)、乙醇(EtOH)(均为分析纯)、四川西陇科学有限公司;1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)(分析纯):北京索莱宝科技有限公司;2,2'-联氮-双-3-乙基苯并噻唑啉-6-磺酸(2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid,ABTS)(分析纯):上海阿拉丁生化科技股份有限公司。
1.2 仪器与设备
BJ-150小型粉碎机:济南柏盛生物科技有限公司;78-1加热磁力搅拌器:常州国华电器有限公司;KQ-300DE数控超声波清洗器:昆山市超声仪器有限公司;Cary60紫外可见分光光度计:美国Agilent Technologies公司。
1.3 方法
1.3.1 DESs合成
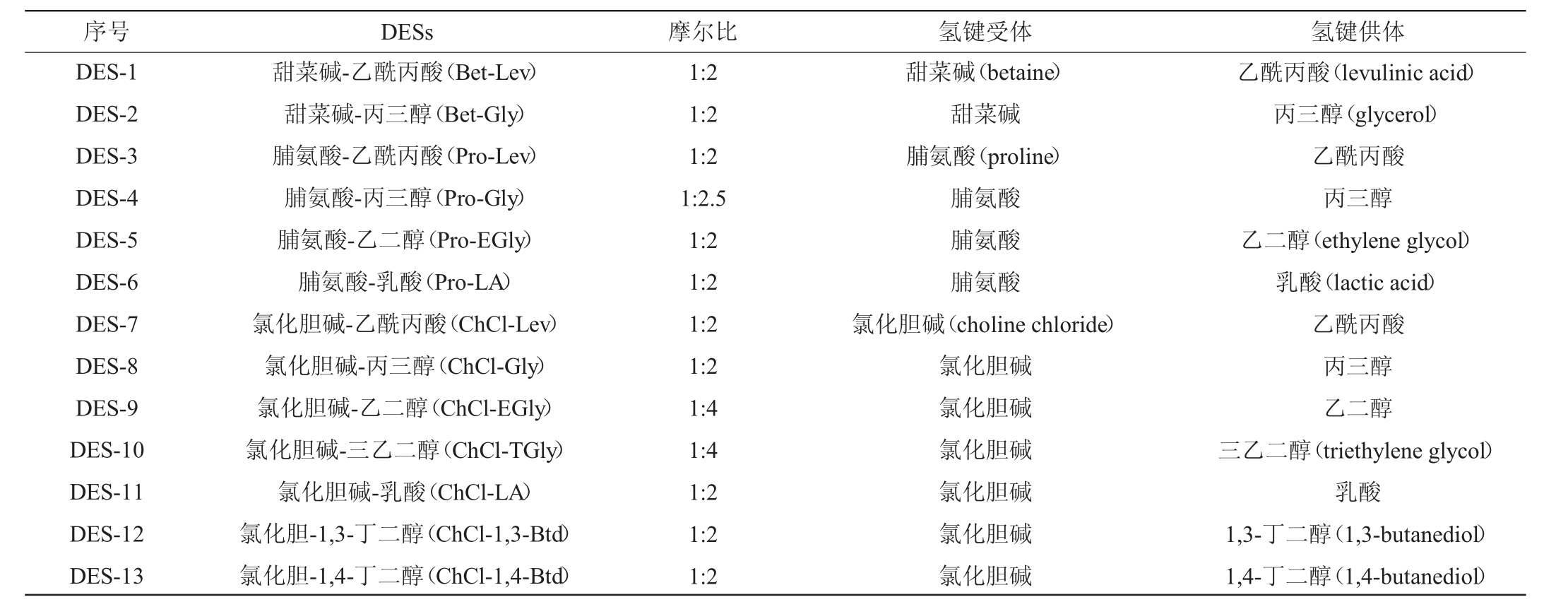
按照表1中的摩尔比合成相应的低共熔溶剂[14-16](DES-1~DES-13),使用磁力加热搅拌器加热至80 ℃,搅拌3~5 h,直至形成均一透明的溶液,合成的低共熔溶剂稳定12 h后,用去离子水稀释后待用。
表1 低共熔溶剂合成列表
Table1 List of deep-eutectic solvents composition
1.3.2 葡萄籽多酚超声辅助提取流程
准确称量0.500 g葡萄籽粉末置于15 mL离心管中。分别加入5 mL稀释后的DESs,并以水、体积分数均为80%乙醇和甲醇作为对照,在超声功率300 W、超声温度40 ℃条件下提取30 min[16],提取液于10 000 r/min离心5 min后,过0.22 μm有机滤膜,用于后续分析。
1.3.3 总酚含量测定
总酚含量测定采用福林酚法[17]。取1 mL适当稀释后的提取液,加入0.5 mL福林酚试剂,混匀后放置5 min,加入1.5 mL20%的碳酸钠溶液,混匀后用去离子水定容至10 mL,室温下静置1 h后在765 nm波长条件下测定吸光度值。用不同质量浓度没食子酸溶液(10~100 mg/L)代替样品溶液制作标准曲线,以没食子酸含量(x)为横坐标、吸光度值(y)为纵坐标绘制没食子酸标准曲线,得到没食子酸标准曲线回归方程为y=0.011 2x+0.052 2,相关系数R2=0.997 2。按照标准曲线回归方程计算样品中总酚含量,结果以mg没食子酸当量(gallic acid equivalent,GAE)/100 g表示,以干基计。
1.3.4 总黄酮含量测定
总黄酮含量测定采用分光光度法[18]。取200 μL稀释后的提取液,加入800 μL体积分数为80%的乙醇溶液,然后加入60 μL 5%亚硝酸钠溶液,混匀后放置5 min,加入60 μL 10%三氯化铝溶液,混匀,放置6 min,加入400 μL 1.0 mol/L氢氧化钠溶液,加入480 μL体积分数为80%乙醇,混匀,室温下避光反应30 min,在510 nm波长处测定吸光度值,用不同质量浓度(50~400 mg/L)的儿茶素溶液制作标准曲线,以儿茶素含量(x)为横坐标、吸光度值(y)为纵坐标绘制儿茶素标准曲线,得到儿茶素标准曲线回归方程为y=0.002 7x-0.007 1,相关系数R2=0.999。按照标准曲线回归方程计算样品中总黄酮含量,结果以mg儿茶素当量(catechin equivalent,CE)/100 g表示,以干基计。
1.3.5 单体酚含量测定
单体酚含量测定采用高效液相色谱(high performance liquidchromatography,HPLC)法[19]。HPLC色谱条件为:Waters-C18反相色谱柱(250 mm×4.6 mm,5 μm),柱温30 ℃;样品进样体积20 μL;流动相A:2%(V/V)乙酸溶液,流动相B:2%(V/V)乙酸-乙腈溶液;流速1 mL/min,采取梯度洗脱(0 min,5%B;40 min,20%B;55 min,27.5%B;65 min,50%B;66~71 min,80%B;73~78 min,5%B)。通过外标法,对比6种单体酚标准品的保留时间,确定色谱峰代表的物质种类,通过峰面积计算出物质的含量。
1.3.6 体外抗氧化活性测定
DPPH自由基清除活性测定:取250 μL稀释后的样品加入2 mL 100 μmol/L的DPPH溶液,混匀,避光反应30 min,于517 nm波长条件下测定吸光度值,用不同摩尔浓度(0~300 μmol/L)的维生素C溶液制作标准曲线,以维生素C含量(x)为横坐标、吸光度值(y)为纵坐标绘制维生素C标准曲线,得到维生素C标准曲线回归方程(y=-2.865 3x+1.079 0,相关系数R2=0.999 5),照标准曲线回归方程计算样品的DPPH自由基的清除能力,结果以mg 维生素C当量(vitamin C equivalent,VCE)/100 g表示[20],以干基计。DPPH自由基清除率计算公式如下:
式中:A空白是DPPH纯溶液在波长517 nm条件下的吸光度值,A样品是反应液在波长517 nm条件下的吸光度值。
ABTS+自由基清除活性测定:配制2.45 mmol/L的过硫酸钾溶液和7 mmol/L的ABTS的溶液,等体积混匀,室温下避光反应16 h得新鲜的ABTS+溶液,使用时用无水乙醇稀释至波长734 nm条件下吸光度值为0.70±0.02。取2 mLABTS+溶液,加入500 μL适当稀释后的提取液,混匀后,室温避光反应10 min,于734 nm波长处测定吸光度值,用不同摩尔浓度(0~60 μmol/L)的维生素C溶液制作标准曲线,以维生素C含量(x)为横坐标、吸光度值(y)为纵坐标绘制维生素C标准曲线,得到维生素C标准曲线回归方程(y=-3.219 7x+0.570 0,相关系数R2=0.999 8),按照标准曲线回归方程计算样品的ABTS+自由基的清除能力,自由基的清除能力以mg VCE/100 g表示[20],以干基计。ABTS+自由基清除率计算公式如下:
式中:A空白是ABTS+自由基纯溶液在波长734 nm条件下的吸光度值,A样品是反应液在波长734 nm条件下的吸光度值。
1.3.7 数据处理
每组实验均重复3次,结果以均值±标准差表示。采用SPSS 20.0软件进行数据统计分析,运用GraphPad Prism 8.0软件进行作图。
2 结果与分析
2.1 不同溶剂对赤霞珠葡萄籽总酚提取的影响
体积分数为80%甲醇、体积分数为80%乙醇和水是植物多酚最常用的提取溶剂,因此本研究中将DESs作为提取溶剂的提取量与上述常见提取溶剂进行对比,赤霞珠葡萄籽不同溶剂提取物中总酚含量检测结果见图1。
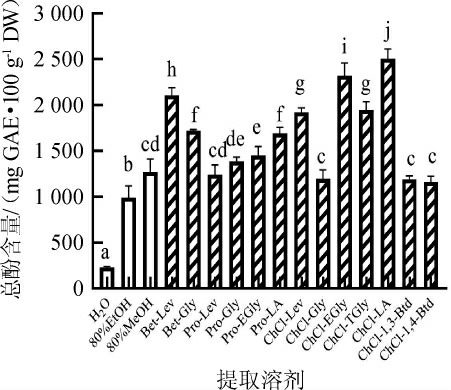
图1 葡萄籽不同溶剂提取物中总酚含量
Fig.1 Total phenol contents in different solvents extracts of grape seed
不同小写字母表示不同提取溶剂葡萄籽提取物中总酚含量差异显著(P<0.05)。
由图1可知,多数DESs对赤霞珠葡萄籽总酚的提取量远高于传统有机溶剂(体积分数为80%乙醇、体积分数为80%甲醇)。氯化胆碱-乳酸(ChCl-LA)、氯化胆碱-乙二醇(ChCl-EGly)和甜菜碱-乙酰丙酸(Bet-Lev)对总酚的提取量较高,分别为2 505.13 mg GAE/100 g、2 323.96 mg GAE/100 g和2109.93mgGAE/100 g,这可能与DESs的极性有关[21-22],氯化胆碱-乳酸(ChCl-LA)提取物中总酚含量分别比体积分数为80%乙醇和体积分数为80%甲醇提高了154%和97%。大多数有机酸作为氢键供体的DESs对赤霞珠葡萄籽总酚的提取量高于甘油作为氢键供体的DESs,如总酚含量:甜菜碱-乙酰丙酸(Bet-Lev)>甜菜碱-丙三醇(Bet-Gly)、脯氨酸-乳酸(Pro-LA)>脯氨酸-丙三醇(Pro-Gly)、氯化胆碱-乙酰丙酸(ChCl-Lev)>氯化胆碱-丙三醇(ChCl-Gly)、氯化胆碱-乳酸(ChCl-LA)>氯化胆碱-丙三醇(ChCl-Gly)。这可能与有机酸作为氢键供体的DESs能与多酚形成较强的氢键作用有关[23-24]。
2.2 不同溶剂对赤霞珠葡萄籽总黄酮提取的影响
赤霞珠葡萄籽不同溶剂提取物中总黄酮含量检测结果见图2。
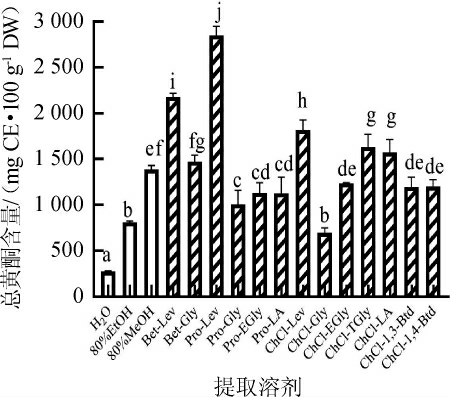
图2 葡萄籽不同溶剂提取物中总黄酮含量
Fig.2 Total flavonoid contents in different solvents extracts of grape seed
不同小写字母表示不同提取溶剂葡萄籽提取物中总黄酮含量差异显著(P<0.05)。
由图2可知,脯氨酸-乙酰丙酸(Pro-Lev)(2 849.444 5 mg CE/100g)、甜菜碱-乙酰丙酸(Bet-Lev)(2181.713mgCE/100g)和氯化胆碱-乙酰丙酸(ChCl-Lev)(1 819.44 mg CE/100 g)对总黄酮的提取量较高,氯化胆碱-三乙二醇(ChCl-Tgly)(1 633.18 mg CE/100 g)和氯化胆碱-乳酸(ChCl-LA)(1 571.45 mg CE/100 g)次之。这些DESs对总黄酮的提取量均显著高于体积分数为80%甲醇(1 385.80 mg CE/100 g)、体积分数为80%乙醇(811.98 mg CE/100 g)和水(274.84 mg CE/100 g)。其中脯氨酸-乙酰丙酸(Pro-Lev)提取物中总黄酮含量分别比体积分数为80%乙醇和体积分数为80%甲醇提高了251%和106%。
2.3 赤霞珠葡萄籽不同溶剂提取物中主要酚类化合物的定量分析
研究表明,酚类化合物的组成和含量与提取溶剂的类型有关[25-26]。赤霞珠葡萄籽不同提取溶剂提取物中单体酚类物质检测的HPLC色谱图见图3,不同提取溶剂提取物中主要单体酚类化合物(没食子酸、儿茶素、表儿茶素、原花青素B1、原花青素B2、丁香酸)的定量分析结果见表2。
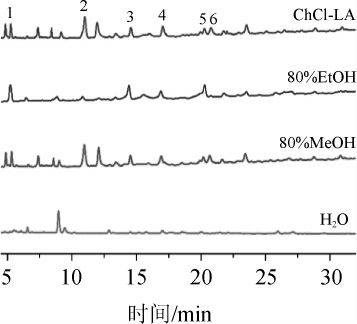
图3 葡萄籽不同提取溶剂提取物中主要单体酚类化合物的高效液相色谱图
Fig.3 High performance liquid chromatograms of main monomer phenolic compounds in different solvents extracts of grape seed
峰1:没食子酸,峰2:原花青素B1,峰3:儿茶素,峰4:原花青素B2,
峰5:丁香酸,峰6:表儿茶素。
表2 葡萄籽不同溶剂提取物中主要单体酚类化合物的含量
Table2 Main monomer phenolic compounds contents in different solvents extracts of grape seed
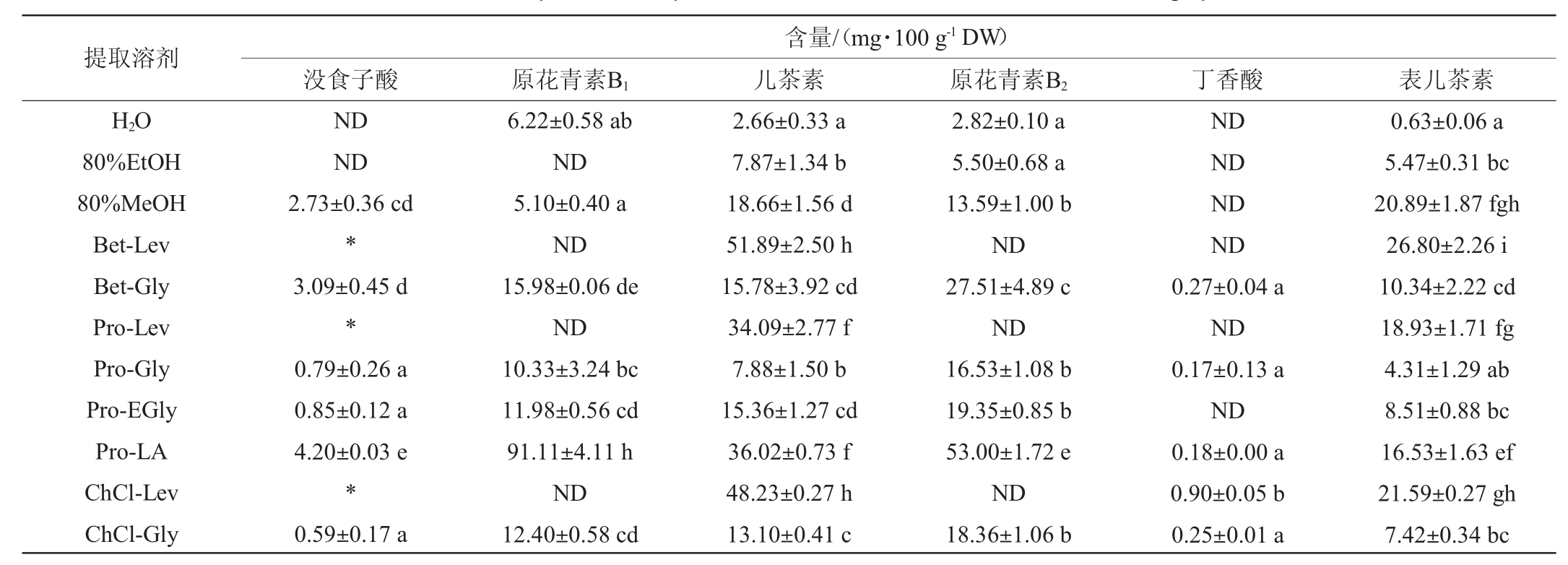
续表
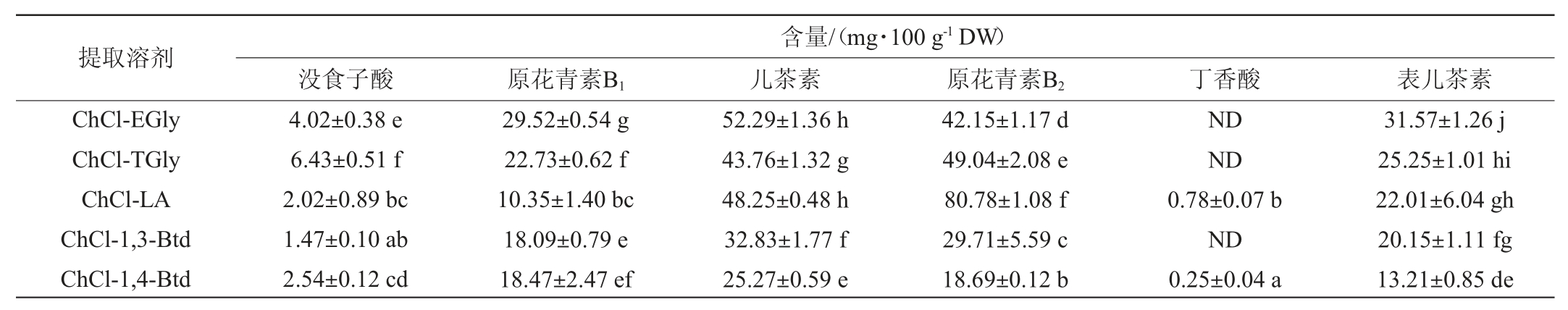
注:不同小写字母表示不同提取溶剂葡萄籽提取物中主要酚类化合物含量的差异显著性(P<0.05);“ND”表示未检出。“*”由于在没食子酸出峰附近有一个高响应值物质,导致无法定量。
由图3及表2可知,对于常规提取溶剂,体积分数为80%的甲醇提取物中单体酚含量较高,H2O提取物中单体酚含量最低。DESs提取物中单体酚的含量显著高于常规提取溶剂(P<0.05),其中氯化胆碱-三乙二醇(ChCl-TGly)中没食子酸含量最高(6.43 mg/100 g),脯氨酸-乳酸(Pro-LA)中原花青素B1含量最高(91.11 mg/100 g),氯化胆碱-乳酸(ChCl-LA)中原花青素B2的含量最高(80.78 mg/100 g),氯化胆碱-乙二醇(ChCl-EGly)中儿茶素(52.29 mg/100 g)、表儿茶素含量最高(31.57 mg/100 g)。较传统溶剂而言,作为赤霞珠葡萄籽酚类物质的提取溶剂,DESs对酚类物质的提取量更高。
2.4 赤霞珠葡萄籽不同溶剂提取物体外抗氧化能力
本研究采用DPPH和ABTS+自由基清除结果表征赤霞珠葡萄籽不同溶剂多酚提取物的体外抗氧化能力。DPPH和ABTS+自由基清除能力的结果表现出良好的一致性。由图4和表3可知,氯化胆碱-乙二醇(ChCl-EGly)(DPPH,3 873.89 mg VCE/100 g;ABTS+,8 898.49 mg VCE/100 g)、脯氨酸-乙二醇(Pro-EGly)(DPPH,3311.15mgVCE/100g;ABTS+,9536.71 mg VCE/100 g)和氯化胆碱-三乙二醇提取物(ChCl-TGly)(DPPH,3212.82mgVCE/100g;ABTS+,8424.39mgVCE/100g)对两种自由基清除效果较强,多数DESs提取物的体外抗氧化活性显著高于体积分数为80%甲醇、体积分数为80%乙醇和水等常规溶剂提取物的体外抗氧化活性(P<0.05)。其中氯化胆碱-乙二醇(ChCl-EGly)的DPPH和ABTS+自由基清除能力分别达到3 873.89 mg VCE/100 g和8 898.49 mg VCE/100 g,分别比体积分数80%甲醇(DPPH,2 715.13 mg VCE/100 g;ABTS+,6 582.70 mg VCE/100 g)高43%和35%。研究表明,提取溶剂的类型显著影响多酚提取物的总酚含量、总黄酮含量,最终影响其抗氧化活性[27-28]。本研究中,较传统溶剂而言,作为赤霞珠葡萄籽酚类物质的提取溶剂,DESs酚类物质提取物的抗氧化活性更强。
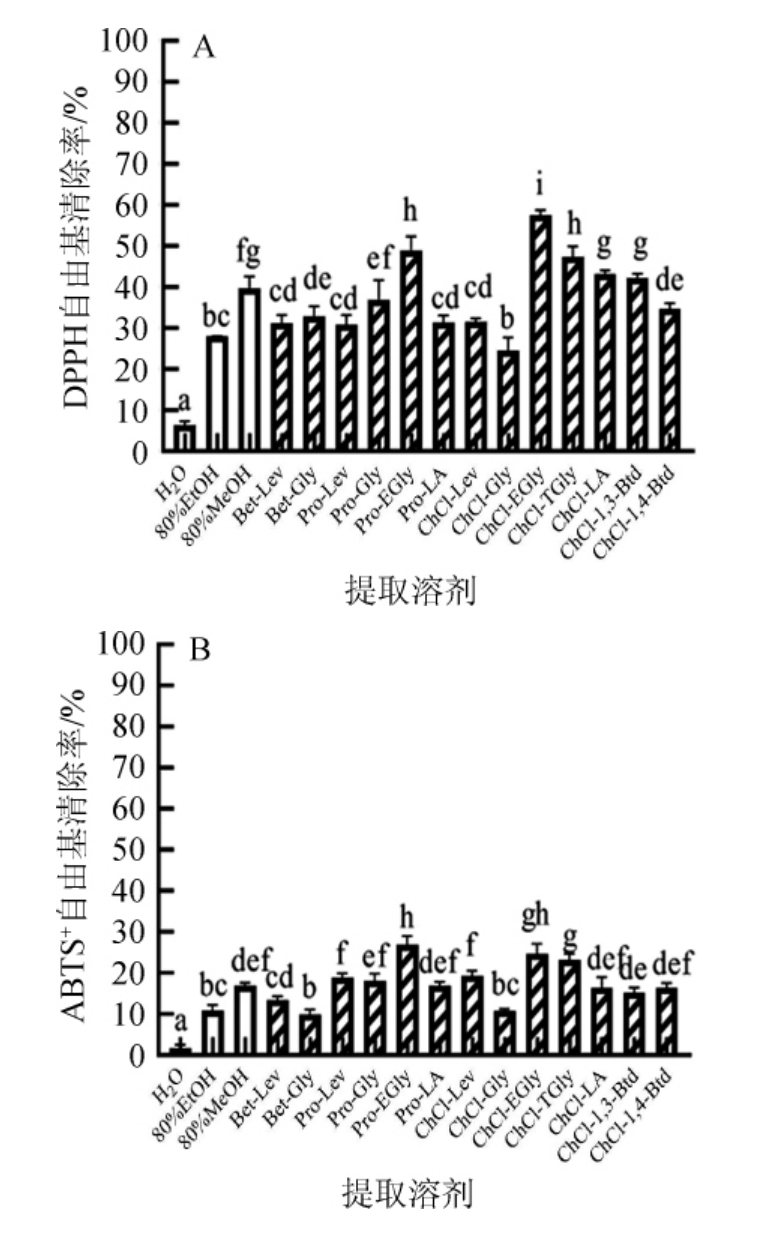
图4 葡萄籽不同提取溶剂提取物DPPH(A)和ABTS+(B)自由基清除率
Fig.4 Radical scavenging rate of DPPH (A) and ABTS+(B) in different solvents extracts of grape seed
不同小写字母表示不同提取溶剂葡萄籽提取物对DPPH和ABTS+自由基清除率差异显著性(P<0.05);稀释倍数:100倍。
表3 葡萄籽不同溶剂提取物中的体外抗氧化活性
Table3 Antioxidant activities in vitro in different solvents extracts of grape seed
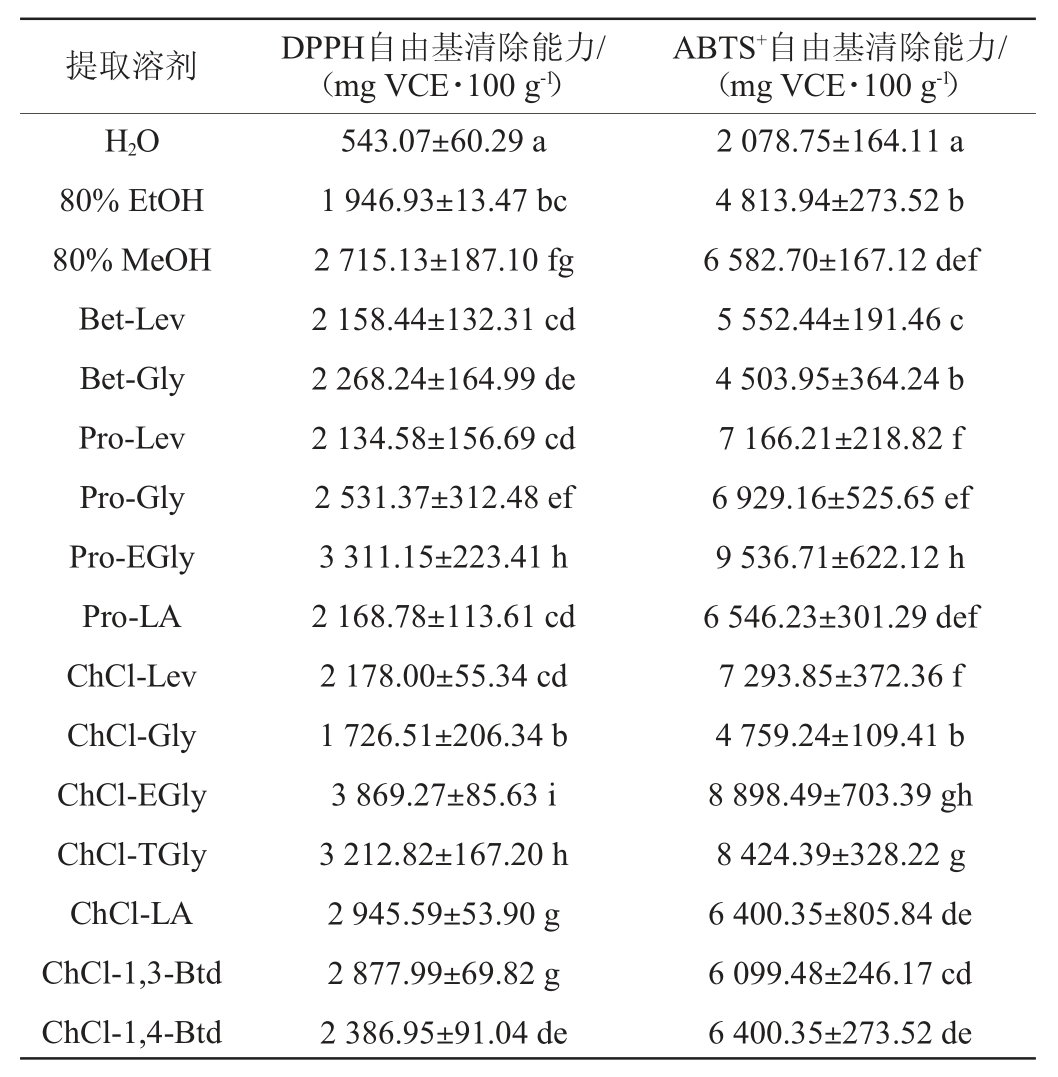
注:不同小写字母表示不同提取溶剂葡萄籽提取物中DPPH和ABTS+自由基清除能力的差异显著性(P<0.05)。
2.5 赤霞珠葡萄籽不同溶剂提取物中酚类物质与其抗氧化能力的相关性分析
采用皮尔森相关系数分析赤霞珠葡萄籽不同溶剂提取物中酚类物质含量与其抗氧化活性的相关性,结果见表4。由表4可知,提取物中总酚含量与DPPH自由基清除能力和ABTS+自由基清除能力呈显著正相关(P<0.05)。说明DESs提取物中总酚含量越高,其抗氧化活性越强,总酚是其体外抗氧化活性主要贡献因素。儿茶素、表儿茶素、原花青素B2和总酚含量呈极显著正相关(P<0.01),儿茶素、表儿茶素和总黄酮、DPPH自由基清除能力以及ABTS+自由基清除能力呈显著正相关(P<0.05)。说明赤霞珠葡萄籽DESs提取物中儿茶素、表儿茶素含量越高,其抗氧化活性越强,儿茶素、表儿茶素是DESs提取物抗氧化活性的主要贡献因素。
表4 葡萄籽不同溶剂提取物中总酚/单体酚含量与其抗氧化能力的皮尔森相关性分析
Table4 Pearson correlation analysis of total phenolic/monomer phenols contents in different solvents extracts of grape seed
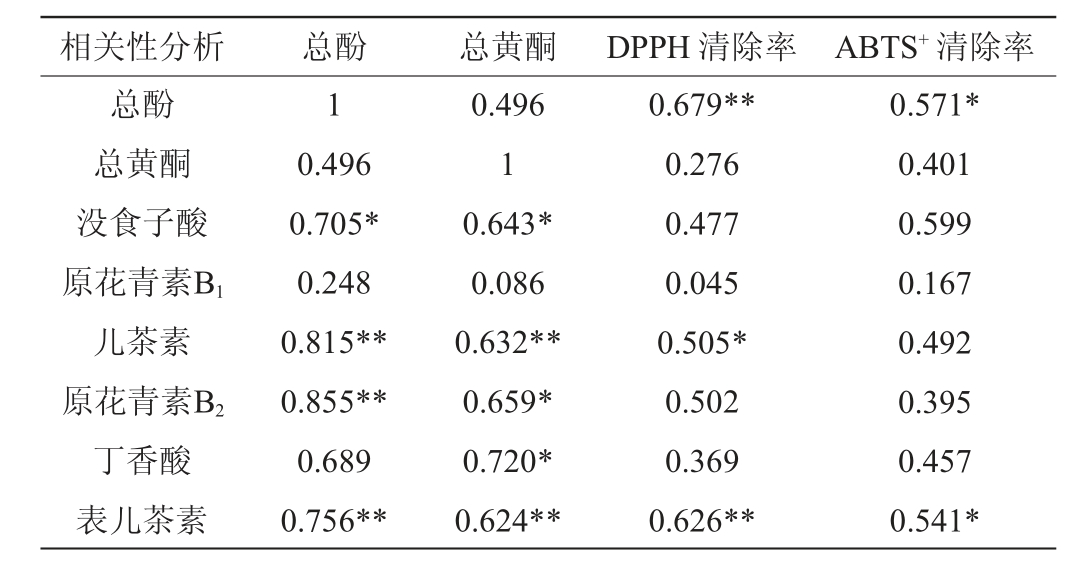
注:“*”表示显著相关(P<0.05);“**”表示极显著相关(P<0.01)。
3 结论
本研究利用低共熔溶剂结合超声辅助提取赤霞珠葡萄籽中的酚类物质,13种DESs中多数DESs对赤霞珠葡萄籽中多酚提取量显著高于常规有机溶剂。其中,氯化胆碱-乳酸(ChCl-LA)提取物中总酚含量最高,为2505.13mgGAE/100g;脯氨酸-乙酰丙酸(Pro-Lev)提取物中总黄酮含量最高,为2 849.44 mg CE/100 g。不同DESs溶剂提取物中主要的酚类物质(没食子酸、儿茶素、表儿茶素、原花青素B1、原花青素B2、丁香酸)的含量显著高于常规提取溶剂。部分DESs多酚提取物还具有较高的体外抗氧化活性,其中,氯化胆碱-乙二醇(ChCl-EGly)(DPPH,3 873.89 mg VCE/100 g)和脯氨酸-乙二醇(Pro-EGly)(ABTS+,9 536.71 mg VCE/100 g)提取物体外抗氧化活性较强。因此,氯化胆碱-乙二醇和脯氨酸-乙二醇溶剂结合超声辅助提取可作为赤霞珠葡萄籽多酚抗氧化成分的高效绿色提取溶剂,研究结果具有重要的应用价值及意义,可为基于多酚的酿酒葡萄皮渣资源化利用奠定基础。
[1]AHMAD B,YADAV V,YADAV A,et al.Integrated biorefinery approach to valorize winery waste:a review from waste to energy perspectives[J].Sci Total Environ,2020,719(6):137315.1-137315.14.
[2] ANDRADE M A,LIMA V,SILVA A S,et al.Pomegranate and grape by-products and their active compounds:are they a valuable source for food applications?[J].Trends Food Sci Technol,2019,86(4):68-84.
[3]PEIXOTO C M,DIAS M I,ALVES M J,et al.Grape pomace as a source of phenolic compounds and diverse bioactive properties[J].Food Chem,2018,253(7):132-138.
[4]金青,马晓云,杨丽丽,等.不同溶剂对酿酒葡萄皮渣多酚组成的提取效果比较[J].中国食品学报,2016,16(4):182-190.
[5]刘雪莲.葡萄皮渣固态发酵生产有机肥的影响因素[J].北方园艺,2015(5):181-183.
[6]郝生宏,胡克伟,杨荣芳,等.酿酒葡萄皮渣在健康养殖中的功能开发与利用[J].饲料研究,2019,42(12):115-117.
[7]郝小燕,牟春堂,丁娜,等.葡萄皮渣在动物饲料中应用的研究进展[J].动物营养学报,2019,31(10):4427-4433.
[8] ZUROB E,CABEZAS R,VILLARROEL E,et al.Design of natural deep eutectic solvents for the ultrasound-assisted extraction of hydroxytyrosol from olive leaves supported byCOSMO-RS[J].Sep Purif Technol,2020,248(10):117054.
[9] KHARE L,KARVE T,JAIN R,et al.Menthol based hydrophobic deep eutectic solvent for extraction and purification of ergosterol using response surface methodology[J].Food Chem,2021,340(3):127979.
[10] VAZQUEZ-GONZALEZ M,FERNANDEZ-PRIOR A,ORIA A B,et al.Utilization of strawberry and raspberry waste for the extraction of bioactive compounds by deep eutectic solvents[J].LWT-Food Sci Technol,2020,130(8):109645.
[11]焦晓波,王高杨,李锦红,等.芝麻渣中蛋白提取方法的比较研究[J].生物技术通报,2021,37(4):1-9.
[12]周萍,刘鹏展,李好,等.桑葚果渣花色苷的低共熔溶剂提取与分离[J].精细化工,2021,38(2):350-357.
[13]孙悦,何莲芝,苏卓文,等.超声辅助低共熔溶剂提取甘草多糖的研究[J].食品研究与开发,2021,42(2):84-91.
[14]BAKIRTZI C,TRIANTAFYLLIDOU K,MAKRIS DP.Novel lactic acidbased natural deep eutectic solvents:Efficiency in the ultrasound-assisted extraction of antioxidant polyphenols from common native Greek medicinal plants[J].J Appl Res Med Aroma,2016,3(3):120-127.
[15] BARBIERI J B,GOLTZ C,CAVALHEIRO F B,et al.Deep eutectic solvents applied in the extraction and stabilization of rosemary(Rosmarinus officinalis L.) phenolic compounds[J]. Ind Crops Prod,2020,144(2):112049.
[16] WU LF,LI L,CHEN S J,et al.Deep eutectic solvent-based ultrasonicassisted extraction of phenolic compounds from Moringa oleifera L.leaves:optimization,comparison and antioxidant activity[J].Sep Purif Technol,2020,247(9):117014.
[17] BEI Q,LIU Y,WANG L,et al.Improving free,conjugated,and bound phenolic fractions in fermented oats(Avena sativa L.)with Monascus anka and their antioxidant activity[J].J Funct Foods,2017,32(5):185-194.
[18]WANG L,LIN X,ZHANG J C,et al.Extraction methods for the releasing of bound phenolics from Rubus idaeus L.leaves and seeds[J]. Ind Crops Prod,2019,135(9):1-9.
[19] TOURNOUR H H,SEGUNDO M A,MAGALHES L M,et al.Valorization of grape pomace:Extraction of bioactive phenolics with antioxidant properties[J].Ind Crops Prod,2015,74(11):397-406.
[20]MÜLLER L,FRÖHLICH K,BÖHM V.Comparative antioxidant activities of carotenoids measured byferric reducing antioxidant power(FRAP),ABTS bleaching assay(αTEAC),DPPH assay and peroxyl radical scavenging assay[J].Food Chem,2011,129(1):139-148.
[21]XU ML,RAN L,CHEN N,et al.Polarity-dependent extraction of flavonoids from citrus peel waste using a tailor-made deep eutectic solvent[J]. Food Chem,2019,297(11):1-10.
[22]刘琴,周游,陈轩,等.超声辅助低共熔溶剂提取芹菜叶中芹菜素及抗氧化性分析[J].现代食品科技,2021,37(3):1-11.
[23]孙悦,刘晓冰,苏卓文,等.微波辅助低共熔溶剂提取鹰嘴豆中黄酮及其抗氧化活性的研究[J].食品工业科技,2020,41(14):120-128.
[24]王乐,王嘉琪,卢绍闯,等.不同溶剂提取穇子多酚的组分分析及其稳定性研究[J].食品科技,2020,45(8):204-210.
[25]林宝妹,张帅,洪佳敏,等.马齿苋不同溶剂提取物的抗氧化活性[J].食品工业,2020,41(3):141-145.
[26]RIBAS-AGUSTI A,MARTIN-BELLOSO O,SOLIVA-FORTUNY R,et al.Food processing strategies to enhance phenolic compounds bioaccessibility and bioavailability in plant-based foods[J].Crit Rev Food Sci Nutr,2018,58(15):2531-2548.
[27] BUBALO MC,CURKO N,TOMASEVIC M,et al.Green extraction of grape skin phenolics by using deep eutectic solvents[J].Food Chem,2016,200(6):159-166.
[28]DALL'ACQUA S,KUMAR G,SINAN K I,et al.An insight into Cochlospermum planchonii extracts obtained by traditional and green extraction methods:Relation between chemical compositions and biological properties by multivariate analysis[J].Ind Crops Prod,2020,147(5):112226.