葡萄产业是山东省特色优势产业,截至2016年,葡萄栽培面积达4.33万hm2,其中酿酒葡萄为1.94万hm2,约占全国的35%[1]。胶东半岛位于山东省东端,属暖温带湿润季风气候,光照充足、降水充沛、温差适宜,利于酿酒葡萄的生长,为山东葡萄的优势产区。但是随着全球气候变化,近几年,山东产区酿酒葡萄遭受极端低温、干旱、盐碱化等不利条件的危害,影响着葡萄产业的可持续发展。研究表明,砧木和接穗互作,不仅提高葡萄对盐碱、干旱、冻害的抗逆性[2-5],还可以影响地上部接穗的生长[6-7]、矿质元素的吸收[8-9]以及果实品质[10-12]的改变。因此,推广嫁接栽培仍然是我国葡萄产业健康发展的首要任务[13]。
赤霞珠(Cabernet Sauvignon,CS)葡萄是世界第二大品种,几乎遍布所有的葡萄种植园,用其酿造的葡萄酒具有典型的紫罗兰和甜椒香味,深受各国人民喜爱[14]。前人对赤霞珠砧穗组合研究较早,但大多集中于砧木对赤霞珠植株的抗逆性[5,15-16]、生长发育及果实品质[17]的影响,关于砧木对葡萄酒的影响报道较少;因此,本研究以4种赤霞珠砧穗组合所酿葡萄酒为试材,研究不同砧木对赤霞珠葡萄酒花色苷单体成分及含量、次生代谢物质以及抗氧化性活性的影响,以期为胶东产区赤霞珠砧穗组合筛选提供理论依据。
1 材料与方法
1.1 材料与试剂
赤霞珠(CS)与4种砧木(Beta、Ru、1103P、5BB)不同砧穗组合的葡萄酒(分别记作CS/Beta、CS/140Ru、CS/1103P、CS/5BB):酿酒果实均取自标准化管理基地,山东省烟台市农业科学研究院蓬莱试验示范基地。
2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐(2,2'-azinobis-(3-ethylbenzthiazoline-6-sulphonate,ABTS)、福林酚试剂、1,1-二苯基-2-苦肼基(1,1-diphenyl-2-picrylhydrazyl,DPPH)(均为分析纯):美国Sigma公司;花青素-3-O-葡萄糖苷(cyanidin-3-O-glucoside,Cy)(纯度≥98%):苏州科铭生物技术有限公司;商业酿酒酵母CECA:上海鼎唐国际贸易有限公司;其余试剂均为国产分析纯。
1.2 仪器与设备
PHS-3C pH计:上海仪电科学仪器股份有限公司;L3S可见分光光度计:上海仪电分析仪器有限公司;GL-20G-Ⅱ离心机:中国安科公司;Agilent 1260 Infinity高效液相色谱(high performance liquid chromatography,HPLC)仪:美国安捷伦科技有限公司。
1.3 试验方法
1.3.1 葡萄酒酿造工艺
采集4个砧穗组合的葡萄果实,成熟后破碎入5 L小罐,按照60 mg/L的量加入SO2;加入酵母,进行主发酵-酒精发酵过程,发酵温度控制在25 ℃,发酵时间6 d,残糖降至5 g/L,主发酵结束,然后进行皮渣分离,分离后进行后发酵,后发酵结束后,终止发酵;进入葡萄酒的陈酿,保持温度20~25 ℃,陈酿2个月后,澄清与过滤后,用于葡萄酒次生代谢物质分析、花色苷单体及抗氧化活性测定,所有指标平行测定3次。
1.3.2 色度测定方法
酒样经0.45 μm滤膜过滤,用相同pH的磷酸氢二钠-柠檬酸缓冲液稀释10倍于1 cm比色皿中,测定波长420 nm、520 nm、620 nm处的吸光度值,色调及色度计算公式:

1.3.3 葡萄酒花色苷单体的测定
每份葡萄酒取样200 mL,经0.2 μm滤膜过滤后采用高效液相色谱仪进行检测。色谱条件:Kromasil C18色谱柱(250 mm×4.6 mm,5 μm),流动相A为甲酸∶水=1∶9(V/V),流动相B为甲酸∶乙腈=1∶9(V/V);洗脱程序:0~1min,3%B;1~12 min,3%~15%B;12~14 min,15%~25%B;14~28min,25%~30%B;28~32 min,30%~4%B;32~40 min,4% B;流速1 mL/min,柱温30 ℃,检测波长525 nm,进样量20 μL。
花色苷定性工作基于已有文献中的紫外光谱图和保留时间等信息的比对分析。物质结构的鉴定参考标准物质及梁振昌[18]的方法。定量分析:建立10~200 mg/L 5个水平的花青素-3-O-葡萄糖苷标准曲线,R2=0.999 2,其他花色苷以相当于花青素-3-O-葡萄糖苷含量计。
1.3.4 葡萄酒次生代谢物质测定
采用Folin-Ciocalteu法[19]测定总酚含量;亚硝酸盐-氯化铝法[20]测定类黄酮含量;pH示差法[21]测定花色苷含量;Folir-Denis[22]法测定单宁含量,以单宁酸计。
1.3.5 体外抗氧化活性测定
DPPH自由基(DPPH·)清除率、ABTS自由基(ABTS+·)清除率参考杨延峰等[23]的方法、铁离子还原能力(ferric ion reducing antioxidant power,FRAP)测定参考陈纯[24]的方法。
1.3.6 数据分析方法
数据整理及作图均采用Excel 2010,显著性分析采用DPS 7.05中Duncan's比较方法,P<0.05。
2 结果与分析
2.1 不同砧木对赤霞珠干红葡萄酒色度、色调的影响
葡萄酒的色度反映了其颜色的深浅;具备高色度葡萄酒,呈现结构感强、醇厚、丰满、味涩以及单宁感强的口感特征;在新酿制的干红葡萄酒中色度越大,酒体的颜色越好。
由图1可知,CS/Beta、CS/1103P、CS/5BB葡萄酒色度无显著差异性(P>0.05),分别比CS/140Ru显著提高84.17%、69.50%、52.12%。葡萄酒的色调反映的是其颜色的种类,与其种类、成熟度和酒龄密切相关,色调越高,葡萄酒颜色的黄色比例越大,反之红色比例越大。4种葡萄酒的色调无显著差异(P>0.05)。
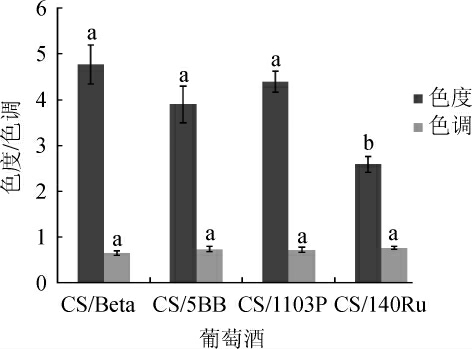
图1 不同砧穗组合赤霞珠葡萄酒色度色调对比
Fig.1 Comparison of chroma and hue of Cabernet Sauvignon wines with different rootstock-scion combinations
不同小写字母表示差异显著(P<0.05),下同。
2.2 不同砧木对赤霞珠干红葡萄酒花色苷单体组分及含量的影响
不同砧穗组合赤霞珠所酿葡萄酒花色苷单体组分及含量见表1。
表1 不同砧穗组合赤霞珠葡萄酒中的花色苷单体组分及含量对比
Table1 Comparison of anthocyanin monomer components and contents in of Cabernet Sauvignon wines with different rootstock-scion combinations
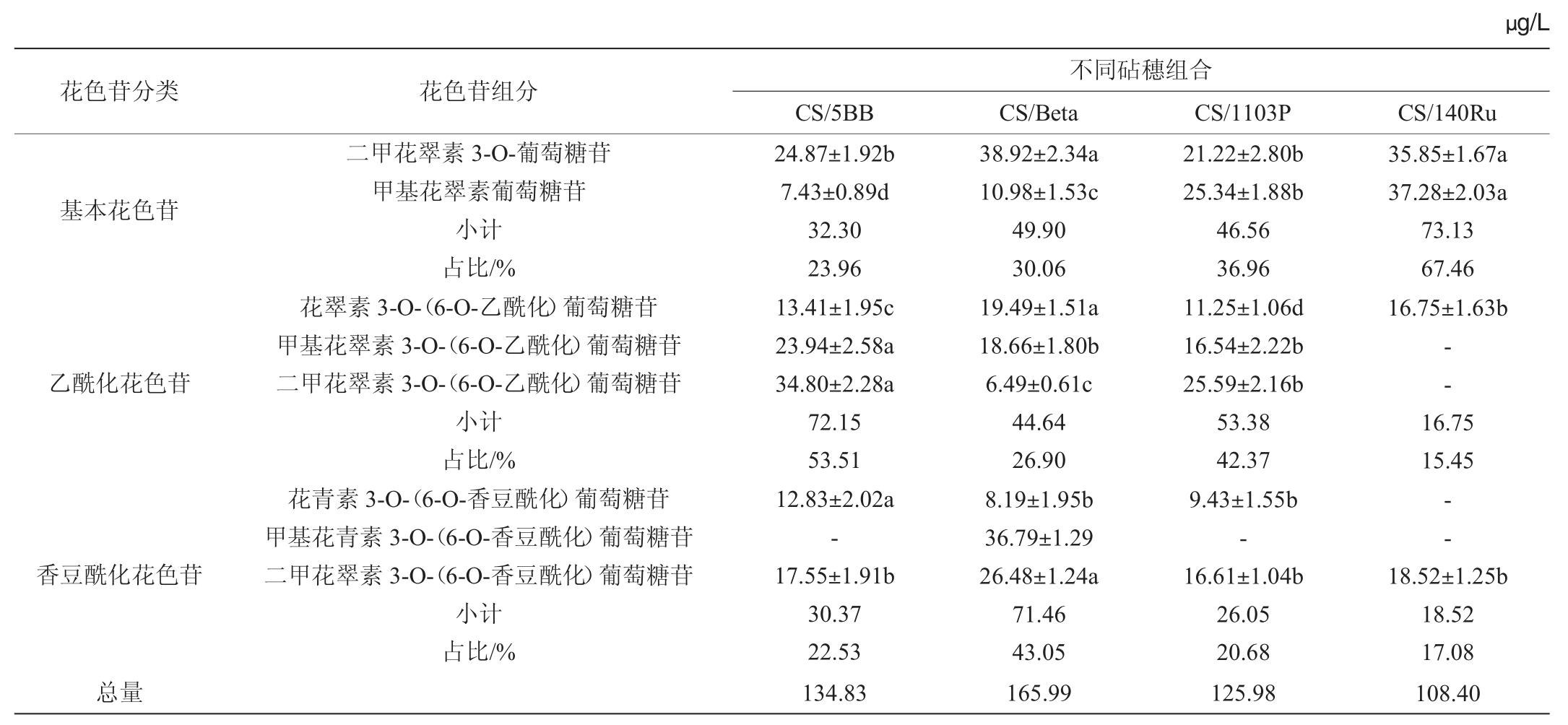
注:“-”表示未检出。
由表1可知,从花色苷单体组分来看,CS/Beta葡萄酒检测到的花色苷单体种类最多,为8种,CS/5BB、CS/1103P葡萄酒均检测到7种,而CS/140Ru葡萄酒只检测到4种主要花色苷,在所有组合中种类最低;不同葡萄酒的主要花色苷也不尽相同,CS/Beta葡萄酒以香豆酰化花色苷为主,CS/5BB葡萄酒、CS/1103P葡萄酒以乙酰化花色苷为主,花色苷单体种类最少的CS/140Ru葡萄酒则以基本花色苷为主;4种葡萄酒均仅检测到2种基本花色苷。
从花色苷单体含量来看,基本花色苷中,二甲花翠素3-O-葡萄糖苷含量以CS/Beta葡萄酒的最高,CS/140Ru次之,CS/Beta的含量比CS/5BB、CS/1103P显著提56.49%、83.41%,CS/140Ru的含量比CS/5BB、CS/1103P显著提高44.15%、68.94%;甲基花翠素葡萄糖苷含量以CS/140Ru葡萄酒最高,分别是CS/5BB、CS/Beta、CS/1103P的5.01倍、3.40倍、1.47倍;乙酰化花色苷中,甲基花翠素3-O-(6-O-乙酰化)葡萄糖苷和二甲花翠素3-O-(6-O-乙酰化)葡萄糖苷含量均以CS/5BB葡萄酒最高,其中,甲基花翠素3-O-(6-O-乙酰化)葡萄糖苷含量分别比CS/Beta、CS/1103P显著增加28.30%、44.74%,二甲花翠素3-O-(6-O-乙酰化)葡萄糖苷含量比CS/1103P显著增加35.99%,甚至达CS/Beta葡萄酒的5.36倍;花翠素3-O-(6-O-乙酰化)葡萄糖苷含量以CS/Beta葡萄酒最高,分别比CS/5BB、CS/1103P、CS/140Ru显著增加45.34%、73.24%、16.36%;香豆酰化花色苷中,花青素3-O-(6-O-香豆酰化)葡萄糖苷以CS/5BB含量最高,分别比CS/Beta、CS/1103P显著增加56.65%、27.25%,甲基花青素3-O-(6-O-香豆酰化)葡萄糖苷、二甲花翠素3-O-(6-O-香豆酰化)葡萄糖苷均以CS/Beta含量最高。从花色苷单体总量来看,CS/Beta含量分别比CS/5BB、CS/1103P、CS/140Ru提高23.11%、31.76%、53.13%。
2.3 不同砧木对赤霞珠干红葡萄酒次生代谢物质含量的影响
由图2可知,CS/Beta葡萄酒中的总酚、类黄酮、花色苷、单宁含量在所测组合中含量最高,CS/5BB次之,但二者的总酚与花色苷含量无显著性差异。
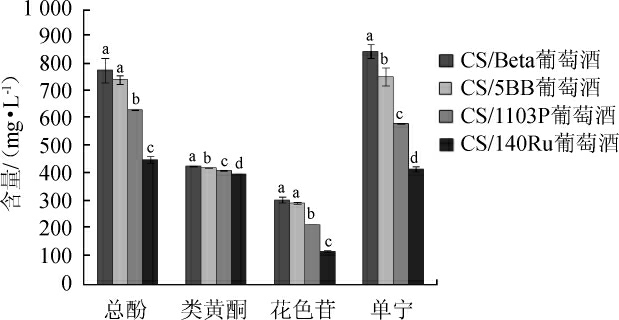
图2 不同砧穗组合赤霞珠葡萄酒中次生代谢物质含量对比
Fig.2 Comparison of secondary metabolites contents in Cabernet Sauvignon wines with different rootstock-scion combinations
CS/Beta葡萄酒总酚含量分别比CS/1103P、CS/140Ru显著提高22.70%、71.56%,类黄酮含量分别比CS/5BB、CS/1103P、CS/140Ru显著提高1.00%、3.55%、6.78%,单宁含量分别比CS/5BB、CS/1103P、CS/140Ru显著提高12.18%、44.77%、102.20%;花色苷含量分别比CS/1103P、CS/140Ru显著提高40.71%、154.53%;CS/5BB葡萄酒的总酚含量分别比CS/1103P、CS/140Ru显著提高17.24%、63.94%,类黄酮含量分别比CS/1103P、CS/140Ru显著提高2.53%、5.73%,单宁含量分别比CS/1103P、CS/140Ru显著提高29.06%、80.26%;花色苷含量分别比CS/1103P、CS/140Ru组合显著提高与34.93%、144.07%。
2.4 不同砧木对赤霞珠干红葡萄酒抗氧化活性的影响
不同砧穗组合赤霞珠葡萄酒抗氧化活性对比见图3。由图3可知,4种葡萄酒的DPPH·清除率、ABTS+·清除率、FRAP值均以CS/Beta葡萄酒最高,CS/5BB葡萄酒次之。
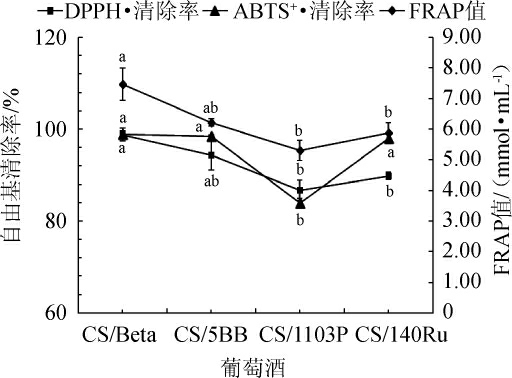
图3 不同砧穗组合赤霞珠葡萄酒抗氧化活性对比
Fig.3 Comparison of antioxidant activity of Cabernet Sauvignon wines with different rootstock-scion combinations
经计算可得,CS/Beta、CS/5BB葡萄酒的DPPH·清除率分别比CS/1103P显著提高14.09%、8.89%,比CS/140Ru显著提高10.02%、5.01%(P<0.05);CS/Beta、CS/5BB、CS/140Ru葡萄酒的ABTS+·清除率分别比CS/1103P显著提高17.89%、17.54%、16.95%(P<0.05),CS/Beta葡萄酒的FRAP值分别比CS/1103P、CS/140Ru显著提高40.75%、26.87%(P<0.05)。
2.5 讨论
花色苷是葡萄酒中的关键呈色物质[25]。本研究表明,砧穗组合影响葡萄酒中的花色单体组分和含量,试验处理中,CS/Beta葡萄酒以香豆酰化花色苷为主,CS/5BB、CS/1103P葡萄酒以乙酰化花色苷为主,CS/140Ru葡萄酒则以基本花色苷为主,而色调色度测定显示,CS/140Ru色度偏低,与其花色苷单体组分和含量均较为单一相一致,这可能是由于葡萄酒酿造过程中,酒精发酵和苹果酸乳酸发酵过程中花色苷单体含量会不同程度转化[26],最终造成花色苷单体含量的变化;也有可能是受贮藏阶段温度、微氧等环境条件对花色苷转化的影响[26],还有可能是砧穗组合直接影响葡萄果实花色苷单体组分与含量,酿造后间接影响葡萄酒花色苷的组分与含量。
酚类物质影响葡萄酒的气味、颜色、口感等形态学指标,并具有抗氧化功能[27],是植物重要的次生代谢物质,也是葡萄酒的品质贡献及功能性物质。葡萄酒中的酚类物质一方面来自发酵过程中的皮渣浸提[28],另一方面来自发酵过程中微生物代谢[29]。本试验研究表明,砧木Beta、5BB显著增加了葡萄酒中的总酚、类黄酮、花色苷、单宁的含量,改善了葡萄酒的色度,增强了葡萄酒的抗氧化活性,即砧木影响葡萄酒酚类物质含量,根据试验设计的唯一差异原则,果实中次生代谢物质的差异源自砧木差异,因此,本试验从一定程度上说明并侧面验证了砧木影响葡萄果实次生代谢产物,这与前人研究结果一致[17,30,11]。
3 结论
试验以4种砧穗组合(CS/Beta、CS/140Ru、CS/1103P、CS/5BB)所产果实酿造的葡萄酒为试材,通过测定不同砧穗组合下赤霞珠葡萄酒的花色苷单体组分与含量、其他次生代谢物质含量及葡萄酒抗氧化活性。结果显示砧木可以改变赤霞珠葡萄酒花色苷单体组分与含量,CS/Beta单体组分最多(8种),且其香豆酰化比例较高,CS/5BB次之(7种),酰化比例较高;砧木Beta对提升赤霞珠葡萄酒的总酚、类黄酮、花色苷、单宁指标作用显著,CS/5BB次之;色度方面,CS/Beta、CS/1103P、CS/5BB优于组合CS/140Ru;抗氧化活性方面,组合CS/Beta、CS/5BB还原力均显著高于组合CS/1103P、CS/140Ru(P<0.05)。综合看,砧木Beta、5BB对于改善赤霞珠葡萄干红葡萄酒品质方面有重要作用,可考虑作为赤霞珠嫁接苗的首选砧木。
[1]唐美玲,王咏梅.山东省葡萄生产存在的主要问题与建议[J].烟台果树,2018(1):6-7.
[2]OKI L R,LIETH J H.Effect of changes in substrate salinity on the elongation of Rosa hybrida L.'Kardinal'stems[J].Sci Hortic,2004,101(1-2):103-119.
[3]刘竞择,曹柠,张艳霞.葡萄砧木冬季抗抽干能力及抗旱性综合评价研究[J].果树学报,2020,37(3):339-349.
[4]綦伟,厉恩茂,翟衡,等.不同砧穗组合葡萄植株对部分根区干旱的生理生化响应[J].应用生态学报,2008(2):306-310.
[5]范宗民,孙军利,赵宝龙,等.不同砧木‘赤霞珠’葡萄枝条抗寒性比较[J].果树学报,2020,37(2):215-225.
[6]王晓玥,张国军,孙磊,等.砧木对葡萄树体生长和内源激素的影响[J].园艺学报,2020,47(11):2107-2120.
[7]户金鸽,白世践,陈光,等.不同砧木对赤霞珠葡萄叶片光合特性及果实品质的影响[J].新疆农业科学,2020,57(5):830-839.
[8]黄冰.砧木对巨峰葡萄钾肥吸收和生长影响的初步研究[D].扬州:扬州大学,2008.
[9]韩真,杜远鹏,翟衡,等.葡萄不同砧木钾营养效率的差异研究[C].中国园艺学会2018 年学术年会论文摘要集,北京:中国园艺学会,2018.
[10]魏灵珠,沈碧薇,程建徽,等.砧木对‘新雅’葡萄生长及果实品质的影响[J].果树学报,2020,37(9):1346-1357.
[11]郝燕,马麒龙,张坤,等.河西走廊不同砧木对‘贵人香’葡萄生长与果实品质的影响[J].果树学报,2017,34(10):1286-1293.
[12]李敏敏,袁军伟,刘长江,等.8 个砧木对河北昌黎产区‘马瑟兰’葡萄生长和果实品质的影响[J].西北农业学报,2017,26(5):745-751.
[13]赵艳侠,张久慧,亓桂梅.葡萄砧木的应用研究现状及展望[J].北方园艺,2019(11):136-142.
[14]管乐,亓桂梅,房经贵.世界葡萄主要品种与砧木利用概述[J].中外葡萄与葡萄酒,2019(1):64-69.
[15]袁军伟,李敏敏,尹勇刚,等.不同砧木嫁接的赤霞珠葡萄对盐胁迫的生理响应[J].中国农业大学学报,2019,24(8):48-59.
[16]刘敏,房玉林.高温胁迫对葡萄幼树生理指标和超显微结构的影响[J].中国农业科学,2020,53(7):1444-1458.
[17]牛锐敏,许泽华,黄小晶,等.砧木对‘赤霞珠’葡萄生长和果实品质的影响[J].西北林学院学报,2020,35(1):124-129.
[18]梁振昌.葡萄果皮花色苷构成特点、遗传规律及其在果实成熟过程中的变化[D].北京:中国科学院大学,2008.
[19]刘芸,仇农学,杨玺玉.葡萄皮渣提取物总酚含量及体外抗氧化活性抑菌活性[J].食品科学,2011,32(1):5-9.
[20]OZDEN M,VARDIN H,SIMSEK M,et al.Effects of rootstocks and irrigation levels on grape quality of Vitis vinifera L.cv.Shiraz[J].Afr J Biotechnol,2010,9(25):3801-3807.
[21] ORAKH H.Total antioxidant activities,phenolics,anthocyanins,polyphenoloxidase activities of selected red grape cultivarsand their correlations[J].Sci Hortic,2007,111(3):235-241.
[22]耿娜娜,李学英,顾丁,等.Folin-Denis 分光光度法测定五倍子中单宁酸的含量[J].安徽农业科学,2013,41(29):11848-11850.
[23]杨延峰,王远兴.基于超高效液相-四级杆-飞行时间串联质谱的南丰蜜桔幼果化学成分分析及抗氧化活性研究[J].中国食品学报,2019,19(2):273-280.
[24]陈纯.甘蔗皮多酚的提取、分离鉴定及抗氧化活性研究[D].杭州:浙江大学,2013.
[25] HE F,LIANG N N,MU L,et al.Anthocyanins and their variation in red wines in monomeric anthocyanins and their color expression[J].Molecules,2012,17(2):1571-1601.
[26]葛谦,刘正庭,陈翔,等.赤霞珠葡萄酒酿造过程中花色苷及颜色参数变化规律[J].中国酿造,2018,37(2):137-141.
[27]回学宽,王艳丽,祝贺,等.葡萄酒中酚类物质的研究进展[J].中国果菜,2019,39(11):65-71.
[28]王燕,李德美,孙智文,等.高效液相色谱法同时测定贺兰山东麓干红葡萄酒7 种酚类物质的方法研究[J].食品与发酵工业,2021(1):1-7.
[29] ROJAS I B,SMITH P A,BARTOWSKY E J.Influence of choice of yeasts on volatile fermentation-derived compounds,colour and phenolics composition in Cabernet Sauvignon wine[J].World J Microb Biot,2012,28(12):3311-3321.
[30]高展,彭媛媛,董凯向,等.不同砧木对马瑟兰葡萄生长及果实品质的影响[J].华北农学报,2019,34(5):170-176.