随着人们保健意识的提升,益生菌因具有增强免疫力、促进肠道消化系统健康、抑菌消炎等功效愈加受到人们关注[1-3]。部分乳酸菌具有益生功能,但目前该类产品多以乳制品为载体,主要以发酵乳饮料形式呈现[4]。果蔬因富含糖类、维生素、矿物质、膳食纤维等营养物质,越来越多研究表明,可作为乳酸菌发酵的良好载体[5-7]。
南瓜(Cucurbita moschata Duch),一年生蔓生草本植物,性温,味甜适口,富含淀粉、蛋白质、胡萝卜素、多种维生素和矿物质,被誉为“营养全能王”[8-10]。南瓜不仅具有较高的食用价值,因其富含南瓜多糖等多种活性物质,还有一定的食疗作用,对心血管疾病、糖尿病等具有一定辅助疗效[11-13]。
研究表明,乳酸菌可在南瓜汁中生长繁殖,在发酵过程中还会产生有机酸、氨基酸等活性产物,能够提高南瓜汁的营养价值[14-16],并且适宜的菌株复配后不仅可以弥补单一菌种发酵的缺陷,而且发酵效果要优于单一菌种发酵[17-19]。
植物乳杆菌(Lactobacillus plantarum)在果蔬类发酵食品中普遍存在,具备较好的发酵果蔬能力[20]。德氏乳杆菌保加利亚亚种(Lactobacillus delbrueckii subsp.bulgaricus)可以产生胞外多糖,具有益生功能。戊糖乳杆菌(Lactobacillus pentosus)能够产生γ-氨基丁酸,提高机体免疫力。嗜酸乳杆菌(Lactobacillus acidophilus)能够产生β-半乳糖苷酶,可加速酸化反应,提高发酵效率,产生发酵芳香气味。嗜热链球菌(Streptococcus thermophilus)可以产生细菌素和维生素等活性代谢产物,提高人体免疫力。肠膜明串珠菌(Leuconostoc mesenteroides)可产生左旋糖酐,有降低血液粘稠度,改善微循环等生理功能。长双歧杆菌(Bifidobacterium longum)可以调节肠道健康,提高机体免疫力。青春双歧杆菌(Bifidobacterium adolensentis)可以调节慢性腹泻、便秘等,具有益生功能[21]。
目前,人们多以单菌种发酵南瓜汁,复合菌种发酵南瓜果浆研究较少。本研究以南瓜果浆为原料,充分利用南瓜果浆的营养物质,首先以活菌数、pH值和可滴定酸为考察对象,对8株益生菌进行筛选,筛选出活菌数最高、发酵能力最强、降酸速度最快、适应性最强的菌株[22],并进行菌株复配试验验证后,在单因素试验的基础上,以活菌数为响应值,根据Box-benhnken中心组合设计原理,结合响应面法优化乳酸菌发酵南瓜浆的发酵工艺条件,获得最佳生产工艺参数。通过复合益生菌发酵南瓜浆,不仅为获取益生菌提供新途径,还可利用发酵特性提高南瓜浆的生物利用率[23-24],为开发一种富含益生菌、具有保健功能的蔬菜饮料提供新的思路。
1 材料与方法
1.1 材料与试剂
1.1.1 原料和菌株
贝贝南瓜(Cucurbita moschata Duch):产自甘肃武威市民勤县;植物乳杆菌(Lactobacillus plantarum)CICC21824、德氏乳杆菌保加利亚亚种(Lactobacillus delbrueckii subsp.bulgaricus)CICC20271、戊糖乳杆菌(Lactobacillus pentosus)CICC24202、嗜酸乳杆菌(Lactobacillus acidophilus)CICC6075、嗜热链球菌(Streptococcus thermophilus)CICC20373、肠膜明串珠菌(Leuconostoc mesenteroides)CICC23614、长双歧杆菌(Bifidobacterium longum)CICC6259、青春双歧杆菌(Bifidobacterium adolensentis)CICC6175:中国工业微生物菌种保藏管理中心。
1.1.2 化学试剂
纤维素酶(20万U/g)、果胶酶(30万U/g):宁夏和氏璧生物技术有限公司;木瓜蛋白酶(20万U/g):南宁庞博生物工程有限公司。
1.1.3 培养基
MRS固体培养基、MRS肉汤培养基:北京奥博星生物技术有限责任公司。
1.2 仪器与设备
BSA224S-CW电子天平:赛多利斯科学仪器(北京)有限公司;ZHJH-C112B型超净工作台:上海智城分析仪器制造有限公司;LRH-250型生化培养箱:上海一恒科学仪器有限公司;BL-75G型立式压力蒸汽灭菌器:上海申安医疗器械厂;Scientz-IID超声波打浆机:宁波新芝生物科技股份有限公司;PB-10酸度计:赛多利斯科学仪器(北京)有限公司。
1.3 试验方法
1.3.1 菌种活化
取超低温冰箱保存的8株益生菌菌株分别在MRS固体培养基上划线活化,适宜温度下恒温培养24 h后,挑取长势较好的单菌落于MRS肉汤培养基中扩培,活化1~2次。充分活化后的菌液在4 ℃、10 000 r/min条件下离心10 min,在超净台中用无菌生理盐水重悬,备用。
1.3.2 南瓜浆制备
选择新鲜、成熟南瓜,清洗后去皮、去籽,切成5 mm均匀薄片在沸水中烫漂5 min,按一定比例加入蒸馏水后打浆。打浆后加入0.2%的纤维素酶、0.1%的果胶酶和0.15%的木瓜蛋白酶,50 ℃酶解1 h后,于110 ℃灭菌5 min[25],迅速冷却至室温备用。
1.3.3 菌株筛选
将重悬后的菌液按照6%的接种量(108 CFU/mL)分别接种于经过预处理的南瓜浆中,在菌株最适生长条件下静置发酵,在第0、4、8、12、16、20和24小时分别取样,测定活菌数、可滴定酸和pH值。
1.3.4 混菌复配试验
将筛选出的植物乳杆菌和嗜热链球菌分别以3∶1、1∶1和1∶3(V/V)的比例进行复配,并且以两株乳酸菌单独发酵作为对照,6%的接种量接种于预处理南瓜浆中,37 ℃静置发酵,在第4、8、12、16、20和24 小时分别取样,测定活菌数、可滴定酸和pH值。
1.3.5 发酵工艺优化单因素试验
在菌种筛选的基础上,选择植物乳杆菌21824和嗜热链球菌20373(1∶1)进行复配发酵,以发酵后的活菌数、可滴定酸和感官评分为考察指标,分别考察料液比(3∶1、2∶1、1∶1、1∶2、1∶3(g∶mL)),接种量(2%、4%、6%、8%、10%)(V/V),发酵温度(28 ℃、31 ℃、34 ℃、37 ℃、40 ℃),发酵时间(12 h、16 h、20 h、24 h和28 h)对发酵南瓜浆的影响。
1.3.6 发酵工艺优化响应面试验
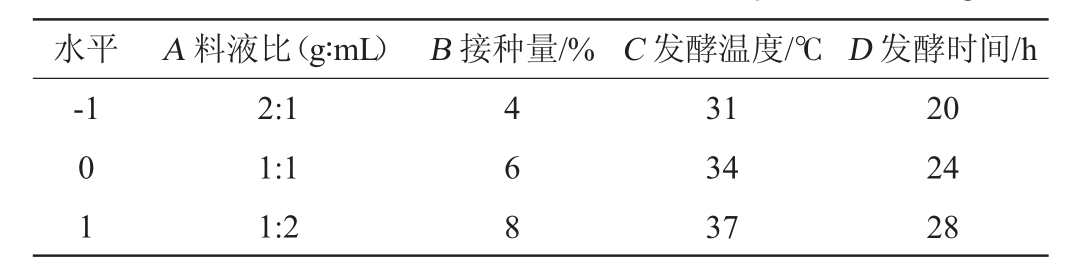
在单因素试验的基础上,以料液比(A)、接种量(B)、发酵温度(C)和发酵时间(D)为自变量,以活菌数(Y)为响应值,运用Design-Expert 8.0.6软件设计Box-Benhnken试验,Box-Benhnken试验设计因素与水平见表1。
表1 Box-Benhnken试验设计因素与水平
Table1 Factors and levels of Box-Behnken experiments design
1.3.7 指标测定和感官评价
活菌数测定:活菌数测定按照国标GB 4789.35—2016《食品安全国家标准食品微生物学检验乳酸菌检验》中的平板计数法,结果以每毫升发酵液中所含活菌的对数值表示,单位为lg(CFU/mL)。
可滴定酸测定:参照国标GB 12456—2008《食品中总酸的测定》中的酸碱滴定法,结果以每升发酵液中乳酸含量表示,单位为mg/mL;pH值测定:采用酸度计测定。
发酵南瓜浆感官评价采用9分制,满分36分。共邀请9名具有食品感官学相关专业人员进行品评,评分细则参考袁晶等[25]的方法,略有修改。感官评价标准见表2。
表2 发酵南瓜浆感官评价标准
Table2 Sensory evaluation standards of fermented pumpkin pulp

1.3.8 数据统计分析
数据重复3次,数据处理和显著性差异分析用Excel2016和SPSS 24.0软件,BBD试验设计的数据处理用Design-Expert 8.0.6软件。
2 结果与分析
2.1 南瓜浆发酵益生菌筛选
2.1.1 不同益生菌发酵南瓜浆中活菌数的变化
不同益生菌发酵南瓜浆过程中活菌数变化见图1。由图1可知,8株益生菌均可在南瓜浆中生长,其中,嗜热链球菌适应性最强,在发酵第4小时时,活菌数数量显著高于其他菌株,达到7.46 lg(CFU/mL),说明该菌株能快速适应南瓜浆环境;发酵至第24小时,菌株进入对数生长期,活菌数为8.52~9.53 lg(CFU/mL)。其中植物乳杆菌活菌数最高,达到9.53lg(CFU/mL),随后依次为嗜热链球菌、嗜酸乳杆菌、长双歧杆菌、青春双歧杆菌、肠膜明串株菌、德氏乳杆菌保加利亚亚种和戊糖乳杆菌,活菌数分别是9.23 lg(CFU/mL)、9.10 lg(CFU/mL)、8.97 lg(CFU/mL)、8.55 lg(CFU/mL)、8.89 lg(CFU/mL)、8.64 lg(CFU/mL)和8.52 lg(CFU/mL)。
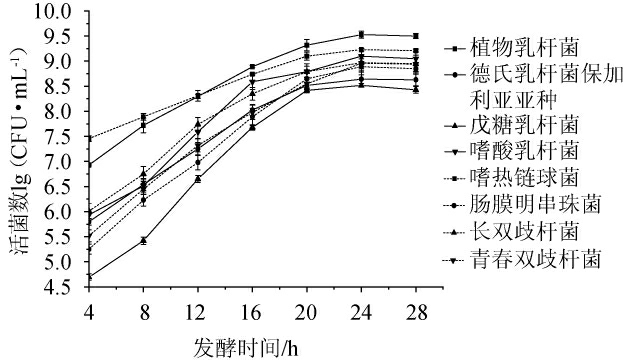
图1 不同益生菌发酵南瓜浆中活菌数的变化
Fig.1 Change of viable count in pumpkin pulp fermented with different probiotics
2.1.2 不同益生菌发酵南瓜浆中pH值的变化
8种益生菌发酵南瓜浆过程中pH值变化见图2。由图2可知,随着发酵时间的延长,体系pH值均呈现逐渐降低的趋势,在0~8 h发酵初期,嗜热链球菌发酵南瓜浆pH降低速度最快,由4.70下降至4.21。在12~28 h发酵中后期,植物乳杆菌pH值降低最快,变化最显著,pH值由发酵第12小时的4.02下降至3.25。至发酵结束(28 h),pH由低到高依次为:植物乳杆菌、嗜热链球菌、戊糖乳杆菌、德氏乳杆菌保加利亚亚种、嗜酸乳杆菌、肠膜明串株菌、长双歧杆菌和青春双歧杆菌,pH值分别为3.25、3.45、3.54、3.56、3.62、3.65、3.89和4.01。
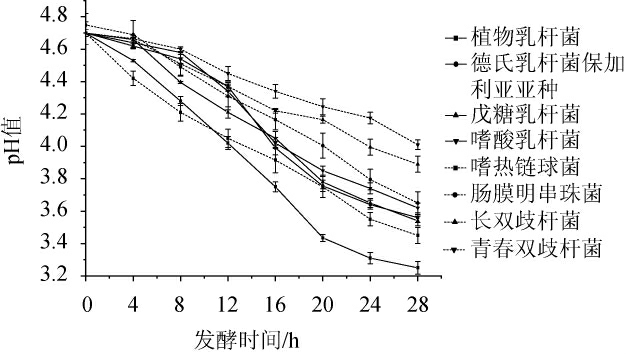
图2 不同益生菌发酵南瓜浆中pH值的变化
Fig.2 Change of pH value in pumpkin pulp fermented with different probiotics
2.1.3 不同益生菌发酵南瓜浆中可滴定酸的变化
不同益生菌发酵过程南瓜浆中可滴定酸变化见图3。由图3可知,随着发酵时间的延长,发酵体系中的可滴定酸呈现逐渐增加的趋势。8株益生菌均可在南瓜浆中发酵产酸,在发酵初期(0~12 h),嗜热链球菌发酵南瓜浆中可滴定酸从发酵前的1.01 mg/mL增长至2.25 mg/mL,增长最为显著,随后增长趋于缓慢;发酵结束时(28 h),植物乳杆菌发酵南瓜浆体系的可滴定酸含量最高,随后依次为德氏乳杆菌保加利亚亚种、戊糖乳杆菌、嗜热链球菌、嗜酸乳杆菌、肠膜明串株菌、长双歧杆菌和青春双歧杆菌,可滴定酸含量分别为:4.28 mg/mL、4.15 mg/mL、4.01 mg/mL、3.51 mg/mL、3.78 mg/mL、3.40 mg/mL、3.01 mg/mL和2.95 mg/mL。说明在适应环境后,植物乳杆菌发酵能力最强,能大量产酸。
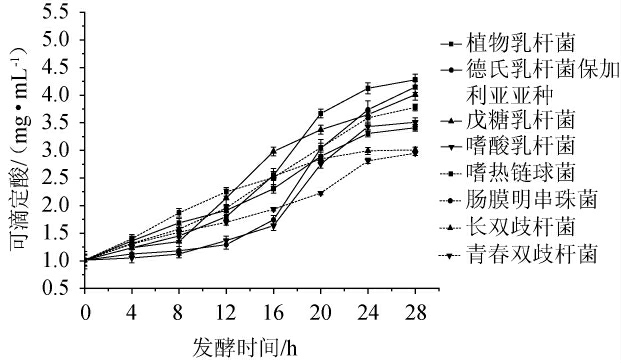
图3 不同益生菌发酵南瓜浆中可滴定酸的变化
Fig.3 Change of titratable acid in pumpkin pulp fermented with different probiotics
综上所述,筛选出活菌数最高、发酵能力最强的植物乳杆菌(Lactobacillus plantarum)CICC21824和降酸速度最快、适应性最强的菌株嗜热链球菌(Streptococcus thermophilus)CICC20373发酵南瓜浆。
2.2 混菌发酵南瓜浆中活菌数、pH值、可滴定酸的变化
选择植物乳杆菌和嗜热链球菌进行单独及复配发酵,植物乳杆菌、嗜热链球菌和复合菌发酵南瓜浆中活菌数、pH值、可滴定酸变化见图4。由图4可知,将植物乳杆菌和嗜热链球菌复配发酵南瓜浆后,比起单一菌种发酵而言,复合菌可互利共生,促进生长繁殖和产酸,并且在复配比为1∶1(V/V)时,发酵效果最佳。嗜热链球菌适应能力最强,降低pH值速度最快,在南瓜浆发酵体系中,它能迅速生长繁殖并且产酸,使南瓜浆快速进入低pH值状态,抑制酵母菌等杂菌生长,为其他乳酸菌提供良好生长环境[26];发酵中后期,植物乳杆菌作为后期主要发酵菌种,生长繁殖良好,产酸量高。因此,选择植物乳杆菌和嗜热链球菌进行1∶1(V/V)复配发酵南瓜浆。
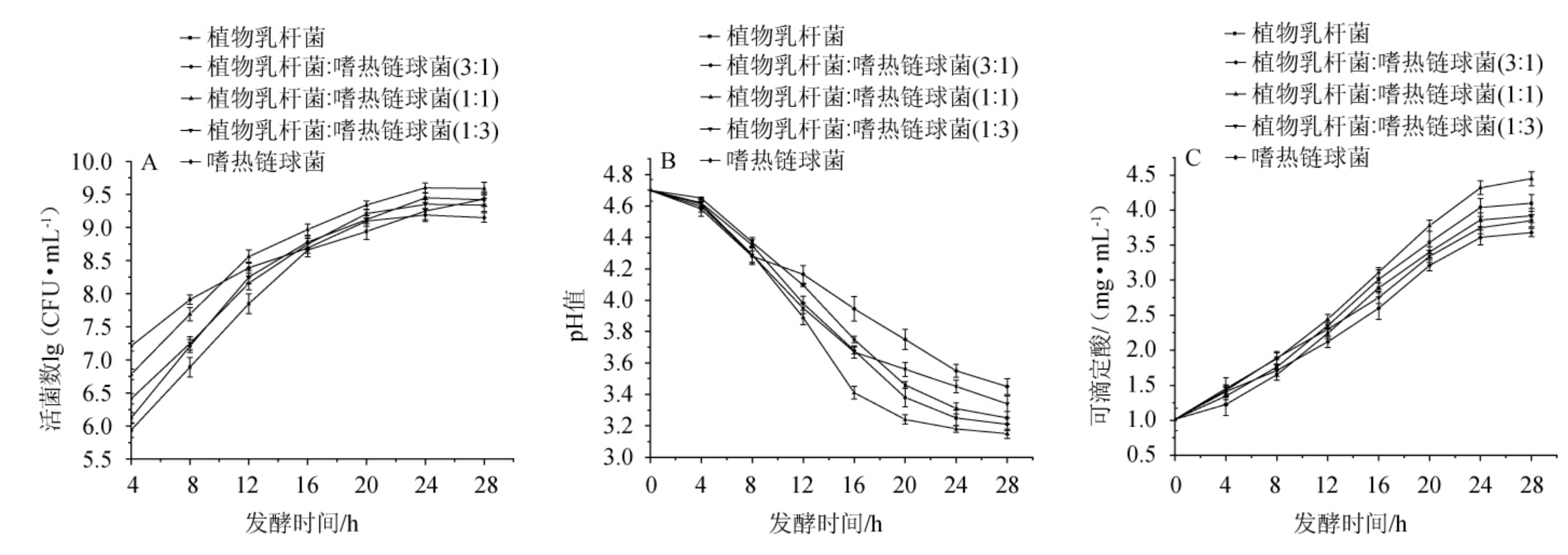
图4 植物乳杆菌、嗜热链球菌及混菌发酵南瓜浆中活菌数(A)、pH值(B)、可滴定酸(C)的变化
Fig.4 Changes of viable count (A),pH value (B) and titratable acid (C) in pumpkin pulp fermented with Lactobacillus plantarum,Streptococcus thermophilus and mixed strains
2.3 发酵工艺优化单因素试验
2.3.1 料液比对发酵南瓜浆中活菌数、可滴定酸和感官评分的影响
料液比对发酵南瓜浆活菌数、可滴定酸和感官评分的影响见图5。由图5可知,随着料液比在3∶1~1.3(g∶mL)范围内变化,发酵体系中的活菌数、可滴定酸和感官评分呈现先升高后降低的趋势。当料液比为1∶1(g∶mL)时,活菌数达到最大值9.89lg(CFU/mL),此时可滴定酸含量为4.73mg/mL,感官评分也最高;而随着料液比的继续增加,活菌数和可滴定酸呈现逐渐下降趋势,并且此时发酵南瓜浆组织过于稀薄,口感寡淡,感官评分较低。因此,选择最适料液比为1∶1(g∶mL)。
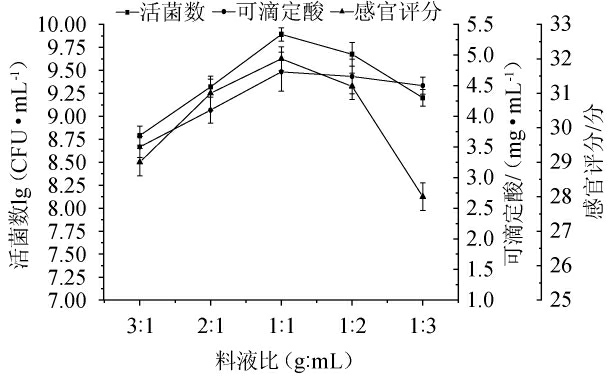
图5 料液比对发酵南瓜浆活菌数、可滴定酸和感官评分的影响
Fig.5 Effect of solid and liquid ratio on viable count,titratable acid and sensory evaluation of fermented pumpkin pulp
2.3.2 接种量对发酵南瓜浆中活菌数、可滴定酸和感官评分的影响
接种量对发酵南瓜浆活菌数、可滴定酸和感官评分的影响见图6。由图6可知,随着接种量在2%~10%(V/V)范围内的增加,发酵体系中的活菌数、可滴定酸和感官评分呈现先升高后趋于平缓的趋势。当接种量为6%(V/V)时,活菌数达到最大值9.75 lg(CFU/mL),感官评分也最高;当接种量为10%时,可滴定酸达到最大值5.25 mg/mL。但接种量过大易导致发酵过快,口感过酸[27]。因此,选择最适接种量为6%(V/V)。
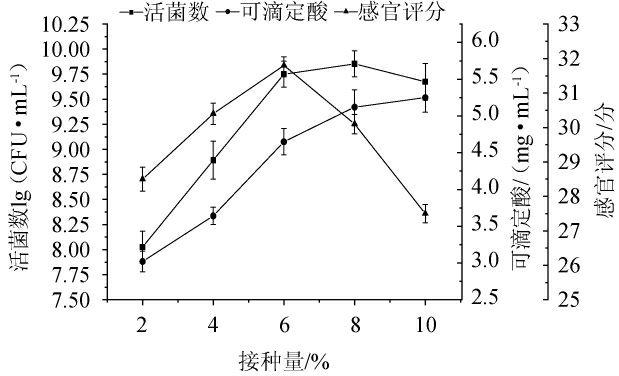
图6 接种量对发酵南瓜浆活菌数、可滴定酸和感官评分的影响
Fig.6 Effect of inoculum on viable count,titratable acid and sensory evaluation of fermented pumpkin pulp
2.3.3 发酵温度对发酵南瓜浆中活菌数、可滴定酸和感官评分的影响
发酵温度对发酵南瓜浆活菌数、可滴定酸和感官评分的影响如图7所示。由图7可知,发酵温度对乳酸菌生长繁殖及产酸量影响较大。随着发酵温度在28~40 ℃范围内的升高,发酵体系中的活菌数和可滴定酸呈现先升高后下降的趋势。当发酵温度为34 ℃时,活菌数达到最大值9.85 lg(CFU/mL),可滴定酸达到最大值4.75 mg/mL,感官评分为31.5分。当发酵温度升高至37 ℃时感官评分达到最大值31.8分,但与34 ℃时的感官评分差异不显著。基于节约能源考虑,选择发酵温度34 ℃为最适发酵温度。
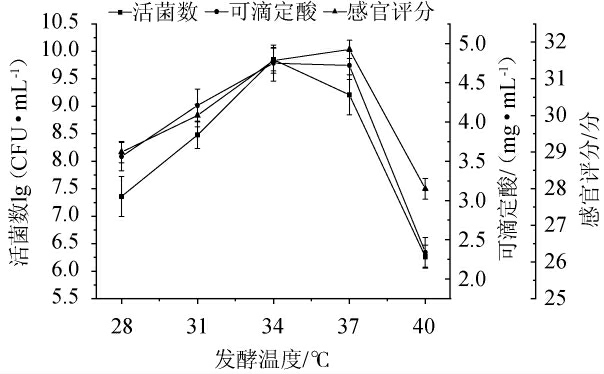
图7 发酵温度对发酵南瓜浆活菌数、可滴定酸和感官评分的影响
Fig.7 Effect of fermentation temperature on viable count,titratable acid and sensory evaluation of fermented pumpkin pulp
2.3.4 发酵时间对发酵南瓜浆活菌数、可滴定酸和感官评分的影响
发酵时间对发酵南瓜浆活菌数、可滴定酸和感官评分的影响见图8。由图8可知,随着发酵时间在12~28 h范围内的延长,发酵体系中的活菌数呈现先升高后趋于平缓的趋势。当发酵时间为24 h时,体系中乳酸菌进入对数期,活菌数达到最大值9.85 lg(CFU/mL);当发酵时间>24 h之后趋于稳定;可滴定酸随着发酵时间的延长不断累积增加,但产酸过多会造成乳酸菌发生自溶,不利于乳酸菌生长[28],并且太长的发酵时间会导致口感过酸,感官评分降低,因此,选择最适发酵时间为24 h。
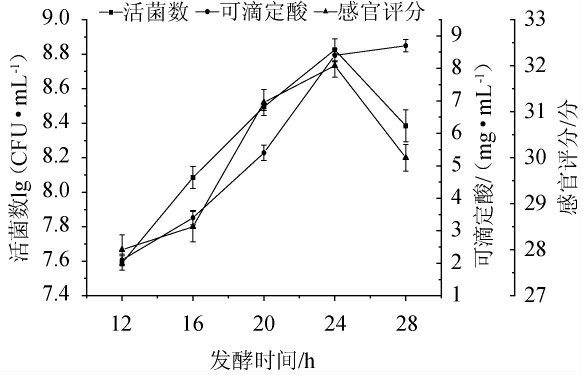
图8 发酵时间对发酵南瓜浆活菌数、可滴定酸和感官评分的影响
Fig.8 Effect of fermentation time on viable count,titratable acid and sensory evaluation of fermented pumpkin pulp
2.4 发酵工艺优化响应面试验
在单因素试验的基础上,以料液比(A)、接种量(B)、发酵温度(C)和发酵时间(D)为自变量,以活菌数(Y)为响应值,同时结合感官评价,运用Design-Expert 8.0.6软件设计响应面试验,Box-Benhnken试验设计及结果见表3。
表3 Box-Benhnken试验设计及结果
Table3 Design and results of Box-Benhnken experiment
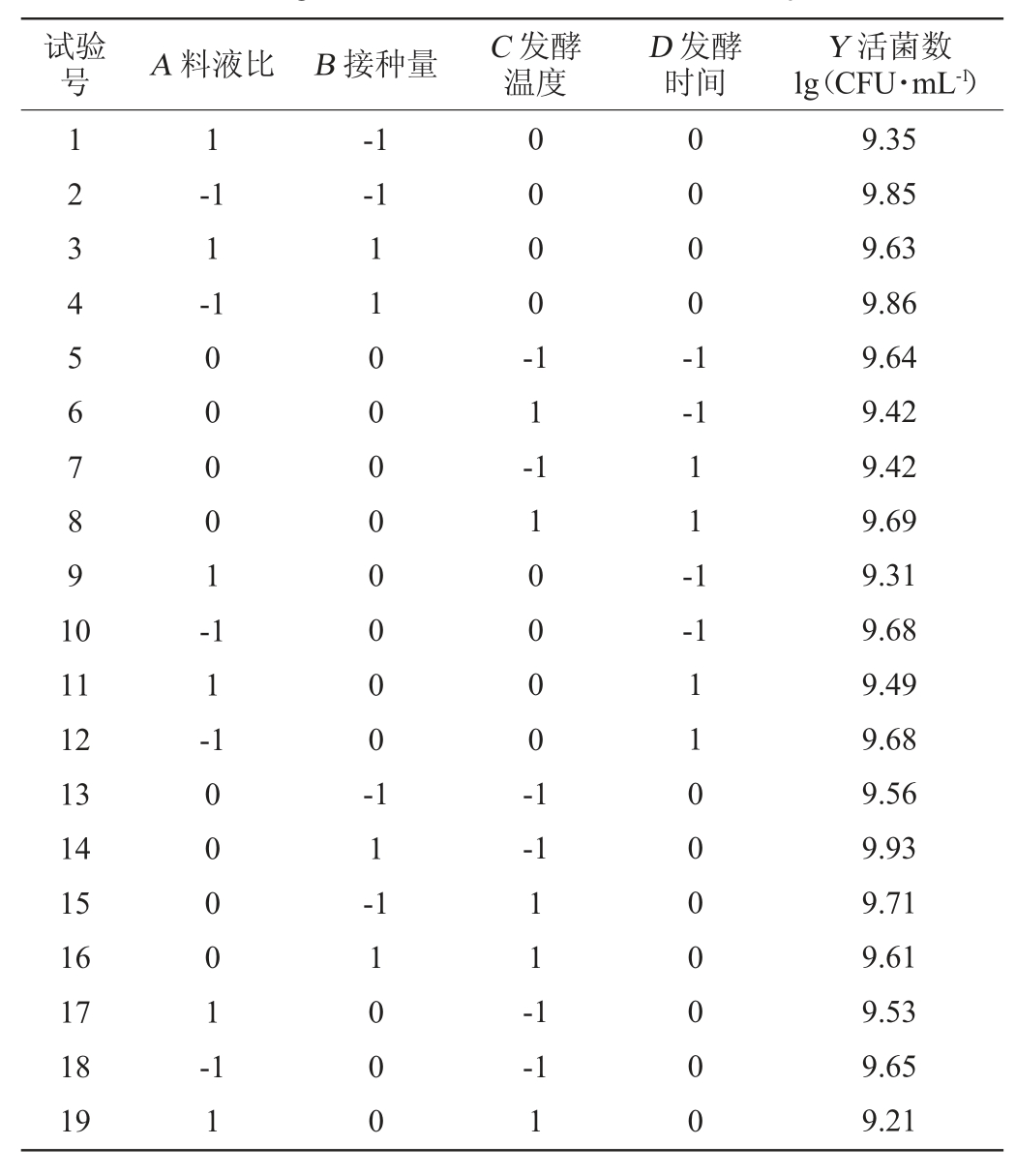
续表
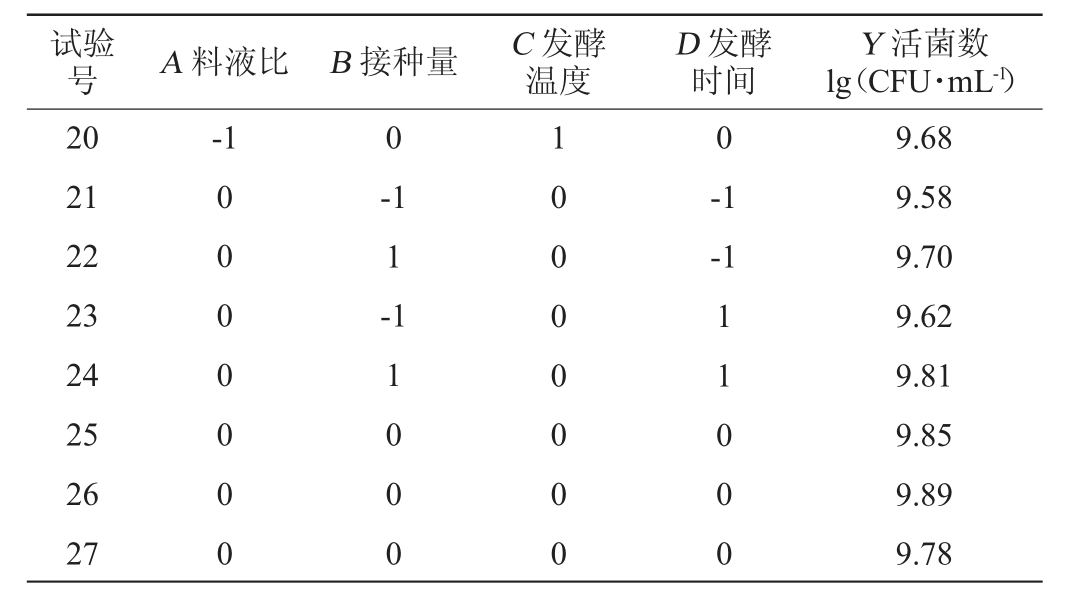
对表3试验结果进行多元回归拟合,获得响应值活菌数(Y)的回归模型方程式为:
Y=9.84-0.16A+0.072B-0.034C+0.032D+0.068AB-0.087AC+0.045AD-0.12BC+0.018BD+0.12CD-0.16A2-0.003B2-0.15C2-0.15D2
由表4可知,该模型极显著(P<0.01),失拟项不显著(P>0.05),模型决定系数R2为0.965 4,校正决定系数R2adj为0.925 1,说明模型与试验结果拟合度较好,可用于实际生产推测。由F值可得各因素对发酵南瓜浆中活菌数含量的影响程度从强到弱依次为料液比>接种量>发酵温度>发酵时间。由P值可得,一次项A、B,交互项AC、BC、CD,二次项A2、C2、D2对活菌数影响极显著(P<0.01),一次项C、D、交互项AB对活菌数影响显著(P<0.05)。
表4 回归模型方差分析
Table4 Variance analysis of regression model
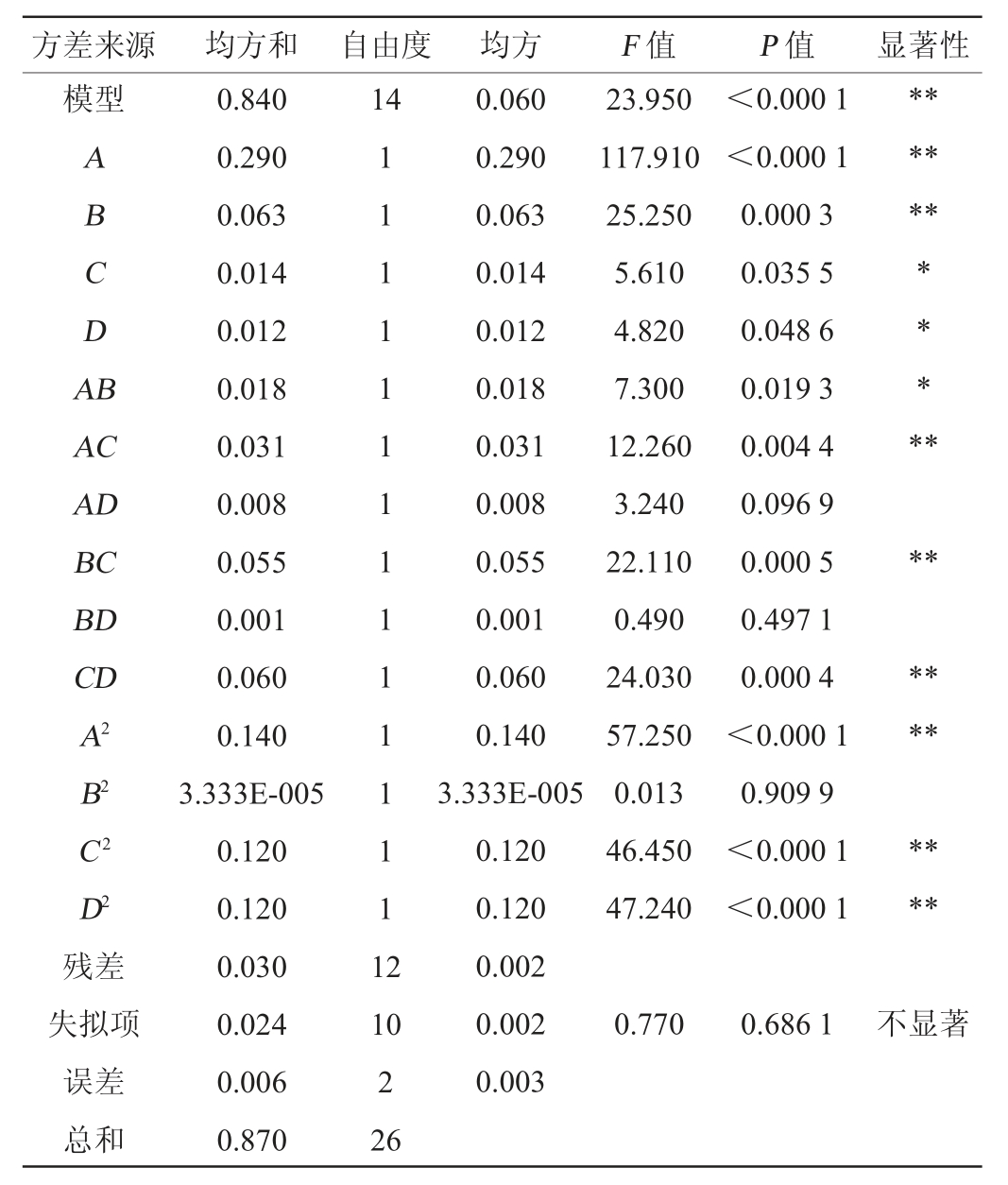
注:“*”表示对结果影响显著(P<0.05),“**”表示对结果影响极显著(P<0.01)。
4个因素交互作用对结果影响的响应面及等高线见图9。由图9可知,活菌数随着料液比的加大、发酵温度的升高、发酵时间的延长而呈现先增加后下降的趋势,并在料液比为1.1∶1~1.4∶1(g∶mL),发酵温度为33.4~35.4 ℃,发酵时间为22~26 h的范围内含量较高;随着接种量的增加,活菌数呈现先增加后趋于平缓的趋势,在接种量为7%~8%,发酵温度为33~35 ℃区间内,活菌数含量最高。
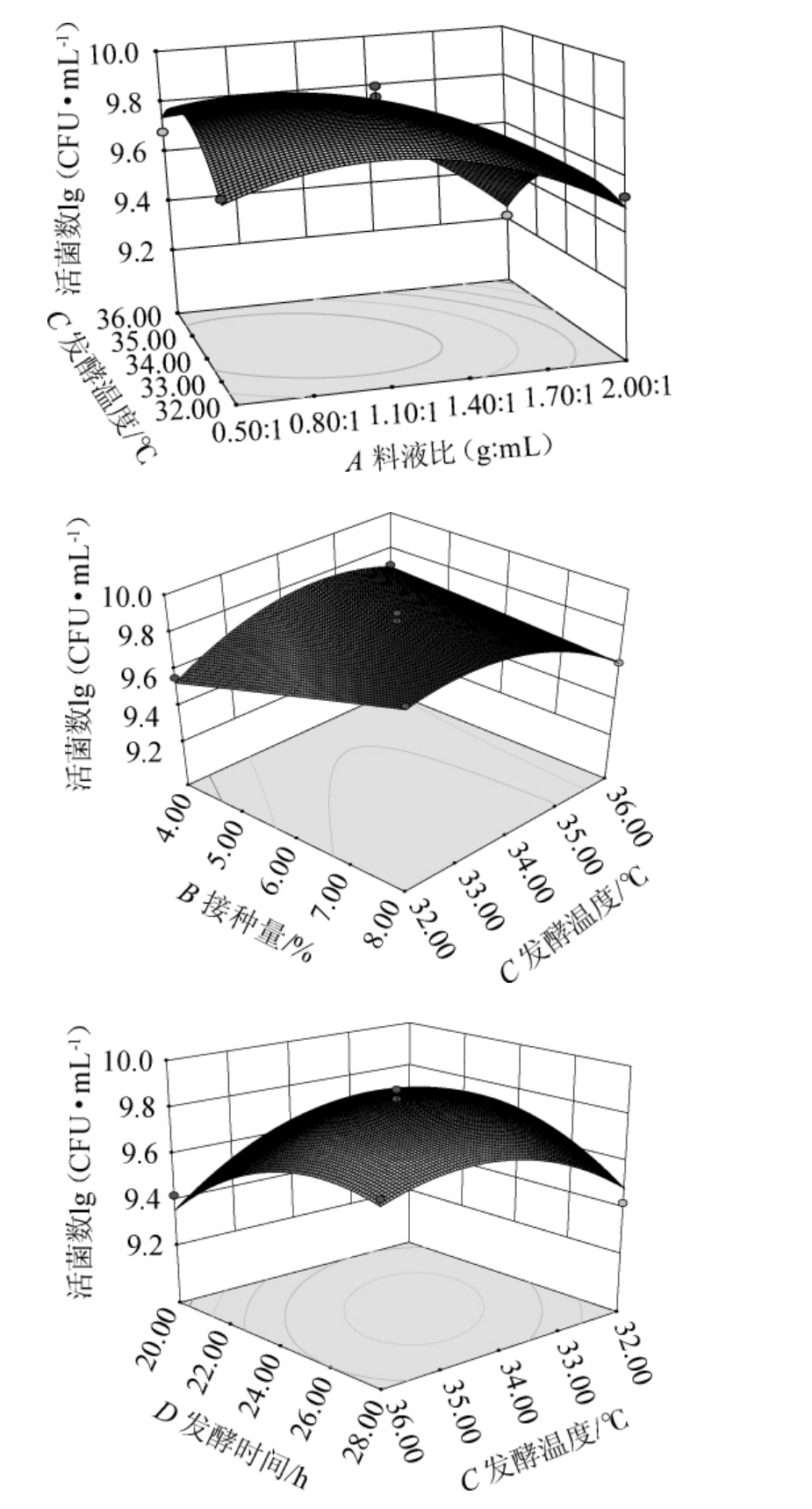
图9 料液比、接种量、发酵时间和发酵温度交互作用对活菌数影响的响应面及等高线
Fig.9 Response surface plots and contour lines of effects of interaction between solid and liquid ratio,inoculum,fermentation time and temperature on viable count
经过Design-Expert 8.0.6软件处理后,得到复合益生菌发酵南瓜浆的最佳工艺条件为:料液比1.26∶1(g∶mL),接种量7.81%(V/V),发酵温度32.93 ℃,发酵时间为24.39 h。在该条件下,预测发酵南瓜浆的活菌数为9.93 lg(CFU/mL)。为便于实际操作同时结合感官评价,将发酵工艺修改为料液比为1∶1(g∶mL),接种量为7.8%(V/V),发酵温度为33 ℃,发酵时间为24 h。在此最佳发酵工艺条件下,活菌数为9.89 lg(CFU/mL),与模型预测值较为吻合。
3 结论
本研究首先筛选出发酵能力最强、活菌数最高的植物乳杆菌(Lactobacillus plantarum)CICC21824和降酸速度最快、适应性最强的嗜热链球菌(Streptococcus thermophilus)CICC20373的两株益生菌菌株,继而按照1∶1的比例进行复合益生菌复配试验,在单因素试验的基础上,以活菌数为响应值,利用Box-Benhnken试验设计优化南瓜浆发酵工艺参数。最后确定复合益生菌发酵南瓜浆的最佳工艺条件为:料液比1∶1(g∶mL),接种量7.8%(V/V),发酵温度33 ℃,发酵时间24 h。在此最佳发酵工艺条件下,活菌数为9.89 lg(CFU/mL)。南瓜浆发酵饮品色泽金黄,感官评分较高,具有发酵产品特有风味,无异味。本研究为开发益生菌产品和南瓜类加工产品提供新思路,为后续研发南瓜发酵类产品提供实验及理论基础。
[1]KOBER M M,BOWE W P.The effect of probiotics on immune regulation,acne,and photo aging[J].Int J Women Dermatol,2015,1(2):85-89.
[2] PIMENTEL T C,MADRONA G S,GARCIA S,et al.Probiotic viability,physicochemical characteristics and acceptability during refrigerated storage of clarified apple juice supplemented with Lactobacillus paracasei ssp.paracasei oligofructose in different package type[J].LWT-Food Sci Technol,2015,63(1):415-422.
[3]CHEN W.Lactic acid bacteria[M].Singapore:Springer Nature Singapore Pte Ltd.and Science Press,2019:181-209.
[4]李楠,刘振民.益生菌与功能发酵乳开发研究进展[J].乳业科学与技术,2020,43(3):31-38.
[5]YOUNG Y K,EDWARD E W,YONG D H,et al.Production of probiotic cabbage juice by lactic acid bacteria[J].Bioresource Technol,2006,97(12):1427-1430.
[6]徐萌萌.益生菌发酵胡萝卜饮料营养特性及其储藏稳定性研究[D].南昌:南昌大学,2016.
[7]杜静婷,施俊凤,贾慧文,等.适于南瓜汁原料益生酵母菌的分离鉴定及发酵工艺优化[J].食品工业科技,2020,41(17):91-97.
[8]黄黎慧,黄群,于美娟.南瓜的营养保健价值及产品开发[J].现代食品科技,2005,21(3):176-179.
[9]何凤林.玉米南瓜复合饮料的研制[J].包装与食品机械,2016,34(1):26-30.
[10]韦云路,李璐,李全宏.南瓜醋的澄清工艺优化及其抗氧化活性研究[J].中国酿造,2018,37(10):31-35.
[11]周春丽,刘伟,李慧,等.混合菌株发酵南瓜汁及其香气分析[J].现在食品科技,2014,30(5):301-310.
[12]DINI I,TENORE G C,DINI A.Effect of industrial and domestic processing on antioxidant properties of pumpkin pulp[J].LWT-Food Sci Technol,2013,53(1):382-385.
[13]KIM M Y,KIM E J,KIM Y N,et al.Comparison of the chemical compositions and nutritive values of various pumpkin(Cucurbitaceae)species and parts[J].Nutr Res Pract,2012,6(1):21-27.
[14]赵晨.益生菌果蔬汁的研究现状[J].现代食品,2020,17:35-40.
[15]马欣,古绍彬,吴影.凝结芽孢杆菌复合干酪乳杆菌发酵南瓜饮料的研制[J].食品与发酵工业,2018,44(7):161-167.
[16]梁莉,程晨,张柳茵,等.乳酸菌和酵母菌复合发酵南瓜汁工艺研究[J].食品研究与开发,2016,37(13):88-92.
[17]仵白敏,杨文博,刘慧,等.复合益生菌协同发酵葡萄汁菌种筛选与工艺优化[J].食品工业科技,2020,41(13):122-127.
[18]欧阳佳,兰雪花,李清明,等.复合乳酸菌发酵淮山工艺优化研究[J].食品研究与开发,2020,41(20):119-123.
[19] LIU W L,FAN M T,SUN S Y,et al.Effect of mixed fermentation by Torulaspora delbrueckii,Saccharomyces cerevisiae,and Lactobacillus plantarum on the sensory quality of black raspberry wines[J].Eur Food Res Technol,2020,246(8):1573-1581.
[20]周印,刘梦阳,赵婧琦,等.植物乳杆菌发酵梨原汁饮料的研究[J].食品研究与开发,2020,41(8):105-111.
[21]中国工业微生物菌种保藏中心.菌种说明书[EB/OL].(2021-04-28).http://sales.china-cicc.org/.
[22]束文秀,吴祖芳,翁佩芳,等.植物乳杆菌和发酵乳杆菌对胡柚汁发酵品质及其抗氧化性的影响[J].食品科学,2019,40(2):152-158.
[23]张桂红,王宏慧,孙靖华.南瓜活性成分的研究进展[J].食品科技,2013,20(4):78-81.
[24]彭兴兴.乳酸菌发酵南瓜浆的研究[D].广州:华南理工大学,2016.
[25]袁晶,康三江,宋娟.响应面法优化乳酸菌发酵苹果浆工艺及其抗氧化活性分析[J].中国酿造,2020,39(12):86-90.
[26]刘玉凌,任亭,彭玉梅,等.老盐水中乳酸菌的筛选鉴定及其在青菜头泡菜中的应用[J].食品与发酵工业,2020,46(2):208-213.
[27]刘佳奇,熊涛,李军波,等.乳酸菌发酵茶饮料的工艺优化及其发酵前后香气成分分析[J].食品与发酵工业,2016,42(8):109-114.
[28]任婷婷,岳田利,魏欣,等.益生菌发酵苹果浆工艺优化及发酵前后挥发性风味成分分析[J].食品科学,2019,40(8):87-93.