随着社会的快速发展和人民生活水平的提高,人们餐桌上逐渐增加了大鱼大肉等高脂食物,同时饮酒成为人们日常生活的一部分,许多场合饮酒伴随着高脂食物的摄入。而今人们开始重视健康的生活方式和饮食习惯,往往只关注不健康的饮酒习惯给机体造成的损伤,而忽视了适量、科学饮酒对机体的影响[1]。已有研究表明,长期过量饮酒会使肝脏功能受损,导致肠道菌群紊乱[2]。然而,适量饮酒能够减少机体炎症反应的发生,有效降低高血压、冠心病、动脉粥样硬化、痴呆等疾病的发病风险[3-4]。
白酒成分复杂,与人体健康的关系尚不明确,如何科学饮酒值得深入探讨[5]。高脂饮食中食物脂肪含量高,长期食用会使体内脂肪水平超出正常范围,当机体的能量摄入多于能量消耗时会导致肥胖,易造成心血管等一系列疾病[6-7]。此外,高脂饮食还能够引起肠道组织氧化应激发生,改变肠道微生态[8]。目前,已有研究表明饮用不同香型和品质的白酒对机体的影响存在差异,而针对高脂饮食的动物研究相对较少。毛华等[9]探索了不同剂量的酱香型白酒对大鼠血脂、血糖、胰岛素敏感性的影响,发现适量饮酒能提高大鼠高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)含量,且不产生胰岛素抵抗;汪家文等[10]探讨了不同浓度清香型白酒对大鼠血脂的影响及其与脑血管病的关系,发现大鼠血清中总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)升高水平或HDL-C降低水平与脑血管病变程度之间存在浓度效应关系;李钰等[11]报道,适量浓香型白酒可以在一定程度上具有预防动脉粥样硬化发生发展的作用;方程[12]研究发现,酱香型白酒通过调节肠道菌群结构可以减轻乙醇诱导的肝损伤;鲁蕾等[13]研究发现,饮用不同品质浓香型白酒对大鼠肠道菌群的影响存在差异,高品质白酒对机体肠道菌群影响更小,更利于维护肠道微生态平衡。已有研究报道,充分发挥白酒中生物活性物质的功效能减轻酒精成分对人体的损害,其中短链脂肪酸及其乙酯能加快乙醇在体内的代谢,降低白酒的醉度,影响肠道内微生物的生长代谢,保护肠黏膜屏障[14]。
近年来,白酒对脂代谢和肠道菌群的影响逐步成为很多人关注的问题。作为中国白酒十一大国标香型之一的馥郁香型白酒鲜有报道,故本研究采用高脂小鼠模型,通过灌胃不同剂量的馥郁香型白酒,研究小鼠脏器、血脂相关指标及肠道菌群结构的变化,旨在探讨一定剂量下馥郁香型白酒对高脂饮食小鼠脂代谢及肠道菌群的影响,为了解该香型白酒饮后舒适度提供参考。
1 材料与方法
1.1 材料与试剂
馥郁香型白酒(酒精度52%vol):市售;无特定病原体(specific pathogen free,SPF)级健康雄性Balb/c小鼠(饲养于农业部农产品质量监督检验测试中心(北京)SPF级动物房(SYXK(京)2020-0052),饲养环境温度维持在(22±1)℃,湿度稳定在(55±5)%,每12 h昼夜气流交替一次):北京维通利华实验动物技术有限公司;基础饲料、高脂饲料:北京华阜康生物科技股份有限公司![]() Pro Kit:美国QIAGEN公司;总胆固醇(TC)测定试剂盒、甘油三酯(TG)测定试剂盒、低密度脂蛋白胆固醇(LDL-C)测定试剂盒、高密度脂蛋白胆固醇(HDL-C)测定试剂盒、超氧化物歧化酶(superoxide dismutase,SOD)检测试剂盒:南京建成生物工程研究所;16S rRNA的V3-V4区引物:上海生工生物工程股份有限公司;琼脂糖:西班牙Biowest公司;FastPfu Polymerase:北京全式金生物技术有限公司;AxyPrep DNAGelExtractionKit:美国Axygen公司;NEXTFLEX
Pro Kit:美国QIAGEN公司;总胆固醇(TC)测定试剂盒、甘油三酯(TG)测定试剂盒、低密度脂蛋白胆固醇(LDL-C)测定试剂盒、高密度脂蛋白胆固醇(HDL-C)测定试剂盒、超氧化物歧化酶(superoxide dismutase,SOD)检测试剂盒:南京建成生物工程研究所;16S rRNA的V3-V4区引物:上海生工生物工程股份有限公司;琼脂糖:西班牙Biowest公司;FastPfu Polymerase:北京全式金生物技术有限公司;AxyPrep DNAGelExtractionKit:美国Axygen公司;NEXTFLEX Rapid DNA-Seq Kit:美国Bioo Scientific公司;MiSeq Reagent Kit v3/NovaSeq Reagent Kits:美国Illumina公司;油红O:阿拉丁试剂(上海)有限公司。
Rapid DNA-Seq Kit:美国Bioo Scientific公司;MiSeq Reagent Kit v3/NovaSeq Reagent Kits:美国Illumina公司;油红O:阿拉丁试剂(上海)有限公司。
1.2 仪器与设备
ME403E天平、AC2-4S1生物安全柜:新加坡ESCO公司;7600全自动生化分析仪:日本HITACHI公司;Illumina Miseq PE300测序仪:美国Illumina公司;NANODROP紫外分光光度计:美国Thermo公司;5427R高速冷冻离心机、ABI![]() 9700型聚合酶链式反应(polymerase chain reaction,PCR)仪:美国ABI公司;DYY-6C电泳仪:北京市六一仪器厂;BX51光学显微镜:日本OLYMPUS公司。
9700型聚合酶链式反应(polymerase chain reaction,PCR)仪:美国ABI公司;DYY-6C电泳仪:北京市六一仪器厂;BX51光学显微镜:日本OLYMPUS公司。
1.3 方法
1.3.1 动物实验
Balb/c小鼠共60只,适应性喂养1周后按体质量随机分为5组,即基础饲料对照组,饲喂基础饲料;高脂饲料模型组、低剂量组、中剂量组和高剂量组,饲喂高脂饲料。每组12只,每6只一笼。按照《中国居民膳食指南》建议男性每日饮酒的酒精量≤25 g为参照,标准人体质量60 kg计算,人体每日饮酒量为100 mL,由此设置52%vol馥郁香型白酒9.1 mL/kg体质量为高剂量组;中剂量组为7.6 mL/kg体质量,相当于成人喝50 mL馥郁香型白酒;低剂量组为6.0 mL/kg体质量。高、中、低剂量组灌胃受试样品,基础饲料对照组和高脂饲料模型组给予蒸馏水,连续灌胃6周。试验期间各组小鼠均自由采食与饮水,每天固定时间进行灌胃处理,每周更换两次垫料,每周记录一次小鼠体质量和食物剩余量。末次处理后,小鼠夜间禁食(不禁水)8 h后,眼球毛细管采血0.5~1.0 mL,随后将小鼠脱颈处死,解剖后摘除肝脏、肾脏、附睾脂肪和肾周脂肪,取出小鼠盲肠内容物1~2 g。
1.3.2 检测方法
脏器系数[15]:用纸吸干肝脏、附睾脂肪和肾周脂肪表面液体,使用电子天平立即分别称量质量,计算小鼠脏器系数,其计算公式如下:
肝脏内脂质、超氧化物歧化酶(superoxide dismutase,SOD)指标:按照各检测指标试剂盒说明书中的要求制备合适的组织匀浆液后进行测定。
附睾脂肪和肾周脂肪的油红O染色切片[16]:分离附睾和肾周脂肪组织,液氮冷冻制作冰冻切片,随后进行油红O溶液染色(0.5 g油红O/100 mL,溶解于异丙醇中),切片于光学显微镜下进行观察。
血清指标:采集的血液于4 ℃静置4 h,4 ℃、4 000 r/min条件下离心15 min,收集上层血清,采用试剂盒方法测定血清中TC、TG、HDL-C、LDL-C含量。
1.3.3 小鼠肠道菌群多样性的分析
参照![]() Kit说明书提取肠道细菌脱氧核糖核酸(deoxyri-bonucleic acid,DNA),以其为模板,使用通用引物338F(5'-ACTCCTACGGGAGGCAGCAG-3')和806R(5'-GGACTACHVGGGTWTCTAAT-3')对细菌的16S rDNA V3-V4可变区基因序列进行PCR扩增。PCR扩增程序:95 ℃预变性3 min;95 ℃变性30 s,55 ℃退火30 s,72 ℃延伸30 s,共27个循环;72 ℃再延伸10 min。PCR扩增体系:5×TransStart FastPfu缓冲液4 μL,2.5 mmol/L脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTPs)2 μL,上游引物(5 μmol/L)0.8μL,下游引物(5 μmol/L)0.8 μL,TransStart FastPfu DNA聚合酶0.4 μL,模板DNA 10 ng,双蒸水(ddH2O)补足至20 μL。每个样本3个重复。应用Illumina Miseq PE300平台(上海美吉生物医药科技有限公司)对PCR扩增产物进行测序。使用fastp[17](version 0.20.0)软件对原始测序序列进行质控;使用软件FLASH[18](version 1.2.11)拼接序列;使用UPARSE[19]软件(version 7.1),根据97%[19-20]的相似度对序列进行操作分类单元(operational taxonomic unit,OTU)聚类并剔除嵌合体;利用RDP classifier[21](version 2.2)对每条序列进行物种分类注释、物种复杂度分析;利用Mothur软件(version 1.31.2)对组间物种的α-多样性进行分析;利用线性判别分析效应量(linear discriminant analysis effect size,LEfSe)软件进行LEfSe多级物种差异线性判别分析(linear discriminant analysis,LDA)。
Kit说明书提取肠道细菌脱氧核糖核酸(deoxyri-bonucleic acid,DNA),以其为模板,使用通用引物338F(5'-ACTCCTACGGGAGGCAGCAG-3')和806R(5'-GGACTACHVGGGTWTCTAAT-3')对细菌的16S rDNA V3-V4可变区基因序列进行PCR扩增。PCR扩增程序:95 ℃预变性3 min;95 ℃变性30 s,55 ℃退火30 s,72 ℃延伸30 s,共27个循环;72 ℃再延伸10 min。PCR扩增体系:5×TransStart FastPfu缓冲液4 μL,2.5 mmol/L脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTPs)2 μL,上游引物(5 μmol/L)0.8μL,下游引物(5 μmol/L)0.8 μL,TransStart FastPfu DNA聚合酶0.4 μL,模板DNA 10 ng,双蒸水(ddH2O)补足至20 μL。每个样本3个重复。应用Illumina Miseq PE300平台(上海美吉生物医药科技有限公司)对PCR扩增产物进行测序。使用fastp[17](version 0.20.0)软件对原始测序序列进行质控;使用软件FLASH[18](version 1.2.11)拼接序列;使用UPARSE[19]软件(version 7.1),根据97%[19-20]的相似度对序列进行操作分类单元(operational taxonomic unit,OTU)聚类并剔除嵌合体;利用RDP classifier[21](version 2.2)对每条序列进行物种分类注释、物种复杂度分析;利用Mothur软件(version 1.31.2)对组间物种的α-多样性进行分析;利用线性判别分析效应量(linear discriminant analysis effect size,LEfSe)软件进行LEfSe多级物种差异线性判别分析(linear discriminant analysis,LDA)。
1.3.4 统计学分析方法
采用SPSS 24.0软件进行数据的统计分析,结果采用“平均值±标准差”(x±s)表示。方差齐时进行单因素方差分析(analysis of variance,ANOVA),LSD检验进行组间两两比较;方差不齐时使用Kruskal-Wallis检验。
2 结果与分析
2.1 馥郁香型白酒对小鼠肝脏系数、肝脏内脂质及SOD活力的影响
基础饲料对照组、高脂饲料模型组以及高脂-低、中、高剂量组小鼠肝脏系数、肝脏内脂质及SOD活力检测结果见表1。
表1 各处理组小鼠肝脏系数、肝脏内脂质及超氧化物歧化酶活力的检测结果
Table1 Determination results of liver coefficient,lipids and superoxide dismutase activity in liver in treatment groups
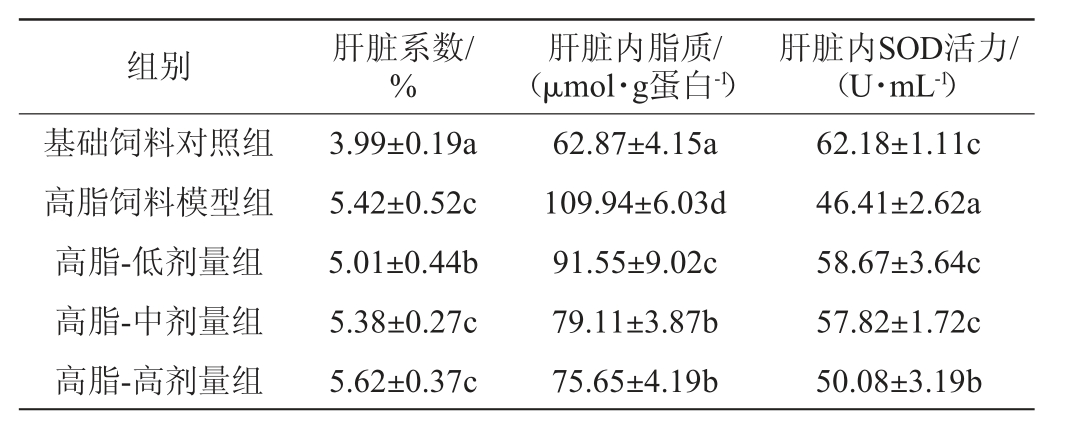
注:每一列不同小写字母表示差异显著(P<0.05)。下同。
由表1可知,与基础饲料对照组相比,高脂饲料模型组小鼠的脏器指数、肝脏内脂质显著增加(P<0.05),SOD活力显著下降(P<0.05),说明高脂饮食会导致小鼠肝脏系数、肝脏内脂质增加、SOD活力下降。与高脂饲料模型组相比,高脂-低剂量组小鼠的肝脏系数显著降低(P<0.05),说明低剂量的馥郁白酒可以缓解高脂引起的小鼠肝脏系数的升高;高脂-低、中、高剂量组小鼠的肝脏内脂质显著下降(P<0.05),SOD活力显著上升(P<0.05),说明饲喂高脂饲料的同时摄入馥郁香型白酒有助于缓解高脂引起的小鼠肝脏内脂质的升高、SOD活力的降低,分析原因可能是适量的馥郁香型白酒具有一定的抗氧化作用,与文献[22]报道结果一致。结果表明,适量饮用馥郁香型白酒能够缓解高脂摄入对肝脏的影响及其脂质的积累,白酒在酿造过程中产生的某些生物活性组分可能对肝脏起到一定的保护作用,机理尚待深入研究[23-24]。
2.2 馥郁香型白酒对小鼠附睾脂肪和肾周脂肪的影响
基础饲料对照组、高脂饲料模型组以及高脂-低、中、高剂量组小鼠附睾脂肪系数和肾周脂肪系数的检测结果见表2。
表2 各处理组小鼠附睾脂肪系数和肾周脂肪系数的检测结果
Table2 Determination results of epididymisadipose and perirenal fat coefficient of mice in treatment groups

由表2可知,与基础饲料对照组相比,高脂饲料模型组小鼠的附睾脂肪系数与肾周脂肪系数显著升高(P<0.05)。与高脂饲料模型组相比,高脂-低、中、高剂量组小鼠的附睾脂肪系数及肾周脂肪系数显著降低(P<0.05),且除高脂-高剂量组小鼠的附睾脂肪系数外,均与基础饲料对照组无显著差异(P>0.05)。说明饲喂高脂饲料的同时摄入馥郁香型白酒有助于缓解高脂引起的附睾脂肪系数及肾周脂肪系数的升高,甚至在一定剂量下可以恢复至基础饲料对照组水平。同时,对附睾脂肪和肾周脂肪的油红O染色切片观察,结果见图1。由图1可知,高脂饲料能够显著增加脂肪滴在附睾和肾周中的聚集,适量的馥郁香型白酒能一定程度地抑制高脂饲料引发的附睾和肾周脂肪滴聚集和增多。
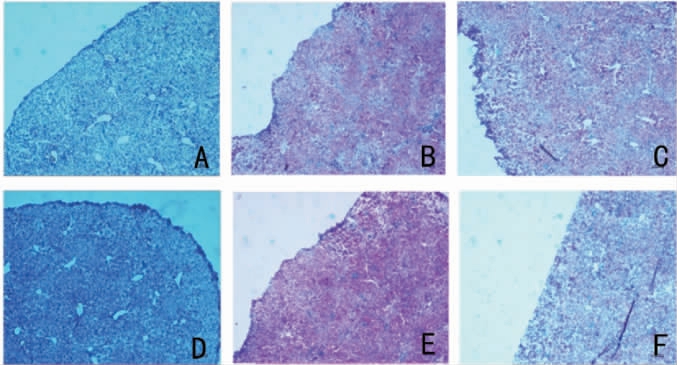
图1 附睾脂肪和肾周脂肪的油红O染色切片
Fig.1 Oil red O stained sections of epididymisadipose and perirenal fat
A:基础饲料对照组附睾内脂肪;B:高脂饲料模型组附睾内脂肪;C:高脂-高剂量组附睾内脂肪;D:基础饲料对照组肾周脂肪;E:高脂饲料模型组肾周脂肪;F:高脂-高剂量组肾周脂肪。
2.3 馥郁香型白酒对小鼠血脂的影响
基础饲料对照组、高脂饲料模型组以及高脂-低、中、高剂量组小鼠血清TC、TG、HDL-C及LDL-C含量的检测结果见表3。
表3 各处理组小鼠血脂相关指标的检测结果
Table3 Determination results of blood lipid related indexes of mice in treatment groups
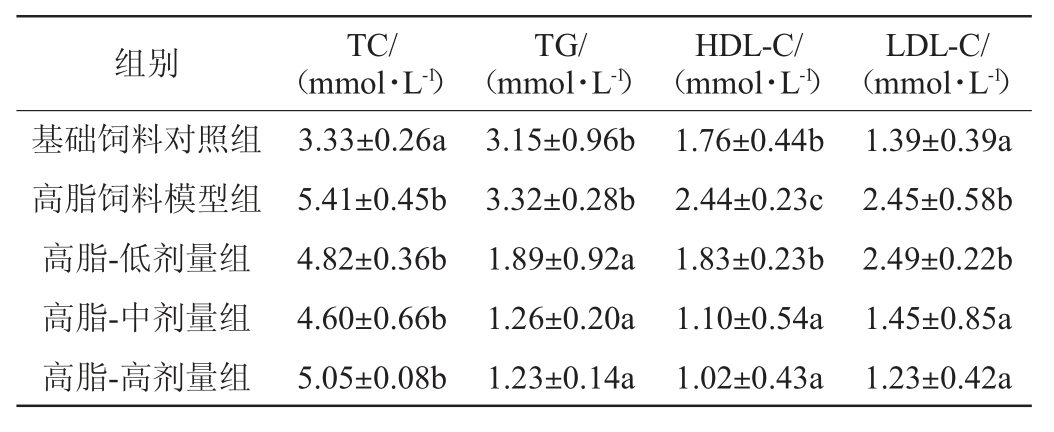
由表3可知,与基础饲料对照组相比,高脂饲料模型组小鼠血清中的TC、HDL-C、LDL-C含量显著升高(P<0.05),TG含量变化不显著(P>0.05)。与高脂饲料模型组相比,除高脂-低剂量组小鼠的LDL-C外,高脂-低、中、高剂量组小鼠血清中的TG、HDL-C及LDL-C含量显著降低(P<0.05),TG含量下降但不显著(P>0.05)。结果表明,适量饮用馥郁香型白酒能够降低高脂饮食带来的血脂指标的升高,降低血脂指标的异常升高有助于预防心脑血管疾病发生和发展[25]。目前对于饮酒与血脂的关系有不同的报道,饮用剂量也各不相同,丁书文等[26]研究发现,少量饮酒无升高HDL-C含量作用,大量饮酒TC含量下降;康金森等[27]研究发现,饮用一定剂量的酒可使高脂血症大鼠血清中TC、TG和LDL-C水平明显降低;类春燕等[28]研究发现,低剂量白酒组LDL含量显著降低,高剂量白酒组HDL明显升高。
2.4 馥郁香型白酒对小鼠肠道菌群的影响
2.4.1 馥郁香型白酒对小鼠肠道菌群多样性的影响
根据《中国居民膳食指南》推荐剂量,选择高脂-高剂量组进一步研究馥郁香型白酒对小鼠肠道菌群的影响。Alpha多样性分析能反映特定区域或生态系统内的丰富度和均匀度[29]。相同物种丰富度的情况下,群落中各物种均匀度越大,则认为群落多样性越高[30]。小鼠肠道菌群α-多样性指数分析结果见表4。
表4 小鼠肠道细菌菌群α-多样性指数分析结果
Table4 Results of alpha diversity indexes analysis of intestinal flora in mice

由表4可知,与基础饲料对照组比较,高脂饲料模型组的OUTs、Shannon指数显著下降(P<0.05),Simpson指数显著升高(P<0.05),ACE指数及Chao1指数无显著变化(P>0.05),说明高脂饮食能降低小鼠肠道菌群的多样性,对丰富度影响不大。与高脂饲料模型组比较,高脂-高剂量组小鼠的OUTs、Shannon指数显著升高(P<0.05),Simpson指数显著下降(P<0.05),ACE指数及Chao1指数无显著变化(P>0.05),说明高脂饮食的同时饮用高剂量馥郁香型白酒对小鼠肠道菌群丰度没有显著变化,而多样性有所提高。结果表明,适量的馥郁香型白酒能够一定程度缓解因高脂饮食导致的肠道菌群多样性失衡。
2.4.2 馥郁香型白酒对小鼠肠道菌群结构的影响
各组小鼠肠道菌群在科、属水平上的注释结果见图2。
由图2a可知,在科分类水平上,基础饲料对照组、高脂饲料模型组、高脂-高剂量组小鼠肠道的主要菌为毛螺菌科(Lachnospiraceae)(相对含量为25.96%、69.14%、49.84%)、脱硫弧菌科(Desulfovibrionaceae)(相对含量为5.04%、17.00%、12.72%)、普雷沃氏菌科(Prevotellaceae)(相对含量为23.42%、0.10%、11.00%)、颤螺旋菌科(Oscillospiraceae)(相对含量为2.95%、1.90%、9.18%)、瘤胃球菌科(Ruminococcaceae)(相对含量为1.16%、1.04%、3.19%)等。毛螺菌科属于厚壁菌门(Firmicutes)的优势菌群,产生丁酸盐将多糖进行降解并产生能量,小鼠吸收后有引起肥胖、糖尿病等代谢疾病的风险[31]。与基础饲料对照组相比,高脂饲料模型组小鼠肠道毛螺菌科含量提高了166.33%,高脂-高剂量组小鼠肠道毛螺菌科含量提高了91.99%,说明饮酒可以对高脂饮食产生大量能量效应有一定抑制作用。有研究表明,在糖尿病患者的粪便中,普雷沃氏菌科的含量显著低于正常人群[32]。本研究中高脂饮食后小鼠肠道的普雷沃氏菌科含量显著低于基础饲料对照组,虽然饮酒后同样引起普雷沃氏菌科含量降低,但与高脂饲料模型组相比普雷沃氏菌科含量上升了109%(P<0.05)。
由图2b可知,在属分类水平上,基础饲料对照组、高脂饲料模型组、高脂-高剂量组小鼠肠道的主要菌为脱硫弧菌属(Desulfovibrio)(相对含量为4.89%,、47.66%、32.97%)、布劳特氏菌属(Blautia)(相对含量为0.64%、15.68%、20.76%)、拟普雷沃菌属(Alloprevotella)(相对含量为21.38%、0.01%、0.15%)、罗斯氏菌属(Roseburia)(相对含量为3.73%、0.49%、2.02%)、瘤胃球菌属(Ruminococcus)(相对含量为0.01%、0.59%、3.90%)等。脱硫弧菌属属于脱硫弧菌科,是一种还原硫酸盐的菌,可以降解短链脂肪酸、氨基酸等营养成分而产生有毒物质H2S,从而破坏肠黏膜屏障,导致内毒素进入循环系统而产生炎症反应[33]。与基础饲料对照组相比,高脂饮食引起小鼠脱硫弧菌属相对含量上升。与高脂饲料模型组相比,饮酒伴随高脂饮食缓解了单纯高脂饮食引起的脱硫弧菌属含量上升,该菌属含量下降30.82%(P<0.05)。罗斯氏菌属属于毛螺菌科,该菌属产生丁酸盐,若同时食用高纤维饮食的小鼠患动脉粥样硬化和炎症减少[34]。与基础饲料对照组相比,高脂饮食引起小鼠罗斯氏菌属相对含量显著下降(P<0.05)。与高脂饲料模型组相比,饮酒伴随高脂饮食缓解了单纯高脂饮食引起的罗斯氏菌属含量下降,该菌属含量上升312.24%(P<0.05)。瘤胃球菌属属于瘤胃球菌科(Ruminococcaceae),可以促进多种多糖和纤维的降解产生短链脂肪酸,且其丰度与酒精性肝硬化、增加肠道通透性及溃疡性结肠炎等呈显著负相关[35]。与基础饲料对照组相比,高脂饲料模型组与高脂-高剂量组中的瘤胃球菌属相对含量均有升高,后者更为显著(P<0.05)。与高脂饲料模型组相比,高脂-高剂量组中瘤胃球菌属相对含量升高了561.02%(P<0.05)。由此可见,适量的馥郁香型白酒显著提高了瘤胃球菌属含量,有助于降低肝病和溃疡性结肠炎的风险,对肠道保持稳态具有一定意义[36]。
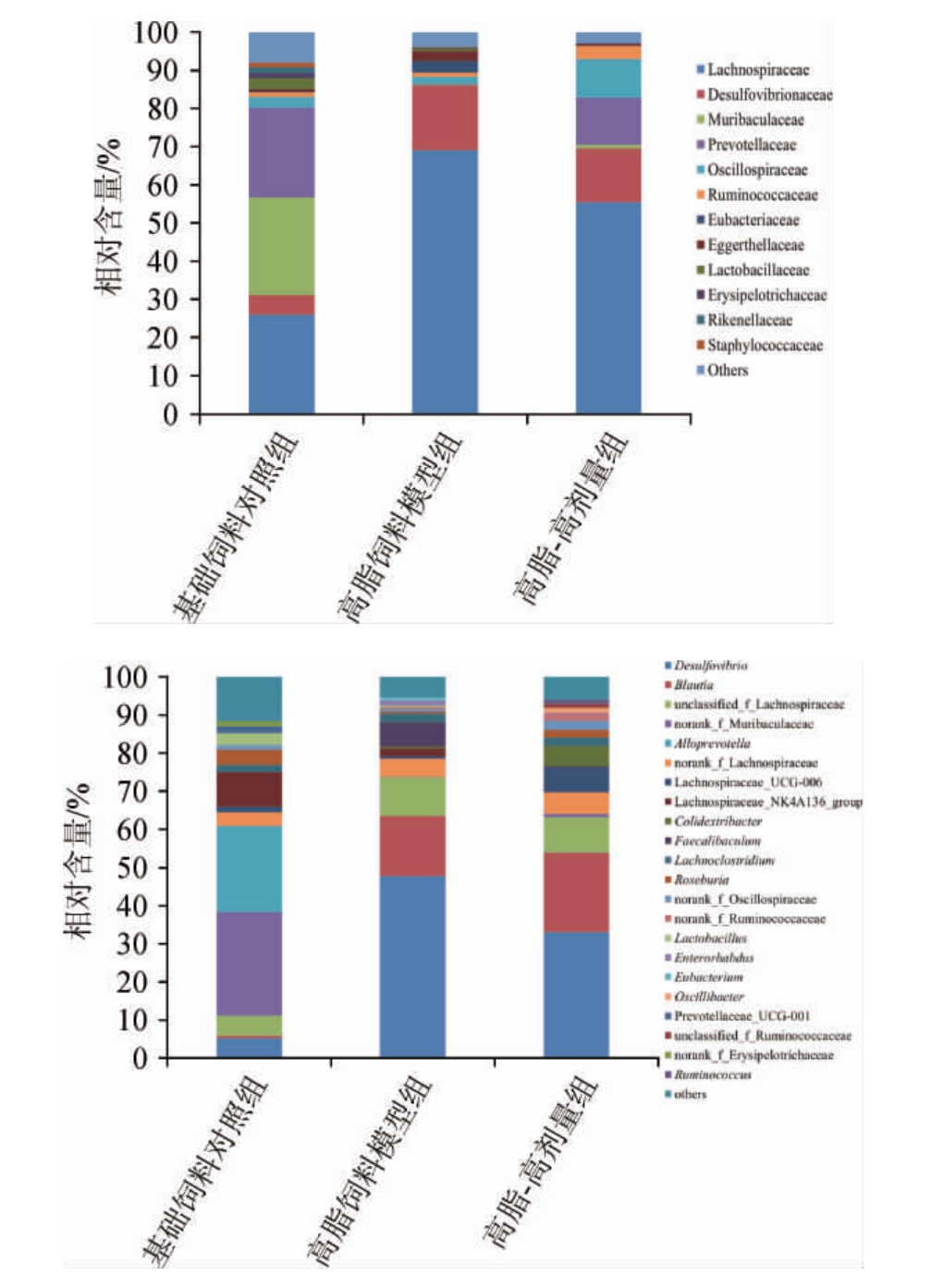
图2 基于科(a)和属(b)水平小鼠肠道菌群结构
Fig.2 Structure of intestinal flora in mice based on family (a) genus (b)level
other:相对含量<1%的其他物种。
2.4.3 差异物种线性判别分析
为了分析基础饲料对照组、高脂饲料模型组及高脂-高剂量组特征细菌类群和显著丰度差异特征,进行了LEfSe多级物种差异线性判别分析,结果见图3。
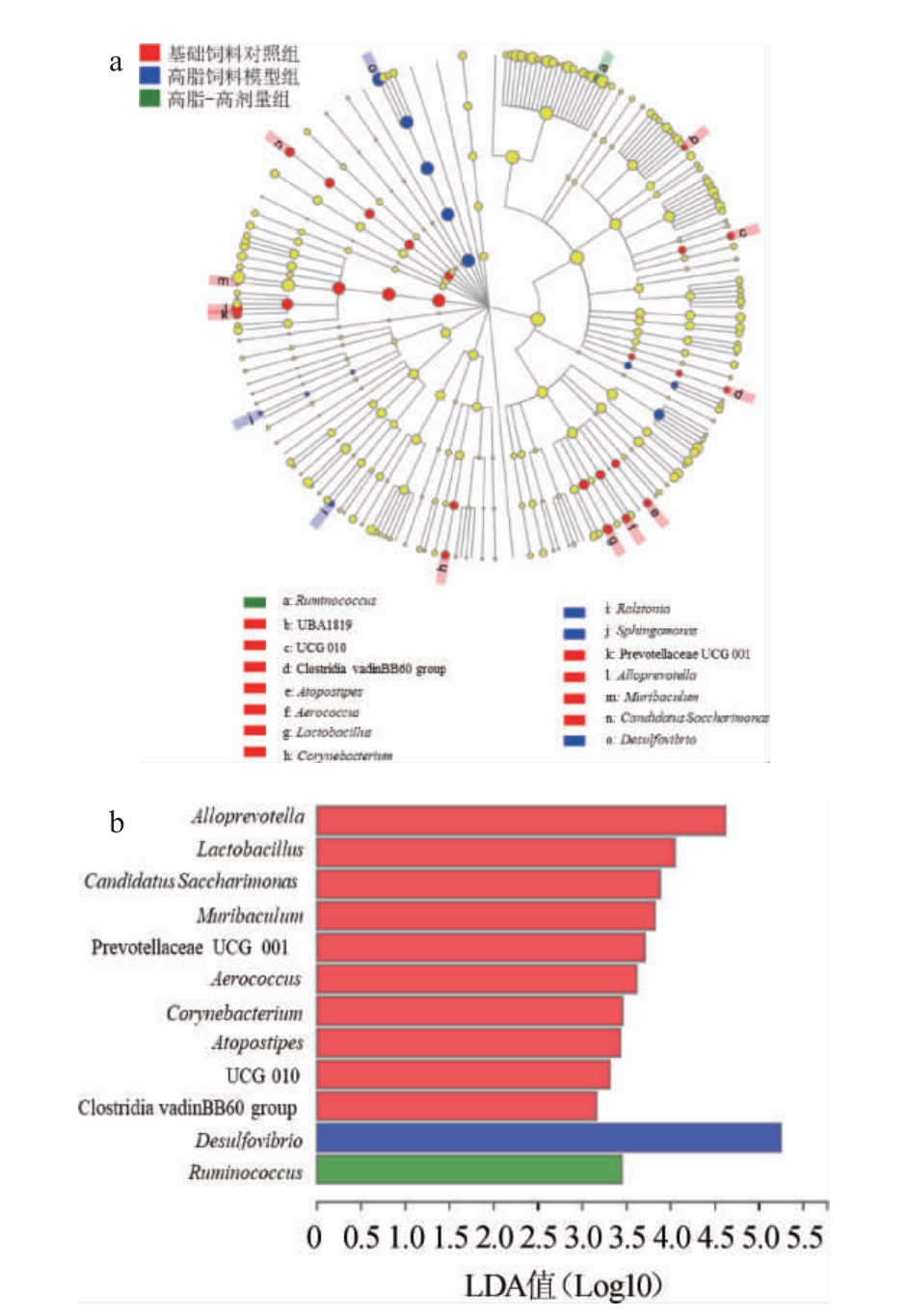
图3 LEfSe多级物种差异线性判别分析
Fig.3 Linear discriminant analysis of LEfSe multilevel species differences
a:差异物种的物种进化分支图;
b:差异物种的LDA值分布图(仅显示LDA值>3的物种)
由图3可知,在基础饲料对照组中,拟普雷沃菌属(LDA值为4.68)、乳酸菌属(LDA值为4.06)、Candidatus Saccharimonas(LDA值为3.90)、Muribaculum(LDA值为3.85)、Prevotellaceae_UCG_001(LDA值为3.74)等红色标记为差异物种,相对含量显著高于高脂饲料模型组和高脂-高剂量组。脱硫弧菌属(LDA值为5.26)在高脂饲料模型组中相对含量显著高于基础饲料对照组和高脂-高剂量组,是对高脂饲料模型组在组间差异具有显著影响的菌属。瘤胃球菌属(LDA值为3.45)在高脂-高剂量组中相对含量显著高于基础饲料对照组和高脂饲料模型组,是对高脂-高剂量组在组间差异具有显著影响的菌属。该结果说明,适量的馥郁香型白酒可以提高瘤胃球菌属含量,有效促进肠道中益生菌的增殖,瘤胃球菌属是判别饮用馥郁香型白酒的特征菌属。
3 结论
本研究通过评估馥郁香型白酒对小鼠脂代谢和肠道菌群的影响,发现适量饮用馥郁香型白酒能够有效控制因高脂饲料引起的小鼠肝脏、附睾脂肪和肾周脂肪系数及其相关脂质的积累,提高肝脏内SOD活力,改善高脂饮食带来的血脂中TG、LDL-C和HDL-C含量的升高,一定程度缓解因高脂饮食导致的肠道菌群多样性失衡。在属水平上,饮酒伴随高脂饮食缓解了高脂饮食引起的脱硫弧菌属相对含量的上升和罗斯氏菌属相对含量的下降,显著增加了瘤胃球菌属相对含量。结果表明,适量饮用馥郁香型白酒对高脂饮食造成的小鼠脂代谢异常和肠道菌群的失衡有一定的缓解作用。
[1]鲁达.适量饮酒有益健康[J].中国酒,2020(Z1):5.
[2]BAJAJ J S.Alcohol,liver disease and the gut microbiota[J].Nat Rev Gastro Hepat,2019,16:235-246.
[3]罗强,刘杰,刘志刚.酱香型白酒中吡嗪类物质体外抗炎作用研究[J].中国酿造,2019,38(7):156-160.
[4] SABIA S,FAYOSSE A,DUMURGIER J,et al.Alcohol consumption and riskofdementia:23yearfollow-upofWhitehallIIcohortstudy[J].BMJ,2018,362:k2927.
[5]罗强,刘杰,刘志刚.酱香型白酒中活性成分的抗氧化活性[J].食品与发酵工业,2019,45(23):84-89.
[6]彭买娇,惠华英,肖嫩群,等.芦笋对高脂饮食小鼠肠道内容物细菌多样性的影响[J].核农学报,2019,33(11):2229-2236.
[7]王勤,杨亦彬.肠道菌群失调对糖尿病及糖尿病肾病影响的研究进展[J].医学综述,2019,25(3):530-534.
[8]杨凤啸,卢敏惠.高脂饮食诱发小鼠肥胖及其对肠道菌群结构影响的研究[J].现代医院,2017,17(6):863-866.
[9]毛华,杜峰,刘廷筑,等.大鼠糖、脂代谢与白酒关系的研究[J].贵州医药,2010,34(11):968-970.
[10]汪家文,刘应时,于晓军,等.不同浓度白酒对大鼠血脂的影响及与脑血管病的关系[J].佛山科学技术学院学报(自然科学版),2011,29(4):27-30.
[11]李钰,张欢,饶家权,等.适量白酒对动脉粥样硬化大鼠血脂及炎性因子的影响[J].现代预防医学,2017,44(13):2347-2350.
[12]方程.基于组学的白酒肝损伤和肠道菌群干预调节机制研究[D].无锡:江南大学,2019.
[13]鲁蕾,陈蕊,范雪佳,等.长期过量饮用不同品质浓香型白酒对大鼠肠道正常菌群影响的研究[J].现代预防医学,2014,41(7):1286-1289.
[14]汪诗欣,开朗,杨静怡,等.浓香型白酒中短链脂肪酸及其乙酯对人体的影响[J].食品与发酵工业,2020,46(16):257-263.
[15]蒋丰岭,周玮忻,伍梓汐,等.黄酒对小鼠肝脏功能及肠道菌群的影响[J].中国酿造,2020,39(7):41-45.
[16]卢冠军,杨安宁,蔡欣,等.Hcy 对动脉粥样硬化小鼠肝脏脂质代谢的影响[J].重庆医学,2014,43(30):4030-4033.
[17]CHEN S,ZHOU Y,CHEN Y,et al.Fastp:an ultra-fast all-in-one FASTQ preprocessor[J].Bioinformatics,2018,34(17):i884-i890.
[18]MAGOC T,SALZBERG S L.FLASH:fast length adjustment of short reads to improve genome assemblies[J].Bioinformatics,2011,27(21):2957-2963.
[19] EDGAR R C.UPARSE:highly accurate OTU sequences from microbial amplicon reads[J].Nat Method,2013,10(10):996-998.
[20]STACKEBRANDT E,GOEBEL B M.Taxonomic note:A place for DNADNA reassociation and 16S rRNA sequence analysis in the present species definition in bacteriology[J].Int J Syst Bacteriol,1994,44(4):846-849.
[21]WANG Q,GARRITY G M,TIEDJE J M,et al.Naive Bayesian classifier for rapid assignment of rRNA sequences into the new bacterial taxonomy[J].Appl Environ Microb,2007,73(16):5261-5267.
[22]袁带秀,申绪湘,覃大保,等.不同浓度白酒对大鼠抗氧化酶活性的影响[J].酿酒科技,2013(10):42-43.
[23]徐岩,范文来,葛向阳,等.科学认识中国白酒中的生物活性成分[J].酿酒科技,2013(9):1-6.
[24]魏梦娇,姚高毅,郭琳.饮用酒和食用酒精暴露诱导小鼠肝脏组织的损伤效应[J].酿酒科技,2020(6):37-41,45.
[25]林琳,田利明,孙振学.健康教育和干预在血脂异常治疗中的实施[J].武警医学院学报,2008,72(9):792-793.
[26]丁书文,魏陵博,戎冬梅.592 例心脑血栓患者饮酒量对血脂、血糖、血压的影响[J].山东中医药大学学报,2004(4):269-271.
[27]康金森,王雪飞,冉新建,等.新疆穆塞勒斯酒对实验性高脂血症大鼠血脂的影响[J].亚太传统医药,2013,9(8):20-21.
[28]类春燕,沈才洪,卢中明,等.低氘白酒对实验性高脂血症大鼠凝血及纤溶系统的影响[J].中国动脉硬化杂志,2011,19(10):819-824.
[29]SCHLOSS P D,WESTCOTT S L,RYABIN T,et al.Introducing mothur:open-source,platform-independent,community-supported software for describing and comparing microbial communities[J].Appl Environ Microb,2009,75(23):7537-7541.
[30]高洁,孙静,黄建,等.开菲尔对高脂金黄地鼠肠道菌群的调节作用研究[J].中国酿造,2017,36(4):15-19.
[31]TURNBAUGH P J,LEY R E,MAHOWALD M A,et al.An obesity-associated gut microbiome with increased capacity for energy harvest[J].Nature,2006,444(7122):1027-1031.
[32] FUGMANN M,BREIER M,ROTTENKOLBER M,et al.The stool microbiota of insulin resistant women with recent gestational diabetes,a high risk group for type 2 diabetes[J].Sci Rep,2015,5(1):1-8.
[33]WEGLARZ L,DZIERZEWICZ Z,SKOP B,et al. Desulfovibrio desulfuricans lipopolysaccharides induce endothelial cell IL-6 and IL-8 secretion and E-selectin and VCAM-1 expression[J]. Cell Mol Biol Lett,2003,8(4):991-1003.
[34] KASAHARA K,KRAUTKRAMER K A,ORG E,et al.Interactions between Roseburia intestinalis and diet modulate atherogenesis in a murine model[J].Nat Microbiol,2018,3:1461-1471.
[35]SHANG Q,SHAN X,CAI C,et al.Dietary fucoidan modulates the gut microbiota in mice by increasing the abundance of Lactobacillus and Ruminococcaceae[J].Food Funct,2016,7(7):3224-3232.
[36]CHIUMENTO S,ROBLIN C,KIEFFER-JAQUINOD S,et al.RuminococcinC,a promising antibiotic produced by a human gut symbiont[J].Sci Adv,2019,5(9):eaaw9969.