糙米是稻谷脱壳后不加工而获得的全谷米粒,与精米相比,其蛋白质、脂肪、总膳食纤维含量高,其中膳食纤维是精米的6倍多,主要存在于糙米表皮层中,糙米也因含有较高的膳食纤维,蒸煮食用起来口感差,发芽处理后,糙米会有显著变化[1-2]。吴晓娟等[3]研究发现,糙米发芽后淀粉显著下降,纤维素和γ-氨基丁酸显著提高;袁周率等[4]通过酵母发酵糙米浆制备酵素,发现维生素B1、维生素B2和γ-氨基丁酸显著提升;陈海旭[5]采用筛选的6株益生菌发酵糙米浆,制备的发酵饮料具有浓郁发酵香味,酸度适中、风味独特,乳酸含量为45 nmol/L;赵志浩等[6]先将粉碎的糙米通过高温α-淀粉酶酶解0.5 h,而后采用边搅拌边喷淋的方式调节水分为22%,挤压膨化,制备预酶解-挤压膨化糙米粉,提高了水溶性和消化率。糙米中的多酚主要是阿魏酸和香豆酸,TIAN S等[7]研究发现,糙米发芽后游离阿魏酸、香豆酸显著增大;OHTSUBO K等[8]研究了糙米发芽72 h后阿魏酸含量从34 mg/100 g增至43 mg/100 g;JIRAPORN B等[9]研究发现,三种糙米发芽48 h总酚分别提高1.12、1.37和1.43倍;MOONGNGARM A等[10]研究发现,稻米发芽4 d后,总酚由62 mg/100 g增至102 mg/100 g。
液态发酵食醋具有原料利用率高、生产周期短、自动化程度高、色泽浅、产品质量稳定等优点,但因其原料单一,纯菌种发酵,发酵周期短,食醋总酸含量高,不挥发酸、氨基酸、可溶性无盐固形物含量低,酸味刺激性强,适合浅色食品调味。谭海刚等[11]针对液态食醋颜色浅,沉淀对其影响更明显的难题,通过分析沉淀组分,采用酸性蛋白酶和糖化酶处理可明显减少沉淀量,提高其稳定性,米醋透光率增加39.08%;邓永建等[12]通过添加麸皮培养的不同乳酸菌发酵液,与醋酸菌混合发酵制备液态米醋,检测出乳酸、琥珀酸、酒石酸、柠檬酸4种不挥发性酸,检测81种挥发性成分,降低了刺激性酸味,增强了米醋香气;蒋忠等[13]采用乳酸菌和酵母菌共酵,使液态米醋不挥发性酸和酯类含量分别提升了10.25倍和1.62倍;胡凯弟等[14]研究了以筛选的优良巴氏醋杆菌为菌种优化发酵条件制备了液态麸醋,其口感柔和、香味独特,游离氨基酸含量为805.29 mg/100 mL,各项指标优于其他液态发酵食醋。
芽孢杆菌是食醋发酵过程中的核心菌群,可代谢蛋白酶、脂肪酶、淀粉酶和纤维素酶,对食醋风味和香气有重要的贡献[15-16]。王宗敏等[17]从镇江香醋醋醅中筛选一株环状芽孢杆菌,其可耐6%vol的乙醇,在pH>4时菌体生长正常,并能促进有机酸、氨基酸和挥发性成分的产生;刘军等[18]从四川晒醋醋醅中筛选一株产纤维酶的苏云金芽孢杆菌,纤维素酶活为161.33 U/g;原海兵等[19]将麸醋醋醅中分离的芽孢杆菌进行优化培养,提高了以豆粕、麸皮为主要成分的培养基的总酚含量为229.8 μg/mL。
阿魏酸(ferulic acid,FA)是一种酚酸,常存在于植物细胞壁中,具有清除自由基、抗氧化、抗血栓、降血脂、防治冠心病、抑菌消炎、预防癌症和抗突变等多种作用[20-21]。FAULDS C等[22]选用木聚糖酶和阿魏酸酯酶协同酶解小麦麸皮,发现可以有效打破细胞壁多糖结构,显著提高阿魏酸的提取效率。前期试验在纳豆的发酵过程中发现纳豆菌还具有代谢产生阿魏酸的酶系,因此将其用于糙米醋中,研究其对液态发酵糙米醋的影响,以期提升糙米醋品质,为工业化生产提供理论基础。
1 材料与方法
1.1 材料与试剂
糙米:湖北凤池实业有限公司;乙酸(食品级)、耐高温α-淀粉酶(4 000 U/g)、糖化酶(10万U/g):上海源叶生物科技有限公司。
酵母膏、葡萄糖、氯化钠、蛋白胨、无水乙醇、乙酸乙酯、氢氧化钠、乙酸(均为分析纯):国药集团化学试剂有限公司。
纳豆菌(Bacillusnatto)WBUSPN01:本试验室保藏菌种。
液体培养基:10 g/L蛋白胨、5 g/L酵母膏、10 g/L NaCl。121 ℃灭菌15 min。
1.2 仪器与设备
MSF-S-50L自动型机械搅拌罐:南京汇科生物工程设备有限公司;LHS-250SC型智能型恒温恒湿箱:上海浦东荣丰科学仪器有限公司;大型SLY-2112B型立式双层大容量恒温培养摇床:金坛市盛蓝仪器制造有限公司;YM系列A型立式压力蒸汽灭菌器:上海三申医疗器械有限公司;PC-420磁力恒温搅拌器:美国Corning公司;QDWZⅠ3000-7D湿法粉碎机:无锡轻大食品有限公司;SW-CJ-2D净化工作台:广州瑞智科学仪器有限公司。
1.3 方法
1.3.1 糙米醋工艺流程及操作要点
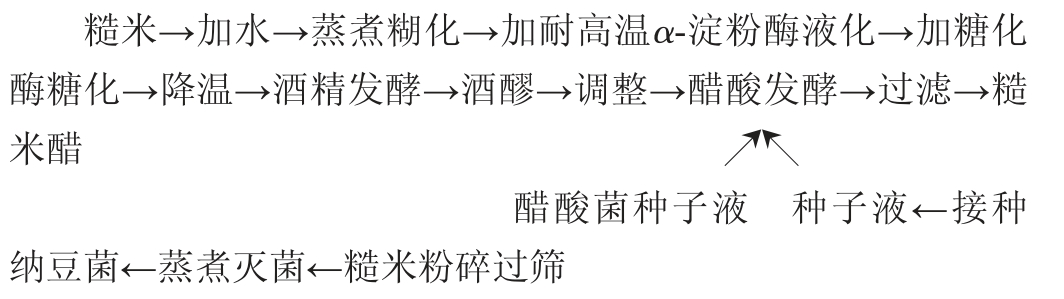
操作要点:
取1 kg糙米,加4 kg水,常压蒸煮25 min,90~95 ℃保温,加入0.5 g耐高温α-淀粉酶保温15 min后降温至65 ℃,加入2.0 g糖化酶,62~65 ℃保温4 h,制备米酒醪。将制备米酒醪通过添加无菌水调整至一定酒精度,而后通过添加乙酸调整至一定总酸。
糙米粉碎至通过100目筛,按质量比1∶9添加水,搅拌均匀,121 ℃灭菌20 min,接种纳豆菌,120 r/min、35 ℃摇床培养28 h,制备纳豆菌种子液。
调整后的米酒醪,摇匀,取100 mL置于三角瓶中,控温,接种醋酸菌种子液9.0%(V/V)和纳豆菌种子液,在转速100 r/min、一定温度条件下发酵至总酸不再升高,过滤,得到糙米醋。
1.3.2 糙米醋醋酸发酵工艺单因素试验
纳豆菌接种量对醋酸发酵的影响:纳豆菌接种量分别设置为0、0.5%、1.0%、1.5%、2.0%、2.5%、3.0%、3.5%,初始乙酸含量0.8%、初始酒精度6.0%vol、发酵温度32 ℃,取醋酸发酵结束时醋汁,测定醋汁阿魏酸和总酸含量,试验做3组平行。
初始乙酸含量对醋酸发酵的影响:初始乙酸含量分别设置为0、0.2%、0.4%、0.6%、0.8%、1.0%、1.2%、1.4%,纳豆菌接种量1.0%、初始酒精度6.0%vol、发酵温度32 ℃,取醋酸发酵结束时醋汁,测定醋汁阿魏酸和总酸含量,试验做3组平行。
初始酒精度对醋酸发酵的影响:初始酒精度分别设置为5.0%vol、5.5%vol、6.0%vol、6.5%vol、7.0%vol、7.5%vol、8.0%vol,纳豆菌接种量1.0%、初始乙酸含量0.8%、发酵温度32 ℃,取醋酸发酵结束时醋汁,测定醋汁阿魏酸和总酸含量,试验做3组平行。
发酵温度对醋酸发酵的影响:发酵温度分别设置为28 ℃、30 ℃、32 ℃、34 ℃、36 ℃、38 ℃,纳豆菌接种量1.0%、初始乙酸含量0.8%、初始酒精度6.0%vol,取醋酸发酵结束时醋汁,测定醋汁阿魏酸和总酸含量,试验做3组平行。
1.3.3 糙米醋醋酸发酵工艺条件优化正交试验设计
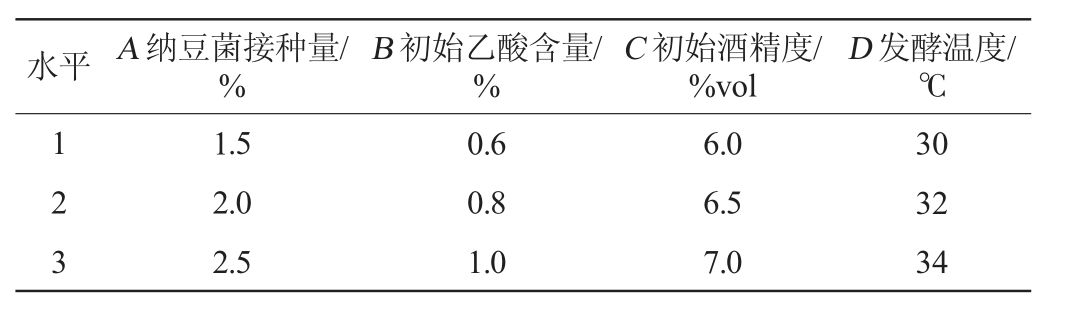
为了研究纳豆菌接种量、初始乙酸含量、初始酒精度、发酵温度对糙米醋品质的影响,在单因素试验的基础上,用L9(34)正交试验设计试验,以阿魏酸和总酸含量为评价指标确定最优条件,正交试验因素与水平见表1。
表1 糙米醋醋酸发酵工艺条件优化正交试验因素与水平
Table1 Factors and levels of orthogonal experiments for acetic acid fermentation process optimization of brown rice vinegar
1.3.4 测定方法
阿魏酸的测定:参照文献[23]中阿魏酸的测定方法,并做适当优化。取醋汁,过滤后,5 000 r/min离心,取上清液10 mL,加入6 mL乙酸乙酯萃取,重复3次,取乙酸乙酯层,合并萃取液,旋转蒸干,得到阿魏酸粗品。用4 mL无水乙醇溶解,于波长286 nm处测定其吸光度值,样品做3个平行试验。
总酸、不挥发酸、氨基酸态氮、可溶性无盐固形物的测定:参考GB 18187—2000《酿造食醋》中规定的方法测定。
2 结果与分析
2.1 糙米醋醋酸发酵工艺优化单因素试验结果与分析
2.1.1 纳豆菌接种量对醋酸发酵的影响
相对于传统固态食醋,液态发酵食醋因其良好的物质和能量交换性能,微生物增殖和代谢更为快捷、原料转化率更高,也因此多菌种发酵时更易相互影响。在传统固态食醋醋酸发酵过程中为醋酸菌、乳酸菌、芽孢杆菌等多种微生物共存,在液态食醋中也能协同发酵。由图1可知,随着纳豆菌接种量的增大,阿魏酸含量显著增大,接种量为2.0%时,阿魏酸含量可达8.46 mg/L,而后稳定。接种纳豆菌对醋汁总酸有一定的影响,当接种量>2.5%之后,总酸开始显著下降,可能是纳豆菌接种量大消耗了过多的碳源,或竞争性抑制醋酸菌的增殖和代谢。因此,选择纳豆菌接种量为2.0%较适宜。
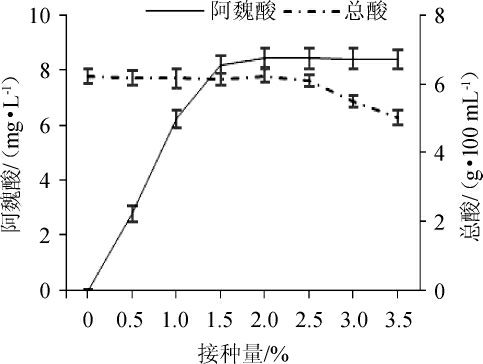
图1 纳豆菌接种量对糙米醋阿魏酸和总酸含量的影响
Fig.1 Effect of Bacillus natto inoculum on ferulic acid and total acid contents of brown rice vinegar
2.1.2 初始乙酸含量对醋酸发酵的影响
前期试验表明,液态食醋发酵起始时,如果乙酸含量为0或很低,尽管初始乙醇充足,总酸仅能达到3.0 g/100 mL,这与KRUSONG W等[24-25]的研究一致,因此糙米醋醋酸发酵起始,须添加一定量乙酸,但乙酸的添加可能会对纳豆菌有抑制作用。
从图2可以看出,随着初始乙酸含量的增大,阿魏酸从6.3 mg/L开始有缓慢减小的趋势,当初始乙酸含量>1.0%时,阿魏酸开始显著减小;而醋汁总酸在初始乙酸含量<0.6%时维持在3.0 g/100 mL,而后显著增大至6.26 g/100 mL,而后又开始减小,醋酸发酵起始阶段添加低浓度的醋酸可以诱导乙醇脱氢酶和乙醛脱氢酶的表达,提高菌体发酵效率及醋酸耐受性。初始乙酸含量过高可能会抑制纳豆菌增殖与代谢,进而影响阿魏酸代谢生成。因此,初始乙酸含量为1.0%时较合适。
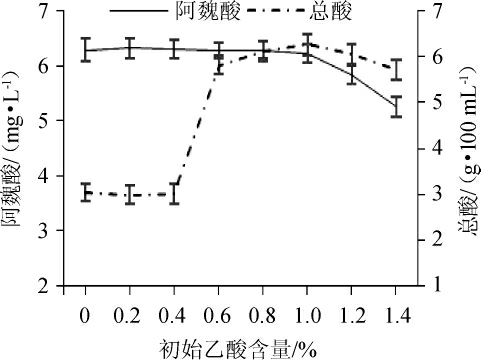
图2 初始乙酸含量对糙米醋阿魏酸和总酸含量的影响
Fig.2 Effect of initial acetic acid contents on ferulic acid and total acid contents of brown rice vinegar
2.1.3 初始酒精度对醋酸发酵的影响
醋酸发酵起始时,酒精度过高会抑制醋酸菌增殖与代谢,甚至导致总酸不会升高[26],同样也会抑制纳豆菌。
由图3可知,初始酒精度由5.0%vol增大至7.0%vol,醋汁中阿魏酸稳定在6.2 mg/L,初始酒精度>7.5%vol时阿魏酸含量显著下降,而总酸随着初始酒精度增至7.0%vol时提升至7.03 g/100 mL,高于7.5%vol时的0.8 g/100 mL,说明醋酸菌增殖受抑制,代谢终止,可能过高的乙醇浓度导致菌体细胞破裂。因此,初始酒精度应为7.0%vol。
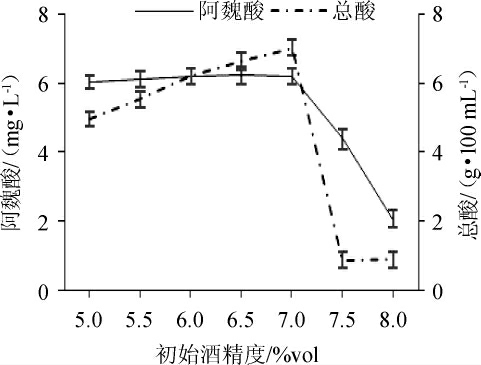
图3 初始酒精度对糙米醋阿魏酸和总酸含量的影响
Fig.3 Effect of initial alcohol contents on ferulic acid and total acid contents of brown rice vinegar
2.1.4 发酵温度对醋酸发酵的影响
醋酸菌和纳豆菌均为温度适宜范围广的微生物,适宜的温度会促进其增殖与代谢活动,进而提高原料利用率。液态食醋醋酸发酵的最佳温度为30 ℃,而纳豆菌发酵纳豆的最佳温度为37 ℃,当两种菌混合发酵时可能会相互影响,从图4可知,阿魏酸与总酸变化趋势一致,先增大后减小,阿魏酸和总酸在发酵温度为32 ℃时分别高达6.24 mg/L和6.25 g/100 mL,但在32~34 ℃时二者含量差异不显著。因此,醋酸发酵温度为32 ℃较适宜。
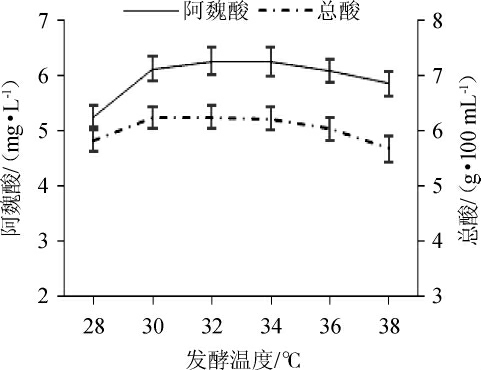
图4 发酵温度对糙米醋阿魏酸和总酸含量的影响
Fig.4 Effect of fermentation temperature on ferulic acid and total acid contents of brown rice vinegar
2.2 糙米醋醋酸发酵工艺条件优化正交试验结果与分析
选取纳豆菌接种量、初始乙酸含量、初始酒精度和发酵温度4个因素进行正交试验设计,正交试验结果见表2,方差分析见表3。
由表2的正交试验结果与分析可知,影响糙米醋汁阿魏酸含量的主次因素为:纳豆菌接种量>初始乙酸含量>发酵温度>初始酒精度,其最佳条件为A3B1C2D2;影响其总酸含量的主次因素为:初始乙酸含量>初始酒精度>纳豆菌接种量>发酵温度,其最佳条件为A2B3C3D2。由表3的方差分析可知,纳豆菌接种量对阿魏酸含量有极显著的影响(P<0.01),初始乙酸含量、发酵温度对其有显著的影响(P<0.05),初始酒精度影响不显著(P>0.05);初始乙酸含量对总酸含量有极显著的影响(P<0.01),而初始酒精度、纳豆菌接种量对其有显著的影响(P<0.05),发酵温度影响不显著(P>0.05)。对于多个考核指标采用综合平衡法确定优方案,虽然纳豆菌接种量对阿魏酸含量影响非常显著,但是接种量2.0%和2.5%时阿魏酸含量差异小,因此从节约资源的角度选A2;初始乙酸含量对总酸含量影响非常显著,因此选B3,同理选C3,最后得出优方案为A2B3C3D2。将优方案与试验组A2B2C3D1进行验证,结果表明,二者醋汁阿魏酸含量分别为6.22mg/L和6.54mg/L,总酸含量分别为7.11g/100mL和7.29 g/100 mL,验证试验证明优方案效果更好,即纳豆菌接种量2.0%、初始乙酸含量1.0%、初始酒精度7.0%vol、发酵温度32 ℃。
表2 糙米醋醋酸发酵工艺条件优化正交试验设计结果与分析
Table2 Results and analysis of orthogonal experiments design for acetic acid fermentation process optimization of brown rice vinegar
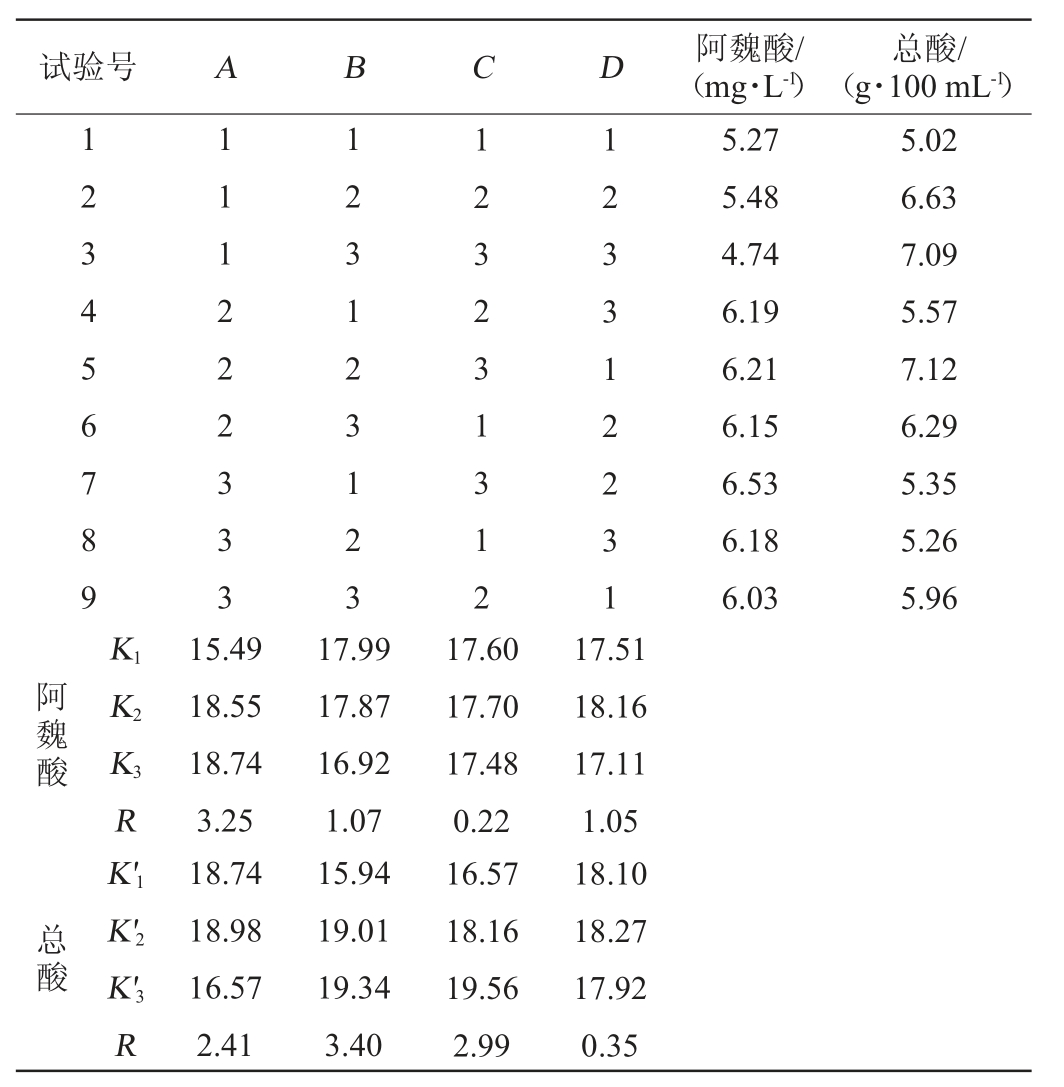
表3 正交试验结果方差分析
Table3 Variance analysis of orthogonal experiment results
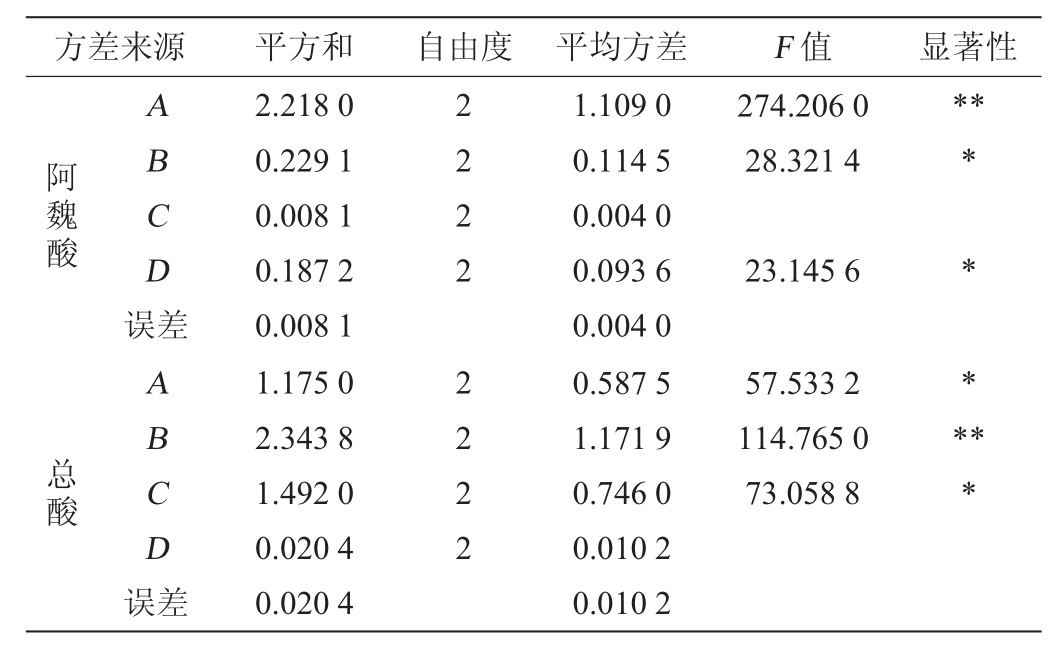
注:“**”表示影响极显著(P<0.01);“*”表示影响显著(P<0.05)。
2.3 糙米醋质量评价
以糙米为原料,采用优化的液态发酵工艺酿造糙米醋,醋酸发酵调整初始乙酸含量为1.0%、初始酒精度为7.0%vol,醋酸菌接种量9.0%、纳豆菌接种量2.0%、发酵温度32 ℃,发酵结束、过滤,酿造糙米醋。糙米醋,暗黄色、澄清、酸味柔和,总酸为7.26g/100 mL、阿魏酸含量为6.57 mg/L,试验制备的糙米醋与不添加纳豆菌酿造的糙米醋相比,理化指标见表4,总酸差异不显著,氨基酸态氮、不挥发酸和可溶性无盐固形物的含量分别是对照组的4.18倍、2.95倍和2倍,新增了阿魏酸成分。接种纳豆菌,与醋酸菌混合发酵,提高了以糙米为原料的液态醋整体品质,特别是新增了功效成分阿魏酸,提升了糙米醋的功能性。
表4 糙米醋与不添加纳豆菌酿造的糙米醋理化指标对比
Table4 Comparison of physical and chemical indexes between brown rice vinegar and brown rice vinegar brewed without Bacillus natto

3 结论
通过单因素和正交试验设计优化,得到醋酸发酵适宜工艺条件为:纳豆菌接种量2.0%、初始乙酸含量1.0%、初始酒精度7.0%、发酵温度32 ℃。按照优化后的工艺条件制备的糙米醋,暗黄色、澄清、酸味柔和,总酸高达7.26 g/100 mL、阿魏酸为6.57 mg/L,试验制备的糙米醋与不添加纳豆菌酿造的糙米醋相比,氨基酸态氮、不挥发酸和可溶性无盐固形物的含量分别提高了4.18倍、2.95倍和2倍。可知,纳豆菌代谢产生的蛋白酶、脂肪酶、纤维素酶、淀粉酶等多种酶系,酶解了糙米营养成分,与醋酸菌混合发酵,提高了糙米醋整体品质,特别是新增了功效物质阿魏酸,提升了糙米醋的功能性。
[1]VELUPPILLAI S,NITHYANANTHARAJAH K,VASANTHARUBA S,et al.Biochemical changes associated with germinating rice grains and germination improvement[J].Rice Sci,2009,16(3):240-242.
[2]MOONGNGARM A,SAETUNG N.Comparison of chemical compositions and bioactive compounds of germinated rough rice and brown rice[J].Food Chem,2010,122(3):782-788.
[3]吴晓娟,从竞远,吴伟,等.糙米发芽前后营养成分的变化及其对发芽糙米糊化特性的影响[J].食品科学,2017,38(18):67-72.
[4]袁周率,苏小军,廖晰晰,等.糙米酵素的营养价值及发酵前后营养成分的变化[J].粮食与饲料工业,2015,29(4):35-38.
[5]陈海旭.益生菌发酵糙米饮料的制作工艺及应用价值研究[D].呼和浩特:内蒙古农业大学,2014.
[6]赵志浩,刘磊,张名位,等.预酶解-挤压膨化对全谷物糙米粉品质特性的影响[J].食品科学,2019,40(1):108-116.
[7] TIAN S,NAKAMURA K,KAYAHARA H.Analysis of phenolic compounds in white rice,brown rice and germinated brown rice[J].J Agric Food Chem,2004,52(15):4808-4813.
[8] OHTSUBO K,SUZUKI K,YASUI Y,et al.Bio-functional components in the processed pre-germinated brown rice by a twin-screw extruder[J].J Food Compos Anal,2005,18(2):303-316.
[9] JIRAPORN B,PAIBOON T,BUNCHA O,et al.Increasing the bio-active compounds contents by optimizing the germination conditions of southern Thai brown rice[J].Sonkanakarin J Sci Technol,2010,32(3):219-230.
[10] MOONGNGARM A,KHOMPHIPHATKUL E.Germination time dependence of bioactive compounds and antioxidant activity in germinated rough rice(Oryza sativa L.)[J].Am J App Sci,2011,8(1):14-15.
[11]谭海刚,李静,申美容.液态发酵米醋稳定性研究[J].中国调味品,2020,45(2):32-35.
[12]邓永建,陆震鸣,张晓娟,等.不同乳酸菌对液态发酵米醋总酸及风味物质的影响[J].食品科学,2020,41(22):97-102.
[13]蒋忠,冯文利,王伟,等.乳酸菌与酵母菌共酵改善食醋品质的研究[J].中国酿造,2015,34(9):104-108.
[14]胡凯弟,赵爽,彭杨,等.液态发酵麸醋工艺优化及其风味品质研究[J].食品与生物技术学报,2017,36(8):869-876.
[15]刘凯凤,杨丽,郑胜蓝,等.山西老陈醋中优势产酸菌的分离纯化及功能分析[J].食品工业科技,2020,41(6):124-130.
[16]邝格灵,张洁,孔德华,等.植物乳杆菌与解淀粉芽孢杆菌对食醋风味的影响[J].中国酿造,2018,37(6):25-29.
[17]王宗敏,陆震鸣,朱青,等.镇江香醋醋醅微生物Bacillus circulans 发酵特性的初步研究[J].中国调味品,2016,41(9):24-28.
[18]刘军,江若宇,王麒麟,等.四川晒醋醋醅中一株产纤维素酶的芽孢杆菌分离筛选[J].食品与发酵工业,2018,44(6):140-144.
[19]原海兵,刘军,韩志双,等.一株分离至传统麸醋醋醅的芽孢杆菌发酵培养基的优化研究[J].中国调味品,2014,39(5):1-5.
[20]KIM H,OH E,MUM J,et al.Oxidative damages in the DNA,lipids,and proteins of rats exposed to isofluranes and alcohols[J]. Toxicology,2006,220(2):169-178.
[21]ITAGAKI S,KUROKAWA T,NAKATA C,et al.In vitro and in vivo antioxidant properties of ferulic acid:A comparative study with other natural oxidation inhibitors[J].Food Chem,2009,114(25):4661-471.
[22] FAULDS C,WILLIAMSON G.Release of ferulic from wheat bran by a ferulic acid esterase(FEA-Ⅲ) from Aspergillus niger[J].Appl Microbiol Biotechnol,1995,43:1082-1087.
[23]何粉霞.小麦麸皮中阿魏酸的提取、结构修饰及生物活性的研究[D].郑州:河南工业大学,2011.
[24]KRUSONG W,YAIYEN S,PORNPUKDEEWATANA S.Impact of high initial concentrations of acetic acid and ethanol on acetification rate in an internal Venturi injector bioreactor[J]. J Appl Microbiol,2015,118(3):629-640.
[25]郑宇,姜春悦,陈兴京,等.醋酸对巴氏醋杆菌生长和代谢活性的影响[J].现代食品科技,2014,30(9):149-153.
[26]戴明辉.液态深层发酵制醋新工艺的探索[J].中国酿造,2005,24(10):8-11.