黄酒是我国传统的发酵酒精饮料[1-2],酒精含量(4%vol~20%vol)较低,其富含营养物质,具有独特风味,被誉为“液体蛋糕”[3-4]。我国黄酒的种类丰富,产品以江浙沪为中心,遍布全国[4-5]。各地黄酒以糯米、黍米、玉米、黑米等富含淀粉的谷物作为主要原料,以酒母、麦曲和酒药等作为糖化发酵剂酿造而成[6],酿造过程包括浸米、蒸饭、摊冷、落缸、发酵、压榨、煎酒和贮存等诸多环节[7]。黄酒的酿造过程中,主要源于糖化发酵剂的酿酒微生物产生各种复杂的分解酶系,通过一系列的生物化学反应过程将原料中淀粉等大分子物质降解和转化为乙醇和糖类、酯类、有机酸类、氨基酸类及其各种醇类物质等。黄酒酿造过程与其他传统酿造食品一样都属于开放式发酵,环境中的微生物也参与发酵过程,与主要酿造微生物共同影响黄酒风味物质的形成[8-9]。因此,研究黄酒中的微生物多样性对控制黄酒酿造工艺、提升黄酒品质具有重要意义。
黄酒中微生物群落结构的研究最早采用传统的培养分离方法,基于菌株的生理生化特性与某种基因序列对酿酒微生物进行分类和鉴定,研究结果具有一定的局限性,LV X C等[10]对红曲酒中酵母菌的研究结果表明,传统微生物学方法不能检测到所有的酵母菌株。随着现代生物技术的发展,逐渐建立起来的变性凝胶梯度电泳(denatured gradient gel electrophoresis,DGGE)技术[11-12]、聚合酶链式反应-变性梯度凝胶电泳(polymerase chain reaction-denaturing gradient gel electrophoresis,PCR-DGGE)[13]等分子生物学方法,使人们更深入了解参与黄酒酿造过程中的微生物种类,这对黄酒酿造微生物研究发挥了积极作用,但是在分析微生物群落结构组成时,以上技术也表现出准确率低、实验条件要求高等缺点。目前,广泛使用的第二代测序技术(second generation sequencing,SGS),又称下一代测序技术(next generation sequencing,NGS)或深度测序(deep sequencing,DS)[14-15],及第三代测序技术(third generation sequencing,TGS)能够克服上述分子生物学技术的缺点,因其具有测序时间短、高通量、成本低、定量准等优点,日益发展成熟,广泛运用于黄酒酿造微生物的研究[16-19]。本文综述了高通量测序技术的发展阶段,详细介绍了该技术的原理、方法、操作流程及数据分析方法,以及高通量测序技术在黄酒微生物多样性的研究中的应用,并对黄酒微生物多样性的研究方向进行了展望,为全面认识黄酒微生物多样性及相关机理,进一步深入开展黄酒微生物的深入研究提供参考依据。
1 高通量测序技术简介
1.1 高通量测序技术的发展阶段
早在20世纪70年代,美国生物化学家SANGER F发明的双脱氧法测序技术(Sanger测序)是第一代测序技术,在脱氧核糖核酸(deoxyribonucleic acid,DNA)聚合酶合成DNA链的过程中加入双脱氧核苷三磷酸(dideoxyribonucleoside triphosphate,ddNTP),得到一系列不同长短的DNA片段[20],这成为当时DNA测序的主流技术。但是,Sanger测序法存在速度较慢、通量较低、成本较高等不足,已经不能满足大规模测序所需的测序深度和测序效率等的要求[21]。
以高通量为特点的第二代测序技术是测序技术发展历程的一个重要里程碑,可以在短时间内产生数以千计甚至百万计的序列,这些序列有助于识别样本中难以培养或不可培养的微生物,可以直接对微生物类群进行全貌的分析,为研究各种微生物和发现一些稀有甚至未知的物种提供了新的研究手段[18,22],目前,下一代测序技术主要包括罗氏(Roche)公司的454焦磷酸测序平台,Illumina公司的Solexa测序技术、ABI公司的SOLiD测序技术和Life Techologies公司的Ion Torrent测序技术。
大部分第二代测序技术也存在局限性,如无法准确全面的测序、依赖于PCR扩增、测序读长较短及其易变异等,无法实现全基因组覆盖。为了更加准确与高效解读DNA序列信息,第三代测序技术已经建立,目前有HelicosBiosciences公司的真单分子测序(true single-molecule sequencing,tSMS)技术、Pacfic Biosciences公司的单分子实时(single molecule real-time,SMRT)测序技术、Oxford Nanopore公司的纳米孔单分子测序技术(Oxford nanopore technologies,ONT)以及VisiGen Biotechnologies公司研发的荧光共振能量转移(fluorescence resonance energy transfer,FRET)测序技术。
1.2 高通量测序技术原理及特点
(1)第二代测序技术
由于传统的测序技术已经不能完全满足各种生境内微生物多样性研究的需要,第二代测序技术应运而生,由于具有测序结果的通量高、可定量、平行测序等优点而被广泛运用于各领域研究中。2005年,罗氏公司(Roche)公司首先推出划时代的新型高通量454焦磷酸测序技术,该技术采用焦磷酸合成测序法[23],利用乳胶系统对DNA分子进行扩增,实现了大规模测序,测序特点为速度快、通量高以及读长长等,可避免传统测序需要进行的荧光标记以及跑胶等繁琐步骤,但在2013年停止了454测序仪的使用。
随后Illumina公司推出Solexa测序技术[21,24],其原理为基于高密度的单分子阵列序列分析,核心技术为聚合酶链式反应(polymerase chain reaction,PCR)和可逆性终止化学反应,实现了边合成边测序。Solexa测序的步骤是:第一步将基因组DNA处理成100~200 bp片段,在两端接上特定的DNA接头后进行扩增,获得单链DNA文库;第二步将带接头的待测DNA片段加入芯片上与其表面的碱基产生互补杂交连接到芯片表面,这些小段的DNA分子经过延伸和桥式扩增后,在flow cell上形成了具有数以亿计单分子簇(Clusters),第三步加入带荧光标记的脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTP)进行边合成边测序,由于这些dNTP的3'末端被一个叠氮基堵住,所以每次反应只能添加一个dNTP,最后记录荧光信号并进一步分析转化为测序碱基信息。现在Illumina公司主要测序平台有Hiseq、MiSeq、NovaSeq 6000等,其优势主要在于测序数据精准度最高可达99.9%,确保了高精确度和真实的单碱基连续测序,而且与其他二代测序平台相比,测序成本也较低和运用领域多,但是序列读长较短。
在以上两种测序技术的基础上,ABI公司在2007年推出基于酶连接法的新一代高通量SOLiD测序技术[25-26],基本测序步骤是:第一步是获得目标DNA小片段,两端加上接头,构建DNA文库;第二步是乳液聚合酶链式反应(PCR)/微珠富集,与454焦磷酸测序类似,但是测序微珠只有1 μm;第三步为加入连接酶进行测序;第四步是数据分析,得到SOLiD原始序列。创新之处在于应用双碱基编码的方式获取DNA序列信息,将每个碱基阅读两次,大大降低了测序带来的错误率,提供了内在的校正功能。
2010年,Life Techologies公司利用半导体芯片技术成功设计出基于Ion Torrent的测序技术[27],基于半导体的微pH计实现了快速地高通量测序。在这项测序技术中,DNA聚合酶以单链DNA为模板,按顺序加入4种非修饰核苷酸中的一个,依据碱基互补配对原则合成互补DNA链,DNA链每延伸一个碱基,就会释放一个质子(H+)而导致pH值改变,通过传感器检测,将化学信号转变为数学信号,最终获得DNA序列信息。基本步骤:首先构建基因文库,在样品DNA两端加上标准接头;然后进行油包水PCR,也叫乳浊液PCR,把文库种到测序珠子上去并进行扩增;最后将上一步洗脱下来的珠子上机测序,通过测量并记录pH值变化而测出DNA序列。该测序平台的主要优势,就是可以从很少量的起始DNA进行测序,测序速度快。
(2)第三代测序技术
第三代测序是以单分子测序技术为基础,不依赖于PCR扩增,具有超长读长和运行快等特点,主要用于突变鉴定(single nucleotide polymorphisms,SNP)检测、基因组测序、甲基化研究等方面[28]。
tSMS平台是由Helicos Biosciences公司推出的第一个商业化的单分子测序平台,其基于光学信号的边合成边测序技术[29-30]。测序时首先进行样品DNA处理,然后在3'末端加上polyA和使用Cy5荧光染料标,同时在末端进行阻断;其次与玻璃芯片上的DNA模板polyT进行杂交并精确定位,之后加入被标记的碱基和DNA聚合酶的混合液,碱基自然延长;最后使用电荷耦合器件(coupled-charge device,CCD)摄像机在光学信号下读取杂交模板信息。当标记解除后,加入新的标记的碱基和DNA聚合酶使反应继续循环下去,从而确定碱基序列。由于采用Cy5荧光基团具有很好的光稳定性、高荧光效率和灵敏的监测系统等,可以读取单个分子,在很大程度上提高了序列分析的精准度,但是这种测序技术也存在测序读长短、输出数据低、错误率高等不足。
Pacific Biosciences公司推出SMRT测序技术,是基于荧光标记的边合成边测序的思想,以SMRT芯片为载体进行测序反应[31-32],核心技术是零模波导孔(zero-mode waveguides,ZMWs)技术,ZMWs是一种直径为100 nm、厚度为70 nm的微小纳米孔,此空间正好可容纳一个DNA聚合酶分子,从而使得在此位置可观察到合成DNA链过程。测序时将样品DNA处理成小片段,以4种不同荧光标记的dNTP作为原料进行合成时,所连接的dNTP会因为反应而在ZMW纳米孔底部短暂停留,在荧光收集设备则可以收集到配对dNTP的荧光信号,根据荧光的种类就可以判定dNTP的种类,从而实现测序。
纳米孔单分子测序技术(ONT)采用“边解链边测序”的方法,其中核酸外切酶与α-溶血素纳米孔相耦合是该测序平台的核心,控制碱基穿过纳米孔的速度是技术的关键;主要原理是将蛋白纳米孔嵌入合成膜,浸在离子溶液中,膜的两侧施加恒定的电势,使离子电流通过纳米孔,由于不同碱基的带电性质不同,通过检测电流信号来确定碱基序列[33-34]。荧光共振能量转移(FRET)测序技术是基于荧光共振能量转移原理对样本基因组进行测序[35],基本步骤是先将被供体荧光基团标记的DNA聚合酶和DNA模板分子固定,掺入四种不同的荧光受体所标记的dNTP,根据碱基发出的荧光信号来判断dNTP的类别以确定基因组信息。这项测序技术是利用电信号测序,处理样品较简单、成本较低等;可是由于DNA通过纳米孔的速度很快,容易导致电流变化不明显,从而降低了测序结果的准确性。
1.3 高通量测序技术的操作流程
高通量测序技术的主要操作流程,一般包括样品准备、总DNA的提取、构建文库、上机测序、原始数据预处理与质控、操作分类单元(operational taxonomic unit,OTU)聚类分析、数据分析等步骤,高通量测序技术的基本操作流程见图1。
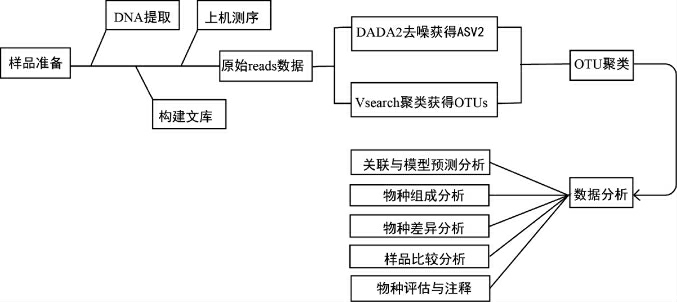
图1 高通量测序技术的基本操作流程
Fig.1 Basic operation flow of high-throughput sequencing technology
1.4 高通量测序技术常用的数据分析方法
高通量测序产出的是原始reads数据,原始数据一般需要使用USEARCH或QIIME进行双端合并、去标签和引物、拼接质控操作,获取样品的代表序列信息,运用Vsearch进行聚类获得OTUs或运用DADA2去噪获得扩增子序列变异体(amplicon sequence variants,ASVs)之后再进行统计分析。然后,可以通过量化每个样本中特征序列的频率来获得特征表,即OTU或ASV表。接着,对特征序列进行分类,通常在界、门、纲、目、科、属和种的层级上进行分类,从而为微生物群提供了更多级别的降维视角,其中OTUs和ASVs的获取主要通过与已经建立的基因数据库比对以获得分类学注释。目前,常用的基因数据库有Greengenes[36]、SILVA[37]、UNITE[38]和GenBank[39]等。在多样性分析中,普遍采用QIIME、Mothur等软件对测序数据进行分析,主要包括相关性分析、聚类分析、物种种类、差异性分析和排序分析等。
2 高通量测序技术在黄酒微生物多样性研究中的应用
2.1 糖化发酵剂对黄酒微生物多样性的影响
在黄酒酿造过程中,酒曲内的微生物主要发挥糖化功能,利用酿酒原料中的营养物质进行繁殖和代谢,将淀粉分解为葡萄糖及其他碳水化合物,供酵母菌发酵利用而产生酒精,并为黄酒的酿造提供各种酶类、有机酸、多肽类、氨基酸等物质,影响黄酒独特的色、香、味特征[40],对黄酒品质产生重要影响[41-42]。
2.1.1 酒药
酒药以籼米粉和辣蓼草等作为主要原料,接种陈药后在适宜条件下进行培养而获得的黄酒酿造用糖化发酵剂,在黄酒酿造过程中起到重要作用[43-44]。臧威等[43]基于传统的分离培养方法对绍兴黄酒酒药中酵母菌的物种资源进行研究,扣囊复膜孢酵母(Saccharomycopsis fibuligera)占有绝对的分布优势,表明扣囊复膜孢酵母对绍兴黄酒酒药的生产性能来说至关重要。CHEN C等[9]利用Illumina MiSeq高通量测序技术揭示了酒药微生物的多样性对绍兴酒发酵过程中发酵特性与挥发性成分的影响,结果表明,酒药中主要的微生物群落为片球菌属(Pediococcus)、魏斯氏属(Weissella)、复膜孢酵母属(Saccharomycopsis)和根霉属(Rhizopus),糖化力与片球菌属、酵母属和根霉属的存在呈显著正相关,而产酸能力与片球菌属、魏斯氏属和根霉属密切相关,产酒精能力与片球菌属和根霉属呈正相关,这些微生物对绍兴酒的发酵活性和风味特征有重要影响。
2.1.2 麦曲
我国黄酒生产用曲的种类多种多样,其中使用最为广泛的是麦曲[45]。麦曲是以小麦作为主要原料,经过粉碎、加水、拌和、成型、堆放,在合适的温度、湿度条件下培养制作而成[44]。制曲过程是开放的,所形成的麦曲微生物群落极其复杂[46],麦曲微生物主要包括丝状真菌、细菌和酵母菌。
JI Z等[47]利用高通量测序技术对上海、浙江和江苏的黄酒麦曲进行分析,绍兴黄酒生麦曲、江苏黄酒生麦曲、上海黄酒生麦曲、接种黄曲霉(Aspergillus flavus)的熟麦曲和天然的熟麦曲在真菌属水平上,真菌的多样性依次下降,曲霉属(Aspergillus)是优势丝状真菌。细菌在黄酒酿造过程中也同样扮演着重要角色,刘芸雅等[48]采用Illumina技术对绍兴黄酒麦曲中细菌16S rDNA可变区序列进行测序,在属水平上的主要优势菌包括糖多孢菌属(Saccharopolyspora)、芽孢杆菌属(Bacillus)、葡萄球菌属(Staphylococcus)、高温放线菌属(Thermoactinomyces)、乳杆菌属(Lactobacillus)、明串珠菌属(Leuconostoc)、乳球菌属(Lactococcus)和肠杆菌属(Enterobacter),而且芽孢杆菌属(Bacillus)和糖多孢菌属表现出突出的分布优势。XIE G F等[17]对麦曲中细菌群落结构进行了基于Illumina技术的高通量测序分析,结果发现第5天麦曲样品中放线菌门(Actinobacteria)的细菌相对丰度达到了87%,其中糖多孢菌属为优势菌属,第30天麦曲样品放线菌门的相对丰度显著下降到40.7%,而糖多孢菌属的相对丰度大幅度下降到8%,芽孢杆菌属和葡萄球菌属的相对丰度分别增加至14.5%和11.6%,根据麦曲中细菌群落结构的显著性变化可以推测不同种类的细菌在麦曲中发挥的作用。
2.2 酿造环节对黄酒微生物多样性的影响
2.2.1 浸米
在黄酒酿造前期,浸米是开始正式发酵之前的关键步骤。浸米不仅能够使原料米吸水膨胀便于蒸煮,而且浆水中存在的微生物可以使浆水酸化,抑制杂菌生长繁殖,对于后续的黄酒发酵过程和风味物质形成都可以发挥积极作用[1,6,49]。姬中伟等[50]对不同原料的米浆水进行研究,发现米浆水中的微生物主要是乳酸菌,糯米浆水酸度明显高于其他原料,观察米浆水的酸度变化对于黄酒生产的发酵控制具有指标性意义。朱小芳等[51]利用Illumina MiSeq高通量测序技术全面分析了米浆水中的细菌群落结构,发现乳杆菌属(Lactobacillus)为米浆水中主要细菌类群,丰度占比为60.7%,其中57.4%的菌群为植物乳杆菌(Lactobacillus plantarum),21.1%的菌群为短乳杆菌(Lactobacillus brevis),另外浆水中也分布有片球菌属、醋酸菌属(Acetobacter)、不动杆菌属(Acinetobacter)等细菌类群。
2.2.2 发酵
发酵是黄酒酿造的重要工序,蒸好的米饭与麦曲、淋饭酒母在陶缸内搅拌混匀,经过3~5 d完成前发酵过程,然后将发酵醪液转入陶坛进行后发酵,发酵周期历时3个月。在发酵醪液内复杂微生物区系的作用下,完成淀粉转化、酒精形成和风味物质产生等重要的生物转化过程[44]。黄酒发酵是系列微生物共同参与的生产过程,包括细菌、霉菌、酵母菌等各种微生物类群[47]。在落缸发酵后,醪液内酵母菌很快发酵产生酒精,随着黄酒发酵在较低的pH下持续进行,发酵醪液处于高酒精和高酸环境,限制了其他杂菌生长,导致大量微生物丰度减少或消失[52]。因为黄酒发酵是微生物作用的结果,任何影响微生物菌群结构变化的因素都会对黄酒的最终品质产生影响,对黄酒发酵过程中微生物多样性的变化研究分析,对指导黄酒生产具有一定意义[53]。
WANG P X等[52]利用454焦磷酸测序技术对绍兴黄酒酿造过程中的细菌多样性进行分析,结果发现处于黄酒不同发酵阶段的细菌群落结构和多样性存在显著差异,发酵醪液中存在10多个细菌属,其中乳杆菌属和芽孢杆菌属为优势微生物种群,在黄酒风味形成中可能起着重要作用。LIU S P等[5]通过MiSeq焦磷酸测序方法研究绍兴黄酒发酵过程中细菌演替规律,发现绍兴黄酒发酵过程中有10个优势细菌属,包括芽孢杆菌属、亮葡菌属(Leuconostoc)、乳球菌属、魏斯氏属、嗜热放线菌属(Thermoactinomyces)、假单胞菌属(Pseudomonas)、糖多孢菌属、葡萄球菌属、肠杆菌属和乳杆菌属,其中芽孢杆菌属和乳酸菌属在黄酒发酵细菌中起主导作用。JI Z等[47]通过Illumina-Miseq高通量测序技术解析黄酒发酵过程中真菌微生物的变化,发现在属的水平上,各个发酵阶段的醪液中优势菌是曲霉属,表明丝状真菌的代谢产物可能对黄酒中主要化学物质的形成有重要贡献。随着发酵的继续进行,物种丰富度逐渐降低,这可能是由于氧气和营养成分的改变,在不同的黄酒发酵阶段中酿酒微生物可以产生不同的有机酸的原因。
3 展望
高通量测序技术方法简单、通量更高、成本较低和速度较快,在黄酒酿造微生物研究中具有重要应用价值,不仅可以阐释黄酒发酵过程中微生物多样性,而且可以检测酿造微生物菌群的动态变化,弥补了传统培养方法的不足。由于第三代测序技术成本较高、准确率低,第二代测序技术仍然为黄酒酿造微生物研究的主流技术。但是,目前利用二代测序技术对黄酒微生物群落结构进行分析,一般只能注释到属水平或者更高的分类阶元而不能准确注释到种水平,难以彻底解析微生物种类结构及其酿造微生物种类与黄酒中成份物质的代谢关系。在未来的黄酒微生物研究中,高通量测序技术与宏基因组学、转录组学相结合,可以更加深入的研究黄酒酿造微生物的生物学功能与群落结构,也为进一步开展优良酿造菌种的筛选和改良、关键微生物代谢产物对黄酒品质的影响等科研课题提供了新的研究手段。
[1]CHEN S,XU Y.The influence of yeast strains on the volatile flavour compounds of Chinese rice wine[J].J I Brewing,2010,116(2):190-196.
[2]YANG Y,XIA Y,WANG G,et al.Effect of mixed yeast starter on volatile flavor compounds in Chinese rice wine during different brewing stages[J].LWT-Food Sci Technol,2017,78:373-381.
[3]HAN F L,XU Y.Identification of low molecular weight peptides in Chinese rice wine(Huangjiu)by UPLC-ESI-MS/MS[J].J I Brewing,2011,117(2):238-250.
[4]REN Q,SUN L,SUN Z,et al.Bacterial succession and the dynamics of flavor compounds in the Huangjiu fermented from corn[J].Arch Microbiol,2020,202(2):299-308.
[5]LIU S P,MAO J,LIU Y Y,et al.Bacterial succession and the dynamics of volatile compounds during the fermentation of Chinese rice wine from Shaoxing region[J].J Microbiol Biotechn,2015,31(12):1907-1921.
[6]ZHU F,LI S,GUAN X F,et al.Influence of vacuum soaking on the brewing properties of japonica rice and the quality of Chinese rice wine[J]. J Biosci Bioeng,2020,130(2):159-165.
[7]JIAO A,XU X,JIN Z.Research progress on the brewing techniques of newtype rice wine[J].Food Chem,2017,215:508-515.
[8]CAO Y,XIE G F,WU C,et al.A study on characteristic flavor compounds in traditional Chinese rice wine-Guyue Longshan rice wine[J].J I Brewing,2010,116(2):182-189.
[9] CHEN C,LIU Y,TIAN H,et al.Metagenomic analysis reveals the impact of Jiuyao microbial diversity on fermentation and the volatile profile of Shaoxing-jiu[J].Food Microbiol,2020,86:103326.
[10] LV X C,HUANG R L,CHEN F,et al.Bacterial community dynamics during the traditional brewing of Wuyi Hong Qu glutinous rice wine as determined by culture-independent methods[J].Food Control,2013,34(2):300-306.
[11]SEKIGUCHI H,TOMIOKA N,NAKAHARA T,et al.A single band does not always represent single bacterial strains in denaturing gradient gel electrophoresis analysis[J].Biotechnol Lett,2001,23(15):1205-1208.
[12] FERRIS M J,MUYZER G,WARD D M.Denaturing gradient gel electrophoresis profiles of 16S rRNA-defined populations inhabiting a hot spring microbial mat community[J].Appl Environ Microbiol,1996,62(2):340-346.
[13]GUAN Z B,ZHANG Z H,CAO Y,et al.Analysis and comparison of bacterial communities in two types of'wheat Qu',the starter culture of Shaoxing rice wine,using nested PCR-DGGE[J]. J I Brewing,2012,118(1):127-132.
[14] SULTAN M,SCHULZ M H,RICHARD H,et al.A global view of gene activity and alternative splicing by deep sequencing of the human transcriptome[J].Science,2008,321(5891):956-960.
[15] SCHUSTER S C.Next-generation sequencing transforms today's biology[J].Nat Methods,2008,5(1):16-18.
[16]SHENDURE J,JI H.Next-generation DNA sequencing[J].Nat Biotechnol,2008,26(10):1135-1145.
[17]XIE G F,WANG L,GAO Q,et al.Microbial community structure in fermentation process of Shaoxing rice wine by Illumina-based metagenomic sequencing[J].J Sci Food Agr,2013,93(12):3121-3125.
[18]HE G Q,LIU T J,SADIQ F A,et al.Insights into the microbial diversity and community dynamics of Chinese traditional fermented foods from using high-throughput sequencing approaches[J].J Zhejiang Univ-SC B,2017,18(4):289-302.
[19]METZKER M L.Sequencing technologies-the next generation[J].Nat Rev Genet,2010,11(1):31-46.
[20]SANGER F,NICKLEN S,COULSON A R.DNA sequencing with chainterminating inhibitors[J].P Natl Acad Sci USA,1977,74(12):5463-5467.
[21]LIU L,LI Y,LI S,et al.Comparison of next-generation sequencing systems[J].J Biomed Biotechnol,2012,2012:251364.
[22] PAN Q,SHAI O,LEE L J,et al.Deep surveying of alternative splicing complexity in the human transcriptome by high-throughput sequencing[J].Nat Genet,2008,40(12):1413-1415.
[23]ROTHBERG J M,LEAMON J H.The development and impact of 454 sequencing[J].Nat Biotechnol,2008,26(10):1117-1124.
[24]DEURENBERG R H,BATHOORN E,CHLEBOWICZ M A,et al.Application of next generation sequencing in clinical microbiology and infection prevention[J].J Biotechnol,2017,243:16-24.
[25] ONDOV B D,ANJANA V,PASSALACQUA K D,et al.Efficient mapping of applied biosystems SOLiD sequence data to a reference genome for functional genomic applications[J]. Bioinformatics,2008,24(23):2776-2777.
[26] MARDIS E R.The impact of next-generation sequencing technology on genetics[J].Trends Genet,2008,24(3):133-141.
[27]TOUMAZOU C,PURUSHOTHAMAN S.Sensing apparatus and method:US,7686929b2[P].2010-06-17.
[28] BLEIDORN C.Third generation sequencing:technology and its potential impact on evolutionary biodiversity research[J]. Syst Biodivers,2016,14(1):1-8.
[29]TREFFER R,DECKERT V.Recent advances in single-molecule sequencing[J].Curr Opin Biotechnol,2010,21(1):4-11.
[30] HARRIS T D,BUZBY P R,BABCOCK H,et al.Single-molecule DNA sequencing of a viral genome[J].Science,2008,320(5872):106-109.
[31]LU H,GIORDANO F,NING Z.Oxford nanopore MinION sequencing and genome assembly[J].Genom Proteom Bioinf,2016,14(5):265-279.
[32]ARDUI S,AMEUR A,VERMEESCH J R,et al.Single molecule real-time(SMRT) sequencing comes of age:Applications and utilities for medical diagnostics[J].Nucleic Acids Res,2018,46(5):2159-2168.
[33]RHOADS A,AU K F.PacBio sequencing and its applications[J].Genom Proteom Bioinf,2015,13(5):278-289.
[34] JAIN M,OLSEN H E,PATEN B,et al.The Oxford Nanopore MinION:delivery of nanopore sequencing to the genomics community[J]. Genome Biol,2016,17(1):239.
[35]ROY R,HOHNG S,HA T.A practical guide to single-molecule FRET[J].Nat Methods,2008,5(6):507-516.
[36] DESANTIS T Z,HUGENHOLTZ P,LARSEN N,et al.Greengenes,a chimera-checked 16S rRNA gene database and workbench compatible with ARB[J].Appl Environ Microbiol,2006,72(7):5069-5072.
[37] QUAST C,PRUESSE E,YILMAZ P,et al.The SILVA ribosomal RNA gene database project:improved data processing and webbased tools[J].Nucleic Acids Res,2013,41(1):590-596.
[38] ABARENKOV K,NILSSON R H,LARSSON K H,et al.The UNITE database for molecular identification of fungi-recent updates and future perspectives[J].New Phytol,2010,186(2):281-285.
[39]MENDOZA L M,NEEF A,VIGNOLO G,et al.Yeast diversity during the fermentation of Andean chicha:a comparison of high-throughput sequencing and culture-dependent approaches[J].Food Microbiol,2017,67:1-10.
[40]ZHANG S,CHEN X,ZHONG Q,et al.Microbial community analyses associatedwithninevarietiesofwine grape carposphere based on high-throughput sequencing[J].Microorganisms,2019,7(12):668.
[41]XIE G F,LI W J,LU J,et al.Isolation and identification of representative fungi from Shaoxing rice wine wheat Qu using a polyphasic approach of culture-based and molecular-based methods[J].J I Brewing,2012,113(3):272-279.
[42] YU L,DING F,YE H.Analysis of characteristic flavour compounds in Chinese rice wines and representative fungi in wheat Qu samples from different regions[J].J I Brewing,2012,118(1):114-119.
[43]臧威,谢广发,孙剑秋,等.绍兴黄酒酒药中酵母菌的物种资源[J].菌物学报,2015,34(6):1078-1084.
[44] 孙剑秋,邹慧君,谢广发,等.黄酒酿造学[M].北京:科学出版社,2019:1-203.
[45]SHANG Y L,CHEN L L,ZHANG Z H,et al.A comparative study on the fungal communities of wheat Qu for Qingshuang-type Chinese rice wine[J].J I Brewing,2012,118(2):243-248.
[46] LIU S,HU J,XU Y,et al.Combined use of single molecule real-time DNA sequencing technology and culture-dependent methods to analyze the functional microorganisms in inoculated raw wheat Qu[J].Food Res Int,2020,132:109062.
[47]JI Z,JIN J,YU G,et al.Characteristic of filamentous fungal diversity and dynamics associated with wheat Qu and the traditional fermentation of Chinese rice wine[J].Int J Food Sci Tech,2018,53(7):1611-1621.
[48]刘芸雅,毛健,孟祥勇,等.绍兴黄酒麦曲及发酵过程中细菌群落结构分析[J].中国食品学报,2017,17(1):201-208.
[49] WEI X L,LIU S P,YU J S,et al.Innovation Chinese rice wine brewing technology by bi-acidification to exclude rice soaking process[J].J Biosci Bioeng,2017,123(4):460-465.
[50]姬中伟,黄桂东,毛健,等.浸米时间对黄酒品质的影响[J].食品与机械,2013,29(1):49-52.
[51]朱小芳,张凤杰,俞剑燊,等.黄酒浸米水中细菌群落结构及优势菌代谢分析[J].食品科学,2017,38(10):82-86.
[52]WANG P X,MAO J,MENG X Y,et al.Changes in flavour characteristics and bacterial diversity during the traditional fermentation of Chinese rice wines from Shaoxing region[J].Food Control,2014,44:58-63.
[53]HONG X,CHEN J,LIU L,et al.Metagenomic sequencing reveals the relationship between microbiota composition and quality of Chinese Rice Wine[J].Sci Rep,2016,6(1):1-11.