肠道疾病包括炎症性肠病[1]、肠易激综合征、结直肠癌、代谢相关类疾病、渗透性腹泻[2]、慢性便秘等疾病。研究表明,肠道疾病的发生与肠道菌群代谢失调密切相关[2-3]。肠道菌群在维护肠道屏障[4]、营养代谢、免疫应答等方面发挥着重要作用。正常情况下,机体内肠道菌群维持动态平衡以保护肠道健康。肠道菌群失衡时会引发代谢紊乱,增加肠道患病风险。因此,维持肠道内菌群的动态平衡尤为重要。目前,主要通过药物对肠道疾病进行治疗,但长期服用药物会不可避免地对机体产生一定的毒副作用。不健康的饮食结构[5]是导致肠道菌群失衡的重要因素,膳食治疗正日益成为治疗肠道疾病领域的热点,通过食物或食药同源的方式治疗肠道疾病,具有更高的安全性。
黄酒作为中国历史悠久的传统酿造酒,其成分复杂,含有丰富的糖、氨基酸、有机酸、蛋白质、维生素和酯类物质[6]。黄酒中糖类物质相对含量较高,具有独特功效。酒药与麦曲微生物可作用于原料稻米与小麦,生成丰富的糖类物质[7]。麦曲以小麦为原料,通过粉碎、加水搅拌后在自然环境下培养制成,酒药是以添加了辣蓼草粉末的米粉经过过筛、打实、切块、接种和晒干等步骤制成,其内部含有丰富的微生物[8]。原料稻米与小麦中淀粉含量较高,蒸煮糊化后被酿造体系中微生物分解为多糖、低聚糖与单、双糖[9]。随着发酵时间的延长,体系内酒精含量逐渐升高。当酒精含量增长至一定程度时,酵母菌的生长与代谢受到抑制,发酵减弱甚至停止,对体系糖的消耗减少,部分糖可残留于黄酒中[9]。
黄酒中的糖种类繁多,含有葡萄糖、麦芽糖、海藻糖、低聚糖与多糖等。黄酒低聚糖可作为活性物质改善肠道环境,达到治疗部分肠道疾病的目的。该文详细论述了黄酒低聚糖的来源、种类与检测现状,并阐明了膳食低聚糖对机体便秘症状的缓解、对肠道炎症的治疗、对肥胖症状的缓解作用及其作用机理,为黄酒低聚糖对肠道疾病的后续功能研究提供了理论基础与新的思路。
1 黄酒低聚糖简介
低聚糖又称寡糖,可分为功能性低聚糖与普通低聚糖两大类[10]。普通低聚糖可在消化道内酶解,直接被消化吸收,功能性低聚糖则难以在消化道内分解,可作为双歧杆菌的增殖因子,直接进入结肠为双歧杆菌利用。在发酵过程中,麦曲与酒药中丰富的微生物赋予了黄酒酿造体系庞大的酶系,体系中含有分支酶、α-淀粉酶、β-淀粉酶、脱支酶、葡萄糖苷转移酶等多种酶类。体系酶作用于原料稻米与小麦可生成种类独特、含量丰富的黄酒低聚糖。
黄酒低聚糖是由3~10个单糖通过糖苷键连接而成的直链或支链的低度聚合糖类,具有独特的功效:①刺激肠内有益菌的增殖与代谢,抑制外源致病菌与肠内腐败菌的生长,平衡肠道菌群;②增加肠腔内短链脂肪酸(short-chain fatty acids,SCFAs)的含量,调节代谢通路,增强肠道屏障,治疗便秘、炎症性肠病等肠道疾病;③调节脂质代谢,改善机体内部激素紊乱,改善机体肥胖[11]。
2 黄酒低聚糖的来源与种类
黄酒低聚糖主要包括稻米、小麦与体系酶作用生成的低聚麦芽糖类,小麦麸皮中阿拉伯木聚糖水解生成的阿拉伯低聚木糖、小麦麸皮中的低聚木糖、小麦麸皮中阿魏酸酯化生成的阿魏酰低聚糖、酵母细胞壁中的甘露低聚糖等。
低聚麦芽糖类包括异麦芽糖、潘糖、异麦芽三糖、麦芽四糖等聚合度(degree of polymerization,DP)<10的短链糖类。黄酒酿造的原料米主要为糯米、粳米与籼米等,糯米中支链淀粉达98%,粳米中支链淀粉占83%,籼米中支链淀粉占70%。黄酒酿造原料米中支链淀粉含量较高,支链淀粉在分支处以α-1,6糖苷键连接。淀粉酶不易切断支链淀粉的α-1,6糖苷键,因此在成品黄酒中残留大量的分枝低聚糖[12]。
来源于细菌与真菌的α-淀粉酶以内切的方式随机作用于淀粉内部的α-1,4糖苷键,将淀粉水解为各种类型的寡糖与α-极限糊精[13];来源于细菌与真菌的β-淀粉酶以外切的方式从淀粉的非还原末端开始水解α-1,4糖苷键,顺次切下一个麦芽糖分子,但顺位切割不可越过α-1,6糖苷键进行,反应遇α-1,6糖苷键自动停止,水解产物为麦芽糖与β-极限糊精;来源于黑曲霉与稻曲霉菌的葡萄糖淀粉酶从还原末端水解α-1,4糖苷键,顺次切下一个葡萄糖单位,水解产物为葡萄糖与β-极限糊精;来源于细菌与真菌的脱支酶以内切方式作用于支链淀粉及糖原中的α-1,6糖苷键,将支链淀粉水解为直链淀粉与小分子直链寡糖;来源于细菌与真菌的分支酶一方面可催化α-1,4 糖苷键的降解,另一方面又可通过形成α-1,6糖苷键将所降解的分子片段连接到受体上,增加淀粉分支度[14]。转苷反应为形成支化结构的基础[15],不同类型的分支酶转移链段的长度不同,一般要求转移链DP>3[16];葡萄糖苷转移酶普遍存在于黑曲霉与稻谷曲霉中,可切断麦芽糖的α-1,4糖苷键,形成葡萄糖残基,也可通过形成α-1,6糖苷键将葡萄糖残基转移至其他糖残基,生成异麦芽糖、潘糖与异麦芽三糖等低聚糖。在α-葡萄糖苷转移酶的作用下,当游离的葡萄糖残基以α-1,6糖苷键连接至葡萄糖分子上时,可形成异麦芽糖;当游离的葡萄糖残基以α-1,6糖苷键连接至麦芽糖分子上时,可形成潘糖;当游离的葡萄糖残基以α-1,6糖苷键连接至异麦芽糖分子上时,可形成异麦芽三糖。
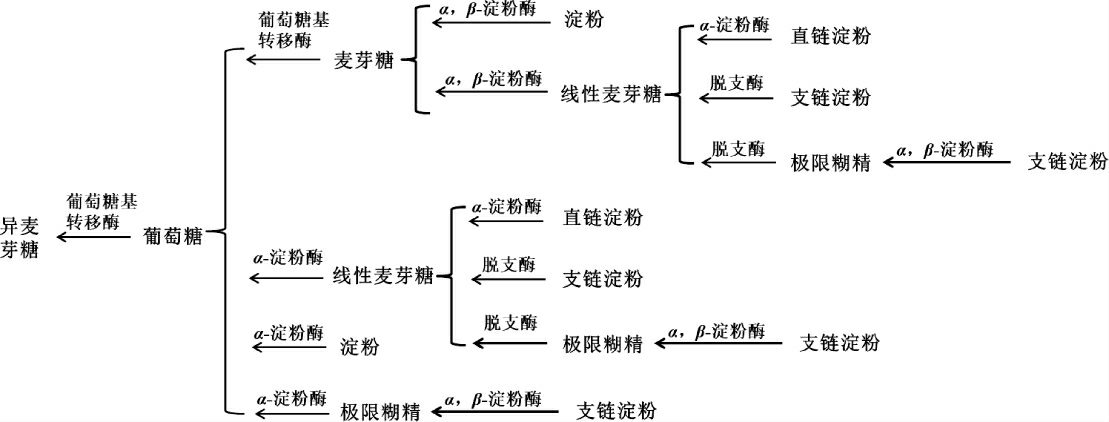
图1 黄酒中异麦芽糖生成途径[12-16]
Fig.1 Pathway of isomaltose production in Huangjiu
阿拉伯木聚糖是存在于稻谷、燕麦、小麦、高粱与大麦等粮食作物的淀粉质胚乳的细胞壁、糊粉层与麸皮中的非淀粉多糖[17-18],可在微生物和小麦本身产生的木聚糖酶的作用下水解生成阿拉伯低聚木糖。小麦中阿拉伯木聚糖的含量在6.3%~6.5%之间[19]。阿拉伯低聚木糖是指以β-1,4-糖苷键连接的2~7个木糖残基为主链,在C-2和/或C-3位置上取代有侧链α-L-阿拉伯呋喃糖基的寡糖[20]。麦曲以小麦为原料制成,酿造过程中,麦麸中部分阿拉伯木聚糖被酶解为阿拉伯低聚木糖与低聚木糖,被保存至成品黄酒中。
小麦麸皮中存在0.4%~1.0%的阿魏酸。作为小麦麸皮中含量最高的酚酸,阿魏酸主要通过酯键与半纤维素交联,通过醚键与木质素相连[21]。通过物理或化学方法可使半纤维素之间的部分糖苷键断裂,从而得到阿魏酸的酯化形式—阿魏酰低聚糖。在发酵条件下,阿魏酸的羧基可通过酯键与低聚糖的羟基相连,生成阿魏酰低聚糖。阿魏酰低聚糖种类繁多,主要包括阿魏酸-阿拉伯糖基-木糖、阿魏酸-阿拉伯糖基-阿拉伯糖、阿魏酸-半乳糖基-半乳糖、阿魏酸-阿拉伯糖基-木二糖、阿魏酸-阿拉伯糖基-木三糖和阿魏酸-阿拉伯糖基-木四糖等[22]。
甘露低聚糖又称甘露寡糖或葡甘露寡聚糖,存在于植物与酵母细胞壁内[23-24],多数情况下以复合物的形式存在,由甘露糖与葡萄糖通过α-1,2糖苷键、α-1,3糖苷键与α-1,6糖苷键连接而成,主要类型包括纯甘露寡糖[25]、葡甘露寡糖、半乳甘露寡糖和半乳葡甘露寡糖。黄酒麦曲与酒药中含有丰富的酵母,酵母细胞壁中含有约6.6%的甘露低聚糖[26]。酵母细胞在自溶及酶解作用下,细胞壁破裂,释放出甘露低聚糖。甘露寡糖结构较稳定[27],能在高温(煎酒)、低pH条件下保持完整的结构,保留至成品黄酒中。
表1 黄酒中低聚糖的种类、来源、作用酶及主要成分
Table1 Types,sources,functional enzymes and main components of oligosaccharides in Huangjiu

3 黄酒低聚糖的检测现状
现如今对黄酒中低聚糖的检测主要集中于低聚异麦芽糖类,主要包括异麦芽糖、潘糖与异麦芽三糖。以元红酒为代表的干型黄酒中低聚异麦芽糖含量达20%以上,以加饭酒为代表的半干型中黄酒低聚糖含量达17%以上,以善酿酒为代表的半甜型黄酒中低聚糖含量达23%以上,以香雪酒为代表的甜型黄酒中低聚糖含量达13%以上。其中,南方黄酒与闵派黄酒中异麦芽糖和潘糖含量相对较高,异麦芽三糖含量相对较低[28]。
目前主要通过高效液相色谱法(high performance liquid chromatography,HPLC)与阴离子交换色谱-积分脉冲安培检测法对黄酒中低聚糖进行检测。黄酒酿造原料中主要淀粉类型为支链淀粉,周昕[29]以HPLC法测定支链淀粉酶解产物,证明支链淀粉被淀粉酶水解后,可生成葡萄糖、麦芽糖、麦芽三糖、麦芽四糖、麦芽五糖、麦芽六糖、麦芽七糖及DP>7的聚合糖类;蔡鑫等[30]利用HPLC法测定5种市售闽派黄酒(沉缸尚客、闽族红、惠泽龙、惠泽龙有机酒、坂面红)中异麦芽糖、异麦芽三糖与潘糖的含量,所测样品低聚糖含量在0.9~8.8 g/L之间;BAI W D等[31]通过柱前衍生高效液相色谱法测定了客家黄酒中的异麦芽糖与异麦芽三糖的含量;胡贝贞等[28]通过高效阴离子交换色谱-积分脉冲安培检测法测得绍兴元红酒、加饭酒、善酿酒和香雪酒中麦芽糖、异麦芽糖、潘糖、麦芽三糖、异麦芽三糖含量总量在3.4~25.5 g/L之间;方晓弟[32]通过1-苯基-3-甲基-5-吡唑啉酮柱前衍生-HPLC测定出广东梅州客家娘酒样品中麦芽糖、异麦芽三糖与潘糖的总量在1.5~11.8 g/L之间。
黄酒低聚糖含量检测仍存在改进空间:①不同检测方法检测出的黄酒低聚糖含量存在差异,目前测定黄酒中低聚糖含量方法主要集中于高效液相色谱法,其测量结果易受到黄酒中其他物质的干扰,产生叠峰。可利用阴离子交换色谱、液相色谱-质谱联用等技术更为精确地检测黄酒中低聚糖含量;②目前只测定了黄酒中低聚异麦芽糖的含量,黄酒中其他短链寡糖(如甘露寡糖、阿拉伯-低聚木糖等)尚未被检测,可通过标品定量检测更多种类的黄酒低聚糖。
4 黄酒低聚糖及膳食低聚糖对部分肠道疾病作用的研究进展
低聚糖具有如下功能[10]:①促进肠道双歧杆菌、乳酸菌等有益菌的增殖;②降低内毒素的表达,保护机体肝脏;③调节胃肠功能,预防便秘;④降低血氨浓度;⑤促进矿物元素吸收;⑥合成维生素等。作为一种新型功能性能源,低聚糖集营养、保健、食疗于一体,广泛应用于食品、保健品、饮料、医药、饲料添加剂等领域。
益生元具有选择性地促进肠道内有益菌的增殖,促进肠道微生物代谢产生SCFAs,降低肠道内pH,改善肠道屏障以及维持肠道渗透压等功效。目前对低聚糖的研究主要集中于其益生功效方面。作为聚合度为3~10的短链糖,非消化性低聚糖因含有α-1,6糖苷键[33-34],不能被人体胃肠道的淀粉酶彻底水解,到达结肠后被结肠中的微生物群作为能源发酵利用,选择性地促进有益菌的增殖,可作为典型的益生元对机体肠道进行调节[35]。因此,进行低聚糖对部分肠道疾病的治疗机制研究具有现实意义。
4.1 黄酒低聚糖及膳食低聚糖对便秘症状的治疗
便秘是世界范围内常见的胃肠道问题,在老年群体与女性群体间发病率较高。便秘会加快皮肤老化,引发头痛、粉刺、痔疮等症状,严重时可诱发结肠癌[36]。泻药常用于治疗便秘,但泻药的频繁使用会产生各种副作用,如严重脱水、电解质紊乱[7]等,甚至有可能损害结肠神经系统,引发心血管疾病[37]。因此,能够有效预防和治疗便秘的食品成为研发热点。有研究表明,低聚糖可明显增加机体的排便次数,缩短结肠运输时间,且几乎不对机体产生任何副作用[38]。低聚糖可促进肠道内乳酸杆菌、双歧杆菌等有益菌的生长,酵解后产生SCFAs,抑制肠道内腐败菌的生长,减少有害代谢产物的积累,平衡肠道微生物组成,调节胃肠道通路,因此可作为益生元治疗便秘[39]。
黄酒低聚糖组分主要包括麦芽低聚糖、甘露低聚糖、阿魏酰低聚糖、阿拉伯低聚木糖、低聚木糖等糖。目前已检测到黄酒中含有丰富的低聚异麦芽糖。低聚异麦芽糖因含有α-1,6糖苷键,可避免被小肠消化,可直接到达结肠被微生物发酵利用。已有研究表明[40],低聚异麦芽糖可增加机体肠道内有益菌群(包括双歧杆菌、乳杆菌等)的数量,促进小肠蠕动,改善机体便秘。
黄酒及膳食低聚糖可通过以下途径治疗机体便秘:①平衡肠道菌群,增强肠道屏障,调节体内激素紊乱,改善菌群代谢特征。肠道内双歧杆菌可被黄酒低聚糖及膳食低聚糖活化,发挥以下功效[41]:a.双歧杆菌生成的凝集素可与肠上皮细胞表面的糖蛋白结合,占据肠粘膜表面,增强肠道屏障;b.双歧杆菌可通过代谢产生抗菌素,抑制肠内有害菌的生长;c.双歧杆菌发酵产生的有机酸可抑制肠道内部分有害菌的生长。②上调肠内SCFAs的含量,调节代谢通路,治疗便秘。SCFAs可调控肠内神经元,产生胆碱能促进作用,加速肠道内物质的传输,增加排便次数。同时,SCFAs可刺激肠内5-羟色胺(5-hydroxytryptamine,5-HT)的分泌,促进肠道蠕动,加快结肠运输。低聚果糖、低聚半乳糖与低聚异麦芽糖可上调小鼠血清中兴奋性递质的表达[42],增加盲肠内容物中有益菌的丰度,增加粪便中短链脂肪酸(主要为乙酸与丁酸)的含量,可有效预防小鼠便秘;莲子低聚糖可通过调节机体肠道菌群、增加SCFAs产量、提高血清激素浓度,促进肠道蠕动等来缩短小鼠排便时间,提高粪便含水量,达到治疗便秘的目的[43];低聚异麦芽糖可平衡便秘引起的大鼠血清激素紊乱,增加便秘大鼠结肠内容物中SCFAs产量,增加肠道微生物的稳定性,缓解地芬诺酯诱导的大鼠便秘[44];魔芋甘露寡糖可调节小鼠肠神经系统参数水平,增强肠道屏障,调节SCFAs产量,下调肠匀浆中5-HT水平,从而调节胃肠功能,缓解便秘[45]。不同剂量、不同种类低聚糖在对小鼠便秘症状均有缓解,但缓解程度不同[46]。
黄酒低聚糖及膳食低聚糖通过调节机体肠道菌群竞争及调节SCFAs代谢通路,最终改善便秘症状,作用条件温和,安全性较高,经济实惠,具有广阔的开发前景。
4.2 黄酒低聚糖及膳食低聚糖对肠道炎症的治疗
肠道微生物群为包含500~1 000个细菌物种的密集微生物群落,可维持机体重要生理机能[47]。菌群结构失衡将损伤肠道屏障,引发机体炎症与代谢综合征等疾病。以双歧杆菌为例,婴儿时期双歧杆菌的丰度可占结肠微生物群总数的90%,在成人阶段则下降至5%以下,在老年人结肠中所占比例进一步减少[48]。双歧杆菌丰度的降低常引起炎症性肠病,损害机体健康。
益生元是临床上应用最多的治疗代谢紊乱的药物。膳食低聚糖作为天然益生元,可活化肠道内双歧杆菌、乳酸杆菌等有益菌,通过平衡肠道菌群来改善代谢紊乱[49-50]。黄酒低聚糖及膳食低聚糖可通过以下途径治疗肠道炎症:①调节肠道菌群,促进肠道有益菌的增殖,抑制外源致病菌和肠内腐败菌的生长,从而改善体内激素紊乱。黄酒低聚糖中低聚异麦芽糖可抑制肠内有害菌的生长,并上调机体内SCFAs的含量,达到改善菌群特征、调节机体代谢的目的[51];海藻酸寡糖可调节高脂饮食小鼠肠道微生物群的整体组成,缓解高脂饮食或抗生素引起的肠道失调,有选择性地增加有益肠道细菌(如乳酸杆菌和阿克曼氏菌属)的相对丰度,并降低致炎细菌(如类杆菌和对聚乳酸菌)的丰度,减少肠道炎症的发生[52];低聚果糖可增加乳酸杆菌、双歧杆菌和普雷沃氏菌属等菌群的数量来平衡肠道的微生物组成,同时通过增加肠绒毛长度、肠粘膜厚度、绒毛高度与隐窝深度之比等来改善肠道参数,使肠道对营养物质进行充分吸收[53]。②低聚糖可通过修复受损肠道屏障治疗肠道炎症。黄酒低聚糖中低聚异麦芽糖可改善机体肠道性能,修复肠粘膜损伤,增强肠道物理屏障,抑制外源致病菌侵入,增强机体免疫力,减少机体患肠道炎症的风险[51];人乳低聚糖可有效增强肠道屏障,并不同程度地调节肠道细胞因子和紧密连接蛋白的表达[54];海藻寡糖可通过维持猪小肠上皮细胞(IPEC-J2细胞)的完整性,增强IPEC-J2细胞的迁移能力来增强猪肠道物理屏障,降低猪患肠道炎症的可能[55];江蓠寡糖可通过减少有害细菌的数量,增强结肠炎小鼠肠道转运、推进运动,增强平滑肌收缩力,生成可溶性细胞间粘附分子等方式解除小鼠胃肠动力障碍,达到治疗小鼠溃疡性结肠炎的目的[56]。
结肠炎症对胃肠动力有抑制作用,这导致了肠道微生物组成的二次失衡,增加有害细菌的丰度,积累有毒代谢物,损害肠道粘膜屏障,加重炎症,造成恶性循环。肠道有益细菌可利用黄酒低聚糖及膳食低聚糖改善肠道内微生态环境,调节胃肠功能,达到治疗肠道炎症的目的。
4.3 黄酒低聚糖及膳食低聚糖对肥胖症状的治疗
作为一种慢性代谢类疾病,肥胖主要由长期的不良饮食与生活习惯导致。机体能量摄入超过能量消耗,进而导致能量失衡,多余脂肪在体内积累[49]。据世界卫生组织统计,截至2016年,世界有39%的成年人处于超重状态,13%的成年人处于肥胖状态。日益严重的肥胖问题导致了类如高血压、糖尿病、高血脂、心脑血管疾病、睡眠障碍等病症[57]。健康人群体内肠道菌群处于动态平衡,一旦打破这种平衡,则易引起代谢紊乱,导致机体肥胖。
饮食模式在平衡肠道菌群方面起主导作用,这将进一步影响机体的能量代谢,进而影响机体健康。黄酒低聚糖中低聚异麦芽糖已被证明可抑制胆固醇的吸收,促进食物的消化,增强机体对矿物元素的吸收[58]。同时由于机体消化道内缺乏分解低聚异麦芽糖的酶,因此低聚异麦芽糖不会引起机体血糖上升,有利于机体肥胖症状的治疗。黄酒低聚糖等膳食低聚糖可被结肠菌群发酵,通过以下途径抑制肥胖[11]:①通过改善肠道菌群的结构,提高肠道内有益菌群竞争力。肥胖人群与消瘦人群相比,肠道内厚壁菌门(Firmicutes)细菌丰度较高,而拟杆菌门(Bacteroidetes)细菌丰度较低。厚壁菌门/拟杆菌门比率(F/B比率)的增加可影响肥胖小鼠饮食和遗传模型中肥胖的发病机制。低聚木糖作用于高脂饮食的大鼠后,可调节肠道菌群结构,肠道内厚壁菌门/拟杆菌门比率显著降低[59];不饱和藻酸盐寡糖通过调节肠道微生物群显著改善了高脂饮食喂养小鼠引起的肥胖和相关异常,选择性地增加了有益肠道细菌的丰度,降低了炎症细菌的相对丰度,可用作治疗肥胖相关代谢疾病的益生元[52];低聚异麦芽糖可改善菌群结构,促进肠内双歧杆菌增殖为肠内优势菌群,改善肠道微环境。②低聚糖被肠道菌群分解利用后产生的SCFAs可影响机体内甘油三酯及胆固醇的代谢。SCFAs在调节机体的食欲和新陈代谢过程中起着关键作用[60]:丙酸可通过激活其游离脂肪酸受体来降低机体食欲并刺激分泌胃肠激素,丁酸可增强脂肪组织中的食欲抑制激素(如瘦素)的分泌。此外,SCFAs还可通过增强脂肪组织中的脂解作用参与调节能量代谢。低聚木糖作用于高脂饮食的大鼠后,大鼠肠道内产SCFAs的细菌和SCFAs含量均增加;甘露寡糖通过调节肠道内微生物的组成,上调干细胞因子的产生,促进肠道内SCFAs的生成显著抑制了高脂饮食引起的小鼠肥胖。③低聚糖可通过改善肠道屏障功能抑制肥胖。壳寡糖可通过平衡肠道微生物群,改善轻度炎症,维护肠道上皮屏障,治疗机体肥胖[57]。④低聚糖通过上调食欲相关激素与信号因子减少肥胖症状。魔芋葡苷低聚糖可有效减缓肥胖大鼠体质量的增加,改善肥胖大鼠的血脂水平,调节脂质代谢紊乱,提高机体的氧自由基清除能力,降低肥胖大鼠肝质量与肝脏指数,减少肝细胞体积和细胞内脂滴量,并降低脂质代谢相关酶的活力[61]。
不健康的饮食与作息常会引起肠道菌群失调,进而导致肥胖。黄酒低聚糖及膳食低聚糖可作为益生元,调节肠道中厚壁菌门与拟杆菌门比例,改善代谢紊乱,调节机体脂质代谢,减少脂肪积累,有效调节治疗机体肥胖。
4.4 黄酒低聚糖对肠道疾病作用的功能预测
黄酒低聚糖来源及种类丰富,含有麦芽低聚糖、甘露低聚糖、阿魏酰低聚糖、阿拉伯低聚木糖、低聚木糖等糖。由其中低聚异麦芽糖对肠道疾病的作用机制可知,低聚糖在机体摄入后可被结肠微生物发酵利用,平衡肠内菌群,增加短链脂肪酸含量,调节机体内部脂质代谢,改善体内激素紊乱,从而增强肠道屏障,达到治疗炎症性肠病、缓解机体便秘、改善机体肥胖的效果。黄酒低聚糖作为多种低聚糖的混合物,理论上可通过与其他膳食低聚糖类似的治疗途径,达到改善肠道环境、治疗部分肠道疾病的效果。
现有报道已检测出黄酒中含有低聚异麦芽糖,根据现有研究推论黄酒中可能存在甘露低聚糖、阿魏酰低聚糖、低聚木糖、甘露低聚糖、阿拉伯木聚糖等。低聚异麦芽糖、甘露低聚糖、低聚木糖、阿拉伯木聚糖等低聚糖可对便秘、肥胖、肠道炎症等肠道疾病进行治疗,后续可尝试提取并分离纯化黄酒中低聚糖,并对其种类及含量进行检测。同时可将组分复杂的黄酒低聚糖与单一成分的膳食低聚糖进行对比,探究黄酒中不同种类的低聚糖是否可发挥协同作用,对肠道疾病有更好的治疗效果,并可对其作用机理进行探究。
5 结论与展望
作为黄酒中重要的生物活性成分,黄酒低聚糖成分复杂,种类繁多,可作为益生元发挥调节肠道菌群、改善肠内环境的功效,正日益成为食品行业研究的热点之一。黄酒低聚糖主要来源于酒药与麦曲微生物对原料稻米与小麦的酶解作用,种类繁多,主要包括麦芽低聚糖、甘露低聚糖、阿魏酰低聚糖、阿拉伯低聚木糖、低聚木糖等。低温、长时的发酵工艺赋予了黄酒低聚糖独特的功效。由膳食低聚糖对肠道疾病的作用机制推测,通过平衡肠道菌群与上调肠腔内短链脂肪酸的含量来调节代谢特定通路,是黄酒低聚糖治疗肠道疾病的机制之一。
目前,膳食低聚糖的提取及功能探究成为该领域的研究热点,后续可从以下方面进行深入探究:①利用阴离子交换色谱、液相色谱-质谱联用等新技术对黄酒低聚糖的种类与含量进行全面检测,更科学准确地表征黄酒中低聚糖含量;②进行黄酒低聚糖的分离纯化与结构表征。通过黄酒减压浓缩、乙醇沉淀、Sevage法除蛋白、膜分离技术、离子交换柱分离、凝胶柱纯化、冷冻干燥等手段进行黄酒低聚糖的分离纯化,借助亲水相互作用色谱、紫外-可见光光谱、红外光谱、核磁共振波谱、扫描电镜、粒径分析仪等对黄酒低聚糖结构进行表征;③可尝试提取特定黄酒低聚糖对肠道疾病进行靶向治疗,研究其代谢通路及量效关系。
[1]王丽娜.肠道菌群与肠黏膜免疫及相关疾病的研究进展[D].重庆:重庆医科大学,2017.
[2]MENG X,ZHANG G,CAO H,et al.Gut dysbacteriosis and intestinal disease:mechanism and treatment[J].J Appl Microbiol,2020,129(4):787-805.
[3]刘嘉奕.肠道菌群与儿科肠道炎症性疾病研究[D].上海:上海交通大学,2019.
[4]沈男,刘毅,盖中涛.肠道菌群与肠道疾病关系的研究进展[J].基础医学与临床,2018,38(7):1034-1037.
[5]谭玲玲,黄梅,马欣,等.基于肠道微生态的慢性肾脏病治疗[J].重庆医学,2017,46(18):2566-2568.
[6]蔡际豪.不同工艺绍兴黄酒风味比对及传统绍兴黄酒风味表征研究[D].杭州:浙江工业大学,2020.
[7] ALSALIMY N,MADI L,AWAISU A.Efficacy and safety of laxatives for chronic constipation in long-term care settings:A systematic review[J].J Clin Pharm Ther,2018,43(5):595-605.
[8]汤斯斯.不同酒曲客家黄酒多糖的特性研究[D].广州:仲恺农业工程学院,2018.
[9]李琴.黄酒中多糖稳定性的研究[D].杭州:浙江农林大学,2017.
[10]台一鸿,石良.功能性低聚糖的生理功能及应用研究进展[J].食品安全导刊,2019(12):175-177,183.
[11]张成楠,李秀婷.功能性低聚糖作用于肠道菌群抑制肥胖的研究进展[J].中国食品学报,2019,19(12):277-283.
[12]刘月,祁国栋,张炳文.黄酒功能成分的研究进展[J].中国酿造,2015,34(11):27-30.
[13]苏红玉.产普鲁兰酶菌株的筛选、基因克隆表达及酶学性质研究[D].广州:华南理工大学,2019.
[14]姜欢.4-α-葡萄糖基转移酶、分支酶对淀粉的改性作用研究[D].无锡:江南大学,2014.
[15]LI X F,MIAO M,JIANG H,et al.Partial branching enzyme treatment increases the low glycaemic property and alpha-1,6 branching ratio of maize starch[J].Food Chem,2014,164:502-509.
[16]陈琛.分支酶修饰蜡质大米淀粉结构与性质研究[D].无锡:江南大学,2019.
[17]王伟旭.基于麦麸阿拉伯木聚糖碱酶法联用制备低聚木糖的研究[D].长春:吉林农业大学,2017.
[18]彭昭君.小麦芽木聚糖内切酶的纯化鉴定及对小麦源阿拉伯木聚糖的降解特性[D].泰安:山东农业大学,2020.
[19]郭萌萌.阿拉伯木聚糖在啤酒酿造中的变化[D].泰安:山东农业大学,2014.
[20]雷钊,尹达菲,袁建敏.阿拉伯木聚糖和阿拉伯低聚木糖的益生功能研究进展[J].动物营养学报,2017,29(2):365-373.
[21]郝希然.小麦麸皮阿魏酰低聚糖的发酵制备工艺及其体外抗氧化活性研究[D].呼和浩特:内蒙古农业大学,2019.
[22]ISHII T.Structure and functions of feruloylated polysaccharides[J].Plant Sci,1997,127(2):111-127.
[23]宋新磊.甘露寡糖和有机硒联合应用对肉鸡的免疫功能及生产性能的影响[D].长春:吉林大学,2018.
[24]陈小瑛.废弃酵母联产甘露寡糖、葡聚糖的研究[D].杭州:浙江工业大学,2017.
[25]宓延红.两种新型甘露聚糖水解酶的生化特征、分子改造与催化特性的研究[D].济南:山东大学,2020.
[26]陈梁城.酵母多糖(β-葡聚糖和甘露寡糖)对动物抗病的调控作用研究[D].长春:吉林农业大学,2015.
[27]李国辉.酵母源甘露寡糖对细菌黏附机制的研究[D].郑州:河南工业大学,2019.
[28]胡贝贞,董文洪,夏碧琪,等.高效阴离子交换色谱-积分脉冲安培检测法同时测定黄酒中的单糖和低聚糖及其指纹图谱的构建[J].色谱,2015,33(6):662-666.
[29]周昕.淀粉酶对大米支链淀粉酶解作用机理的研究[D].合肥:安徽农业大学,2017.
[30]蔡鑫,高慧民,黄琳琳,等.HPLC 法测定闽派黄酒主要功能成分[J].酿酒科技,2014(11):101-103.
[31]BAI W D,FANG X D,ZHAO W H,et al.Determination of oligosaccharides and monosaccharides in Hakka rice wine byprecolumn derivation highperformance liquid chromatography[J].J Food Drug Anal,2015,23(4):645-651.
[32]方晓弟.广东客家娘酒中低聚糖的研究[D].广州:仲恺农业工程学院,2013.
[33] HORTON D.Advances in carbohydrate chemistry and biochemistry[M].US:Elsevier Science&Technology,2009:11-13.
[34]王海松,任鹏飞.不同单糖组成的低聚糖对人肠道菌群的调节作用[J].中国食品学报,2020,20(7):44-52.
[35]BINDELS L B,DELZENNE N M,CANI P D,et al.Towards a more comprehensive concept for prebiotics[J].Nat Rev Gastro Hepat,2015,12(5):303-310.
[36]PEERY A F,DELLON E S,LUND J,et al.Burden of gastrointestinal disease in the United States:2012 Update[J].Gastroenterology,2012,143(5):1125-1126.
[37]RODRIGUEZ R W.Off-label uses of alvimopan and methylnaltrexone[J].Am J Health-Syst Ph,2014,71(17):1450-1455.
[38] HAN S H,HONG K B,KIM E Y,et al.Effect of dual-type oligosaccharides on constipation in loperamide-treated rats[J].Nutr Res Pract,2016,10(6):583-589.
[39]操然.低聚糖生理功能及其提取技术的研究进展[J].中国野生植物资源,2015,34(4):33-37.
[40]刘重慧,张静,范誉川,等.低聚异麦芽糖调节肠道菌群及润肠通便作用的研究[J].食品工业科技,2018,39(7):298-302.
[41]任红立,汪晶晶,宋建楼,等.功能性低聚糖的研究进展[J].饲料博览,2016(4):35-39.
[42]王琳琳.双歧杆菌对便秘的影响及其作用机理研究[D].无锡:江南大学,2017.
[43] SU H,CHEN J H,MIAO S,et al.Lotus seed oligosaccharides at various dosages with prebiotic activity regulate gut microbiota and relieve constipation in mice[J].Food Chem Toxicol,2019,134:110838.
[44] LAN J H,WANG K L,CHEN G Y,et al.Effects of inulin and isomalto-oligosaccharide on diphenoxylate-induced constipation,gastrointestinal motility-related hormones,short-chain fatty acids,and the intestinal flora in rats[J].Food Funct,2020,11(10):9216-9225.
[45]LIU X Y,CHEN S,YAN Q J,et al.Effect of Konjac mannan oligosaccharides on diphenoxylate-induced constipation in mice[J]. J Funct Foods,2019,57:399-407.
[46]WANG L L,HU L J,YAN S,et al.Effects of different oligosaccharides at various dosages on the composition of gut microbiota and short-chain fatty acids in mice with constipation[J].Food Funct,2017,8(5):1966-1978.
[47]KACZMAREK J L,THOMPSON S V,HOLSCHER H D.Complex interactions of circadian rhythms,eating behaviors,and the gastrointestinal microbiota and their potential impact on health[J].Nutr Rev,2017,75(9):673-682.
[48] RIVIERE A,SELAK M,LANTIN D,et al.Bifidobacteria and butyrateproducing colon bacteria:Importance and strategies for their stimulation in the human gut[J].Front Microbiol,2016,7:979.
[49]HUANG L L,CHEN J,CAO P Q,et al.Anti-obese effect of glucosamine and chitosan oligosaccharide in high-fat diet-induced obese rats[J].Mar Drugs,2015,13(5):2732-2756.
[50]ZHENG J P,YUAN X B,CHENG G,et al.Chitosan oligosaccharides improve the disturbance in glucose metabolism and reverse the dysbiosis of gut microbiota in diabetic mice[J].Carbohyd Polym,2018,190:77-86.
[51]陈国旺.谷氨酰胺和低聚异麦芽糖对断奶仔猪免疫机能及小肠功能的影响[D].大庆:黑龙江八一农垦大学,2016.
[52] LI S Y,WANG L N,LIU B,et al.Unsaturated alginate oligosaccharides attenuated obesity-related metabolic abnormalities by modulating gut microbiota in high-fat-diet mice[J].Food Funct,2020,11(5):4773-4784.
[53] CSERNUS B,CZEGLEDI L.Physiological,antimicrobial,intestine morphological,and immunological effects of fructooligosaccharides in pigs[J].Arch Anim Breed,2020,63(2):325-335.
[54]SULIGOJ T,VIGSNAES L K,ABBEELE P V D,et al.Effects of human milk oligosaccharides on the adult gut microbiota and barrier function[J].Nutrients,2020,12(9):2808.
[55]XIONG B H,LIU M,ZHANG C,et al.Alginate oligosaccharides enhance small intestine cell integrity and migration ability[J]. Life Sci,2020,258:118085.
[56]K-DA S,PEERAKIETKHAJORN S,SIRINGORINGO B,et al.Oligosaccharides from Gracilaria fisheri ameliorate gastrointestinal dysmotility and gut dysbiosis in colitis mice[J].J Funct Foods,2020,71:104021.
[57]HE N N,WANG S,LV Z Y,et al.Low molecular weight chitosan oligosaccharides (LMW-COSs) prevent obesity-related metabolic abnormalities in association with the modification of gut microbiota in high-fat diet(HFD)-fed mice[J].Food Funct,2020,12(6):510-518.
[58]李虎.芭蕉芋淀粉酶法制备低聚异麦芽糖和磷酸寡糖的研究[D].上海:上海交通大学,2014.
[59]FEI Y Q,WANG Y,PANG Y L,et al.Xylooligosaccharide modulates gut microbiota and alleviates colonic inflammation caused by high fat diet induced obesity[J].Front Physiol,2019,10:1601.
[60] YAN S K,SHI R J,LI L,et al.Mannan oligosaccharide suppresses lipid accumulation and appetite in western-diet-induced obese mice via reshaping gut microbiome and enhancing short-chain fatty acids production[J]. Mol Nutr Food Res,2019,63(23):1900521.
[61]李浩霞,周中凯,商文婷,等.魔芋葡甘低聚糖对肥胖大鼠高脂血症及肝损伤的调节作用[J].中国食品学报,2020,20(6):81-87.