羧肽酶(carboxypeptidases,CPs)是指能专一催化水解多肽链羧基末端氨基酸的一类外肽酶,是一种具有重要应用潜力的工业酶制剂。羧肽酶的应用主要涉及到生物、化学、医学等多个学科领域。在食品和饲料工业,可用于制备高F值寡肽[3],去除赭曲霉素[4],多肽脱苦、生物活性多肽的延长或特异性修饰[5];在生物学领域,可用于多肽的合成[6]及多肽氨基酸序列测定[7];在医学用途方面,通过体内羧肽酶的检测达到诊断和治疗疾病的目的[8-9]。近几年,羧肽酶的新功能和新用途不断被发现和拓展,使得羧肽酶具有更高的研究价值和更广阔的应用前景。
目前,羧肽酶酶制剂商品供应主要来源于猪胰腺,但价格昂贵[10-11]。因此,利用微生物获得大量的羧肽酶,具有重要的现实意义[12-13]。黑曲霉(Aspergillus niger)是国际上公认的安全发酵微生物,且适合采用固态发酵的方式[14],而黑曲霉生产羧肽酶发酵工艺条件鲜见报道[15]。本研究是在前期筛选分离纯化获得的羧肽酶活力较高的黑曲霉(Aspergillus niger)H1-6的基础上,利用固态发酵技术,优化其产酶发酵工艺参数,并考察发酵粗酶液在酱油酿造发酵中的应用效果,为实现羧肽酶的规模化生产、降低成本来满足商业化的需要,对推动我国相关产业发展具有重要意义。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
黑曲霉(Aspergillus niger)H1-6:本实验室筛选获得,马铃薯培养基斜面保藏于4 ℃冰箱。
1.1.2 化学试剂
碳源(麸皮、玉米芯粉、甘蔗渣、米糠)、氮源(豆粕、花生粕、菜籽油饼、玉米粉):市售;羧肽酶底物(N-苄氧羰酰基-L-苯丙氨酰-L-亮氨酸(N-carbobenzyloxy-L-phenylalanyl-L-leucine,N-CBZ-Phe-Leu)):美国Sigma-Aldrich公司。其他试剂均为国产分析纯。
1.1.3 培养基
斜面培养基:马铃薯葡萄糖琼脂(potato dextrose agar,PDA)培养基,称取PDA培养基干粉39 g,加入蒸馏水或去离子水1 000 mL,搅拌加热煮沸至完全溶解,121 ℃高压灭菌15 min。
固体发酵培养基:称取一定量的碳源、氮源和无机盐,加水,121 ℃高压灭菌20 min。
1.2 仪器与设备
SW-CJ-ZFD型双人单面净化工作台:苏州净化设备有限公司;DHP-9162型电热恒温培养箱:上海博迅实业有限公司;722N型可见分光光度计:上海精密科学仪器有限公司。
1.3 方法
1.3.1 菌株的活化
将黑曲霉菌株H1-6接种于PDA培养基进行活化,30 ℃培养3~4 d,待长满孢子后备用。
1.3.2 单孢子悬液的制备
取培养好的PDA斜面,加入无菌生理盐水,用接种环刮下黑曲霉菌株H1-6孢子后转移至装有玻璃珠的无菌锥形瓶中,充分摇动使孢子散开,将孢子浓度调整到1×108CFU/mL,备用[16]。
1.3.3 固态发酵培养
500 mL三角瓶装100 g固态发酵培养基,固态培养基的具体配方根据单因素试验和响应面分析试验设计,通过添加1 mol/L HCl或NaOH水溶液来调节培养基的初始pH值,然后121 ℃高压灭菌20 min,待培养基冷却到室温(20~25)℃,按培养基质量的比例接种孢子悬液(1×108CFU/mL),在32 ℃条件下,恒温培养3 d后获得成曲,培养期每天翻曲2次。试验平行3次[17],结果取平均值。
1.3.4 粗酶液的制备
参考文献[16],并略作修改。分别称取10 g成曲,研磨后加入100 mL无菌水,40 ℃浸提1 h,期间搅拌2~3次。用中速定性滤纸过滤,滤液即为粗酶液。同时测定曲料水分,酶活力用曲料干基质量表示,即mU/g[18]。
1.3.5 羧肽酶活力的测定方法
采用镉-茚三酮法测定羧肽酶的活力[19]。羧肽酶酶活定义:在30 ℃,pH 3.7的条件下,每秒钟产生1 mmol的酪氨酸所需的酶量为一个酶活单位(mU)。
1.3.6 羧肽酶粗酶液在酱油酿造中的应用
结合固态发酵培养条件试验结果,添加0~2.5 U/kg成曲羧肽酶,采用高盐稀态发酵法酿造酱油,在成曲加18%盐水前,先将羧肽酶粗酶液溶解到盐水中,发酵后压榨出油检测氨基态氮含量[20]。
1.3.7 产酶条件优化单因素试验
按100 g固体发酵培养基,分别称取45%碳源(麸皮、玉米芯、米糠及甘蔗渣),45%氮源(豆粕、花生粕、玉米粉及油菜籽粉),10%无机盐(K2PO3、MgSO4、MnSO4·H2O、FeCl3·H2O和CaCl2),分别按40%、45%、50%、55%和60%加入蒸馏水,置于500 mL三角瓶,调节培养基的初始pH值分别至5.0、5.5、6.0、6.5和7.0,121 ℃灭菌20 min,待培养基冷却,按培养基质量的比例接种黑曲霉菌株H1-6孢子悬液(1×108 CFU/mL)0.5%、1.0%、1.5%和2.0%,在32 ℃条件下,恒温培养3 d获得成曲,成曲按照方法1.3.4提取粗酶液并按照1.3.5方法测定羧肽酶活力。所有的试验平行3次[17],结果取平均值。
1.3.8 产酶条件优化响应面试验
(1)Plackett-Burman(PB)试验设计
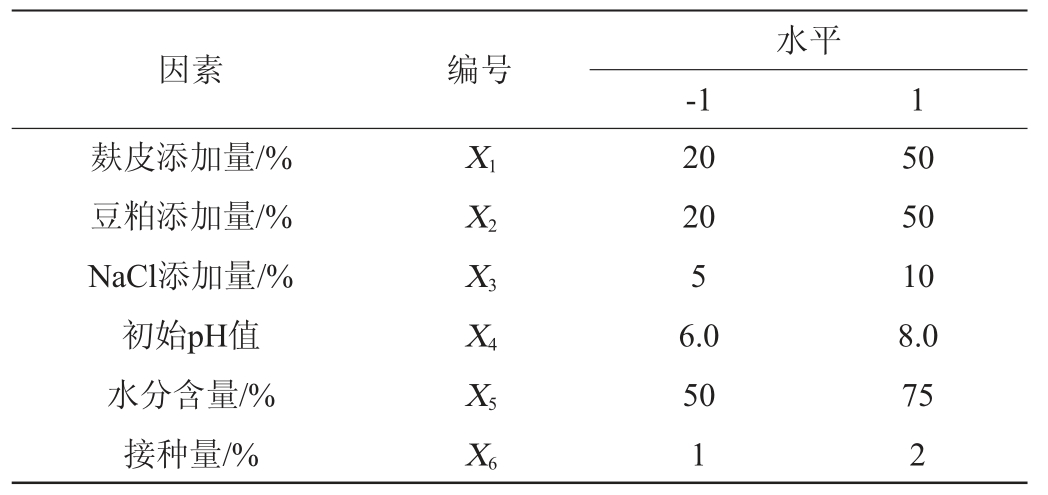
在单因素试验结果的基础上,以羧肽酶酶活为响应值,利用PB试验分析麸皮添加量(X1)、豆粕添加量(X2)、NaCl添加量(X3)、初始pH值(X4)、水分含量(X5)、接种量(X6)等6个因素,每个因素取2个水平,PB试验设计因素与水平见表1。
表1 Plackett-Burman试验设计因素与水平
Table 1 Factors and levels of Plackett-Burman tests design
(2)最陡爬坡试验
依据PB试验结果,以各个显著影响因素效应的大小设定变化步长;依据变化的梯度方向确定爬坡方向,快速逼近最佳值区域;确定主要影响因素为麸皮添加量、水分含量和接种量,将此3个因素进行最陡爬坡试验。
(3)Box-Behnken 试验设计
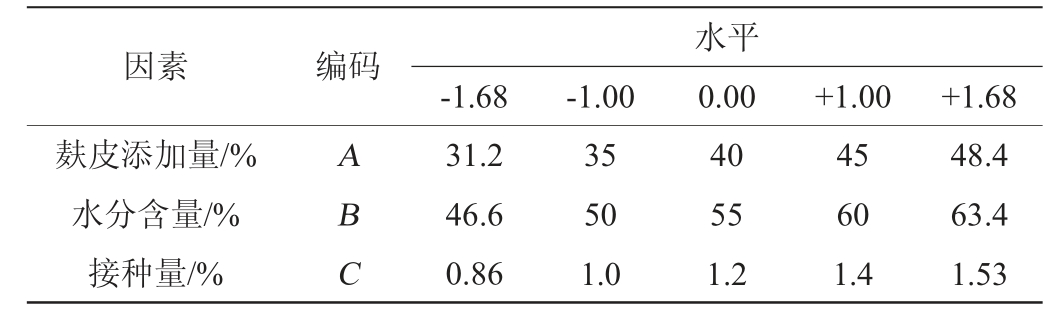
根据Box-Behnken 试验设计原理(中心组合试验设计原理),进行3因素3水平15个试验组的响应面试验,分析每个因素主效应与交互效应,绘制响应曲面,求出最佳值,获得最佳产酶条件。以羧肽酶酶活力(Y)为响应值,优化麸皮添加量(A)、水分含量(B)和接种量(C),Box-Behnken试验设计因素与水平见表2。
表2 Box-Benhnken试验设计因素及水平
Table 2 Factors and levels of Box-Benhnken tests design
1.3.9 数据处理
所有试验结果以“平均值±标准偏差”形式表示。利用SPSS 22.0软件进行方差分析(analysis of variance,ANONA)检验,P<0.05表示差异显著,P<0.01表示差异极显著。采用Design-Expert 8.0.7软件进行响应面试验数据分析[21]。
2 结果与分析
2.1 产酶条件优化单因素试验
由表3可知,当碳源为麸皮时,羧肽酶的固态发酵酶活力最高(640±32)mU/g,其他依次为玉米芯粉、米糠和甘蔗渣;当氮源为豆粕时,羧肽酶的酶活力最高(703±11)mU/g,其他依次为花生粕、玉米粉和菜籽油饼;无机盐中的NaCl对羧肽酶的固态发酵酶活力有正相关性,其他的K2PO3、MgSO4、MnSO4·H2O、FeCl3·H2O和CaCl2则没有影响;黑曲霉接种量为1.0%时,羧肽酶的固态发酵酶活力达到最高(746±22)mU/g;初始pH值为6.5时,羧肽酶的固态发酵酶活力最高(773±16)mU/g;水分含量为55%时,羧肽酶的固态发酵酶活力最高(826±23)mU/g。
表3 产酶条件优化单因素试验结果
Table 3 Results of single factor tests for optimization of enzymeproduction conditions
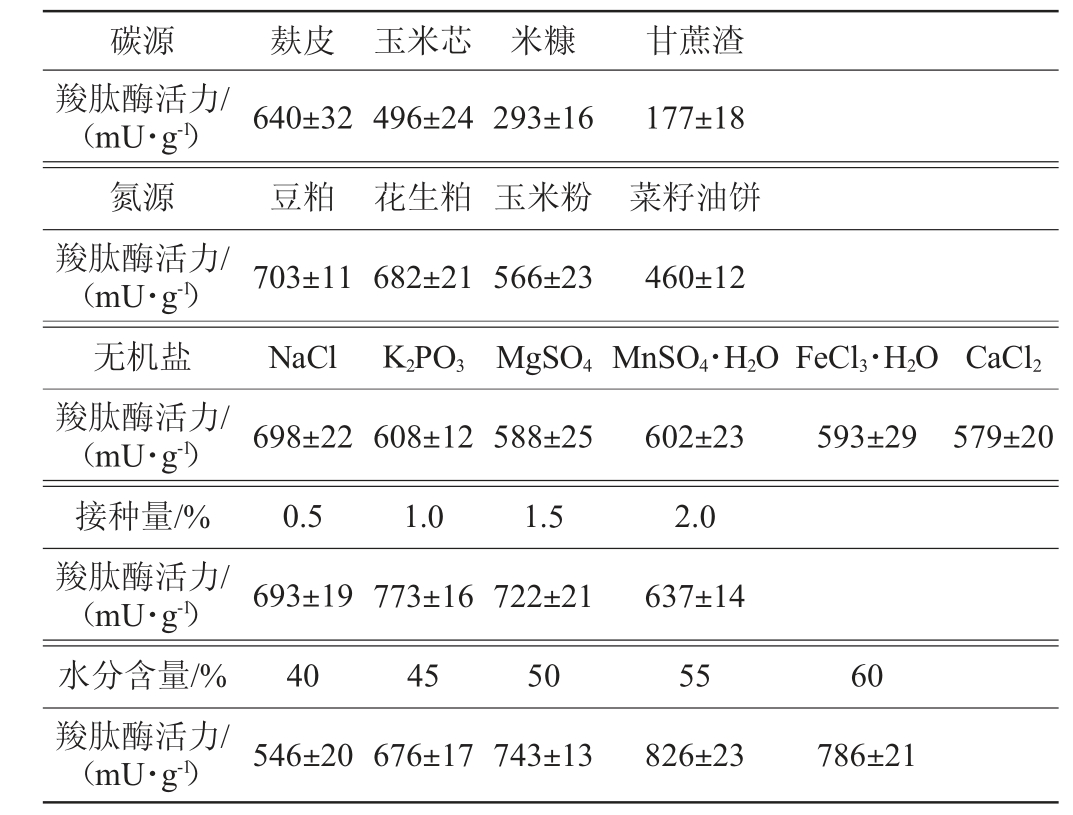
因此,选用麸皮为碳源,添加量为45%;豆粕为氮源,添加量为45%;氯化钠为无机盐,添加量为10%,并调节初始pH值为6.5、黑曲霉H1-6接种量为1.0%,水分含量为55%。
2.2 Plackett-Burman试验设计及结果
在上述单因素试验结果的基础上,以羧肽酶酶活为响应值,利用Plackett-Burman试验设计分析麸皮添加量(X1)、豆粕添加量(X2)、NaCl添加量(X3)、初始pH值(X4)、水分含量(X5)、接种量(X6)等6个因素的显著性,每个因素取2个水平,每个试验重复3次。为了估计试验误差,另设3个虚拟变量。PB试验设计及结果见表4,方差分析见表5。
表4 Plackett-Burman 试验设计及结果
Table 4 Design and results of Plackett-Burman tests
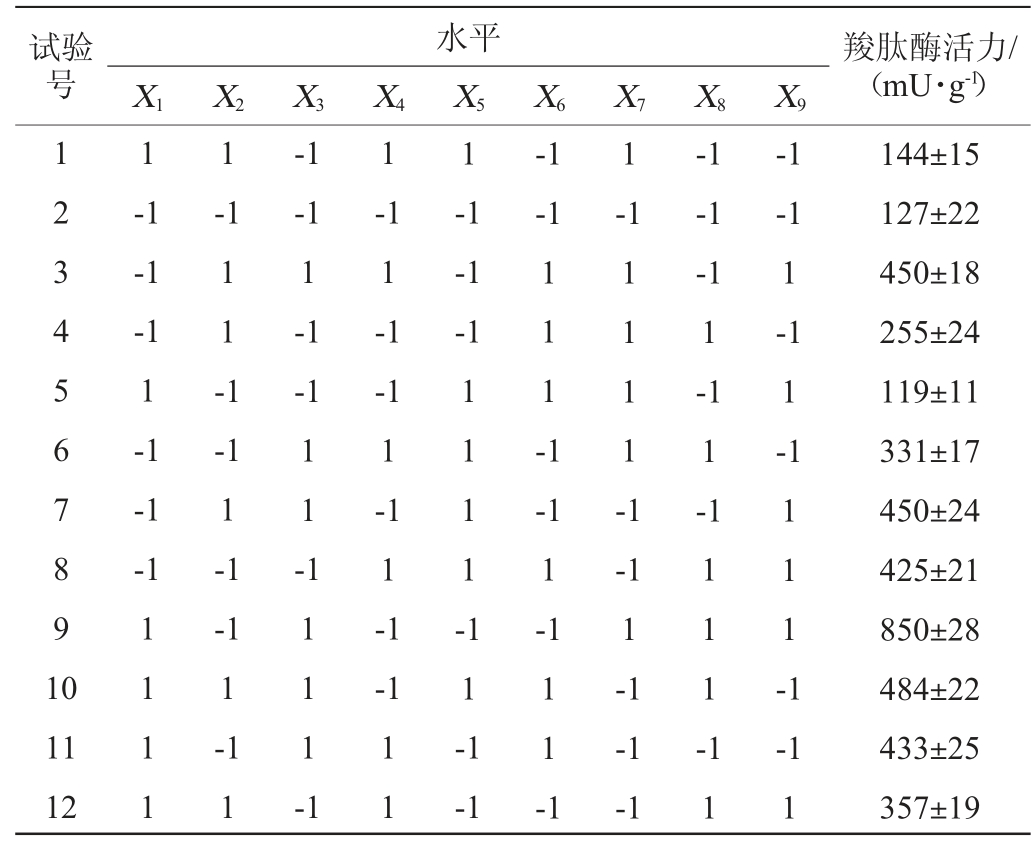
表5 Plackett-Burman试验结果方差分析
Table 5 Variance analysis of Plackett-Burman tests results
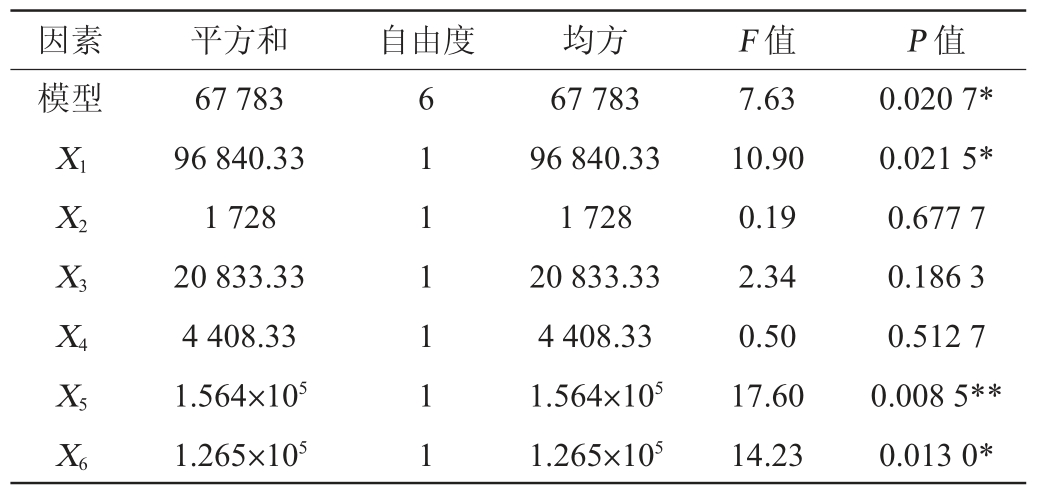
注:“*”表示对结果影响显著(P<0.05);“**”表示对结果影响极显著(P<0.01)。
由表5可知,此模型P=0.020 7<0.05,说明回归方程显著;该模型的决定系数R2为0.9015,调整决定系数R2为0.7833,表明多项式模型拟合较好。影响黑曲霉H1-6固态发酵产羧肽酶的显著因素分别是麸皮添加量X1(P=0.021 5)、水分含量X5(P=0.008 5)和接种量X6(P=0.013 0),P值均<0.05,可以作为进一步优化的因素,其他因素对结果影响不大,在下一步研究中,取中间值。因此,选用麸皮添加量、水分含量以及黑曲霉H1-6接种量作为最陡爬坡试验因素。
2.3 最陡爬坡试验结果
根据Plackett-Burman试验结果确定的3个主要显著因素,其中麸皮添加量(A)对酶活力表现为正效应,水分含量(B)和黑曲霉H1-6接种量(C)对酶活力表现为负效应,根据这3个显著影响因素效应的大小确定试验的爬坡方向和变化步长,以最快的速度逼近最大响应值(酶活力)的区域[22]。其余因素则依据效应关系,分别选择对应的水平[23]。最陡爬坡试验设计与结果见表6。
表6 最陡爬坡试验设计和结果
Table 6 Design and results of the steepest ascent tests
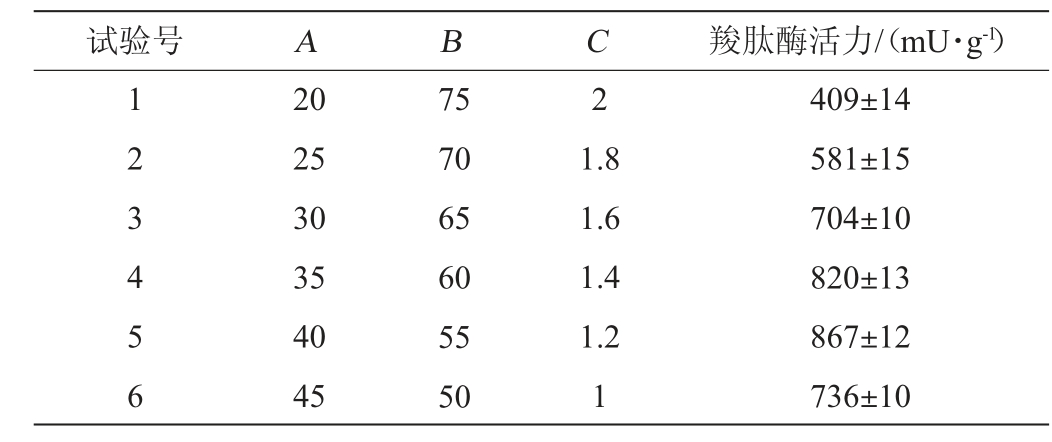
由表6可知,随着3个主要影响因素含量的变化,羧肽酶活力呈现先升高后降低,羧肽酶活力在试验第5组的条件下,羧肽酶活力最高(867±12)mU/g。因此,选择试验第5组的条件作为响应面设计因素水平的中心点,即麸皮添加量(A)、水分含量(B)和接种量(C)分别为40%、55%和1.2%。
2.4 响应面法优化试验结果
根据Box-Behnken 试验设计原理(中心组合试验设计原理),设计3因素5水平共20个试验点的响应面分析试验,其中有14个析因点,6个零点重复,以羧肽酶酶活力(Y)为响应值,以估计试验误差,分析黑曲霉H1-6固态发酵羧肽酶活力的最佳条件。Box-Behnken试验设计与结果见表7,方差分析结果见表8。
表7 Box-Behnken试验设计与结果
Table 7 Design and results of Box-Behnken tests
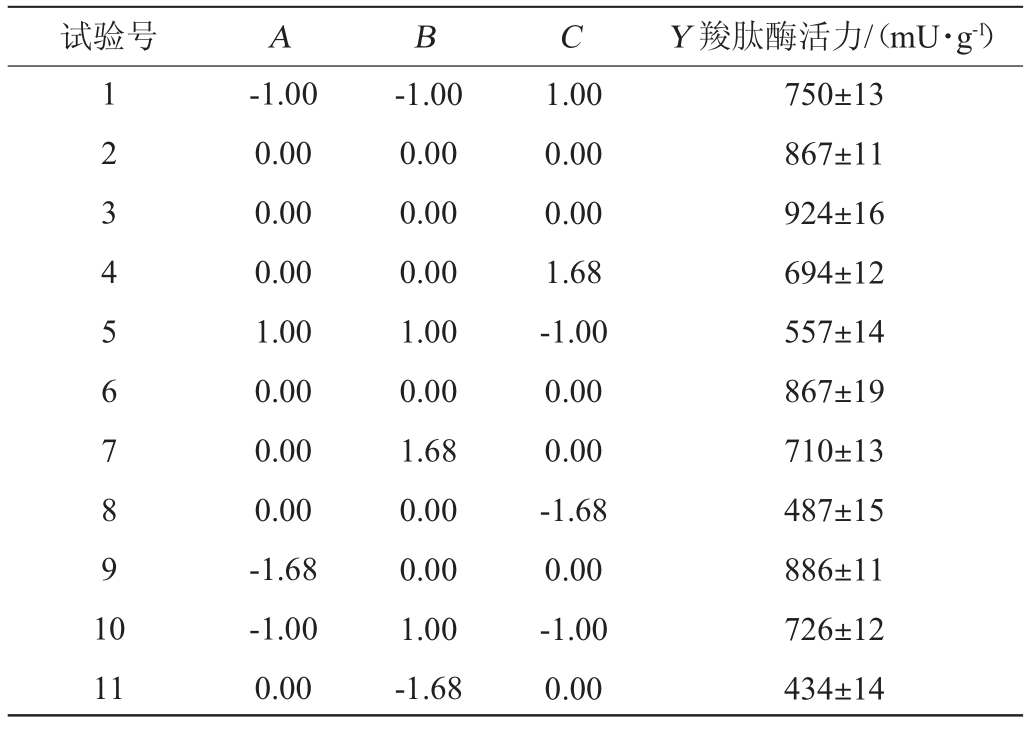
续表
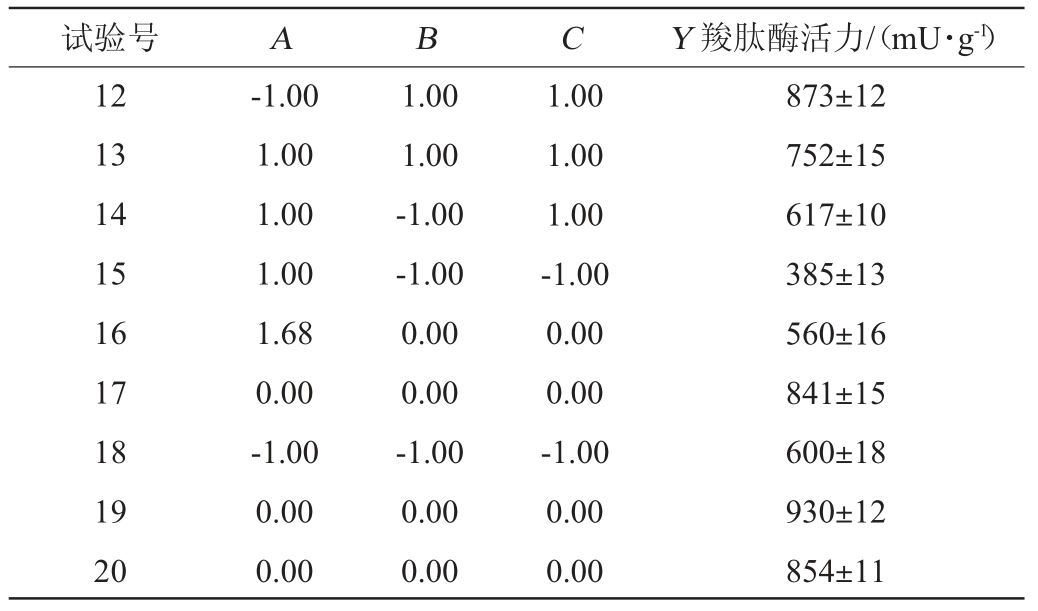
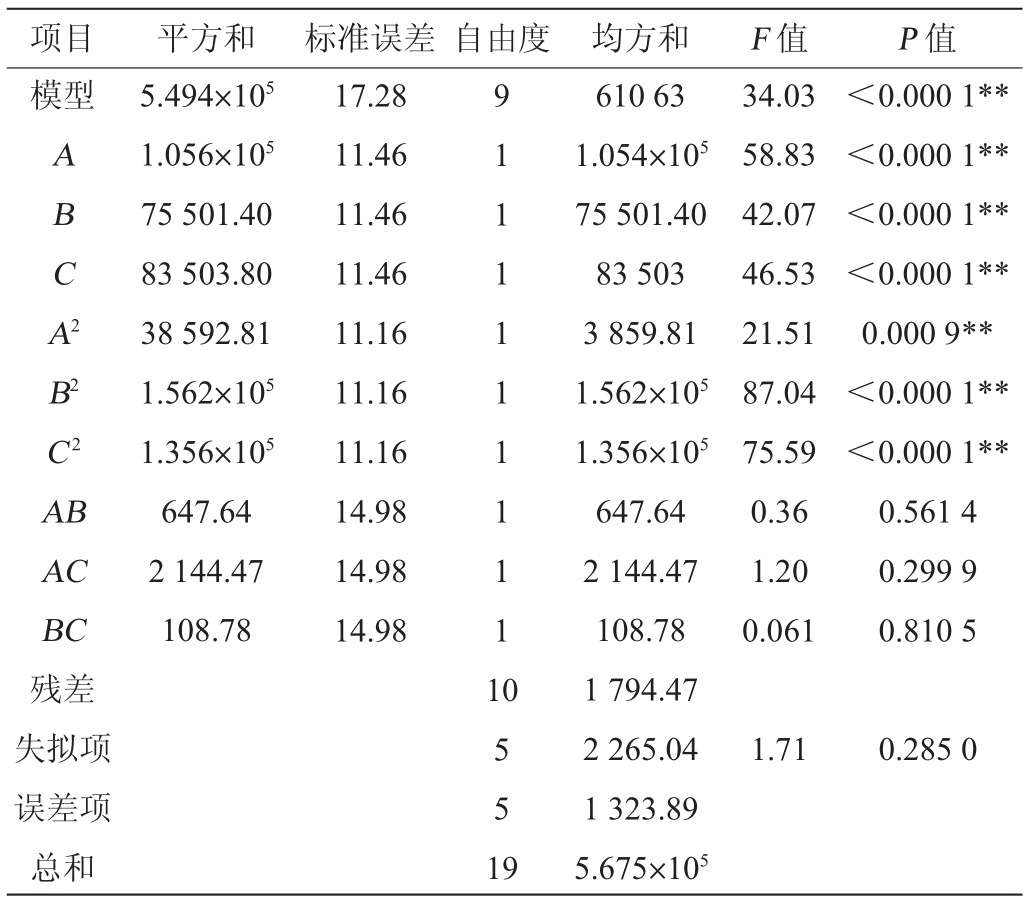
表8 回归模型的方差分析
Table 8 Variance analysis of regression model
以羧肽酶活力为响应值,运用Design-Expert 8.0.7软件进行回归拟合,得到酶活力(Y)与麸皮含量(A)、含水量(B)与接种量(C)的二次多项回归方程:
由表7可以看出,在α=0.01水平时,H1-6菌株产羧肽酶响应面试验模型回归极显著(P<0.000 1),并且失拟项不显著(P=0.285 0>0.05),表明该方程对试验数据拟合良好。该模型决定系数R2=0.968 4,说明96.84%的试验数据可用该模型解释,调整决定系数R2Adj=0.939 9,证明该模型可以很好的拟合试验数据。根据各因素P值大小,一次项A、B、C,二次项A2、B2、C2对羧肽酶活力影响极显著(P<0.01)。
根据Box-Behnken试验结果,应用Design-Expert 8.0.7软件对数据进行分析拟合,得到各因素交互作用对羧肽酶活力影响的响应面及等高线见图1。由图1可知,麸皮添加量(A)、水分含量(B)和接种量(C)3个因素之间互有交互作用,但对结果均无显著影响(P>0.05)。
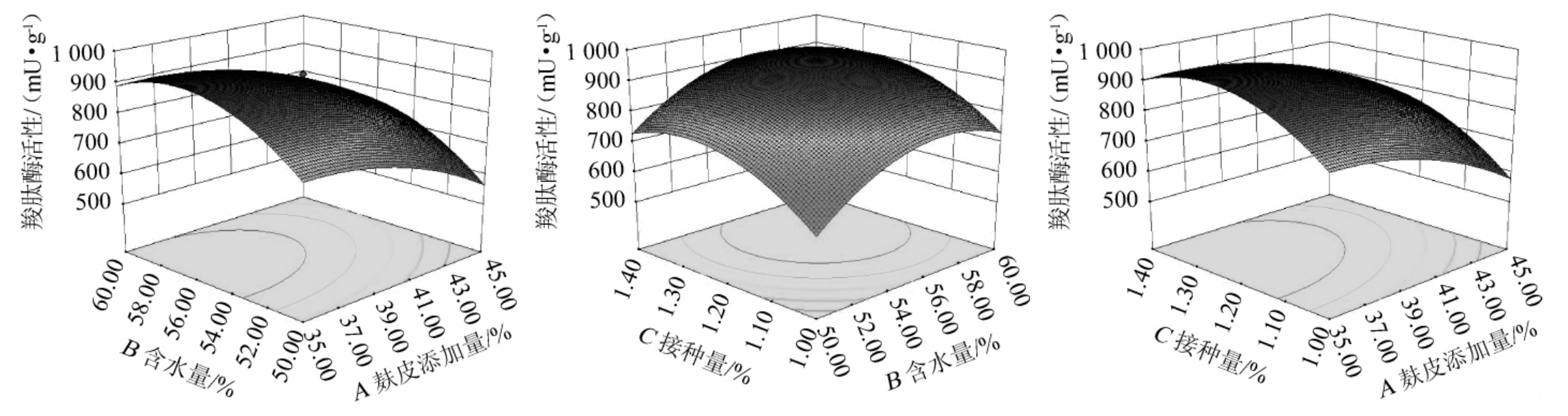
图1 麸皮添加量、含水量及接种量对黑曲霉H1-6固态发酵产羧肽酶活力的响应面及等高线
Fig.1 Response surface polts and contour lines for effects of interaction between bran addition,moisture and inoculum on carboxypeptidase activity produced by Aspergillus niger H1-6 with solid-state fermentation
2.5 响应面验证试验
为了验证该模型预测的可靠性与准确性,通过单因素试验与响应面试验最优产酶条件为:得到A=-0.769、B=0.318、C=0.331,即麸皮添加量为36.16%,水分含量为56.59%,接种量为1.27%。此条件下模型预测的羧肽酶活力理论值为950.39 mU/g。考虑到实际操作的便利性,将最优产酶条件修正为:麸皮添加量为36%,含水量为56.6%,接种量为1.3%(即1.3×106 CFU/g)。在此优化条件下,制曲培养3 d,测定成曲中羧肽酶活力,3次平行试验羧肽酶活力实际值为938.33 mU/g,与预测值接近,说明实验值与预测值有较好的拟合性,所得产酶条件可以用于指导实际发酵。
2.6 羧肽酶在酱油酿造中的添加量试验
氨基酸态氮含量指的是以氨基酸形式存在的氮元素的含量,酱油中的香味就是各种氨基酸的自然效果,该指标越高,说明酱油中氨基酸含量越高,鲜味越好[24]。已经证实羧肽酶能够水解多肽和蛋白质C端的氨基酸,应用于氨基酸生产以及食品工业中的脱苦和风味提升等方面[25]。因此,将不同添加量的羧肽酶添加到发酵酱醪中,然后进行发酵、压榨出油检测,不同羧肽酶添加量对酱油中氨基态氮含量的影响结果见图2。
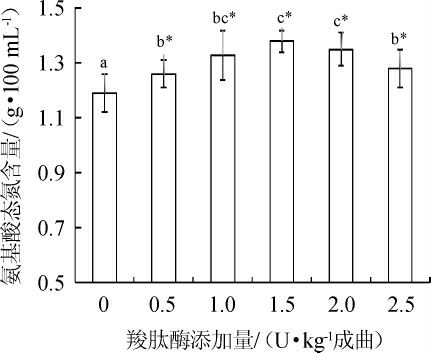
图2 不同羧肽酶添加量对酱油中氨基酸态氮含量的影响
Fig.2 Effect of different carboxypeptidase addition on amino nitrogen contents in soy sauce
由图2可知,与对照样品相比较,添加0~2.5 U/kg成曲的羧肽酶粗酶液后氨基态氮都有所提高,这可能是添加羧肽酶后,酱醪中更多的多肽被水解成氨基酸。此外,随着羧肽酶添加量的增加,氨基态氮含量显著增加,但羧肽酶添加量到一定程度(1.5 U/kg成曲),氨基态氮含量增加不显著。因此建议羧肽酶的添加量控制在1.5 U/kg成曲。
3 结论
本研究考察了不同碳源、氮源、初始pH值、多种无机盐、水分含量及接种量对黑曲霉H1-6固态发酵产羧肽酶的影响。在单因素试验及Plackett-Burman试验的基础上,采用中心组合响应面法对产酶条件进行优化,并建立了酶活力与麸皮、水分含量及接种量之间的二次多项回归模型,得出最优发酵条件为:麸皮添加量36%,豆粕添加量50%、NaCl添加量10%、初始pH值为6.0、含水量56.6%,接种量为1.3%(即1.3×106 CFU/g)。在此优化条件下,羧肽酶的酶活力达到938.33 mU/g。在最优发酵条件下获得的发酵羧肽酶粗酶液添加到酱油酿造中,能有效提高酱油中氨基态氮的含量,进而提高其鲜味,并且最佳添加量为1.5 U/kg成曲。该研究结果为羧肽酶生产应用的研究提供实验基础。下一步研究将继续在合适的生物反应器进行放大试验生产,以促进羧肽酶固态发酵生产实现工业化。
[1]吴静,闵柔,邬敏辰,等.羧肽酶研究进展[J].食品与生物技术学报,2012,31(8):793-801.
[2]叶玲飞,罗光宇,向建华,等.丝氨酸羧肽酶及其类蛋白的研究进展[J].植物生理学报,2013,49(2):122-126.
[3] PEDROCHE J,YUST-MDEL M,LQARI H,et al.Production of Brassica carinata protein hydrolyzates with a high Fisher's ratio using immobilized proteases[J].J Agric Food Chem,2006,54:7621-7627.
[4] ABRUMBOSA L,VENANCIO A.Isolation and purification of an enzyme hydrolyzing ochratoxin A from Aspergillus niger[J].Biotechnol Lett,2007,29(3):1909-1914.
[5]LIU F,YASUDA M.Debittering effect of Monascus carboxypeptidase during the hydrolysis of soybean protein[J].J Ind Microbiol Biotechnol,2005,32(2):487-489.
[6]高彦飞,王红霞.蛋白质及多肽C 段测序的研究进展[J].分析化学评述与进展,2007,35(4):1820-1826.
[7]余先红,汪晓娟,钟星,等.耐热羧肽酶Taq 基因在毕赤酵母中的表达[J].生物工程学报,2014,30(11):1791-1795.
[8]TOPILOW A A,DAVIS J M,VERNICK J J,et al.Confirmation of a potential biomarker for early-stage pancreatic cancer[J].Cancer Biomark,2012,10(1):27-33.
[9]JAMIN Y,SMYTH L,ROBINSON S P,et al.Noninvasive detection of carboxypeptidase G2 activity in vivo[J].NMR Biomed,2011,24(3):343-350.
[10]冯红霞.羧肽酶菌株的筛选及其酶的分离纯化、酶学性质的研究[D].南京:南京农业大学,2002.
[11]闵柔,黄芳,曾妍,等.宇佐美曲霉羧肽酶成熟肽基因的表达及鉴定[J].中国生物制品学杂质,2013,26(3):176-180.
[12]陈丹.米曲霉羧肽酶O 在毕赤酵母中的表达鉴定及其脱苦效应的研究[D].广州:华南理工大学,2014.
[13]张欢欢.在毕赤酵母中过量表达来源于雅致放射毛霉的羧肽酶Y[D].无锡:江南大学,2018.
[14]张忠平,杨旭.黑曲霉WS003 固态发酵制备果胶酶条件的优化[J].中国调味品,2017,42(9):58-60.
[15] SHANKAR S K,MULIMANI V H.α-Galactosidase production by Aspergillus oryzae in solid-state fermentation[J].Bioresource Technol,2007,98(8):958-961.
[16]高大响,黄小忠.1 株黑曲霉固态发酵豆渣生产纤维素酶及淀粉酶工艺的优化[J].江苏农业科学,2017,45(22):218-220.
[17]朱强,王瑞鑫,吴铖迪,等.黑曲霉SP7-2 固态发酵产生淀粉糖化酶工艺优化[J].发酵与食品工业,2019,45(8):98-102.
[18]叶茂,邓毛程,张远平,等.小麦粒度对酱油制曲和酱油质量的影响[J].食品与发酵工业,2014,40(3):149-151.
[19]付静,杨媚,李理,等.雅致放射毛霉3.2778 羧肽酶性质及其活性中心结构的研究[J].中国酿造,2010,216(3):30-33.
[20]叶茂,邓毛程,顾宗珠,等.一种耐盐性酯酶在高盐稀态酱油酿造过程中的应用研究[J].中国调味品,2016,41(11):59-61.
[21]李婷婷,陈雪,程涛,等.基于响应面优化酿酒酵母培养体系[J].中国酿造,2020,39(11):126-131.
[22]胡娜,吴鑫颖,邱树毅,等.利用黑曲霉B1401 发酵废弃茶末浸提液产单宁酶的工艺优化[J].食品工业科技,2018,39(15):205-212.
[23]金伟,聂光军,王丽,等.黑曲霉固态发酵生产单宁酶的条件优化[J].生物加工过程,2013,11(3):7-12.
[24]包启安.酱油科学与酿造技术[M].北京:中国轻工业出版社,2011:203-210.
[25] PINTO G A,TARDIOLI P W,CABRERA-PADILLA R Y,et al.Amino acids yields during proteolysis catalyzed by carboxypeptidase A are strongly dependent on substrate pre-hydrolysis[J].Biochem Eng J,2008,39(5):328-337.