高粱(Sorghum bicolor L.)是禾本科、高粱属植物,是我国白酒酿造的主要原料[1],红缨子高粱是国酒茅台酿造用的唯一有机高粱品种,具有淀粉含量高、纤维层粗厚、耐蒸煮等特性,非常适用于茅台酒的酿造[2]。然而,红缨子是茅台镇特产的一种有机糯高粱,异地生长的红缨子其品质和特性与茅台镇相比有一定差距。土壤是植物赖以生存的根本,健康的土壤是保证粮食安全的关键[3],土壤健康一般通过物理、化学和生物学指标来衡量[4],其中微生物的组成、结构、功能就是一项非常重要的指标[5-6]。土壤中存在着地球上种类最为丰富的细菌、古菌、真菌、病毒等微生物群落[7],土壤微生物的存在影响土壤有机质的合成以及营养物质的转化,直接影响植物的生长[8-9]。
土壤微生物与植物有着协同进化的关系,一方面植物为微生物提供生长所需营养物质,另一方面土壤微生物将有机物转化为无机物供植物生长吸收[10]。同时,根际土壤微生物可作为抵御病原菌侵入植物根系的第一道防线[11],提升土传病害的根际免疫[12-13]。土壤细菌占土壤微生物的70%~90%,是土壤中分布最广、含量最多,丰富度最高的一类,能够有效促进有机质的分解及营养元素的释放[14]。根际是植物-土壤-微生物相互作用的中心[15],根际微生物具有分解植物根际有机质、固定氮元素、进行养分转化等功能,在植物生长发育过程中发挥着极为重要的作用[16]。因此,推测茅台镇特产的有机高粱红缨子,其特有的品质离不开其根际细菌的分布和组成。目前,针对酿酒高粱根际微生态特征的研究相对较少,且研究技术不够先进,深度不够,特别是针对茅台镇优质酿酒高粱根际细菌群落特征的研究几乎空白。
高通量测序技术是对传统测序的一次革命性改变,能够一次对几十万到几百万条脱氧核糖核酸(deoxyribonucleic acid,DNA)分子进行序列测定,具有自动化、通量高、成本低等特点,该技术的出现加速了微生物生态学的发展,它能在整体水平上破译原位复杂环境中土壤微生物群落多样性[10,17]。因此,本研究旨在通过高通量测序技术分析茅台镇及其周边地区所种植的红缨子高粱根际细菌群落特征,这样能够全面获得高粱根际微生物类群信息,分析茅台镇特有的微生物特征,对深入分析优质高粱的生长环境,从而扩大其生产面积有重要意义。
1 材料与方法
1.1 材料与试剂
红缨子高粱根际土壤:采集于贵州省茅台镇、坛厂镇、鸭溪镇大面积种植的高粱根际土;E.Z.N.A.Soil DNA Kit(D5625-01):美国OMEGA公司;Qubit2.0 DNA检测试剂盒(Q10212):美国Life公司;Taq DNA Polymerase(Ep0406):美国Thermo公司;SanPrep柱式DNA胶回收试剂盒(SK8192):生工生物工程(上海)股份有限公司。
1.2 仪器与设备
Pico-21台式离心机:美国Thermo Fisher公司;GL-88B漩涡混合器:海门市其林贝尔仪器制造有限公司;TND03-H-H混匀型干式恒温器:深圳拓能达科技有限公司;DYY-6C型电泳仪电源、DYCZ-21电泳槽:北京市六一仪器厂;凝胶成像系统:美国UVP公司;T100TM Thermal Cyeler聚合酶链式反应(polymerase chain reaction,PCR)仪:伯乐生命医学产品(上海)有限公司。
1.3 方法
1.3.1 样品的采集
本研究选取的三个样地分别位于贵州省茅台镇、坛厂镇、鸭溪镇,茅台镇是国酒茅台的原产地,位于仁怀市西13 km,海拔575 m,北纬27°51'13.03",东经106°23'3.76";坛厂镇位于仁怀市南部,距茅台镇大约12 km,海拔772 m,北纬27°46'23.10",东经106°21'55.52";鸭溪镇位于遵义市播州区西部,距茅台镇70 km,海拔772 m,北纬27°35'17.12",东经106°41'41.82"。采样时间为2017年7月3日。每个样地设置3块100×100 m 固定实验样地,在每块实验样地中设置5×5 m样方3个,每个样方内随机选取5株高粱,除去高粱根部2 cm表层土,取2~20 cm深的土壤剖面,剪取带有细根的根系,轻轻抖落附在根上的土壤,将剩下的土壤用小刷子刷至无菌自封袋中,贴好标签置于冰盒中带回实验室,保存于-80 ℃箱中用于土壤微生物高通量测序。
1.3.2 土壤微生物的高通量测序
土壤微生物总DNA采用E.Z.N.A.Soil DNA Kit提取,以其为模板PCR扩增细菌16S rRNA V3-V4区基因序列,所用引物为V3-V4通用引物341F(5'-CCCTACACGACGCTCTTCCGATCTG(barcode)CCTACGGGNGGCWGCAG-3')和805R(5'-GACTGGAGTTCCTTGGCACCCGAGAATTCCAGACTACHVGGGTATCTAATCC-3'),引物添加特异Barcode序列标记用于区分不同样品。PCR扩增体系:10×PCR buffer 5 μL,脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTP)(10 mmol/L)0.5 μL,模板DNA 10 ng,正、反向引物(50 μmol/L)各0.5 μL,聚合酶(5 U/μL)0.5 μL,补充双蒸水(ddH2O)至50 μL。PCR扩增条件:94 ℃预变性3 min;94 ℃变性30 s,55 ℃退火30 s,72 ℃延伸30 s,共25个循环,最后72 ℃延伸10 min。PCR扩增产物用2%琼脂糖凝胶电泳检测,采用SanPrep柱式DNA胶回收试剂盒回收PCR扩增产物,委托生工生物工程(上海)股份有限公司进行测序。
1.3.3 数据分析
通过barcode区分样品序列,并对各样本序列进行质量控制(quality control,QC),去除非靶区域序列及嵌合体。基于操作分类单元(operational taxonomic unit,OTU)聚类分析,首先将多条序列根据其序列之间的距离进行聚类,后根据序列之间的相似性作为域值分成操作分类单元(OTU)。利用Mothur软件以及R语言程序包“VennDiagram”分析并绘制韦恩(Venn)图分析统计样本中共有和独有的OTU的数目,直观的展现出环境中样品之间的异同。对处理后序列进行物种分类分析,采用RDP classifier软件,基于伯杰氏细菌分类方法将序列进行域(domain)、门(phylum)、纲(class)、目(order)、科(family)、属(genus)水平物种分类,对每个样本和每个物种单元分类进行序列丰度计算构建样本和物种分类单元序列丰度矩阵,利用SPSS 22.0对不同样地间同一菌群的相对丰度进行方差分析。通过加权Unifrac计算进化树中不同环境样本间Unique branch长度总和,来衡量样本间物种组成的相似度,利用R语言程序包“pheatmap”绘制样本距离热图。
2 结果与分析
2.1 不同样地间高粱根际共有和独有的OTU的数目
通过分析样本中共有和独有的OTU数目绘制Venn图,结果见图1。由图1可知,高粱根际共发现了17 687个细菌OTU,不同样地之间表现为茅台镇(8 241)>坛厂镇(7 482)>鸭溪镇(7 457);三个样地共有OTU为1 352个;茅台镇和坛厂镇共有OTU为2 510个;茅台镇和鸭溪镇共有OTU为2 340个,坛厂镇和鸭溪镇共有OTU为1 995个。结果可以看出不同样地高粱根际细菌物种数量有明显差别,茅台镇细菌OTU数量最多,且独有的OTU最多,说明茅台镇高粱根际细菌物种数最多,且特有细菌种类最多;茅台镇与坛厂镇、茅台镇与鸭溪镇所共有的OTU较坛厂镇与鸭溪镇多,说明茅台镇高粱根际细菌种类在其他样地分布较多。有研究发现,土壤微生物多样性越高,其生态功能、抗环境胁迫和作物生产能力都明显增高[18],可以推测茅台镇高粱根际土壤相较其他样地更健康,更利于植物的生长。
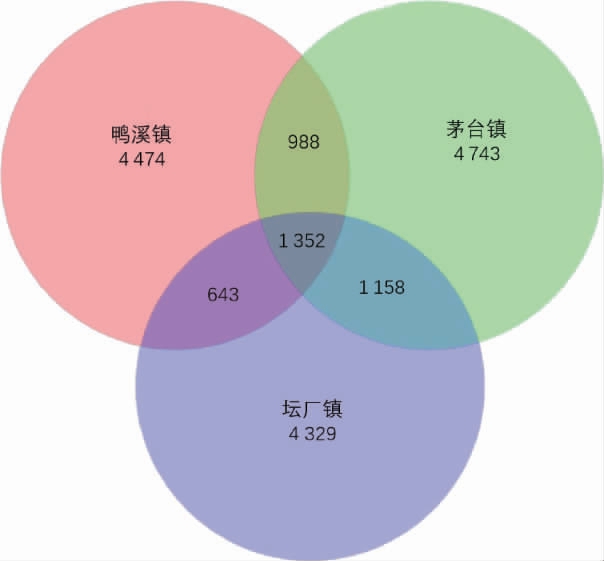
图1 不同样地共有和独有的细菌OTU数量
Fig.1 Numbers of mutual and unique bacterial OTU among different sample plots
2.2 不同样地高粱根际细菌群落结构分析
为解析不同样地高粱根际细菌群落结构特征,对聚类后的OTU代表序列进行物种注释。三个样地高粱根际细菌OUT隶属于25门、55纲、118目、214科、674属。将相对丰度<1%的细菌归于other。基于OTU聚类的结果绘制门水平下细菌菌群分布条形图,结果见图2。由图2可知,在门水平上,三个样地高粱根际细菌群落组成相似,但相对丰度在不同样地间存在较大差异。变形菌门(Proteobacteria)细菌在三个样地高粱根际分布最多,且不同样地间相对丰度差异并不显著,拟杆菌门(Bacteroidetes)细菌在三个样地间分布较多,也未表现出显著差异,说明变形菌门和拟杆菌门细菌在高粱根际土壤中的生态幅较宽,可能在生态环境构建和物质循环过程中起重要作用。绿弯菌门(Chloroflexi)、浮霉菌门(Planctomycetes)细菌在三个样地间也有较高的分布,且差异显著(P<0.05)。其中茅台镇绿弯菌门的相对丰度最高为16.19%,坛厂镇和鸭溪镇较低仅为8.01%和3.84%;坛厂镇的浮霉菌门相对丰度最高为10.84%,茅台镇和鸭溪镇分别为8.96%和8.02%。绿弯菌门在生物圈分布较广,参与了碳(C)、氮(N)、硫(S)等元素的生物地球化学循环,可以吸收同化环境中生物和非生物来源的多种有机酸物质,用于解决日益严重的环境污染问题[19]。茅台镇和坛厂镇酿酒高粱根际细菌中的硝化螺旋菌门(Nitrospirae)细菌相对丰度显著高于鸭溪镇(P<0.05)。研究发现,硝化螺旋菌门对处理高强度有机废水具有关键作用[20]。从结果可以看出,茅台镇高粱根际能够分解污染有机物的细菌分布较广,这在很大程度上能够减少污染物对高粱生长的影响,提高高粱的品质。
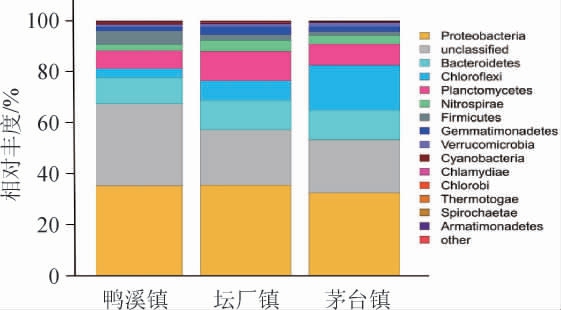
图2 基于门水平不同样地酿酒高粱根际细菌群落结构
Fig.2 Bacterial community structure of liquor-making sorghum rhizosphere in different plots based on phylum level
基于OTU聚类的结果绘制属水平下细菌菌群分布条形图,结果见图3。
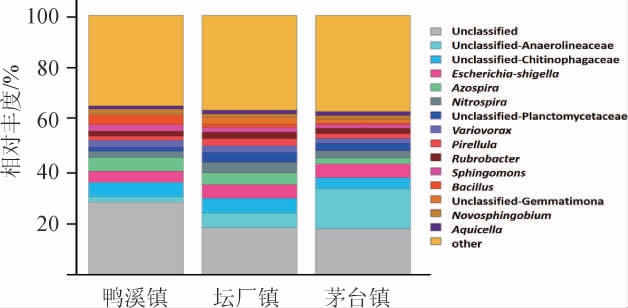
图3 基于属水平不同样地酿酒高粱根际细菌群落结构
Fig.3 Bacterial community structure of liquor-making sorghum rhizosphere in different plots based on genus level
由图3可知,在属水平上,未能分类的厌氧绳菌科(Anaerolineaceae)细菌在茅台镇和坛厂镇分布最多,未能分类的噬几丁质菌科(Chitinophagaceae)细菌在鸭溪镇分布最广。未能分类的厌氧绳菌科细菌在茅台镇占比最高达14.2%,显著高于坛厂镇和鸭溪镇(P<0.05)。研究证明厌氧绳菌是沙漠演变为绿洲过程中出现的重要性指示生物[21],多适合生活在高水砂、高氨、相对低盐、高pH值的环境中[22]。可以看出,茅台镇高粱品质与其长期生长环境土壤理化性质有明显的关系,且与厌氧绳菌的生长环境相关。未能分类的噬几丁质菌科、埃希氏菌-志贺氏菌属(Escherichia-Shigella)细菌在三个样地间差异不显著;坛厂镇和鸭溪镇的固氮螺菌属(Azospira)细菌相对丰度显著高于茅台镇(P<0.05),茅台镇和坛厂镇的未能分类的浮霉菌科(Planctomycetaceae)细菌相对丰度显著高于鸭溪镇(P<0.05)。浮霉菌是目前发现的具有厌氧氨氧化功能的细菌来源[23],在过量施用氮肥的农田土壤生态系统氮移除[24-26]方面有重要作用,属于生态友好型微生物,对全球氮循环具有重要意义。可以推测此类细菌可以改善茅台镇高粱根际土壤过量施氮肥情况,从而保证高粱品质。
采用样本间加权Unifrac距离矩阵绘制距离热图,结果见图4。由图4可知,茅台镇和坛厂镇高粱根际细菌组成和分布相似度最高,其次为坛厂镇和鸭溪镇,茅台镇和鸭溪镇的距离最远。说明距离对高粱根际细菌组成和分布有一定的影响,距离越近其相似度越高。
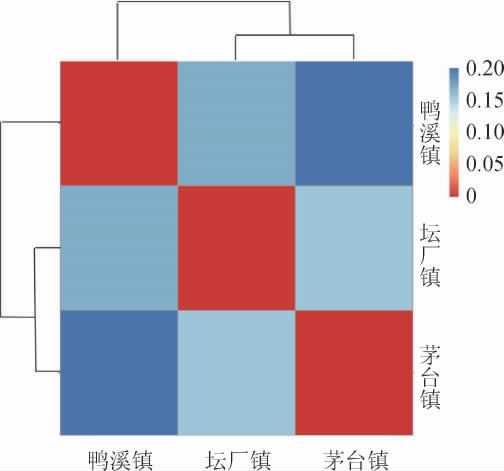
图4 不同样地酿酒高粱根际间细菌群落相似度距离热图
Fig.4 Distance heap map of bacterial community similarity of liquor-making sorghum rhizosphere among different plots
3 结论
茅台镇高粱根际细菌物种数、特有细菌种类最多,且茅台镇高粱根际细菌种类在其他样地分布较多。三个样地细菌群落组成相似,但相对丰度存在较大差异。在门水平上,变形菌门细菌在三个样地分布最多,且相对丰度差异不显著。绿弯菌门、浮霉菌门在三个样地间有较高的分布,不同样地间差异显著,且绿弯菌门在茅台镇的相对丰度最高。在属水平上,茅台镇未能分类的厌氧绳菌科细菌丰富度显著高于坛厂镇和鸭溪镇。聚类分析结果显示茅台镇和坛厂镇的细菌分布和组成相似度最高。
[1]孙婷,田建平,胡新军,等.基于高光谱成像技术的酿酒高粱品种分类[J].食品与发酵工业,2021,47(5):186-192.
[2]倪德让,孔祥礼,孙崇德,等.红缨子高粱淀粉分子结构及糊化特性研究[J].中国酿造,2019,38(12):75-79.
[3]朱永官,彭静静,韦中,等.土壤微生物组与土壤健康[J].中国科学:生命科学,2021,51(1):1-11.
[4] SINGH B P,COWIE A L,CHAN K Y,et al.Soil health and climate change[M].Berlin:Springer,2011:25-45.
[5]DE VRIES F T,WALLENSTEIN M D.Below-ground connections underlying above-ground food production:a framework for optimising ecological connections in the rhizosphere[J].J Ecol,2017,105:913-920.
[6] HERMANS S M,BUCKLEY H L,CASE B S,et al.Using soil bacterial communities to predict physico-chemical variables and soil quality [J].Microbiome,2020,8:257-276.
[7]朱永官,沈仁芳,贺纪正,等.中国土壤微生物组:进展与展望[J].中国科学院院刊,2017,32(6):554-565.
[8]张骏达,李素艳,孙向阳,等.基于高通量测序技术的不同年代公园绿地土壤细菌多样性[J].微生物学通报,2019,46(1):65-74.
[9]罗达,刘顺,史作民,等.川西亚高山不同林龄云杉人工林土壤微生物群落结构[J].应用生态学报,2017,28(2):519-527.
[10]姜雪薇,马大龙,臧淑英,等.高通量测序分析大兴安岭典型森林土壤细菌和真菌群落特征[J].微生物学通报,2021,48(4):1093-1105.
[11]WELLER D M,RAAIJMAKERS J M,GARDENER B B M S,et al.Microbial populations responsible for specific suppressiveness to plant pathogens[J].Annu Rev Phytopathol,2002,40:309-348.
[12]WEI Z,FRIMAN V P,POMMIER T,et al.Rhizosphere immunity:targeting the underground for sustainable plant health management[J].Front Agr Sci Eng,2020,7:317-328.
[13]HUANG X Q,LIU S Z,LIU X,et al.Plant pathological condition is associated with fungal community succession triggered by root exudates in the plantsoil system[J].Soil Biol Biochem,2020,151:108046.
[14]陈法霖,张凯,郑华,等.PCR-DGGE 技术解析针叶和阔叶凋落物混合分解对土壤微生物群落结构的影响[J].应用与环境生物学报,2011,17(2):145-151.
[15]崔佩佩,武爱莲,王劲松,等.不同施肥处理对高粱根际土壤微生物功能多样性的影响[J].华北农学报,2018,33(5):195-202.
[16]武华周,娄德钊,涂娜娜,等.抗,感青枯病桑树根际细菌群落结构与多样性[J].福建农业学报,2020,35(9):1004-1011.
[17]牛世全,龙洋,李海云,等.应用IlluminaMiSeq 高通量测序技术分析河西走廊地区盐碱土壤微生物多样性[J].微生物学通报,2017,44(9):2067-2078.
[18]CHEN Q L,CUI H L,SU J Q,et al.Antibiotic resistomes in plant microbiomes[J].Trend Plant Sci,2019,24:530-541.
[19]鲜文东,张潇橦,李文均.绿弯菌的研究现状及展望[J].微生物学报,2020,60(9):1801-1820.
[20]AKINORI I,TAKESHI T,TAKASHI N,et al.In situ detection and quantification of uncultured members of the phylum nitrospirae abundant in methanogenic wastewater treatment systems[J].Microb Environ,2009,24(2):97-104.
[21]LI C H,TANG L S,JIA Z J,et al.Profile changes in the soil microbial community when desert becomes oasis[J].PLoS One,2015,10(10):e0139626.
[22]王怡静,夏晶晶,于景丽,等.水分驱动半干旱区河流沉积物/土壤厌氧绳菌群落的空间异质性[J].微生物学通报,2020,47(9):2807-2821.
[23]魏亚茹,王怡静,马巧丽,等.粉粒氨氮和水分影响浮霉菌门群落的空间分化[J].微生物学通报,2020,47(9):2732-2745.
[24] NIE S A,LEI X M,ZHAO L X,et al.Response of activity,abundance,and composition of anammox bacterial community to different fertilization in a paddy soil[J].Biol Fert Soils,2018,54(8):977-984.
[25] TSUSHIMA I,OGASAWARA Y,KINDAICHI T,et al.Development of high-rate anaerobic ammonium-oxidizing (anammox) biofilm reactors[J].Water Res,2007,41(8):1623-1634.
[26] DE COCKER P,BESSIERE Y,HERNANDEZ-RAQUET G,et al.Enrichment and adaptation yield high anammox conversion rates under low temperatures[J].Bioresource Technol,2018,250:505-512.