豉香型白酒是岭南地方性传统产品之一,盛产于珠江三角洲地区,至今有近130年的生产历史[1],是具有南国特色的地方性产品,其产品酒精度低,具有“玉洁冰清,豉香独特,醇和甘滑,余味爽净”的独特风味[2]。年出口量历来可达万t[3]。豉香型白酒生产工艺特点比较独特,也是我国传统蒸馏白酒中酒精含量最低的白酒品种,其中酒精度<40%vol,白酒低度化成为当前白酒发展的重要趋势[4-6]。
“曲为酒之魂”,酒曲优劣与白酒酒体质量和产酒率密切相关。白酒的发酵过程是由多种微生物参与的复杂的生化反应的过程[7]。豉香型白酒采用大米为原料,以米饭、黄豆、饼泥、酒饼叶和饼丸所制成的酒饼作为糖化发酵剂,属小曲酒。酒饼是熟料培菌,以米饭、黄豆为主要材料,还加入较大量的饼泥及饼叶等辅料,原材料粗糙,夹杂的杂质较多;而饼丸是生料培菌,以米粉为主要原料,加入少量的饼叶及药材,因而酒饼密度比饼丸大。用大酒饼作为主要糖化发酵剂,采用边糖化边发酵的工艺,经蒸馏、陈肉坛浸、勾调而成的,不直接或间接添加食用酒精及非自身发酵产生的呈色呈香呈味物质,具有豉香特点的白酒[8]。前人对豉香型白酒酒饼中的霉菌和酵母等微生物进行了初步的分离研究,发现酒饼中主要有酵母、霉菌、细菌和放线菌等各种微生物,但对细菌、放线菌在其中的作用并没有做进一步的探讨,也没有对其中的酵母、霉菌进行系统全面的分类研究[9-12]。豉香型白酒一轮完整的发酵,采用原料一次加曲后的半固态双边发酵工艺,整个发酵过程历时15~20 d,因此酒饼微生物及发酵过程发酵醪液中微生物的动态变化成为影响豉香型白酒风味及质量的重要因素。董士伟[13]以豉香型白酒发酵原料等为研究对象进行产酯酵母的筛选,得到一株有强产酯能力的酵母菌。吴雪梅[14-15]通过对饼丸的微生物种类、数量及主要理化指标进行为期一年的监测,发现一年内饼丸中的霉菌总数较酒饼中的波动较大;对豉香型酒曲和发酵醪液的微生物组成、数量及主要理化指标进行初步分析,结果表明,从一级种到白酒醪液,其微生物种类及数量变化较大;由于培养条件不同,酒曲理化指标及酶活力也相差较远。
本课题组通过聚合酶链式反应-变性梯度凝胶电泳(polymerase chainreaction-denaturing gradient gel electrophoresis,PCR-DGGE)技术结合系统发育同源研究豉香型白酒在生产过程中的酒丸、酒饼和发酵醪液中的微生物群落结构,分析豉香型白酒酒曲中微生物区系的构成及变化,对判断和鉴定白酒生产中与特征风味物质相关的关键微生物、指导生产工艺改进具有重要的理论和实践意义。
1 材料与方法
1.1 材料与试剂
豉香型白酒生产用酒丸(0、1 d、2 d、3 d、4 d)、酒饼(0、1 d、10 d、22 d、33 d)和发酵醪液(0、3 d、5 d、7 d、10 d、14 d):均由广东省九江酒厂提供。
脱氧核糖核酸(deoxyribonucleicacid,DNA)Marker、PCR试剂、DNA提取试剂盒和感受态细胞:大连Takara公司;丙烯酰胺(分析纯)、甲叉双丙烯酰胺(分析纯)、去离子甲酰胺(分析纯)、四甲基乙二胺(tetramethylethylenediamine,TEMED):广州捷瑞生物工程有限公司;尿素、氯化钠、NaOH(均为分析纯):天津市福晨化学试剂厂;冰乙酸(分析纯):天津市富宇精细化工有限公司;溴化十六烷基三甲铵(cetyltrimethylammonium bromide,CTAB)、十二烷基硫酸钠(sodium dodecyl sulfate,SOD):广州威佳科技有限公司;Tris base(分析纯)、乙二胺四乙酸(ethylene diamine tetraacetic acid,EDTA);北京普博欣生物科技有限公司;乙醇(分析纯):天津市科密欧化学试剂有限公司;氨苄青霉素(分析纯):美国Biosharp公司;甲醛(分析纯):天津市科密欧化学试剂有限公司;回收纯化试剂盒:上海生物工程有限公司;Goldview:北京赛百盛基因技术有限公司;硝酸银:广东光华化学厂有限公司;蛋白酶K(40 U/mg):百川开泰生物技术(北京)有限公司;RNase A:翌圣生物科技(上海)有限公司。
1.2 仪器与设备
PC 300PCR 仪:Eppendorf Master personal;Tanon EPS 100电泳仪:上海天能科技有限公司;TDL-5-A低速台式大容量离心机:上海安亭科学仪器厂;ChemiDocXRS+凝胶成像系统、JY-TD331A型变性梯度电泳仪:美国Bio Rad公司;BIOBASE高速冷冻离心机:Eppendorf(中国)有限公司。
1.3 方法
1.3.1 发酵原料样本预处理
酒饼和酒丸样品预处理[16]:称取7 g样品,用15 mL无菌磷酸盐缓冲液(phosphate buffer solution,PBS)悬浮,漩涡振荡5 min,1 000 r/min离心5 min,取上清,沉淀用PBS缓冲液重复洗涤2~3次,离心后收集全部上清。10 000 r/min离心5 min,收集细胞沉淀。分别用PBS洗3次,-20 ℃保存备用。
醪液样品预处理:将发酵醪液1 000 r/min离心5 min,去沉淀,取25 mL上清液于50 mL离心管,10 000 r/min离心5 min,收集细胞沉淀,用PBS洗涤2~3次,洗净的菌体悬浮在1.5 mL PBS(pH 7.0)中,用枪吹打后振荡均匀,转入2 mL EP管中,-20 ℃保存备用。
1.3.2 微生物总DNA的提取纯化
首先加入565 μL TE缓冲液(pH 8.0)重悬菌体,取40 μL 10%SDS和20 μL蛋白酶K(10 mg/mL),混合均匀,置于37 ℃反应1 h,再加入100 μL 5 mol/L NaCl,混匀,65 ℃2 min。将80 μLCTAB/NaCl裂解液混匀,65 ℃反应30 min,加入等体积的酚∶氯仿∶异戊醇(25∶24∶1,V/V),12 000 r/min离心10 min。再加入等体积氯仿∶异戊醇(24∶1,V/V),混匀12 000 r/min离心5 min。然后取0.7倍体积异丙醇以沉淀DNA,12 000 r/min离心10 min,取500 μL体积分数70%乙醇洗涤,提取得到DNA加50 μL双蒸水(ddH2O)溶解,在DNA粗提液中加2 μL RNase A,37 ℃反应1 h,-20 ℃保存。
1.3.3 PCR扩增
扩增的DNA片段为细菌的16S部分序列,扩增长度约230 bp。PCR引物采用16S rRNA细菌V3区通用引物[17]。引物序列为:R518-GC(CGCCCGCCGCGCGCGGCGGGCGGGGCGGGGGCACGGGGGGCCATTACCGCGGCTGCTGG)和F341(TACGGGAGGCAGCAG)。PCR扩增体系(50 μL)为:5 μL 10×buffer,0.25 μL Taq酶(5 U/μL),4 μL脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTPs)Mixture,0.25 μL引物(40 μmol/L),2.5 μL DNA。Touch Down PCR扩增程序为94 ℃预变性4 min后进入20个循环,94 ℃、30 s;60 ℃、30 s(每循环一次后温度降低0.5 ℃);72 ℃、1 min;进入10个循环,94 ℃、30 s;50 ℃、30 s;72 ℃、1 min,最后72 ℃延伸10 min。
针对真菌18SrRNA基因进行相关真菌群落结构的解析,PCR扩增引物为GC-fung*[18]和NS1[19]。引物序列为:GC-fung*:CGCCCGCCGCGCGGCGGGCGGGGCGGGGGCATTCCCCGTTACCCGTTG;NS1:GTAGTCATATGCTTGTCTC。PCR扩增体系(50μL)为:10×buffer 5 μL,Taq酶(5U/μL)0.25μL,4 μL dNTPs Mixture,0.25 μL引物(40 μmol/L),2.5 μL DNA。PCR扩增程序94 ℃预变性5 min后进入20个循环,94 ℃、45 s;50 ℃、45 s(每循环一次后温度降低0.5 ℃);72 ℃、1 min;接着进入10个循环,94 ℃、45 s;50 ℃、45 s;72 ℃、1 min,最后72 ℃延伸10 min。
1.3.4 DGGE分析
参考江汶钰等[20]的方法,取5 μL PCR产物进行DGGE分析。采用变形梯度为30%~60%、浓度为8%的聚丙烯酰胺凝胶在1×TAE缓冲液中85 V,60 ℃电泳9 h,银染法。
1.3.5 DGGE条带的克隆测序及分析
扩增回收片段,试剂盒纯化PCR产物,克隆并挑取克隆子,送至生工生物工程(上海)股份有限公司测序。根据测序结果,利用基本局部比对搜索工具(basic local alignment search tool,BLAST)在美国国家生物技术信息中心(national center of biotechnology information,NCBI)GenBank核酸序列数据库进行同源序列搜索,以比较代表菌株与已知相应序列的相似程度。
1.3.6 软件分析
将DGGE图谱经Quantity One V4.62软件数字化分析后,对图谱进行了Shannon-Wiener多样性指数[21]分析;采用DNAMAN等软件对细菌16S rRNA V3区和真菌PCR测序序列进行比对聚类分析,邻接(neighbor-joining,NJ)法构建系统进化树。
2 结果与分析
2.1 发酵原料中细菌群落结构分析
结合图1、图2和表1发现,发酵乳杆菌(Lactobacillus fermentum)(条带4、6、15)、胚牙乳杆菌(Lactobacillus plantarum)(条带28)和乳酸片球菌(Pediococcus acidilactici)(条带7、10)在酒丸和酒饼两个阶段条带均明显存在,但在醪液发酵阶段则开始急剧减弱;乳酸乳球菌(Lactococcus lactis subsp.Cremoris)(条带8、9)和卤代单胞菌(Halomonas arcis)(条带2)仅存在0 d酒丸样品中出现,金黄杆菌属(Chryseobacterium sp.)(条带5)也仅出现在0 d酒丸和0 d酒饼中;发酵醪液多样性指数随发酵时间的增加,细菌种类先减少后增加,细菌总量(条带数)分布趋于均匀。魏斯氏菌属(Weissella)(条带11、22)仅在酒丸0 d和醪液发酵后期出现,据报道此菌种在此之前只有在浓香型和芝麻香型酒中酿造微生物中检测到,推测该菌种在酒类酿造过程中形成的某种特殊代谢产物可能造就了某些白酒不同的品质[22]。干酪乳杆菌(Lactobacillus panis)(条带1)在三个阶段的条带均有出现,但处于较低水平,在醪液发酵后期略有增长;干酪乳杆菌(Lactobacillus pontis)(条带18)、罗伊氏乳杆菌(Lactobacillus reuteri)(条带19、20)胃肠乳杆菌(Lactobacillus gastricus)(条带21)仅出现于发酵醪液阶段,处于优势地位,且保持稳定。弯曲乳酸杆菌(Lactobacillus crispatus)(条带13、17、29)仅在醪液发酵期出现,且处于优势地位,并在14 d醪液种群数量增加;未培养的乳酸杆菌属(Uncultured Lactobacillus sp.)(条带14、25)仅存在于14 d发酵醪液出现。

图1 细菌16S rRNA V3基因DGGE电泳图(A)及泳道识别图(B)
Fig.1 Electrophoretic diagram (A) and lane identification map (B)DGGE bacterial 16S rRNA V3 gene
0 W~4W:贮藏0~4天酒丸;0B、1B、10B、22B、33B:贮藏0 d、1 d、10 d、22 d、33 d的酒饼;0L、3L、5L、7L、10L、14L:0 d、3 d、5 d、7 d、10 d、14 d的发酵醪液。下同。
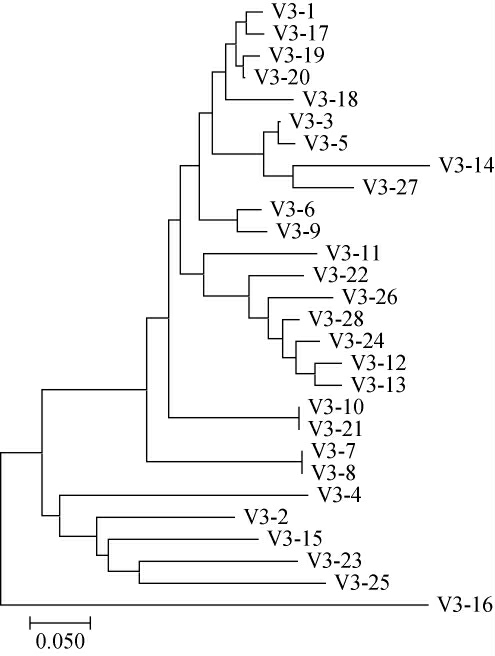
图2 分离条带基于16S rRNA序列系统发育树
Fig.2 Phylogenetic tree of separated strips based on 16S rRNA
表1 细菌16S rRNA V3区基因的DGGE切胶条带的测序结果分析
Table 1 Analysis of sequencing results of DGGE cut tape of bacteria gene in 16S rRNA V3 region

备注:V3代表“细菌”,其后缀编号“1、2、3……”与图1 DGGE电泳条带编号相对应。
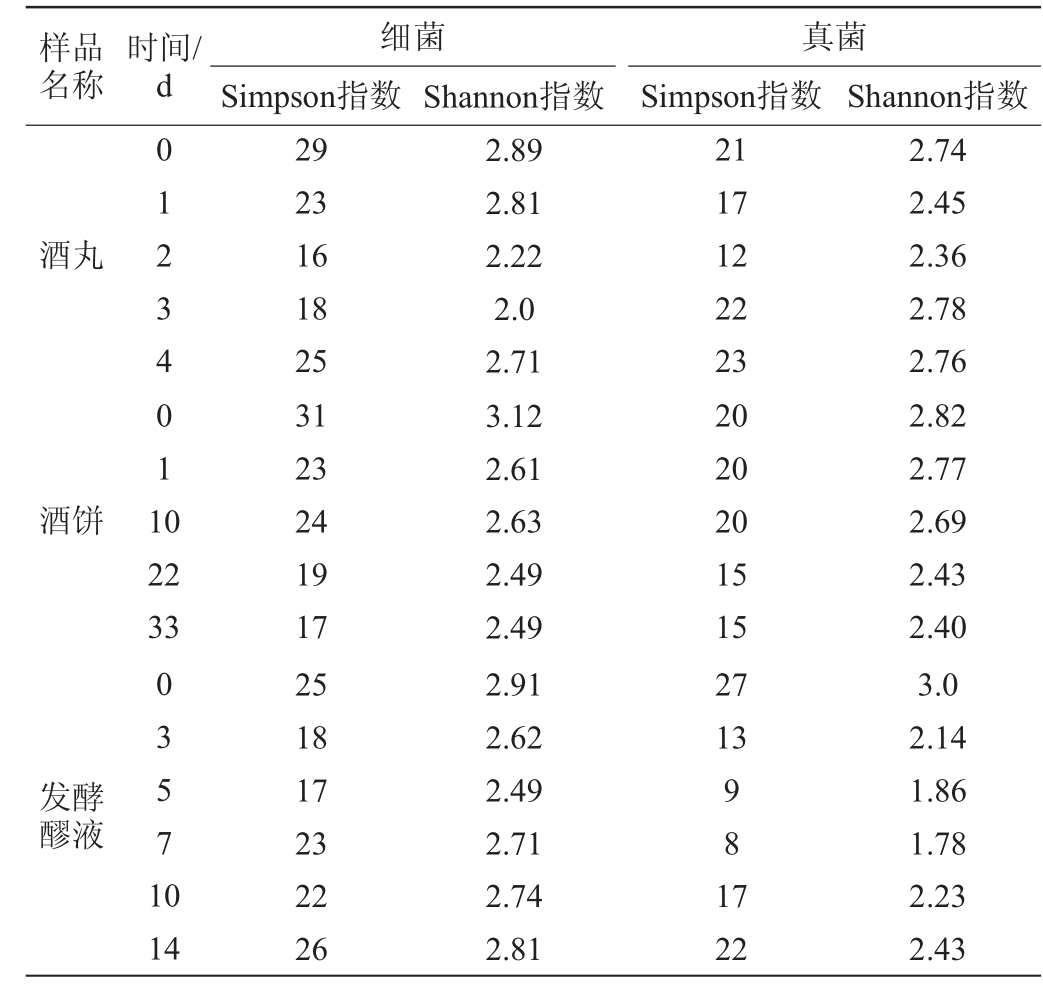
由表2可知,酒丸多样性指数随着贮藏时间的增加,优势细菌种类有所下降,贮藏第4天细菌种类又有所上升;而酒饼随着贮藏时间增加,微生物种类随之减少,贮藏22 d后则保持稳定;醪液中随着发酵时间的延长,细菌多样性有所减少。
表2 微生物的DGGE指纹图谱多样性指数
Table 2 Diversity indexes of microorganisms DGGE fingerprint
结合表2和图2,此次研究发现了许多尚未在豉香型白酒的研究中报道过的细菌菌属,如卤代单胞菌类(Halomonas),金黄杆菌属(Chryseobacterium),假单胞菌属(Pseudomonas),肠杆菌属(Enterobacter),未培养的细菌(Uncultured bacterium)及多种乳杆菌属(Lactobacillus),这些细菌的理化特性和在豉香型白酒生产过程中发挥的功能性作用有待于进一步深入研究。
2.2 发酵原料中真菌群落结构分析
由图3 和表2可知,在白酒生产过程中各样本的真核微生物种类和数量都发生了不同程度的变化,其中,三类样本中0 d样本均有较高的多样性。DGGE图谱显示,酒饼微生物多样性随着贮藏时间的增加也随之下降,而酒丸储藏后期和发酵醪液后期真菌的检出条带数及丰度值却有较大幅度的回升。

图3 豉香型白酒真菌DGGE电泳图(A)及泳道识别图(B)
Fig.3 Electrophoretic map (A) of fungal DGGE and lane identification map (B) of Chi-flavor Baijiu
由图4和表3可知,存在于三个阶段中且在整个酵母群落中处于优势地位的是乳酸菌(Kluyveromyces lactis)、酿酒酵母(Saccharomyces cerevisiae)、奥默柯达菌(Kodamaea ohmeri)三种酵母菌。扣囊复膜酵母(Saccharomycopsis fibuligera)在酒饼丸时期处于优势地位,特别是发酵初期,随发酵时间的增加而逐渐减弱。它能够表达生成淀粉液化酶和糖化酶,能够产生淀粉分解酶类的子囊酵母菌之一,可提高出酒率及酒质,且可以产生甲羟戊酸促进其他微生物的生长[23-24]。乳酸克鲁维酵母(Kluyveromyces lactis)(条带11)存在于三类样品中,且处于优势地位,并随发酵时间增加而逐渐减弱,是一种能够以乳酸作为其唯一的碳源和能源的酵母,并能生产芳香族化合物,同时还可能会刺激乳酸菌的生长[25]。酿酒酵母(Saccharomyces cerevisiae)(条带4﹑5、10)和光滑假丝酵母(Candida glabrata)(条带6、8)在酒丸和酒饼时期较为活跃,而在白酒发酵期则开始减弱,与我们通常的预期存在差异,原因可能与DGGE的呈现效果有关。热带假丝酵母(Candida tropicalis)(条带15)和奥默柯达菌(Kodamaea ohmeri)(条带17)仅在酒饼阶段出现,且较为活跃,在其他两个阶段并未出现。皮炎芽生菌(Endom-yces sp.)(条带7)和印度毛黴菌Mucor indicus(条带13)仅存在于0 d酒饼样品中,而青霉亚曲霉(Aspergillus penicillioide)(条带19)仅出现于0 d和33 d酒饼中。
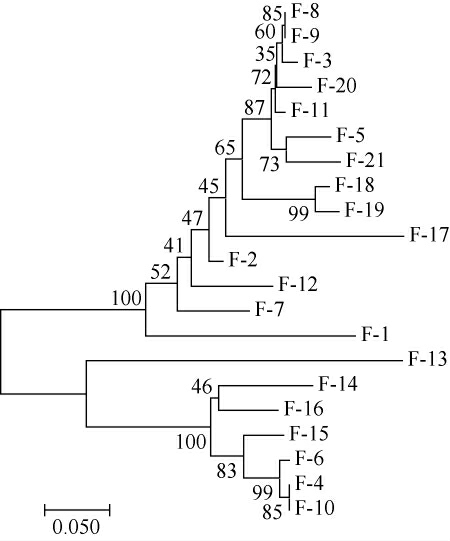
图4 分离条带的18S rRNA系统发育树
Fig.4 Phylogenetic tree of strains 18S rRNA
表3 真菌18S rRNA区基因的DGGE切胶条带的测序结果分析
Table 3 Sequencing results of DGGE bands of fungal 18S rRNA region genes

备注:F代表“真菌”,其后缀编号“1、2、3……”与图3 DGGE电泳条带编号相对应。
3 结论
利用PCR-DGGE技术研究酒丸、酒饼和发酵醪液的不同发酵期的细菌和真菌群落结构,其中细菌除乳杆菌属(Lactobacillus)外,同时还检测到了卤代单胞菌(Halomonas)、金黄杆菌属(Chryseobacterium)、假单胞菌属(Pseudomonas)、小球菌属(Pediococcus)、融合魏斯氏乳酸菌(Weissella cibaria)、木质素溶解肠杆菌(Enterobacter lignolyticus)和未培养的细菌属(uncultured bacterium)等不同种属的细菌,这些类群在不同时期、不同类型的样本中的呈现存在一定差异,或始终存在,或阶段性出现,或数量不同等。而且多样性指数显示,随着贮藏时间的增加,酒丸和发酵醪液中优势细菌种类有所下降,后期细菌种类又有所上升;酒饼则随着贮藏时间增加,微生物种类随之减少,贮藏22 d后则保持稳定;在真菌群落结构及多样性的分析中,除酵母外,其他菌有印度毛黴菌(Mucor indicus)、帚状曲霉(Aspergillus penicillioide)、栗蕈寄生菌属(Endomyces sp.)等,各类群在不同时期、不同类型的样本中的呈现同样存在一定差异。其中酒丸和发酵醪液中微生物的多样性随着时间的增加,优势真菌种类有所下降,贮藏后期真菌种类又有所上升;酒饼随着贮藏时间增加,微生物种类不断减少,趋于稳定。实验检测出多种未培养微生物,表明相较于传统的分离培养法,采用PCR-DGGE技术分析豉香型白酒的细菌菌落结构,结果更全面、更直观,这也为进一步提高白酒质量提供有力的支撑。
[1]潘丽娟,赖嘉雯,赵文红,等.豉香型白酒研究现状[J].中国酿造,2020,39(10):21-25.
[2]杨帅,皇甫洁,董建辉,等.清雅型“玉冰烧”白酒酒体风格特征研究[J].中国酿造,2020,39(4):49-52.
[3]黄清意,李湘銮,费永涛,等.陈肉酝浸对豉香型白酒风味影响的研究进展[J].食品与发酵工业,2020,46(19):284-288.
[4]刘勇.谈低度化白酒发展现状[J].酿酒,2020,47(3):26-27.
[5]曹云刚.汾酒发酵过程中香味成分变化规律的研究[D].太原:山西大学,2011.
[6]赵树堃.中国白酒低度化概述[J].现代农业科技,2011(2):364-365.
[7]赵皓静,王晓丹,邱树毅,等.液质发酵食品中微生物群落及与乳酸菌间相互作用研究进展[J].微生物学通报,2021,48(3):960-973.
[8]陈少平,关芊彤,方毅斐.大酒饼发酵力检测方法探究[J].现代食品,2018(9):147-149.
[9]徐丽萍.泸型大曲中产酯酵母的筛选鉴定及产酯条件优化[J].中国酿造,2016,35(2):74-75.
[10]向玉萍,邱树毅,曹文涛,等.酱香型白酒核心产区大曲中霉菌的分离及鉴定[J].食品与发酵科技,2021,57(2):56-65.
[11]徐成勇,刘泉勇,郭波,等.豉香型白酒酒饼微生物的分离[J].食品与发酵工业,2002,28(10):10-12.
[12]萧暖章.豉香型白酒酒曲中酵母分离、选育和鉴定[J].四川食品与发酵,2008(1):14-15.
[13]董士伟.豉香型白酒中功能微生物的筛选与应用[D].郑州:河南工业大学,2012.
[14]吴雪梅.豉香型白酒不同季节酒曲微生物的研究[J].酿酒,2013,40(1):63-66.
[15]吴雪梅.豉香型白酒酒曲微生物的研究[J].酿酒科技,2013(6):61-64.
[16]高亦豹.聚合酶链式反应-变性梯度电泳技术(PCR-DGGE)研究中国白酒大曲中微生物群落结构[D].无锡:江南大学,2010.
[17]MUYZER G,DE WAAL E C,UITTERLINDEN A G.Profiling of complex microbial populations by denaturing gradient gel electrophoresis analysis of polymerase chain reaction-amplified genes coding for 16S rRNA[J].Appl Environ Microbiol,1993,59(3):695-700.
[18]MAY L A,SMILEY B,SCHMIDT M G.Comparative denaturing gradient gel electrophoresis analysis of fungal communities associated with whole plant corn silage[J].Canad J Microbiol,2001,47(9):829-841.
[19]BOONMEE S,ZHANG Y,CHOMNUNTI P,et al.Revision of lignicolous Tubeufiaceae based on morphological reexamination and phylogenetic analysis[J].Fungal Divers,2011,51(1):63-102.
[20]江汶钰,徐学锋,杨幼慧.豉香型白酒酒饼中细菌PCR-DGGE 分析方法的建立[J].现代食品科技,2015,31(10):307-312.
[21]ZOETENDAL E G,AKKERMANS A D L,DE VOS W M.Temperature gradient gel electrophoresis analysis of 16S rRNA from human fecal samples reveals stable and host-specific communities of active bacteria[J].Appl Environ Microbiol,1998,64(10):3854.
[22]姚粟,刘洋,葛媛媛,等.芝麻香型白酒高温大曲细菌群落多样性研究[C]//广州:第五届全国微生物资源学术暨国家微生物资源平台运行服务研讨会,2013.
[23]于欣君.扣囊复膜酵母菌酸性蛋白酶基因在解脂耶罗维亚酵母菌中表达和重组酸性蛋白酶的应用[D].青岛:中国海洋大学,2011.
[24]刘志磊,曹健,王德良,等.清香型大曲及酒醅中拟内孢霉的分离鉴定[J].中国酿造,2011,30(3):38-41.
[25]梁龙,牟光庆,陈历俊,等.乳酸克鲁维酵母与乳酸菌混菌发酵对乳糖降解条件的优化[J].中国乳品工业,2013,41(5):12-14.