杂色曲霉毒素(sterigmatocystin,SMC)、黄曲霉毒素(aflatoxins,AFTs)两者结构相似,都具有较强的致癌性,普遍存在于大米、小麦、玉米等谷物中[1-3],常协同污染谷物及其制品。摄入被杂色曲霉毒素或者黄曲霉毒素污染的谷物易致癌、致畸,还极易在体内蓄积残留,严重威胁人类健康[4-5]。谷物源性运动食品是指以谷物类原料制成的针对运动人群开发的一类补充营养素的食品。因其是针对特殊人群研发的一种食品,对安全性要求高,所以需要对这类产品中相关毒素残留情况进行监控。
目前对食品中杂色曲霉毒素和黄曲霉毒素的测定方法主要有薄层色谱法(thin layer chromatography,TLC)、高效液相色谱法(high performance liquid chromatography,HPLC),高效液相色谱-串联质谱法(high performance liquid chromatography-tandemmassspectrometry,HPLC-MS/MS)等[6-11]。TLC法具有操作简便、成本低廉等优点,但重复性差,往往作为定性筛查方法;HPLC法具有灵敏度高、重现性好、普及性广等优点,但对复杂基质样品存在杂峰干扰等问题;HPLCMS/MS法具有分辨率高的优点,采用同位素内标法可准确定量,可作为定性定量检测食品中杂色曲霉毒素的确证方法。本研究运用QuEChERS前处理净化技术,避免一般前处理耗材成本较高的问题[12-13],并依据质谱检测器具有特异选择性以及高灵敏度的特性[14],提高了方法的检出限和定量限,可为谷物源性运动食品中杂色曲霉毒素和黄曲霉毒素的监控提供技术支持。
1 材料与方法
1.1 材料与试剂
杂色曲霉毒素标准溶液(100.0 μg/mL),黄曲霉毒素(aflatoxin,AF)B1、黄曲霉毒素B2(AFB2)、黄曲霉毒素G1(AFG1)、黄曲霉毒素G2(AFG2)混合标准溶液(200.0 μg/mL):上海安谱实验科学科技有限公司;C18吸附剂:美国Agilent科技有限公司;甲醇、乙腈、甲酸(色谱纯):美国Merck公司;无水硫酸镁、氯化钠、柠檬酸钠、柠檬酸氢二钠(分析纯):国药集团化学试剂有限公司;植物蛋白营养粉(大豆蛋白)、小麦低聚肽运动营养粉、花生低聚肽运动营养粉、玉米肽运动营养强化粉:市售。
1.2 仪器与设备
LC-30A高效液相色谱仪:日本岛津公司;AB SCIEX Triple TOF 5600高分辨质谱仪:美国AB SCIEX公司;TD-5高速离心机:上海卢湘仪器有限公司。
1.3 实验方法
1.3.1 样品前处理
称取谷物源性运动食品5.0 g,加入20 mL提取液,超声提取10 min。将盐析剂[15-16](无水硫酸镁/氯化钠/柠檬酸钠二水合物/柠檬酸氢二钠盐倍半水合物=4∶1∶1∶0.5(g∶g))加入样品中混匀后4 000 r/min离心2 min。吸取1.0 mL上清液并加入净化剂,涡旋1 min后4 000 r/min离心2 min,取上清液过滤后进行分析。比较不同的提取液(乙腈-水(85∶15,V/V)、乙腈-水(70∶30,V/V)、甲醇-水(85∶15,V/V)、乙腈-水-甲酸(85∶14∶1,V/V))、净化剂组合(30 mgSiO2+30mgC18、30 mg NH2+30 mgC18、30 mg弗罗里硅土+30 mg C18)对5种真菌毒素检测效果的影响[17-21]。
1.3.2 标准溶液的配制
取适量的杂色曲霉毒素标准溶液和黄曲霉毒素混合标准溶液,以甲醇为溶剂配制成质量浓度0.1 ng/mL、0.5 ng/mL、1.0 ng/mL、2.0 ng/mL、5.0 ng/mL、10.0 ng/mL的系列标准溶液,置于棕色瓶中避光保存。
1.3.3 液相色谱条件
选用Atalantis T3耐高压色谱柱(2.1 mm×150 mm,3 μm);样品进样量为2.0 μL;流动相A为0.15%甲酸溶液,流动相B为乙腈,流速为0.2 mL/min;梯度洗脱条件为0~0.5 min 90%A,2.0~5.0 min 10%A,5.1~10.0 min 90%A。
1.3.4 质谱条件[22-25]
电喷雾离子源(electrospray ionization,ESI):正离子电离(ESI+);监测模式:多反应监测(multiple-reaction monitoring,MRM);离子源温度:105 ℃;毛细管电压:3.0 kV;脱溶剂气流量:10 L/min;锥孔流量:0.5 L/min;去溶剂温度:400 ℃;其他质谱参数见表1。
表1 5种真菌毒素的多反应监测扫描模式的质谱参数
Table 1 Mass spectrometry parameters of multi reaction monitoring scanning mode for 5 mycotoxins
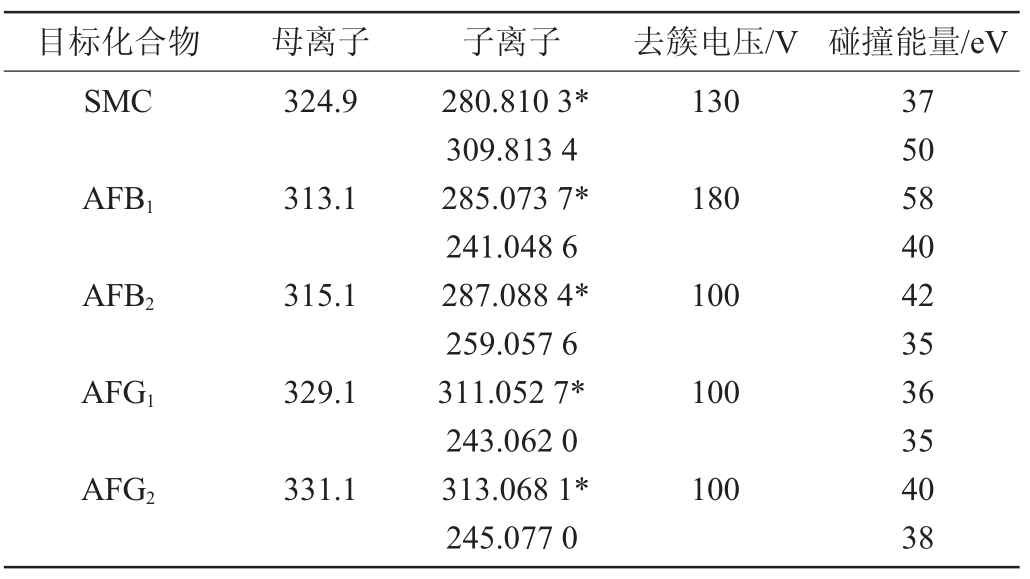
注:“*”表示定量离子。
2 结果与分析
2.1 色谱条件的优化
2.1.1 流动相的选择
为了使杂色曲霉毒素、4种黄曲霉毒素能够有效分离,比较了在不同组分流动相(乙腈-水、甲醇-水、乙腈-0.1%甲酸溶液和乙腈-5 mmol/L乙酸铵溶液)条件下5种目标物的响应值和峰形,结果见图1。由图1可知,流动相体系中含有乙腈会改善起到增强目标物响应值的作用,在水相中加入0.1%甲酸溶液时杂色曲霉毒素和4种黄曲霉毒素的响应值较高,与其他3种流动相相比具有显著性差异(P<0.05),因此选择乙腈-0.1%甲酸溶液作为流动相。

图1 不同流动相对5种真菌毒素响应值的影响
Fig.1 Effect of different mobile phases on response value of 5 mycotoxins
不同小写字母表示差异显著(P<0.05)。下同。
2.1.2 流动相中甲酸溶液的优化
由于杂色曲霉毒素和4种黄曲霉毒素属于极性化合物[16],流动相的组成会影响目标物的分离和离子化效率,从而影响到检测的灵敏度。为了促进目标化合物的离子化,选择乙腈和甲酸溶液作为流动相的组成,其中甲酸含量分别为0.05%、0.10%、0.15%和0.20%。结果表明,当甲酸溶液为0.15%时,杂色曲霉毒素和4种黄曲霉毒素的离子化效果最好,离子丰度最强,因此选择0.15%甲酸溶液与乙腈组成流动相进行梯度洗脱。
在乙腈-0.15%甲酸溶液得到5种真菌毒素的总离子流图见图2。由图2可知,杂色曲霉毒素和4种黄曲霉毒素的离子化效果最好,离子丰度最强。
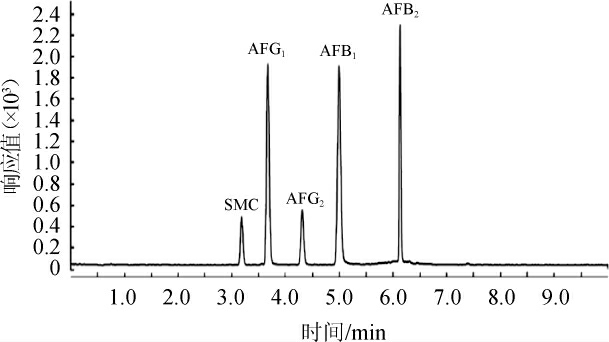
图2 乙腈-0.15%甲酸溶液流动相条件下5种真菌毒素标准品总离子流色谱图
Fig.2 Total ion flow chromatogram of 5 mycotoxins standard using acetonitrile-0.15% formic acid solution as mobile phase
2.2 QuEChERS前处理方法的优化
2.2.1 提取液的选择
真菌毒素化合物易溶于甲醇、乙腈、水等极性溶剂中,常用提取液有乙腈-水、甲醇-水、乙腈-水-甲酸等类型[17-19]。本试验具体比较了4种提取溶剂:乙腈-水(85∶15,V/V)、乙腈-水(70∶30,V/V)、甲醇-水(85∶15,V/V)、乙腈-水-甲酸(85∶14∶1,V/V)。试验以大豆基质的谷物源性运动食品为对象,并添加5种真菌毒素制得阳性质控样品(加标量均为1 μg/kg,混合均匀后放置一周检测)。比较不同类型提取液对样品中杂色曲霉毒素和4种黄曲霉毒素提取效果的影响,结果以5种真菌毒素的测定值为比较依据,结果见图3。
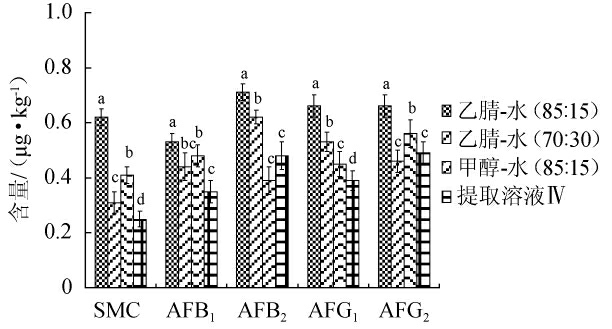
图3 不同提取液对5种真菌毒素回收率的影响
Fig.3 Effect of different extraction solution on recovery rate of 5 mycotoxins
不同小写字母表示差异显著(P<0.05)。下同。
由图3可知,不同提取液对杂色曲霉毒素和4种黄曲霉毒素的回收率存在显著差异(P<0.05),当选择乙腈-水(85∶15,V/V)作为提取液时,加标样品中5种真菌毒素的检出含量最高,能达到0.53~0.71 μg/kg。在此比例的提取液中,5种极性化合物的真菌霉素在提取液中的分配系数高,故目标物的测定值较理想。
2.2.2 净化剂的优化
由图4可知,3组净化剂组合对加标样品中杂色曲霉毒素和4种黄曲霉毒素检测含量的影响差异显著(P<0.05),30 mg SiO2+30 mg C18的组合对净化谷物源性运动食品的效果较好,加标样品中5种真菌毒素的检测含量能达到0.86~0.97 μg/kg,所以本试验选择了30 mg SiO2+30 mg C18作为净化剂组合效果较好。
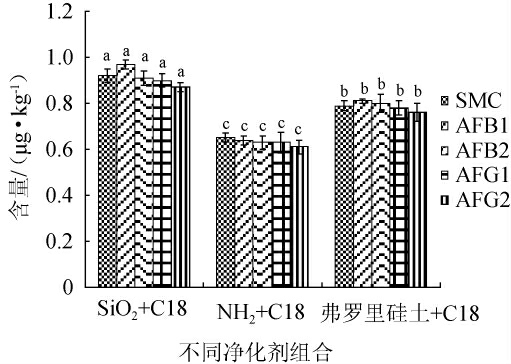
图4 不同净化剂组合对5种真菌毒素回收率的影响
Fig.4 Effect of different combinations of purifying agents on recovery rate of 5 mycotoxins
2.3 方法的线性范围与灵敏度
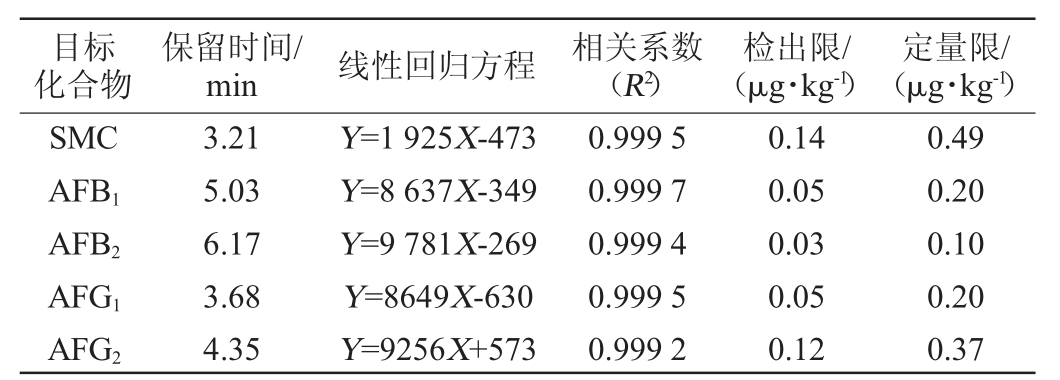
在乙腈-0.15%甲酸流动相体系中,按上述条件进行测定,绘制标准曲线。取5种真菌毒素最低浓度的标准品溶液,连续进样6次,考察色谱保留时间及峰面积的相对标准偏差(relative standard deviation,RSD),以信噪比(S/N)=10计算定量限(limit of quantitation,LOQ),以S/N=3计算检出限(limit of detection,LOD)。实验结果5种目标组分在0.1~10.0 ng/mL范围内均具有良好的线性关系,详细结果见表2。
表2 5种真菌毒素的保留时间、线性回归方程、相关系数、检出限与定量限
Table 2 Retention time,linear regression equation,correlation coefficient,detection limit and quantitative limit of 5 mycotoxins
2.4 方法的精密度与回收率
在加标回收实验中,选用谷物源性运动食品常见的小麦粉基质、玉米基质、大豆基质、花生基质共4种基质(样品5种真菌毒素均未检出),分别对3种不同加标量(SMC:0.5 μg/kg、5 μg/kg和10 μg/kg,AFB1、AFG1:0.2 μg/kg、2 μg/kg和4μg/kg,AFB2:0.1μg/kg、1μg/kg和2μg/kg,AFG2:0.4μg/kg、4 μg/kg和8 μg/kg)的加标样品连续5次的测定进行评价,考察谷物源性运动食品中杂色曲霉毒素和黄曲霉毒素的回收率及方法精密度相对标准偏差(RSD),测定结果见表3。
表3 谷物源性运动食品中杂色曲霉毒素和黄曲霉毒素的回收率及方法精密度试验
Table 3 Recovery rate and method precision test of sterigmatocystin and aflatoxins in cereal-derived sports food
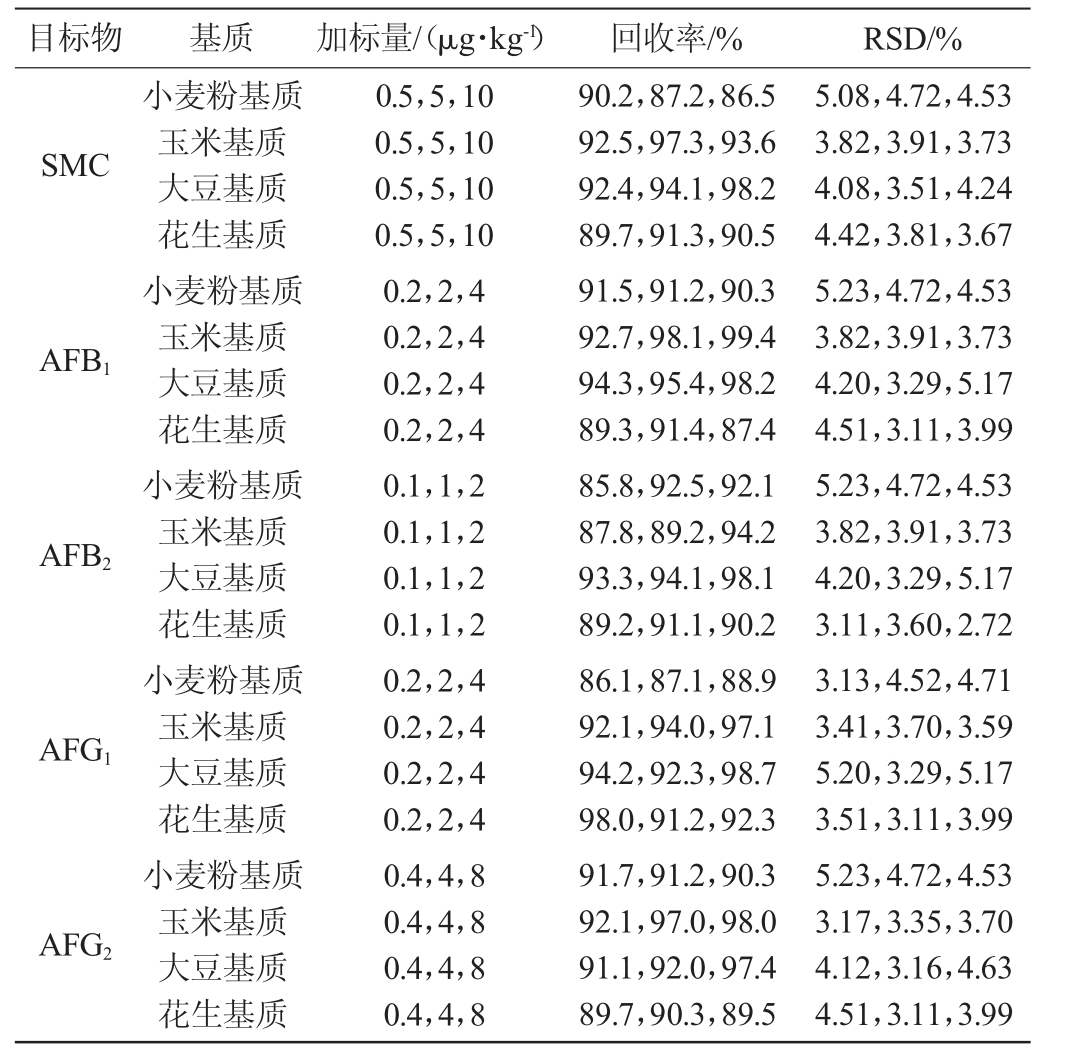
由表3可见,在4种不同的谷源性运动食品基质中,杂色曲霉毒素和4种黄曲霉毒素的平均回收率为85.8%~99.4%,方法精密度RSD为2.72%~5.23%,说明本实验的检测数据的准确度和精密度可行。
2.5 实际样品分析
通过本试验建立的HPLC-MS/MS方法对市售的20份谷源性运动食品中的杂色曲霉毒素和4种黄曲霉毒素进行定量分析。20份样品中均未检出杂色曲霉毒素和黄曲霉毒素,整体情况良好。
3 结论
本研究建立的QuEChERS-HPLC-MS/MS检测谷物源性运动食品中杂色曲霉毒素和黄曲霉毒素的分析方法,可有效去除谷物源性运动食品中的干扰物对目标峰的影响,实现对样品中5种真菌毒素类的定性和定量分析。样品经乙腈-水(85∶15,V/V)提取后,再由30 mg SiO2+30 mg C18净化剂组合处理,在4种不同的源性基质中加标回收率能达到85.8%~99.4%,并具有可靠的准确度和精密度。适用于谷物源性运动食品中杂色曲霉毒素和黄曲霉毒素的分析和定量检测。
[1]赵亚荣,刘香香,赵洁,等.食品中杂色曲霉毒素污染状况研究进展[J].中国卫生检验杂志,2016,28(5):680-682.
[2]李玮,艾连峰,马育松,等.超高效液相色谱-飞行时间质谱测定牛奶中9 种真菌毒素[J].分析科学学报,2019,35(5):675-678.
[3]王鸿雁.固相萃取串联高效液相色谱检测谷物中杂色曲霉素[J].农业科技与信息,2017(2):29-31.
[4]DUARTE S C,LINO C M,PENA A.Food safety implications of ochratoxin A in animal-derived food products[J].Vet J,2012,192(3):286-292.
[5] VALLE-ALGARRA F M,MATEO E M,MATEO R,et al.Determination of type A and type B trichothecenes in paprika and chili pepper using LCtriple quadrupole-MS and GC-ECD[J].Talanta,2011,84(4):1112-1117.
[6]刘青,曾广丰,王志元.QuEChERS 净化技术结合高效液相色谱-串联质谱法测定食用贝类产品中4 种脂溶性贝类毒素[J].现代食品科技,2015,31(12):338-344.
[7]王鸿雁.固相萃取串联高效液相色谱检测谷物中杂色曲霉毒素[J].食品科学,2017,38(2):29-31.
[8]赵亚荣,石阶平,黄健祥.高效液相色谱-串联质谱法测定大米与小米中柄曲霉素残留[J].分析测试学报,2016,35(8):1041-1045.
[9] OPLATOWSKA S M,SAJIC N,XU Y,et al.Fast and sensitive aflatoxin B1 and total aflatoxins ELISAs for analysis of peanuts,maize and feed ingredients[J].Food Control,2016,63:239-245.
[10]MATUMBA L,VAN POUCKE C,BISWICK T,et al.A limited survey of mycotoxins in traditional maize based opaque beers in Malawi[J].Food Control,2014,36(1):253-256.
[11]黎睿,谢刚,王松雪.高效液相色谱法同时检测粮食中常见8 种真菌毒素的含量[J].食品科学,2015,36(6):148-151.
[12]李浩.免疫亲和柱层析净化-高效液相色谱法检测中药材中赭曲霉毒素A[J].中国药业,2015,24(12):61-63.
[13]VICTOR M D,LARA F J,GARCIA A M,et al.Evaluation of dispersive liquid-liquid microextraction for the determination of patulin in apple juices using micellar electrokinetic capillary chromatography[J].Food Control,2013,31(2):353-358.
[14]ANTEP H M,MERDIVAN M.Development of new dispersive liquid-liquid microextraction technique for the identification of zearalenone in beer[J].Anal Met,2012,12(4):4129-4134.
[15]FERNANDES P J,BARROSN,CMARA J S.A survey of the occurrence of ochratoxin A in Madeira wines based on a modified QuEChERS extraction procedure combined with liquid chromatography-triple quadrupole tandem mass spectrometry[J].Food Res Int,2013,54(1):293-301.
[16]ARROYO N,GAMIZ L,GARCIA A M.Determination of ochratoxin A in wines by capillary liquid chromatography with laser induced fluorescence detection using dispersive liquid-liquid microextraction[J].Food Chem,2012,135(2):368-372.
[17]王文珺,刘怡菲,韩霄,等.玉米赤霉烯酮一步ELISA 法的建立及应用[J].食品工业科技,2016,37(14):78-82.
[18]莫瑾,龚强,周慧平.高效液相色谱-串联质谱法检测茶叶中的赭曲霉毒素A[J].食品安全质量检测学报,2016,7(1):182-187.
[19]ANDRADE P D,DANTAS R R,MOURA-ALVES TLDSD,et al.Determination of multi-mycotoxins in cereals and of total fumonisins in maize products using isotope labeled internal standard and liquid chromatography/tandem mass spectrometry with positive ionization[J].J Chromatogr A,2017,1490:138-147.
[20]刘柱,陈万勤,沈潇冰,等.多功能柱净化-柱后光化学衍生-高效液相色谱法同时检测玉米和花生中9 种真菌毒素[J].分析科学学报,2014,30(2):168-172.
[21]孙雪,郗存显,唐柏彬,等.复合免疫亲和柱净化-液相色谱-串联质谱法测定动物源食品中6 种黄曲霉毒素和6 种玉米赤霉醇类真菌毒素残留量[J].分析化学,2016,44(6):970-978.
[22]苏碧玲,谢维平,欧阳燕玲.QuEChERS 净化-超高效液相色谱-串联质谱法测定婴幼儿谷类辅助食品中12 种真菌毒素[J].中国食品卫生杂志,2016,28(4):467-471.
[23]刘笑笑,丁辉,吴福祥,等.杂质吸附固相萃取-液相色谱串联质谱法同时测定粮食中15 种真菌毒素[J].粮油食品科技,2020,32(1):160-167.
[24]李单单,贺金涛.高效液相色谱法测定枸杞中的黄曲霉毒素[J].农产品加工,2020,23(4):231-235.
[25]李莉,李硕.分散固相萃取-超高效液相色谱-串联质谱法同时测定玉米油中4 种黄曲霉毒素[J].化学分析计量,2020,29(6):231-238.