我国是水果和蔬菜生产和消费大国,水果年产量达1.5亿t,蔬菜年产量超过6亿t。农药是果蔬生产的必要保障,菊酯类农药作为第二大杀虫剂类农药,由于其具有杀虫谱广、药效迅速、药效时间长、抗性低、对光和热稳定等特点,使用量占据了近30%的农药市场,被广泛应用于蔬果除虫防治[1-3]。由于菊酯类农药的大量和大范围使用,暴露于环境中的菊酯是引起人类和动物慢性毒性效应的主要因素,而且,菊酯类被报道是水环境中具有最高生态毒理学活性的农药[4-6]。此外,菊酯还会对生物构成累积风险,甚至在陆地生物、海洋哺乳动物和沉积物中也能发现[7]。已报道的菊酯的毒性效应和健康风险有:神经毒性、细胞毒性、基因毒性、生殖毒性、生长发育毒性、代谢毒性、摄入风险、残留风险、致癌风险等。因此水果蔬菜菊酯类农药残留监管显得尤为重要[8-10]。
国家卫健委、农业农村部及市场监管总局联合发布的GB 2763—2019《食品安全国家标准食品中农药最大残留限量》中明确规定了11种菊酯类农药及其同分异构体在蔬菜水果中的使用范围和最大使用量。即使国家强制标准中已有限量要求,但是食用农产品中菊酯类农药的残留量超标事件一直屡禁不止,根据全国抽检数据显示菊酯类农药经常被使用于韭菜、芹菜、青椒、豇豆、梨、柑橘,且不合格率的问题较为突出[11-12]。
目前蔬菜水果中菊酯类农药残留量的检测多采用气相色谱法、气相色谱-质谱法、液相色谱-质谱法等[13-15],这些方法虽具有结果准确可靠、检测限低,但其方法样品前处理繁琐耗时,仪器昂贵庞大,检测费用成本高,环境条件和人员技能要求高,不能适应大批量样品的现场快速检测要求,因此迫切需要开发简便高效的快检方法,填补蔬菜水果中菊酯类的快速检测方法规范性文件的缺失[16-18]。目前市面上流通的蔬菜水果中菊酯类快检试剂盒,主要采用的是胶体金免疫层析法,由于缺乏统一的检验方法的约束,产品质量参差不齐、好坏难辨,准确度不高,检出限虚标[19-20],无法满足同时检测一类菊酯农残的市场需求,本快检检测方法的研制势在必行。本研究将选购市场上常见的菊酯类农残快速检测产品,对快速检测蔬菜水果中菊酯农残的前处理步骤进行研究和简化,同时对胶体金方法检测性能进行技术上统一规定,考察每种快检产品在果蔬基质样品检测中的灵敏度、特异性、假阳性率、假阴性率和准确度,同时考察产品的适用性,另外对各快检产品进行整体性评价,旨在为水果蔬菜中菊酯类农残日常监管、重大活动保障、案件稽查提供简便、快捷、准确的技术支撑,提高监管效能。
1 材料与方法
1.1 材料与试剂
本试验所用蔬菜、水果样品:市售(经GB 23200.113—2018《植物源性食品中208种农药及其代谢物残留量的测定气相色谱-质谱联用法》测试,本次所购蔬菜本底不含本方法中的11种菊酯类农药);氟胺氰菊酯、氟氯氰菊酯和高效氟氯氰菊酯、氟氰戊菊酯、甲氰菊酯、联苯菊酯、氯氟氰菊酯和高效氯氟氰菊酯、氯菊酯、氯氰菊酯和高效氯氰菊酯、醚菊酯、氰戊菊酯和顺式氰戊菊酯、溴氰菊酯11种菊酯农药及其同分异构体标准品(纯度均≥99%):农业部环境保护科研监测所;氯化钠、乙腈、甲醇、乙酸乙酯、丙酮、曲拉通、硼砂、磷酸氢二钠、磷酸二氢钠、Tris-盐酸(纯度均≥99%):国药集团化学试剂有限公司。
1.2 仪器与设备
B114127491电子天平:梅特勒-托利多国际贸易有限公司;YPNSY-12携式样品浓缩仪:金坛区西城新瑞仪器厂;FSJ-A05N6小熊牌粉碎机:天猫旗舰店;5811FN879374冷冻离心机:德国艾本德公司。
1.3 方法
本方法采用竞争抑制免疫层析原理。样品中菊酯类农残与胶体金标记的特异性抗体发生结合,抑制了抗体与试纸条/检测卡中检测线(T线)上抗原的结合,从而导致T线颜色深浅的变化。通过T线与控制线(C线)颜色深浅比较,对样品中的菊酯类农残进行定性判定。
1.3.1 前处理方法
(1)直接稀释法:称取5 g捣碎蔬菜、水果样品于50 mL塑料离心管中,加入5 mL稀释液(Tris-盐酸缓冲溶液,pH 8.5),充分振荡混匀,用于测定。
(2)直接提取法:称取5 g捣碎蔬菜、水果样品于50 mL塑料离心管中,加入5 mL提取液(乙腈∶乙酸乙酯=2∶8),涡旋混匀,加入1.5 g NaCl剧烈振荡数次,4 000 r/min离心5 min。准确吸取2.5 mL上清液于10 mL离心管中,40 ℃下空气吹至近干,加入1 mL稀释液进行复溶,用于测定。
1.3.2 提取条件优化
(1)提取溶剂的选择
考察4种提取溶剂乙腈、甲醇、乙酸乙酯和丙酮对菊酯类农药的提取效果,选择最佳提取溶剂。
(2)提取试剂的优化
比较当5 mL提取剂中乙腈与乙酸乙酯体积比为5∶5、4∶6、3∶7、2∶8以及纯乙酸乙酯对模拟阳性样本中11种菊酯提取率的影响,选择最佳提取试剂。
(3)稀释液的选择
比较pH 8.5的Tris-盐酸溶液、0.5%曲拉通-硼砂缓冲溶液、0.5%曲拉通-磷酸盐缓冲溶液3种稀释液对样品进行处理后胶体金试纸条的显色效果,选择最佳稀释液。
(4)加样量的选择
取菊酯质量浓度为2 mg/kg的模拟样品,比较当样品加样量分别为80 μL、120 μL、200 μL、240 μL加于金标微孔时试纸条的显色反应,选择最佳加样量。
1.3.3 提取率的计算
提取率的计算公式如下:
1.3.4 检出限测定
取菊酯质量浓度为1 mg/kg、2 mg/kg、4 mg/kg(其中甲氰菊酯的质量浓度达到0.25 mg/kg、0.5 mg/kg、1.0 mg/kg)的模拟样品,按照前处理方法和分析步骤进行处理,观察试纸条最终的显色效果。
1.3.5 试剂条测定
吸取上述待测液200 μL于金标微孔中,抽吸5~10次混匀,3 min后将试纸条插入微孔中。6 min后进行结果判定。检测线(T线)颜色比控制线(C线)颜色深或者检测线(T线)颜色与控制线(C线)颜色相当,表明样品中菊酯类残留量低于方法检测限,判定为阴性;检测线(T线)不显色或检测线(T线)颜色比控制线(C线)颜色浅,表明样品中菊酯类残留量高于方法检测限,判定为阳性;控制线(C线)不显色,表明不正确操作或试纸条无效。
1.3.6 实验方法学研究
(1)产品方法性能指标的测定
称取以大白菜、韭菜和柑橘为代表的空白基质样品,11种菊酯混标制成添加水平为0、1 mg/kg、2 mg/kg和4 mg/kg的盲样样品各50份,共计600份样品。按上述前处理方法和测定方法进行测定。
(2)交叉反应
制备5 g大白菜、韭菜、柑橘的空白基质样品,分别添加10 μg、20 μg、40 μg苯、萘、乙酸乙酯、有机磷酸酯类农药(马拉硫磷、苯硫磷、喹硫磷)、氨基甲酸酯类农药(甲萘威、异丙威)的标准溶液,按照上述测定方法考察含有相同基团的物质对试剂盒的影响。
(3)环境温度的影响
利用菊酯混标添加量为1 mg/kg、2 mg/kg的模拟样品在14~40 ℃范围进行环境温度适应性考察,每份浓度样品进行3次平行测试。
(4)与参比方法一致性
称取以大白菜、韭菜、柑橘等为代表的空白基质样品,11种菊酯混标添加量为1 mg/kg、2 mg/kg的盲样样品各60份。分别用本研究建立的快检方法和标准参比方法GB 23200.113—2018《植物源性食品中208种农药及其代谢物残留量的测定气相色谱-质谱联用法》进行检测,对方法一致性进行研究。
2 结果与分析
2.1 前处理方法的比较
在韭菜、柑橘和大白菜的空白基质样品中添加菊酯类标准溶液,分别制成添加水平为0、2 mg/kg、4 mg/kg、8 mg/kg、10 mg/kg、20 mg/kg的样品,分别采用直接稀释法和直接提取法进行前处理,胶体金试剂条进行检测,以检出阳性结果最低值作为其检出限,结果见表1。结果表明,直接稀释法的检出限较高,达到10 mg/kg,无法满足检测要求;直接提取法检出限低至2 mg/kg,可满足现场检测的要求。
表1 前处理方法的检出限比较
Table 1 Comparison of detection limits for preprocessing methods
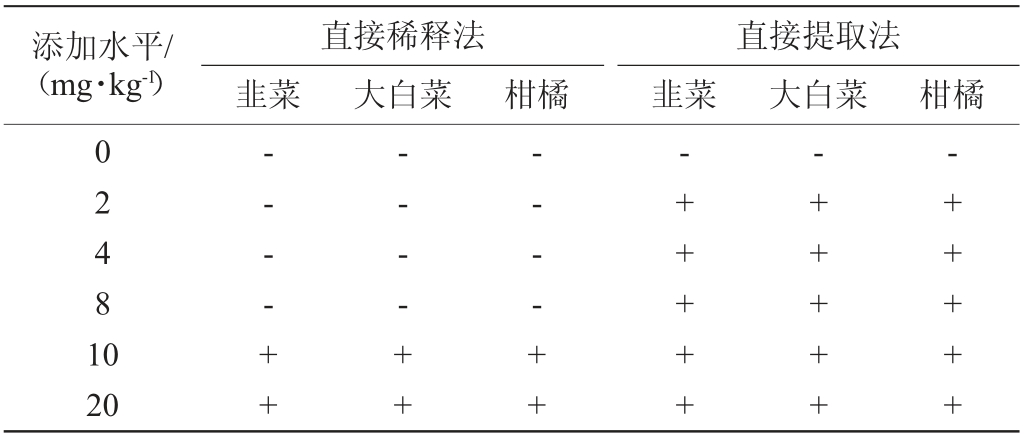
注:“+”表示结果呈阳性;“-”表示结果呈阴性。
2.2 提取溶剂的选择
利用胶体金试纸条和参比方法对比考察了4种不同浓度的提取溶剂(乙腈、甲醇、乙酸乙酯和丙酮)对甲氰菊酯类农药的提取效果,结果见表2。由表2可知,4种提取溶剂(乙腈、甲醇、乙酸乙酯和丙酮)对甲氰菊酯的提取效果为:乙腈>乙酸乙酯>丙酮>甲醇;其中乙腈对甲氰菊酯的提取回收率可达98%~102%;考虑乙腈空气吹干速度慢,而乙酸乙酯吹干速度较快,因此,综合考虑本实验采用乙腈与乙酸乙酯复合溶剂作为提取溶剂。
表2 不同提取溶剂对甲氰菊酯提取效果比较
Table 2 Comparison of extraction effects of cypermethrin with different extraction solvents
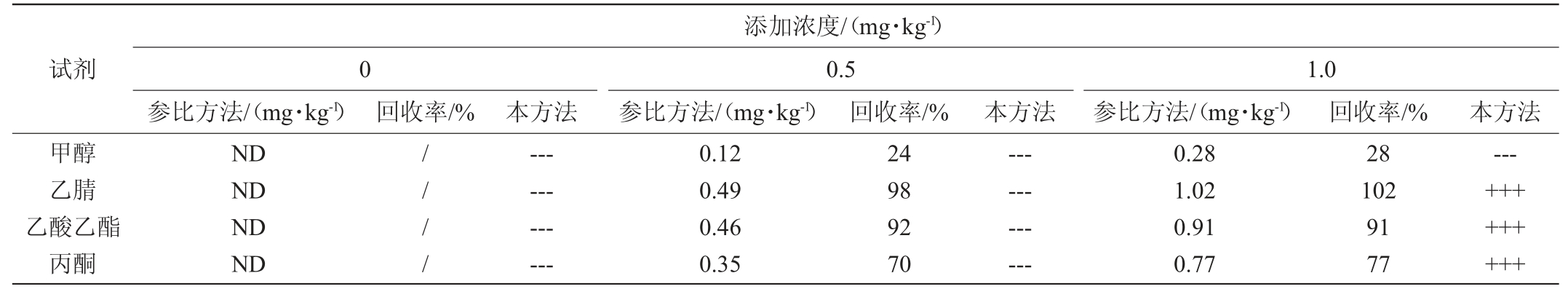
注:“ND”表示未检出;“+”表示结果呈阳性;“-”表示结果呈阴性;“---”和“+++”分别表示重复3次结果阴性和阳性。
2.3 提取试剂的优化
比较5 mL提取剂中乙腈与乙酸乙酯不同配比对模拟阳性样本中11种菊酯提取率的影响,结果见图1。由图1可知,当5 mL提取剂中乙腈与乙酸乙酯体积比为5∶5、4∶6、3∶7、2∶8和纯乙酸乙酯时,11种菊酯的提取率无显著性变化,考虑到吹干速率和环保低毒的要求,同时乙酸乙酯的毒性低于乙腈,尽量选择对环境和实验人员友好的溶剂配比,因此最终采用的提取剂中乙腈与乙酸乙酯最佳体积比为2∶8。
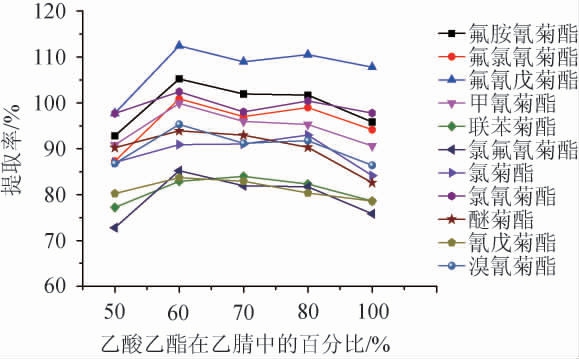
图1 乙腈与乙酸乙酯不同体积积比对11种菊酯提取率的影响
Fig.1 Effect of different volume ratios of acetonitrile and ethyl acetate on extraction yield of 11 kinds of permethrins
2.4 稀释液的选择
考虑到11种拟除虫菊酯的理化性质以及硝酸纤维素膜(nitrocellulose filter membrane,NC)特性,选取终质量浓度为2 mg/kg的大白菜基质加标样,分别使用pH 8.5的Tris-盐酸溶液,0.5%曲拉通-硼砂缓冲溶液,0.5%曲拉通-磷酸盐缓冲溶液这3种稀释液对样品进行处理后,经胶体金试纸条检测后结果见图2。
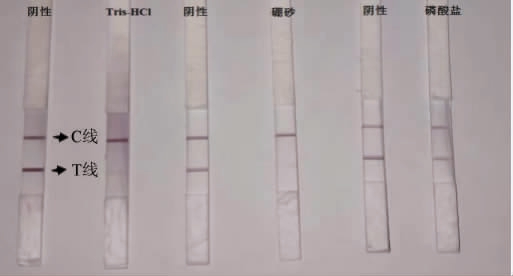
图2 三种稀释液显色情况
Fig.2 Color rendering of three diluents
由图2可知,用硼砂缓冲溶液混合试剂作为稀释液时,C线较浅;用磷酸盐缓冲溶液混合试剂作为稀释液时,阳性样中T线没有明显浅于C线,不利于判断,而用Tris-盐酸溶液作为稀释液时,T线和C线显色稳定,颜色均匀,区分度明显,有利于结果判定,故选用Tris-盐酸溶液作为稀释液。
2.5 加样量的选择
结果表明,当加样量为80 μL时,胶体金试纸条表现出层析速度较慢,且T线附近底色呈现较深红色;当加样量为120 μL时,C线显色,但颜色较浅;当加样量为240 μL时,NC膜吸附样液色素过多导致试纸条背景色太深,上述情况均不利于显色结果的观察和判断。而当取样量为200 μL时,检测结果重复性好,C线和T线颜色区分明显,利于判断。因此,待测液的加样量选择200 μL。
2.6 检出限测定
由图3可知,10种菊酯质量浓度为2 mg/kg,甲氰菊酯质量浓度为0.5 mg/kg时,C线显色明显且T线不显色,为阳性结果,因此,11种菊酯及其同分异构体的检出限为2 mg/kg(其中甲氰菊酯的检出限为0.5 mg/kg)。
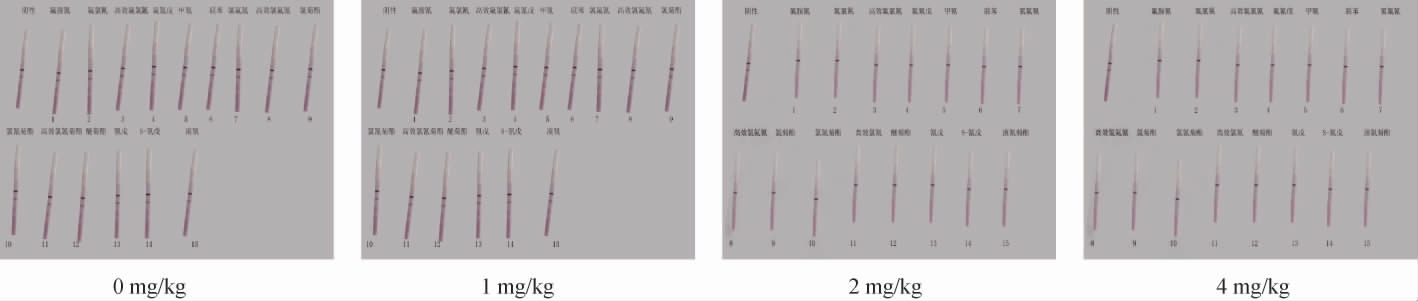
图3 11种菊酯及其同分异构体的试纸条显色情况
Fig.3 Color rendering of test strips of 11 permethrins and their isomers
2.7 产品方法性能指标的测定
由表3可知,大白菜、韭菜和柑橘基质阳性样品均检出300个阳性结果,假阴性率均为0;大白菜、韭菜和柑橘基质阴性样品均检出300个阴性结果,假阳性率均为0;并且优化后的检测方法测定的大白菜、韭菜和柑橘基质样品灵敏度、特异性均为100%。上述性能指标均符合食药监科便函[2017]43号《食品快速检测方法评价技术规范》[21]的技术要求。
表3 方法性能指标的计算结果
Table 3 Calculation results of performance indexes of the methods
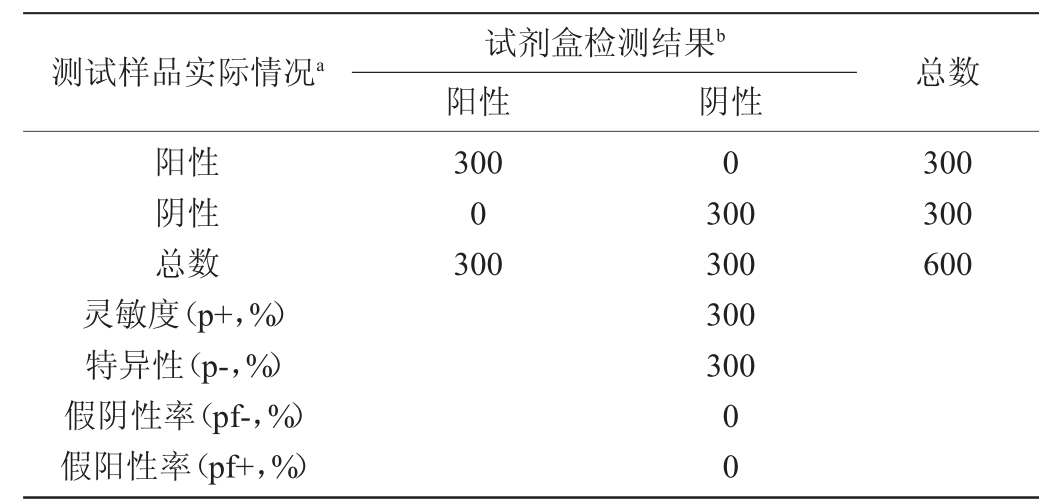
注:a表示参考方法的检测结果,b表示试剂盒方法的检测结果。
2.8 交叉反应
根据文献资料以及菊酯类农药的化学结构分析,考虑到菊酯可能与含有苯环、酯键、间苯氧基的结构的物质存在交叉反应,当萘、乙酸乙酯、有机磷酸酯类、氨基甲酸酯类标准品添加水平在2 mg/kg时,进行菊酯类胶体金试纸条交叉反应测试,结果如图4所示。结果表明,菊酯类胶体金试纸条判定结果均为阴性,上述结构的物质及农药与本方法的试剂盒无交叉反应。
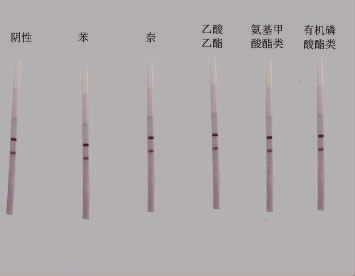
图4 交叉反应试纸条显色情况
Fig.4 Color rendering of cross reaction test strips
2.9 环境温度影响
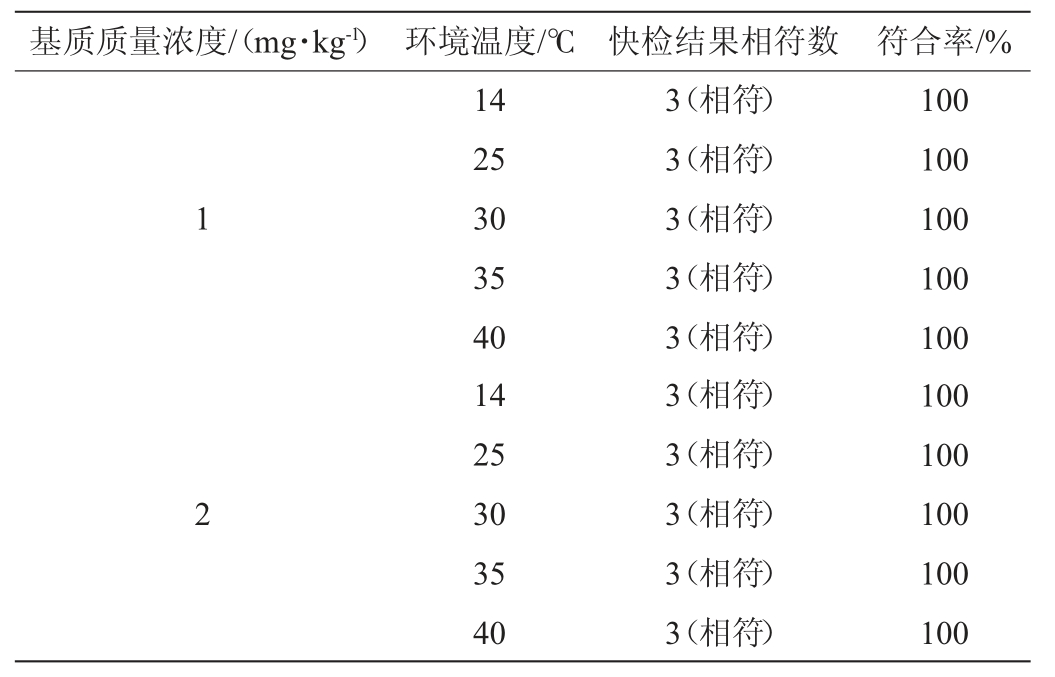
由表4可知,本方法对环境温度不敏感,环境温度14~40 ℃之间均可,测定3次的快检结果与国标结果均相符,符合率为100%。
表4 温度耐变性实验结果
Table 4 Results of temperature variability test
2.10 与参比方法一致性分析
分别用建立的快速检测方法与标准参比方法GB 23200.113—2018《植物源性食品中208种农药及其代谢物残留量的测定气相色谱-质谱联用法》检测6种不同基质的果蔬阴性样品和模拟阳性样品,结果表明,菊酯类农残胶体金试纸条的检测结果与参比方法检测结果的符合率为100%,通过卡方检验得出x2=0,即本方法与参比方法的阳性确证比率在95%的置信区间内没有显著性差异,方法的假阳性率、假阴性率均为0,表明该方法选择性强,准确度高,胶体金卡/试纸条能够有效应用于蔬菜水果中菊酯类农残的现场检测。
3 结论
选用蔬菜(韭菜、大白菜和芹菜)及水果(柑橘、苹果、梨)作为研究对象,对11种菊酯及其同分异构体的胶体金快速检测试剂盒产品进行方法学研究。研究表明,直接提取法在检测蔬果时,检出限较低,能够满足日常监管检测需要;在前处理条件优化下,菊酯类胶体金快检检测方法的检出限可以达到2 mg/kg;该方法的灵敏度为100%,特异性为100%,假阳性率为0,假阴性率为0。交叉反应率结果显示萘、乙酸乙酯、有机磷酸酯类、氨基甲酸酯类与本方法试剂盒无交叉反应。环境温度适应性考察显示本方法对环境温度不敏感。同时,与参比方法进行一致性分析比较时,结果表明与参比方法阳性确证比例在95%的置信区间内没有统计学差异(P>0.05)。
本研究研制出菊酯类农药残留速测盒产品,该法操作简便、快速,样品只需进行简单的处理,然后采用速测试剂进行检测,20 min内即可出结果。此外,该产品灵敏度高,对常见拟除虫菊酯类农药的最低检出限可达到2 mg/kg;检测样品时,其结果与气相色谱-质谱联用法的测定结果基本吻合,检测速度远快于气质联用法,适合于现场快速检测。
[1]胡静,郭逸蓉,梁晓,等.菊酯类农药广谱型免疫层析试纸条的研究及应用[J].分析化学,2016,44(12):1900-1906.
[2]季芯羽,叶泰,袁敏,等.菊酯类农药代谢物分子印迹荧光传感器的制备及应用[J].分析测试学报,2019,38(12):1487-1492.
[3]唐玮.果蔬中菊酯类农药-氯氰菊酯检测技术的研究进展[J].食品安全质量检测学报,2019,10(12):3739-3743.
[4]BARKOSKI J M,PHILIPPAT C,TANCREDI D,et al.In utero pyrethroid pesticide exposure in relation to autism spectrum disorder (ASD) and other neurodevelopmental outcomes at 3 years in the MARBLES longitudinal cohort[J].Environ Res,2020,11(4):95-103.
[5]IQBAL S,IQBAL M M,JAVED M,et al.Modified QuEChERS extraction method followed by simultaneous quantitation of nine multi-class pesticides in human blood and urine by using GC-MS[J].J Chromatogr B,2020,1152(1):122-129.
[6] GHANIM K A,SHAHID M,VIJAYARAG H P,et al.Sub-lethal effect of synthetic pyrethroid pesticide on metabolic enzymes and protein profile of non-target Zebra fish,Danio rerio[J].Saudi J Biol Sci,2020,27(1):441-447.
[7]ZHANG X Q,HAO X X,HUO S S,et al.Isolation and identification of the Raoultella ornithinolytica-ZK4 degrading pyrethroid pesticides within soil sediment from an abandoned pesticide plant[J].Arch Microbiol,2019,25(19):168-179.
[8]CURL C L,PORTER J,PENWELL I,et al.Effect of a 24-week randomized trial of an organic produce intervention on pyrethroid and organophosphate pesticide exposure among pregnant women[J].Environ Int,2019,115(132):104-113.
[9]BRAVO N,GRIMALT J O,BOCCA B,et al.Urinary metabolites of organophosphate and pyrethroid pesticides in children from an Italian cohort(PHIME,Trieste)[J].Environ Res,2019,32(176):108-117.
[10]PASUPULETI R R,TSAI P C,PONNUSAMY V K.A fast and sensitive analytical procedure for monitoring of synthetic pyrethroid pesticides'metabolites in environmental water samples[J].Microchemical J,2019,75(148):355-363.
[11]卢琦,李慧冬,丁蕊艳,等.基于QuEChERS 法前处理的GC-MS 检测梨中7 种菊酯类农药残留[J].农药,2019,58(5):356-358.
[12]赵宏梅,卞红正,方玲.QuEChERS-GC-MS/MS 方法测定蔬菜、水果中的联苯菊酯和溴氰菊酯农药残留[J].安徽农学通报,2019,25(8):94-97.
[13]许宝明,许元媛.气相色谱法测定地表水中痕量溴氰菊酯[J].污染防治技术,2018,31(6):90-92.
[14]黄芳茹.气相色谱法测定水中百菌清和溴氰菊酯的方法研究[J].海峡科学,2018(2):12-16.
[15]李世艳,唐刚.分散固相萃取-气相色谱法测定茶叶中氯氰菊酯残留量[J].现代农业科技,2018(5):103-105.
[16]陆单,叶泰,徐斐,等.基于猪肝酶杂化“纳米花”即时比色法检测氰戊菊酯[J].分析实验室,2020,39(10):1155-1159.
[17]季芯羽,叶泰,袁敏,等.菊酯类农药代谢分子印迹荧光传感器的制备及应用[J].分析测试学报,2019,38(12):1487-1492.
[18]胡静,郭逸蓉,梁晓,等.菊酯类农药广谱型免疫层析试纸条的研究及应用[J].分析化学,2016,44(12):1900-1906.
[19]殷玉洁.枸杞中菊酯类农药残留ELISA 检测方法研究[J].银川:宁夏医科大学,2017.
[20]谢俊平,黄秋婷,刘君,等.速测盒法快速检测果蔬中拟除虫菊酯类农药残留[J].中国卫生检验杂志,2016,26(9):1229-1231.
[21]国家食品药品监督管理总局.食药监科便函[2017]43 号《食品快速检测方法评价技术规范》[EB/OL].http://law.foodmate.net/show-190696.html.