灵芝(Ganoderma lucidum)又名仙草、瑞草,属灵芝属,多孔菌科真菌,其中包括赤芝和紫芝的干燥子实体[1]。属担子菌门(Basidionmycota),担子菌纲(Basidiomycetes),非褶菌目(Aphyllophorales),灵芝科(Ganodermataeea)类真菌。灵芝三萜类化合物是灵芝中除灵芝多糖外另一类重要的活性物质。它的基本构成是由30个碳原子组成,具有很高的脂溶性,其分子质量通常在400~600之间,具有比较复杂的化学结构,其结构由六个异戊二烯单位聚合而成。三萜类化合物大多数为四环和五环三萜,少数为链状、单环、双环和三环三萜[2]。灵芝三萜类化合物具有保肝护肝、抗肿瘤、增强免疫、抗氧化、降血脂血糖等功效[3-4],在食品生产加工以及临床医学领域具有广泛的应用前景。
三七(Panax notoginseng)药渣中含有大量的粗蛋白、粗纤维、粗多糖、粗脂肪等有机物和磷、钙、镁等矿质元素以及一些微量元素锌、锰等,适合作为发酵基质使用[5]。相关研究人员以三七渣为原料,变废为宝,成功开发了多种高附加值的产品[6-7]。采用灵芝固态发酵三七渣生产灵芝三萜可以为三七渣的资源化利用开辟一条新的途径,但三七渣的营养组成不能满足灵芝生长及灵芝三萜合成的需求。本研究以三七渣为基质,固体发酵生产灵芝三萜,通过单因素试验及Box-Behnken试验对三七渣固体培养基的制备条件进行了优化,使其更适合灵芝生长及灵芝三萜的合成。选择采用三七渣培养基产灵芝三萜,既能够实现三七渣的资源化利用,提高其附加值,又能够为灵芝三萜的生产提供一条新的低成本途径,以期为工业规模利用三七渣固态发酵生产灵芝三萜提供培养基组成的基础数据。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
川芝6号(国品认菌2007045,川审菌2004007):由四川省农业科学院土壤肥料研究所微生物室提供;三七渣:取自成都市某中成药厂,经日晒、烘干、粉碎、过筛后置于干燥器中备用,主要成分为真蛋白9.97%、粗蛋白12.28%、粗纤维27.45%、还原糖2.19%、总糖48.87%、淀粉30.35%[8]。
1.1.2 化学试剂
酵母浸出粉(生化试剂)、齐墩果酸(纯度>98%)、磷酸二氢钾、葡萄糖(均为分析纯):成都市科龙化工试剂厂。
1.1.3 培养基
种子液培养基:20 g土豆,2.0 g葡萄糖,0.3 g酵母粉,0.2 g蛋白胨,0.1 g KH2PO4,0.06 g MgSO4,1 000 mL蒸馏水。
121 ℃灭菌20 min。
马铃薯葡萄糖琼脂(potato dextrose agar,PDA)培养基:20g土豆,2.0g葡萄糖,0.3g酵母粉,0.2 g蛋白胨,0.1 gKH2PO4,0.06 g MgSO4,2.0 g琼脂粉,1 000 mL蒸馏水。121 ℃灭菌20 min。
三七渣固体培养基:采用过60目筛的三七渣10.00 g,酵母浸出粉3%,培养基初始含水量为60%,pH自然。121 ℃灭菌30 min。
1.2 仪器与设备
SF-130中药分析研磨机:长沙中南制药机械厂;PYX-280H-C恒温恒湿生化培养箱:广东韶关科力试验仪器有限公司;QYC—211水浴恒温振荡器:上海福玛实验设备有限公司;VT1300L-U超净工作台:苏州安泰空气技术有限公司:LDZX-50KB高压灭菌锅:上海申安医疗器械厂;UV-2550紫外可见分光光度计:日本SHIMADZU公司。
1.3 方法
1.3.1 菌种的活化
将川芝6号接入PDA培养基中,于28 ℃条件下恒温静置培养7~8 d,用于菌种的活化扩大培养。
1.3.2 种子液制备及固态发酵
用打孔器在PDA培养基的边缘打取0.25 cm2的灵芝菌丝块,接入装液量为100 mL/250 mL种子液培养基中,置于水浴恒温振荡器中,在150 r/min、28 ℃条件下振荡培养4 d,得到灵芝菌种子液。将川芝6号孢子种子液10%接种至三七渣固态发酵培养基,培养温度为28 ℃,培养时间为12 d。
1.3.3 发酵培养基组成优化
(1)单因素试验
分别考察三七渣固态发酵培养基中酵母浸出粉添加量(0、1%、2%、3%、4%、5%、6%)、磷酸二氢钾添加量(0、0.125%、0.250%、0.375%、0.500%、0.625%)、初始水含量(30%、40%、50%、60%、70%、80%)对灵芝三萜产量的影响。
(2)Box-Behnken试验[9]
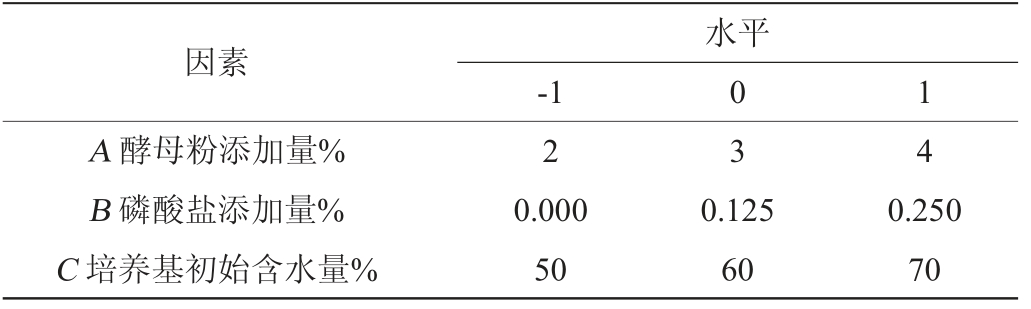
在单因素试验的基础上,以灵芝三萜产量(Y)为响应值,酵母粉添加量(A)、磷酸盐添加量(B)及培养基初始含水量(C)为自变量,采用响应面法优化发酵条件,并用-1、0、1对每个自变量的低、中、高3个水平进行编码,Box-Behnken试验设计因素与水平见表1。
表1 Box-Behnken试验设计因素与水平
Table 1 Factors and levels of Box-Behnken experiments design
1.3.4 灵芝三萜含量的测定[10-11]
准确称取0.50 g发酵培养物,置于50 mL比色管中,加入12.5 mL体积分数为75%乙醇进行超声处理(温度40 ℃;功率250 W;时间45 min),超声处理结束后,加体积分数为75%的乙醇溶液定容至50 mL,摇匀,再经过5 000 r/min离心10 min,取上清液保存备用。
吸取0.1 mL上清液置于比色管中(空白样加0.1 mL无水乙醇),用沸水浴加热煮干其中的溶剂,再依次加入5%的香草醛溶液0.2 mL、高氯酸0.8 mL,摇匀后放入水浴锅中60 ℃保温处理20 min。取出冷却,加5 mL冰乙酸,摇匀,在波长550 nm处测定其吸光度值。
以齐墩果酸为对照品,采用上述方法制作齐墩果酸标准曲线,按照齐墩果酸标准曲线回归方程计算发酵培养物中灵芝三萜的含量。
2 结果与分析
2.1 培养基优化单因素试验
2.1.1 酵母浸出粉添加量对灵芝三萜产量的影响
氮源是影响微生物酶合成的重要因素之一[12],相对于无机氮源而言,灵芝能够更好地利用有机氮源[13]。C/N对微生物的生长影响较大,适宜的C/N能够更好的促进菌体的生长及代谢产物的生成[14]。有研究表明酵母提取物是产生三萜类化合物的最佳氮源[15-16],因此本次研究按0、1%、2%、3%、4%、5%、6%的比例在三七渣中添加酵母浸出粉,进行固态发酵,考察其对发酵培养物中灵芝三萜产量的影响,结果如图1所示。
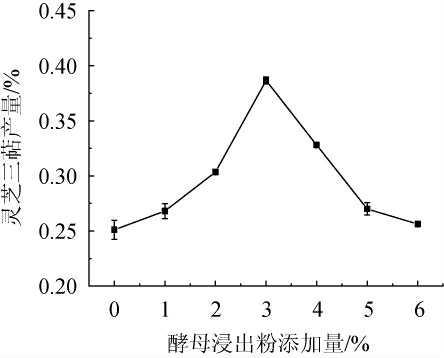
图1 酵母浸出粉添加量对灵芝三萜产量的影响
Fig.1 Effect of yeast extract powder addition on Ganoderma lucidum triterpenoids yield
由图1可以看出,酵母浸出粉添加量在0~3%范围内的增大,灵芝三萜的产量随之增加;当酵母浸出粉添加量为3%时,灵芝三萜产量达到最大值,为0.39%;当酵母浸出粉添加量>3%之后,灵芝三萜产量有所下降。这是因为适当的氮源有助于菌体的生长、发育和次级代谢,但当氮源过多时会使转录因子Are A在促进氮源代谢的过程时还会激活硝酸还原酶产生抑制灵芝三萜合成的NO,导致灵芝三萜产量降低[17-18],只有添加合适量的氮源才能够促进灵芝菌体的生长及灵芝三萜的合成。因此,最佳酵母浸出粉添加量为3%。
2.1.2 初始含水量对灵芝三萜产量的影响
培养基的初始含水量是影响固态发酵过程中次级代谢产物生产的重要因素之一[19]。本次试验中分别调节培养基的初始含水量为:30%、40%、50%、60%、70%、80%,考察培养基初始含水量对发酵培养物中灵芝三萜产量的影响,结果如图2所示。
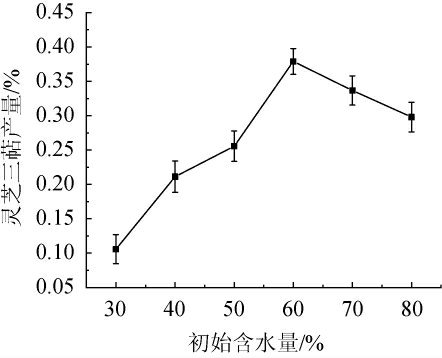
图2 初始含水量对灵芝三萜产量的影响
Fig.2 Effect of initial moisture contends on Ganoderma lucidum triterpenoids yield
由图2可以看出,当培养基初始含水量为30%~60%时,灵芝三萜的产量随之增加;当培养基初始含水量为60%时,灵芝三萜产量达到最大值,为0.38%;当培养基初始含水量>60%之后,灵芝三萜的产量随之下降。这与采用中药渣发酵[20]、竹粉发酵[21]培养灵芝的研究结果相似。含水量过低或者过高都不利于灵芝三萜的生产,这是因为一方面,适当的含水量才有利于该体系热传递以及CO2、O2的交换;另一方面,三七渣基质颗粒间的自由水也能够作为良好的载体起到一定的传质作用。当基质中含水率过低时,基质中的自由水不足以维持灵芝的生长需求,进而破坏其新陈代谢平衡;当基质中含水率过高时,培养基容易黏结成团,从而影响物料的透气性,不利于微生物生长繁殖及代谢产物的生成[22]。因此,最佳培养基初始含水量为60%。
2.1.3 磷酸盐添加量对灵芝三萜产量的影响
磷元素是多种微生物细胞组成物质,如菌体核酸、蛋白、细胞膜等的重要成分[23];钙元素能够中和菌体生长过程中产生的有机酸,还有助于菌体细胞膜的稳定性[24];钾元素能够对细胞内酸碱度起到一定的调节作用,另外在酶促反应中还可作为辅助因子或激活剂。由此可见,无机盐是影响微生物菌体生长和繁殖的重要因素[25]。
本研究选取磷酸二氢钾作为磷源。在三七渣基质中按0、0.125%、0.250%、0.375%、0.500%、0.625%的比例添加KH2PO4,考察其对发酵培养物中灵芝三萜产量的影响,结果如图3所示。
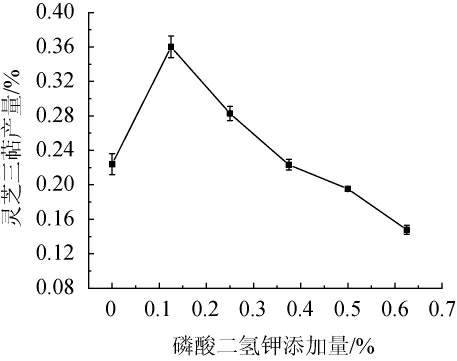
图3 磷酸二氢钾添加量对灵芝三萜产量的影响
Fig.3 Effect of potassium dihydrogen phosphate addition on Ganoderma lucidum triterpenoids yield
由图3可知,当磷酸二氢钾添加量为0~0.125%时,灵芝三萜的产量随着磷酸二氢钾添加量的增加而增加;当磷酸二氢钾添加量为0.125%时,灵芝三萜产量达到最大值,为0.36%;当磷酸二氢钾添加量>0.125%之后,灵芝三萜的产量随之下降。当磷酸二氢钾添加量继续增大,灵芝三萜含量会逐渐减少。可能的原因在于,磷元素添加过量,会导致渗透压的不平衡以及抑制参与中心代谢和次级代谢等的一系列基因的转录表达,从而对灵芝菌体的生长和代谢产物的合成起到抑制作用[26-27]。因此,最佳磷酸二氢钾添加量为0.125%。
2.2 培养基优化响应面试验
2.2.1 Box-Behnken试验设计与结果
在单因素试验的基础上,以灵芝三萜产量(Y)为响应值,酵母粉添加量(A)、磷酸盐添加量(B)及培养基初始含水量(C)为自变量,采用响应面法优化发酵条件,Box-Behnken试验设计及结果见表2,方差分析见表3。
表2 Box-Behnken试验设计与结果
Table 2 Design and results of Box-Behnken experiments
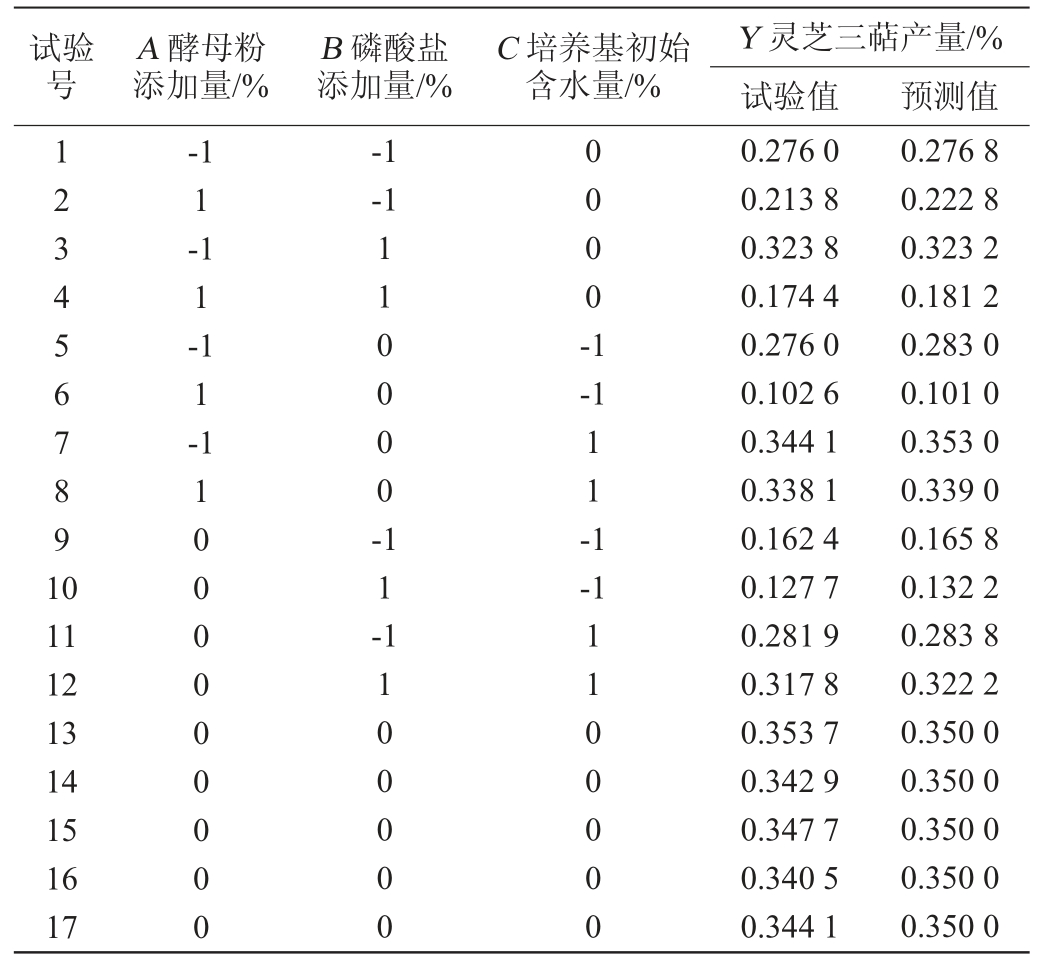
表3 回归模型的方差分析
Table 3 Variance analysis of regression model
注:“**”表示对结果影响极显著(P<0.01)。
通过Design-Expert8.0.6软件对表2中的试验数据进行多元回归拟合,得到灵芝三萜产量(Y)对酵母浸出粉的添加量(A)、磷酸盐的添加量(B)及培养基初始含水量(C)的多元回归方程:
由表3可知,该回归模型极其显著(P<0.0001),而失拟项不显著(P>0.05),决定系数R2=0.997 9,校正决定系数R2Adj=0.995 2,说明该模型可以解释大约99.52%的灵芝三萜含量响应值的变化。由此可见该二元回归模型可以用来分析与预测该发酵体系中灵芝三萜含量的实际情况。一次项A、C、交互项AB、AC、BC及二次项A2、B2、C2均对灵芝三萜含量的影响极显著(P<0.01);一次项B对灵芝三萜含量的影响不显著(P>0.05)。该三种因素对于灵芝三萜含量的影响程度排序为:培养基初始含水量(C)>酵母浸出粉添加量(A)>磷酸盐添加量(B)。
2.2.2 影响因素的交互作用分析[28-29]
利用Design-Expert 8.0.6软件绘制回归模型的三维响应面及等高线,考察不同因素之间的交互作用对灵芝三萜产量的影响,结果见图4。
由图4A可知,酵母浸出粉添加量与磷酸盐添加量交互作用极显著。当三七渣中酵母浸出粉和磷酸二氢钾添加量较少时,灵芝三萜含量较低。随着酵母浸出粉和磷酸二氢钾添加量的增加,灵芝三萜含量开始增加,但当二者添加到一定量之后灵芝三萜含量会有轻微下降。
由图4B可知,酵母浸出粉添加量和培养基初始含水量两者之间的交互作用极显著。当培养基初始含水量处于较低水平时,灵芝三萜的含量也较低。这是因为初始含水量低时,氮源等营养物质的溶解浸出及传递受阻,灵芝不能充分利用营养物质。
由图4C可知,磷酸二氢钾添加量和培养基初始含水量之间的交互作用极显著。当培养基初始含水量处于较低水平时,随着磷酸盐添加量的增加,灵芝三萜的含量先增加后减少,但整体处于一个较低的水平,可见磷酸盐添加量对灵芝三萜产量的影响不显著,这与回归模型方程显著性分析结果相同。
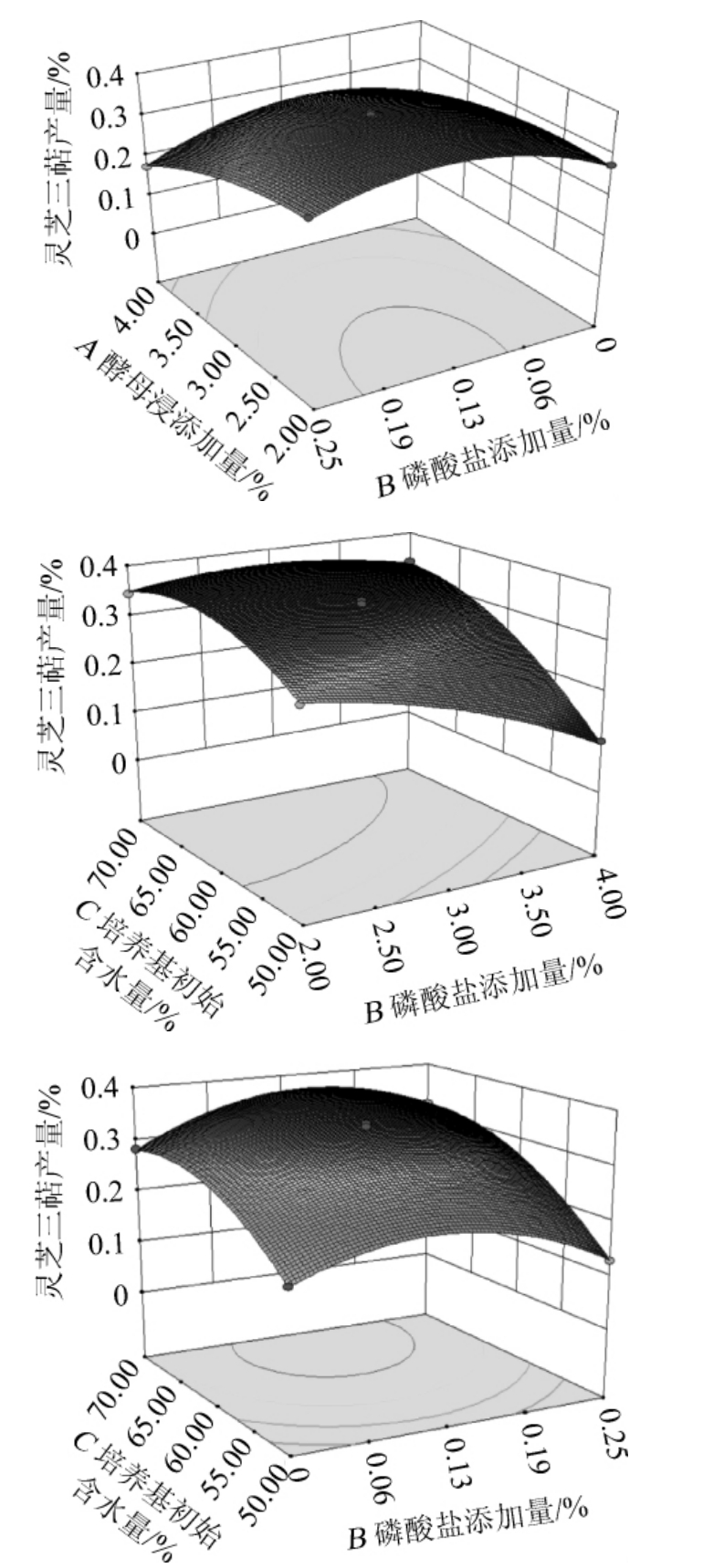
图4 酵母浸出粉添加量、磷酸盐添加量和培养基初始含水量交互作用对灵芝三萜产量影响的响应面及等高线
Fig.4 Response surface plots and contour lines of effects of interaction between the yeast extract addition,the phosphate addition and initial substrate moisture on Ganoderma lucidum triterpenoids yield
响应值对影响因素的敏感程度,可以由三维响应图中各影响因素曲面的陡峭程度来判断[30]。由图4可知,培养基含水量影响最为显著,其曲面最为陡峭,灵芝三萜含量随培养基含水量的变化而显著变化;酵母粉添加量的曲面较为陡峭,对灵芝三萜含量影响相对显著,但其曲面较于培养基含水量稍显平缓;磷酸盐添加量曲面坡度较于酵母粉添加量显平缓。该结论与回归模型分析结果一致,各因素对灵芝三萜含量的影响程度排序为:培养基初始含水量>酵母粉添加量>磷酸盐添加量。
通过对该多元回归模型方程求偏导与解逆矩阵,求得该模型的极值点:酵母浸出粉添加量为2.47%,磷酸二氢钾添加量为0.145%,培养基初始含水量为65.47%,在此优化条件下,发酵培养物中灵芝三萜产量的预测值为0.380%。考虑实际操作条件,将发酵条件调整为酵母浸出粉添加量为2.5%,磷酸二氢钾添加量为0.15%,培养基初始含水量为65%,在此优化发酵条件下,进行3次平行验证试验,发酵培养物中灵芝三萜含量实际值为0.367%,与预测值相差不大,比未优化前提高了0.013%。
3 结论
本次研究通过单因素试验,以灵芝三萜产量为评价指标,考察了酵母浸出粉添加量、培养基初始含水量、磷酸二氢钾添加量对固态发酵结果的影响,并通过响应面分析优化确定灵芝固态发酵三七渣生产灵芝三萜的培养基制备条件为:采用过60目筛的中药渣,酵母浸出粉添加量为2.5%,磷酸二氢钾添加量为0.15%,培养基初始含水量为65%。在此优化发酵条件下,发酵培养物中灵芝三萜含量为0.367%,比优化前提高了0.013%。
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:188.
[2]LI G H,LI Y,MEI X L,et al.Study progress on triterpenoids in Ganoderma lucidum[J].Chinese Tradition Herbal Drug,2015,46(12):1858-1862.
[3]WU Y L,HAN F,LUAN S S,et al.Triterpenoids from Ganoderma lucidum and their potential anti-inflammatory effects[J].J Agr Food Chem,2019,67(18):5147-5158.
[4] COR D,KNEZ Z,HRNCIC M K.Antitumour,antimicrobial,antioxidant and antiacetylcholinesterase effect of Ganoderma lucidum terpenoids and polysaccharides:A review[J].Molecules,2018,23(3):649-669.
[5]郭义东,冯兴,杨晓燕,等.中药渣综合利用研究进展[J].成都大学学报(自然科学版),2015,34(2):125-128.
[6] LI S J,WANG Y,DU G Y,et al.Production of single cell protein from Chinese medicinal herb residues by solid-state fermentation[J].J Chinese Med Mat,2016,39(1):59-62.
[7] HU W,TAN X D,HUANG F,et al.Enzymatic characteristics of amylase from notoginseng residues by solid state fermentation[J].J Chinese Cerea Oil Associat,2014,29(5):110-114.
[8]谭显东,胡伟,王浪,等.利用三七渣固态发酵灵芝菌的研究[J].环境污染与防治,2015,37(7):61-65,70.
[9]李莉,张赛,何强,等.响应面法在试验设计与优化中的应用[J].试验室研究与探索,2015,34(8):41-45.
[10]周晓,王成忠,李双,等.灵芝中三萜类化合物的研究进展[J].齐鲁工业大学学报,2014,28(4):47-50.
[11]SHEN S F,ZHU L F,WU Z J,et al.Production of triterpenoid compounds from Ganoderma lucidum spore powder using ultrasound-assisted extraction[J].Preparat Biochem Biotechnol,2020,50(3):302-315.
[12]张晓燕,李鑫,王静,等.碳源和氮源对固态发酵制备β-甘露聚糖酶的影响[J].南京林业大学学报(自然科学版),2015,39(4):143-148.
[13]解修超,贾少杰,彭浩,等.灵芝多糖液体发酵调控及药理作用研究进展[J].陕西理工大学学报,2018,34(6):65-70.
[14]王庆武,丛倩倩,谢新国,等.不同碳氮比培养基对泰山赤灵芝农艺性状的影响[J].中国食用菌,2017,36(2):27-29,32.
[15]任钰,郭昊,杨海波,等.樟芝产生三萜类化合物的液体培养条件的响应面法优化[J].基因组学与应用生物学,2019,38(5):2221-2229.
[16]冯杰,冯娜,贾薇,等.氮源对灵芝菌丝体液态深层发酵合成灵芝三萜的影响[J].菌物学报,2016,35(6):722-733.
[17]朱静,宋书琪,岳思宁,等.灵芝转录因子AreA 的生物学功能[J].菌物学报,2020,39(1):57-65.
[18]ZHU J,SUN Z H,SHI D K,et al.Dual functions of AreA,a GATA transcription factor,on influencing ganoderic acid biosynthesis in Ganoderma lucidum[J].Environ Microbiol,2019,21(11):4166-4179.
[19]李雪琪.固态发酵工程技术的研究应用分析[J].科技资讯,2019,17(11):219-220.
[20]杨宗渠,李长看,雷志华,等.灵芝固态发酵研究进展[J].北方园艺,2017(7):200-204.
[21]王超,许文静,余学军,等.灵芝发酵竹粉基质产菌质多糖的条件优化[J].中国食品学报,2014,14(3):94-99.
[22]YANG H L,MIN W H,BI P Y,et al.Stimulatory effects of Coix lacrymajobi oil on the mycelial growth and metabolites biosynthesis by the submerged culture of Ganoderma lucidum[J].Biochem Eng J,2013,76:77-82.
[23]翟双星,冯杰,冯娜,等.灵芝三萜液态深层发酵的研究进展[J].农学学报,2018,8(1):118-124.
[24]LI H J,ZHANG D H,HAN L L,et al.Further improvement in ganoderic acid production in static liquid culture of Ganoderma lucidum by integrating nitrogen limitation and calcium ion addition[J].Bioproc Biosyst Eng,2016,39(1):75-80.
[25]PALIYA B S,CHAUDHARY H S,VERMA S,et al.Optimization of fermentation media composition of Ganoderma lucidum for improved production of antioxidant and antimicrobial compounds[J].Pharmacog Communicat,2014,4(1):35-41.
[26]尹守亮,张玉秀,张琪,等.无机磷酸盐对链霉菌合成次级代谢产物的影响[J].中国生物工程杂志,2015,35(9):105-113.
[27]KAMLESH K Y,NEELIMA S,RAM R.Responses to phosphate deprivation in yeast cells[J].Curr Genet,2016,62(2):301-307.
[28]MUSTAFA S R,HUSAINI A,HIPOLITO C N,et al.Application of response surface methodology for optimizing process parameters in the production of amylase by Aspergillus flavus NSH9 under solid state fermentation[J].Brazil Arch Biol Technol,2016,59(6):1-10.
[29] SEHRAWAT R,PANESAR P S,SWER T L,et al.Response surface methodology(RSM)mediated interaction of media concentration and process parameters for the pigment production by Monascus purpureus MTCC 369 under solid state fermentation[J].Pigment Resin Technol,2017,46(1):14-20.
[30]宋佳敏,王鸿飞,孙朦,等.响应面法优化金蝉花多糖提取工艺及抗氧化活性分析[J].食品科学,2018,39(4):275-281.