鸡枞菌(Collybia albuminosa)又名白蚁菇、鸡宗、鸡丝菇、三坛菌,主要分布于我国云南、四川、贵州等地区,是一种十分珍贵的食药用大型真菌[1-2]。现代研究表明,鸡枞菌含有人体必需的氨基酸、蛋白质、维生素、脂类、糖类、核黄酸、尼克酸、麦角甾醇以及钙、磷、铁等多种营养元素[3-5]。多糖是鸡枞菌中天然存在的物质,研究表明,鸡枞菌多糖具有降血脂[6]、增强机体免疫力[7]、预防动脉硬化[8]、抗菌消炎[9]、抗肿瘤[10]、抗氧化[11-12]、保护肝脏[13]等多种功能。鸡枞菌多糖主要是从菌丝体[14]和子实体[15-16]中提取,由于野生鸡枞菌数量少,栽培周期长,从中大规模提取多糖受到限制。近几年来,对鸡枞菌的研究已由菌种分离、液体培养条件等转向生物活性物质的研究,并取得了一系列研究成果。QI J等[17]从鸡枞菌子实体中分离到对小鼠PC12细胞具有不同神经抑制作用的脑苷脂。有研究表明,鸡枞菌菌丝体醇提物具有很好的清除自由基的能力[8,18]。
本试验通过液体深层发酵,研究鸡枞菌液体发酵培养基组成和发酵条件对胞外水溶性多糖产量的影响,并进一步探讨水溶性多糖与抗氧化的相关性,旨在为鸡枞菌液体发酵生产胞外水溶性多糖提供理论参考,同时为鸡枞菌胞外多糖的深度开发提供技术支持。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种
鸡枞菌(Collybia albuminosa)Z-1:保藏于湖南农业大学生物科学技术学院微生物研究室。
1.1.2 主要试剂
葡萄糖、蔗糖、麦芽糖、(NH4)2SO4、KH2PO4(分析纯):国药集团化学试剂有限公司;酵母提取粉、酵母膏、蛋白胨:上海盛思生化科技有限公司;苯酚(分析纯):天津恒兴化学试剂制造有限公司;MgSO4·7H2O(分析纯):湖南化学试剂总厂;1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picryl hydrazyl,DPPH)、2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐(diammonium2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonate,ABTS):合肥博美生物科技有限公司;玉米粉、玉米淀粉、豆粕粉(无虫蛀和霉变):市售;酵母粉:西安维特生物科技有限责任公司。
1.1.3 培养基
马铃薯葡萄糖琼脂(potatodextroseagar,PDA)培养基[19]:土豆200g,葡萄糖20g,琼脂粉20g,H2O1000mL,pH值自然。
液体种子培养基:土豆汁200 g/L,玉米粉10 g/L,酵母膏10 g/L,KH2PO4 1.5 g/L、MgSO4·7H2O 1.0 g/L,pH自然。
基础发酵培养基:葡萄糖5%,酵母膏2%,KH2PO40.15%,MgSO4·7H2O 0.1%,维生素B1 0.001%。
以上培养基均在115 ℃条件下灭菌30 min。
1.2 仪器与设备
72EE紫外可见光分光光度计:上海光谱仪器有限公司;himac CR 21G高速冷冻智能离心机:日本Hitachi公司;SX-500高压蒸汽灭菌锅:日本TOMY株式会社;QYC2112恒温振荡培养箱:上海福玛实验设备有限公司。
1.3 方法
1.3.1 培养方法
斜面菌种培养:将保存于4 ℃冰箱的菌种接种于斜面培养基上,30 ℃的恒温培养箱中培养5~6 d,备用。
液体种子培养:将培养成熟的斜面菌种接种于装有150 mL液体种子培养基的300 mL三角瓶中,30 ℃、160 r/min恒温振荡培养3 d。
发酵培养:按5%(V/V)接种量将培养好的液体种子接种于装有150 mL基础发酵培养基的300 mL三角瓶中,30 ℃、160 r/min恒温振荡培养5 d,3次重复。
1.3.2 产胞外多糖发酵条件研究
发酵方法同1.3.1,考察碳源种类(葡萄糖、蔗糖、麦芽糖、玉米淀粉、乳糖)及添加量(3%、4%、5%、6%、7%)、氮源种类(酵母膏、蛋白胨、酵母提取粉、豆饼粉、(NH4)2SO4)及添加量(1.0%、1.5%、2.0%、2.5%、3.0%)、KH2PO4添加量(0.05%、0.10%、0.15%、0.20%、0.25%)、MgSO4·7H2O(0、0.05%、0.1%、0.15%、0.2%)、接种量(3%、4%、5%、6%、7%)、装液量(110 mL/300 mL、130 mL/300 mL、150 mL/300 mL、170 mL/300 mL、190 mL/300 mL)、种龄(3 d、4 d、5 d、6 d、7 d)和发酵时间(3 d、4 d、5 d、6 d、7 d)对胞外多糖产量的影响。每个试验重复3次。
1.3.3 发酵条件优化响应面试验
在单因素试验结果的基础上,选择装液量(A)、种龄(B)和发酵时间(C)为自变量,以胞外多糖产量(R1)为响应值,依据Box-Benhnken中心组合设计原理,运用Design-Expert V12.0.3.0软件设计响应面试验,因素与水平见表1。
表1 发酵条件优化响应面试验因素与水平
Table 1 Factors and levels of response surface methodology for fermentation conditions optimization

1.3.4 胞外多糖测定
(1)发酵液预处理:将发酵液于10 000 r/min、4 ℃条件下离心15 min,取上清液用3倍体积的体积分数95%乙醇沉淀并置于4 ℃冰箱过夜,过滤,将沉淀于80 ℃条件下溶解,Sevag法脱蛋白后转移至100 mL容量瓶中定容。
(2)胞外多糖含量测定:参照文献[20]提供的方法进行。
1.3.5 胞外多糖体外抗氧化活性测定
DPPH自由基清除能力测定:参照文献[21]提供的方法进行测定;ABTS自由基清除能力测定:参照文献[22]提供的方法进行测定;OH自由基清除能力测定:参照文献[23]提供的方法进行测定。
1.3.6 数据处理
数据处理与显著性差异分析采用SPSS 12.0软件对结果进行分析。响应面优化设计分析利用Design Expert 12.0.3.0软件。
2 结果与分析
2.1 发酵条件研究
2.1.1 碳源种类对胞外多糖产量的影响
分别在基础发酵培养基中加入5%的蔗糖、麦芽糖、玉米淀粉、乳糖替代葡萄糖,其他条件不变,考察不同碳源对鸡枞菌产水溶性胞外多糖产量的影响,结果见图1。由图1可知,不同碳源对鸡枞菌发酵液中多糖产量影响较大,麦芽糖为碳源时,多糖产量最高,为291.67μg/mL。玉米淀粉次之,乳糖为碳源时,胞外多糖产量最低。因此,选择麦芽糖作为最适碳源。

图1 不同碳源对胞外多糖产量的影响
Fig.1 Effect of different carbon sources on exopolysaccharide yield
2.1.2 麦芽糖添加量对胞外多糖产量的影响
改变基础发酵培养基中麦芽糖添加量分别为3%、4%、5%、6%、7%,其他条件不变,考察麦芽糖添加量对鸡枞菌产水溶性胞外多糖产量的影响,结果见图2。由图2可知,在一定范围内,随着麦芽糖添加量的增加,胞外多糖产量也随之增加。当麦芽糖添加量为6%时,多糖产量最高,达384.35 μg/mL。但麦芽糖添加量超过6%,多糖产量下降明显。原因为过多添加碳源,改变了培养基中的碳氮比,从而影响鸡枞菌的生长和多糖的合成分泌。故选择最佳麦芽糖添加量为6%。
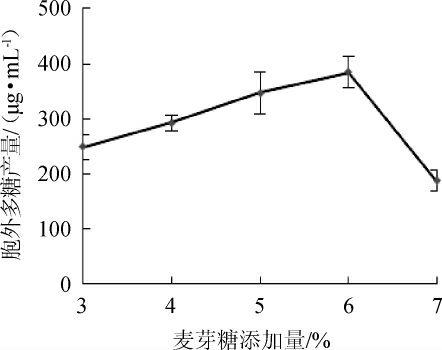
图2 麦芽糖添加量对胞外多糖产量的影响
Fig.2 Effect of maltose addition on exopolysaccharide yield
2.1.3 氮源种类对胞外多糖产量的影响
分别在基础发酵培养基中加入2%的蛋白胨、酵母提取粉、豆饼粉、(NH4)2SO4替代酵母膏,保持氮含量为0.22 g/100 mL,其他条件不变,考察不同氮源对鸡枞菌产水溶性多糖产量的影响,结果见图3。从图3可知,当酵母提取粉为氮源时,胞外多糖产量最高达420.49 μg/mL,酵母粉和酵母膏次之,故选择酵母提取粉作为最适氮源。
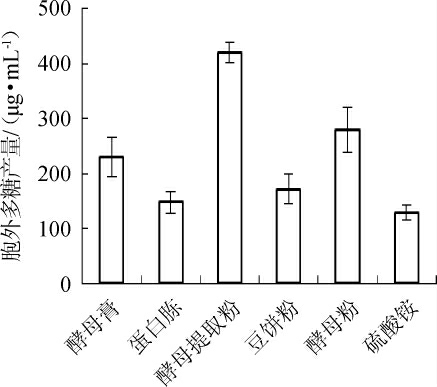
图3 不同氮源种类对胞外多糖产量的影响
Fig.3 Effect of different nitrogen sources types on exopolysaccharide yield
2.1.4 酵母提取粉对胞外多糖产量的影响
改变基础发酵培养基中酵母提取粉添加量分别为1.0%、1.5%、2.0%、2.5%、3.0%,其他因素不变,考察酵母提取粉添加量对鸡枞菌产水溶性胞外多糖产量的影响,结果见图4。由图4可知,鸡枞菌产胞外多糖产量随酵母提取粉添加量增加而减少,当酵母提取粉添加量为1.5%时,多糖产量达451.63 μg/mL,继续增加酵母提取粉添加量,多糖产量显著下降。主要原因为培养基中氮源浓度过高,导致菌体大量生长、发酵液变稠、溶氧水平下降,从而影响了鸡枞菌胞外多糖的合成和分泌。故选择最佳酵母提取粉添加量为1.5%。
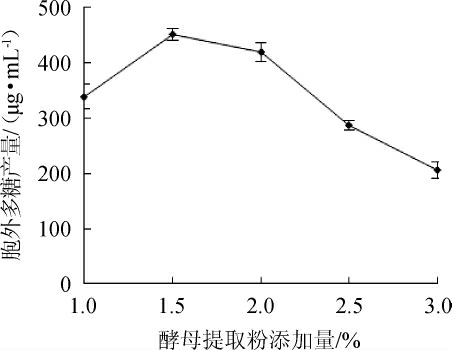
图4 酵母提取粉添加量对胞外多糖产量的影响
Fig.4 Effects of yeast extract addition on exopolysaccharide yield
2.1.5 KH2PO4添加量对胞外多糖产量的影响
磷是微生物生长、繁殖、代谢不可缺少的营养元素之一,适量的磷有利于微生物生长和代谢,若培养基中缺少磷,则影响微生物对碳源的利用,但磷过量则抑制代谢产物的合成,甚至对菌体产生毒性作用。改变基础发酵培养基中KH2PO4的添加量,其他条件不变,考察KH2PO4添加量对鸡枞菌产水溶性胞外多糖产量的影响,结果见图5。由图5可知,在一定范围内,多糖产量随KH2PO4添加量的增加而增加。当KH2PO4添加量为0.1%时,胞外多糖产量最高,达491.37 μg/mL,但KH2PO4添加量超过0.1%,多糖产量下降。故选择最佳KH2PO4添加量为0.1%。
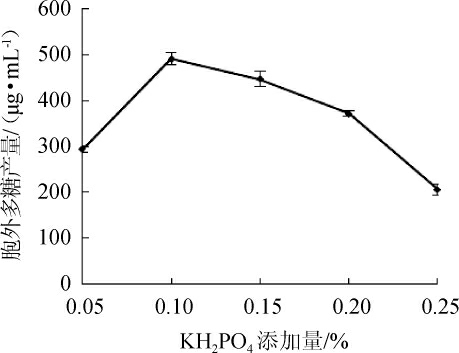
图5 KH2PO4添加量对胞外多糖产量的影响
Fig.5 Effect of KH2PO4 addition on exopolysaccharide yield
2.1.6 MgSO4·7H2O添加量对胞外多糖产量的影响
镁是微生物生长和代谢不可缺少的微量元素之一,也是微生物细胞内酶活性中心的组成部分,具有提高酶活性的功能。添加适量的镁元素,有助于菌体的生长和提高代谢活性,但浓度过高,一方面提高了培养基的渗透压,另一方面可能对菌体产生毒性,进而影响菌体代谢产物的合成。MgSO4·7H2O添加量对鸡枞菌产水溶性胞外多糖产量的影响见图6。由图6可知,当MgSO4·7H2O添加量为0.05%时,胞外多糖的产量达511.74 μg/mL,但添加量超过0.05%,多糖产量显著下降。故选择最佳MgSO4·7H2O添加量为0.05%。
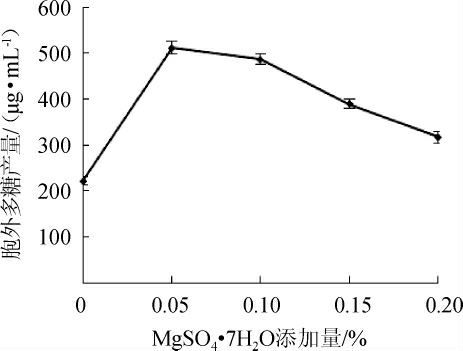
图6 MgSO4·7H2O添加量对胞外多糖产量的影响
Fig.6 Effect of MgSO4·7H2O addition on polysaccharide yield
2.1.7 接种量对胞外多糖产量的影响
在上述试验结果的基础上,改变接种量分别为3%、4%、5%、6%、7%,考察接种量对鸡枞菌产水溶性胞外多糖产量的影响,结果见图7。由图7可知,在一定的接种量范围内,随着接种量的增加胞外多糖产量随之增加。当接种量为6%时,胞外多糖产量最高,为521.33 μg/mL,但接种量超过6%,多糖产量下降。故选择最佳接种量为6%。
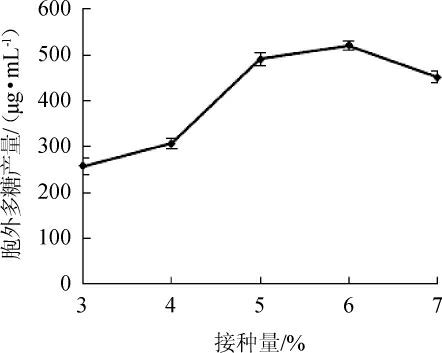
图7 接种量对胞外多糖产量的影响
Fig.7 Effect of inoculum on exopolysaccharide yield
2.1.8 装液量对胞外多糖产量的影响
在上述试验结果的基础上,于300mL三角瓶中分别装入110 mL、130 mL、150 mL、170 mL、190 mL发酵培养基,考察装液量对鸡枞菌产水溶性胞外多糖产量的影响,结果见图8。由图8可知,随着装液量的增加,多糖产量随之增加。当装液量为150 mL/300mL时,胞外多糖产量最高,为559.41 μg/mL,但装液量超过150 mL/300 mL时,多糖产量下降,原因为装液量太大,影响培养液中的溶氧量,从而影响菌体的生长及多糖的合成和分泌,故选择最佳装液量为150 mL/300 mL。
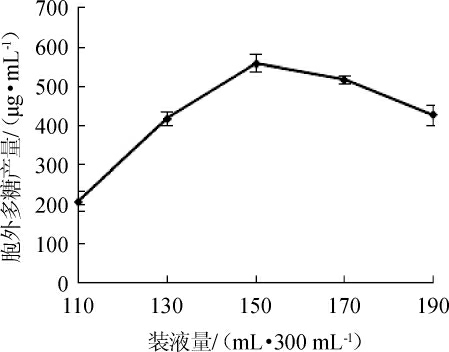
图8 装液量对胞外多糖产量的影响
Fig.8 Effect of liquid volume on exopolysaccharide yield
2.1.9 种龄对胞外多糖产量的影响
按5%接种量在基础发酵培养基中分别接入培养3 d、4 d、5 d、6 d、7 d的液体种子,考察菌株不同种龄对鸡枞菌产水溶性胞外多糖产量的影响,结果见图9。由图9可知,在一定的种龄范围内,胞外多糖含量随种龄的增加而增加。当种龄为5 d时,多糖含量达到591.24 μg/mL,但种龄超过5 d,多糖产量下降。其原因为种龄太小,种子液中细胞数量少,导致延迟期延长,而种龄太大,菌体自溶,同样会影响胞外多糖的合成和分泌,故选择最佳种龄为5 d。

图9 种龄对胞外多糖产量的影响
Fig.9 Effect of seed age on exopolysaccharide yield
2.1.10 发酵时间对胞外多糖产量的影响
在上述试验结果的基础上,分别于发酵的第3天、第4天、第5天、第6天、第7天取样,测定发酵液中胞外多糖的产量,考察不同的发酵时间对鸡枞菌产水溶性胞外多糖产量的影响,结果见图10。由图10可知,胞外多糖产量随发酵时间的延长而提高,当发酵时间为6 d时,发酵液中胞外多糖产量达679.27 μg/mL,但发酵时间超过6 d,多糖产量下降,可能是由于鸡枞菌自身产生了能降解胞外多糖的酶,使胞外多糖产量下降,故选择最佳发酵时间为6 d。

图10 发酵时间对胞外多糖产量的影响
Fig.10 Effect of fermentation time on exopolysaccharide yield
2.2 响应面优化试验结果
在单因素试验结果的基础上,以水溶性胞外多糖产量为响应值,选择对胞外多糖产量影响较大的因素装液量、种龄和发酵时间进行3因素3水平响应面优化试验。试验结果见表2。对回归方程进行方差分析,结果见表3。
表2 发酵条件优化响应面试验设计及结果
Table 2 Design and results of response surface methodology for fermentation conditions optimization
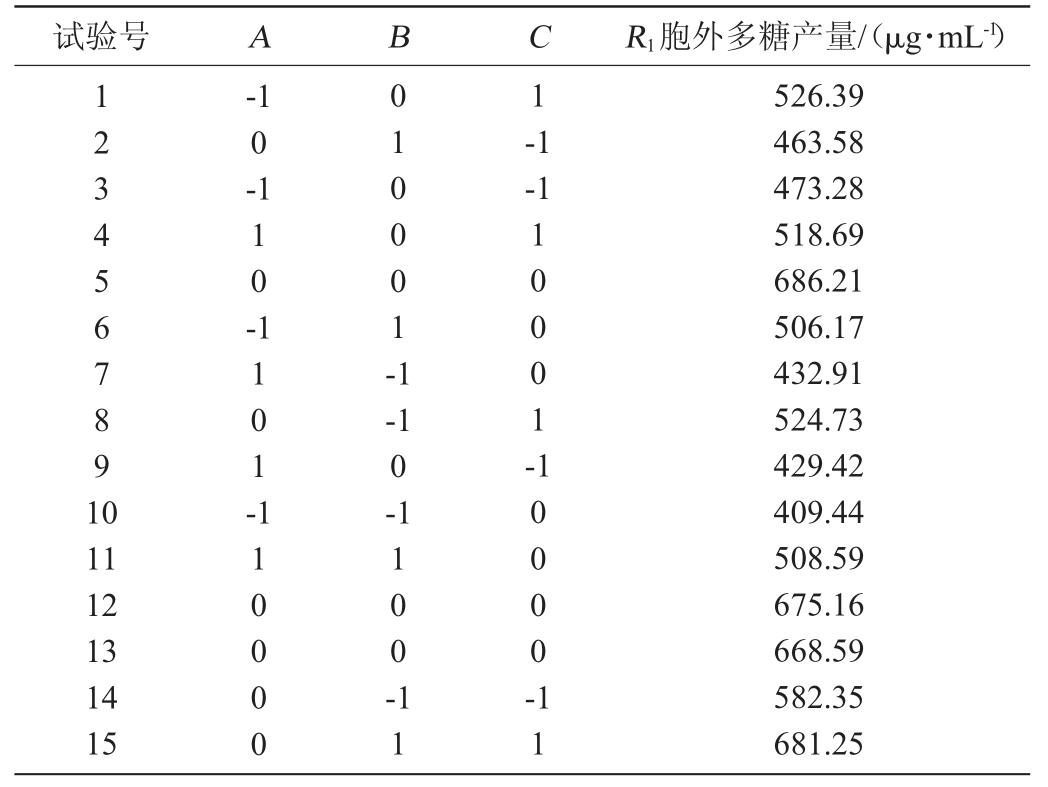
利用响应面Design-Expert V12.0.3.0软件对水溶性多糖产量进行多元回归拟合,获得胞外多糖的回归模型方程:
从表3可以看出,模型极显著(P<0.01),失拟项不显著(P>0.05),复相关系数R2为0.975 6,校正决定系数R2为0.931 8,说明模型方程拟合度良好。发酵时间对发酵产胞外多糖的影响最大,种龄次之,装液量最小。结合表中F值可知,发酵时间(C)、种龄和发酵时间的交互项(BC)、装液量的二次项(A2)和种龄的二次项(B2)为极显著影响因素(P<0.01),种龄(B)和发酵时间的二次项(C2)为显著影响因素(P<0.05),其他因素影响较小(P>0.05)。采用Design-Expert V12.0.3.0软件对胞外多糖产量的回归方程进行分析,装液量、种龄和发酵时间各因素交互作用的响应面图见图11。
表3 以水溶性多糖产量为评价指标的回归模型方差分析结果
Table 3 Results of variance analysis of regression model with water soluble polysaccharide yield as evaluation index
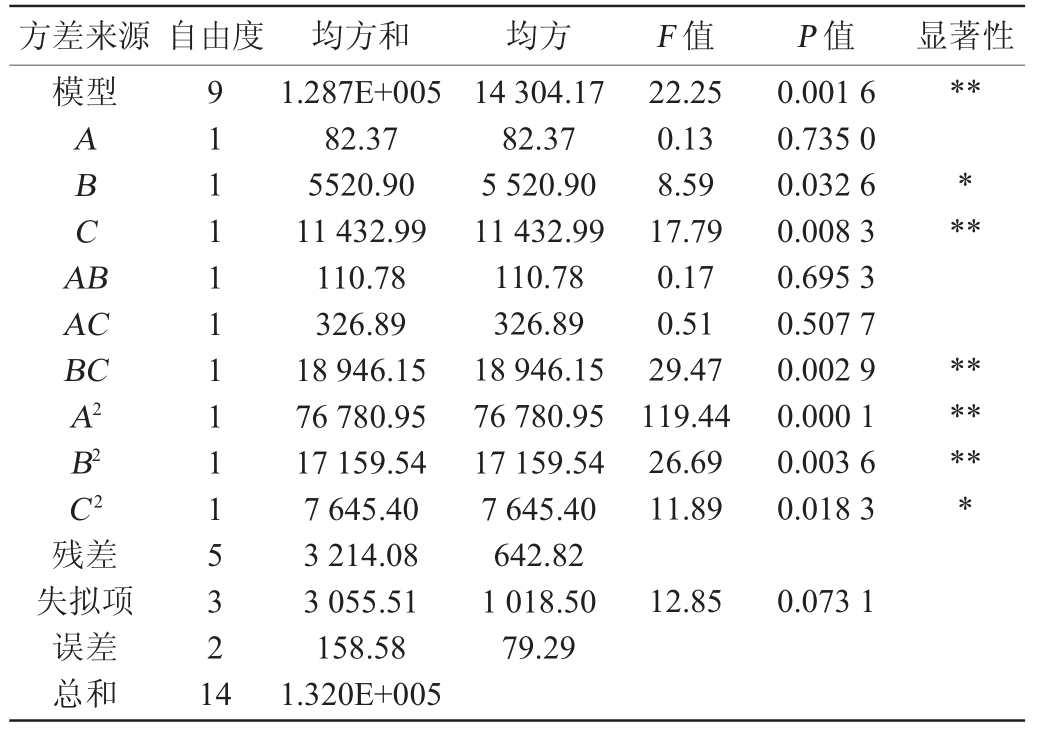
注:“**”表示对结果影响极显著(P<0.01);“*”表示对结果影响显著(P<0.05)。
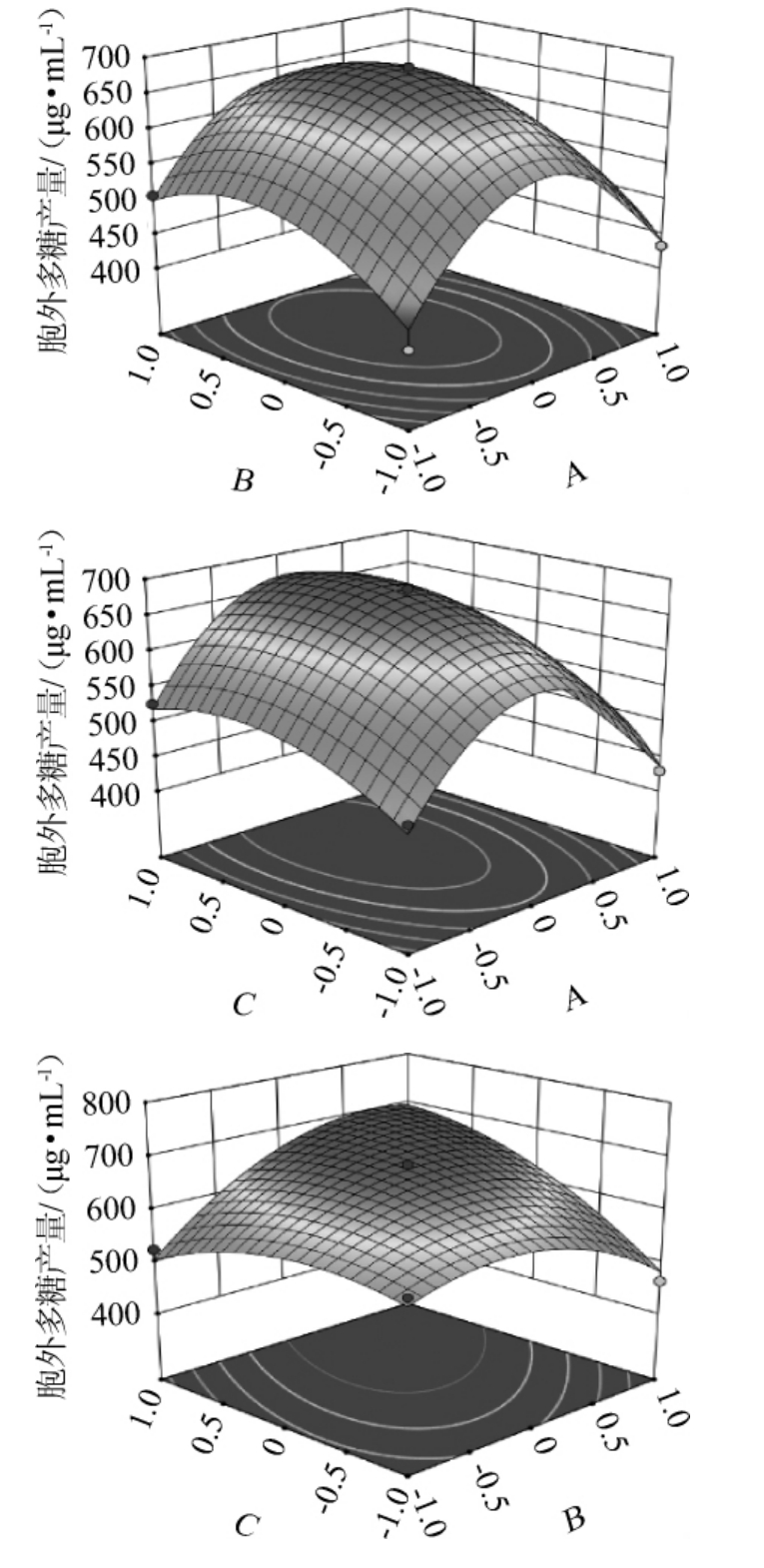
图11 各因素交互作用对胞外多糖产量影响的响应面和等高线
Fig.11 Response surface plots and contour lines of effects of interaction between each factor on exopolysaccharides yield
由图11可以看出,种龄和发酵时间之间的交互作用极显著(P<0.01),而装液量和种龄、装液量和发酵时间之间的交互作用均不显著(P>0.05)。通过Design-Expert V12.0.3.0软件对鸡枞菌液体发酵产胞外多糖工艺进行优化处理,以水溶性胞外多糖产量为评价指标,得到鸡枞菌液体发酵产胞外多糖的适宜工艺条件为:种龄5.07d,装液量149.58mL/300mL,发酵时间6.92 d,此时胞外多糖的理论产量为683.72 μg/mL。为了验证模型的可靠性,考虑实际操作情况,将发酵条件调整为种龄5 d,装液量150 mL/300 mL,发酵时间7 d,通过3次重复试验得到胞外多糖平均产量为671.57 μg/mL,与理论值相差1.78%。说明使用该回归模型优化鸡枞菌液体发酵产胞外多糖的条件是可行的。
2.3 胞外多糖抗氧化能力初步研究
2.3.1 DPPH自由基清除能力
由图12可知,鸡枞菌胞外多糖具有较强的DPPH自由基活性。随着胞外多糖浓度的增加,清除率显著提高。当胞外多糖质量浓度为1.2 mg/mL时,对DPPH自由基的清除率达到77.18%。

图12 胞外多糖浓度对DPPH自由基清除率的影响
Fig.12 Effect of exopolysaccharide concentration on DPPH free radical scavenging rate
2.3.2 ABTS自由基清除能力
由图13可知,在胞外多糖质量浓度0.2~0.6 mg/mL的范围内,随着多糖质量浓度的增加,ABTS自由基清除能力增强。但多糖浓度超过0.6 mg/mL时,对ABTS自由基清除能力增长减缓。当多糖质量浓度为1.2 mg/mL时,ABTS自由基清除率达95.74%。
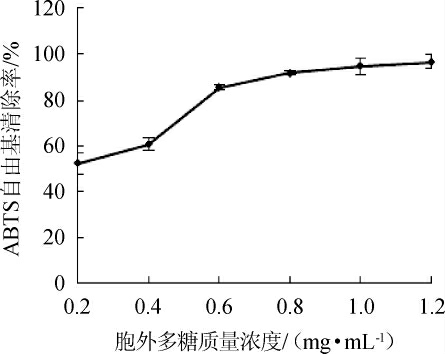
图13 胞外多糖浓度对ABTS自由基清除率的影响
Fig.13 Effect of exopolysaccharide concentration on ABTS free radical scavenging rate
2.3.3 OH自由基清除能力
由图14可知,随着胞外多糖质量浓度的增加,OH自由基清除率随之提高。当胞外多糖质量浓度为0.2~0.8 mg/mL范围内,OH自由基清除率增加迅速,但胞外多糖浓度增加,清除率增速放缓。当胞外多糖质量浓度为1.2 mg/mL时,OH自由基清除率达80.04%。
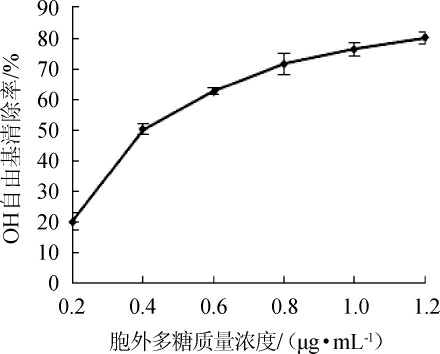
图14 胞外多糖浓度对OH自由基清除率的影响
Fig.14 Effect of exopolysaccharide concentration on OH free radical scavenging rate
3 结论
该研究通过单因素试验和响应面试验研究了鸡枞菌液体深层发酵产胞外多糖的培养基组成和发酵条件,并研究了其对DPPH,ABTS,OH自由基的清除效果。结果表明,最佳发酵培养基组成和发酵条件为麦芽糖6%,酵母提取粉1.5%,KH2PO4 0.1%,MgSO4·7H2O 0.05%,维生素B1 0.001%,接种量6%,装液量150 mL/300 mL,种龄5 d,发酵时间7 d。在此条件下,胞外多糖产量达671.57 μg/mL。抗氧化试验结果表明,鸡枞菌胞外多糖在质量浓度为1.2 mg/mL时,对DPPH、ABTS、OH自由基的清除率分别达77.18%、95.74%和80.04%,显示了鸡枞菌胞外多糖在天然保健品中的应用具有广阔的开发前景。
[1]胡尚勤,刘天贵,李贤柏.鸡枞菌的培养条件研究[J].食品与生物技术学报,2008,27(1):67-70.
[2]赵星.云南6 种鸡枞菌子实体与菌丝体呈味物质及液体培养的研究[D].昆明:云南大学,2015.
[3]耿燕,陆震鸣,许泓瑜,等.鸡枞菌液体发酵菌粉成分分析[J].食用菌学报,2013,20(2):60-63.
[4]李艳.HPLC 检测黑皮鸡枞菌中的水溶性维生素[J].食品研究与开发,2018(17):124-128.
[5]栗铭鸿,李官浩,朴守焕,等.鸡枞菌不同溶剂提取物成分分析及抗氧化作用研究[J].食品与机械,2018(1):144-148.
[6]王一心,杨桂芝,狄勇.鸡枞菌降血脂作用的实验研究[J].中华临床医学研究杂志,2003(8):1-2.
[7]鲁新成,何庆邦.鸡枞多糖的分离及其性质研究[J].贵州科学,1996,14(3):24-26.
[8] MAU J L,CHANG C N,HUANG S J,et al.Antioxidant properties of methanolic extracts from Grifola frondosa,Morchella esculenta and Termitomyces albuminosus mycelia[J].Food Chem,2004,87(1):111-118.
[9]陆奕宇,敖宗华,成成,等.鸡枞菌粉提取物镇痛抗炎作用的研究[J].中成药,2007,29(12):1742-1745.
[10]张灵芝.鸡枞菌子实体多糖分离纯化与结构分析及抗肿瘤活性研究[D].广州:华南理工大学,2009.
[11]ZHAO H,LI S,ZHANG J,et al.The antihyperlipidemic activities of enzymatic and acidic intracellular polysaccharides by Termitomyces albuminosus[J].Carbohydr Polym,2016,7:1227-1234.
[12]王思芦,王红明,赵艮勇,等.鸡枞菌多糖对鲫的生长性能、抗氧化及免疫功能的影响[J].淡水渔业,2019(1):87-91.
[13]赵云霞,陶明煊,程光字,等.鸡枞菌多糖对急性酒精引损伤小鼠超微病理结构及ADH2,ALDH2 mRNA 表达的影响[J].食品科学,2015,36(5):195-199.
[14]赵化杰.黑皮鸡枞菌菌丝体多糖的结构表征及慢性肝损伤修复研究[D].泰安:山东农业大学,2020.
[15]吴素蕊,严明,张鑫,等.响应面法优化水提黑皮鸡枞菌多糖工艺[J].食品工业,2016(5):169-172.
[16]张恒,郑俏然,李敏.响应面法优化超声波辅助提取鸡枞菌多糖及其抗氧化活性研究[J].食品与发酵科技,2017(2):13-18,121.
[17]QI J,OJIKA M,SAKAGAMI Y.Neuritogenic cerebrosides from an edible Chinese mushroom.Part 2:Structures of two additional termitomycesphins and activity cement of an inactive cerebroside by droxylation[J].Bioorg Med Chem,2001,9(8):2171-2177.
[18]卢彩会,郭晓萌,牟德华.黑皮鸡极菌水提物和醇提物的主要成分及抗氧化性研究[J].食品工程,2016(3):35-39.
[19]杨革.微生物学实验教程[M].北京:科学出版社,2005:36-41.
[20]鲁晓岩.苯酚-硫酸法测定北冬虫夏草多糖含量[J].食品工业科技,2002(4):69-70.
[21]马虎飞,王思敏,杨章民.陕北野生枸杞多糖的体外抗氧化活性[J].食品科学,2011,32(3):60-63.
[22]TAI Z,CAI L,DAI L,et al.Antioxidant activity and chemical constituents of edible flower of Sophora viciifolia[J].Food Chem,2011,126:1648-1654.
[23]张贺,王倩雯,曹龙奎.玉米皮多糖的提取及抗氧化性研究[J].粮食与油脂,2015,28(6):47-49.