凝结芽孢杆菌(Bacillus coagulans)作为一种益生菌,其功能及益生特性日益受到人们广泛的关注。凝结芽孢杆菌可调节肠道中细菌的生长,改善粘膜屏障功能,并影响肠粘膜和全身免疫系统[1-2];可通过改变pH值来优化矿物质的吸收;可通过产生消化酶对碳水化合物的消化产生重大影响,并且可以通过降解肠道中的胆固醇来降低胆固醇水平,甚至可以产生维生素等重要的营养物质[3-4]。此外,凝结芽孢杆菌在发酵生长后期可以形成芽孢[5],抵御胃的酸性环境到达肠道,萌发后有助于碳水化合物和蛋白质的消化[6];凝结芽孢杆菌能够促进肠道形成抵御各种病原体的环境,有利于营养物质的消化吸收[7],并且促进有益细菌的繁殖以及肠内细胞健康所需的短链脂肪酸的产生[8]。不同的凝结芽孢杆菌菌株,特性存在差异,如:从土壤中分离出来的凝结芽孢杆菌NRS27,嗜热且对维生素D有大量需求;从鸭的排泄物中分离出的凝结芽孢杆菌BC07,耐酸耐胆盐,并且乳酸的产量高达43.2 g/L;从鸡排泄物中分离出的凝结芽孢杆菌C-4,具体抑制大肠杆菌(Escherichia coli)、金黄色葡萄球菌(Staphylococcus aureus)[9-12]等特性。
通过常规发酵方式产生的生物质存在局限性,且随着市场对益生菌产品的需求量增加,生物质对于制药、乳制品以及益生菌具有非常重要的价值[13]。因此,需要探究增殖凝结芽孢杆菌的方法以增强生物质的积累[14]。目前,国内外对凝结芽孢杆菌在发酵培养方面有一些报道。GAO S F等[15]使用一定浓度的碳酸钙、磷酸二氢钠、蛋氨酸,采用分段式补料批次发酵的方式,对1株畜禽用凝结芽孢杆菌进行发酵培养,活菌数由6.80×109CFU/mL提高到8.30×109CFU/mL;葛风清等[16]利用麸皮和豆粕粉等作为培养基,对凝结芽孢杆菌AHU1366进行液体深层发酵培养,OD600nm值达到19.68;严涛等[17]利用糖蜜对凝结芽孢杆菌BC01进行发酵优化,使活菌数最高达到6.7×109 CFU/mL。一般的凝结芽孢杆菌耐受性较差,那么优化其产孢能力从而提高其耐受性成为必要条件,AMAHA M等[18]通过调节培养基组分来提高凝结芽孢杆菌芽孢产率的研究时发现,在培养基中加入硫酸锰后,产孢能力提高了3倍,且初始pH在6.0时产芽孢能力最强;路程等[19]利用麸皮水代替蒸馏水对凝结芽孢杆菌T50进行发酵优化,并发现在pH值接近中性时芽孢产率可达到94.3%。上述报道对于凝结芽孢杆菌的活菌数或菌体浓度方面有一定的提升,但菌株的生产能力还有待提高。
因此,本研究以凝结芽孢杆菌CNJD为研究对象,采用单因素及响应面试验优化该菌株增殖的发酵工艺,旨在有效提高凝结芽孢杆菌CNJD活菌数,为进一步研究提高其芽孢产率奠定基础。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种
凝结芽孢杆菌(Bacillus coagulans)CNJD:分离自湖北工业大学南区菜市场泡菜腌水,保藏于湖北工业大学微生物制剂团队。
1.1.2 试剂
蔗糖、木糖、淀粉、葡萄糖、牛肉膏、蛋白胨、胰蛋白胨、酵母粉、酵母浸粉、玉米芯粉、小麦麸皮、氯化铵、玉米粉、硫酸铵、尿素、硝酸钠、豆粕、磷酸二氢钾、氯化钠、硫酸镁、氯化钙、硫酸锰、溴甲酚紫:国药集团化学试剂有限公司。其他试剂均为国产分析纯或生化试剂。
1.1.3 培养基
酵母浸出粉胨葡萄糖(yeast extract peptone dextrose,YPD)培养基:蛋白胨20 g/L,酵母浸粉10 g/L,葡萄糖20 g/L,pH 6.6,121 ℃高压蒸汽灭菌20 min。
初始发酵培养基[20]:葡萄糖20 g/L、蛋白胨10 g/L、NaCl 5 g/L,pH自然,121 ℃高压蒸汽灭菌20 min。
1.2 仪器与设备
SW-CJ-1D型单人净化工作台:苏州净化设备有限公司;BXM-30R立式压力蒸汽灭菌锅:上海博讯实业有限公司医疗设备厂;AR1140型电子分析天平:奥豪斯国际贸易(上海)有限公司;PHS-25 pH计:上海精密科学仪器有限公司;ZHWY-2102C恒温培养振荡器:上海智城分析仪器制造有限公司;EVOLUTION300型可见光分光光度计:赛默飞世尔科技(中国)有限公司。
1.3 方法
1.3.1 菌种活化
将斜面保存的凝结芽孢杆菌CNJD接种于YPD培养基,45 ℃、160 r/min条件下振荡培养24 h。
1.3.2 凝结芽孢杆菌CNJD增殖发酵条件的优化
将活化的凝结芽孢杆菌CNJD按1%(V/V)的接种量接种于初始发酵培养基中,装液量为100 mL/300 mL,在45 ℃、160 r/min条件下,依次考察发酵时间(0~24 h)、发酵温度(35℃、40℃、45℃、50℃、55℃、60℃)、接种量(2%、4%、6%、8%、10%)、初始pH值(4、5、6、7、8、9、10)、装液量(25 mL/250 mL、50mL/250mL、75mL/250mL、100mL/250mL、125mL/250mL)、摇床转速(120r/min、140r/min、160r/min、180r/min、200r/min、220 r/min)对凝结芽孢杆菌活菌数的影响,凝结芽孢杆菌的活菌数采用活菌计数法进行测定[21]。
1.3.3 凝结芽孢杆菌CNJD增殖发酵培养基的优化
(1)单因素试验
在发酵条件优化后的初始发酵培养基的基础上,依次考察碳源种类(蔗糖、木糖、淀粉、玉米芯粉、小麦麸皮、葡萄糖,添加量为20 g/L)及添加量(5 g/L、10 g/L、20 g/L、30 g/L、40 g/L、50 g/L),氮源种类(氯化铵、蛋白胨、玉米粉、硫酸铵、尿素、硝酸钠、豆粕、胰蛋白胨、酵母浸粉,添加量为10 g/L)对凝结芽孢杆菌CNJD活菌数的影响。
选取较好的三种氮源,分别两两做复合氮源比例优化试验,比例分别为1∶1、1∶2、2∶1,并考察总添加量(5 g/L、10 g/L、15 g/L、20 g/L、25 g/L、30 g/L)对凝结芽孢杆菌CNJD活菌数的影响。
最后,考察无机盐种类(磷酸二氢钾、氯化钠、硫酸镁、氯化钙、硫酸锰,添加量为1.0 g/L)对凝结芽孢杆菌CNJD活菌数的影响。
(2)Plackett-Burman试验设计
在单因素试验的基础上,采用Plackett-Burman设计筛选试验,以蔗糖、胰蛋白胨、酵母浸粉、磷酸氢二钾、氯化钠、硫酸锰为自变量,以活菌数为响应值,筛选出对凝结芽孢杆菌CNJD活菌数影响较为显著的因素[22]。
(3)最低添加量试验
从Plackett-Burman试验设计中挑选出不显著性因素,考虑到后期投入生产中成本效益的最大化,研究对凝结芽孢杆菌活菌数影响不显著的因素的最低添加量。
(4)最陡爬坡试验
从Plackett-Burman设计试验中挑选出显著性因素进行最陡爬坡试验,依据显著性因素正负效应,设计合理的步长,增加试验的密集度,来逼近效果最好的区域[23]。
(5)中心组合设计试验
根据最陡爬坡试验结果,采用Design-Expert 8.0.6.1软件对凝结芽孢杆菌CNJD活菌数试验数据进行方差分析及多元回归方程拟合,依据回归方程绘制响应面图,并预测发酵培养基的最佳组成[24]。
1.3.4 数据统计分析
应用Design-Expert 8.0.6.1进行数据处理和分析,包括回归分析、二次多项式回归方程、方差分析和响应面图。所有试验重复3次,实验数据表示为“平均值±标准偏差”。
2 结果与分析
2.1 凝结芽孢杆菌CNJD增殖发酵条件的优化
不同发酵条件对凝结芽孢杆菌CNJD生长的影响见图1。
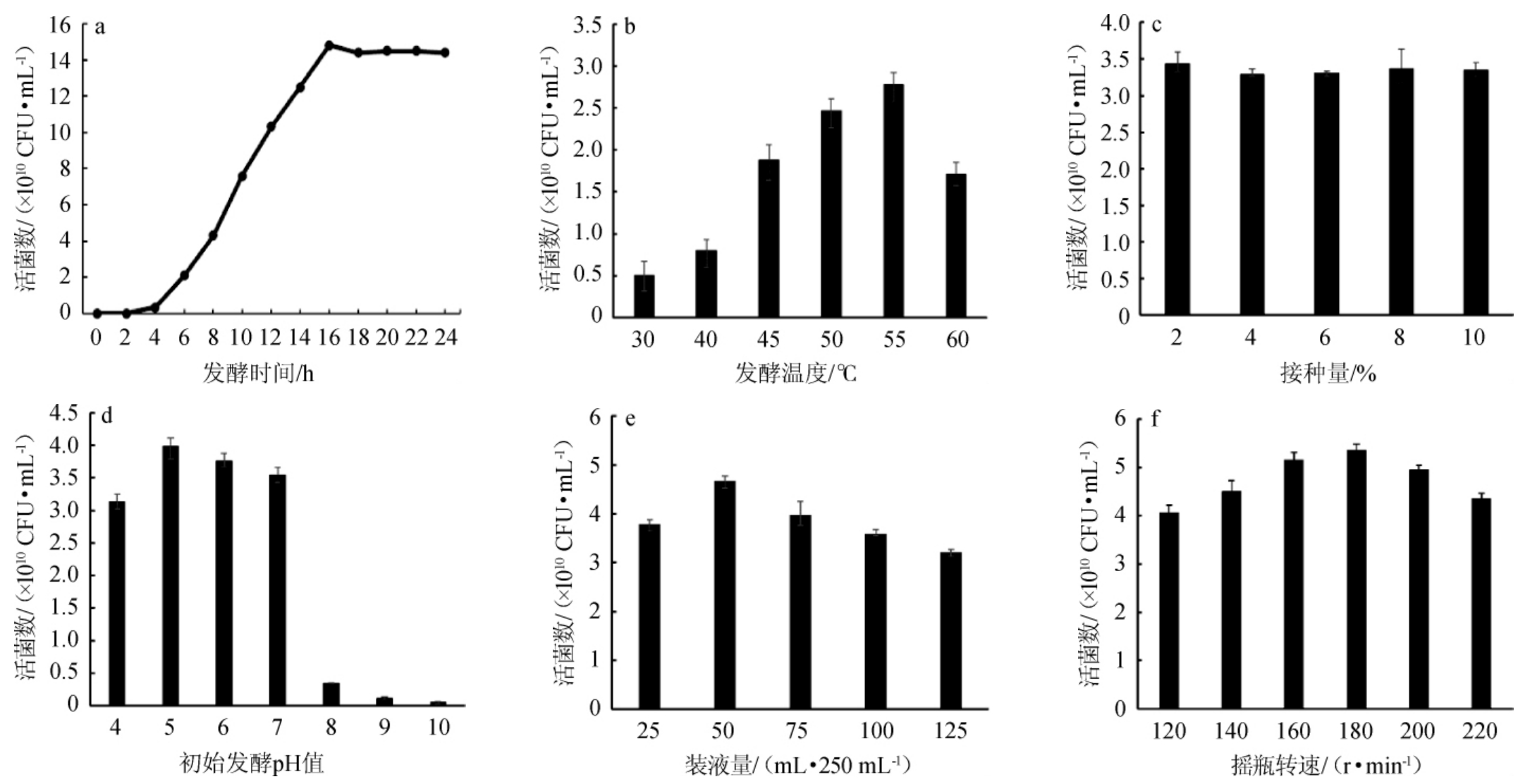
图1 不同发酵条件对凝结芽孢杆菌CNJD活菌数的影响
Fig.1 Effect of different fermentation conditions on the viable number of Bacillus coagulans CNJD
由图1a可知,发酵0~4 h为菌体生长的迟缓期,4~16 h为对数生长期,16~24 h为稳定期,16 h活菌数最高为(1.48±0.11)×1010 CFU/mL,故确定最优发酵时间为16 h。
由图1b可知,随着发酵温度的升高,菌体活菌数呈先升高后下降的趋势,当发酵温度为55 ℃时,活菌数最高为(2.78±0.13)×1010 CFU/mL,故确定最优发酵温度为55 ℃。
由图1c可知,当接种量逐渐增大时,菌体活菌数并无明显变化,考虑到后期利用发酵罐高密度发酵菌体,接种量过大在操作接种这一步骤时可能会提高染菌几率,故确定最优接种量为2%。
由图1d可知,随着初始发酵pH值的升高,菌体活菌数呈先升高后下降的趋势,当初始发酵pH值为5.0时,菌体生长最好,活菌数最高为(3.98±0.14)×1010 CFU/mL,故确定最优初始发酵pH值为5.0。
由图1e可知,随着装液量的增大,菌体活菌数呈先升高后下降的趋势,当装液量为50 mL/250 mL时,菌体生长最好,活菌数最高为(4.67±0.17)×1010 CFU/mL,表明此时摇瓶中的溶氧最适合该菌体生长,故确定最优装液量为50 mL/250 mL。
由图1f可知,随着转速的升高,菌体活菌数呈先升高后下降的趋势,分析原因可能是,在发酵过程中,摇瓶转速影响菌体发酵过程中的溶氧,若是转速太高,溶氧增大,则容易抑制凝结芽孢杆菌这种兼性厌氧菌的生长,若转速太低,会影响菌体的二分裂,从而导致菌体生长迟缓。当摇瓶转速为180 r/min时,菌体生长最好,活菌数最高为(5.37±0.15)×1010CFU/mL,故确定最优摇瓶转速为180 r/min。
2.2 凝结芽孢杆菌CNJD增殖发酵培养基的优化
2.2.1 碳源种类及添加量对凝结芽孢杆菌CNJD生长的影响
碳源种类及添加量对凝结芽孢杆菌CNJD生长的影响见图2。
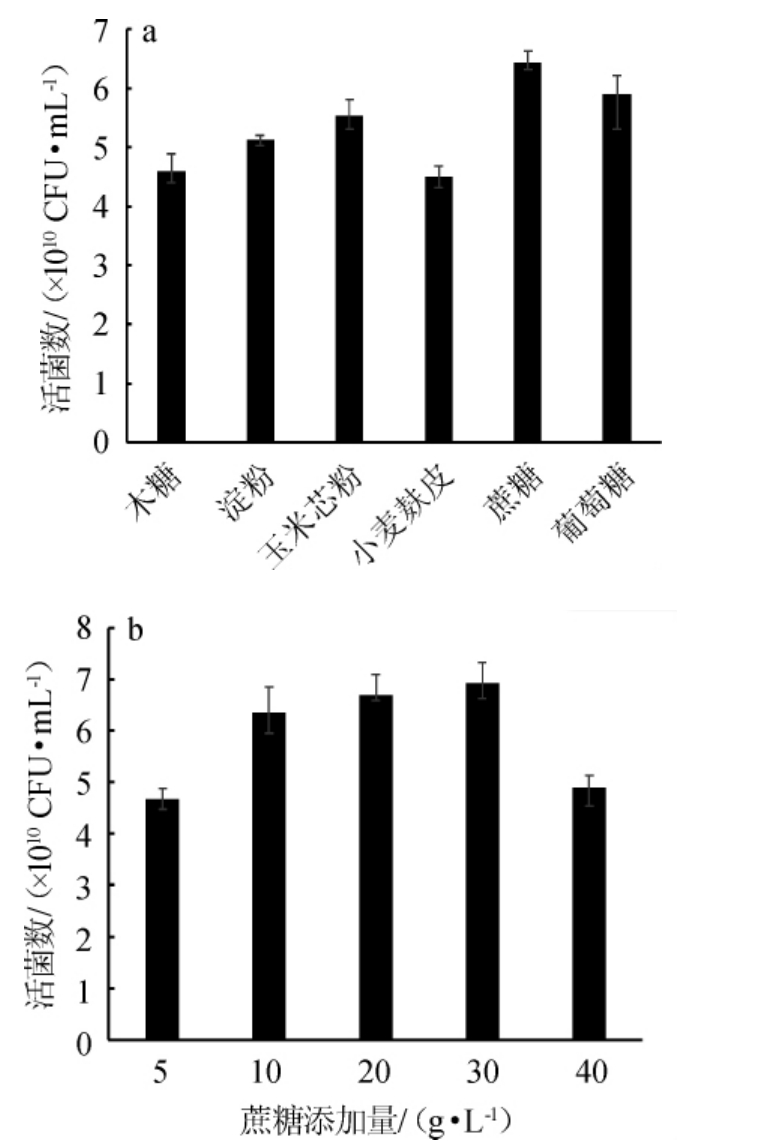
图2 碳源种类(a)及蔗糖添加量(b)对凝结芽孢杆菌CNJD生长的影响
Fig.2 Effect of carbon source types (a) and sucrose addition (b) on the growth of Bacillus coagulans CNJD
由图2a可知,当蔗糖作为发酵培养基的碳源时,活菌数最高,为(6.45±0.12)×1010 CFU/mL。分析原因可能是等体积的蔗糖作为碳源相较于葡萄糖来说,更容易在菌体发酵时提供一个低渗透压的环境[25],故确定最佳碳源为蔗糖。
由图2b可知,当蔗糖添加量为30 g/L时,活菌数最高,为(6.93±0.16)×1010 CFU/mL。当蔗糖的添加量较少时,由于培养基中营养物质的缺乏,导致菌体生长受限;而当蔗糖的添加量过多时,培养基的粘度上升,造成培养基中溶氧的不足,从而导致菌体的生长受到抑制[26],故确定最佳蔗糖添加量为30 g/L。
2.2.2 氮源种类及添加量对凝结芽孢杆菌CNJD生长的影响
氮源种类对凝结芽孢杆菌CNJD生长的影响见图3。
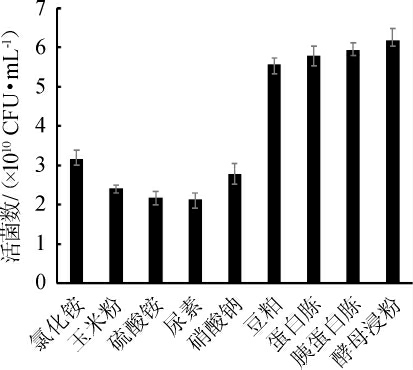
图3 氮源种类对凝结芽孢杆菌CNJD生长的影响
Fig.3 Effect of nitrogen source types on the growth of Bacillus coagulans CNJD
无机氮源对于微生物生长来说吸收较快,但在发酵过程中无机氮源会影响培养基中的pH值;相较于无机氮源,有机氮源含有大量的无机盐及生长因子,并且含有丰富的微量元素[27],由图3可知,当氮源为酵母浸粉、胰蛋白胨、蛋白胨、豆粕时,活菌数较高,又考虑到豆粕为工业副产品,出于生产成本以及资源再利用角度考量,使用豆粕代替活菌数较高的蛋白胨来进行复合氮源优化。因此选用酵母浸粉、胰蛋白胨和豆粕作为复合氮源。复合氮源比例及添加量对凝结芽孢杆菌CNJD生长的影响分别见表1和图4。
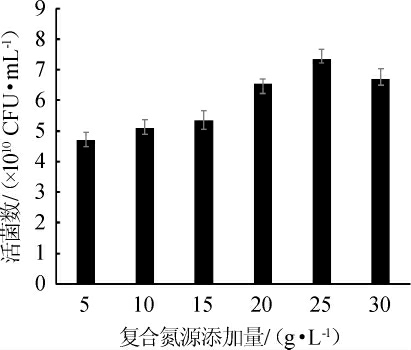
图4 复合氮源添加量对凝结芽孢杆菌CNJD生长的影响
Fig.4 Effect of compound nitrogen source addition on the growth of Bacillus coagulans CNJD
表1 复合氮源比例对凝结芽孢杆菌CNJD生长的影响
Table 1 Effect of compound nitrogen source ratio on the growth of Bacillus coagulans CNJD
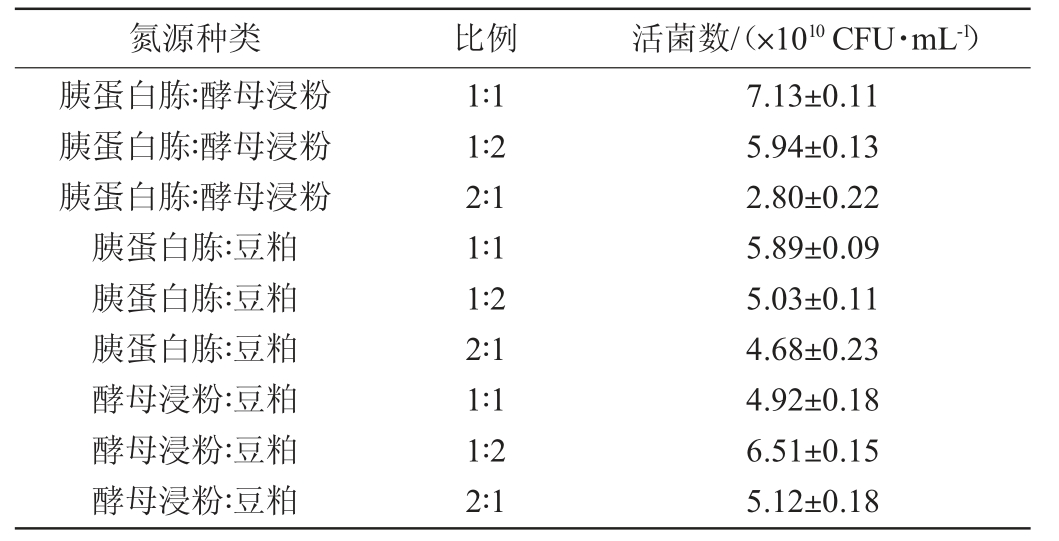
由表1可知,氮源的复合使用对于微生物生长起到了一定的促进作用,当胰蛋白胨∶酵母浸粉=1∶1时,菌株的活菌数最高,为(7.13±0.15)×1010 CFU/mL,故选用胰蛋白胨∶酵母浸粉=1∶1作为复合氮源。
由图4可知,随着复合氮源添加量的增多,活菌数也不断增加,当添加量为25 g/L时,活菌数最高,为(7.35±0.15)×1010 CFU/mL,故确定最优氮源添加量为25 g/L。
2.2.3 无机盐种类对凝结芽孢杆菌CNJD生长的影响
无机盐种类对凝结芽孢杆菌CNJD生长的影响见图5。
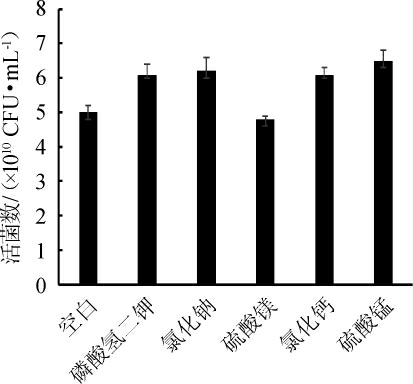
图5 无机盐种类对凝结芽孢杆菌CNJD生长的影响
Fig.5 Effect of inorganic salt type on the growth of Bacillus coagulans CNJD
由图5可知,磷酸氢二钾、氯化钠、氯化钙和硫酸锰这几种单一无机盐,对凝结芽孢杆菌CNJD的生长具有积极影响,故选择磷酸氢二钾、氯化钠、氯化钙和硫酸锰进行后续的PB试验。
2.2.4 Plackett-Burman试验设计
通过对单因素试验结果分析,确定了PB试验的因素,然后通过PB试验筛选得到对凝结芽孢杆菌活菌数有显著性影响的组分,以便对培养基的组分进行进一步的优化。按照Design-Expert 8.0.6.1软件设计PB试验,试验次数12次,每组3个平行,PB试验设计及结果见表2,试验方差及主效应分析见表3。
表2 Plackett-Burman试验设计及结果
Table 2 Design and results of Plackett-Burman experiments
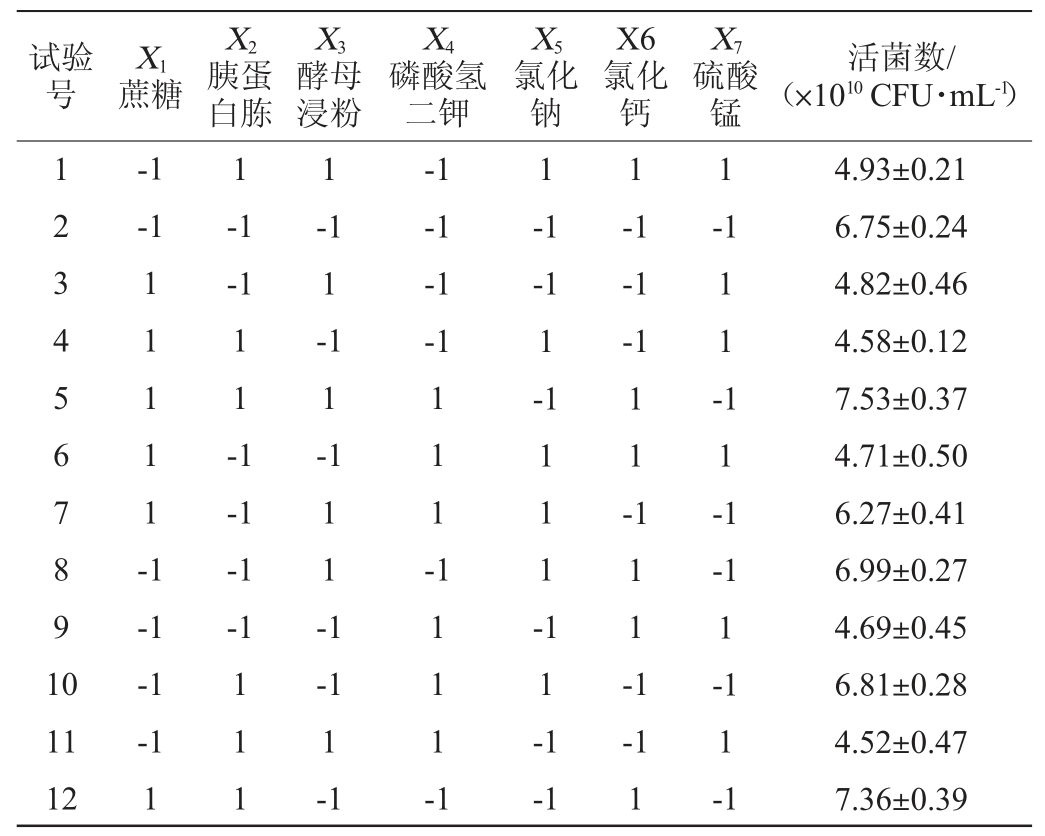
表3 Plackett-Burman试验方差及主效应分析
Table 3 Variance and main effect analysis of Plackett-Burman experiments
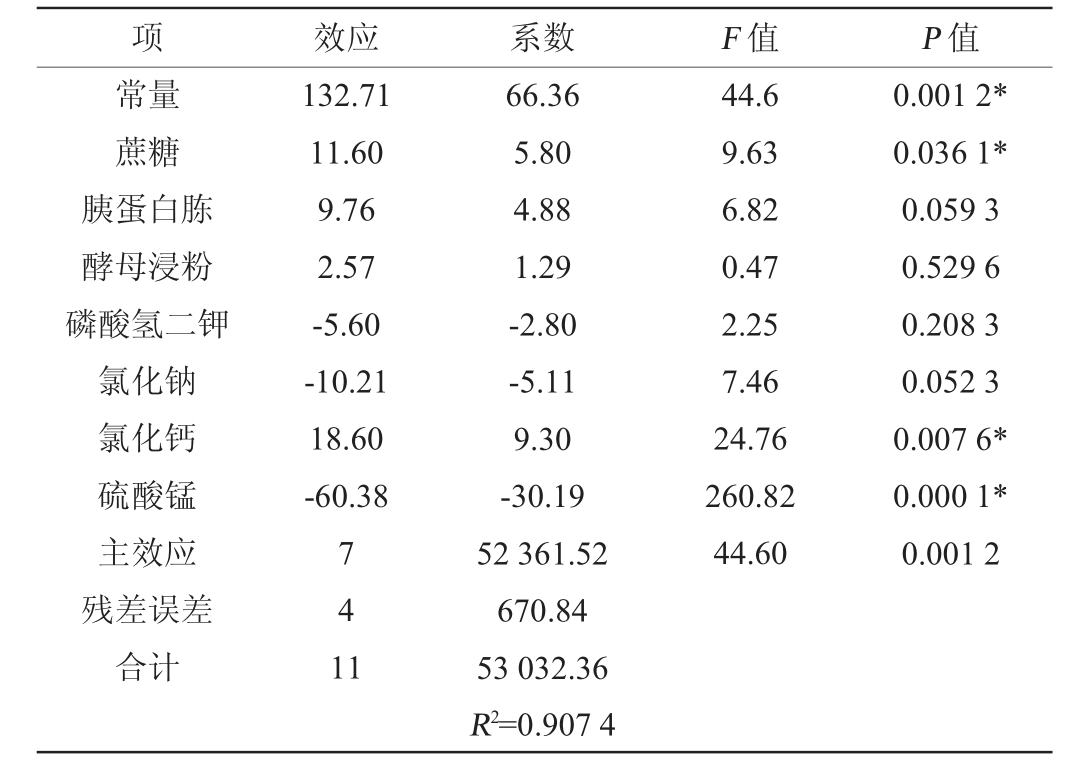
注:“*”表示对结果影响显著(P<0.05)。下同。
由表3可知,回归模型的P值<0.05,显著。蔗糖、氯化钙、硫酸锰对凝结芽孢杆菌CNJD的活菌数影响显著(P<0.05),且其中蔗糖、氯化钙为正效应,硫酸锰为负效应,而其他因素对结果影响不显著(P>0.05)。由表4的方差分析可知,决定系数R2=0.907 4,表明90.74%的数据都能用此模型来解释。
2.2.5 最低添加量试验
根据Plackett-Burman设计试验得到的影响菌株活菌数的不显著因素,即磷酸氢二钾、氯化钠、胰蛋白胨、酵母浸粉,做最低添加量试验,结果见表4。
表4 不显著因素的最低添加量试验
Table 4 Minimum addition experiments of insignificant factors

在发酵生产过程中,经济效益、产品成本是首要考虑因素,所以为了极大程度的减少成本,选择每个因素下活菌数最高的添加量作为最低添加量,即磷酸氢二钾0 g/L、氯化钠1.50 g/L、胰蛋白胨10.00 g/L、酵母浸粉10.00 g/L。
2.2.6 最陡爬坡试验
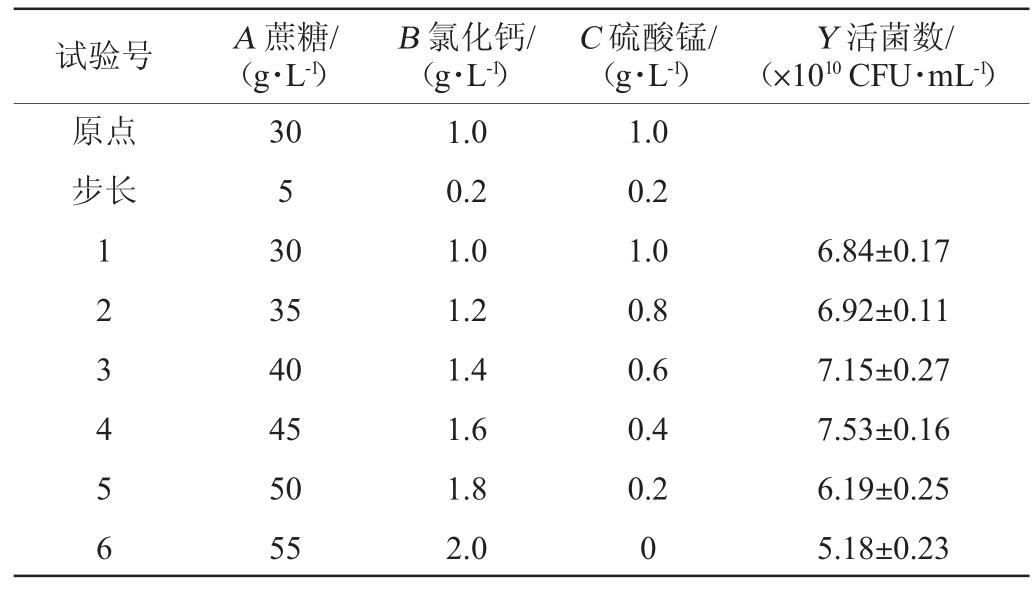
固定酵母浸粉10.00 g/L,氯化钠1.50 g/L,胰蛋白胨10.00 g/L,根据Plackett-Burman试验结果,选取影响显著的因素蔗糖(A)、氯化钙(B)、硫酸锰(C)为考察因素,活菌数(Y)为响应值,按照各因素的正负效应设定最陡爬坡试验。
由表5可知,当蔗糖、氯化钙和硫酸锰的添加量分别为45.00 g/L、1.60 g/L和0.40 g/L时,凝结芽孢杆菌的活菌数最高,为(7.53±0.16)×1010 CFU/mL,因此将其作为中心复合试验的中心点,进一步优化组分的添加量。
表5 最陡爬坡试验设计及结果
Table 5 Design and results of the steepest climb experiments
2.2.7 中心组合设计试验
通过最陡爬坡试验得到的中心点:蔗糖45.00 g/L、氯化钙1.60 g/L、硫酸锰0.40 g/L,以此为中心点,固定酵母浸粉10.00 g/L,氯化钠1.50 g/L,胰蛋白胨10.00 g/L,以活菌数为响应值进行3因素5水平的中心复合设计试验,试验设计及结果见表6,方差分析结果见表7。
表6 中心复合设计试验结果
Table 6 Results of center composite design experiments

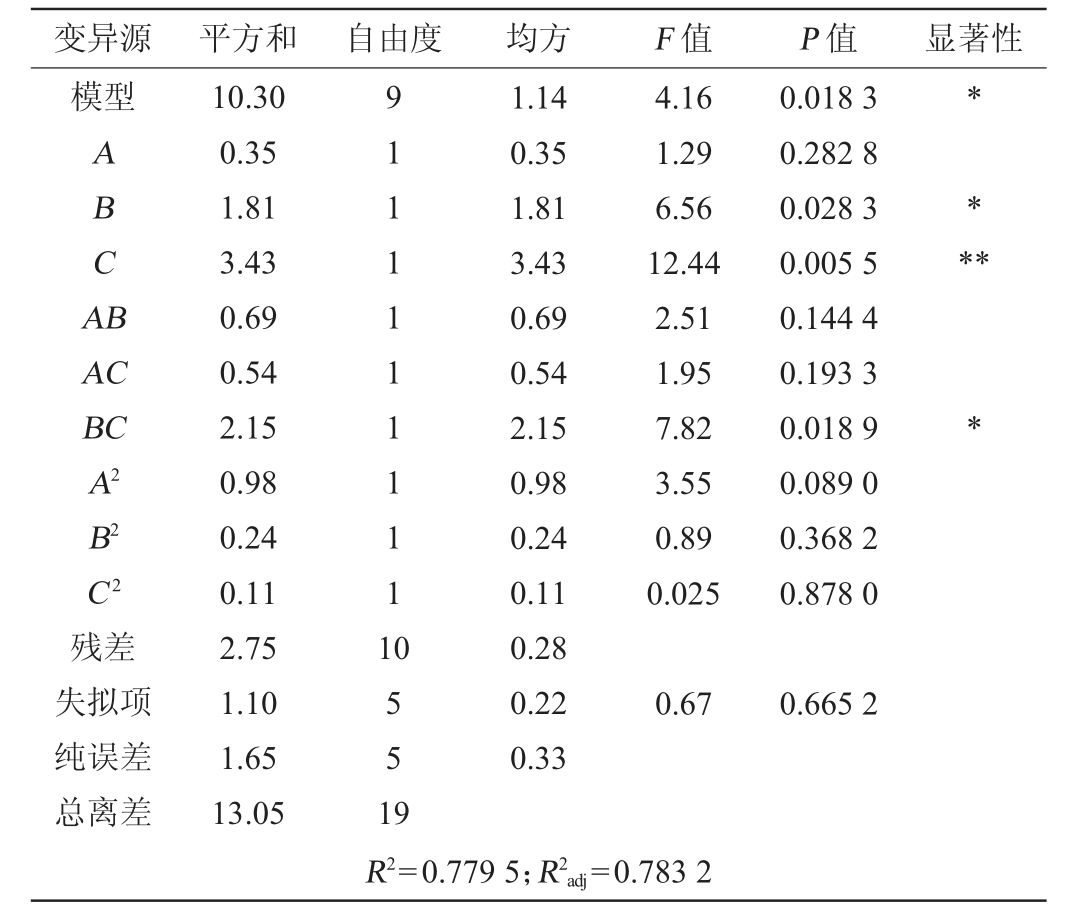
表7 响应面试验的方差分析结果
Table 7 Variance analysis results of response surface experiments
注:“**”表示对结果影响极显著(P<0.01);“*”表示对结果影响显著(P<0.05)。
利用Design-Expert 8.0.6.1软件对表6试验数据进行二次多项回归拟合,得到的模型方程为Y=-39.529 08+1.501 12A+9.411 82B+58.491 05C-0.293 75AB-0.517 5AC-25.937 5BC-0.010416A2+3.256 64B2-2.176 24C2。由表7可知,模型的P值<0.05,显著;失拟项的P值>0.05,不显著,说明该模型与试验值拟合较好,可用于活菌数的预测。决定系数R2=0.779 5,表明预测有22.05%的变异情况不能由该模型解释。方程中一次项B、交互项BC对活菌数影响显著(P<0.05),一次项C对活菌数影响极显著(P<0.01),其他项对结果影响不显著(P>0.05)。其中氯化钙与硫酸锰交互作用对活菌数影响的响应面及等高线图见图6。
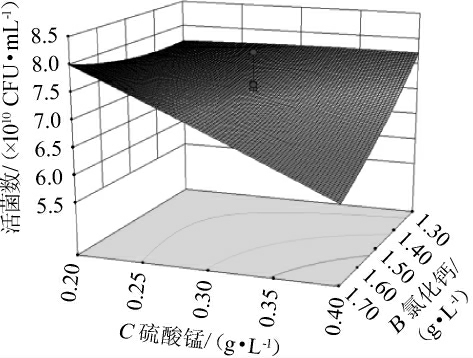
图6 氯化钙与硫酸锰的交互作用对凝结芽孢杆菌CNJD活菌数影响的响应面和等高线
Fig.6 Response surface plots and contour lines of effects of interaction between CaCl2 and MgSO4 on the viable number of Bacillus coagulans CNJD
由图6可知,氯化钙与硫酸锰的交互作用对凝结芽孢杆菌CNJD活菌数影响的响应面有最高点,且等高线呈椭圆,说明两因素间交互作用明显,与方差分析结果一致。
由模型和软件分析得到凝结芽孢杆菌CNJD的最优培养基组成为蔗糖48.59 g/L,氯化钙1.70 g/L,硫酸锰0.33 g/L,活菌数预测值为7.99×1010 CFU/mL,在此优化条件下进行3次重复试验,活菌数为(7.86±0.25)×1010 CFU/mL。实测值与回归方程预测值吻合良好。
3 结论
本研究以活菌数为评价指标,采用单因素试验得到凝结芽孢杆菌CNJD增殖的最优培养条件为:接种量2%、初始发酵pH值5.0、培养温度55 ℃、摇床转速180 r/min、发酵时间16 h、装液量50 mL/250 mL。在此基础上,采用单因素试验及响应面试验优化得到最优培养基组成为:蔗糖48.59 g/L,酵母浸粉10.00 g/L,胰蛋白胨10.00 g/L,氯化钙1.70 g/L,硫酸锰0.33 g/L,氯化钠1.50 g/L。在此优化条件下,凝结芽孢杆菌的活菌数为(7.86±0.25)×1010CFU/mL。
[1]XIAO S S,MI J D,MEI L,et al.Microbial diversity and community variation in the intestines of layer chickens[J].Animals,2021,11(3):840.
[2]PYNE D B,WEST N P,COX A J,et al.Probiotics supplementation for athletes-clinical and physiological effects[J].Eur J Sport Sci,2015,15(1):63-72.
[3]DUCATELLE R,EECKHAUT V,HAESEBROUCK F,et al.A review on prebiotics and probiotics for the control of dysbiosis:present status and future perspectives[J].Animal,2015,9(1):43-48.
[4]YOO J Y,KIM S S.Probiotics and prebiotics:present status and future perspectives on metabolic disorders[J].Nutrients,2016,8(3):173.
[5]ABDEL-RAHMAN M A,HASSAN E D,FOUDA A,et al.Evaluating the effect of lignocellulose-derived microbial inhibitors on the growth and lactic acid production by Bacillus coagulans Azu-10[J].Fermentation,2021,7(1):17.
[6] AHMED Y A,EI-HAFEZ A A E,ZAYED A E.Histological and histochemical studies on the esophagus,stomach and small intestines[J].Varanus Niloticus,2009,2(1):35-48.
[7]AMADI B,ZYAMBO K,CHANDWE K,et al.Adaptation of the small intestine to microbial enteropathogens in Zambian children with stunting[J].Nat Microbiol,2021,6(3):445-454.
[8]LEE Y,YOSHITSUGU R,KIKUCHI K,et al.Combination of soya pulp and Bacillus coagulans lilac-01 improves intestinal bile acid metabolism without impairing the effects of prebiotics in rats fed a cholic acid-supplemented diet[J].Br J Nutr,2016,116(4):603-610.
[9]卜红宇,张彦斌,高瑞霞,等.2015 年内蒙古地区31 批保健食品中污染菌的分离与鉴定[J].食品安全质量检测学报,2016,7(4):1483-1488.
[10]汪攀,易敢峰,孙自博,等.一株凝结芽孢杆菌的分离鉴定及益生性研究[J].中国畜牧兽医,2017,44(4):1195-1202.
[11]MUKHERJEE N,MITRA S,GOSWAMI A,et al.Evaluation of the growth response of spore forming lactic acid Bacillus-Bacillus coagulans in presence of oxide nanoparticles[J].Appl Nanosci,2020,21(10):4075-4086.
[12]姚晓红,吴逸飞,杨家帅,等.凝结芽孢杆菌的筛选、鉴定及抑菌特性的初步研究[J].浙江农业科学,2015(7):1091-1094.
[13]李锴骁,杨婉秋,庞煜,等.凝结芽孢杆菌的研究进展[J].化学与生物工程,2019,36(10):1-6.
[14] FAN R,BURGHARDT J P,TAO X,et al.Removal of small-molecular byproducts from crude fructo-oligosaccharide preparations by fermentation using the endospore-forming probiotic Bacillus coagulans[J].Fermentation,2020,6(1):1-16.
[15]GAO S F,KONG L H,ZHOU Y H,et al.The Influence on Fermentation Level of Bacillus coagulans by Adopting Segmented Fed-batch Fermentation Technology[J].China Animal Husbandry &Veterinary Medicine,2013,40(2):80-83.
[16]葛风清,孙玲玲,曹钰.益生凝结芽孢杆菌AHU1366 的液体深层发酵培养[J].饲料研究,2007,2007(7):63-66.
[17]严涛,朱建国,姜甜,等.一株凝结芽孢杆菌的分离筛选及产孢条件优化[J].微生物学通报,2018,45(2):238-249.
[18]AMAHA M,ORDAL Z J.Sporulation requirements of Bacillus coagulans var.thermoacidurans in complex media[J].J Bacteriol,1956,72(1):34.
[19]路程,周长海,于红梅,等.凝结芽孢杆菌T50 产芽孢条件优化的研究[J].中国酿造,2009,28(7):93-95.
[20]谭才邓、廖延智、朱美娟、黄亿璇、黄思乐、姚勇芳.凝结芽孢杆菌高密度发酵及产孢关键因素研究[J].食品科技,2020,45(7):11-18.
[21]钱存柔,黄仪秀.微生物学实验教程[M].北京:北京大学出版社,1999:198-199.
[22] LIU Z,CHEN Y,HU Y.Simultaneous separation and determination of seven chelating agents using high-performance liquid chromatography based on statistics design[J].J Sep Sci,2020,43(4):719-726.
[23]刘颖,张彬彬,孙冰玉,等.枯草芽孢杆菌高产中性蛋白酶发酵条件的优化[J].食品科学,2014,35(13):166-170.
[24]杨浩,胡华,罗鹏程,等.Plackett-Burman 设计与响应面法优化毕赤酵母产重组抗菌肽LL-37 发酵培养基[J].检验医学与临床,2016,13(19):2703-2705.
[25]刘秀.渗透压对黑曲霉发酵生产葡萄糖酸钠及菌体自身生理代谢的影响[D].上海:华东理东大学,2017.
[26]林丹乐,谢永婷,王雪梅.低聚木糖对变异链球菌生长和产酸影响的体外研究[J].中国实用口腔科杂志,2019,12(8):480-485.
[27]杨德.有机氮源对泰乐菌素发酵生产影响的研究[J].中国化工贸易,2016,8(6):43-46.