高血压(hypertension)是指收缩压≥140 mmHg,舒张压≥90 mmHg,并且对心脏、脑、肾和其他器官具有功能或器质性损害的一种常见疾病。对于原发性高血压,食物中的血管紧张素转换酶(angiotensin converting enzyme,ACE)抑制肽可用于控制血压[1-2]。ACE抑制肽抑制血管紧张素I向血管紧张素II的转化,从而抑制血管收缩并减缓血压的升高。基于ACE抑制肽毒副作用小、降压效果显著的特点,研究人员致力于构建定量构效关系模型,指导合成高效的药物模型。
以往对ACE抑制肽的研究主要针对ACE抑制肽的制备、分离纯化及检测技术、蛋白质来源等,本研究针对食源性ACE抑制肽的序列信息、降压机制及ACE抑制肽的定量构效关系进行了概括。总结了能够描述氨基酸理化性质的定量构效关系(quantitative structure-activity relationship,QSAR)模型,指出了存在的问题和未来的研究方向,为指导ACE抑制肽的分子设计、合成新型降压药物奠定基础。
1 ACE抑制肽作用机理及制备来源
1.1 血管紧张素转换酶
血管紧张素转换酶(ACE、激肽酶Ⅱ或肽基-羧基肽酶)是一种血管内皮细胞膜结合酶,其作用机制是将氨基酸切割成两段来水解肽链C端的二肽残基。其广泛分布于人体组织中,在附睾、睾丸和肺组织中含量丰富。其中肺毛细血管内皮细胞中的ACE活性最高。ACE分为体细胞血管紧张素转换酶(soma-tic angiotensin converting enzyme,sACE)和睾丸血管紧张素转换酶(testic ACE,tACE);sACE是由1 306个氨基酸组成的多联糖蛋白,存在于内皮和上皮细胞中;tACE含701个氨基酸残基,分布在雄性动物的睾丸和精子中,它与sACE的C端结构域有相同结构(除前36个氨基酸残基)[3]。sACE由两个高度同源的具有60%相似性的蛋白结构域N、C-domain组成,包含His-Glu-X-X-His和Zn2+。两种结构域在底物和抑制剂的特异性及氯离子激活等方面存在较大差异。sACE的C-domain将十肽血管紧张素I(Angiotensin I,AngI)水解为八肽血管紧张素Ⅱ(Angiotensin Ⅱ,Ang Ⅱ);而两种结构域又可共同完成舒缓激肽的水解。
血管紧张素转换酶粘附在内皮细胞表面,可分解并释放到血液循环中。其主要功能是催化血管紧张素I向血管紧张素II的转化,并灭活缓激肽。ACE的分子质量为120~150 kDa,最适pH为7.5~8.3,等电点(isoelectric point,PI)为4.7,沉降系数为7.9s,是一种能被Zn2+和Cl-激活[4-5]的由单肽链组成的糖蛋白。ACE是治疗高血压、心力衰竭、2型糖尿病和糖尿病肾病的理想靶点。
1.2 高血压产生机制
原发性高血压(essential hypertension,EH)的发生是由于血管收缩活性的增加或舒张活性的降低,血压的相对稳定受多种活性物质以及血压调节系统的影响。这种调节系统包括肾素-血管紧张素系统(renin-angiotensin system,RAS)、交感神经系统(sympathetic nervous system,SNS)、一氧化氮合酶/一氧化氮(nitric oxide synthase/nitric oxide,NOS/NO)、内皮素、胰岛素、血浆同型半胱氨酸等[6-7]。肾素-血管紧张素系统和激肽释放酶-激肽系统(kallikrein-kinin system,KKS)作为一对拮抗系统用以维持人体血压平衡。在RAS系统中,ACE使失活的血管紧张素转换酶Ⅰ水解为血管紧张素转换酶Ⅱ,作用于小动脉,引起血管平滑肌收缩,增加外周血管阻力,血压上升。同时ACE还刺激肾上腺皮质球区分泌醛固酮,增加钠含量和血容量水平,促使血压升高;在KKS系统中,舒缓激肽(bradykinin,BK)能够扩张毛细血管、增加其通透性,从而降低血压。然而,ACE能将缓激肽降解为无效片段,使其不能发挥降压的作用。如果局部组织ACE含量和活性增加,将直接导致缓激肽含量下降和血管紧张素转换酶Ⅱ含量增加,从而促进血压升高。
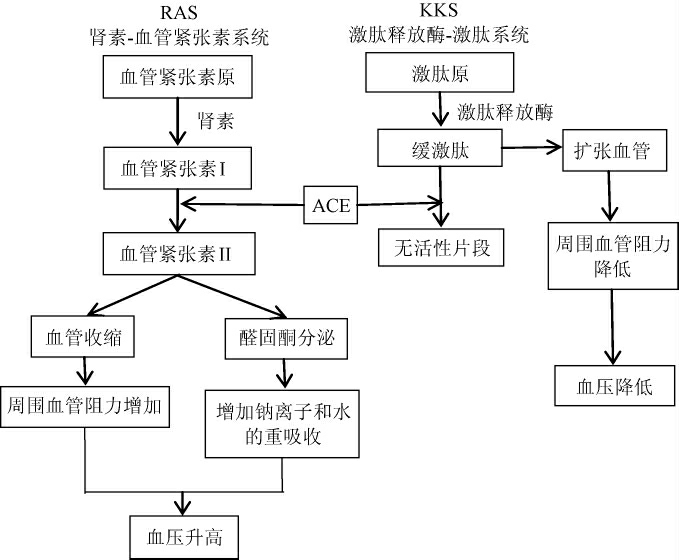
图1 肾素-血管紧张素系统、激肽释放酶-激肽系统血压调节机制
Fig.1 Blood pressure regulation mechanism of RAS and KKS system
1.3 ACE及其抑制肽的相互作用
ACE活性位点中有S1、S'1和S'2三个亚位点,它们易与C末端有疏水性氨基酸残基或竞争性抑制剂的抑制肽作用。位于S1、S'1间的Zn2+从酰胺键的酮基得电子参与水解使肽键裂解并释放二肽[8]。ACE和抑制肽间的有多个氢键作用,稳定了非催化酶-肽复合物的结构,促进ACE抑制肽的活性[9]。
ACE抑制肽直接与血管紧张素转换酶结合,使其作用丧失,减少血管紧张素II的合成,从而缓解血管收缩、醛固酮分泌造成的血压升高;同时无法使缓激肽失活成为无效片段,促进血管扩张,降低血压。所以,ACE抑制肽的摄入能有效地抑制局部ACE的含量增加、活性增强,有效抑制血压升高[10]。
1.4 食源性ACE抑制肽的制备
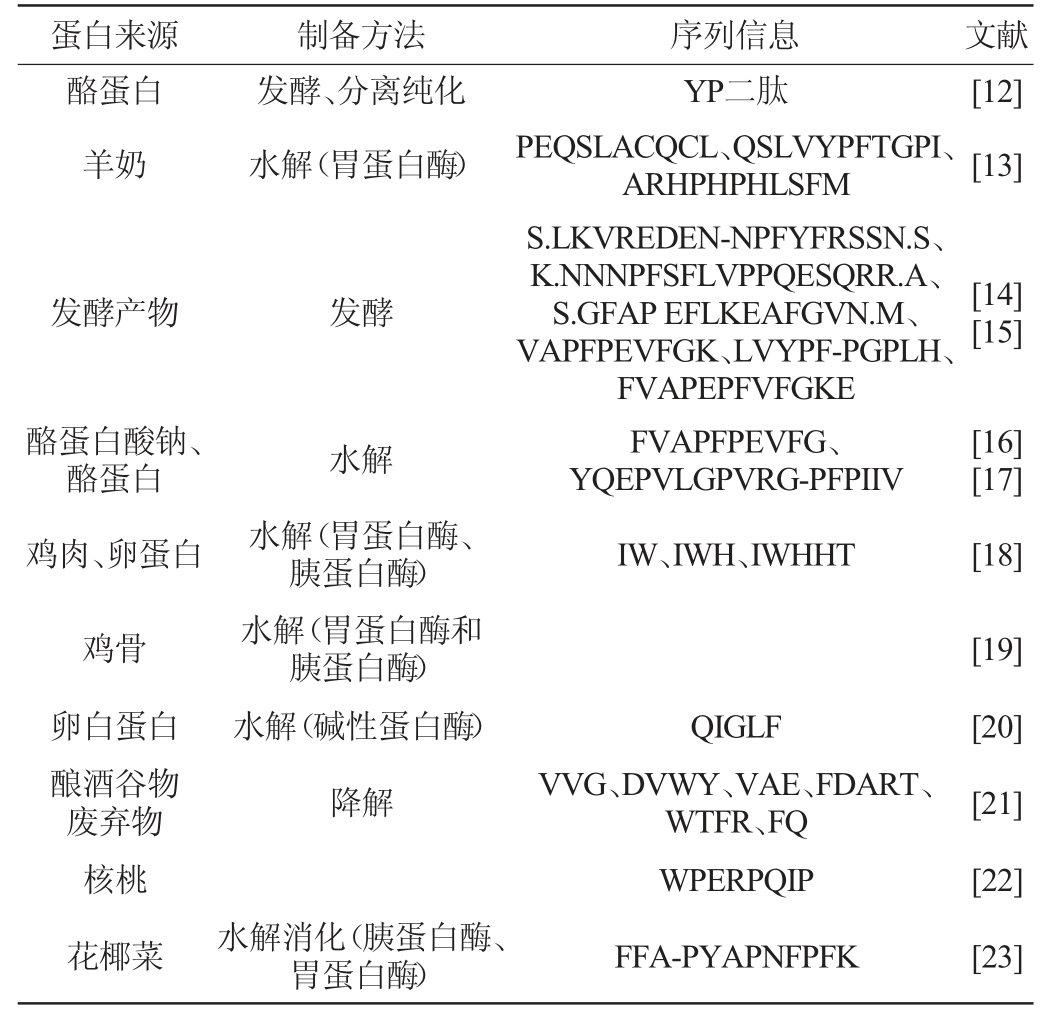
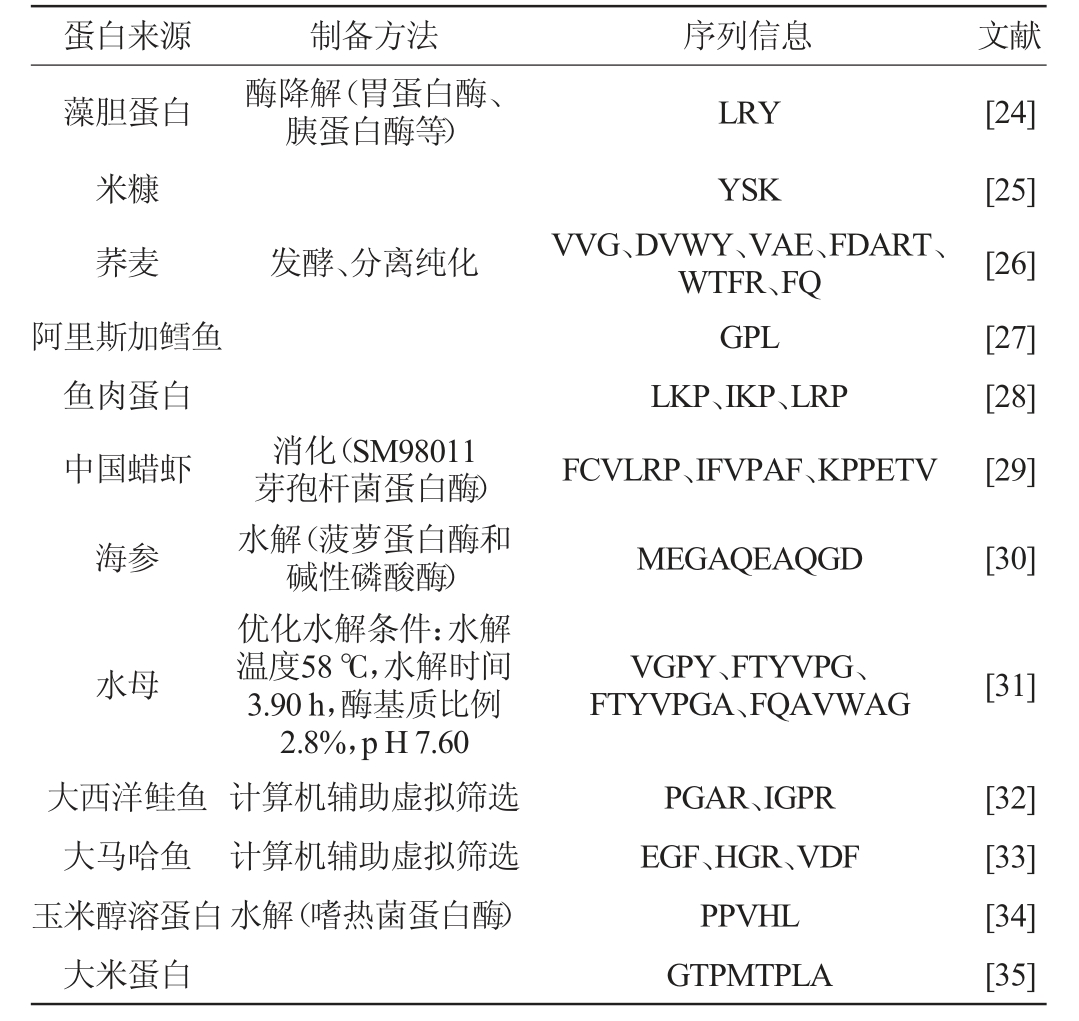
食源性ACE抑制肽活性强、安全性高,多从天然蛋白质中水解得到,具有广泛的生物学功能。研究者从乳源、发酵食物、动植物、海洋生物中获得大量ACE抑制肽,为研究打下了坚实的基础。ACE抑制肽通常通过酶水解、发酵和脱氧核糖核酸(deoxyribonucleic acid,DNA)重组等方法制备,最常用的制备方法是通过酶水解的形式。发酵法是在食品发酵过程中,利用微生物产生的蛋白酶和肽酶水解蛋白质,释放功能性多肽的方法降低了成本。DNA重组法通过鉴定高活性ACE抑制肽的序列,并进一步融合成能在体系中高效表达的ACE抑制肽,克隆至表达载体并转接至宿主菌进行表达[11]。对食源性ACE抑制肽来源和序列信息进行汇总见表1。
表1 食源性血管紧张素转换酶抑制肽来源和序列信息
Table 1 Source and sequence information of foodborne angiotensin converting enzyme inhibitory peptide
续表
2 定量构效关系研究
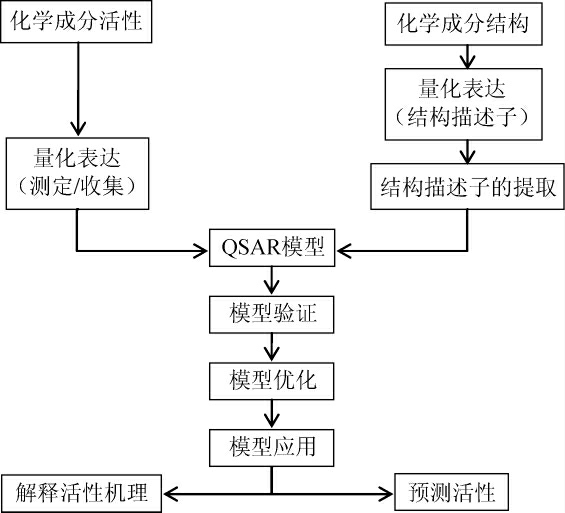
图2 定量构效关系原理
Fig.2 Principle of quantitative structure-activity relationship
定量构效关系(QSAR)是研究有机小分子和生物大分子相互作用和有机小分子在生物体内的吸收、分布、代谢和排泄的一种方法,可以深入研究ACE抑制肽的结构和活性机制,了解ACE抑制肽活性对血压的影响,优化ACE抑制肽的结构以改变其活性,指导生产高效、低成本的抗高血压药物。QSAR可以建立ACE抑制肽的生物活性与分子结构之间的定量关联模型,筛选和设计有效的药物模型,是ACE抑制肽研究的热点。
QSAR研究方法最早由HANSCH等确立,将分子电性、立体效应与分子活性联系构建定量模型。随着计算机辅助手段的发展,QSAR从二维(two dimension,2D)发展到六维。
2.1 二维定量构效方法
2D-QSAR主要包括Hansch法、基团贡献法和分子连接性指数法三类。多元线性回归法(multiple linear regression,MLR)、主成分分析法(principal components,PCA)、偏最小二乘法(partial least squares,PLS)和人工神经网络法(artificial neural networks,ANN)为其主要的建模方法。Hansch法是假设化合物活性和可计算测量物化性质相联系,采用多重自由能相关法,最后再利用多元线性回归法就能得到目标的模型;基团贡献法则适用于对具有相同母体的有机物的毒性评估;分子连接性指数法是根据骨架原子连接排列方式来描述分子结构特征的一种方法。
2.2 三维定量构效方法
3D-QSAR有分子形状分析、距离几何方法、比较分子力场分析、比较分子相似因子分析以及虚拟受体等。其方法是在分子水平上认为,影响生物活性的相互作用主要是非共价性立体和静电作用,在模型建立后通过非交叉验证的相关系数R2、方差比F和绝对标准差S来作为其预测准确能力的依据。
2.3 高维定量构效方法
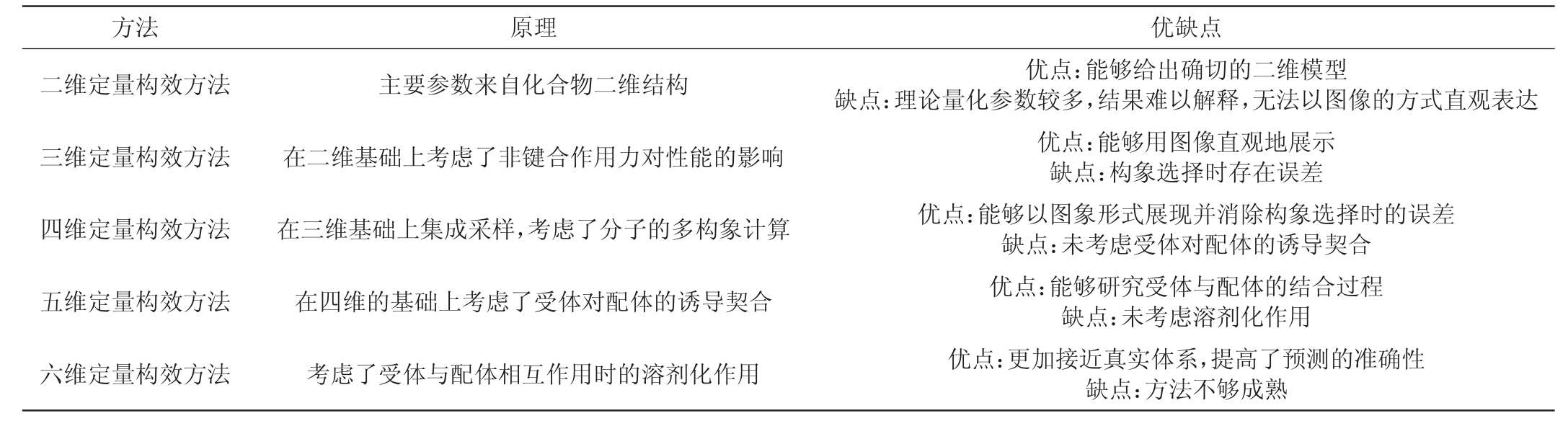
四维定量构效是在三维的基础上考虑了分子的多构象计算;五维定量构效是在四维的基础上考虑了受体对配体的诱导契合;六维定量构效进一步考虑了受体和配体相互作用时的溶剂化作用。
表2 定量构效关系方法的原理及优缺点
Table 2 Principles,advantages and disadvantages of quantitative structure-activity relationship method
3 ACE抑制肽定量构效研究进展
HELLBERG S等[36-37]对20种天然氨基酸的29种理化参数进行了分类,将其分为固体大小、分子亲水性和电荷性质三类,称为z-标度(Z-scales)。采用主成分分析法(PCA)对29个理化参数描述的氨基酸的主要性质进行了总结。Z1主要与亲水性有关,Z2主要与固体尺寸有关,Z3主要与电荷性质有关。通过偏最小二乘分析得到两个潜在变量。实验结果表明,该模型预测能力较好,但不能表达构象信息。
COLLANTES E R等[38]构建了氨基酸结构并分析了氨基酸的构象,优化能量,计算量子化学参数。用氨基酸的各向同性表面积(isotropic surface area,ISA)来描述侧链基团的疏水性和分子体积。用电荷指数(charge index,ECI)描述受体侧链基团的极性和受体与侧链的偶极相互作用。实验结果表明,该过程中使用的描述子较少,所有的描述子都是根据氨基酸的空间结构计算出来的。ISA-ECI比Z-scales有更大的自由度,因此更容易研究非天然氨基酸。
林治华等[39]基于肽链的一级结构,构建了分子电负性边距矢量(molecular electronegativity edge-distance vector,VMED)。二肽由两个氨基酸残基组成,结构简单,难以形成复杂的三维结构。能方便地计算出电边缘矢量,并具有良好的活性相关性。
彭剑秋[5]将SVHEHS的13个主成分命名为SVHEHS1-SVHEHS13,分别将多元线性回归(MLR)、偏最小二乘法(PLS)、人工神经网络(ANN)用于ACE抑制肽的QSAR研究。实验表明,MLR模型方程提供的多肽活性影响信息更有针对性,模型有较好的预测效果;PLS模型获得了不同长度肽段结构与活性关系信息,模型的拟合能力、内部预测能力和稳健性良好,外部预测能力也在合理范围内;结果显示ANN模型与PLS模型有相同的预测能力。
张艳萍等[40]用PLS、支持向量机(support vector machine,SVM)、主成分分析-支持向量机(principal component analysis-support vector machine,PCA-SVM)对食源性ACE抑制二肽建模,发现三种模型的预测能力无显著差异,均能预测ACE抑制肽的活性。SVM、PCA-SVM的预测力相对较强。梅虎等[41]用PLS对苦味二肽和血管舒缓激肽促进剂建模,实验表明,VHSE比Z-scales有更精切的物化意义,并含有更丰富的氨基酸结构信息。
梅虎[42]分析了20种氨基酸的拓扑结构。从70个结构和拓扑性质中选取25个特征。通过主成分分析(PCA)得到三个主成分。对于每个氨基酸都用得分矢量VSTV1、VSTV2、VSTV3作为新的描述子代替原始矩阵。用VSTV描述子比较MLR、主成分回归(principal component regression,PCR)、PLS、人工神经网络和BP算法(artificial neural network and BP algorithms,BP-ANN)、SVM。对象为苦味二肽、血管收缩素转化酶抑制剂、血管舒缓激肽促进剂、后叶催产素和HLA-A*0201限制性CTL表位。研究表明,各种模型的建模结果基本一致。对于不同的建模对象,五种模型各有优势。
李玲霄[43]对20种氨基酸建立初始构象,通过主成分分析,分别用三类描述子的前6、3、6个主成分对氨基酸进行结构表征,代替原始矩阵,并命名为SVGMW。对血管紧张素转换酶抑制剂、苦味二肽和后叶催产素进行研究,发现SVGMW能系统表征多肽结构和生物活性间的信息,研究过程简单可靠,适用范围广,不受外界影响。运用同样的方法,筛选出几何描述符47个、特征值信息44个、分子几何反比度信息41个,通过主成分分析,用三种描述子的前6、3、2个主成分对氨基酸进行结构表征,代替原始矩阵,命名为SVGER。对血管紧张素转换酶抑制剂、苦味二肽和后叶催产素进行研究,发现SVGER也能够系统表征多肽结构和生物活性间的信息,适用范围广且不受外界影响。
4 展望
在目前研究中,定量构效关系能准确找到抑制肽结构信息与生物活性的关系,指导合成高效降压药,在药物研究中起到很重要的作用。随着研究人员对ACE抑制肽的深入了解,获得了越来越多的有效信息,但同时也存在很多问题:①由于ACE的三维结构和长肽在立体空间中的强柔性,导致二维定量构效关系很难涉及分子空间构象的变化。此后应针对长肽分子展开更高维定量构效关系的研究。②目前的肽类结构描述子优势互补,但从长远来看,还需要解决几个关键性问题:a.拟肽和环肽结构表征的问题;b.不同长度肽的结构表征问题;c.结构复杂导致的计算复杂度过高的问题。③在定量构效关系研究中,以支持向量机为代表基于核函数的建模方法成为主流,但目前需要解决几个基于核函数的各种方法的问题:a.核函数的选择;b.参数的寻优;c.计算速度的提高;d.结果的可解释性等。④前人对多肽空间位阻以及多肽对ACE活性中心Zn2+正四面体结构的影响进行了深入研究,此后可通过荧光猝灭、等温滴定量热法等实验方法对多肽与ACE之间的结合能进行研究。⑤此前研究多针对ACE抑制肽活性的体外模拟,此后可通过制备高效的ACE抑制肽进行生物实验,探究其生物利用度。
[1]许新月,崔文玉,柏雨岑,等.食用菌ACE 抑制肽制备及其功能活性研究进展[J].山东农业科学,2019,51(11):157-160,167.
[2]安桂香,庄桂东,徐振凯,等.食物中血管紧张素转化酶抑制肽的研究进展[J].食品研究与开发,2006,27(6):173-175.
[3]王晓丹,薛璐,胡志和,等.ACE 抑制肽构效关系研究进展[J].食品科学,2017,38(5):305-310.
[4]管骁,彭剑秋,金周筠,等.食源性血管紧张素转化酶抑制肽的研究进展[J].食品与发酵工业,2011,37(7):135-141.
[5]彭剑秋.ACE 抑制肽定量构效关系研究[D].上海:上海理工大学,2012.
[6]王先梅,杨丽霞.原发性高血压发病机制的研究进展[J].西南国防医药,2005(1):98-100.
[7]赵连友,王先梅.高血压病发病机制的研究现状[J].解放军保健医学杂志,2004(2):67-70.
[8]周育,韩三青,王茹茹,等.食源血管紧张素转化酶抑制肽研究进展[J].安徽农业大学学报,2019,46(5):751-760.
[9] TU M L,LIU H X,ZHANG R Y,et al.Analysis and evaluation of the inhibitory mechanism of a novel angiotensin-I-converting enzyme inhibitory peptide derived from casein hydrolysate[J].J Agric Food Chem,2018,66(16):4139-4144
[10]段秀,张玉锋,庄永亮.食源性血管紧张素转化酶抑制肽研究进展[J].食品工业科技,2012,33(20):388-393.
[11]赵爽,刘昆仑,陈复生.食源性ACE 抑制肽研究进展[J].粮食与油脂,2017,30(3):37-40.
[12]YAMAMOTO N,MAENO M,TAKANO T.Purification and characterization of an antihypertensive peptide from a yogurt-like product fermented by Lactobacillus helveticus CPN4[J].J Dairy Sci,1999,82(7):1388-1393.
[13]IBRAHIM H R,AHMED A S,MIYATA T.Novel angiotensin-converting enzyme inhibitory peptides from caseins and whey proteins of goat milk[J].J Adv Res,2017,8(1):63-71.
[14]SINGH B P,VIJ S.Growth and bioactive peptides production potential of Lactobacillus plantarum strain C2 in soy milk:A LC-MS/MS based revelation for peptides biofunctionality[J].LWT-Food Sci Technol,2017,86:293-301.
[15]ELKHTAB E,EL-ALFY M,SHENANA M,et al.New potentially antihypertensive peptides liberated in milk during fermentation with selected lactic acid bacteria and kombucha cultures[J].J Dairy Sci,2017,100(12):9508-9520.
[16]ROBERT M C,RAZANAME A,MUTTER M,et al.Identification of angiotensin-Ⅰ-converting enzyme inhibitory peptides derived from sodium caseinate hydrolysates produced by Lactobacillus helveticus NCC 2765[J].J Agric Food Chem,2004,52(23):6923-6931.
[17]ROJAS-RONQUILLO R,CRUZ-GUERRERO A,FLORES-NÁJERA A,et al.Antithrombotic and angiotensin-converting enzyme inhibitory properties of peptides released from bovine casein by Lactobacillus casei Shirota[J].Int Dairy J,2012,26(2):147-154.
[18]IROYUKIFUJITA H,EIICHIYOKOYAMA K,YOSHIKAWA M.Classification and antihypertensive activity of angiotensin I-converting enzyme inhibitory peptides derived from food proteins[J].Food Sci,2000,65(4):564-569.
[19]CHENG F Y,WAN T C,LIU Y T,et al.Determination of angiotensin-Ⅰconverting enzyme inhibitory peptides in chicken leg bone protein hydrolysate with alcalase[J].Anim Sci J,2009,80(1):91-97.
[20]YU Z P,ZHAO W Z,LIU J B,et al.QIGLF,a novel angiotensin Ⅰ-converting enzyme-inhibitory peptide from egg white protein[J].J Sci Food Agric,2011,91(5):921-926.
[21]CONNOLLYA,O'KEEFFE M B,PIGGOTT C O,et al.Generation and identification of angiotensin converting enzyme(ACE)inhibitory peptides from a brewers'spent grain protein isolate[J].Food Chem,2015,176:64-71.
[22]LIU M,D U M,ZHANG Y,et al.Purification and identification of an ACE inhibitory peptide from walnut protein[J].J Agric Food Chem,2013,61(17):4097-4100.
[23] CHIOZZI R Z,CAPRIOTTI A L,CAVALIERE C,et al.Identification of three novel angiotensin-converting enzyme inhibitory peptides derived from cauliflower by-products by multidimensional liquid chromatographyand bioinformatics[J].J Funct Food,2016,27:262-273.
[24]TOMOE F,YOSHIKATSU M,HAJIME Y,et al.Angiotensin I converting enzyme inhibitory peptides derived from phycobiliproteins of dulse palmariapalmata[J].Mar Drugs,2016,14(2):32.
[25] WANG X M,CHEN H X,FU X G,et al.A novel antioxidant and ACE inhibitory peptide from rice bran protein:Biochemical characterization and molecular docking study[J].LWT-Food Sci Technol,2017,75(3):93-99.
[26]KOYAMA M,NARAMOTO K,NAKAJIMA T,et al.Purification and identification of antihypertensive peptides from fermented buckwheat sprouts[J].J Agric Food Chem,2013,61(12):3013-3021.
[27]BYUN H G,KIM S K.Purification and characterization of angiotensin Ⅰconverting enzyme(ACE)inhibitory peptides from Alaska pollack(Theragra chalcogramma)skin[J].Process Biochem,2001,36(12):1155-1162.
[28]NAGAI T,SUZUKI N,NAGASHIMA T.Antioxidative activities and angiotensin Ⅰ-converting enzyme inhibitory activities of enzymatic hydrolysates from commercial Kamaboko type samples[J].Food Sci Tech Int,2006,12(4):335-346.
[29] HE H L,CHEN X L,SUN C Y,et al.Analysis of novel angiotensin-Ⅰ-converting enzyme inhibitory peptides from protease-hydrolyzed marine shrimp Acetes chinensis[J].J Pept Sci,2006,12(11):726-733.
[30] ZHAO Y,LI B,DONG S,et al.A novel ACE inhibitory peptide isolated from Acaudina molpadioidea hydrolysate[J].Peptides,2009,30(6):1028-1033.
[31]LIU X,ZHANG M,SHI Y,et al.Production of the angiotensin Ⅰconverting enzyme inhibitory peptides and isolation of four novel peptides from jellyfish(Rhopilema esculentum)protein hydrolysate[J].J Sci Food Agr,2016,96(9):3240-3248.
[32]YU Z,CHEN Y,ZHAO W,et al.Identification and molecular docking study of novel angiotensin-converting enzyme inhibitory peptides from Salmo salar using in silico methods[J].J Sci Food Agr,2018,98(10):3907-3914.
[33]YU Z,FAN Y,ZHAO W,et al.Novel angiotensin-converting enzyme inhibitory peptides derived from oncorhynchus mykiss nebulin:Virtual screeningand in silico molecular docking study[J].J Food Sci,2018,83(9):2375-2383.
[34]MIYOSHI S,ISHIKAWA H,KANEKO T,et al.Structures and activity of angiotensin converting enzyme inhibitors in an alpha-zein hydrolysate[J].Agrie Biol Chem,1991,55(5):1313-1318.
[35] OKAMOTO A,HANAGATA H,MATSUMOTO E,et al.Angiotensin I converting enzyme inhibitory activities of various fermented foods[J].Biosci Biotech Bioch,1995,59(6):1147-1149.
[36]HELLBERG S,SJÖSTRÖM M,SKAGERBERG B,et al.Peptide quantitative structure-activity relationships,a multivariate approach[J].Med Chem,1987,30:1126-1135.
[37] HELLBERG S,ERIKSSON L,JONSSON J,et al.Minimum analogue peptide sets(MAPS)for quantitative structure-activity relationships[J].Int J Pept Protein Res,1991,37:414-424.
[38] COLLANTES E R,DUNN W J.Amino acid side chain descriptors for quantitative structure activity relationship studies of peptide analogues[J].J Med Chem,1995,38(4):2705-2713.
[39]林治华,刘树深,李志良.寡肽结构参数化及定量构效关系研究[J].化学学报,2001,59(7):1001-1008.
[40]张艳萍,成忠,俞远志.基于3 种建模法的食源性ACE 抑制二肽QSAR研究[J].浙江科技学院学报,2015,27(3):174-182.
[41]梅虎,周原,孙立力.氨基酸结构描述子矢量VHSE 及其在肽QSAR中的应用[J].化学通报,2005(7):534-540.
[42]梅虎.肽的定量构效关系研究[D].重庆:重庆大学,2005.
[43]李玲霄.基于三种不同方法对肽类药物的QSAR 研究[D].西安:陕西科技大学,2017.