喹乙醇、卡巴氧属于喹恶啉抗菌药,因其能够促进畜禽的生长,提高瘦肉率,曾在养殖业中广泛应用[1-2]。但动物基体对于喹乙醇、卡巴氧有蓄积作用,并且会引起动物产生畸形,人体食用残留此类药物的动物后也会造成危害,因此许多国家将喹乙醇及卡巴氧列为禁用药物[3-5]。但由于该类药物价格低廉、应用方便,养殖业仍有违规添加及超剂量添加的现象存在。动物源性运动营养品是指以畜禽类的动物源性原料制成的针对运动人群开发的一类补充蛋白质的食品。因其是针对特殊人群食用的一种食品,具有一定的特殊性,对食品的安全性要求高,所以更需要对这类产品中喹乙醇及卡巴氧代谢物的残留情况进行检测和监控。
因喹乙醇和卡巴氧原药在动物体内代谢迅速,能产生多种代谢产物,喹乙醇的主要代谢产物为3-甲基-喹喔啉-2-羧酸(3-methyl-quinoxaline-2-carboxy,MQCA),卡巴氧的主要代谢产物为喹恶啉-2-羧酸(quinoxaline-2-carboxylic acid,QCA),两者在动物体内残留量相对稳定,因此一般将MQCA及QCA分别作为喹乙醇及卡巴氧的残留标示物[6-7]。目前对MQCA及QCA常用的检测方法有酶联免疫法、高效液相色谱法和高效液相色谱-质谱联用法[8-12]。动物源性运动食品中基质复杂,酶联免疫法易出现假阳性;高效液相色谱法检出限较高,基质干严重,前处理复杂;而高效液相色谱-质谱联用法抗干扰能力和定性能力较强,可以在降低检出限的同时避免假阳性的产生。目前检测MQCA及QCA的样品对象多局限在猪肉、鸡肉、鸡蛋等[13-17]。为了使检测方法更加适合动物源性运动食品的特性,本研究对前处理方法进行了改进,拟采用碱水解的前处理方式提取目标物,并优化固相萃取柱法净化提取液,建立动物源性运动食品中MQCA及QCA的固相萃取-高效液相色谱-串联质谱法(solid phase extraction-high performance liquid chromatography-tandem mass spectrometry,SPE-HPLC-MS/MS)检测方法,以期为检测和监管运动食品中喹乙醇及卡巴氧代谢物残留提供技术保障和参考。
1 材料与方法
1.1 材料与试剂
MQCA标准品(纯度99%)、QCA标准品(纯度99%):中国计量科学研究院;动物源性运动食品:市售。
1.2 仪器与设备
Agilent1120型高效液相色谱仪:美国Agilent公司;API 3500 QTrap 超高压液相色谱-三重四级杆串联质谱仪:美国AB公司;Waters Atalantis T3色谱柱(2.1 mm×50 mm,3 μm)、Waters ACQUITY UPLC BEH C18柱色谱柱(2.1 mm×50 mm,1.7 μm):美国Waters公司;HLB固相萃取柱(60 mg/3 mL)、C18固相萃取柱(60mg/3mL)、PAX固相萃取柱(60mg/3mL):杭州赛析科技有限公司。
1.3 试验方法
1.3.1 SPE-HPLC-MS/MS色谱条件
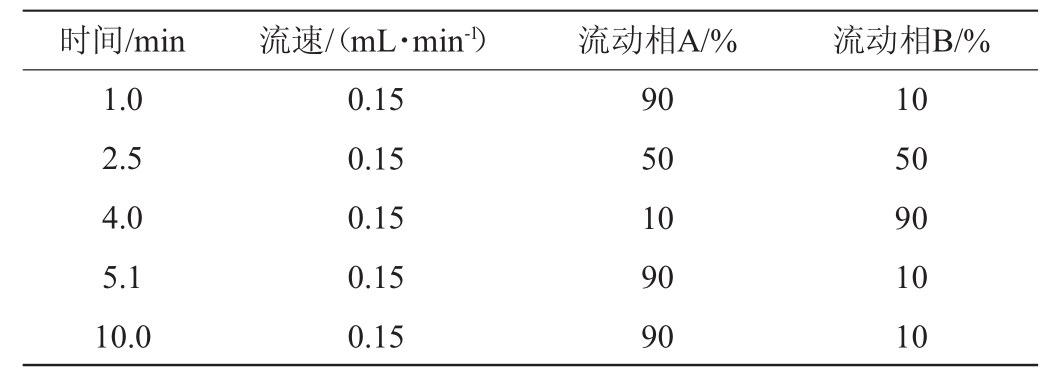
Waters Atalantis T3色谱柱(2.1 mm×50 mm,3 μm);进样体积5 μL;色谱柱温度30 ℃;流动相A为0.1%甲酸溶液,B为乙腈;梯度洗脱条件如表1所示。
表1 HPLC-MS/MS梯度洗脱条件
Table 1 HPLC-MS/MS gradient elution conditions
1.3.2 质谱条件
电喷雾离子(electrospray ionization,ESI)源正离子模式;监测模式:多反应监测(multi reaction monitoring,MRM);离子源温度:105 ℃;毛细管电压:3.0 kV;脱溶剂气流量:10 L/min;锥孔流量:0.5 L/min;去溶剂温度:400 ℃。
1.3.3 样品的提取与净化
称取5 g(精确至0.01 g)动物源性运动食品样品至50 mL离心管中,加入25 mL的2 mol/L NaOH溶液,混合均匀,50 ℃水浴条件下水解60 min。然后再加入HCl溶液将水解液调至pH值7.0后,5 000 r/min离心5 min。取上清液加入PAX阴离子固相萃取柱,分别用6 mL甲醇和水依次活化后上样,首先弃去流出液,然后用6 mL水洗涤,弃去流出液,用3 mL 1%的氨水甲醇溶液洗脱,收集洗脱液并于40 ℃氮气吹干。残余样品用1.0 mL流动相溶解混匀,用0.22 μm有机滤膜过滤,供液相串联质谱检测。
1.3.4 标准曲线的建立
分别称量10 mg MQCA和QCA标准品,用甲醇配制成1mg/mL的标准混合储备液,再稀释成质量浓度均为1μg/mL的中间标准溶液。临用前,将0.1%甲酸水溶液配制成质量浓度为0.1~50.0 ng/mL的系列标准溶液,以标准品质量浓度(X)为横坐标,峰面积(Y)为纵坐标绘制标准曲线。
1.3.5 方法学考察
以未检出MQCA和QCA的动物源性运动食品为空白基质,加入3个梯度的混合标液,碱水解提取后使用固相萃取柱净化和富集后,上机检测MQCA和QCA的含量,计算回收率,并对每个结果测定6次,进行精密度与重复性的测定。
2 结果与分析
2.1 色谱柱的选择
由于MQCA和QCA为极性化合物[18],实验考察了Waters AtalantisT3色谱柱(2.1mm×50mm,3μm)和WatersACQUITY UPLC BEH C18色谱柱(2.1 mm×50 mm,1.7 μm)对MQCA和QCA分离效果的影响,结果见图1。
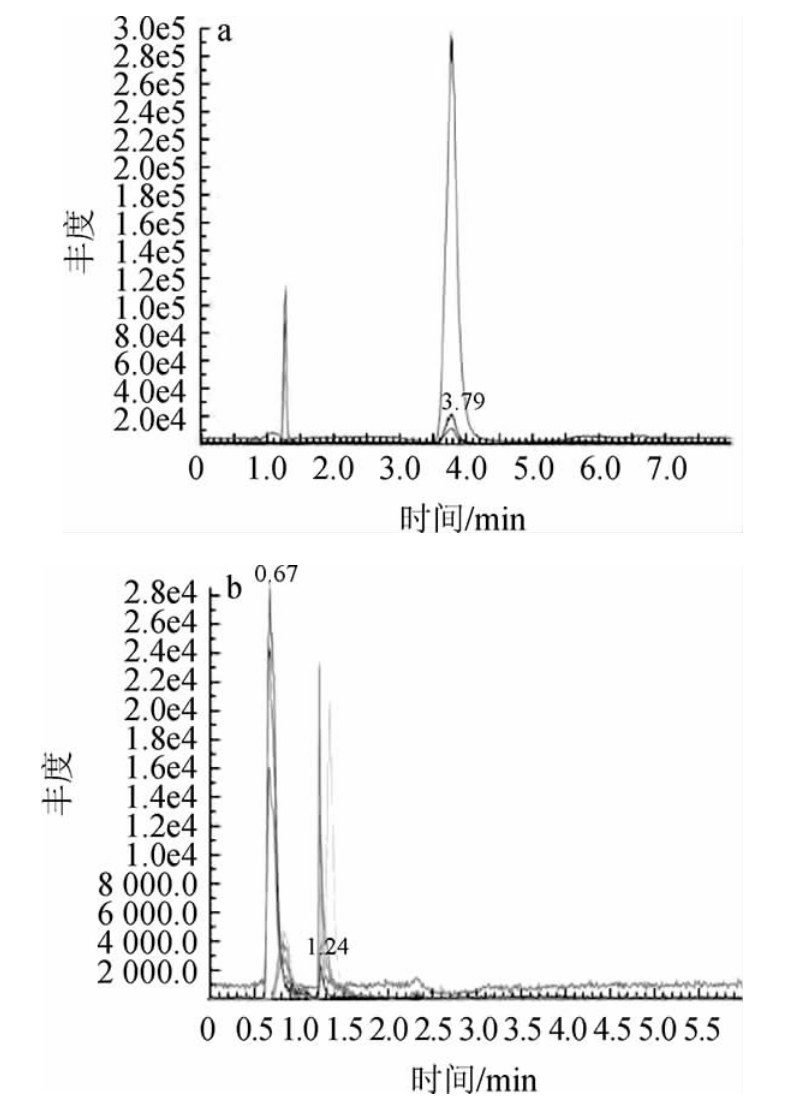
图1 不同色谱柱条件下MQCA及QCA的总离子流色谱图
Fig.1 Total ion chromatogram of MQCA and QCA under different chromatographic column conditions
由图1可知,Waters Atalantis T3色谱柱具有明显的优势,对极性化合物具有较好的保留效果,MQCA及QCA的峰形得到改善,与基质中的杂质也有较好的分离度,峰型尖锐,整个分离过程可以在5 min内完成。因此,本试验选择Waters Atalantis T3色谱柱。
2.2 流动相体系的选择
流动相的不同组成会影响MQCA及QCA的分离和离子化效率,从而影响到目标物的检测灵敏度[19-20]。在流动相选择中,比较了甲醇、乙腈、甲醇-0.1%甲酸、乙腈-0.1%甲酸、甲醇-0.1%氨水、乙腈-0.1%氨水作为流动相时MQCA及QCA检测灵敏度及出峰情况。
结果发现,流动相体系中含有乙腈会改善起到目标物峰形的作用,乙腈-0.10%甲酸及乙腈-0.1%氨水均能分离测定MQCA及QCA。但乙腈-0.1%氨水流动相体系下,MQCA响应低且QCA峰形拖尾展宽严重;乙腈-0.1%甲酸体系下,两个目标物均有较高响应,峰形窄,这是因为在ESI+模式下流动相中加入了0.1%的甲酸,提供质子来源,显著提高了目标物离子化效率。
2.3 质谱条件的选择
用质量浓度为20 ng/mL的混合标准溶液,对MQCA及QCA进行一级和二级质谱扫描,并优化质谱参数,具体质谱分析参数见表2。
表2 多反应监测模式下MQCA及QCA的质谱参数
Table 2 MS parameters of MQCA and QCA under multi reaction monitoring mode

注:“*”为定量离子。
2.4 方法的线性范围、回归方程、相关系数、检出限及定量限
在乙腈-0.1%甲酸流动相体系中,以表1梯度洗脱的步骤检测,绘制MQCA及QCA的标准曲线,其线性回归方程、相关系数、检出限及定量限见表3。由表3可知,MQCA及QCA在0.1~50 ng/mL的质量浓度范围内均具有良好的线性关系,相关系数(R2)均>0.999。检出限均为0.05 μg/kg,定量限均为0.20 μg/kg。结果表明,方法的灵敏度能满足检测要求。
表3 MQCA及QCA的出峰时间、标准曲线回归方程、相关系数、检出限及定量限
Table 3 Peak time,standard curve regression equation,correlation coefficient,detection limit and quantitative limit of MQCA and QCA

2.5 前处理方式的优化
2.5.1 碱水解条件的选择优化
MQCA及QCA在动物源性样品中与基质一般以共价键结合,需对样品进行水解,常用的有酶水解、酸水解、碱水解3种方法[21-22]。其中酶解法耗时长,酸解法提取效率不高,后续净化效果不理想。本试验采用强碱水解的方式短时间内将目标物从基质中解离出来[23-25]。
通过比较不同的碱水解时间以及NaOH碱溶液的浓度,以水解液状况评价水解效果,优化碱水解条件。选择水解时间分别为20 min、40 min、60 min、80 min、100 min、120 min,NaOH溶液浓度分别采用0.2 mol/L、0.5 mol/L、1.0mol/L、2.0 mol/L、5.0 mol/L、10.0 mol/L,在60 ℃条件下对样品进行水解。结果表明,NaOH碱溶液浓度在0.2~1.0 mol/L时,水解过程耗时较长,120 min后水解液中有样品基质残渣剩余,水解不完全;NaOH碱溶液浓度在5.0~10.0 mol/L时,水解液变得浓稠,不利于后续的提取净化步骤。选择2.0 mol/L NaOH碱溶液水解60 min时,样品被完全水解,没有样品基质残渣剩余,MQCA及QCA能从样品中被完全释放出来。因此,选择2.0 mol/L NaOH碱溶液水解60 min为最佳条件。
2.5.2 SPE柱的选择优化
由于MQCA及QCA的化学结构中具有喹喔啉-1,4-二氮氧结构,其在弱碱或者酸性条件下能离子化成为分子,实验对已经商品化的HLB、C18以及PAX共3种固相萃取小柱的净化效果进行对比,记录目标物峰面积,分析不同类型的SPE柱对MQCA及QCA提取的影响,结果见图2。
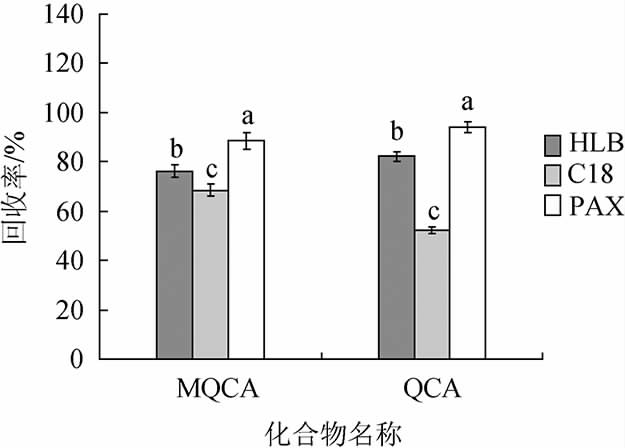
图2 MQCA及QCA经不同SPE柱处理后的回收率
Fig.2 Recovery rate of MQCA and QCA treated by different SPE columns
由图2可知,PAX固相萃取柱回收率最好(MQCA回收率88.5%,QCA回收率94.2%),两个目标组分的回收率最高,且不同类型SPE柱间目标组分的回收率差异显著(P<0.05)。因此选择PAX固相萃取柱进行固相萃取净化,且对60 mg/3 mL和150 mg/6 mL两种规格的PAX固相萃取柱进行比较,发现对MQCA及QCA都有非常好的保留,回收率没有明显差异,从节省成本的角度考虑,PAX固相萃取柱(60 mg/3 mL)更为合适。
2.6 方法的精密度与加标回收率
在加标回收实验中,分别选用蛋奶类动物源性基质和肉类动物源性基质2种动物源性基质的样品,分别添加2倍限量(低)、5倍限量(中)和10倍限量(高)(0.4 μg/kg、1.0 μg/kg和2.0 μg/kg)的3个水平混合标准品,每个结果测定6次,进行精密度及加标回收率的试验,计算相对标准偏差(relative standard deviation,RSD)结果见表4。
表4 加标回收率及精密度试验结果
Table 4 Standard recovery rate and precision test results
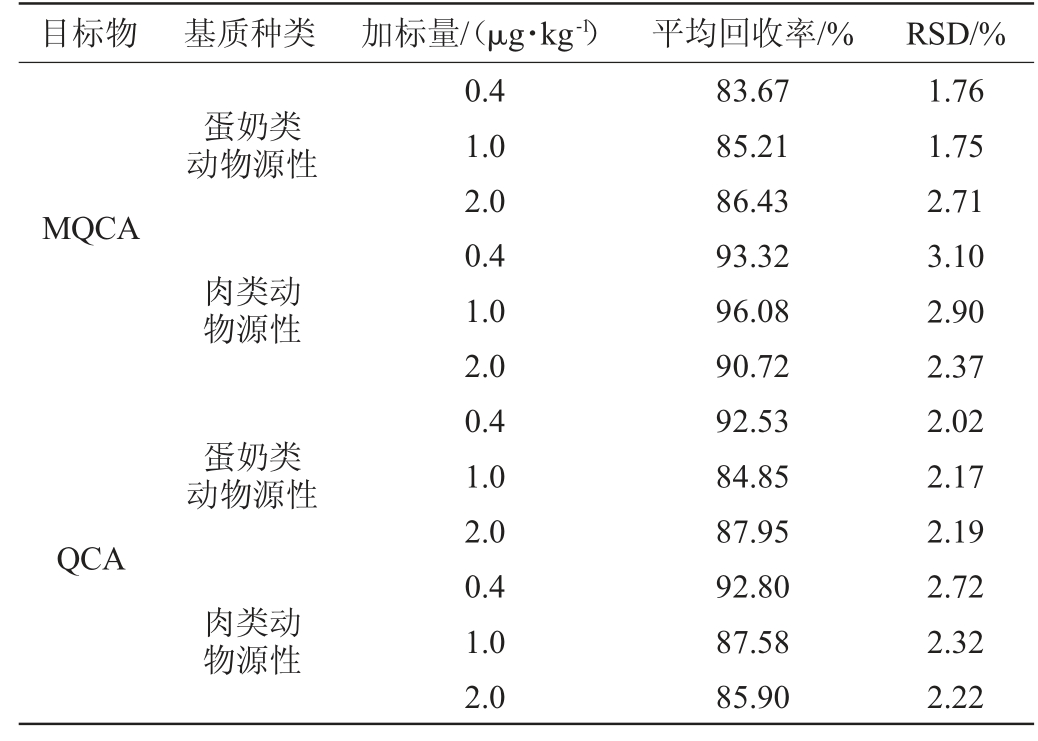
由表4可知,在两种不同的种类基质样品中,MQCA及QCA的平均回收率为83.67%~96.08%,在80%~120%范围内;精密度实验结果相对标准偏差(relative standard deviation,RSD)为1.75%~3.10%,RSD均<5%,说明本实验的检测数据的准确度和精密度良好。
3 结论
本研究通过在碱性环境下水解提取样品中的MQCA及QCA,经PAX固相萃取柱(60 mg/3 mL)净化处理后,建立了一种快速、准确检测MQCA及QCA在动物源性运动食品中残留量的SPE-HPLC-MS/MS方法。在蛋奶类动物源性基质和肉类动物源性基质中的加标回收率为83.67%~96.08%,精密度实验结果相对标准偏差为1.75%~3.10%(n=6)。该方法具有可靠的准确度和精密度,能准确快速有效地检测动物源性运动食品中的MQCA及QCA的残留量,可为该方面的分析和监控提供技术支持。
[1]谢洁,龚晓云,翟睿,等.动物源性食品中喹噁啉类药物及其代谢物残留检测技术研究进展[J].食品安全质量检测学报,2018,9(15):3985-3963.
[2]陆桂萍,曲斌,耿士伟,等.液相色谱-串联高分辨质谱测定鸡肉中卡巴氧、喹乙醇的代谢物残留[J].中国家禽,2016,38(2):33-36.
[3]LIU Z Y,SUN Z L.The metabolism of carbadox,olaquindox,mequindox,quinocetone,and cyadox:An overview[J].Med Chem,2013,9(8):1017-1027.
[4]陈俊秀,张秀清,李文廷,等.超高效液相色谱-串联质谱法测定奶酪中喹乙醇及其代谢物[J].食品安全质量检测学报,2018,9(12):3171-3176.
[5]农业部.中华人民共和国农业部第2638 号公告停止在食品动物中使用喹乙醇、氨苯胂酸、洛克沙胂等3 种兽药[S].北京:农业部兽医局,2018.
[6]PEREIRA H A,KASUS J A,GRIFFITH G L.Peptide compounds and methods of production and use thereof:US,9624283[P].2017-04-18.
[7]黄学泓,张林田,张冬辉.超高效液相色谱串联质谱法测定全价饲料中5 种喹噁啉类药物[J].饲料检测,2015(11):48-52.
[8]张静余,杨卫军,严敏鸣.液相色谱-串联质谱法测定水产品中喹乙醇和卡巴氧的代谢物残留量[J].食品安全质量检测学报,2018,9(14):3788-3793.
[9]LIU Z,PAN J.A practical method for extending the biuret assay to protein determination of corn-based products[J].Food Chem,2017,62(5):48-49.
[10]杨挺,许秀琴,赵健,等.高效液相色谱-串联质谱法测定猪血中盐酸可乐定和盐酸赛庚啶[J].肉类研究,2015,29(6):25-28.
[11]ARROYO-MANZANARES N,GÁMIZ-GRACIA L,GARCÍACAMPANˇA A M.Alternative sample treatments for the determination of sulfonamides in milk by HPLC with fluorescence detection[J].Food Chem,2014,143(11):459-464.
[12]肖利龙,花锦.超高效液相色谱法-串联质谱法测定兔肉中喹乙醇代谢物残留量[J].农产品加工,2015(12):53-55.
[13]李洪波,许小友,黄志伟,等.超高效液相色谱-串联质谱法测定饲料中的恩诺沙星和喹乙醇药物的含量[J].饲料工业,2016,37(22):53-57.
[14]孙清荣,李楠,郭礼强,等.HPLC-MS/MS 法测定猪肉中克伦特罗和莱克多巴胺[J].食品研究与开发,2016,37(20):154-157.
[15]ROSE A,FUNK D,NEIGER R.Comparison of refractometry and biuret assay for measurement of total protein concentration in canine abdominal and pleural fluid specimens[J].J Am Vet Med A,2016,248(7):789-793.
[16]张静,高玉时,唐梦君,等.高效液相色谱-串联质谱法同时测定鸡肉、鸡蛋中喹乙醇和卡巴氧及代谢物残留[J].食品安全质量检测学报,2019,10(2):469-475.
[17]SAPAN C V,LUNDBLAD R L.Review of methods for determination of total protein and peptide concentration in biological samples[J].Pro Clin Appl,2015,9(3/4):268-276.
[18]KAUR P,SINGH S K,GULATI M,et al.UV spectrophotometric method for estimation of polypeptide-k in bulk and tablet dosage forms[J].J Appl Spectrosc,2016,82(6):1060-1063.
[19]李佩佩,张小军,严忠雍,等.免疫亲和柱净化-超高效液相色谱-串联质谱检测鱼虾中3-甲基-喹噁啉-2-羧酸[J].食品科学,2016,37(24):257-261.
[20]史艳伟,孟丽华,江桂英.高效液相色谱法测定渔业用水中喹乙醇代谢物残留量[J].中国渔业质量与标准,2019,9(1):64-67.
[21]师真,杨在英,张瑞雨,等.超高效液相色谱-串联质谱法检测罗非鱼中喹乙醇及其衍生物[J].食品安全质量学报,2020,11(6):1803-1807.
[22]谢小华,周德山,宋向明,等.高效液相色谱法测定水产品中喹乙醇残留量[J].理化检验-化学分册,2011,47(1):102-103.
[23]郑玲,吴玉杰,李湧,等.高效液相色谱-串联质谱法测定动物源食品中3-甲基喹喔啉-2-羧酸和喹喔啉-2-羧酸残留[J].色谱,2012,30(7):660-664.
[24]郭霞,孙振中,戚隽渊,等.南美白对虾中喹乙醇及其代谢物3-甲基-喹恶啉-2-羧酸残留的高效液相色谱-串联质谱检测[J].中国农业大学学报,2014,19(1):156-160.
[25]赵珊,郭巧珍,张晶,等.超高压液相色谱-串联质谱法测定鱼组织中卡巴氧及喹乙醇代谢物[J].食品安全质量检测学报,2013,4(1):124-128.