乳酸菌(lactic acid bacteria)是一类能够利用碳水化合物进行发酵产生大量乳酸的细菌的统称。乳酸菌在自然界中分布相当广泛,其应用价值也比较高,相关研究已证明乳酸菌具有维持肠道生理平衡、免疫调节、降低胆固醇、抗氧化等益生功能[1-4],已广泛用于食品、工业等领域[5-6]。
肠道中的乳酸菌能激活淋巴细胞或巨噬细胞产生细胞因子,进而促进免疫细胞的增殖、分化或增强免疫反应[7]。PATURI G等[8]采用乳杆菌对小鼠进行灌胃,发现小鼠肠道中的白介素(interleukin,IL)-10和干扰素(interferon,IFN)-γ水平增加,免疫球蛋白(immune globulin,IgA)分泌也增加,证明乳杆菌可以提高小鼠免疫系统的功能。鼠李糖乳杆菌(Lactobacillus rhamnosus)LV108干预免疫抑制模型大鼠4周,显著增加了大鼠肠道内乳酸菌、双歧杆菌,降低了肠杆菌、肠球菌的含量,证明乳杆菌可以增加肠道有益菌,减少有害菌的数量[9]。大量实验表明,益生菌可以通过影响固有免疫和适应性免疫应答,从而在肠道和全身水平引起免疫调节作用[10-13]。
环磷酰胺(cyclophosphamide,CTX)是一种烷基化剂,广泛用于治疗肿瘤和癌症[14]。然而,有研究表明,CTX对人和动物的正常细胞都有毒性作用,其中骨髓抑制和免疫抑制是最常见的两种副作用[15],故CTX常被用来构建免疫抑制小鼠模型[16]。本研究以源于发酵泡菜中的乳酸菌BC299为研究对象,采用形态观察、生理生化试验及分子生物技术对其进行菌种鉴定,研究其耐酸、耐胆盐、耐抗生素能力,并采用CTX诱导免疫抑制小鼠,研究其对免疫抑制模型小鼠肠道菌群多样性和丰度的影响,为益生菌影响免疫调节奠定理论基础。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种菌株BC299:由本课题组筛选,保藏于中国科学院微生物研究所菌种保藏中心,菌种保藏号为CGMCC6326。
1.1.2 培养基
MRS液体培养基[17]:牛肉膏10.0 g,酵母膏5.0 g,蛋白胨10.0 g,葡萄糖20.0 g,磷酸氢二钾2.0 g,无水乙酸钠5.0 g,硫酸镁0.2 g,硫酸锰0.05 g,柠檬酸铵2.0 g,吐温80 1.0 mL,加蒸馏水定容至1 000 mL,调节pH至6.2~6.4,115 ℃高压蒸汽灭菌15 min。固体培养基中添加琼脂粉15~20 g。
1.1.3 主要试剂
革兰氏染色试剂盒:南京建成生物有限公司;0.3%牛胆盐:天津市英博生化试剂有限公司;16S rDNA基因聚合酶链式反应(polymerase chain reaction,PCR)扩增引物:天津金唯智生物科技有限公司;10%福尔马林:天津市江天化工有限公司;API 50 CHL试剂盒:法国梅里埃公司;卡那霉素、链霉素、红霉素、氯霉素、氨苄西林、青霉素G、利福平和头孢噻吩:上海生工生物工程股份有限公司。
1.2 仪器与设备
YS100生物显微镜:日本NIKON公司;SU-1510扫描式电子显微镜:日本日立公司;全自动凝胶成像仪:美国BIO-RAD公司;Multiskan GO型酶标仪:美国Thermo公司;HFsafe 900型超净工作台:上海力申科学仪器有限公司。
1.3 试验方法
1.3.1 菌株BC299的鉴定
形态学鉴定:参照《伯杰氏细菌鉴定手册》[18]对菌株BC299的形态进行鉴定。
生理生化鉴定:参照《伯杰氏细菌鉴定手册》[18]进行生理生化实验,并采用API 50 CHL试剂条进行碳水化合物发酵试验。
分子生物学鉴定:参考王海英等[19-20]的方法采用细菌通用引物27F(5'-AGAGTTTGATCCTGGCTCAG-3')、1492R(5'-GGTTACCTTGTTACGACTT-3')对菌株BC299的16S rDNA基因序列进行PCR扩增,PCR扩增产物送至天津金唯智生物科技有限公司进行测序。将得到的序列提交至美国国家生物技术信息中心(national center for biotechnology information,NCBI)的GenBank数据库中进行基本局部比对搜索工具(basic local alignment search tool,BLAST)同源性比对搜索,选取同源性较高的模式菌株的16S rDNA基因序列,采用Mega 4.1软件构建系统发育树。
1.3.2 菌株BC299生长曲线及产酸曲线的测定
将-80 ℃冻藏的菌株BC299划线于MRS固体培养基,37 ℃活化培养24 h;挑取单菌落,接种至3 mL MRS液体培养基中,37 ℃静置培养24 h作为种子液;按3%(V/V)的接种量将种子液接种于MRS液体培养基中,37 ℃静置培养,每隔3 h取样,测定其在波长600 nm处的吸光度值(OD600nm值)及pH值的变化。
1.3.3 菌株BC299对模拟胃酸及牛胆盐耐受性的测定
将菌株BC299种子液按4%(V/V)的接种量接种于pH=2.0的MRS液体培养基[21],37 ℃静置培养,培养0 h、1 h、2 h时取样,采用梯度稀释法涂布于MRS固体培养基进行菌落计数[22],从而确定菌株BC299对模拟胃酸的耐受性。
将菌株BC299种子液按4%(V/V)的接种量接种于含0.3%牛胆盐的MRS液体培养基,以不含胆盐的MRS液体培养基作为对照,37 ℃静置培养。每隔一定时间取样,测定其在波长600 nm处的吸光度值升高0.3所需要的时间[23-24],从而确定菌株BC299对0.3%牛胆盐的耐受性。
1.3.4 菌株BC299的药敏试验
根据凡琴等[25]的方法,进行菌株BC299的药敏试验。将菌株BC299按4%(V/V)的接种量接种于MRS液体培养基中37 ℃静置培养至对数期,离心收集菌体并用生理盐水调整菌液浓度至0.5麦氏比浊度,然后用灭菌的棉棒蘸取少量的菌液,分别接种于含卡那霉素、链霉素、红霉素、氯霉素、氨苄西林、青霉素G、利福平和头孢噻吩的MRS固体培养基,质量浓度均分别为512 μg/mL、256 μg/mL、128 μg/mL、64 μg/mL、32 μg/mL、16 μg/mL、8 μg/mL、4 μg/mL、2 μg/mL、1 μg/mL、0.5 μg/mL、0.25 μg/mL和0.125 μg/mL,37 ℃培养24~48 h,记录菌株的最低抑菌浓度(minimal inhibitory concentration,MIC)值,确定菌株的耐药性。
1.3.5 免疫抑制模型小鼠的构建及处理
参考WANG X等[26]的方法构建免疫抑制模型小鼠,将雄性BALB/c小鼠随机分成3组,即正常组、模型组、实验组。模型组和实验组小鼠,在试验第1~3天、18天和22天腹腔注射80 mg/kg CTX,以诱导建立免疫抑制模型,正常组腹腔注射等量生理盐水。在第4~28天,实验组连续灌胃菌株BC299的菌悬液(1×109 CFU/mL)0.2 mL,正常组和模型组连续灌胃生理盐水0.2 mL。
1.3.6 小鼠小肠的HE染色
选取小鼠相同位置的小肠部分浸泡至10%福尔马林溶液中,固定好后送样至武汉塞维尔生物科技有限公司做HE染色切片。
1.3.7 小鼠肠道粪便16S rDNA测序
在灌胃结束后,无菌采集各组小鼠粪便,收集完成后,立即将粪便放入-80 ℃冰箱保存。委托天津金唯智生物科技有限公司进行肠道菌群分析。
2 结果与分析
2.1 乳酸菌BC299的鉴定
2.1.1 形态学鉴定结果
将菌株BC299在MRS固体培养基上培养48 h,观察菌落及细胞形态,结果见图1。由图1可知,菌株BC299的菌落呈乳白色,圆形,中心凸起,边缘整齐。个体呈现单独存在或短链状排列,细胞呈短杆状,宽0.4~0.6 μm,长1.3~2.3 μm,无芽孢,无鞭毛。
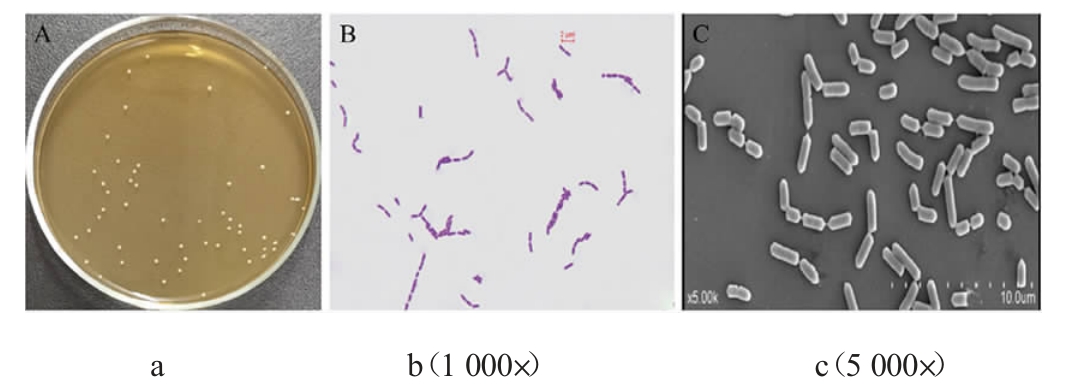
图1 菌株BC299的菌落(a)及细胞(b,c)形态
Fig.1 Colony (a) and cell (b,c) morphology of strain BC299
2.1.2 生理生化试验鉴定结果
菌株BC299的生理生化试验结果见表1。由表1可知,菌株BC299为革兰氏阳性菌;过氧化氢酶及硝酸盐还原试验呈阴性;不运动;不产硫化氢;能酸化和凝固牛乳;10 ℃生长;45 ℃不生长;可以耐受45%的NaCl。应用API 50 CHL试剂条对菌株BC299发酵碳水化合物的能力进行测定,结果见表2。将表2结果输入API LAB Plus鉴定系统进行比对,比对结果显示菌株BC299为植物乳杆菌(Lactobacillus plantarum)。参考《伯杰氏细菌鉴定手册》[18]、《乳酸菌分类鉴定及实验方法》[27],初步判定菌株BC299为乳杆菌属(Lactobacillus sp.)。
表1 菌株BC299的生理生化试验结果
Table 1 Results of physiological and biochemical tests of strain BC299
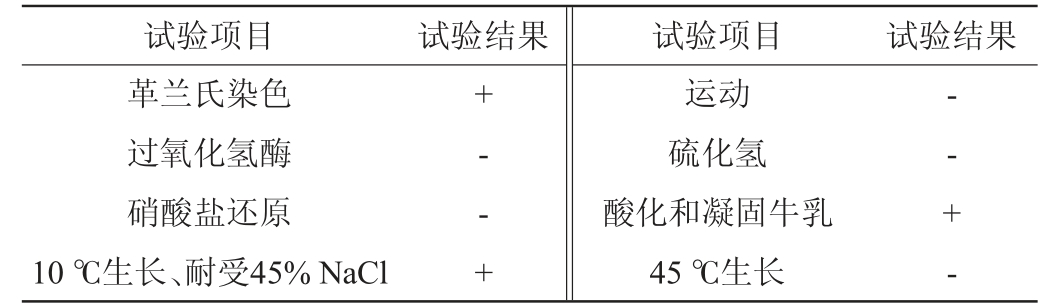
注:“-”表示结果呈阴性,“+”表示结果呈阳性。下同。
表2 菌株BC299的碳水化合物发酵试验结果
Table 2 Results of carbohydrate fermentation tests of strain BC299
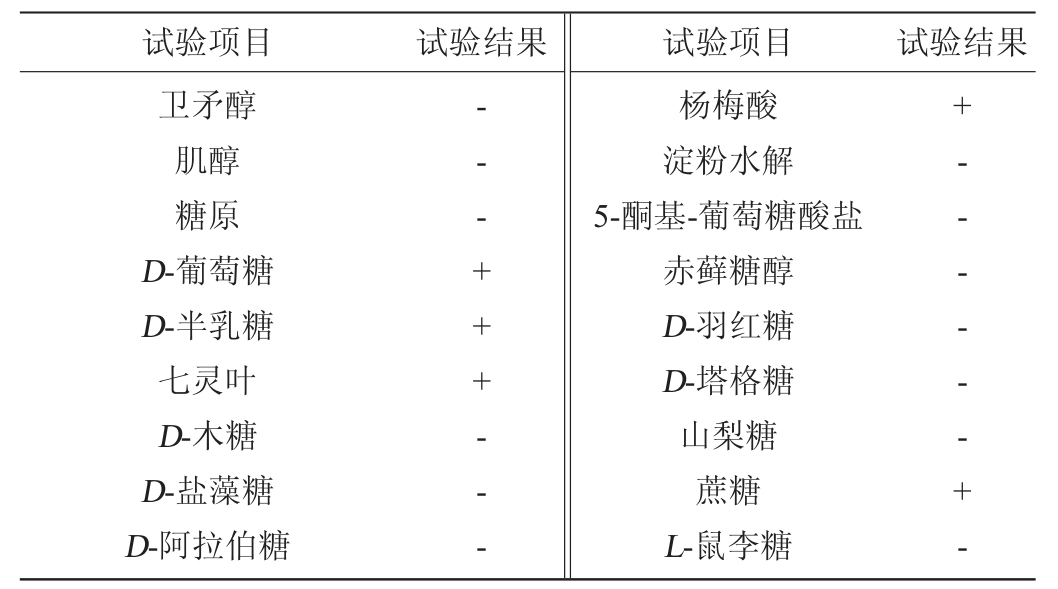
续表

2.1.3 分子生物学鉴定结果
基于16S rDNA基因序列,菌株BC299的系统发育树见图2。由图2可知,菌株BC299与植物乳杆菌(Lactobacillus plantarum)S-24处于同一个分支,同源性为100%,亲缘关系最近,结合形态观察及生理生化试验结果鉴定菌株BC299为植物乳杆菌(Lactobacillus plantarum),其在NCBI GenBank数据库中的序列号为MW221321.1。
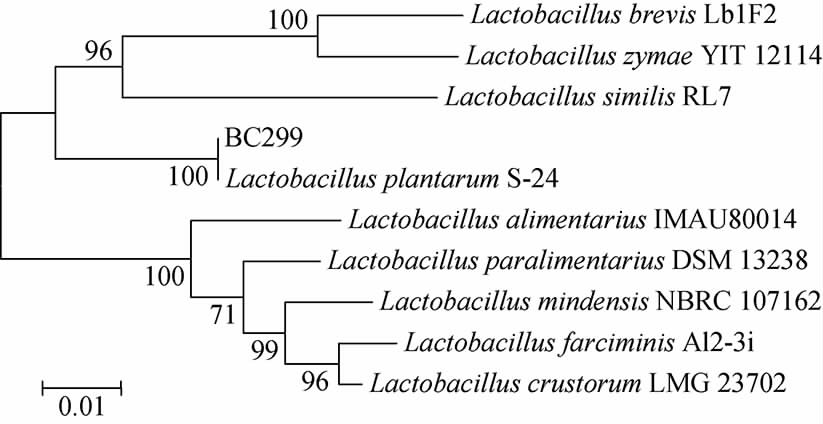
图2 基于16S rDNA基因序列菌株BC299的系统发育树
Fig.2 Phylogenic tree of strain BC299 based on 16S rDNA gene sequences
2.2 植物乳杆菌BC299的生长特性
2.2.1 生长曲线和产酸曲线
菌株BC299的生长曲线及产酸曲线见图3。由图3可知,菌株BC299在培养的0~3 h处于生长适应期,生长代谢缓慢,产酸较少;从第3小时开始,菌株BC299的生长速度不断加快,进入生长对数期,菌体呈几何级数递增,由生长代谢产生的有机酸也在不断地积累,pH值下降;21 h后进入稳定期,菌体数量和pH值均趋于稳定。
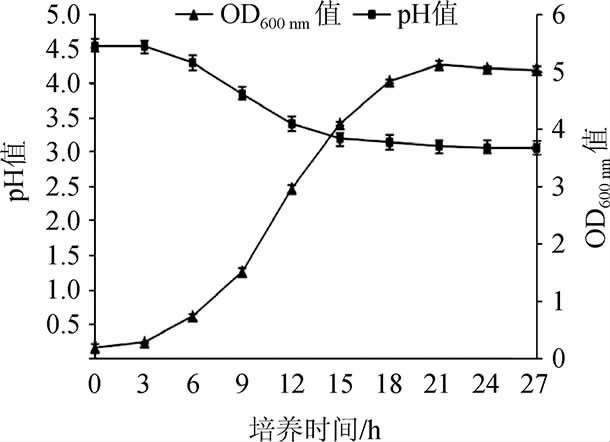
图3 植物乳杆菌BC299的生长曲线和产酸曲线
Fig.3 Growth and acid production curve of Lactobacillus plantarum BC299
2.2.2 耐酸及耐胆盐特性
菌株BC299的耐酸特性见表3。由表3可知,在pH=2.0环境中,菌株BC299培养2 h后,活菌数由初始的(2.51±1.01)×108 CFU/mL下降至(1.81±1.58)×106 CFU/mL,一般认为益生菌产品发挥功能特性的活菌数临界值为106 CFU/mL[28],说明菌株BC299有在肠道中存活并发挥作用的可能性。
表3 植物乳杆菌BC299对酸的耐受性
Table 3 Tolerance of Lactobacillus plantarum BC299 to acid

菌株BC299的耐胆盐特性见表4。由表4可知,菌株BC299在含0.3%牛胆盐的环境中,OD600nm值升高0.3的生长延滞时间为0.61 h,参考BAO Y等[23]从内蒙古传统发酵乳制品中分离获得的乳杆菌株在0.3%胆盐下耐受性结论,菌株BC299具有良好的胆盐耐受性。
表4 植物乳杆菌BC299对胆盐的耐受性
Table 4 Tolerance of Lactobacillus plantarum BC299 to bile salts

2.2.3 耐药性
菌株BC299对8种抗生素的MIC值见表5。
表5 植物乳杆菌BC299对8种抗生素的最小抑制浓度值
Table 5 Minimum inhibitory concentrations value of Lactobacillus plantarum BC299 on 8 antibiotics
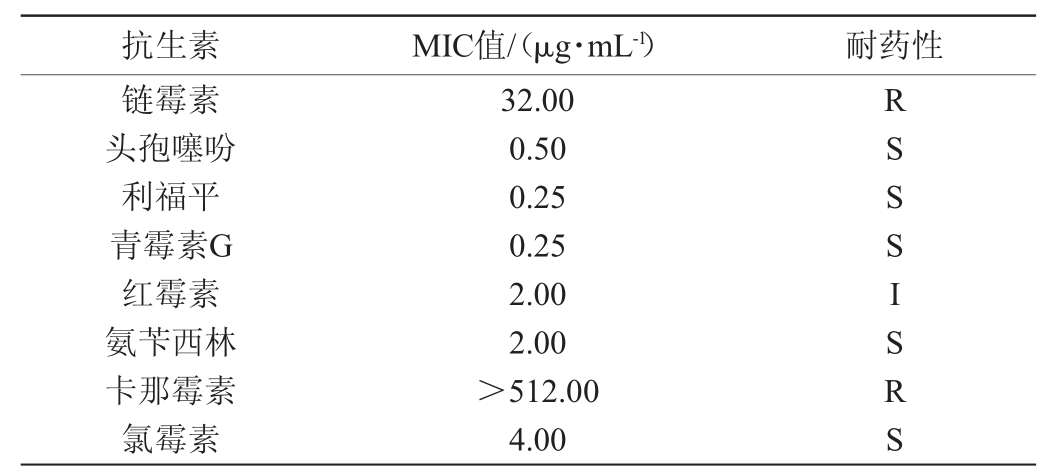
注:S为敏感;I为中敏;R为耐药。
由表5可知,菌株BC299对卡那霉素和链霉素呈现出耐药性,对红霉素表现为中敏感,对氯霉素、氨苄西林、青霉素G、利福平和头孢噻吩表现为敏感。
2.3 植物乳杆菌BC299对免疫抑制小鼠肠道菌群的影响
2.3.1 免疫抑制小鼠小肠HE切片结果
菌株BC299对小鼠小肠HE切片的影响见图4。由图4可知,正常组小鼠小肠绒毛排列整齐,组织结构清晰;模型组小鼠小肠绒毛变短萎缩,组织结构混乱;实验组小鼠小肠组织的绒毛长度及组织形态较模型组有一定程度改善。以上结果表明,菌株BC299对免疫抑制小鼠小肠组织状态有一定调节作用。
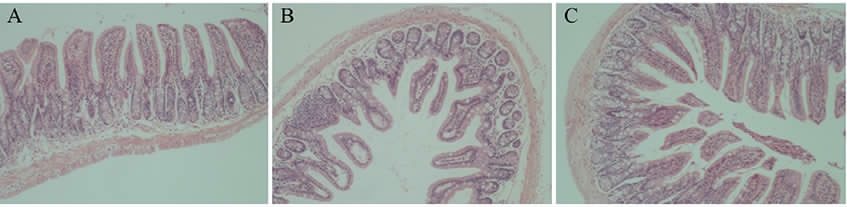
图4 小鼠小肠的组织病理学观察结果(400×)
Fig.4 Histopathology observation results of small intestine of mice(400×)
A:正常组;B:模型组;C:实验组。
2.3.2 小鼠粪便样本中菌群OTU数及α多样性分析
小鼠粪便样本中菌群操作分类单元(operational taxonomic unit,OTU)结果见图5。由图5可知,正常组、模型组与实验组小鼠的肠道菌群总OTUs值分别为241个、241个和243个,各组之间没有显著性差异(P>0.05)。小鼠粪便样本中菌群α多样性分析结果见表6。由表6可知,3组小鼠粪便样本的Coverage均>0.99,说明样本中序列没有被测出的概率较低,取样合理,具有代表性。ACE指数和超1(Chao1)指数反映了分类学上的物种丰富度,香农(Shannon)指数和辛普森(Simpson)指数反映了样本中微生物的多样性。ACE指数、Chao1指数、Shannon指数和Simpson指数在各组别之间没有存在显著性差异(P>0.05),故进一步对各组小鼠在门和科水平上的菌群相对丰度进行比较分析。
表6 小鼠粪便样本中菌群alpha多样性指数
Table 6 Alpha-diversity indexes of flora in mice fecal samples
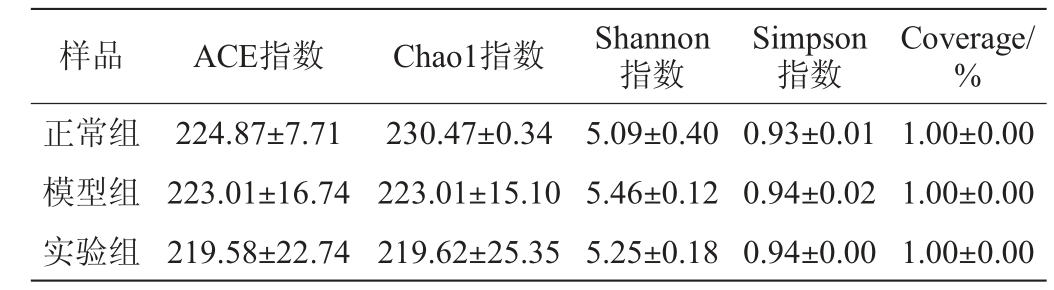
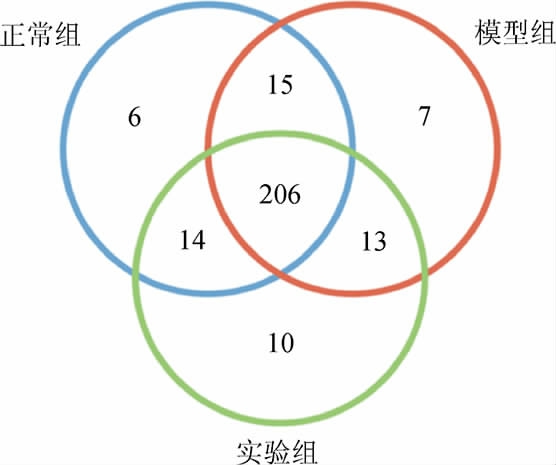
图5 小鼠粪便样本中菌群操作分类单元数量
Fig.5 Operational taxonomic unit number of microflora in mice fecal samples
2.3.3 小鼠粪便样本在门水平上的菌群丰度及差异
菌株BC299对免疫抑制小鼠肠道菌群门水平的影响见图6。由图6可知,拟杆菌门(Bacteroidetes)、硬壁菌门(Firmicutes)和放线菌门(Actinobacteria)占据了门水平整个丰度的90%以上。与正常组相比,模型组拟杆菌门相对丰度降低,实验组拟杆菌门相对丰度增加。与正常组相比,模型组硬壁菌门相对丰度升高,实验组硬壁菌门相对丰度降低。结果表明,菌株BC299对免疫抑制小鼠肠道菌群在门水平上的主要菌群的丰度有一定的影响。
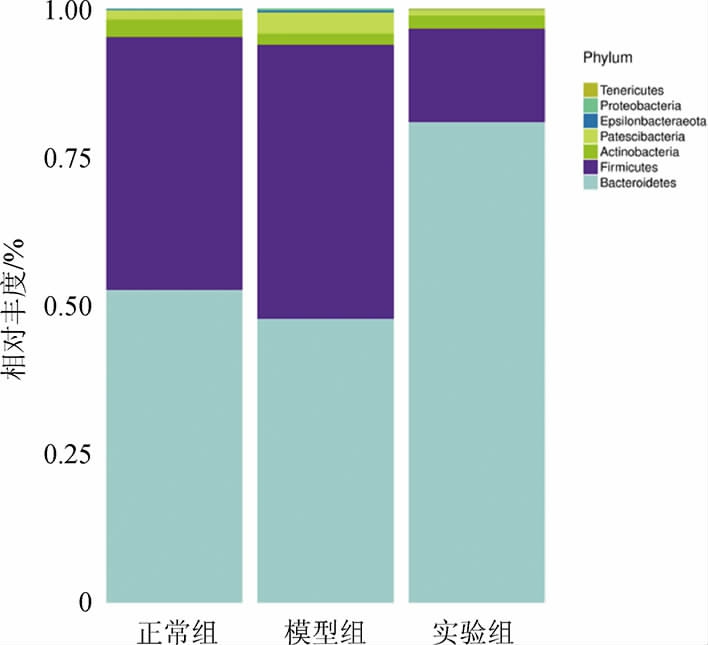
图6 肠道菌群门水平的细菌分类学分析
Fig.6 Bacterial taxonomic profiling of gut microbiota at the phylum level
2.3.4 小鼠粪便样本在科水平上的菌群丰度及差异
菌株BC299对免疫抑制小鼠肠道菌群科水平的影响见图7。由图7可知,毛螺菌科(Lachnospiraceae)、乳酸杆菌科(Lactobacilaceae)、普雷沃氏菌科(Prevotellaceae)、瘤胃球菌科(Ruminococcaceae)和拟杆菌科(Bacteroidaceae)的相对丰度较高。占比较高的毛螺菌科、瘤胃球菌科和拟杆菌科的相对丰度结果见表7。由表7可知,与正常组相比,模型组给药CTX造成了毛螺菌科相对丰度的增加;与模型组相比,给予菌株BC299悬液后,实验组毛螺菌科丰富度显著降低(P<0.05)。与正常组相比,模型组瘤胃球菌科的相对丰度显著增加(P<0.05);与模型组相比,实验组瘤胃球菌科相对丰度显著降低(P<0.05),拟杆菌科相对丰度显著增加(P<0.05)。有研究显示,毛螺菌科和瘤胃球菌科与免疫反应呈负相关;在免疫抑制改善组小鼠肠道菌群中拟杆菌科丰度较高[29]。结果表明,菌株BC299能够正向调节与免疫相关菌群的相对丰度。
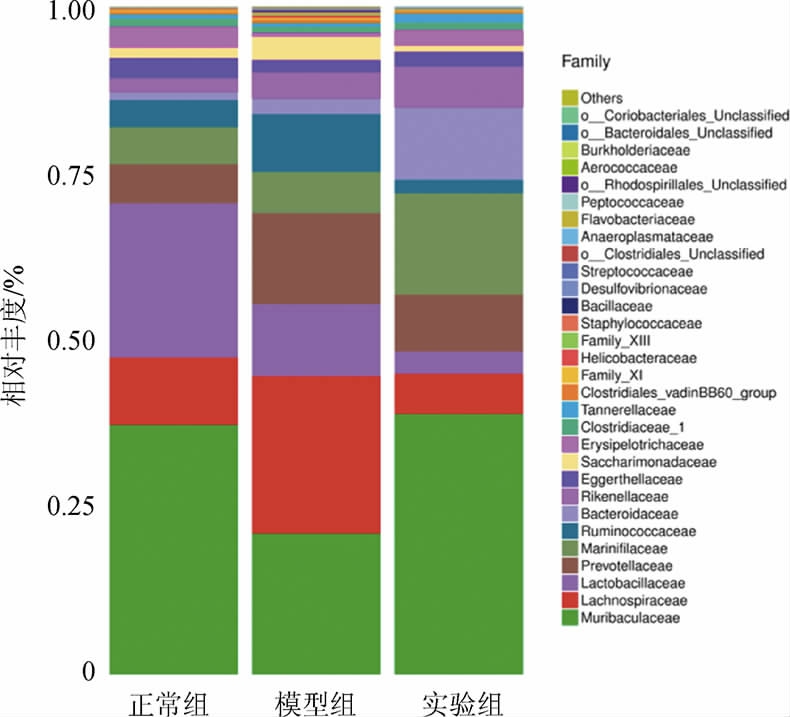
图7 肠道菌群科水平的细菌分类学分析
Fig.7 Bacterial taxonomic profiling of gut microbiota at the family level
表7 科水平优势菌的相对丰度
Table 7 Relative abundance of dominant bacteria at the family level

注:“#”表示模型组与正常组比较具有显著性差异(P<0.05);“*”表示实验组与模型组比较具有显著性差异(P<0.05)。
3 结论
以传统发酵泡菜中分离得的一株乳酸菌BC299为研究对象,经过形态学鉴定、生理生化鉴定和16S rDNA基因序列分析,鉴定该菌株为植物乳杆菌(Lactobacillus plantarum),其对pH2.0和0.3%胆盐具有良好的耐受性,对卡那霉素和链霉素呈现出耐药性,对红霉素表现为中敏感,对氯霉素、氨苄西林、青霉素G、利福平和头孢噻吩均表现为敏感。动物试验结果表明,植物乳杆菌BC299能够改善CTX诱导小鼠的小肠绒毛和组织形态的破坏,对免疫抑制小鼠的肠道菌群具有调节作用,能正向调节与免疫相关菌群的相对丰度,使小鼠肠道内毛螺菌科(Lachnospiraceae)和瘤胃球菌科(Ruminococcaceae)的相对丰度显著降低(P<0.05),拟杆菌科(Bacteroidaceae)的相对丰度显著增加(P<0.05)。
[1]OHLAND C L,MACNAUGHTON W K.Probiotic bacteria and intestinal epithelial barrier function[J].Am J Physiol-Gastr L,2010,298(6):G807-G819.
[2]任大勇.益生乳酸杆菌的黏附及免疫调节作用研究[D].长春:吉林大学,2013.
[3]KUMAR M,NAGPAL R,KUMAR R,et al.Cholesterol-lowering probiotics as potential biotherapeutics for metabolic diseases[J].J Diab Res,2012,2012(3):902-917.
[4]赵吉春.植物乳杆菌抗氧化评价及抗氧化机制研究[D].无锡:江南大学,2018.
[5]唐贤华,张崇军,隋明.乳酸菌在食品发酵中的应用综述[J].粮食与食业,2018,25(6):44-46.
[6]杜兰威,单蕊,赵蕾,等.乳酸菌的功能及其在食品工业中的应用[J].食品研究与开发,2019,40(13):221-224.
[7]XIE J H,YU Q,NIE S P,et al.Effects of Lactobacillus plantarum NCU116 on intestine mucosal immunity in immunosuppressed mice[J].J Agr Food Chem,2015,63(51):10914-10920.
[8]PATURI G,PHILLIPS M,JONES M,et al.Immune enhancing effects of Lactobacillus acidophilus LAFTI L10 and Lactobacillus paracasei LAFTI L26 in mice[J].Int J Food Microbiol,2007,115(1):115-118.
[9]薛梅.鼠李糖乳杆菌LV108 对免疫低下大鼠肠道菌群及代谢的影响研究[D].扬州:扬州大学,2016.
[10]DE VRESE M,SCHREZENMEIR J.Probiotics and non-intestinal infectious conditions[J].Brit J Nutr,2002,88(S1):S59-66.
[11]NOVERR M C,HUFFNAGLE G B,et al.Does the microbiota regulate immune responses outside the gut?[J].Trends Microbiol,2004,12(12):562-568.
[12]肖雪筠,张奕,新华·那比.四种新疆发酵驼乳源益生菌对小鼠的免疫调节作用[J].食品工业科技,2017,38(4):337-341.
[13]TANG C,SUN J,ZHOU B,et al.Effects of polysaccharides from purple sweet potatoes on immune response and gut microbiota composition in normal and cyclophosphamide treated mice[J].Food Funct,2018,9(2):937-950.
[14]刘俊业,李乐乐,江素鑫,等.环磷酰胺的临床应用及其毒性防治[J].吉林医药学院学报,2019,40(6):449-451.
[15]冯立志,何伟平,詹少锋,等.健脾补血方改善环磷酰胺诱导的小鼠骨髓及免疫抑制的机制研究[J].中药新药与临床药理,2019,30(8):904-909.
[16]许江城.4 周龄幼龄大鼠环磷酰胺免疫抑制模型的建立及应用[D].北京:中国农业大学,2017.
[17]张玢,许女,习傲登,等.一株降胆固醇作用乳酸菌KF5 的分离与鉴定[J].天津科技大学学报,2009,24(2):17-20.
[18]BUCHANAN R E,GIBBONS N E.伯杰氏细菌鉴定手册[M].北京:北京科学出版社,1984:797-807.
[19]王海英.番木瓜酵素的研究与制备[D].天津:天津科技大学,2018.
[20]孙宁,雷敬玲,吴晓青,等.自然发酵酸笋中乳酸菌的筛选鉴定及益生特性研究[J].中国酿造,2020,39(6):63-68.
[21]郭翔.降胆固醇益生乳酸菌筛选及其功能机理的研究[D].无锡:江南大学,2009.
[22]吕源玲.耐酸耐胆盐益生乳酸菌的筛选与鉴定[J].食品与机械,2017,33(6):42-45.
[23]BAO Y,ZHANG Y C,ZHANG Y,et al.Screening of potential probiotic properties of Lactobacillus fermentum isolated from traditional dairy products[J].Food Control,2010,21(5):695-701.
[24]赵芳,李艳琴,李彬春.模拟人体胃肠道环境筛选益生乳杆菌[J].微生物学通报,2016,43(6):1396-1403.
[25]凡琴,刘书亮,李娟,等.中国市售酸奶乳酸菌的耐药性分析[J].卫生研究,2012,41(3):476-479.
[26]WANG X,WANG Z Q,WU H H,et al.Sarcodon imbricatus polysaccharides protect against cyclophosphamide-induced immunosuppression via regulating Nrf2-mediated oxidative stress[J].Int J Biol Macromol,2018,120(Pt A):736-744.
[27]凌代文,东秀珠.乳酸细菌分类鉴定及实验方法[M].北京:中国轻工业出版社,1999:4-37.
[28]SHIN H S,LEE J H,PESTKA J J,et al.Viability of bifidobacteria in commercial dairy products during refrigerated storage[J].J Food Prot,2000,63(3):327-331.
[29]DING Y,YAN Y,CHEN D,et al.Modulating effects of polysaccharides from the fruits of Lycium barbarum on the immune response and gut microbiota in cyclophosphamide-treated mice[J].Food Funct,2019,10(6):3671-3683.