凯里红酸汤是源自于贵州黔东南地区的一种风味食物,经自然发酵而成。研究发现[1-2],凯里红酸汤富含乙酸、乳酸等有机酸和柠檬烯、柠檬醛和亚油酸乙酯等挥发性成分,还富含辣椒碱、番茄红素等植物活性成分。有研究认为其富含的有机酸可以用作肠道粘膜上皮的能量底物,对于维持肠道上皮细胞的紧密连接(tight junction,TJ)结构和肠道上皮粘膜的完整性有重要的作用[3-5]。紧密连接是肠上皮细胞间的主要连接方式[6],其功能的实现受紧密连接相关蛋白Occludin、Zonulaoccludens-1(ZO-1)表达的调控,高脂血症发生和进展过程中患者小肠紧密连接结构破坏[7],粘膜通透率增大,造成肠粘膜损害,因此值得通过检测小肠黏膜紧密连接相关蛋白来探讨凯里红酸汤干预对高脂血症与小肠粘膜上皮紧密连接之间的关系。食物中长链脂肪酸(long-chain fatty acid,LCFA)摄入增多是导致血脂代谢异常的一项重要因素,机体摄入的脂肪主要通过小肠以脂肪酸的形式完成吸收,其中LCFA经过多种膜转运蛋白及胞质转运蛋白共同协作进入小肠细胞[8-9],研究显示,小肠上皮细胞膜蛋白脂肪酸转位酶(fatty acid translocase,FAT/CD36)和脂肪酸转运蛋白4(fatty acid transport protein 4,FATP4)与LCFA吸收密切相关[10-11],并且在前期实验中发现凯里红酸汤可以抑制血脂和体质量的升高[1]。因此,富含乙酸等有机酸的凯里红酸汤可能对高脂血症产生影响,同时恢复被破坏的高脂血症大鼠小肠紧密连接结构。本实验通过检测肠粘膜紧密连接相关蛋白Occludin、ZO-1和调控长链脂肪酸吸收蛋白FATP4和FAT/CD36,研究凯里红酸汤与脂质代谢之间的联系。
1 材料与方法
1.1 材料与试剂
1.1.1 动物
30只无特定病原体(specificpathogenfree,SPF)级Sprague Dawley(SD)雄性大鼠:由贵州医科大学实验中心提供,8周龄,体质量(180±20)g,许可证号scxk(黔)-2018-0001,饲养于贵州医科大学动物实验中心。
1.1.2 试剂与饲料
玉梦牌凯里红酸汤:贵州明仁食品厂;TB GreenTM Premix EX TaqTM II:宝生物工程大连有限公司;FAT/CD36、FATP4、Occludin、Zo-1引物:贵阳金工科技有限公司;Trizol:美国invitrogen公司;10×聚合酶链式反应(polymerase chain reaction,PCR)buffer、RNasin:美国Promega公司;SYBR Green PCR Master Mix:日本Toyobo公司;二喹啉甲酸(butyleyanoacrylate,BCA)蛋白定量试剂盒:北京索莱宝生物科技有限公司;FAT/CD36、Occludin、ZO-1抗体:美国Affinity Biosciences;FATP4抗体:英国Abcam公司。
基础饲料(粗蛋白22%,粗脂肪4%,粗纤维5%,粗灰分8%,粗水分10%,无氮浸出物52%,钙1.24%,磷0.92%,赖氨酸1.34%,蛋氨酸+胱氨酸0.72%):贵州医科大学动物实验中心。高脂饲料配方按照1996年卫监委发布的《保健品功能学评价程序和检验方法》中的比例:78.8%基础饲料,添加1%的胆固醇、10%的蛋黄粉、10%的猪油以及0.2%的胆盐。
1.2 仪器与设备
TDL-5000bR台式高速离心机:上海安亭仪器厂;MyCyclerTMThermal Cycler实时荧光定量聚合酶链式反应仪(quantitative real-time polymerase chain reaction,qPCR):美国Bio-rad公司;TMReal-Time System(CFX96)、ChemiDocTM Imaging System、Thermal Cycler(100TM):美国Bio-Rad公司;ABI 9700型GeneAmp PCR仪:美国Thermo Scientific公司;VORTEX-5旋涡振荡器:中国QILIBEIER公司;Lx-20全自动生化分析仪:美国Beckman Coulter公司。
1.3 方法
1.3.1 高脂血症大鼠模型建立
体质量为(180±20)g的8周龄SD雄性大鼠30只,随机分为模型组20 只与阴性组10只,在适应性喂养7 d后,按照《保健品功能学评价程序和检验方法》模型组以高脂膳食喂饲SD大鼠90 d复制高脂血症大鼠模型,阴性组饲喂普通饲料,待大鼠出现总甘油三酯(triglyceride,TG)、总胆固醇(total cholesterol,TC)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)中两项指标为阳性,即模型组与阴性组相比有统计学意义(P<0.05)即判定建模成功。
1.3.2 大鼠分组与干预
高脂血症大鼠造模判定成功后,将大鼠采用随机数字法分为对照组、实验组,每组10只SD大鼠。经过前期前往黔东南凯里进行的基线调查,了解人的酸汤的摄入量,根据《实验动物学》的换算关系确定了本实验的酸汤灌胃剂量,其中实验组以4 g/(kg·d)酸汤灌胃,饲喂高脂饲料;对照组以等容蒸馏水灌胃,饲喂高脂饲料。阴性组普通饲料自然喂养,同时等容蒸馏水灌胃,持续干预11周。由于玉梦牌酸汤在出厂前经过熬煮,所以根据玉梦牌酸汤的使用说明将酸汤稀释成浓度为40%的灌胃液,按照体质量灌胃。
1.3.3 一般形态学观察
干预过程中,每日观察大鼠的一般形态学特征,包括活动度、四肢状态、精神状态和食欲、毛发情况以及死亡情况。每周称量大鼠体质量。
1.3.4 标本采集
给与大鼠高脂饲料造模90 d时,自大鼠尾尖采血,以检测血脂水平。血液样本采集方法:干预11周时,所有大鼠禁食12 h,称取体质量;腹腔注射戊巴比妥钠30 mg/kg,断尾采集血液1.5 mL,4 000 r/min离心15 min制备血清用于血脂分析。开腹取出回肠组织,-80 ℃冻存,用于脂肪酸吸收和紧密连接相关蛋白的测定。
1.3.5 大鼠TG、TC、LDL-C、HDL-C的测定
与贵州医科大学大学城医院检验室生化科合作,采用全自动生化分析仪Lx-20测定血清TC、TG、LDL-C和HDL-C。
1.3.6 WesternBlot检测小肠粘膜上皮组织β-actin、FAT/CD36、FATP4、ZO-1和Occludin蛋白相对表达水平
将回肠组织从-80 ℃冰箱取出,取50~100 mg组织加入研磨管,加入液氮后研磨,之后加入1 mL 1∶100的裂解液和苯甲基磺酰氟(phenylmethanesulfonyl fluoride,PMSF)混合液。每个样品进行10 s的超声破碎。4 ℃、12 000 r/min离心15 min。使用BCA蛋白试浓度测定试剂盒进行蛋白定量,加上样缓冲液煮沸使蛋白质变性。将产物进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodiumdodecylsulfate-polyacrylamide gel electrophoresis,SDS-PAGE)电泳,湿转法将蛋白转印至聚偏二氟乙烯膜(polyvinylidene fluoride,PVDF),一抗(1∶300)、二抗(1∶1 000)进行杂交。电化学发光(electrochemiluminescence,ECL)试剂盒来检测蛋白,操作步骤按照试剂盒说明进行。凝胶成像分析系统进行图像采集。通过ImageJ系统测得样品目标蛋白的灰度值G,蛋白表达量计算公式为:
蛋白表达量=ΔG干预组/ΔG阴性组
其中ΔG=G目标蛋白/G内参蛋白,本实验所选用的内参蛋白是甘油醛-3-磷酸脱氢酶;将阴性组结果作为1,ΔG干预组/ΔG阴性组表示干预组相对阴性组的表达量倍数。
1.3.7 PCR检测小肠粘膜上皮组织中β-actin、FAT/CD36、FATP4、ZO-1和Occludin mRNA表达水平
将回肠组织从-80 ℃冰箱取出,称取50~100 mg组织,在匀浆器中加入0.6 mL Trizol,对组织进行匀浆处理,加入Trizol0.4mL,在冰盒静置15min。4℃、12000r/min离心5min。吸取上清液,每1 mL加入0.2 mL氯仿,混匀后冰盒静置5 min,低温离心,4 ℃、12 000 r/min 5 min低温离心后管内液体分为3层:底层沉淀(粉色)、中间层、上层为透明层,吸取150 μL上层透明层的上清液液于EP管中,加入150 μL异丙醇,涡旋器混匀,-20 ℃保存30 min后,4 ℃、12 000 r/min离心15 min。弃掉上清液,保留底部沉淀。4 ℃、7 500 r/min离心10 min,弃掉上清液。30 min自然晾干,加入RNase-free溶解底部沉淀的核糖核酸(ribonucleic,RNA),无肉眼可见的沉淀,加入10~20 μL RNase-free,酶标仪测定提取的RNA的浓度和纯度。
按qPCR试剂盒操作说明书配制反应体系,在qPCR仪以3步法进行PCR,40循环后采集荧光信号,实验重复3次。PCR引物由贵阳金工有限公司合成,见表1,采用荧光定量PCR法进行相对定量分析。
表1 PCR引物序列
Table 1 Sequence of PCR primers

通过Real-time System测得样品的Ct值,mRNA相对表达量计算公式如下:
mRNA相对表达量=2-ΔΔCt
其中ΔΔCt=ΔCt干预组-ΔCt阴性组;ΔCt=Ct目的基因-Ct内参基因;将阴性组结果作为1,2-ΔΔCt表示干预组相对阴性组的表达量倍数。
1.3.8 统计学方法
数据采用SPSS for Windows 22.0软件进行录入、整理和统计分析;计量资料均使用(x¯±S)来表示,满足方差齐性和正态性分布检验,多组间计量资料的分析采用单因素方差分析,体质量的分析使用重复测量的单因素方差分析,组间比较采用最小显著性差异(least significant difference,LSD)法进行检验。检验水准α=0.05。
2 结果与分析
2.1 一般形态学观察
实验期间未出现异常表现和死亡现象,大鼠的精神状态稳定,摄食和饮水均正常。对照组大鼠行动缓慢,活动量减少,反应迟缓,出现腹部肥胖状态,毛发较阴性组的大鼠稀疏、无光泽,实验组大鼠较对照组大鼠行动敏捷,反应迅速,无腹部肥胖的状态,毛发恢复光泽,接近阴性组大鼠。
由图1可知,在干预开始的第0周时,对照组、实验组间大鼠的体质量之间差异无统计学意义(P>0.05),阴性组体质量低于对照组(P<0.05)。酸汤干预2周后,相较于对照组,实验组体质量出现降低趋势,但是差异无统计学意义(P>0.05)。酸汤干预8周后,实验组体质量低于对照组(P<0.05)。在第10周,实验组相比对照组体质量进一步降低(P<0.05)。
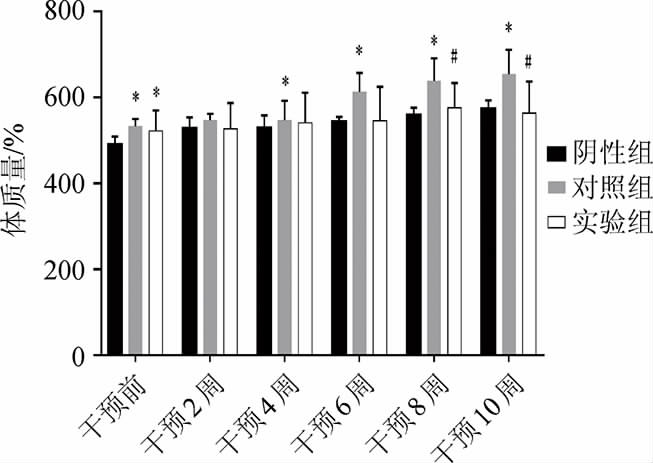
图1 凯里红酸汤对各组大鼠体质量影响
Fig.1 Effect of Kaili red sour soup on rats body mass in each group
“*”表示与阴性组相比差异显著(P<0.05);“#”表示与对照组相比差异显著(P<0.05)。下同。
2.2 凯里红酸汤对大鼠血脂水平的影响
由表2可知,相较于对照组,实验组的大鼠TG、TC、LDL-C均显著降低(P<0.05),而HDL-C差异不显著(P>0.05)。阴性组大鼠的TG、TC、LDL-C也均显著低于对照组(P<0.05)。
表2 酸汤干预后的血脂变化
Table 2 Changes in blood lipid after acid decoction intervention
mmol/L

注:“*”表示与对照组相比差异显著(P<0.05)。
2.3 小肠上皮ZO-1、Occludin、FATP4、FAT/CD36 mRNA水平
如图2所示,与阴性组相比较,对照组的FAT/CD36的表达显著升高(P<0.05),FATP4的表达有升高趋势,但是差异无统计学意义(P>0.05);ZO-1和Occludin mRNA表达显著降低,差异有统计学意义(P<0.05)。与阴性组相比较,实验组的FATP4和FAT/CD36的表达显著低于阴性组(P<0.05);紧密连接相关基因ZO-1、Occludin也显著低于阴性组(P<0.05),但是相较于高脂血症大鼠已经接近正常大鼠水平。相较于对照组,实验组的FATP4和FAT/CD36 mRNA表达显著降低(P<0.05);ZO-1表达升高,差异有统计学意义(P<0.05)。
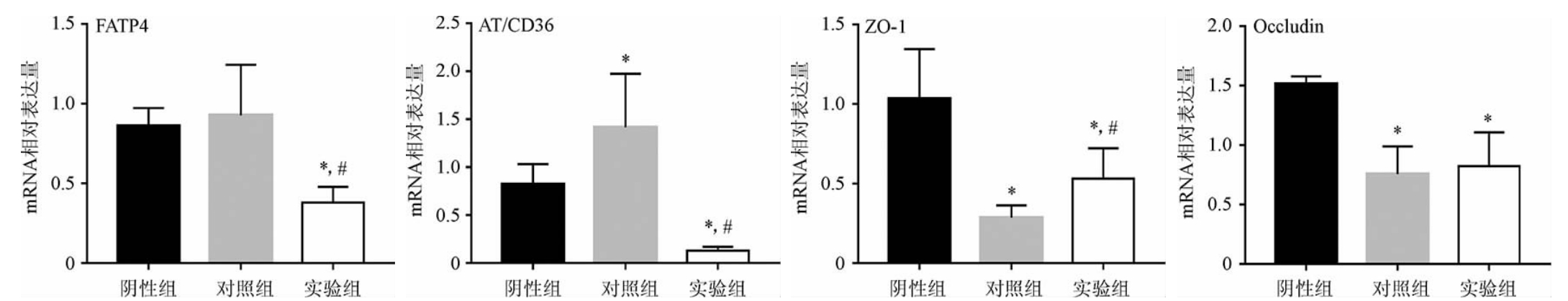
图2 凯里红酸汤对小肠粘膜上皮FAT/CD36、FATP4、Occludin和ZO-1的mRNA表达的影响
Fig.2 Effect of Kaili red sour soup on mRNA expression of FAT/CD36,FATP4,Occludin and ZO-1 in small intestinal mucosas epithelium
2.4 小肠上皮ZO-1、Occludin、FATP4、FAT/CD36蛋白表达水平
如图3所示,与阴性组相比较,对照组肠道上皮FATP4和FAT/CD36蛋白表达显著升高(P<0.05),ZO-1和Occludin的蛋白表达显著降低(P<0.05)。与对照组相比较,实验组的肠道上皮中FATP4和FAT/CD36蛋白表达显著降低(P<0.05),ZO-1和FAT/CD36蛋白表达显著升高(P<0.05)。
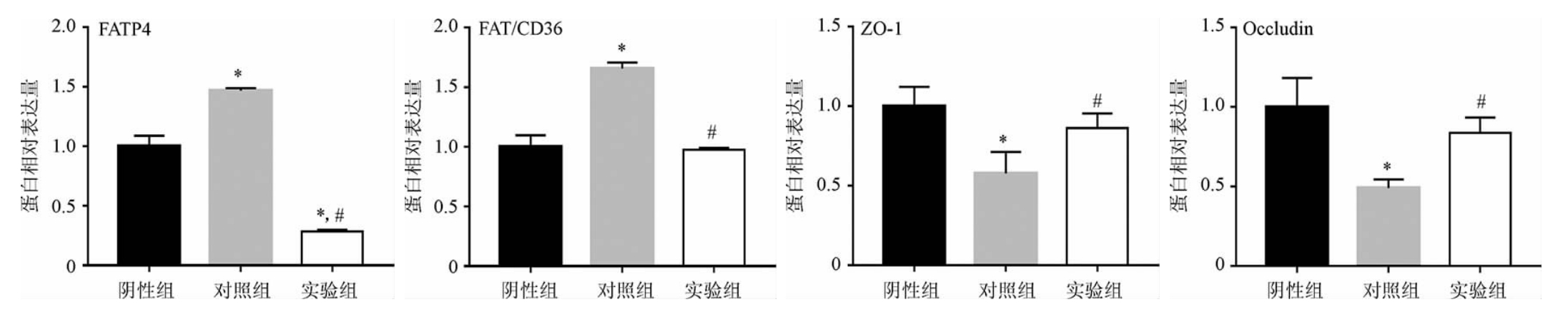
图3 凯里红酸汤对小肠粘膜上皮FAT/CD36、FATP4、Occludin和ZO-1的蛋白表达的影响
Fig.3 Effect of Kaili red sour soup on FAT/CD36,FATP4,Occludin and ZO-1 protein expression in small intestinal mucosas epithelium
2.5 讨论
高脂血症是动脉粥样硬化等心脑血管疾病和II型糖尿病的危险因素,影响人类的身体健康,进而引发脑血栓、冠心病等疾病。饮食因素导致的能量过剩对高脂血症的发生和发展有着重要的影响。经过90 d的高脂血症大鼠建模后,本研究发现喂养高脂饲料的大鼠体质量明显高于阴性组,又符合能量过剩引起高脂血症的观点,与高脂饲料会导致高脂血症的观点一致,酸汤干预后大鼠体质量增长受到抑制。
膳食中最主要的脂类是甘油三酯,进入小肠后被胆盐乳化成微粒,然后在肠内的脂肪酶的作用下转化成为脂肪酸。其中长链脂肪酸(LCFA)需要在小肠上皮粘膜细胞的相关脂肪酸转运蛋白的协助下才能进入小肠细胞[12]。既往的研究发现,FAT/CD36和FATP4对LCFA的转运起重要的作用[13]。LCFA经过FATP4和FAT/CD36的协同作用后,进入细胞膜内侧,与FABPs结合。在本实验中,大鼠经过高脂饲料喂养后,FAT/CD36和FATP4的mRNA和蛋白表达升高,说明高脂饲料喂养能够使大鼠小肠上皮的FAT/CD36代偿性的表达升高,肠道中的SCFA吸收上升,并导致血脂代谢异常,最终引起高脂血症。酸汤干预后大鼠的小肠上皮的中FAT/CD36和FATP4 mRNA和蛋白表达下降,提示了酸汤可能通过抑制小肠上皮的FAT/CD36 和FATP4来影响血脂代谢和能量代谢,抑制高脂血症的发生和发展。
小肠上皮细胞的连接方式主要是紧密连接[8]。紧密连接的结构主要是相邻的小肠上皮细胞细胞膜之间形成索条状结构,通过紧密连接相关的蛋白使索条密切并列在一起,形成了密切的细胞间隙,是小肠上皮粘膜上皮的结构功能的基础,阻止大分子物质的通过[14]。Occludin和ZO-1是重要的紧密连接相关基因,紧密连接结构的破坏伴随着小肠粘膜上皮的通透性升高和小肠粘膜上皮的炎症反应,BRUN P等[15]研究发现小肠粘膜紧密连接结构与脂质代谢异常之间的联系,肠道革兰氏阴性菌产生的内毒素会进入血液循环,与内毒素结合蛋白(LPS binding protein,LBP)结合侵袭肝脏,可以影响血脂代谢[16-19]。本实验结果显示,经过高脂饲料喂养后,Occludin和ZO-1蛋白和mRNA表达下调,这一结果提示喂养高脂饲料导致高脂血症的大鼠的紧密连接结构破坏,可能伴随着炎症反应和水肿等,与其他研究者的研究结果相符,可能会导致肠道微生态的破坏[20-21],影响能量代谢。凯里红酸汤干预后,大鼠的ZO-1 mRNA、蛋白表达Occludin的蛋白表达明显升高,说明酸汤干预能够上调ZO-1和Occludin的表达,恢复高脂血症大鼠遭到破坏的小肠上皮紧密连接结构[22-23]。酸汤干预后大鼠的ZO-1和Occludin mRNA表达量低于正常大鼠,说明11周的酸汤干预只是一定程度恢复了被破坏的肠道上皮紧密连接结构,并未恢复到破坏前的水平[24-25]。
3 结论
通过灌胃摄入的方式观察贵州凯里红酸汤对高脂血症大鼠模型的小肠上皮脂肪酸吸收蛋白和紧密连接蛋白的调控作用。摄入凯里红酸汤期间测量大鼠的体质量和血脂,摄入11周后测定大鼠小肠上皮的脂肪酸转位酶CD36(FAT/CD36)、脂肪酸转运蛋白(FATP4)、紧密连接相关蛋白Occludin和紧密连接跨膜蛋白(ZO-1)的表达。结果表明,凯里红酸汤可以降低高脂血症大鼠的体质量,恢复被破坏的肠道黏膜上皮的紧密连接结构,抑制肠道粘膜上皮的LCFA转运蛋白的表达,具有减肥的功效。
[1]鲁杨.凯里红酸汤成分及其对大鼠血脂调节作用研究[D].贵阳:贵州医科大学,2019.
[2]鲁杨,王楠兰,李贤,等.凯里红酸汤主要营养和功能成分的分析研究[J].食品研究与开发,2019,40(7):163-166.
[3]BEARDS E,TUOHY K,GIBSON G.Bacterial,SCFA and gas profiles of a range of food ingredients following in vitro fermentation by human colonic microbiota[J].Anaerobe,2010,16(4):420-425.
[4]刁慧.猪肠道微生物与SCFAs 对肠道结构和功能的影响及其机制[D].雅安:四川农业大学,2017.
[5]PLUZNICK J.A novel SCFA receptor,the microbiota,and blood pressure regulation[J].Gut Microbes,2014,5(2):202-207.
[6]袁榴翼,李小锦,尹清晟,等.中药干预肠道菌群改善肠黏膜屏障功能的研究进展[J].中草药,2018,49(8):1932-1938.
[7]KIMURA I,INOUE D,HIRANO K,et al.The SCFA receptor GPR43 and energy metabolism[J].Front Endocrin,2014,5:85.
[8]MIELE L,VALENZA V,LA TORRE G,et al.Increased intestinal permeability and tight junction alterations in nonalcoholic fatty liver disease[J].Hepatology,2009,49(6):1877-1887.
[9]颜士禄,张铁鹰,刘强.脂肪酸的吸收与脂肪酸结合蛋白[J].饲料工业,2008(17):17-21.
[10]ADESHIRLARIJANEY A,ZOU J,TRAN H Q,et al.Amelioration of metabolic syndrome by metformin associates with reduced indices of lowgrade inflammation independently of the gut microbiota[J].Am J PhysiolEndocrin Metab,2019,317(6):E1121-E1130.
[11]GLATZ J F,LUIKEN J J,BONEN A.Membrane fatty acid transporters as regulators of lipid metabolism:implications for metabolic disease[J].Physiol Rev,2010,90(1):367-417.
[12]NASSIR F,WILSON B,HAN X,et al.CD36 is important for fatty acid and cholesterol uptake by the proximal but not distal intestine[J].J Biol Chem,2007,282(27):19493-19501.
[13]HAENEN D,ZHANG J,SOUZA D S C,et al.A diet high in resistant starch modulates microbiota composition,SCFA concentrations,and gene expression in pig intestine[J].J Nutr,2013,143(3):274-283.
[14]RENAUD H J,CUI J Y,LU H,et al.Effect of diet on expression of genes involved in lipid metabolism,oxidative stress,and inflammation in mouse liver-insights into mechanisms of hepatic steatosis[J].PLoS One,2014,9(2):e88584.
[15]BRUN P,CASTAGLIUOLO I,DI LEO V,et al.Increased intestinal permeability in obese mice:new evidence in the pathogenesis of nonalcoholic steatohepatitis[J].Am J Physiol Gastr L,2007,292(2):G518-G525.
[16]BRANDT A,NIER A,JIN C J,et al.Consumption of decaffeinated coffee protects against the development of early non-alcoholic steatohepatitis:Role of intestinal barrier function[J].Redox Biol,2019,21:101092.
[17]LI W,YANG H,ZHAO Q,et al.Polyphenol-rich loquat fruit extract prevents fructose-induced nonalcoholic fatty liver disease by modulating glycometabolism,lipometabolism,oxidative stress,inflammation,intestinal barrier,and gut microbiota in mice[J].J Agr Food Chem,2019,67(27):7726-7737.
[18]SPRUSS A,BERGHEIM I.Dietary fructose and intestinal barrier:potential risk factor in the pathogenesis of nonalcoholic fatty liver disease[J].J Nutr Biochem,2009,20(9):657-662.
[19]ZHAO Z,CHEN L,ZHAO Y,et al.Lactobacillus plantarum NA136 ameliorates nonalcoholic fatty liver disease by modulating gut microbiota,improving intestinal barrier integrity,and attenuating inflammation[J].Appl Microbiol Biotechnol,2020,104(12):5273-5282.
[20]郭海,宋爽,才秀莲.支持细胞波形蛋白及紧密连接结构蛋白在染锰大鼠睾丸中的表达[J].解剖科学进展,2017,23(2):177-180.
[21]刘涛,刘霞,张驰,等.肠黏膜机械屏障与肠易激综合征的关系[J].中国中医药现代远程教育,2018,16(11):141-144.
[22]孙英健,张银花.伊维菌素对肠上皮紧密连接结构和功能的影响[C].广州:中国毒理学会第六届全国毒理学大会,2013.
[23]杨丽娟.甲基苯丙胺调节紧密连接结构蛋白的表达改变血脑屏障通透性[J].中国病理生理杂志,2008(6):1172.
[24]张园,赵楠楠,赵海君,等.紧密连接结构中相关蛋白在自然妊娠和辅助生殖技术来源胎盘组织中的表达[J].中华妇产科杂志,2014,49(2):125-129.
[25]赵伟东,周娜,梁悦,等.EphA2 受体参与维持脑微血管内皮细胞的紧密连接结构:“细胞活动生命活力”[C].北京:中国细胞生物学学会全体会员代表大会暨第十二次学术大会,2011.