白酒是中华民族的瑰宝,它凝聚着我国劳动人民的智慧,至今已有几千年的历史。由于原料、酒曲、工艺及地处环境等因素的差异,我国白酒又形成了风格特色各异的不同香型[1]。正宗大曲酱香白酒应使用贵州红缨子糯高粱,采用“四高两长”(高温制曲、高温堆积、高温发酵、高温馏酒和生产周期长、贮存时间长)独特的酿造工艺,使得众多微生物共同参与白酒发酵,使其具有“酱香突出,幽雅细腻,酒体醇厚,回味悠久,空杯留香持久”的风格特点和丰富口感,深受广大消费者的青睐。酱香型白酒在中国白酒产业中虽然产量占比不高,但利润大幅提升,呈现出快速发展的良好势态。2019年仅仁怀酱香白酒以中国白酒总产量3%的份额,实现了全国白酒业超40%的利润。
酱香型白酒酿造中微生物的生长代谢具有十分重要的作用,将原料中的淀粉、蛋白质和脂肪等营养物质进行分解、转化,生成相应的代谢产物,赋予白酒独特风味和营养价值[2]。酱香型白酒生产企业强调保持传统工艺的同时也十分重视科学技术的应用。酱香型白酒的科学研究起始于20世纪50年代末。目前,国内学者对其酿酒微生物、酿造工艺和酒体特征成分等方面进行了深入的研究,取得了不少研究成果,推动了酱香型白酒产业不断向机械化、智能化方向发展[3-4]。
随着生物技术的进步,各种微生物分析技术逐步应用于酱香型白酒发酵研究中,人们逐渐认识到酿酒微生物的丰富多样及其贡献。本文总结了近20年微生物分析技术在酱香型白酒研究中的应用情况,并对酱香型白酒微生物研究提出了展望,旨在推动酱香白酒行业的技术升级和高质量发展。
1 微生物分析技术及其应用
随着科技的发展,微生物分析技术不断地推陈出新。从最初的传统可培养技术,到不依赖于菌种培养的生物标记法,再到依赖于聚合酶链式反应(polymerase chain reaction,PCR)的分子生物学分析技术等的应用,均在酿酒微生物菌群分析方面取得了较为全面精准的分析结果。
1.1 传统可培养方法
传统可培养方法是最早应用的微生物研究手段,它通过适宜的分离筛选条件得到纯菌,经生态学观察和生理生化实验,进行微生物的种属归类[5]。Biolog全自动微生物鉴定系统的出现使得鉴定工作简单快速,确保鉴定的完整性与准确性。Biolog基于微生物对底物利用能力的差异,通过系统读取信息并与数据库对比,得出鉴定结果,因此也称为代谢指纹技术。2008年WANG C L等[6]研究酱香型大曲不同发酵时期、不同层面的微生物群落动态变化,从中分离出200多株酿酒微生物,并通过形态学及生理生化鉴定发现芽孢杆菌、曲霉菌、酿酒酵母为大曲中优势菌属。2013年董瑞丽等[7]应用Biolog技术从酱香型大曲中分离到的一株细菌进行鉴定,实现了Biolog技术在酱香型大曲菌种鉴定中的首次应用。
但是传统可培养方法也存在局限性。自然界中可培养的微生物只占总数的0.1%~10%,绝大多数微生物无法实现纯菌培养[8]。对于厌氧菌的培养,厌氧环境是关键。但厌氧环境不易形成,需要特殊设施设备。直到自动厌氧手套箱的出现,有利推动了厌氧微生物的研究。2018年王晓丹等[9]借助于厌氧手套箱从下层糟醅中分离筛选到4株厌氧细菌,并经形态学观察和核糖体脱氧核糖核酸(ribosomal deoxyribonucleic acid,rDNA)基因同源性分析鉴定为丁酸梭菌、解木聚糖梭菌、近端梭菌和煎盘梭菌。
1.2 生物标记法
生物标记法是指依据微生物细胞中特定生物化学物质的种类、数量来反映某类微生物的组成与数量的一种方法。常用的标记物有醌、脂肪酸和麦角甾醇[10]。常用的方法有醌指纹法(quinone profile,QP)、磷脂脂肪酸(phospholipid fatty acid,PLFA)图谱法等[11-12]。这些方法不依赖于分离培养,对样品直接进行微生物定性定量分析。但其微生物的分类水平较低,不能鉴定到种。对于微生物群系更为详细的分析,还需借助其他鉴定方法。1985年TUNLID首次应用PLFA技术对油菜根际微生物的群落结构进行了研究,后来逐渐引入到土壤、发酵食品以及白酒酿造等多种微生物研究领域中[13]。2017年赵金松等[14]应用PLFA技术对酱香、浓香和清香型大曲微生物群落结构进行研究,发现不同工艺大曲微生物群落结构差异明显,制曲温度的升高对大曲微生物多样性影响较大。
1.3 分子生物学技术
随着分子生物学的发展,分子生物学分析技术正在逐步取代生物标记法,广泛应用于酿酒微生物的研究中。
1.3.1 rDNA基因同源性分析
rDNA基因具有良好的进化保守性、适宜分析的长度以及与进化距离相匹配的良好变异性,所以成为分子鉴定的标准标识序列。通常用于微生物鉴定、亲缘关系和系统进化树构建的序列有细菌16S rDNA基因、真菌26S rDNA基因D1/D2区或转录间隔区(internal transcribed spacer,ITS)序列。张荣等[15]应用rDNA基因同源性分析,将高温大曲中分离筛选到的3株产酱香的G+杆菌鉴定为地衣芽孢杆菌。
1.3.2 克隆文库的构建
克隆文库技术最早在1991年被GIOVANNONI等用来分析浮游细菌多样性[16],目前已广泛应用于白酒微生态研究中。常用细菌16S rDNA基因、真菌18S rDNA基因以及ITS基因克隆文库等进行分析。克隆文库法因避开了纯化培养,能够鉴定不可培养微生物,而且因其针对微生物的16SrDNA或18S rDNA全长,能更为全面准确地反映样品中的微生物多样性。2014年叶光斌等[17]通过16S rRNA基因文库技术研究郎酒超高温大曲中细菌群落结构,发现细菌群落组成较为单一,主要以芽孢杆菌科和高温放线菌科为主。
1.3.3 限制性内切酶片段长度多态性技术
限制性内切酶片段长度多态性技术(restriction fragment length polymorphism,RFLP)是利用不同种属的微生物基因组DNA被限制性内切酶酶切可产生分子质量不同的DNA片段,通过酶切图谱与数据库的比对,分析微生物种群的差异以及种属鉴定。2012年颜林春等[18]从福矛高温大曲中分离出89株芽孢杆菌,对其16S rDNA进行PCR-RFLP分析,揭示了福矛高温大曲中可培养芽孢杆菌的丰富多样。
1.3.4 核糖体DNA扩增片段限制性内切酶分析
核糖体DNA扩增片段限制性内切酶分析(amplified ribosomal DNA restriction analysis,ARDRA)是20世纪末在美国发展起来的一项现代生物鉴定技术,也是一种PCR技术和RFLP技术相结合的方法。该技术是选择性扩增微生物rDNA保守性片段,将扩增的rDNA片段进行限制性酶切,通过酶切图谱来对菌种多样性进行分析[19]。LI H等[20]应用ARDRA技术和16S rDNA基因克隆文库的建立,从酱香型大曲中鉴定出了枯草芽孢杆菌、地衣芽孢杆菌和解淀粉芽孢杆菌等优势细菌。
1.3.5 变性梯度凝胶电泳技术
变性梯度凝胶电泳技术(denaturing gradient gel e1ectrophoresis,DGGE)的原理是在聚丙烯酰胺凝胶基础上,引入变性剂梯度,从而使长度相同但序列不同的DNA片段区分开。对目的条带进行测序分析,即可得到相关微生物信息。随后又发展出其衍生技术,即温度梯度凝胶电泳(temperature gradient gel electrophoresis,TGGE)。1993年MUYZER G首次将DGGE技术引入到微生物多样性分析,后来逐渐应用于微生物相关的各个领域[21]。该技术的应用中发现一些问题:(1)对大于500 bp的DNA片段分离度较差,只能选用rRNA基因中某些可变区进行分析,因此包含的信息量较少;(2)无法检出样品中相对含量低于1%的微生物,从而忽略一些含量低的关键微生物;(3)同一个菌株也可能有多个拷贝的核糖体RNA基因,由于突变的存在势必会使这些拷贝体之间存在差异,从而高估微生物多样性。虽然存在以上缺陷,但该技术因其无需培养微生物,快速且低成本等突出优点,目前在酱香型白酒酿酒微生物分析研究中仍然与高通量测序技术并行成为当前最常用的分析方法。谭映月等[22]应用DGGE技术研究制曲过程中细菌菌群结构及其演变规律,结果发现随着大曲的发酵,细菌多样性下降,发酵后期芽孢杆菌属和乳酸杆菌属成为绝对优势菌,对酱香风味的形成至关重要。
1.3.6 实时荧光定量PCR
实时荧光定量PCR(real-timequantitativepolymerasechain reaction,RT-qPCR)是一种基于特异性引物在DNA扩增反应中以荧光化学物质标记并测量每个PCR循环后产物总量的方法。由于在PCR扩增的指数时期,模板的Ct值和起始拷贝数存在线性关系,以此作为定量的依据,通过标准曲线对特定菌起始拷贝数进行定量分析。它具有高特异性、高灵敏度的优点,广泛应用于发酵食品微生物定量分析[23]。由于该技术对引物特异性要求高,目前在酿造微生物研究中仍处于探索阶段。邵明凯等[24]应用DGGE技术和实时荧光定量PCR技术对产量、酒质较高的第五轮次和较低的第七轮次酿造过程中酵母群落结构进行解析,同时分析糟醅中的代谢组分,结果表明酵母菌群多样性较丰富,酵母菌菌群变化对白酒产量及品质影响明显。
1.3.7 高通量测序技术
在Sanger发明第一代测序技术以来测序技术不断革新,开发出二代测序技术。二代测序技术具有通量高、准确率高、可获得定性及相对定量信息以及成本低廉等优点,而且能检测出稀有种属,能全面客观地揭示微生物群落信息,具有先进性和优越性[25]。但由于第二代测序技术测序读长所限,只能以rRNA基因部分可变区为扩增和测序靶点,导致对微生物的鉴定只能停留在“属”或“科”的水平,不能精准描述微生物群落结构。随着测序技术的不断发展,研发人员开发出了第三代测序技术。它在序列长度和测序速度上得到了大幅度提升。
自2006年,高通量测序技术(high-throughput sequencing,HTS)在微生物研究中的应用呈现明显的上升趋势,于2014年首次应用于白酒酿造微生物的研究。目前白酒酿酒微生物研究中,应用最多是第二代测序技术,在对其他发酵食品、肠道微生物的研究中已引入了三代测序技术。王莉等[26]应用高通量测序技术对不同时间的窖泥及环境土壤微生物区系进行分析,发现在土壤驯化成窖泥的过程中,微生物多样性逐渐降低,乳杆菌科、梭菌科和瘤胃菌科厌氧微生物逐渐成为优势种群。
1.4 宏基因组学技术
随着测序技术的进步和生物信息学的发展,宏基因组学技术也在微生物群落代谢与功能研究中得到了应用。高通量测序数据的处理算法和生物信息学数据库成为宏基因组学发展的重要基础,也是目前宏基因组学发展的一个技术瓶颈[27]。利用高通量测序技术获得的数据进行物种分类学注释的同时也可以进行功能注释和代谢通路分析[16]。
各种微生物分析技术均有其优缺点,在不断地发展和完善的同时,相互弥补相互推进。酱香型白酒酿造研究中,以传统微生物培养技术为基础,并引入多种分子生物学技术,使酿酒微生物的研究从表型特征的鉴定深入到遗传特性的鉴定,为微生物研究提供可信度高、灵敏度高、重复性好且客观、快速的分析方法。生物技术推陈出新,将会更加有力地推动白酒酿造微生态的解析。
2 微生物分析技术在酱香型白酒发酵研究中的应用
2.1 应用阶段
酱香型白酒酿酒微生物的来源广泛,来源于大曲、糟醅、窖泥、原料、生产用水、设备、环境及空气等。酿酒过程中微生物代谢主要发生在高温制曲、堆积发酵和窖池发酵三个阶段。因此,酱香型白酒酿酒微生物研究主要围绕该三个阶段展开。
2.1.1 高温制曲阶段
酱香型白酒生产中高温大曲作为糖化剂、发酵剂和生香剂,对酒质具有至关重要的作用。酱香型大曲选用小麦为原料,以适量优质母曲作为接种源,发酵温度高达65 ℃,经过3~6个月的贮存后方可投入生产。在开放式环境下不同来源的微生物不断更替富集,经长期自然选择,在大曲中形成以细菌、酵母菌和霉菌为主的微生物体系[28]。经过高温制曲能够存活下的优势菌主要为耐热的芽孢杆菌属细菌,因此酱香型大曲也可以说是细菌曲。
大曲中细菌和霉菌都可以分泌多种水解酶;酵母菌虽然在大曲中的数量不多,但仍是一类产酒生香的关键功能菌;放线菌在发酵过程中通过代谢抗生素调节多菌种混合发酵途径和代谢。在酱香型白酒酿造过程中众多微生物相互作用,最终影响着酱香型白酒的发酵及风味物质的形成。
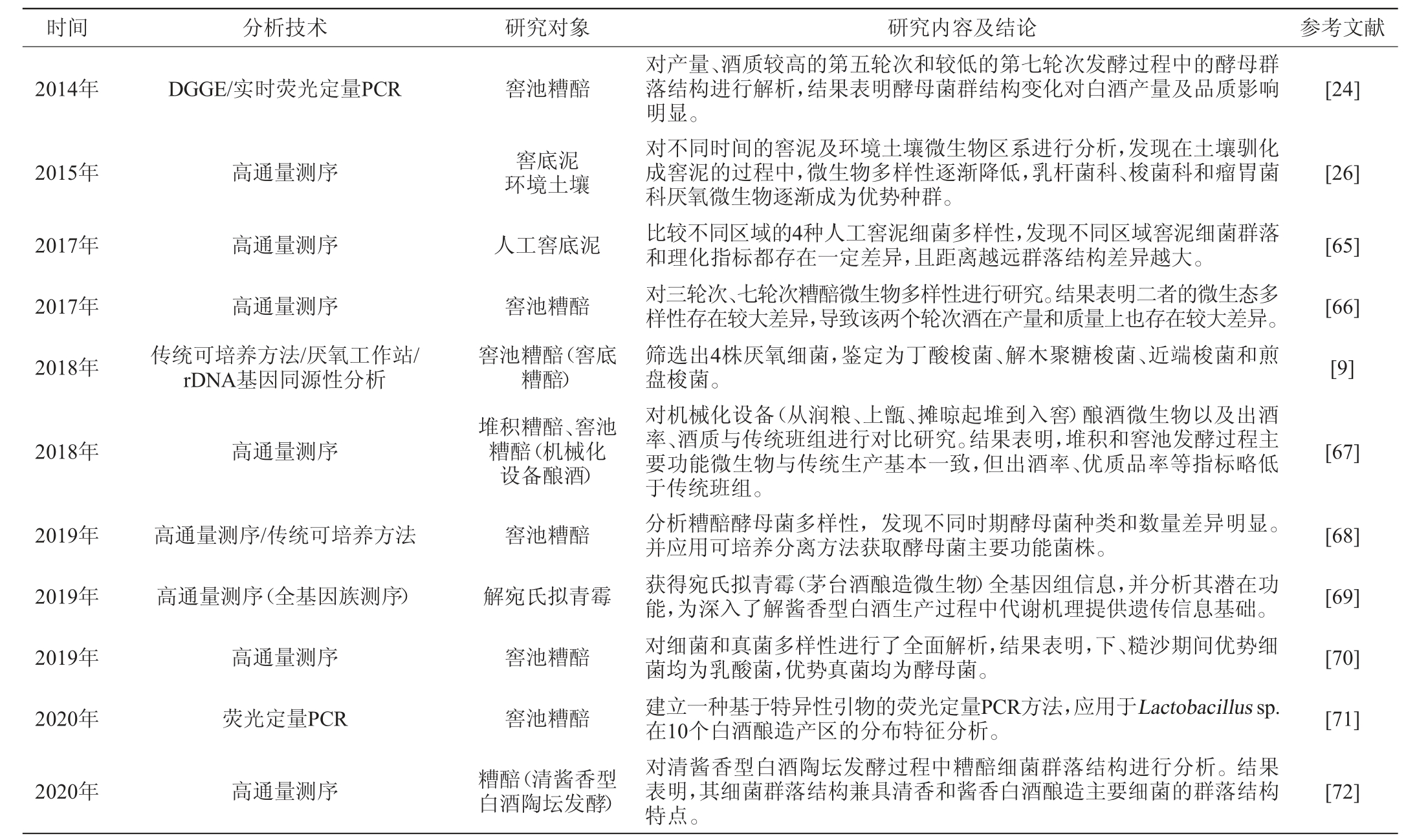
随着微生物分析手段不断更新,拓展了大曲微生物的研究范围,对大曲菌群进行更为全面、实时、精确的研究。目前,在酱香型白酒制曲阶段,对于酿酒微生物的研究主要集中在大曲发酵的不同阶段、不同层面微生物群落结构及其变化以及不同区域甚至不同工艺大曲之间微生物群落差异分析(详见表1)。
表1 酱香型大曲微生物多样性研究近况
Table 1 Recent research on the microbial diversity of sauce-flavor Daqu

续表

不同区域、不同阶段、不同层面微生物群落结构及变化揭示着酱香型大曲明显的时空特征。大曲微生物群落结构与环境因子的关系、微生物相互作用以及代谢产物的深入研究将有助于揭示白酒微生物酿造机理,有助于确定关键微生物及特征成分,有利于指导生产更多的优质酱香型白酒。
2.1.2 堆积发酵阶段
高温制曲过程中酵母菌被高温杀死得所剩无几。堆积过程中网罗环境及空气中的微生物,尤其富集酵母菌,因此该阶段称为“二次制曲”。高温堆积淘汰了一部分杂菌,驯化了耐高温菌,有利于酿酒微生物的繁殖代谢,使原料中淀粉、蛋白质等大分子物质产生初步的分解,生成酱香物质或其前体物质,为入窖发酵创造条件[44]。糟醅堆积在酱香型白酒质量和产量的重要性也得到了证实。
该阶段主要围绕不同酿酒轮次、不同堆积时间及不同位置的堆积糟醅展开酿酒微生物的分析研究,揭示着环境因素对微生物菌群的影响以及不同的菌群结构对于不同轮次酒酒体差异的影响(详见表2)。
表2 堆积糟醅微生物多样性研究近况
Table 2 Recent research on the microbial diversity of stacking Zaopei

不同堆积时间、不同空间位置形成不同的菌群结构,从而造就酒体差异。堆积环境因素、微生物相互作用对微生物菌群的相关性研究以及不同菌群对酒体相关性研究,有助于揭示微生物发酵在酒体风味形成的重要性,从而指导优化生产工艺,提高原料利用率和优质酒产率。
2.1.3 窖池发酵阶段
窖池发酵阶段是产酒的过程,也是大量风味物质生成的重要环节。酱香型白酒生产中,窖内发酵由于发酵工艺及所处位置的不同,形成了上、中、底层等三个层次。其糟醅微生物分布及生长代谢有明显差异,这些差异是造就不同酒体(即上层窖面酒、中层醇甜酒、底部窖底酒)风格的重要原因[55]。随着发酵的进行,窖池内部会形成高乙醇含量、低氧、低pH值的特点,微生物数量下降,形成一系列对白酒产香产气影响较大的厌氧微生物体系[56]。研究者们借用现代科技技术,在窖池发酵不同时期、不同位置的微生物群落分析、功能菌的筛选以及不同区域微生物差异分析等方面展开了大量研究(详见表3)。由于窖底酒在酱香型白酒勾调中的重要地位,窖泥厌氧微生物的研究也开始受到重视。
表3 窖池微生物多样性研究近况
Table 3 Recent research on the microbial diversity in pits

续表
2.2 微生物分析技术在酱香型白酒研究中作用
酱香型白酒独特的工艺造就独特的微生物群落结构及其生物代谢过程,这是形成酱香风味的重要物质保障。研究酱香型白酒酿造过程中微生物及其代谢过程,对于揭示其风味形成、品质提升以及工艺优化都具有重要意义。目前,研究人员根据各种微生物分析技术的特点,使其以较为适宜的方式致力于酱香型白酒微生物研究(见图1)。
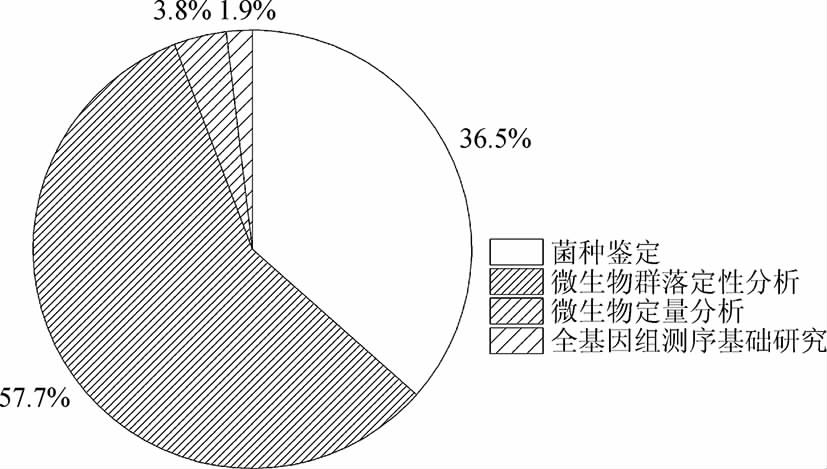
图1 酱香型白酒酿酒微生物研究概况
Fig.1 Research situation on brewing microorganisms of sauce-flavor Baijiu
2.2.1 菌种鉴定
目前微生物分析技术用于酱香型白酒酿酒微生物的分离及鉴定研究较多,通过可培养方法或厌氧工作站获得纯菌,并通过形态学观察和生理生化实验、Biolog微生物自动鉴定系统或者rDNA基因同源性分析进行菌株鉴定。获得纯种微生物是微生物研究的基础,对于菌株发酵特性研究、耐受性研究、酶学研究、代谢产物研究、相互作用研究、菌株强化应用以及微生物全基因组测序都具有重要的意义。
2.2.2 微生物群落定性分析
目前微生物分析技术用于酱香型白酒酿酒微生物群落多样性分析和差异分析占绝大多数。微生物多样性和差异分析最常用的分析方法有PCR-DGGE技术、16S rRNA基因文库以及高通量测序。对于可培养微生物,可通过稀释涂布培养法进行多样性分析。李登勇等[39]应用高通量测序技术,对不同产地、不同酒厂、生产场地及陈曲时间酱香型大曲群落组成进行研究,发现酱香型大曲的微生物群落具有显著的时空性特征。很多学者在应用基因文库构建技术或rDNA基因同源性分析方法研究酿酒微生物群落多样性时常联合应用ARDRA、RFLP或随机扩增多态性DNA(random amplified polymorphic DNA,RAPD)等技术,先对所涉及微生物进行分型,再对代表性样品进行测序,即减轻工作量,也避免了重复测序。边名鸿等[60]构建古菌16S rDNA文库研究酱香型窖泥中古菌群落结构时联合应用了ARDRA技术筛分出不同的古菌类型。除此之外,PLFA技术也应用于酿酒微生物群落分析。赵金松等[14]采用PLFA技术对清香、浓香和酱香型大曲微生物多样性进行对比分析,解析不同工艺大曲微生物群落结构存在明显的差异,并随着制曲温度的升高,微生物多样性具有下降趋势。
2.2.3 微生物定量分析
在酿酒微生物研究过程中,除了定性分析,有时定量分析也是有必要的。对于复杂样本中的可培养微生物,可以通过稀释涂布法进行相对定量分析。在不进行纯培养的情况下,可通过克隆文库构建的方法观察微生物的相对数量。生物标记法也可用于复杂样本中某类微生物的定量分析。目前,高通量测序在微生物相应分类水平上根据微生物丰度进行相对定量分析。但相对定量难以准确反映微生物的生长变化趋势及其代谢活力。荧光定量PCR技术是目前微生物分析技术中最为准确的定量分析方法。该方法不仅可以揭示酿酒环境中的微生物分布特点,也有助于揭示某种微生物的代谢功能,弥补相对定量数据的不足。杜如冰等[71]应用荧光定量PCR技术实现了白酒酿造系统中乳杆菌属(Lactobacillus sp.)的鉴定和定量,为进一步结合宏组学数据揭示在整个酿酒系统中该菌的功能和价值研究提供了有效方法和参考。
2.2.4 全基因组测序基础研究
获得关键微生物全基因组信息,有助于了解该菌在酿酒过程中的代谢机理,对酱香型白酒风味物质和健康因子调控研究具有重要的意义。王和玉等[69]对茅台酒酿造优势菌—宛氏拟青霉进行全基因组测序,发现参与代谢及风味物质合成的基因及其代谢通路,为解析其酿造功能提供了重要的生物信息学基础。
3 展望
现代生物技术使得酱香型白酒的生产和科研水平都取得了较大的进步。但由于酱香型白酒酿造工艺较为复杂,至今还有很多发酵机理方面的问题还未得到探明。统览近20年相关文献,发现对酿酒微生物的研究主要集中在酿酒微生物多样性构成、功能菌株的筛选及应用,而对发酵过程中功能微生物间的相互作用、香气成分的微生物溯源研究较少。欲弄清白酒发酵的本质,还需要加大微生物分析技术在以下几个方面的应用研究力度。①微生物代谢特征与功能研究;②环境因素对微生物生长代谢的影响;③白酒关键特征物质和有害代谢产物的微生物溯源;④关键微生物及特征物质的确定;⑤风味物质比例对白酒质量的影响;⑥主要功能微生物的相互作用研究;⑦菌剂制备和应用;⑧现有数据库的利用及完善。
随着生物技术的发展,对酿酒微生物的研究已从细胞水平上升至分子生物学水平,已积累大量宏基因组学、转录组学、蛋白质组学及代谢组学相关数据,有待于充分利用和完善。相信随着微生物分析手段的更新发展和各类组学在微生物群落代谢及功能研究中的更多更广泛的应用,酱香型白酒酿酒微生物群落、物质代谢及其与酒质的关系更加清晰化,在发酵机理研究中取得突破性的进展。为此,酱香型白酒企业在秉承传统工艺的同时还需要加大科研力度,借助于先进的理论和技术,推动白酒微生物及代谢研究更上一个层次,全面解析酱香型白酒酿造机理,从而进行科学合理的工艺改造及优化,推动酱香白酒行业的技术升级和高质量发展。
[1]赵爽,杨春霞,窦屾,等.白酒生产中酿酒微生物研究进展[J].中国酿造,2012,31(4):5-10.
[2]任聪,杜海,徐岩.中国传统发酵食品微生物组研究进展[J].微生物学报,2017,57(6):885-898.
[3]刘晓光,谢和,屈直,等.酱香型白酒风味物质的形成与微生物关系的研究现状与进展[J].贵州农业科学,2007,35(2):131-134.
[4]袁启均.生物学视角下酱香型白酒的研究进展[J].江西化工,2017(4):57-58.
[5]范光先,王和玉,崔同弼,等.茅台酒生产过程中的微生物研究进展[J].酿酒科技,2006(10):75-77.
[6]WANG C L,SHI D J,GONG G L.Microorganisms in Daqu:a starter culture of Chinese Maotai-flavor liquor[J].World J Microbiol Biotechnol,2008,24:2183-2190.
[7]董瑞丽,乔晓艳,李杨,等.酱香型大曲中一株细菌的分离及其Biolog鉴定[J].酿酒,2013,40(1):45-47.
[8]潘虎,卢向阳,董俊德,等.未培养微生物研究策略概述[J].生物学杂志,2012,29(1):79-83.
[9]王晓丹,白小燕,曾超,等.酱香型白酒酿造过程中厌氧细菌的分离鉴定[J].食品与发酵工业,2018,44(2):55-61.
[10]王毅,罗惠波,王彩虹.小曲酒酿造微生物研究进展[J].酿酒科技,2014(4):78-82.
[11]HU H Y,LIM B R,GOTO N,et al.Analytical precision and repeatability of respiratory quinones for quantitative study of microbial community structure in environmental samples[J].J Microbiol Meth,2001,47:17-20.
[12]JOERGENSEN R G,WICHERN F.Quantitative assessment of the fungal contribution to microbial tissue in soil[J].Soil Biol Biochem,2008,40(12):2977-2991.
[13]ZHENG J,LIANG R,ZHANG L Q,et al.Characterization of microbial communities in strong aromatic liquor fermentation pit muds of different ages assessed by combined DGGE and PLFA analyses[J].Food Res Int,2013,54(1):660-666.
[14]赵金松,郑佳,沈才洪,等.基于磷脂脂肪酸分析技术的大曲微生物群落结构多样性研究[J].食品工业科技,2017,38(1):160-164.
[15]张荣,徐岩,范文来,等.酱香大曲中地衣芽孢杆菌及其特征风味代谢产物的分析研究[J].工业微生物,2010,40(3):7-12.
[16]郭壮,赵慧君,雷敏,等.白酒窖泥微生物多样性研究方法及进展[J].食品研究与开发,2018,39(22):200-207.
[17]叶光斌,王彩虹,乔晓艳,等.超高温大曲细菌微生物群落结构的研究[J].酿酒科技,2014(4):5-8.
[18]颜林春,张守财,马校卫,等.福矛高温大曲中芽孢杆菌16S rDNARFLP 及系统发育分析[J].生物技术,2012,22(2):53-58.
[19]陈晓蕾,张忠泽.微生物的ARDRA 检测[J].微生物学杂志,1999,19(4):40-43.
[20]LI H,LIAN B,DING Y H,et al.Bacterial diversity in the central black component of Maotai Daqu and its flavor analysis[J].Annal Microbiol,2014,64(4):1659-1669.
[21]司波,徐瑾,廖永红.PCR-DGGE 技术概述及其在白酒领域的应用[J].中国酿造,2013,32(6):16-20.
[22]谭映月,胡萍,谢和,等.应用PCR-DGGE 技术分析酱香型白酒酒曲细菌多样性[J].酿酒科技,2012(10):107-111.
[23]LIU C L,WANG H Y,WU Z Y,et al.Development of a real-time PCR for quantification of the family Syntrophomonadaceae in pit mud from Chinese Luzhou-flavour liquor distilleries[J].J I Brewing,2015,121(1):155-162.
[24]邵明凯,王海燕,徐岩,等.酱香型白酒发酵中酵母群落结构及其对风味组分的影响[J].微生物学通报,2014,41(12):2466-2473.
[25]赵亮,王莉,汪地强,等.白酒微生物群落研究技术现状与二代测序数据分析方略[J].酿酒科技,2016(7):88-96.
[26]王莉,王亚玉,王和玉,等.酱香型白酒窖底泥微生物组成分析[J].酿酒科技,2015(1):12-15.
[27]王慧丽,郭安源.环境微生物宏基因组学数据库利用[J].生物技术通报,2015,31(11):78-88.
[28]罗小叶,王晓丹,邱树毅,等.酱香酒生产过程中的微生物研究[J].酿酒科技,2018(10):108-113.
[29]栗伟.酱香型大曲中细菌的分离与分析[J].酿酒,2012,39(3):37-40.
[30]刘效毅,郭坤亮,辛玉华.高温大曲中微生物的分离与鉴定[J].酿酒科技,2012(6):52-55.
[31]班世栋,王晓丹,陈孟强,等.酱香型大曲中具产酶功能霉菌的分离筛选[J].酿酒,2014,41(4):31-36.
[32]程才璎,刘晓风,袁月祥,等.酱香型白酒酒曲和连续七轮次堆积酒醅的细菌群落结构[J].应用与环境生物学报,2014,20(5):825-831.
[33]邓皖玉,王会,赵荣寿,等.高温大曲中产酱味霉菌的分离及研究[J].酿酒科技,2015(3):9-11.
[34]孟天毅,李长文,山其木格,等.酱香强化大曲发酵过程中微生物的变化[J].酿酒科技,2015(5):65-68.
[35]王婧,王晓丹,罗晓叶,等.酱香大曲中高产蛋白酶功能细菌的筛选及鉴定[J].中国酿造,2015,34(10):43-46.
[36]罗小叶,邱树毅,陆安谋,等.酱香大曲产香酵母的分离及鉴定[J].食品与发酵工业,2016,42(12):26-31.
[37]鲁珍,有小娟,李恩中,等.高温大曲中两株产酱香菌的分离鉴定[J].河南科学,2016,34(5):683-686.
[38]梁晨,杜海,徐岩.大曲贮存过程中原核微生物群落结构及风味成分演替规律[J].微生物学通报,2017,44(2):384-393.
[39]李登勇,黄钧,丁晓菲,等.酱香大曲间微生物群落结构时空特征的表征[J].食品工业科技,2018,39(23):139-145.
[40]戴奕杰,李宗军,田志强.酱香型白酒大曲和糟醅的真菌多样性分析[J].现代食品科技,2018,34(7):97-104.
[41]戴奕杰,李宗军,田志强.酱香型白酒大曲和糟醅的细菌多样性分析[J].食品科学,2019,40(4):152-159.
[42]任爱容,黄永光,涂华彬.茅台镇酱香型白酒酿造大曲及环境中可培养细菌多样性及功能分析[J].食品科学,2020,41(14):195-202.
[43]孙利林,李立郎,胡萍,等.酱香型白酒第四轮次酒酿造过程中真菌多样性分析[J].中国酿造,2019,38(11):24-30.
[44]戴奕杰,田志强,黄家岭,等.酱香型白酒生物化学及微生物学研究进展[J].酿酒科技,2016(3):100-105.
[45]唐玉明,任道群,姚万春,等.酱香型酒糟醅堆积过程温度和微生物区系变化及其规律性[J].酿酒科技,2007(5):54-58.
[46]WU Q,CHEN L Q,XU Y.Yeast community associated with the solid state fermentation of traditional Chinese Maotai-flavor liquor[J].Int J Food Microbiol,2013,166(2):323-330.
[47]徐超英,曹文涛,赖世强,等.酱香型白酒糟醅中产酒精酵母的筛选及鉴定[J].酿酒科技,2014(2):4-6.
[48]山其木格,梁慧珍,张长霞,等.堆积糟醅过程中微生物种群的变化规律[J].食品与生物技术学报,2016,35(3):330-335.
[49]程足杰,熊双丽,杨跃寰,等.不同堆积时间酱香型白酒酒醅细菌群落比较研究[J].食品与发酵科技,2016,52(5):84-87.
[50]韩兴林,潘学森,尚柯,等.酱香高温堆积酒醅中原核微生物构成的分析[J].酿酒,2017,44(1):22-27.
[51]李欣,王彦华,林静怡,等.高通量测序技术分析酱香型白酒酒醅的微生物多样性[J].福建师范大学学报(自然科学版),2017,33(1):51-59.
[52]黄蕴利,黄永光,胡建峰,等.酱香型白酒第二轮次酒发酵过程微生物多样性研究[J].中国酿造,2017,36(9):30-35.
[53]胡小霞,黄永光,涂华彬,等.酱香型白酒1 轮次酿造细菌的菌群结构[J].食品科学,2020,41(14):175-182.
[54]王欢,席德州,黄永光,等.酱香型白酒机械化酿造不同轮次堆积发酵细菌菌群结构多样性分析[J].食品科学,2020,41(2):188-195.
[55]胡峰,钟方达,胡建锋,等.酱香型白酒窖内不同层次酒醅微生物与酒体风格的研究[J].酿酒科技,2014(9):48-52.
[56]曾超,邱树毅,胡宝东,等.白酒酿造体系厌氧微生物研究进展[J].中国酿造,2015,34(7):24-27.
[57]沈海月,范文来,徐岩.白酒生产中高效降解糠醛微生物的筛选与鉴定[J].食品工业科技,2010,31(3):207-209.
[58]WU Q,XU Y,CHEN L.Diversity of yeast species during fermentative process contributing to Chinese Maotai-flavour liquor making[J].Lett Appl Microbiol,2012,55(4):301-307.
[59]孙剑秋,刘雯雯,臧威,等.基于26S rDNA D1/D2 序列分析酱香型白酒酒醅中酵母菌的群落结构[J].微生物学报,2012,52(10):1290-1296.
[60]边名鸿,叶光斌,杨晓东,等.酱香型窖泥古菌群落结构的研究[J].酿酒科技,2012(8):51-53.
[61]吴莉莉,王海燕,徐岩,等.酱香型与清香型白酒发酵过程中乳酸菌菌群的差异性分析[J].微生物学通报,2013,40(12):2182-2188.
[62]黄治国,邓杰,卫春会,等.酱香型白酒酒醅细菌的分离鉴定[J].酿酒科技,2014(6):27-29.
[63]黄治国,赵斌,邓杰,等.不同地域酱香型白酒酒醅细菌群落比较研究[J].酿酒科技,2014(3):28-31.
[64]王晓丹,庞博,陆安谋,等.酱香型白酒酿造过程中窖池内酵母变化趋势研究[J].酿酒科技,2014(10):9-13.
[65]蔡雪梅,蒋英丽,吴联海,等.不同区域酱香型白酒人工窖底泥细菌多样性及其影响因子[J].食品科学,2017,38(10):87-91.
[66]郭敏,黄永光,邱树毅,等.高通量测序在酱香白酒微生态多样性研究中的应用[J].中国酿造,2017,36(5):146-151.
[67]张健,李波,程平言,等.酱香型白酒制酒机械化生产试验的研究[J].中国酿造,2018,37(12):148-153.
[68]郝飞,吕锡斌,吴耀领,等.酱香型白酒酿造酒醅中酵母菌多样性研究[J].菌物学报,2019,38(5):620-630.
[69]王和玉,刘延峰,张巧玲,等.1 株来源于茅台酒酿造过程宛氏拟青霉MTDF-01 的全基因组测序及分析[J].食品科学,2019,40(24):185-192.
[70]吕锡斌,吴耀领,郝飞,等.高通量测序技术分析酱香型白酒下造沙轮次的微生物多样性[J].酿酒科技,2019(3):52-58,64.
[71]杜如冰,吴群,徐岩.基于三步荧光定量PCR 技术揭示不同产区白酒酿造系统中Lactobacillus sp.的分布特征[J].微生物学通报,2020,47(1):1-12.
[72]胡小霞,黄永光,蒋想,等.清酱香型白酒陶坛发酵细菌群落结构多样性分析[J].食品科学,2020,41(8):130-138.