蛹虫草[Cordyceps militaris(L.)Link]又名北冬虫夏草或北虫草,是子囊菌门(Ascomycota)肉座菌目(Hypocreales)麦角菌科(Clavicipitaceae)虫草属(Cordyceps)的模式菌种[1]。研究表明,蛹虫草富含虫草素、虫草多糖、虫草酸、超氧化物歧化酶(superoxide dismutase,SOD)、蛋白质、矿物质等活性物质[2-4]。其中,虫草素、虫草酸及虫草多糖是蛹虫草子实体的主要活性成分,虫草素(cordycepin)即3'-脱氧腺苷,它是CUNNINGHAM等于1950年首次从蛹虫草寄生的昆虫中分离出的抗菌物质[5-6],具有抗肿瘤、抗菌、抗病毒和免疫调节等功效;虫草酸即甘露醇,对人体内羟基自由基具有良好的清除作用,此外,还可降低颅内压和眼内压[7-9];虫草多糖具有调节免疫、抗氧化等生物活性作用[10-12]。由于蛹虫草野生资源稀缺,因此,蛹虫草的人工培养是当前研究的热点。
大量研究表明,培养基对子实体的产量有很大的影响,适宜的培养基有利于虫草素等核苷类物质、虫草酸、虫草多糖等主要活性物质的合成,从而增加出草率,降低生产成本[13-16]。目前针对固体培养基选择的研究结果不尽一致,其原因可能是所选蛹虫草菌种、培养条件不同等造成的。张显科等[17]研究发现大米是栽培蛹虫草的最佳培养基。冯景刚等[18]研究发现以小麦培养基培养的蛹虫草子实体干重大,出草质量好,优于大米、玉米、小米等。刘桂君等[19]采用燕麦、小米、大麦、大米4种培养基质固体培养蛹虫草,研究出不同的培养基质对蛹虫草中虫草酸及核苷类物质的合成具有显著差异。目前对蛹虫草子实体人工培养的固体基质单一,且目标产物多局限于提高子实体中的虫草素,而对于其他活性物质虫草酸、虫草多糖的研究鲜有报道。为提高蛹虫草子实体中多种活性物质,从而为目标产物选择实验培养基质,本研究采用不同固体培养基对蛹虫草进行培养,观察蛹虫草子实体的生长状况、检测主要活性物质并测定抗氧化活性,以期为后续蛹虫草发酵生产获取不同目标产物提供参考。
1 材料与方法
1.1 材料与试剂
1.1.1 材料及菌种
大米、小米、麦麸、小麦、薏仁米(培养基质)(均为食品级):市售。
蛹虫草菌(Cordyceps militaris)CM01:来源于本实验室。
1.1.2 试剂
蛋白胨(生化试剂):北京鸿润宝顺科技有限公司;乙腈(分析纯):淄博研晟新材料有限公司;虫草素标准品(纯度≥98.0%):上海诗丹德标准技术服务有限公司;1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)标准品(纯度≥98.77%)、2,2'-联氮-双-3-乙基苯并噻唑啉-6-磺酸(2,2'-azino-bis-3-ethylbenzothiazoline-6-sulfonic acid,ABTS)标准品:美国MedChemExpress公司。
1.1.3 培养基
马铃薯葡萄糖琼脂(potato dextrose agar,PDA)培养基:青岛日水生物技术有限公司。
种子液培养基:蛋白胨2 g,葡萄糖4 g,MgSO4 0.2 g,KH2PO4 0.1 g,200 mL蒸馏水。121 ℃灭菌30 min。
营养液:种子液培养基与蒸馏水按照1∶1配制。
固体培养基:①小米20 g;②大米20 g;③薏仁米20 g;④小麦20 g;⑤小米15 g+麦麸5 g;⑥小麦15 g+麦麸5 g;⑦大米15 g+麦麸5 g;⑧薏仁米15 g+麦麸5 g。
1.2 仪器与设备
1260高效液相色谱仪:美国Agilent公司;TGL27A高速离心机:上海高致精密仪器有限公司;YXQ-LS-75SII高压灭菌锅:广州罡然机电设备有限公司;SW-CJ-1D无菌操作台:苏州净化设备有限公司;UV-2450紫外可见分光光度计:日本岛津公司;THZ-D菌种振荡培养箱:苏州培英实验设备有限公司。
1.3 方法
1.3.1 菌种的活化及培养
从4 ℃冰箱中取出菌种斜面,在25 ℃恒温培养箱中活化2 h备用。待培养基冷却之后进行接种,25 ℃、120 r/min摇床培养3 d。
1.3.2 子实体培养
配制干料培养基:根据固体培养基基质配方,将原料放入培养瓶用水泡3 h,将水倒掉之后按照干料∶营养液=1∶1.5(g∶mL)的配比加入营养液,115 ℃灭菌45 min,冷却后无菌操作,将200 μL种子液接种到灭好菌的培养基中,于25 ℃条件下培养40~50 d,即可收获子实体。
1.3.3 测定方法
(1)虫草素的测定[20]
采用高效液相色谱法测定虫草素含量,其色谱条件:ZORBAX SB-C18色谱柱(250 mm×4.6 mm×5 μm);流动相为乙腈-水(5∶95,V/V);流速1 mL/min;检测波长260 nm;柱温25 ℃;进样量1 μL。
虫草素标准曲线绘制:精确称取6.8 mg虫草素标准品,置于25 mL容量瓶中,加超纯水定容,使虫草素标准品质量浓度为272 mg/L,过0.22 μm滤膜,然后再依次稀释成0.531 25 mg/mL、1.062 5 mg/mL、2.125 mg/mL、4.25 mg/mL、8.5 mg/mL、17 mg/mL、34 mg/mL的系列虫草素标准溶液。在色谱条件下依次进样,以虫草素质量浓度(x)为横坐标,峰面积(y)为纵坐标,绘制虫草素标准曲线,得到回归方程为y=121.83x-84.383,相关系数R2=0.999 3。
样品中虫草素提取:收获子实体,60 ℃烘干、粉碎。精确称取0.2 g粉末于具塞试管当中,加入10 mL无菌水摇匀,超声提取(功率200 W)1 h并且每隔20 min摇匀一次,超声提取结束后在4 500 r/min的条件下离心15 min,取上清液经0.45 μm滤膜过滤,取滤液得到待测液。按照标准曲线回归方程计算样品中虫草素含量。
(2)虫草酸的测定
采用高效液相色谱法测定虫草酸含量。甘露醇标准曲线的制作:根据马麦艳等[21]的方法,稍作修改。甘露醇标样100 mg,加蒸馏水100 mL配制成质量浓度为1 000 μg/mL的甘露醇溶液,然后用蒸馏水分别稀释成所需浓度。取相应浓度甘露醇标准溶液各1 mL于不同试管中,加入1 mL 15 mmol/L高碘酸钠溶液混匀,室温条件下放置10 min,加2 mL 0.1%L-鼠李糖溶液混合后加4 mL新配制的Nash试剂,水浴加热15 min显色,冷却,在波长412 nm处测定吸光度值(OD412nm值),以甘露醇标准溶液质量浓度(x)为横坐标,OD412nm值(y)为纵坐标绘制虫草酸标准曲线。得到回归方程y=0.004 2x-0.008 3,相关系数R2=0.999 1。
样品处理及甘露醇测定方法:分别准确称量蛹虫草子座粉末1.0 g,各加入20 mL超纯水沸水浴提取1 h,将提取液离心(5 000 r/min、8 min)取上清液补水至20 mL,保存样品,待测。按照标准曲线回归方程计算样品中虫草酸含量。
(3)虫草多糖的测定[22]
蛹虫草多糖提取:称取子实体粉末0.1 g于试管中,加入2 mL NaOH(1 mol/L)于70 ℃烘箱70 min,漏斗过滤,加入2~3 mL蒸馏水冲洗试管残渣,定容至250 mL容量瓶中,待测。
葡萄糖标准曲线绘制:精确称取干燥葡萄糖,配制成100 μg/mL标准溶液。分别吸取0 mL、0.2 mL、0.4 mL、0.6 mL、0.8 mL、1.0 mL、1.2 mL于试管中,再添加蒸溜水使其达到2 mL。吸取苯酚(6%)1 mL于试管中,再吸取5 mL浓硫酸,静置10 min。于旋涡混合仪上混匀,静置20 min,以蒸馏水为空白对照,于波长490 nm处测吸光度值,以葡萄糖标准溶液质量浓度(x)为横坐标,OD490nm值(y)为纵坐标绘制葡萄糖标准曲线。得到回归方程:y=8.424 3x-0.005,相关系数R2=0.999 2。
(4)抗氧化活性测定
DPPH自由基(DPPH·)清除率的测定[23]:准确称取2 mg DPPH,用无水乙醇溶解并定容至50 mL。取DPPH自由基乙醇溶液4 mL加入经处理的1 mL样品中,室温暗反应30 min,以无水乙醇代替样品为空白对照,测定其在波长517 nm处的吸光度值。DPPH自由基清除率按照以下公式计算:
式中:A0为空白吸光度值;Ai为样品吸光度值;A1为样品溶液本底的吸光度值。
ABTS自由基(ABTS·)清除率的测定[24-25]:取7.4 mmol/L的ABTS原液与等量2.45 mmol/L过硫酸钾混合、在黑暗中放置12~14 h,于波长734 nm处测定吸光度值。样品经过离心后取40 μL,加水稀释至1 mL,加入6 mL ABTS工作液,混合均匀后在波长734 nm处测吸光度值,无水乙醇作为空白,ABTS+·清除率按照以下公式计算:
式中:A0为空白吸光度值;Ai为样品吸光度值;A1为样品溶液本底的吸光度值。
2 结果与分析
2.1 不同固体培养基培养蛹虫草生长情况
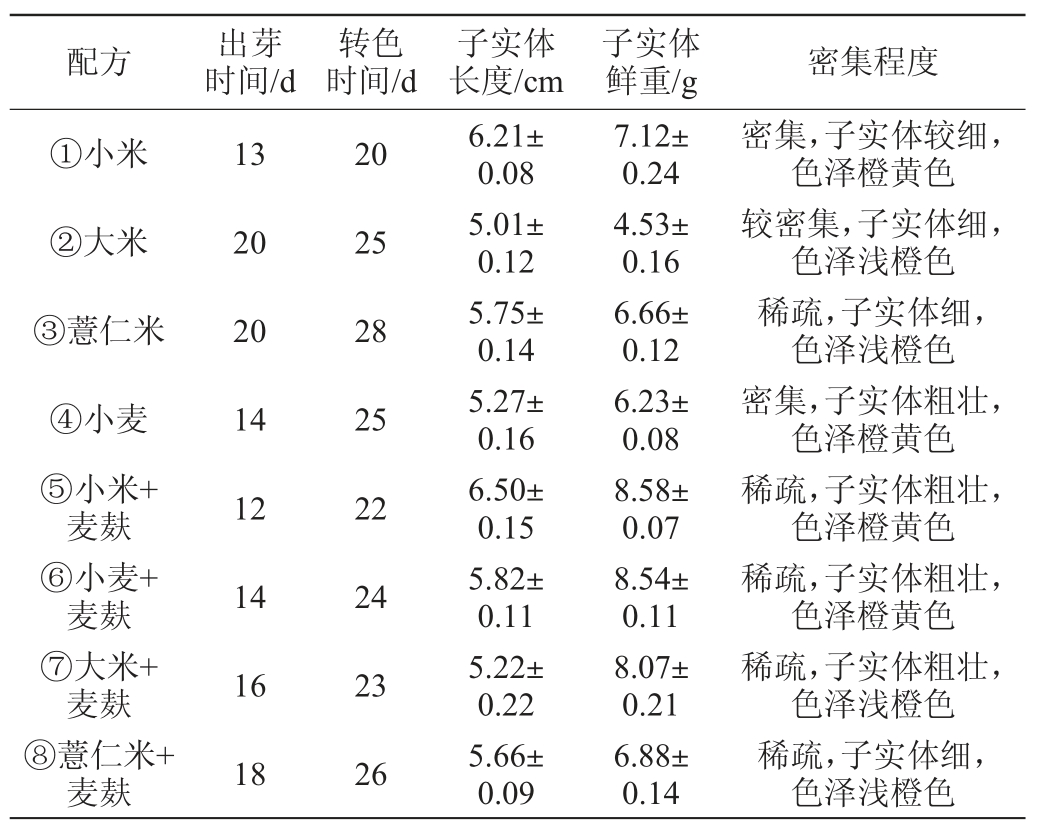
菌丝在固体培养基上培养45 d,不同固体培养基培养蛹虫草的生长情况如表1所示。由表1可知,蛹虫草在不同固体培养基上均能生长,采用小米+麦麸配方时,蛹虫草出芽时间最快,为12 d;蛹虫草子实体长度最长,为(6.50±0.15)cm,子实体鲜质量最重,为(8.58±0.07)g,子实体生长密集,粗壮,色泽为橙黄色。
表1 不同固体培养基培养蛹虫草生长情况
Table 1 Growth of Cordyceps militaris cultured on different solid media
2.2 不同固体培养基对蛹虫草虫草素含量的影响
由图1可知,不同固体培养基培养蛹虫草,其子实体中虫草素含量不同。其中,小米+麦麸培养基培养出的蛹虫草子实体中虫草素的含量最高,为(6.53±0.06)mg/g;小麦+麦麸培养基次之,为(5.31±0.09)mg/g;大米培养基培养的蛹虫草子实体中虫草菌素含量最低,仅为(2.13±0.07)mg/g。除大米培养基外,其他配方培养基所培养的子实体虫草素均高于刘红等[26]所培养的蛹虫草子实体中虫草素含量(2.147 2 mg/g)。
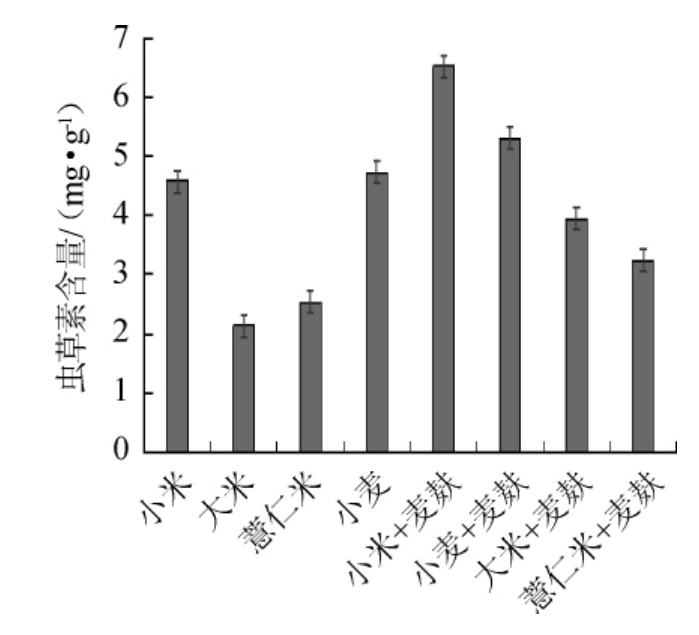
图1 不同固体培养基培养蛹虫草子实体的虫草素含量
Fig.1 Cordycepin content in Cordyceps militaris fruit bodies cultured on different solid media
2.3 不同固体培养基对蛹虫草虫草酸含量的影响
由图2可知,不同固体培养基培养蛹虫草,其子实体中虫草酸含量不同。其中,小米+麦麸培养基培养出的蛹虫草子实体中虫草酸的含量最高,为(7.66±0.21)mg/g,小麦+麦麸培养基次之,为(6.97±0.51)mg/g,大米培养基培养的蛹虫草子实体中虫草酸含量最低,仅为(2.66±0.14)mg/g。
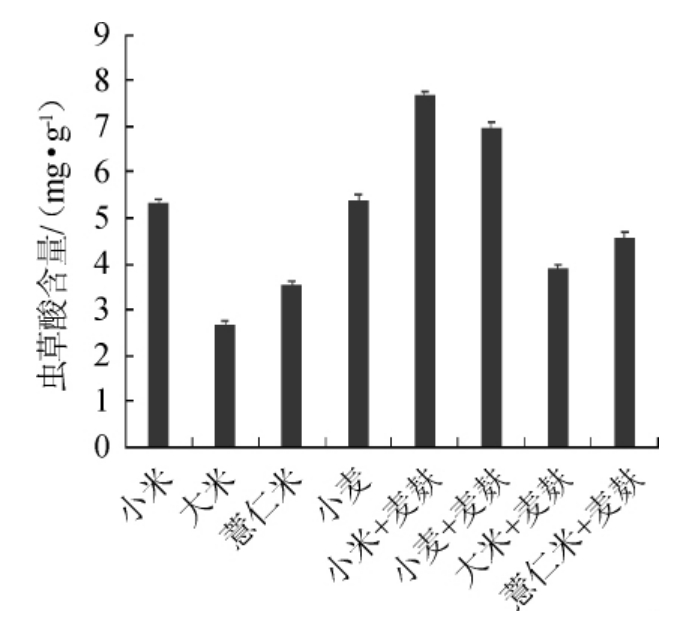
图2 不同固体培养基培养蛹虫草子实体的虫草酸含量
Fig.2 Cordyceps acid content in Cordyceps militaris fruit bodies cultured on different solid media
2.4 不同固体培养基对蛹虫草虫草多糖含量的影响
由图3可知,不同固体培养基培养蛹虫草,所收获的子实体中虫草多糖含量不同。其中,贵州特色杂粮薏仁米培养基所培养的蛹虫草子实体中虫草多糖的含量最高,为(59.07±1.89)mg/g;小麦+麦麸培养基次之,为(52.60±1.73)mg/g;小米培养基培养的蛹虫草子实体中虫草多糖含量最低,仅为(36.30±0.94)mg/g。
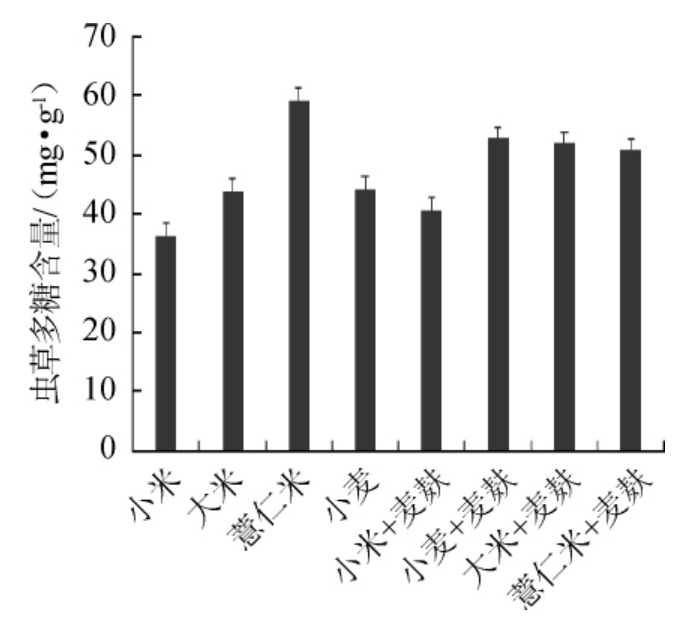
图3 不同固体培养基培养蛹虫草子实体的虫草多糖含量
Fig.3 Cordyceps polysaccharide content in Cordyceps militaris fruit bodies cultured on different solid media
2.5 蛹虫草活性物质、自由基清除率相关性分析
由图4可知,8种不同固体培养基培养蛹虫草子实体DPPH自由基清除率和ABTS自由基清除率的范围分别为25.77%~66.84%和22.82%~68.28%。其中,薏仁米+麦麸培养蛹虫草子实体DPPH自由基消除率及ABTS自由基清除率均高于其他培养基,分别为(66.84±0.77)%和(68.28±0.28)%;小麦+麦麸培养蛹虫草子实体DPPH自由基消除率及ABTS自由基清除率次之,为(56.11±1.11)%和(57.16±0.25)%;大米培养蛹虫草子实体DPPH自由基消除率及ABTS自由基清除率效果最弱,仅为(30.85±2.08)%和(33.62±1.47)%。
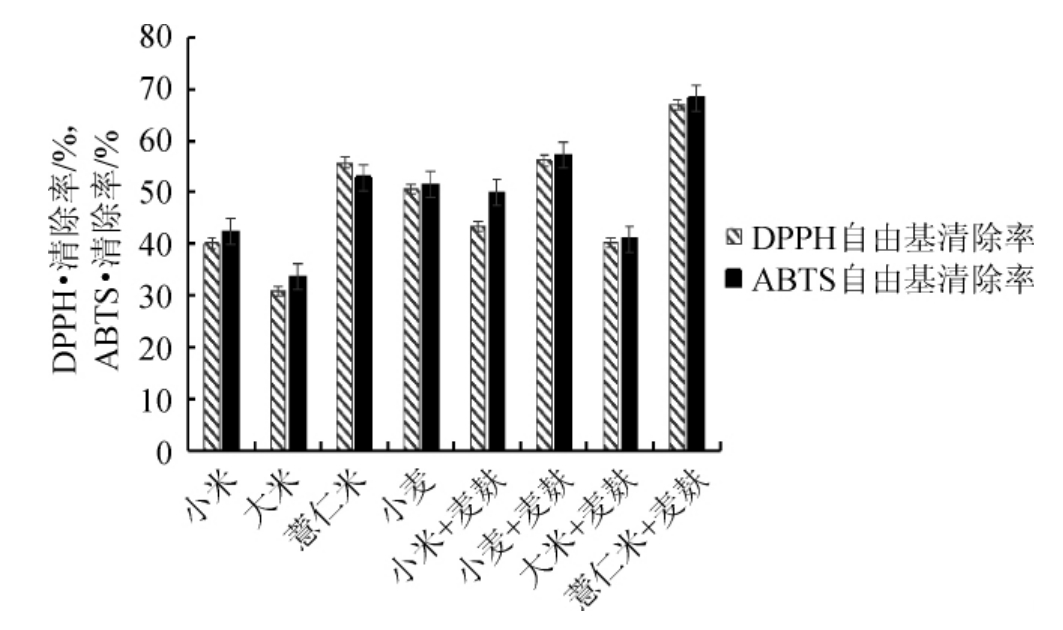
图4 不同固体培养基培养蛹虫草子实体的抗氧化活性
Fig.4 Antioxidant activity of Cordyceps militaris fruit bodies cultured on different solid media
表2 蛹虫草活性物质与自由基清除率的相关性分析
Table 2 Correlation analysis of active substance and free radical scavenging rate of Cordyceps militaris
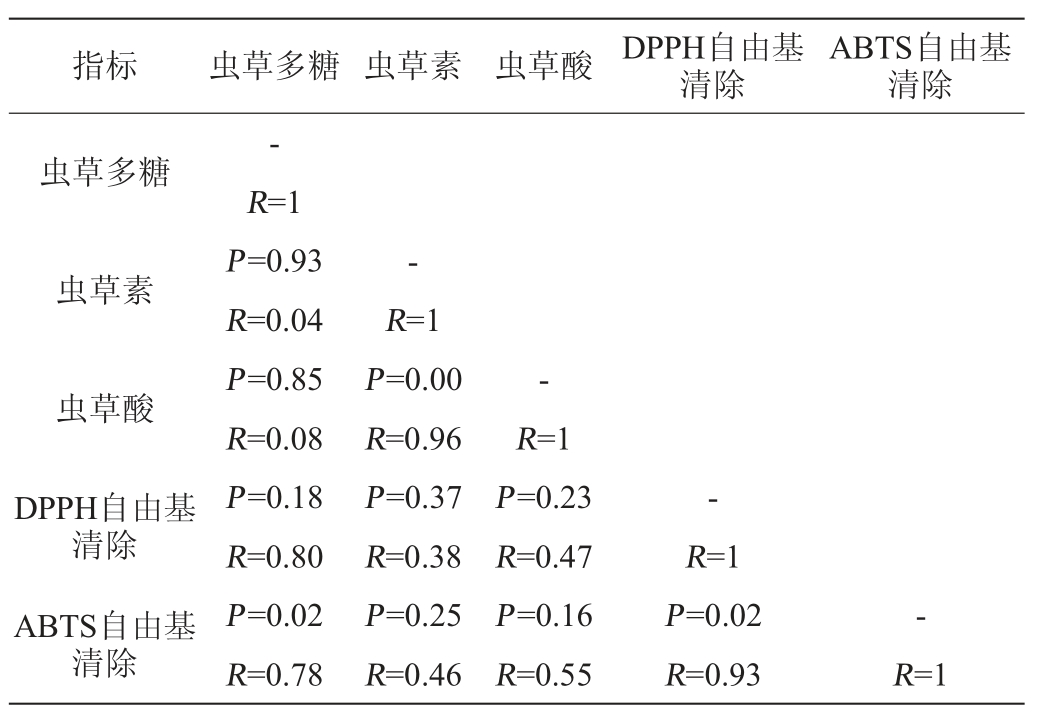
从表2可知,ABTS自由基清除和虫草多糖呈显著的正相关性(P=0.02,R=0.78),DPPH自由基清除和ABTS自由基清除呈显著的正相关性(P=0.02,R=0.93),虫草素和虫草酸呈显著的正相关性(P=0.00,R=0.96)。
3 结论
不同培养基质(薏仁米、小米、小麦、大米等)对蛹虫草子实体生长情况、虫草素、虫草酸、虫草多糖及抗氧化活性均有影响。其中,小米+麦麸培养基培养蛹虫草子实体的生长情况较佳,出芽时间最快,为12 d,子实体最长,为(6.50±0.15)cm,鲜质量最重,为(8.58±0.07)g,其虫草素和虫草酸含量最高,分别为(6.53±0.06)mg/g和(7.66±0.21)mg/g;薏仁米培养基培养蛹虫草子实体虫草多糖含量最高,为(59.07±1.89)mg/g,薏仁米+麦麸培养基抗氧化活性最强,DPPH自由基消除率和ABTS自由基清除率分别为(66.84±0.77)%、(68.28±0.26)%。
小米+麦麸中虫草酸和虫草素等核苷类物质含量最高,薏仁米中虫草多糖含量高及抗氧化性强。因此,小米+麦麸适当的复配比例可用于人工培养高产虫草素、虫草酸的蛹虫草子实体,薏仁米更适合适合培养高产多糖和抗氧化性强的蛹虫草子实体。
[1]刘璐,高冰,丁城,等.蛹虫草面酱发酵工艺研究[J].中国酿造,2017,36(3):188-191.
[2]曾宏彬,宋斌,李泰辉,等.蛹虫草研究进展及其产业化前景[J].食用菌学报,2011,18(2):70-74.
[3]LEE J S,KWON D S,LEE K R,et al.Mechanism of macrophage activation induced by polysaccharide from Cordyceps militaris culture broth[J].Carbohyd Polym,2015,120:29-37.
[4]CHAN J S L,BARSEGHYAN G S,ASATIANI M D,et al.Chemical composition and medicinal value of fruiting bodies and submerged cultured mycelia of caterpillar medicinal fungus Cordyceps militaris CBS-132098(Ascomycetes)[J].Int J Med Mushroom,2015,17(7):649-659.
[5]JOWS.Cordycepin-enriched Cordyceps militaris induces immunomodulation and tumor growth delay in mouse-derived breast cancer[J]. Oncol Report,2013,30(4):1996-2002.
[6]JEN C Y,LIN C Y,HUANG B M,et al.Cordycepin induced MA-10 mouse leydig tumor cell apoptosis through caspase-9 pathway[J].Evidence-Based Complement Alternat Med,2011:984537.
[7]张晓卿,李媚,蓝丽红,等.比色法测定发酵液中甘露醇的含量[J].化工技术与开发,2004,33(2):33-35.
[8]XIA Y L,LUO F F,SHANG Y F,et al.Fungal cordycepin biosynthesis is coupled with the production of the safeguard molecule pentostain[J]. Cell Chem Biol,2017,24:1-11.
[9]YAMAMOTO K,SHICHIRI H,UDA A,et al.Apoptotic effects of the extracts of Cordyceps militaris via Erk phosphorylation in a renal cell carcinoma cell line[J]. Phytother Res,2015,29(5):707-713.
[10]UEDA Y,MORI K,SATOH S,et al.Anti-HCV activity of the Chinese medicinal fangus Cordyceps militaris[J]. Biochem Bioph Res Co,2014,447(2):341-345.
[12]周思静,刘桂君,尚宏忠,等.蛹虫草人工培养技术研究进展[J].江苏农业科学,2014,42(7):13-17.
[13]DWORECKA K B.Cordyceps fungi as a natural killers,new hopes for medicine and biological control factors[J]. Ann Parasitol,2014,60(3):151-158.
[14]ZENG Y,ZHANG Y,ZHANG L,et al.Structural characterization and antioxidant and immunomodulation activities of polysaccharides from the spent rice substrate of Cordyceps militaris[J].Food Sci Biotechnol,2015,24(5):1591-1596.
[15]YU S,CHEN S T,LI W,et al.Hypoglycemic activity through a novel combination of fruiting body and mycelia of Cordyceps militaris in high-fat diet-induced type 2 diabetes mellitus mice[J].J Diabetes Res,2015,2015:1-10.
[16]侯金鑫,张金秀,赵晓静,等.蛹虫草液体发酵产物冻干粉的抗氧化活性及保肝作用[J].药物评价研究,2014(1):25-29.
[17]张显科,刘文霞.不同培养料栽培蛹虫草试验研究[J].中国食用菌,1997,16(2):21-22.
[18]冯景刚,张迪,刘在民.不同培养基对北虫草子实体产量与质量的影响[J].辽宁林业科技,2008(6):24-25.
[19]刘桂君,周思静,林金星.培养基质对蛹虫草中虫草酸及核苷类物质的影响[J].食品与发酵工业,2015,41(5):94-98.
[20]汤佳鹏,柳依婷,赵强.等.蛹虫草发酵产虫草素的培养条件研究[J].食品工业科技,2012,33(21):181-187.
[21]马麦艳,马琴,陈方圆,等.不同培养介质对蛹虫草子实体生长及产量的影响[J].现代农业科技,2017(23):54-61.
[22]周广乙.蛹虫草多糖和D-甘露醇的发酵研究[D].长沙:中南林业科技大学,2015.
[23]YEN G C,CHEN H Y.Antioxidant activity of various tea extracts in relation to their antimutagenicity[J].J Agr Food Chem,1995,43:27-37.
[24]CHANG K C,JUN K H.Anthocyanins from soybean seed coat inhibit the expression of TNF-a-induced genes associated with ischemia/reperfusion in endothelial cell by NF kB-dependent pathway[C].第十五届国际药理学大会论文集.北京:中国药理学会,2006:157.
[25]OH J,JO H,CHO A R,et al.Antioxidant and antimicrobial activities of various leafy herbal teas[J].Food Control,2013,31(2):403-409.
[26]刘红,马辉,曹宏,等.不同蛹虫草杂粮培养基的生产性能及滋味物质分析[J].食品工业科技,2019,40(12):77-84.