全球变暖对葡萄的采收和品质都有不同程度的影响,葡萄果实中的总糖增加,与此同时果糖的浓度也在增加[1]。高糖度的发酵条件下,在发酵的初期酵母会受到高糖造成的高渗透压胁迫,另外在发酵的后期高浓度的酒精会对酵母有强烈的抑制作用[2-4],尤其乙醇含量的增加对酵母对于果糖的利用的抑制作用要高于葡萄糖[5-6],因此在发酵后期往往导致发酵不彻底,残糖过高尤其是果糖,而果糖的甜度是葡萄糖的两倍对葡萄酒的口感及后期储存带来不利影响[7-8]。
酵母在酒精发酵过程中所需要的营养成分以氮源最为重要,葡萄汁中的氮源可分为有机氮和无机氮,有机氮主要包括氨基酸、多肽和蛋白质,无机氮主要是铵态氮和硝态氮,其中酵母能够直接利用的氮源称为可同化氮(yeast assimilable nitrogen,YAN),包括游离氨基酸(脯氨酸除外)、小分子多肽和铵态氮[9-11]。酵母可以直接吸收氨基酸用于蛋白质合成,不需要通过自身代谢合成所需要的氨基酸[12],氨基酸的添加可以增强合成葡萄糖转运蛋白的能力,代谢糖的能力更强。研究表明添加可同化氮刺激酵母对果糖的利用要高于对葡萄糖的利用。因此对于高糖度的葡萄原料在酒精发酵过程中通过合理补充氮源可以预防发酵不彻底[13],避免果糖残留过多。酵母细胞壁又叫酵母皮(yeast hull),占细胞干质量的10%~25%,酵母细胞壁的网状结构有助于吸附酵母在发酵过程中产生的中链脂肪酸(如己酸、辛酸和癸酸)、农药残留、赭曲霉素A等有害物质[14-15]。另外酵母细胞壁中富含甾醇和不饱和脂肪酸等生长因子,这些生长因子有助于保持膜的流动性,维持细胞膜的生物活性,增强细胞对乙醇的耐受性[16]。氧气的存在是酵母合成麦角甾醇和不饱和脂肪酸所必须的,在酒精发酵的无氧条件下,酵母可以吸收发酵液中的不饱和脂肪酸和甾醇并结合到细胞膜中。此外酵母细胞壁在加入葡萄醪/葡萄汁后部分不溶的成分悬浮在发酵液中可以作为二氧化碳的成核中心,降低二氧化碳的溶解度,减轻二氧化碳对酵母的毒害[17]。
在宁夏和新疆葡萄产区经常会遇到葡萄原料糖度过高发酵缓慢甚至停滞的问题,为了提高葡萄酒酵母在高糖度条件下的发酵性能使酒精发酵更为彻底,本研究在高糖度条件下通过在发酵过程中添加酵母源有机营养和酵母细胞壁进行实验,对比了单一有机氮源和酵母细胞壁在不同添加时期的效果的差异,以及有机氮源与酵母细胞壁配合添加与单一添加的差异,以期为高糖度葡萄原料的酒精发酵提供参考依据。
1 材料与方法
1.1 材料与试剂
葡萄汁(宁夏红寺堡产区赤霞珠葡萄,总糖286.2 g/L,调整后总酸8.8 g/L,发酵液浊度332 NTU):宁夏长城天赋酒庄。
葡萄酒活性干酵母CEC01、酵母源有机氮源FN502、酵母细胞壁CW101:安琪酵母股份有限公司。
L-酒石酸(分析纯):上海源叶生物科技有限公司;葡萄糖、果糖(均为分析纯):美国Sigma公司;无水乙醇(色谱纯),硫酸(分析纯):国药集团化学试剂有限公司。
1.2 仪器与设备
LRH-系列生化培养箱:上海一恒科技有限公司;BSA2202S电子天平:赛多利斯科学仪器(北京)有限公司;LKTC-B1-T恒温水浴锅:金坛市城东新瑞仪器厂;PHS-3C酸度计:上海仪电科学仪器股份有限公司;ZORBAX碳水化合物分析柱(4.6 mm×250 mm,5 μm)、HP1100高效液相色谱仪(具有示差折光检测器和自动进样器):美国安捷伦公司;SHZ曲型循环水真空泉:郑州长城科工贸有限公司;KQ100DB型超声波清洗器:昆山市超声仪器有限公司。
1.3 方法
1.3.1 酒精发酵
选择晚采收的赤霞珠葡萄作为发酵原料,为减小葡萄原料不均匀带来的误差,本实验采用未澄清的葡萄汁进行发酵实验。取260 mL发酵原料置于500 mL三角瓶中,然后接种酵母,酵母接种量250 mg/L,放入恒温培养箱中发酵,温度设为25 ℃。每隔24 h在同一时间点测定一次发酵处理样的质量,通过前后的质量差代表CO2的生成量,并根据每天的CO2生成量绘制发酵曲线。根据CO2的生成量确定营养的添加时间,首先根据每个三角瓶中发酵液的体积及发酵液的糖浓度估算出总的CO2的生成量(约为41 g),然后根据CO2的生成量分别在发酵的初始阶段、发酵的1/6、1/3、1/2、2/3(对应的CO2的生成量分别为0、6.8 g、13.7 g、20.5 g、27.3 g)添加酵母源有机氮FN502或者酵母细胞壁CW101,添加量为200 mg/L,分别用FN0、FN1、FN2、FN3、FN4和CW0、CW1、CW2、CW3、CW4表示。另外设置了4种有机氮FN502和酵母细胞壁CW101的组合添加方案:(1)在发酵进行1/3时同时添加FN502和CW101(各添加200 mg/L);(2)在发酵进行1/6时添加FN502,在发酵进行1/2时添加CW101(各添加200 mg/L);(3)在发酵进行1/3时添加FN502,发酵进行2/3时添加CW101(各添加200 mg/L);(4)在发酵进行1/2时同时添加FN502和CW101(各添加200 mg/L),分别用FC1、FC2、FC3、FC4表示。当24 h间隔CO2的生成量<1.0 g时,可以判定酒精发酵基本结束。每个处理样设置2个重复。
1.3.2 酒样常规理化指标测定
酒精参照GB/T 15038—2006《葡萄酒、果酒通用分析法》[18]测定。
1.3.3 葡萄糖、果糖、总残糖含量的测定
发酵样品的处理:将发酵样品在取样容器中混匀,取混匀后的适量样品4 000 r/min离心10 min,精密称取一定质量离心后的上清液至容量瓶中,用纯水定容并稀释合适的倍数,使其浓度在曲线范围内,将稀释后溶液经0.45 μm滤膜过滤后上机测试。
色谱条件:用0.005 mol/L H2SO4溶液作为流动相,流速为0.6 mL/min,柱温65 ℃,平衡流动相待仪器基线走平稳后进样,进样量为20 μL。
通过液相检测出葡萄糖和果糖的含量,总残糖=葡萄糖+果糖。
1.3.4 数据分析
运用SPSS 22.0软件在0.05水平下进行单因素方差分析和邓肯氏多重比较,采用Origin Pro 9.0进行数据统计和绘图。
2 结果与分析
2.1 发酵曲线
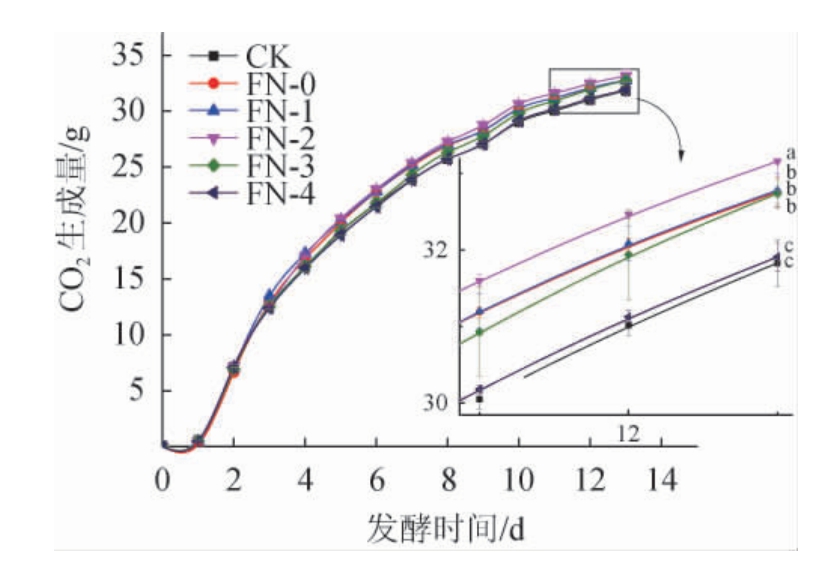
图1 不同发酵时期添加有机氮FN502的发酵曲线
Fig.1 Fermentation curve of adding organic nitrogen FN502 in different fermentation periods
不同字母代表结果差异显著(P<0.05)。下同。
由图1可知,与对照(未添加FN502或CW101)相比,当有机氮FN502和酵母同时加入葡萄汁后,在最开始并没有明显的提高酒精发酵的速度,而在酒精发酵进行1/6时添加有机氮FN502明显提高了酒精发酵速度,在酒精发酵后期二者的发酵速度基本一致;在酒精发酵进行1/3时添加有机氮FN502,酒精发酵速度得到迅速提升;在发酵进行1/2时添加有机氮FN502,对酒精发酵速度的提升较为缓慢;而在酒精发酵进行2/3时添加有机氮FN502,则对酒精发酵的速度没有明显的影响,葡萄酒酵母在指数生长期之后由于代谢所产生的酒精及中链脂肪酸(如己酸、辛酸和癸酸)的抑制作用使酵母的细胞膜流动性变差,同时细胞膜上的转运蛋白活性降低[19],导致对营养物质的吸收能力下降[20],因此需要在酵母活性生长过程中提供给细胞营养及生存因子,在酒精发酵的中后期一旦生长停止,即使补充营养和生存因子也不能达到理想的效果[21]。
发酵结束时,在酒精发酵进行1/3时添加有机氮FN502的处理组最终产生的CO2总质量显著高于对照和其他处理组(P<0.05),在酵母接种时同时添加有机氮FN502和在酒精发酵进行1/6及1/2时添加有机氮FN502,三种处理之间最终产生的CO2总质量没有明显差异(P>0.05),但均显著高于对照和在酒精发酵进行2/3时添加有机氮FN502的处理组(P<0.05)。而在酒精发酵进行2/3时添加有机氮FN502则与对照没有明显差异(P>0.05)。说明在发酵进行1/3时添加有机氮FN502效果最好,此时正值酵母生长的对数期,酵母生长繁殖活跃,酵母吸收营养的能力更强,同时也需要更多的营养来促进细胞合成,在酒精发酵的中后期对酒精的耐受性和代谢糖的能力也相对更强。
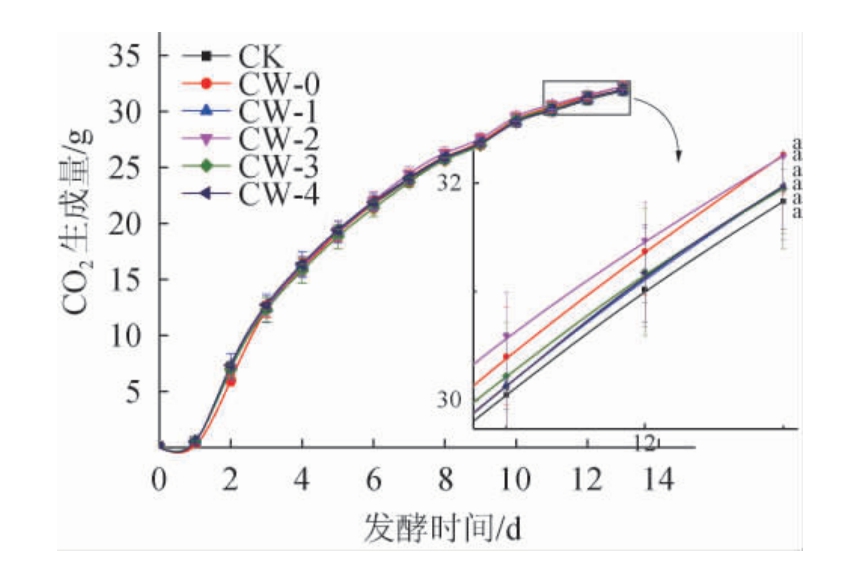
图2 不同发酵时期添加酵母细胞壁CW101的发酵曲线
Fig.2 Fermentation curve of adding yeast cell wall CW101 in different fermentation periods
由图2可知,与对照相比,在酒精发酵的不同时期添加酵母细胞壁CW101对整个酒精发酵速度没有显著的影响,尤其酵母细胞壁CW101在酵母接种后立即添加,在发酵的起始阶段还会对发酵速度产生一定的抑制作用,但在发酵3 d后发酵速度开始逐渐超过对照。在酒精发酵结束后,不同时期添加酵母细胞壁CW101的处理组最终产生的CO2总质量与对照相比没有明显差异(P>0.05)。对于过度澄清的葡萄汁,其中悬浮的颗粒同时被去除,浊度降低的同时,颗粒表面吸附的营养和生存因子也会被除去,因此会更容易出现发酵缓慢甚至发酵停滞,而酵母细胞壁的添加可以增加葡萄汁的浊度,NICOLINI G等[22]研究认为葡萄汁的浊度在100 NTU上下是能够保持果香又能够防止发酵停滞的最佳折中浊度。另外酵母细胞壁含有丰富的甾醇和不饱和脂肪酸等生存因子,酵母在生长繁殖过程中可以吸收这些生存因子以提高对酒精的耐受性,促进糖的消耗,另外酵母细胞壁可以作为CO2的成核中心,细小的CO2聚集在细胞壁周围形成更大的气泡析出,从而降低CO2的溶解度,减轻CO2对酵母细胞的毒害。
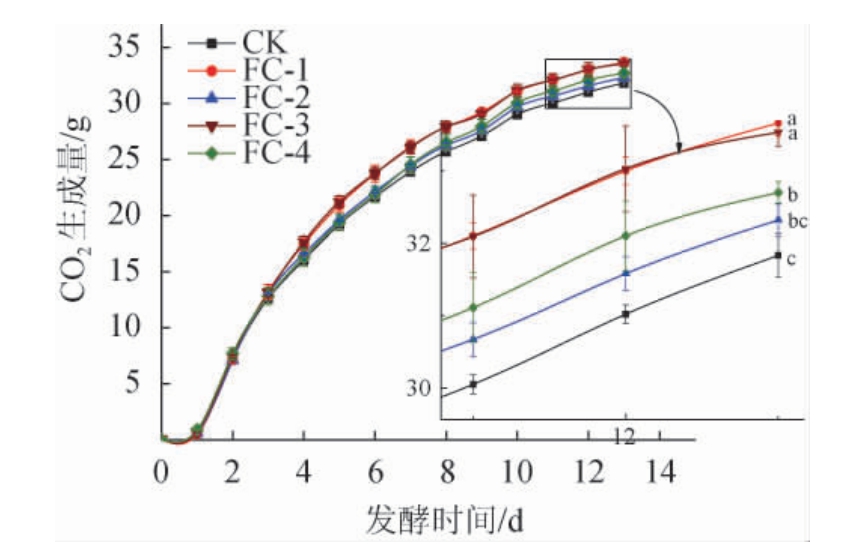
图3 不同发酵时期组合添加有机氮FN502和酵母细胞壁CW101的发酵曲线
Fig.3 Fermentation curve of adding organic nitrogen FN502 and yeast cell wall CW101 in different fermentation periods
由图3可知,与对照相比,处理组FC-1可以明显的快速提高酒精发酵速度(P<0.05);处理组FC-3与FC-1的作用效果相近,二者没有明显的差异(P>0.05)。与对照相比,处理组FC-2对酵母的酒精发酵速度没有明显的提升(P>0.05),而处理组FC-4与对照相比虽然对酒精发酵速度有明显的提升(P<0.05),但是与FC-2相比差异不明显(P>0.05)。在发酵结束后,FC-1和FC-3最终产生的CO2总质量没有显著差异(P>0.05),二者均显著的高于对照和FC-2和FC-4(P<0.05);FC-4显著高于对照(P<0.05),但与FC-2相比差异不显著(P>0.05);FC-2与对照相比没有显著的差异(P>0.05)。以上结果说明FC-1和FC-3处理组对酵母酒精发酵的促进作用最好。
2.2 发酵结束后酒精度与乙酸结果分析
由表1可知,单独添加有机氮FN502时,在酒精发酵进行1/3时添加有机氮FN502,酵母最终的发酵酒精度最高,最高为16.6%vol;单独添加酵母细胞壁CW101时,处理组CW-3的最终酒精度最高,为16.4%vol;当有机氮FN502和酵母细胞壁CW101组合使用时,FC-1和FC-3的最终酒精度最高,均为16.9%vol,均显著的高于对照和其他添加方式(P<0.05)。与对照相比,酵母有机氮FN502和酵母细胞壁CW101的添加均显著降低了乙酸的产生(P<0.05),其中有机氮FN502在酒精发酵进行2/3之前效果最好,酵母细胞壁CW101在酒精发酵进行1/2时效果最好。
表1 酒样酒精度和乙酸含量检测结果
Table 1 Detection results of alcohol content and acetic acid contents of wine samples
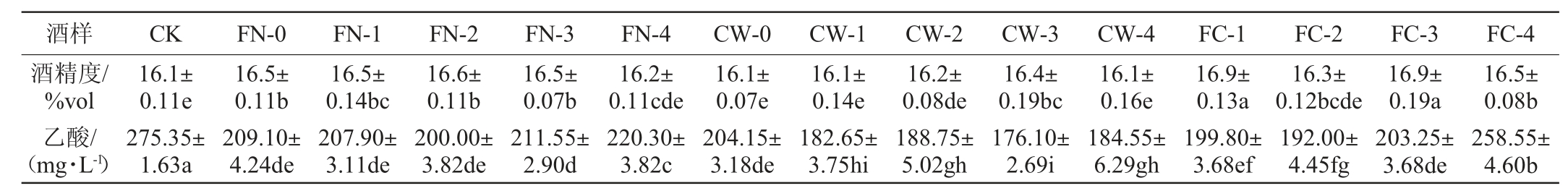
注:不同字母代表差异显著(P<0.05)。
2.3 发酵结束后葡萄糖和果糖结果分析
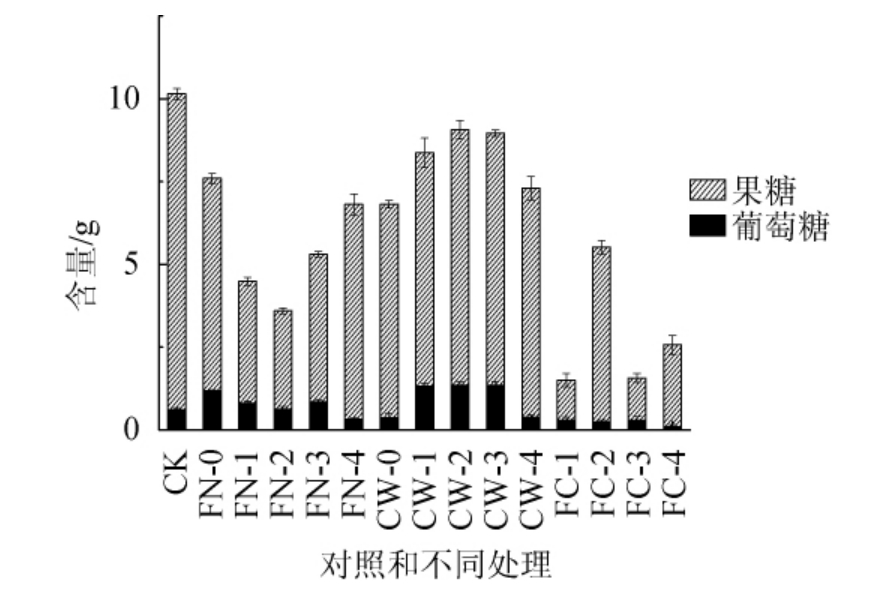
图4 不同酒样酒精发酵结束后葡萄糖、果糖含量和果糖/葡萄糖对比
Fig.4 Comparison of glucose,fructose contents and fructose/glucose in different wine samples after alcoholic fermentation
由图4可知,有机氮FN502单独添加时,在酒精发酵进行1/3时添加有机氮FN502,最终总残糖最低,总残糖为3.60 g/L;与对照相比,在酒精发酵的不同时期添加有机氮FN502均降低了最终的总残糖;最终残糖以果糖为主,果糖的含量大概是葡萄糖含量的4~24倍。酵母对于葡萄糖和果糖的代谢存在明显的差异,虽然果糖与葡萄糖同时使用,但葡萄糖首先从发酵液中耗尽,这导致发酵过程中消耗的葡萄糖和果糖数量之间的差异[23-24]。FN-0、FN-1、FN-2和FN-3的果糖/葡萄糖的比值均比对照小4~5倍左右,由此可见有机氮FN502的添加促进了果糖的消耗,这与左松等[25]的研究结果一致,而由于果糖和葡萄糖共用一套膜运输和酶催化体系,所以就导致葡萄糖的利用相对下降,因此FN-0、FN-1、FN-2和FN-3处理组发酵结束后葡萄糖的含量反而均高于对照。而在酒精发酵进行2/3时添加有机氮FN502对果糖消耗的促进作用则相对其他4种处理更小。酵母细胞壁CW101单独添加时,5种添加方式对酵母果糖消耗的促进作用均高于对照,但不如有机氮FN502。CW-1、CW-2和CW-3处理组对酵母对果糖消耗的促进作用较小,而又限制了葡萄糖的消耗,所以最终总残糖相对于CW-0和CW-4要高。有机氮FN502和酵母细胞壁CW101组合添加时,FC-1和FC-3处理组对果糖消耗的促进作用最好,最终总残糖也最低,总残糖分别为1.50 g/L和1.58 g/L。
综合对比有机氮FN502和酵母细胞壁CW101组合添加时FC-1和FC-3对于酵母对果糖的消耗促进作用最好,总残糖也最低。与对照相比,酵母源有机营养和酵母细胞壁的添加均降低了最终的总残糖。
3 结论
通过酵母源有机营养和酵母细胞壁的添加,可以提高葡萄酒酵母在高糖度葡萄原料条件下的发酵速度和最终发酵酒度,降低乙酸的产量和最终总残糖含量。酵母源有机氮FN502单独添加时,在不同的添加时期对葡萄酒酵母的酒精发酵影响存在差异,其中在酒精发酵进行1/3时添加对葡萄酒酵母的发酵速度促进作用最强,并能促进葡萄酒酵母对果糖的消耗,总残糖也最低。酵母细胞壁CW101单独添加时,在不同添加时期对葡萄酒酵母的发酵速度均没有明显的促进作用,与对照相比,在酒精发酵进行2/3之前添加均能降低残总糖,但作用效果不如有机氮FN502。在酒精发酵进行1/3时同时添加有机氮FN502和酵母细胞壁CW101(各200 mg/L),或在酒精发酵进行1/3时添加有机氮FN502(200 mg/L),进行2/3时添加酵母细胞壁CW101(200 mg/L),对葡萄酒酵母的酒精发酵速度及果糖消耗促进作用均高于对照及二者分别单独使用,最终酒精度均为16.9%vol,总残糖分别为1.50 g/L和1.58 g/L。有机氮FN502和酵母细胞壁CW101的添加均可显著(P<0.05)降低乙酸的产量。
[1]JONES G V,WHITE M A,COOPER O R,et al.Climate change and global wine quality[J].Climatic Change,2005,73(3):319-343.
[2]STANLEY D,BANDARA A,FRASER S,et al.The ethanol stress response and ethanol tolerance of Saccharomyces cerevisiae[J]. J Appl Microbiol,2010,109(1):13-24.
[3]毕新煜,刘功良,姜弘佳,等.酵母菌高糖耐受机制的研究进展[J].中国酿造,2017,36(10):1-4.
[4]杜春迎,赵辉,赵志昌,等.发酵工业中酿酒酵母耐性机制的研究进展[J].食品工业科技,2012,33(13):378-382.
[5]BAUER F F,PRETORIUS I S.Yeast stress response and fermentation efficiency:How to survive the making of wine-A review[J].S Afr J Enol Viticult,2000,21:27-51.
[6]LICCIOLI T,CHAMBERS P J,JIRANEK V.A novel methodology independent of fermentation rate for assessment of the fructophilic character of wine yeast strains[J].J Ind Microbiol Biot,2011,38(7):833-843.
[7]SANTOS J,SOUSA M J,CARDOSO H,et al.Ethanol tolerance of sugar transport,and the rectification of stuck wine fermentations[J].Microbiology,2008,154(2):422.
[8]赵文英,贾万利.葡萄酒酿酒酵母果糖利用影响因素的研究进展[J].生物技术通报,2014(12):29-32.
[9]BELL S J,HENSCHKE P A.Implications of nitrogen nutrition for grapes,fermentation and wine[J].Aust J Grape Wine Res,2010,11(3):242-295.
[10]惠竹梅,吕万祥,刘延琳.可同化氮素对葡萄酒发酵香气影响研究进展[J].中国农业科学,2011,44(24):5058-5066.
[11]HANNAM K D,NEILSEN G H,FORGE T,et al.The concentration of yeast assimilable nitrogen in Merlot grape juice is increased by N fertilization and reduced irrigation[J].Can J Plant Sci,2013,93(1):37-45.
[12]郭在力,栾静,孙玉梅.可同化氮对葡萄酒发酵影响的研究进展[J].中国酿造,2016,35(4):19-23.
[13]姜越,潘婷,惠竹梅.模拟葡萄汁中可同化氮和还原糖对酵母发酵特性的影响[J].食品科学,2018,39(2):131-137.
[14]MUNOZ E,INGLEDEW W M.Yeast hulls in wine fermentations-a review[J]. J Wine Res,1990,1(3):197-209.
[15]卢新军,张方方,许引虎.酵母细胞壁对葡萄酒中酵母发酵代谢的影响[J].酿酒科技,2015(4):49-51.
[16]CASALTA E,CERVI M F,SALMON J M,et al.White wine fermentation:interaction of assimilable nitrogen and grape solids[J].Aust J Grape Wine Res,2013,19(1):47-52.
[17]MUNOZ E,INGLEDEW W M.Effect of yeast hulls on stuck and sluggish wine fermentations:Importance of the lipid component[J]. Appl Environ Microbiol,1989,55(6):1560-1564.
[18]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 15038—2006 葡萄酒、果酒通用分析方法[S].北京:中国标准出版社,2006.
[19]MAURICIO J C,SALMON J M.Apparent loss of sugar transport activity in Saccharomyces cerevisiae may mainly account for maximum ethanol production during alcoholic fermentation[J].Biotechnol Lett,1992,14(7):577-582.
[20]REIFENBERGER E,BOLES E,CIRIACY M.Kinetic Characterization of individual hexose transporters of Saccharomyces cerevisiae and their relation to the triggering mechanisms of glucose repression[J].Eur J Biochem,1997,245(2):324-333.
[21]BISSON L F.Stuck and sluggish fermentations[J]. Am J Enol Viticult,1999,50(2):107-119.
[22]NICOLINI G,MOSER S,ROMAN T,et al.Effect of juice turbidity on fermentative volatile compounds in white wines[J].Vitis-Geilweilerhof,2011,50(3):131-135.
[23]FLEET G H.The microbiology of alcoholic beverages[J].Microbiol Fermented Foods,1998:217-262.
[24]BERTHELS N J,OTERO R R C,BAUER F F,et al.Correlation between glucose/fructose discrepancy and hexokinase kinetic properties in different Saccharomyces cerevisiae wine yeast strains[J].Appl Microbiol Biot,2008,77(5):1083-1091.
[25]左松,伍时华,张健,等.不同时间添加氮源对酵母GJ2008 果糖与葡萄糖利用的影响[J].食品与发酵工业,2014,40(4):18-22.